SKRIPSI
KARAKTERISASI SIMPLISIA DAN SKRINING FITOKIMIA
SERTA UJI AKTIVITAS ANTIOKSIDAN EKSTRAK RUMPUT
LAUT COKLAT (
Sargassum
polycystum
C.A. Agardh)
MENGGUNAKAN METODE BETAKAROTEN
ASAM LINOLEAT
OLEH:
RUTH AGUSTINA SILABAN
NIM 091501127
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
KARAKTERISASI SIMPLISIA DAN SKRINING FITOKIMIA
SERTA UJI AKTIVITAS ANTIOKSIDAN EKSTRAK RUMPUT
LAUT COKLAT (
Sargassum polycystum
C.A. Agardh)
MENGGUNAKAN METODE BETAKAROTEN
ASAM LINOLEAT
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh
Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
RUTH AGUSTINA SILABAN
NIM 091501127
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
KARAKTERISASI SIMPLISIA DAN SKRINING FITOKIMIA
SERTA UJI AKTIVITAS ANTIOKSIDAN EKSTRAK RUMPUT
LAUT COKLAT (
Sargassum polycystum
C.A. Agardh)
MENGGUNAKAN METODE BETAKAROTEN
ASAM LINOLEAT
OLEH:
RUTH AGUSTINA SILABAN NIM 091501127
Dipertahankan di hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada tanggal : 11 Oktober 2013
Pembimbing I, Panitia Penguji,
Dra. Aswita Hafni Lubis, M.Si., Apt. Dra. Hera Ginting, M.Si., Apt. NIP 195304031983032001 NIP 194909101980031002
Pembimbing II,
Dra. Aswita Hafni Lubis, M.Si., Apt. NIP 195304031983032001
Dra. Suwarti Aris, M.Si., Apt NIP 195111021977102001
Drs. Panal Sitorus, M.Si., Apt. NIP 195310301950031002
Dra. Erly Sitompul, M.Si., Apt. NIP 195006121980032001
Fakultas Farmasi
Universitas Sumatera Utara Dekan,
KARAKTERISASI SIMPLISIA DAN SKRINING FITOKIMIA SERTA UJI AKTIVITAS EKSTRAK RUMPUT LAUT COKLAT
(Sargassum polycystum C.A. Agardh) MENGGUNAKAN
METODE β-KAROTEN-ASAM LINOLEAT ABSTRAK
Rumput laut coklat (Sargassum polycystum C.A. Agardh) termasuk famili Sargassaceae merupakan salah satu rumput laut yang banyak tersebar di pantai Indonesia. Rumput laut coklat sudah lama dikenal dan dimanfaatkan masyarakat sebagai bahan obat-obatan dan bahan makanan. Rumput laut mengandung vitamin A, B1, B2, B6, B12, vitamin C dan beta karoten yang merupakan senyawa antioksidan yang dapat menangkal radikal bebas dan dapat mencegah berbagai macam penyakit. Tujuan penelitian ini adalah untuk mengetahui karakteristik simplisia, kandungan senyawa kimia, serta uji aktivitas antioksidan dari ekstrak rumput laut dengan metode β-karoten-asam linoleat.
Ekstrak diperoleh secara perkolasi bertahap dengan menggunakan pelarut n-heksan, etil asetat, dan etanol 96% kemudian dipekatkan menggunakan rotary evaporator dan dikeringkan menggunakan freeze dryer sehingga diperoleh ekstrak kental. Uji aktivitas antioksidan terhadap ekstrak
rumput laut dilakukan dengan metode β-karoten-asam linoleat pada 0-120
menit dengan interval waktu 15 menit pada panjang gelombang 470 nm. Sebagai pembanding digunakan butil hidroksitoluena (BHT) dan kuersetin.
Hasil karakteristik simplisia rumput laut diperoleh kadar air 5,95%, kadar sari larut dalam air 10,28%, kadar sari larut dalam etanol 4,01%, kadar abu total 18,13%, kadar abu tidak larut asam 2,55%. Hasil skrining fitokimia diperoleh bahwa rumput laut mengandung senyawa steroid/triterpenoid, glikosida, dan saponin. Hasil uji aktivitas antioksidan ekstrak n-heksan, etil asetat, dan etanol rumput laut dengan metode β-karoten-asam linoleat pada konsentrasi 2000, 3000, 4000 ppm dengan urutan kekuatan aktivitas antioksidan adalah EESP > EEASP > ENSP. Apabila dibandingkan dengan kekuatan antioksidan pembanding maka berturut-turut BHT (100 ppm) > Kuersetin (100 ppm) > EESP > EEASP > ENSP. Jika dibandingkan berdasarkan konsentrasi maka kekuatan antioksidan dengan konsentrasi ekstrak rumput laut 4000 ppm > 3000 ppm > 2000 ppm.
CARACTERIZATION OF PHYTOCHEMICALS SIMPLISIA AND SCREENING TEST AND ANTIOXIDANT ACTIVITIES
(Sargassum polycystum C.A. Agardh) BROWN SEAWEED
EXTRACT BY USING THE METHOD OF
β-CAROTENE-LINOLEIC ACID ABSTRACT
The brown seaweed (Sargassum polycystum C.A. Agardh) including spare Sargassaceae is one of the many scattered seaweed on the coast of Indonesia. It is known and used by the public as medicement and food. It contain vitamin A, B1, B2, B6, B12, C and betakaroten that are antioxidant compounds that may ward off free radicals that can prevent various diseases. The purpose of this study was to determine the characterization of simplex, to determine the chemical compounds contained and to know the antioxidant activity of seaweed extracts using the method of β-carotene-linoleic acid.
Gradual percolation extract obtained using solvents n-hexane, ethyl acetate, and ethanol 96% which is then concentrated by rotary evaporatory and then dried with a freeze dryer to obtain viscous extract. The antioxidant activity of seaweed extracts was tested using by the method of β-carotene-linoleic acid at 0-120 minutes with 15 minutes intervals at a wavelength of 470 nm. For comparison used butyl hydroxytoluene (BHT) and quercetin.
The result of seaweed simplex characteristics obtained 5.95% level of water content, levels of water-soluble extract 10.28%, levels of ethanol-soluble extract 4.01%, total ash content 18.13% and ash content that does not dissolve in acid 2.55%. Phytochemical screening result obtained that seaweed contains compounds of steroids/triterpenoids, glycosides, and saponins. The results of antioxidant activity of the seaweed n-hexane, ethyl acetate, ethanol extract used the method of β-carotene-linoleic acid on concentrations 2000 ppm, 3000 ppm, 4000 ppm with the order of antioxidant power EESP > EEASP > ENSP. When compared with the antioxidant power comparators consecutive, BHT (100 ppm) > quercetin (100 ppm) > EESP > EEASP > ENSP. When compared based on concentrations of seaweed extracts were obtained the seaweed extract 4000 ppm > 3000 ppm > 2000 ppm.
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN JUDUL ... ii
LEMBAR PENGESAHAN SKRIPSI ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 4
1.4 Tujuan Penelitian ... 4
1.5 Manfaat Penelitian ... 4
1.6 Kerangka Pikir Penelitian ... 5
BAB II TINJAUAN PUSTAKA ... 6
2.1 Uraian Tumbuhan ... 6
2.1.2 Morfologi tumbuhan ... 6
2.1.3 Sistematika tumbuhan ... 7
2.1.4 Nama daerah ... 7
2.1.5 Kandungan kimia ... 7
2.1.6 Kegunaan ... 8
2.2 Ekstrak ... 8
2.3 Radikal Bebas ... 9
2.3.1 Radikal bebas dan penyakit degeneratif ... 12
2.3.1 Perlindungan tubuh terhadap radikal bebas ... 13
2.4 Antioksidan ... 13
2.4.1 Antioksidan Alami ... 15
2.5 Spektrofotometri UV-Visible ... 15
2.6 Metode Pengukuran Antioksidan ... 16
BAB III METODE PENELITIAN ... 18
3.1 Alat-Alat ... 18
3.2 Bahan-Bahan ... 18
3.3 Pengumpulan Bahan Tumbuhan ... 19
3.3.1 Pengambilan bahan tumbuhan ... 19
3.3.2 Identifikasi tumbuhan ... 19
3.3.3 Pembuatan simplisia ... 19
3.4 Pembuatan Pereaksi ... 20
3.4.1 Pereaksi besi (III) klorida 1% ... 20
3.4.3 Pereaksi timbal (II) asetat 0,4 M ... 20
3.4.4 Pereaksi Mayer ... 20
3.4.5 Pereaksi Molisch ... 20
3.4.6 Pereaksi Dragendorf ... 20
3.4.7 Pereaksi kloralhidrat ... 21
3.4.8 Pereaksi asam sulfat 2N ... 21
3.4.9 Pereaksi natrium hidroksida 2N ... 21
3.4.10 Pereaksi Bouchardat ... 21
3.4.11 Pereaksi Liebermann-Burchard ... 21
3.5 Pemeriksaan Karakteristik Simplisia ... 21
3.5.1 Pemeriksaan makroskopik ... 22
3.5.2 Pemeriksaan mikroskopik ... 22
3.5.3 Penetapan kadar air simplisia ... 22
3.5.4 Penetapan kadar sari yang larut dalam air ... 23
3.5.5 Penetapan kadar sari yang larut dalam etanol ... 23
3.5.6 Penetapan kadar abu total ... 24
3.5.7 Penetapan kadar abu yang tidak larut dalam asam ... 24
3.6 Skrining Fitokimia ... 24
3.6.1 Pemeriksaan alkaloid ... 24
3.6.2 Pemeriksaan flavonoid ... 24
3.6.3 Pemeriksaan glikosida ... 25
3.6.4 Pemeriksaan glikosida atrakinon ... 26
3.6.6 Pemeriksaan tanin ... 26
3.6.7 Pemeriksaan steroid/triterpenoid ... 27
3.7 Pembuatan Ekstrak Rumput Laut Coklat ... 27
3.8 Pengujian Kemampuan Antioksidan Dengan Spektofotometer Visibel ... 28
3.8.1 Metode β-karoten-asam linoleat ... 28
3.8.1.1 Pembuatan larutan blanko ... 28
3.8.1.2 Pembuatan larutan stok β-karoten ... 28
3.8.1.3 Pembuatan larutan induk sampel uji ENSP ... 28
3.8.1.4 Pembuatan larutan induk sampel uji EEASP... 28
3.8.1.5 Pembuatan larutan induk sampel uji EESP... 29
3.8.1.4 Pembuatan larutan uji ENSP ... 29
3.8.1.5 Pembuatan larutan uji EEASP ... 29
3.8.1.6 Pembuatan larutan uji EASP ... 29
3.8.1.7 Pembuatan larutan pembanding butil hidrosianisol (BHA), butil hdroksitoluena (BHT), dan kuersetin ... 30
3.8.1.8 Penentuan aktivitas antioksidan menggunakan metode β-karoten-asam linoleat ... 30
BAB IV HASIL DAN PEMBAHASAN ... 31
BAB V KESIMPULAN DAN SARAN ... 42
5.1 Kesimpulan ... 42
5.2 Saran ... 42
DAFTAR PUSTAKA ... 43
DAFTAR TABEL
Halaman
4.1 Hasil karakterisasi simplisia rumput laut coklat ... 32
4.2 Hasil skrining fitokimia ... 33
4.3 Persentase aktivitas antioksidan ekstrak n-heksan
rumput laut coklat dari berbagai konsentrasi ... 34
4.4 Persentase aktivitas antioksidan ekstrak etilasetat
rumput laut coklat dari berbagai konsentrasi ... 35
4.5 Persentase aktivitas antioksidan ekstrak etanol
rumput laut coklat dari berbagai konsentrasi ... 35
4.6 Hasil analisis ENSP dengan BHT dan kuersetin secara Anova ... 38
4.7 Hasil analisis ENSP dengan BHT dan kuersetin secara Tukey ... 38
4.8 Hasil analisis EEASP dengan BHT dan kuersetin secara Anova .. 39
4.9 Hasil analisis EEASP dengan BHT dan kuersetin secara Tukey ... 39
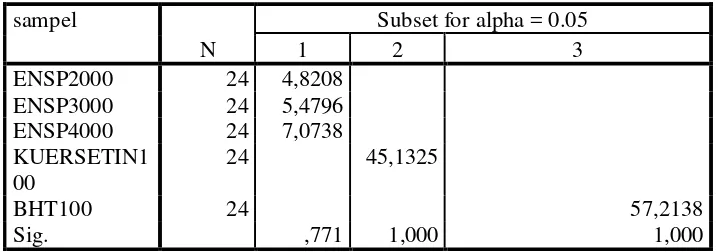
4.10 Hasil analisis EESP dengan BHT dan kuersetin secara Anova .... 40
4.11 Hasil analisis EESP dengan BHT dan kuersetin secara Tukey ... 40
4.12 Hasil analisis ENSP, EEASP, EESP dengan BHT dan
DAFTAR GAMBAR
Gambar
Halaman
1.1 Skema kerangka pikir penelitian ... 5
2.1 Rumus bangun β-karoten ... 16
4.1 Grafik persentase aktivitas antioksidan versus waktu ENSP, BHT, dan kuersetin ... 36
4.2 Grafik persentase aktivitas antioksidan versus waktu EEASP, BHT, dan kuersetin ... 36
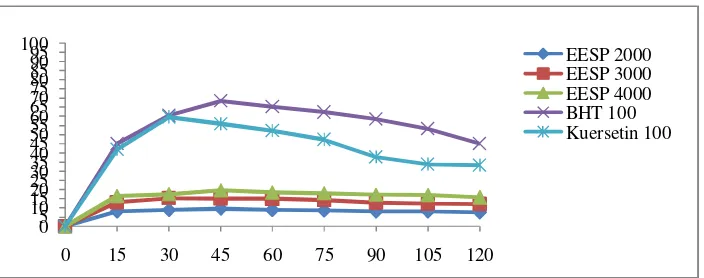
4.3 Grafik persentase aktivitas antioksidan versus waktu EESP, BHT, dan kuersetin ... 37
4.4 Simplisia rumput laut coklat ... 46
4.5 Serbuk simplisia rumput laut coklat ... 47
4.6 Mikroskopik serbuk simplisia ... 48
4.8 Bagan pembuatan serbuk simplisia rumput laut coklat ... 49
4.9 Bagan pembuatan ekstrak rumput laut coklat ... 50
4.10 Bagan pengujian aktivitas antioksidan ... 51
DAFTAR LAMPIRAN
Lampiran
Halaman
1. Identifikasi bahan tumbuhan ... 45
2. Gambar simplisia rumput laut coklat ... 46
3. Gambar serbuk simplisia rumput laut coklat ... 47
4. Mikroskopik rumput laut coklat ... 48
5. Bagan pembuatan serbuk simplisia ... 49
6. Bagan pembuatan ekstrak rumput laut coklat ... 50
7. Bagan pengujian aktivitas antioksidan ... 51
8. Perhitungan penetapan kadar air ... 53
9. Perhitungan penetapan kadar sari larut dalam air ... 54
10. Perhitungan penetapan kadar sari larut dalam etanol ... 55
11. Perhitungan penetapan kadar abu total ... 56
12. Perhitungan penetapan kadar abu tidak larut asam ... 57
13. Data absorbansi dan hasil uji aktivitas antioksidan ekstrak n-heksan rumput laut coklat ... 58
14. Data absorbansi dan hasil uji aktivitas antioksidan ekstrak etilasetat rumput laut coklat ... 61
15. Data absorbansi dan hasil uji aktivitas antioksidan ekstrak etanol rumput laut coklat ... 64
16. Data absorbansi dan hasil uji aktivitas antioksidan butil hidroksi Toluen (BHT) dan kuersetin ... 67
17. Contoh perhitungan nilai aktivitas antioksidan metode β-karoten- asam linoleat ... 69
KARAKTERISASI SIMPLISIA DAN SKRINING FITOKIMIA SERTA UJI AKTIVITAS EKSTRAK RUMPUT LAUT COKLAT
(Sargassum polycystum C.A. Agardh) MENGGUNAKAN
METODE β-KAROTEN-ASAM LINOLEAT ABSTRAK
Rumput laut coklat (Sargassum polycystum C.A. Agardh) termasuk famili Sargassaceae merupakan salah satu rumput laut yang banyak tersebar di pantai Indonesia. Rumput laut coklat sudah lama dikenal dan dimanfaatkan masyarakat sebagai bahan obat-obatan dan bahan makanan. Rumput laut mengandung vitamin A, B1, B2, B6, B12, vitamin C dan beta karoten yang merupakan senyawa antioksidan yang dapat menangkal radikal bebas dan dapat mencegah berbagai macam penyakit. Tujuan penelitian ini adalah untuk mengetahui karakteristik simplisia, kandungan senyawa kimia, serta uji aktivitas antioksidan dari ekstrak rumput laut dengan metode β-karoten-asam linoleat.
Ekstrak diperoleh secara perkolasi bertahap dengan menggunakan pelarut n-heksan, etil asetat, dan etanol 96% kemudian dipekatkan menggunakan rotary evaporator dan dikeringkan menggunakan freeze dryer sehingga diperoleh ekstrak kental. Uji aktivitas antioksidan terhadap ekstrak
rumput laut dilakukan dengan metode β-karoten-asam linoleat pada 0-120
menit dengan interval waktu 15 menit pada panjang gelombang 470 nm. Sebagai pembanding digunakan butil hidroksitoluena (BHT) dan kuersetin.
Hasil karakteristik simplisia rumput laut diperoleh kadar air 5,95%, kadar sari larut dalam air 10,28%, kadar sari larut dalam etanol 4,01%, kadar abu total 18,13%, kadar abu tidak larut asam 2,55%. Hasil skrining fitokimia diperoleh bahwa rumput laut mengandung senyawa steroid/triterpenoid, glikosida, dan saponin. Hasil uji aktivitas antioksidan ekstrak n-heksan, etil asetat, dan etanol rumput laut dengan metode β-karoten-asam linoleat pada konsentrasi 2000, 3000, 4000 ppm dengan urutan kekuatan aktivitas antioksidan adalah EESP > EEASP > ENSP. Apabila dibandingkan dengan kekuatan antioksidan pembanding maka berturut-turut BHT (100 ppm) > Kuersetin (100 ppm) > EESP > EEASP > ENSP. Jika dibandingkan berdasarkan konsentrasi maka kekuatan antioksidan dengan konsentrasi ekstrak rumput laut 4000 ppm > 3000 ppm > 2000 ppm.
CARACTERIZATION OF PHYTOCHEMICALS SIMPLISIA AND SCREENING TEST AND ANTIOXIDANT ACTIVITIES
(Sargassum polycystum C.A. Agardh) BROWN SEAWEED
EXTRACT BY USING THE METHOD OF
β-CAROTENE-LINOLEIC ACID ABSTRACT
The brown seaweed (Sargassum polycystum C.A. Agardh) including spare Sargassaceae is one of the many scattered seaweed on the coast of Indonesia. It is known and used by the public as medicement and food. It contain vitamin A, B1, B2, B6, B12, C and betakaroten that are antioxidant compounds that may ward off free radicals that can prevent various diseases. The purpose of this study was to determine the characterization of simplex, to determine the chemical compounds contained and to know the antioxidant activity of seaweed extracts using the method of β-carotene-linoleic acid.
Gradual percolation extract obtained using solvents n-hexane, ethyl acetate, and ethanol 96% which is then concentrated by rotary evaporatory and then dried with a freeze dryer to obtain viscous extract. The antioxidant activity of seaweed extracts was tested using by the method of β-carotene-linoleic acid at 0-120 minutes with 15 minutes intervals at a wavelength of 470 nm. For comparison used butyl hydroxytoluene (BHT) and quercetin.
The result of seaweed simplex characteristics obtained 5.95% level of water content, levels of water-soluble extract 10.28%, levels of ethanol-soluble extract 4.01%, total ash content 18.13% and ash content that does not dissolve in acid 2.55%. Phytochemical screening result obtained that seaweed contains compounds of steroids/triterpenoids, glycosides, and saponins. The results of antioxidant activity of the seaweed n-hexane, ethyl acetate, ethanol extract used the method of β-carotene-linoleic acid on concentrations 2000 ppm, 3000 ppm, 4000 ppm with the order of antioxidant power EESP > EEASP > ENSP. When compared with the antioxidant power comparators consecutive, BHT (100 ppm) > quercetin (100 ppm) > EESP > EEASP > ENSP. When compared based on concentrations of seaweed extracts were obtained the seaweed extract 4000 ppm > 3000 ppm > 2000 ppm.
BAB I
PENDAHULUAN
1.1Latar Belakang
Indonesia sebagai negara kepulauan di perairan tropis diketahui
memiliki keanekaragaman jenis biota yang tinggi, termasuk keanekaragaman
jenis alganya (Atmadja, 1992). Rumput laut atau alga yang juga dikenal
dengan nama seaweed merupakan bagian terbesar dari tanaman laut. Rumput
laut telah digunakan sebagai makanan dan obat-obatan (Winarno, 1990;
Anggadiredja, dkk., 2010).
Sebagai sumber gizi, rumput laut memiliki kandungan karbohidrat
(gula atau vegetable-gum), protein, sedikit lemak, polisakarida sulfat. Selain
itu, rumput laut juga mengandung vitamin-vitamin, seperti vitamin A, B1, B2,
B6, B12, dan C, betakaroten, serta mineral, seperti kalium, kalsium, fosfor,
natrium, zat besi, dan iodium. Beberapa jenis rumput laut juga mengandung
protein yang cukup tinggi (Anggadiredja, dkk., 2011).
Rumput laut (Sargassum polycystum C.A. Agardh) digunakan secara
komersil di Indonesia sebagai sumber penghasil alginat, pemanis agar, bahan
obat penyakit kantung kemih, bahan obat penyakit gondok, sayuran, dan juga
kosmetik (Anggadiredja, dkk., 2011).
Dewasa ini dunia kesehatan banyak membahas tentang radikal bebas (free
radical) dan antioksidan. Hal ini terjadi karena sebagian besar penyakit diawali
penyebab terbesar terjadinya penuaan dan penyakit degeneratif, misalnya, penyakit
jantung koroner, stroke, diabetes melitus dan kanker (Ko, et al., 2009).
Antioksidan adalah zat yang dapat menetralisir radikal bebas dengan
memberikan elektronnya kepada molekul radikal bebas sehingga tidak lagi
menjadi radikal bebas. Radikal bebas merupakan senyawa yang memiliki satu
atau lebih elektron yang tidak berpasangan dan bersifat sangat reaktif. Selain
terdapat di luar tubuh, radikal bebas juga secara normal dibentuk di dalam
tubuh. Radikal bebas terbentuk di dalam tubuh akibat produk sampingan proses
metabolisme ataupun karena tubuh terpapar radikal bebas melalui pernafasan
(Praptiwi, dkk., 2006).
Radikal bebas dalam jumlah kecil masih dapat ditoleransi, namun
berbahaya dalam jumlah yang berlebih. Radikal bebas akan merusak DNA,
protein dan lipid, perubahan ini dapat mempercepat proses penuaan bahkan
menyebabkan berbagai penyakit (Kosasih, dkk., 2004; Silalahi, 2006).
Tubuh kita terdapat sistem enzim (misalnya enzim superoksida
dismutase) yang dapat berperan sebagai antioksidan. Enzim ini dapat berperan
aktif dalam menanggulangi masalah radikal bebas. Di dalam tubuh jumlah
radikal bebas lebih banyak dari enzim yang terdapat di dalam tubuh, saat itulah
tubuh memerlukan tambahan antioksidan dari luar tubuh (Kumalaningsih,
2006; Kosasih, dkk., 2004).
Kebanyakan senyawa antioksidan yang diisolasi dari sumber alami
adalah berasal dari bahan tumbuhan yang dapat berupa senyawa fenolik atau
sayur-sayuran, dan rumput laut. Antioksidan sintetik yang dibuat dari bahan-bahan
kimia yaitu butylated hydroxy toluena (BHT), butylated hydroxyanisole
(BHA), TBHQ, PG, dan NDGA yang ditambahkan pada makanan untuk
mencegah kerusakan lemak (Kumalaningsih, 2006).
Metode yang digunakan untuk uji aktivitas antioksidan adalah β
karoten-asam linoleat. Metode βkaroten asam linoleat merupakan metode
spektrofotometri yang didasarkan pada kemampuan antioksidan untuk
mencegah pemucatan warna jingga karoten akibat oksidasi dalam sistim emulsi
asam linoleat dan β-karoten. Pemucatan warna jingga karoten ditunjukkan
dengan penurunan absorbansi dan aktivitas antioksidan. (Prakash, 2001;
Rosidah, et al., 2008; Ko, et al., 2009).
Berdasarkan hal di atas, penulis melakukan uji karakterisasi simplisia,
skrining fitokimia serta uji aktivitas antioksidan dengan metode pemucatan
(bleaching) β-karoten-asam linoleat dari ekstrak n-heksana, etil asetat, dan
etanol rumput laut coklat (Sargassum polycystum C.A. Agardh).
1.2 Perumusan Masalah
Perumusan masalah dari penelitian ini adalah:
1. Apakah karakteristik simplisia rumput laut coklat (Sargassum
polycystum C.A. Agardh) hasil penelitian ini dapat dijadikan sebagai
pembanding pada penelitian selanjutnya?
2. Apakah golongan senyawa kimia yang terkandung dari simplisia rumput
3. Apakah senyawa kimia ekstrak rumput laut coklat (Sargassum
polycystum C.A. Agardh) mempunyai aktivitas antioksidan
menggunakan metode β-karoten-asam linoleat?
1.3 Hipotesis
1. Karakteristik simplisia rumput laut coklat (Sargassum polycystum C.A.
Agardh) dari hasil penelitian ini dapat dijadikan sebagai pembanding
pada penelitian selanjutnya.
2. Golongan senyawa kimia yang terkandung dari simplisia rumput laut
coklat (Sargassum polycystum C.A. Agardh) dapat diketahui.
3. Senyawa kimia yang terkandung dalam ekstrak rumput laut coklat
(Sargassum polycystum C.A. Agardh) mempunyai aktivitas antioksidan
dengan menggunakan metode β-karoten-asam linoleat.
1.4 Tujuan Penelitian
1. Untuk memperoleh karakteristik simplisia rumput laut coklat
(Sargassum polycystum C.A. Agardh) yang dapat dijadikan sebagai
pembanding pada penelitian selanjutnya.
2. Untuk mengetahui senyawa kimia yang terkandung dari simplisia
rumput laut coklat (Sargassum polycystum C.A. Agardh).
3. Untuk mengetahui aktivitas antioksidan dari masing-masing ekstrak
1.5 Manfaat Penelitian
Hasil dari penelitian ini diharapkan dapat memberikan informasi
tentang karakteristik simplisia, senyawa kimia, dan aktivitas antioksidan dari
ekstrak rumput laut coklat (Sargassum polycystum C.A. Agardh) secara in vitro
dengan menggunakan metode β-karoten-asam linoleat.
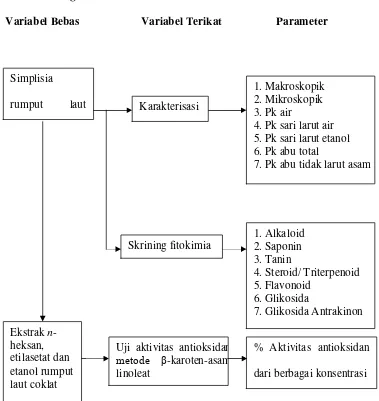
1.6 Kerangka Pikir Penelitian
Variabel Bebas Variabel Terikat Parameter
Gambar 1.1 Skema kerangka pikir penelitian Simplisia
rumput laut Karakterisasi
1. Makroskopik 2. Mikroskopik 3. Pk air
4. Pk sari larut air 5. Pk sari larut etanol 6. Pk abu total
7. Pk abu tidak larut asam
Skrining fitokimia
1. Alkaloid 2. Saponin 3. Tanin
4. Steroid/ Triterpenoid 5. Flavonoid
6. Glikosida
7. Glikosida Antrakinon Ekstrak n
-heksan, etilasetat dan etanol rumput laut coklat
Uji aktivitas antioksidan
metode β-karoten-asam
linoleat
% Aktivitas antioksidan
BAB II
TINJAUAN PUSTAKA
2.1 Uraian tumbuhan
Rumput laut merupakan salah satu komoditas hasil laut yang penting
serta tumbuh dan tersebar hampir di seluruh perairan Laut Indonesia.
Tumbuhan ini bernilai ekonomi tinggi dalam bidang industri makanan maupun
bukan makanan (industri kosmetik, tekstil dan farmasi) untuk memenuhi
permintaan dalam negeri maupun luar negeri (Handayani, dkk., 2004).
Rumput laut atau algae termasuk divisi Thallophyta (tumbuhan
bertalus) karena mempunyai struktur kerangka tubuh (morfologi) yang tidak
berdaun, berbatang dan berakar, semuanya terdiri dari talus saja (Aslan, 1998).
Uraian tumbuhan meliputi habitat tumbuhan, morfologi tumbuhan, sistematika
tumbuhan, nama daerah, nama asing, kandungan kimia dan kegunaan
tumbuhan.
2.1.1 Habitat tumbuhan
Sargassum tumbuh di perairan yang terlindung maupun yang berombak
besar pada habitat batu. Beberapa jenis atau varietas dari Sargassum terdapat
dalam jumlah besar di laut Sargasso. Alga di laut ini berasal dari daerah pantai.
Saat mereka patah dari induknya, mereka hanyut ke laut lepas dan berkembang
biak disana (Romimohtarto, 2009).
2.1.2 Morfologi tumbuhan
Morfologi Sargassum polycystum C.A. Agardh tidak jauh berbeda
holdfast membentuk cakram kecil dan di atasnya terdapat stolon yang rimbun
berekspansi ke segala arah. “Batang” pendek dengan percabangan utama
tumbuh rimbun di bagian ujungnya mencapai tinggi sekitar 2 meter. Vesicle
atau gelembung udara (bladder) yang umumnya bulat telur dan talus berwarna
coklat (Anggadiredja, dkk., 2011).
2.1.3 Sistematika tumbuhan
Berikut ini adalah sistematika tumbuhan:
Divisi : Phaeophyta
Kelas : Phaeophyceae
Bangsa : Fucales
Suku : Sargassaceae
Marga : Sargassum
Jenis : Sargassum polycystum C.A. Agardh
2.1.4 Nama daerah
Nama daerah tumbuhan ini di Kepulauan Seribu adalah oseng (Aslan,
1998).
2.1.5 Kandungan kimia
Sargassum polycystum C.A. Agardh mengandung alginat, vitamin C, vitamin E (α-tokoferol), mineral, karotenoid, klorofil, florotanin, polisakarida
sulfat, asam lemak, dan asam amino. Sargassum polycystum C.A. Agardh juga
mengandung senyawa metabolit sekunder yaitu steroid/ triterpenoid
2.1.6 Kegunaan
Sargassum polycystum C.A. Agardh memiliki potensial dalam
penyembuhan penyakit kantung kemih, gondok, kolesterol, digunakan sebagai
kosmetik, sumber alginat, antioksidan (Anggadiredja, dkk., 2011).
2.2 Ekstrak
Ekstrak adalah sediaan pekat yang diperoleh dengan mengekstraksi zat
aktif dari simplisia nabati atau simplisia hewani menggunakan pelarut yang
sesuai, kemudian semua atau hampir semua pelarut diuapkan dan massa atau
serbuk yang tersisa diperlakukan sedemikian hingga memenuhi baku yang
telah ditetapkan (Ditjen POM, 1995).
Metode ekstraksi menurut Goeswin (2007), Anief (2000) dan Ditjen
POM (2000) ada beberapa cara, yaitu:
1. Maserasi
Maserasi adalah suatu cara penyarian simplisia dengan cara merendam
simplisia tersebut dalam pelarut dengan beberapa kali pengocokan atau
pengadukan pada temperatur kamar.
2. Perkolasi
Perkolasi adalah suatu cara penyarian simplisia menggunakan
perkolator dimana simplisianya terendam dalam pelarut yang selalu baru dan
umumnya dilakukan pada temperatur kamar. Prosesnya terdiri dari tahapan
pengembangan bahan, tahap maserasi antara, tahap perkolasi sebenarnya
(penetesan dan penampungan ekstrak) terus-menerus sampai diperoleh ekstrak
3. Refluks
Refluks adalah proses penyarian dengan pelarut pada temperatur titik
didihnya dalam jangka waktu tertentu dimana pelarut akan terkondensasi
menuju pendingin dan kembali ke labu.
4. Sokletasi
Sokletasi adalah proses penyarian kontinu menggunakan alat soklet,
dimana pelarut akan terkondensasi dari labu menuju pendingin, kemudian jatuh
membasahi sampel dan mengisi bagian tengah alat soklet. Tabung sifon juga
terisi dengan larutan ekstraksi dan ketika mencapai bagian atas tabung sifon,
larutan tersebut akan kembali ke dalam labu.
5. Digesti
Digesti adalah proses penyarian dengan pengadukan kontinu pada
temperatur yang lebih tinggi dari temperatur kamar, umumnya dilakukan pada
suhu 40-50oC.
6. Infundasi
Infundasi adalah proses penyarian dengan menggunakan pelarut air pada
temperatur 90oC selama 15 menit.
7. Dekoktasi
Dekoktasi adalah proses penyarian dengan menggunakan pelarut air
pada temperatur 90oC selama 30 menit.
2.3 Radikal Bebas
Radikal bebas adalah setiap molekul yang mengandung satu atau lebih
maupun lingkungan. Di dalam tubuh, setiap proses normal yang melibatkan
oksigen akan menghasilkan radikal bebas. Sumber radikal bebas, baik endogen
maupun eksogen terjadi melalui sederetan mekanisme reaksi yaitu
pembentukan awal radikal bebas, lalu perambatan atau terbentuknya radikal
baru dan tahap terakhir yaitu pemusnahan atau pengubahan menjadi senyawa
stabil dan tak reaktif. Sumber endogen dapat melewati autooksidasi, oksidasi
enzimatik, fagositosis dalam respirasi atau transport elektron di mitokondria.
Sedangkan dari lingkungan, radikal bebas bisa berasal dari polusi udara (asap
rokok, asap kenderaan bermotor), radiasi ultraviolet, olahraga berlebihan,
bahan racun dalam pestisida, insektisida, bahan cat perabot rumah tangga,
makanan berlemak, alkohol dan kopi serta stres yang berlebihan (Sauriasari,
2006).
Radikal bebas sangat reaktif dan dengan mudah menjurus ke reaksi
yang tidak terkontrol, menghasilkan ikatan silang pada DNA, protein, lipida,
atau kerusakan oksidatif pada gugus fungsional yang penting pada biomolekul
ini. Perubahan ini akan menyebabkan proses penuaan. Radikal bebas juga
terlibat dan berperan dalam penyebab dari berbagai penyakit degeneratif, yakni
kanker, aterosklerosis, jantung koroner, katarak dan penyakit degenerasi saraf
seperti parkinson (Silalahi, 2006).
Sifat radikal bebas yang tidak stabil menyebabkan reaksi menerima atau
memberikan elektron dengan molekul sekitarnya. Kebanyakan molekul ini
bukan radikal bebas melainkan makromolekul biologi seperti lipid, protein,
beruntun yaitu terbentuknya radikal bebas baru yang bereaksi lagi dengan
makromolekul lain (Kosasih, dkk., 2004).
Pembentukan radikal bebas dan reaksi oksidasi pada biomolekul akan
berlangsung sepanjang hidup. Radikal bebas yang sangat berbahaya dalam
makhluk hidup antara lain adalah golongan hidroksil (OH-), superoksida (O-2),
nitrogen monooksida (NO), peroksidal (RO-2), peroksinitrit (ONOO-), asam
hipoklorit (HOCl) dan hydrogen peroksida (H2O2) (Silalahi, 2006).
Secara umum tahapan reaksi pembentukan radikal bebas adalah sebagai
berikut:
I. Inisiasi
RH + initiator → R● II. Propagasi
R● + O2 → ROO●
ROO● + RH → ROOH + R● III. Terminasi
R● + R●→ RR ROO● + R●→ ROOR
Tahap inisiasi adalah tahap awal terbentuknya radikal bebas. Tahap
propagasi adalah tahap perpanjangan radikal berantai, di mana terjadi reaksi
antara suatu radikal dengan senyawa lain dan menghasilkan radikal baru.
Tahap terminasi adalah tahap akhir, terjadinya pengikatan suatu radikal bebas
dengan radikal bebas yang lain sehingga menjadi tidak reaktif lagi. Ketika
proses tersebut terjadi maka siklus reaksi radikal telah berakhir
2.3.1 Radikal bebas dan penyakit degeneratif
Sel-sel di dalam tubuh mengalami kerusakan oksidatif setiap hari.
Diperkirakan bahwa DNA di dalam sel mengalami sepuluh ribu benturan yang
bersifat oksidatif per hari. Biomolekul lain seperti protein dan lipida juga
rentan terhadap kerusakan oksidatif. Sebagian besar dari kerusakan ini
diperbaiki tetapi kerusakan yang tidak dipulihkan tertimbun selama hidup dan
mengarah pada proses penuaan serta menimbulkan penyakit degeneratif.
Radikal bebas dan proses oksidatif berperan baik pada inisiasi maupun
stimulasi karsinogenesis. Hipotesis oksidatif karsinogenesis menyatakan bahwa
banyak karsinogen dapat menghasilkan radikal bebas yang akan merusak
sel-sel. DNA mengandung gugus reaktif yang sensitif terhadap radikal bebas dan
kerusakan oksidatif dapat menjurus ke mutasi yang merusak (Silalahi, 2006).
2.3.2 Perlindungan tubuh terhadap radikal bebas
Tubuh juga memiliki mekanisme perlindungan lain yang meliputi
sistem enzimatik dan substansi tertentu yang disebut free radical scavenger
(pemburu radikal bebas) yang akan berusaha memusnahkan radikal bebas.
Sistem enzim tersebut antara lain superoksidase dismutase (SOD), katalase,
dan glutathion peroxidase. Daya tempur pemburu radikal bebas tersebut dapat
diperkuat dengan pemberian vitamin yang kita makan seperti vitamin E,
vitamin C, betakaroten dan lain-lain (Kosasih, dkk., 2004).
Berbagai vitamin yang berfungsi sebagai antioksidan tersebut banyak
terdapat di sekitar kita, baik yang alami maupun berupa suplemen (Kosasih,
sitokrom P450 di dalam hati dan sel-sel saluran pencernaan. Sitokrom P450
adalah suatu senyawa yang mengandung besi yang turut dalam suatu proses
yang mengubah senyawa endogen dan toksin dari luar tubuh menjadi metabolit
yang tidak berbahaya dan mudah larut dalam air dan akhirnya dikeluarkan dari
tubuh. Di samping itu, senyawa karsinogen juga dapat dimodifikasi melalui
konjugasi dengan suatu gula (asam glukoronat), sulfat, gugus metil, atau
glutation (GSH). Beberapa enzim glutathion-S-transferase (GST) berperan
untuk mentransfer GSH ke berbagai karsinogen membentuk senyawa
konjugasinya dengan GSH yang netral dan mudah larut dalam air sehingga
mudah dikeluarkan dari tubuh (Silalahi, 2006).
Gen P53 yang sudah diidentifikasi sebagai suatu gen penekan tumor
adalah cara lain untuk mencegah pertumbuhan kanker yakni dengan menunda
pembelahan sel sehingga sel memiliki kesempatan untuk mereparasi
kerusakan. Enzim-enzim berpindah ke atas dan ke bawah pada struktur DNA
(DNA double helix) untuk mereparasi komponen yang rusak (Silalahi, 2006).
2.4 Antioksidan
Antioksidan adalah senyawa yang mempunyai struktur molekul yang
dapat memberikan elektronnya dengan cuma-cuma kepada molekul radikal
bebas tanpa terganggu sama sekali dan dapat memutus reaksi berantai dari
radikal bebas. Antioksidan merupakan senyawa pemberi elektron (elektron
donor) atau reduktan. Senyawa ini memiliki berat molekul kecil, tetapi mampu
menginaktivasi berkembangnya reaksi oksidasi, dengan cara mencegah
sangat reaktif. Atas dasar fungsinya, antioksidan dapat dibedakan menjadi
lima: (Kumalaningsih, 2006)
a. Antioksidan primer, merupakan sistem enzim pada tubuh manusia,
contohnya: enzim superoksida dismutase.
b. Antioksidan sekunder, merupakan antioksidan alami yang dapat diperoleh dari tanaman atau hewan berupa tokoferol, vitamin C, β
-karoten, flavonoid dan senyawa fenolik yang berfungsi menangkap
radikal bebas serta mencegah terjadinya reaksi berantai sehingga tidak
terjadi kerusakan yang lebih besar.
c. Antioksidan tersier (sintetik), dibuat dari bahan-bahan kimia yang
biasanya ditambahkan ke dalam bahan pangan untuk mencegah
terjadinya reaksi autooksidasi. Antioksidan tersier bekerja memperbaiki
sel sel dan jaringan yang rusak karena serangan radikal bebas. Senyawa
antioksidan sintetik yang secara luas digunakan adalah butylated
hydroxyanisole (BHA), butylated hydroxytoluen (BHT),propil galat.
d. Oxygen scavenger, yang mampu mengikat oksigen sehingga tidak
mendukung reaksi oksidasi reduksi, misalnya vitamin C.
e. Chelators atau sequestrant, yang dapat mengikat logam yang
mengkatalisis reaksi oksidasi misalnya asam sitrat.
Senyawa-senyawa polifenol seperti flavonoid mampu menghambat
antioksidan melalui mekanisme penangkapan radikal dengan cara
menyumbangkan satu elektron yang tidak berpasangan dalam radikal bebas
Antioksidan yang ada di dalam tubuh yang sangat terkenal adalah
enzim superoksida dismustase. Enzim ini sangat penting sekali karena dapat
melindungi hancurnya sel-sel dalam tubuh akibat serangan radikal bebas.
Bekerjanya enzim ini sangat dipengaruhi oleh mineral-mineral seperti mangan,
seng, tembaga dan selenium (Kumalaningsih, 2006).
Antioksidan alami yaitu antioksidan yang dapat diperoleh dari tanaman
atau hewan berupa tokoferol, vitamin C, betakaroten, flavonoid dan senyawa
fenolik (Kumalaningsih, 2006). Salah satu antioksidan alami yang berperan
sebagai antioksidan adalah flavonoid. Senyawa ini berperan sebagai penangkap
radikal bebas karena mengandung gugus hidroksil. Karena bersifat sebagai
reduktor, flavonoid dapat bertindak sebagai donor hidrogen terhadap radikal
bebas (Silalahi, 2006).
2.4.1 Antioksidan alami
Sayur-sayuran dan buah-buahan kaya akan zat gizi (vitamin, mineral,
serat pangan) serta berbagai kelompok zat bioaktif lain yang disebut zat
fitokimia. Zat bioaktif ini bekerja secara sinergis meliputi mekanisme enzim
detoksifikasi, peningkatan sistem kekebalan, pengurangan agregasi platelet,
pengaturan sintesis kolesterol dan metabolisme hormon, penurunan tekanan
darah, antioksidan, antibakteri serta efek antivirus (Silalahi, 2006).
2.5 Spektrofotometri UV-Visible
Absorbansi energi oleh suatu zat dalam larutan yang homogen dapat
visible pada panjang gelombang 380 nm sampai 760 nm dan spektrofotometri
ultraviolet pada panjang gelombang diatas 200 nm (Levie, 1997).
Spektrofotometer pada dasarnya terdiri dari sumber sinar,
monokromator, sel untuk zat yang diperiksa, detektor, penguat arus dan alat
ukur atau pencatat. Spektrofotometri serapan merupakan metode pengukuran
serapan radiasi elektromagnetik pada panjang gelombang tertentu, yang diserap
zat. Spektrofotometri yang sering digunakan untuk mengukur serapan larutan
atau zat yang diperiksa adalah spektrofotometri ultraviolet dengan panjang
gelombang 190-380 nm dan visibel (cahaya tampak) dengan panjang
gelombang 380-780 nm (Ditjen POM, 1979).
Ahli kimia telah lama menggunakan warna sebagai bantuan dalam
mengenali zat-zat kimia. Spektrofotometri dapat dianggap sebagai perluasan
suatu pemeriksaan visual, yaitu dengan menggunakan alat untuk mengukur
absorpsi energi radiasi macam-macam zat kimia dan memungkinkan
dilakukannya pengukuran kualitatif dari suatu zat dengan ketelitian yang lebih
besar (Day dan Underwood, 1986).
2.6 Metode Pengukuran Antioksidan
Beberapa tahun belakangan ini, pengujian absorbansi oksigen radikal
telah digunakan untuk mengevaluasi dan mengukur aktivitas antioksidan pada
makanan, serum dan cairan biologi lainnya. Metode analisa ini mengukur
aktivitas dari antioksidan dalam melawan radikal bebas seperti 1,1-
diphenyl-2-picrylhydrazyl (DPPH) radikal, anion superoksida radikal (O2·), hidroksi
digunakan untuk mengukur aktivitas antioksidan dari produk makanan dapat
memberikan hasil yang beragam tergantung pada spesifitas dari radikal bebas
yang digunakan sebagai reaktan (Sunarni, dkk., 2007).
Pada uji aktifitas antioksidan dengan menggunakan metode β
-karoten-asam linoleat, radikal bebas terbentuk dari hidroperoksid yang dihasilkan oleh
asam linoleat. Radikal bebas asam linoleat terbentuk karena pengurangan atom
hidrogen dari satu gugus metilen dialil yang menyerang ikatan rangkap pada
beta karoten sehingga terjadi oksidasi beta karoten yang menyebabkan
hilangnya gugus kromofor yang memberi warna orange (Rosidah, et al., 2008).
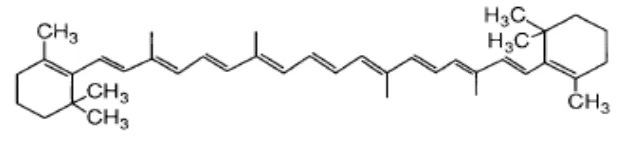
[image:31.612.179.488.360.444.2]Perubahan warna ini dapat diukur secara spektrofotometri.
Gambar 2.1 Rumus bangun β-karoten
Panjang gelombang maksimum (λmaks) yang digunakan dalam
pengukuran metode β-karoten-asam linoleat menurut literatur adalah 470 nm
(Rosidah, et al., 2008; Sugiastuti, 2002). Lama pengukuran metode β
-karoten-asam linoleat menurut literatur yang direkomendasikan adalah 0 menit sampai
BAB III
METODE PENELITIAN
Metode penelitian yang dilakukan adalah penelitian eksperimental.
Penelitian meliputi pengumpulan bahan tumbuhan, identifikasi bahan
tumbuhan, karakterisasi simplisia, skrining fitokimia, pembuatan ekstrak n
-heksan, pembuatan ekstrak etil asetat, pembuatan ekstrak etanol, dan uji
aktivitas antioksidan dengan metode β-karoten-asam linoleat dengan
menggunakan alat spektrofotometer visibel.
3.1 Alat-Alat
Alat-alat yang digunakan pada penelitian ini meliputi alat-alat gelas
laboratorium, aluminium foil, blender (National), lemari pengering, oven
listrik, neraca kasar (O’Haus), neraca digital (Vibra), seperangkat alat destilasi
penetapan kadar air, desikator, stopwatch, kaca objek, kaca penutup, cawan
porselin, lemari pengering, krus tang dan pisau, rotary evaporator (Heidolph
VV-300), freeze dryer (Edwards), mikroskop (Boeco, BM-180, Halogen
Lamp), tanur (Gallenkamp), kamera digital, spektofotometer UV/Vis Shimadzu
UV-1800).
3.2 Bahan-Bahan
Bahan yang digunakan pada penelitian adalah rumput laut coklat
Sargassum polycystum C.A. Agardh dan air suling. Bahan-bahan kimia yang
Tween 40, asam linoleat, butil hidrokswitoluena (BHT), kuersetin, produksi
E-Merck: etanol, toluen, raksa (II) klorida, kalium iodida, bismuth (III) nitrat,
asam nitrat pekat, besi (III) klorida, asam klorida pekat, asam sulfat pekat,
timbal (II) asetat, kloralhidrat, kloroform, isopropanol, benzen, asam asetat
anhidrida, natrium hidroksida, amil alkohol. Bahan kimia berkualitas teknis:
etanol 96%, n-heksan dan etilasetat.
3.3 Pengumpulan Bahan Tumbuhan
Pengambilan bahan tumbuhan dilakukan secara purposif yaitu tanpa
membandingkan dengan tumbuhan daerah lain. Bahan penelitian adalah talus
rumput laut coklat yang diperoleh dari Desa Pal 7, Kecamatan Sosorgadong
Kabupaten Tapanuli Tengah, Provinsi Sumatera Utara dan dikumpulkan pada
bulan Desember 2012. Sampel yang digunakan pada penelitian ini adalah sama
dengan sampel yang digunakan pada penelitian Roni Aritonang.
3.3.1 Identifikasi tumbuhan
Identifikasi tumbuhan dilakukan di Pusat penelitian Oseanografi LIPI,
Jakarta. Hasil identifikasi tumbuhan dapat dilihat pada Lampiran 1, halaman
46. Gambar rumput laut coklat dapat dilihat pada Lampiran 2, halaman 47.
3.3.2 Pembuatan simplisia rumput laut coklat
Rumput laut coklat (Sargassum polycystum C.A. Agardh) yang telah
dikumpulkan, dibersihkan, dicuci, ditiriskan kemudian ditimbang sebagai berat
basah. Bahan ini kemudian dikeringkan di lemari pengering hingga kering,
berat kering. Bahan kemudian diserbuk dengan menggunakan blender.
Diperoleh berat basah sebesar 15 kg dan berat kering sebesar 1,9 kg.
3.4 Pembuatan Pereaksi
3.4.1 Pereaksi besi (III) klorida 1%
Sebanyak 1 g besi (III) klorida dilarutkan dalam air suling sampai 100
ml (Depkes, 1995).
3.4.2 Pereaksi asam klorida 2 N
Sebanyak 17 ml asam klorida pekat diencerkan dengan air suling
sampai 100 ml (Depkes, 1995).
3.4.3 Pereaksi timbal (II) asetat 0,4 M
Timbal (II) asetat sebanyak 15,17 g dilarutkan dalam air suling bebas
CO2 hingga 100 ml (Depkes, 1995).
3.4.4 Pereaksi Mayer
Sebanyak 1,4 g raksa (II) klorida, kemudian dilarutkan dalam air suling
hingga 60 ml. Pada wadah lain ditimbang sebanyak 5 g kalium iodida lalu
dilarutkan dalam 10 ml air suling. Kedua larutan dicampurkan dan
ditambahkan air suling hingga diperoleh larutan 100 ml (Depkes, 1995).
3.4.5 Pereaksi Mollish
Sebanyak 3 g α-naftol dilarutkan dalam asam nitrat 0,5 N hingga 100
ml (Depkes, 1995).
3.4.6 Pereaksi Dragendorff
Sebanyak 0,8 g bismut nitrat dilarutkan dalam asam nitrat pekat 20 ml
50 ml air suling. Campuran didiamkan sampai memisah sempurna. Larutan
jernih diambil dan diencerkan dengan air suling secukupnya hingga 100 ml
(Depkes, 1995).
3.4.7 Pereaksi kloralhidrat
Sebanyak 50 g kristal kloralhidrat ditimbang lalu dilarutkan dalam 20
ml air suling (Depkes, 1995).
3.4.8 Pereaksi asam sulfat 2 N
Sebanyak 5,5 ml asam sulfat pekat diencerkan dengan air suling hingga
diperoleh 100 ml (Depkes, 1995).
3.4.9 Pereaksi natrium hidroksida 2 N
Sebanyak 8 g kristal natrium hidroksida dilarutkan dengan air suling
sebanyak 100 ml (Depkes, 1995).
3.4.10 Pereaksi Bouchardat
Sebanyak 4 g kalium iodida dilarutkan dalam air suling secukupnya
kemudian ditambahkan 2 g iodida sedikit demi sedikit cukupkan dengan air
suling (Depkes, 1995).
3.4.11 Pereaksi Liebermann-Burchard
Campur secara perlahan 5 ml asam asetat anhidrit dengan 5 ml asam
sulfat pekat tambahkan etanol hingga 50 ml (Harborne, 1984).
3.5 Pemeriksaan Karakteristik Simplisia
Pemeriksaan karakteristik simplisia meliputi pemeriksaan makroskopik,
penetapan kadar sari yang larut dalam etanol, penetapan kadar abu total,
penetapan kadar abu yang tidak larut dalam asam (WHO, 1998).
3.5.1 Identifikasi makroskopik simplisia
Identifikasi makroskopik simplisia dilakukan dengan mengamati bentuk
luar dari simplisia rumput laut coklat (Sargassum polycystum C.A. Agardh).
3.5.2 Identifikasi mikroskopik simplisia
Pemeriksaan mikroskopik dilakukan terhadap serbuk simplisia rumput
laut coklat. Serbuk simplisia ditaburkan diatas kaca objek yang telah ditetesi
dengan larutan kloralhidrat dan ditutup dengan kaca penutup, kemudian
diamati di bawah mikroskop.
3.5.3 Penetapan kadar air
Penetapan kadar air dilakukan dengan metode Azeotropi (destilasi
toluen). Alat terdiri dari alas bulat 500 ml, alat penampung, pendingin, tabung
penyambung dan tabung penerima.
a. Penjenuhan toluen
Sebanyak 200 ml toluena dan 2 ml air suling dimasukkan ke dalam labu
alas bulat, dipasang alat penampung dan pendingin, kemudian didestilasi
selama 2 jam. Destilasi dihentikan dan dibiarkan dingin selama 30 menit,
kemudian volume air dalam tabung penerima dibaca dengan ketelitian 0,05 ml.
b. Penetapan kadar air simplisia
Sebanyak 5 g serbuk simplisia yang telah ditimbang seksama,
dimasukkan ke dalam labu yang berisi toluen jenuh tersebut, lalu dipanaskan
tetes untuk tiap detik sampai sebagian besar air terdestilasi, kemudian
kecepatan destilasi dinaikkan sampai 4 tetes tiap detik. Setelah semua air
terdestilasi, bagian dalam pendingin dibilas dengan toluen. Destilasi
dilanjutkan selama 5 menit, kemudian tabung penerima dibiarkan mendingin
pada suhu kamar. Setelah air dan toluen memisah sempurna, volume air dibaca
dengan ketelitian 0,05 ml. Selisih kedua volume air yang dibaca sesuai dengan
kandungan air yang terdapat dalam bahan yang diperiksa. Kadar air dihitung
dalam persen (v/b) (WHO, 1998).
3.5.4 Penetapan kadar sari larut dalam air
Sebanyak 5 g serbuk simplisia dimaserasi selama 24 jam dalam 100 ml
air kloroform (2,5 ml kloroform dalam air suling 1000 ml) dalam labu
bersumbat sambil sesekali dikocok selama 6 jam pertama, dibiarkan selama 18
jam, kemudian disaring. Diuapkan 20 ml filtrat sampai kering dalam cawan
penguap yang berdasar rata yang telah dipanaskan dan ditara. Sisa dipanaskan
pada suhu 105°C sampai bobot tetap. Kadar dalam persen sari yang larut dalam
air dihitung (Depkes, 1995).
3.5.5 Penetapan kadar sari yang larut dalam etanol
Sebanyak 5 g serbuk simplisia dimaserasi selama 24 jam dalam 100 ml
etanol 96% dalam labu bersumbat sambil dikocok sesekali selama 6 jam
pertama, kemudian dibiarkan selama 18 jam. Disaring cepat untuk menghindari
penguapan etanol. Sejumlah 20 ml filtrat diuapkan sampai kering dalam cawan
pada suhu 105ºC sampai bobot tetap. Hitung persen kadar sari yang larut dalam
etanol 96% (Depkes, 1995).
3.5.6 Penetapan kadar abu total
Sebanyak 2 g serbuk yang telah digerus dan ditimbang seksama
dimasukkan dalam krus porselin yang telah dipijar dan ditara, kemudian
diratakan. Krus dipijar perlahan-lahan sampai arang habis, pijaran dilakukan pada
suhu 600ºC selama 3 jam kemudian didinginkan dan ditimbang sampai diperoleh
bobot tetap. Hitung persen kadar abu (Depkes, 1995).
3.5.7 Penetapan kadar abu yang tidak larut dalam asam
Abu yang diperoleh dalam penetapan kadar abu dididihkan dalam 25 ml
asam klorida encer selama 5 menit, bagian yang tidak larut dalam asam
dikumpulkan, disaring melalui kertas saring dipijarkan sampai bobot tetap,
kemudian didinginkan dan ditimbang. Hitung persen kadar yang tidak larut
dalam asam (Depkes, 1995).
3.6 Skrining Fitokimia
Skrining fitokimia dilakukan menurut Depkes (1979) dan Farnsworth
(1966) untuk mengetahui golongan senyawa alkaloida, flavonoid, glikosida,
glikosida antrakinon, saponin, tanin, dan steroida/triterpenoida.
3.6.1 Pemeriksaan alkaloida
Ekstrak diitimbang sebanyak 0,5 g kemudian ditambahkan 1 ml asam
klorida 2 N dan 9 ml air suling, dipanaskan diatas penangas air selama 2 menit,
diambil tabung reaksi, lalu kedalamnya dimasukkan 0,5 ml filtrat. Pada
masing-masing tabung reaksi
1. ditambahkan 2 tetes pereaksi Mayer
2. ditambahkan 2 tetes pereaksi Bouchardat
3. ditambahkan 2 tetes pereaksi Dragendorff
Alkaloida positif jika terjadi endapan atau kekeruhkan pada paling sedikit dua
hari tiga percobaan diatas (Depkes, 1995).
3.6.2 Pemeriksaan flavonoida
Sebanyak 10 g ekstrak ditambahkan 10 ml air panas, dididihkan selama
5 menit dan disaring dalam keadaan panas, ke dalam 5 ml filtrat ditambahkan
0,1 g serbuk magnesium dan 1 ml asam klorida pekat dan 2 ml amil alkohol,
dikocok dan dibiarkan memisah. Flavonoida positif jika terjadi warna merah
atau kuning atau jingga pada lapisan amil alkohol (Farnsworth, 1966).
3.6.3 Pemeriksaan glikosida
Ekstrak ditimbang sebanyak 3 g, lalu disari dengan 30 ml campuran
etanol 95% dengan air (7:3) dan 10 ml asam klorida 2 N, direfluks selama 2
jam, didinginkan dan disaring. Diambil 20 ml filrat ditambahkan 25 ml air
suling dan 25 ml timbal (II) asetat 0,4 M, dikocok, didiamkan 5 menit lalu
disaring. Filtrat disari dengan 20 ml campuran isopropanol dan kloroform
(2:3), dilakukan berulang sebanyak 3 kali. Sari air dikumpulkan dan diuapkan
pada temperatur tidak lebih dari 50ºC. Sisanya dilarutkan dalam 2 ml metanol.
Larutan sisa digunakan untuk percobaan berikut: 0,1 ml larutan percobaan
ditambahkan 2 ml air dan 5 tetes pereaksi Mollish. Kemudian secara
perlahan-lahan ditambahkan 2 ml asam sulfat pekat melalui dinding tabung,
terbentuknya cincin berwarna ungu pada batas kedua cairan menunjukkan
glikosida (Depkes, 1995).
3.6.4 Pemeriksaan glikosida antrakinon
Ekstrak ditimbang sebanyak 0,2 g, kemudian ditambahkan 5 ml asam
sulfat 2 N, dipanaskan sebentar, setelah dingin ditambahkan 10 ml benzena,
dikocok dan didiamkan. Lapisan benzena dipisahkan dan disaring, kocok lapisan
benzena dengan 2 ml NaOH 2 N, didiamkan. Lapisan air berwarna merah dan
lapisan benzena tidak berwarna menunjukan adanya antrakinon (Depkes, 1995).
3.6.5 Pemeriksaan saponin
Ekstrak ditimbang sebanyak 0,5 g dan dimasukan ke dalam tabung
reaksi, lalu ditambahkan 10 ml air panas, dinginkan kemudian dikocok
kuat-kuat selama 10 detik. Jika terbentuk busa setinggi 1-10 cm yang stabil tidak
kurang dari 10 menit dan tidak hilang dengan penambahan 1 tetes asam klorida
2N menunjukan adanya saponin (Depkes, 1995).
3.6.6 Pemeriksaan tanin
Ekstrak ditimbang sebanyak 1 g, dididihkan selama 3 menit dalam 100
ml air suling lalu didinginkan dan disaring. Pada filtrat ditambahkan 1-2 tetes
peraksi besi (III) klorida 1%. Jika terjadi warna biru kehitaman atau hijau
3.6.7 Pemeriksaan steroida/triterpenoida
Sebanyak 1 g sampel dimaserasi dengan 20 ml n-heksan selama 2 jam,
lalu disaring. Filtrat diuapkan dalam cawan penguap. Pada sisa ditambahkan
beberapa tetes pereaksi Liebermann-Burchard. Timbulnya warna biru atau biru
hijau menunjukan adanya steroida, sedangkan warna merah, merah muda atau
ungu menunjukkan adanya triterpenoida (Harborne, 1984).
3.7 Pembuatan Ekstrak Rumput Laut Coklat
Pembuatan ekstrak rumput laut coklat dilakukan secara perkolasi bertahap.
Prosedur pembuatan ekstrak: sebanyak 500 g serbuk simplisia dibasahi dengan n
-heksan dan dibiarkan selama 3 jam. Kemudian dimasukkan ke dalam alat
perkolator, lalu dituang cairan penyari n-heksan sampai semua simplisia terendam
dan terdapat selapis cairan penyari diatasnya, mulut tabung perkolator ditutup
dengan alumunium foil dan dibiarkan selama 24 jam, kemudian kran dibuka dan
dibiarkan tetesan ekstrak mengalir dengan kecepatan perkolat diatur 1 ml/menit,
perkolat ditampung. Perkolasi dihentikan jika 500 mg perkolat yang keluar
terakhir diuapkan, tidak meninggalkan sisa. Perkolat yang diperoleh kemudian
dipekatkan dengan alat rotary evaporator setelah itu di freeze dryer hingga
diperoleh ekstrak kental. Ampas dikeringkan lalu diekstraksi dengan
menggunakan pelarut berturut-turut etilasetat dan etanol dengan prosedur yang
3.8 Pengujian Kemampuan Antioksidan dengan Spektrofotometer Visibel
3.8.1 Metode β-karoten-asam linoleat 3.8.1.1 Pembuatan larutan blanko
Asam linoleat 20 mg dan tween 40 200 mg dimasukkan kedalam labu
erlenmeyer 50 ml, kemudian ditambahkan 10 ml air suling dan 40 ml air
beroksigen (Rosidah, et al., 2008).
3.8.1.2 Pembuatan larutan stok β-karoten
Serbuk β-karoten 1 mg dalam 1 ml kloroform dan ditambah dengan 20
mg asam linoleat dan 200 mg tween 40. Kloroform kemudian diuapkan dari
campuran dengan rotavapor. Residu yang tertinggal dilarutkan dengan 10 ml
air suling, dicampur sehingga homogen lalu ditambahkan 40 ml air beroksigen,
dicampur homogen (Rosidah, et al., 2008).
3.8.1.3 Pembuatan larutan induk sampel uji ekstrak n-heksan rumput laut coklat (ENSP)
Sebanyak 125 mg masing-masing sampel uji ekstrak n-heksan
ditimbang, dimasukkan ke dalam labu tentukur 25 ml dilarutkan dengan etanol
lalu volumenya dicukupkan dengan etanol sampai garis tanda (konsentrasi
5000 ppm).
3.8.1.4 Pembuatan larutan induk sampel uji ekstrak etilasetat rumput laut coklat (EEASP)
Sebanyak 125 mg masing-masing sampel uji ekstrak etilasetat
ditimbang, dimasukkan ke dalam labu tentukur 25 ml dilarutkan dengan etanol
lalu volumenya dicukupkan dengan etanol sampai garis tanda (konsentrasi
3.8.1.5 Pembuatan larutan induk sampel uji ekstrak etanol rumput laut coklat (EESP)
Sebanyak 125 mg masing-masing sampel uji ekstrak etanol ditimbang,
dimasukkan ke dalam labu tentukur 25 ml dilarutkan dengan etanol lalu
volumenya dicukupkan dengan etanol sampai garis tanda (konsentrasi 5000
ppm).
3.8.1.6 Pembuatan larutan uji ekstrak n-heksan rumput laut coklat
Larutan induk ENSP dipipet sebanyak 4 ml; 6 ml; 8 ml kemudian
dimasukkan ke dalam labu tentukur 10 ml dengan etanol lalu volumenya
dicukupkan dengan etanol sampai garis tanda (untuk mendapatkan konsentrasi
2000 ppm, 3000 ppm, 4000 ppm).
3.8.1.7 Pembuatan larutan uji ekstrak etilasetat rumput laut coklat
Larutan induk EEASP dipipet sebanyak 4 ml; 6 ml; 8 ml kemudian
dimasukkan ke dalam labu tentukur 10 ml dengan etanol lalu volumenya
dicukupkan dengan etanol sampai garis tanda (untuk mendapatkan konsentrasi
2000 ppm, 3000 ppm, 4000 ppm).
3.8.1.8 Pembuatan larutan uji ekstrak etanol rumput laut coklat
Larutan induk EESP dipipet sebanyak 4 ml; 6 ml; 8 ml kemudian
dimasukkan ke dalam labu tentukur 10 ml dengan etanol lalu volumenya
dicukupkan dengan etanol sampai garis tanda (untuk mendapatkan konsentrasi
3.8.1.9 Pembuatan larutan pembanding butil hidroksitoluen (BHT) dan kuersetin
Sebanyak 5 mg masing-masing butil hidroksitoluena (BHT) dan
kuersetin ditimbang, kemudian dilarutkan dalam labu tentukur 50 ml dengan
etanol, lalu volumenya dicukupkan dengan etanol sampai garis tanda
(konsentrasi 100 ppm).
3.8.1.10 Penentuan aktivitas antioksidan ekstrak n-heksan, etilasetat dan etanol rumput laut coklat menggunakan metode β-karoten-asam linoleat
Larutan stok β-karoten sebanyak 4 ml dipipet ke dalam tabung-tabung
uji yang masing-masing berisi 0,2 ml larutan ekstrak n-heksan rumput laut
coklat (konsentrasi 2000 ppm, 3000 ppm, dan 4000 ppm), butil hidroksitoluena
(konsentrasi 100 ppm), dan kuersetin (konsentrasi 100 ppm). Penyerapan UV
setiap sampel dan blanko (tanpa β-karoten) diukur langsung (0 menit) sampai
120 menit pada panjang gelombang 470 nm dengan spektrofotometer.
Pengukuran diulang sebanyak 3 kali untuk setiap ekstrak etil asetat dan etanol
seperti prosedur yang dilakukan diatas. Aktivitas Antioksidan (AA) ditentukan
dengan menggunakan rumus berikut:
AA = 100[1− ( A −A ) ( A −A )]
A0 dan A00 ialah serapan sampel dan blanko pada waktu 0 menit. At dan
At0 ialah serapan sampel dan blanko pada waktu t menit (Rosidah, et al., 2008).
Pengujian yang sama dilakukan pada larutan ekstrak etilasetat dan
etanol rumput laut coklat dengan prosedur yang sama seperti yang dilakukan di
BAB IV
HASIL DAN PEMBAHASAN
Tumbuhan yang telah diidentifikasi di Lembaga Ilmu Pengetahuan
Indonesia (Indonesian Institute of Science) Pusat Penelitian Oseanografi
(Research Center for Oceanography), Jl. Pasir Putih I, Ancol Timur, Jakarta
adalah Sargassum polycystum C.A. Agardh suku Sargassaceae.
Hasil pemeriksaan makroskopik rumput laut coklat segar memiliki
bentuk thalli silindris berduri-duri kecil merapat, holdfast membentuk cakram
kecil dengan diatasnya secara karakteristik terdapat stolon yang rimbun
berekspansi ke segala arah. Batang pendek dengan percabangan utama tumbuh
rimbun di bagian ujungnya. Daun kecil, lonjong, pinggir bergerigi, ujung
melengkung rata atau runcing, urat daun tidak begitu jelas. Warna coklat
kehitaman, berbau khas, dan tidak berasa.
Hasil pemeriksaan mikroskopik serbuk simplisia rumput laut coklat
dicirikan dengan adanya sel-sel parenkim, sel-sel parenkim yang berisi pigmen
berwarna coklat dan sel-sel propagule.
Hasil pemeriksaan kadar air, kadar sari larut dalam air, kadar sari larut
dalam etanol, kadar abu total dan kadar abu yang tidak larut asam dapat
Tabel 4.1 Hasil pemeriksaan karakteristik simplisia rumput laut coklat Sargassum polycystum C.A. Agardh
No. Parameter Hasil (%)
1. Kadar air 5,95
2. Kadar sari larut dalam air 10,28
3. Kadar sari larut dalam etanol 4,01
4. Kadar abu total 18,13
5. Kadar abu tidak larut dalam asam 2,55
Hasil pemeriksaan kadar air dari serbuk simplisia rumput laut coklat
memenuhi persyaratan dari buku Materia Medika Indonesia yaitu tidak
melebihi dari 10%. Kadar air yang melebihi persyaratan memungkinkan
pertumbuhan jamur. Penetapan kadar sari larut dalam air dan etanol serta
penetapan kadar abu total dan kadar abu tidak larut dalam asam pada umumnya
memiliki persyaratan yang berbeda-beda pada tiap simplisia. Karakteristik
simplisia pada serbuk rumput laut coklat tidak tercantum dalam buku Materia
Medika Indonesia. Penetapan kadar sari yang larut dalam air untuk mengetahui
kadar sari yang larut dalam air. Penetapan kadar sari larut dalam etanol adalah
untuk mengetahui kadar sari senyawa-senyawa yang larut dalam pelarut polar.
Penetapan kadar abu total untuk mengetahui kadar zat anorganik pada simplisia
sedangkan penetapan kadar abu tidak larut dalam asam untuk mengetahui
kadar zat anorganik yang tidak larut dalam asam (Depkes, 1978).
Hasil skrining fitokimia dari serbuk simplisia rumput laut coklat dapat
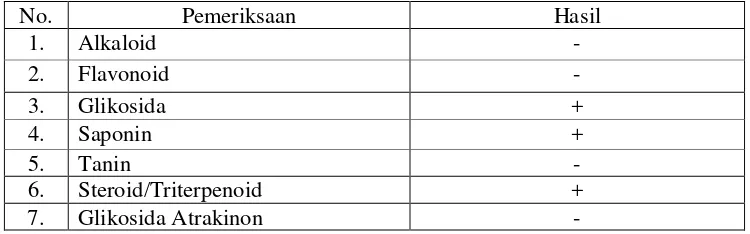
[image:46.612.132.500.130.221.2]Tabel 4.2 Hasil skrining fitokimia simplisia rumput laut coklat Sargassum polycystum C.A. Agardh
No. Pemeriksaan Hasil
1. Alkaloid -
2. Flavonoid -
3. Glikosida +
4. Saponin +
5. Tanin -
6. Steroid/Triterpenoid +
7. Glikosida Atrakinon -
Hasil skrining fitokimia menunjukkan adanya senyawa saponin,
steroid/triterpenoid, dan glikosida. Senyawa-senyawa tersebut bertindak
sebagai penangkap radikal bebas karena gugus hidroksil yang dikandungnya
dapat mendonorkan hidrogen kepada radikal bebas (Kumalaningsih, 2006;
Silalahi, 2006). Hasil di atas menunjukkan bahwa simplisia rumput laut coklat
memiliki potensi sebagai antioksidan.
Hasil uji aktivitas antioksidan ekstrak rumput laut coklat dengan
metode β-karoten-asam linoleat didasarkan atas hilangnya warna β-karoten
oleh adanya radikal bebas yaitu hidroperoksid yang berasal dari asam linoleat. β-karoten akan kehilangan sifatnya sebagai antioksidan karena terjadi proses
oksidasi yang menyebabkan ikatan rangkap pada β-karoten berikatan dengan
atom hidrogen dari salah satu gugus metilen dialil pada asam linoleat, sehingga β-karoten akan kehilangan gugus kromofor yang memberikan warna jingga.
Intensitas warna β-karoten dapat diukur pada panjang gelombang 470 nm.
[image:47.612.125.500.130.247.2]Tabel 4.3 Persentase aktivitas antioksidan ekstrak n-heksan rumput laut coklat Sargassum polycystum C.A. Agardh dari berbagai konsentrasi
dengan metode β-karoten-asam linoleat
Waktu
% Aktivitas antioksidan ENSP 2000 ppm ENSP 3000 ppm ENSP 4000 ppm BHT 100 ppm Kuersetin 100 ppm
0 0,00 0,00 0,00 0,00 0,00
15 5,56 6,04 6,21 44,99 41,86
30 6,08 6,89 7,64 60,42 59,50
45 7,10 7,79 8,72 68,51 55,76
60 5,46 5,98 8,04 65,17 52,07
75 5,07 5,09 7,35 62,14 47,16
90 4,44 4,89 7,07 58,38 37,69
105 3,30 4,12 6,17 53,07 33,78
120 1,57 3,13 5,48 44,97 33,24
Tabel 4.4 Persentase aktivitas antioksidan ekstrak etilasetat rumput laut coklat Sargassum polycystum C.A. Agardh dari berbagai konsentrasi
dengan metode β-karoten-asam linoleat
Waktu
% Aktivitas antioksidan EEASP 2000 ppm EEASP 3000 ppm EEASP 4000 ppm BHT 100 ppm Kuersetin 100 ppm
0 0,00 0,00 0,00 0,00 0,00
15 6,75 6,75 8,05 44,99 41,86
30 7,36 8,08 8,81 60,42 59,50
45 7,89 9,22 9,49 68,51 55,76
60 7,40 8,95 8,73 65,17 52,07
75 7,33 8,37 8,54 62,14 47,16
90 7,01 7,94 8,18 58,38 37,69
105 6,49 6,92 8,02 53,07 33,78
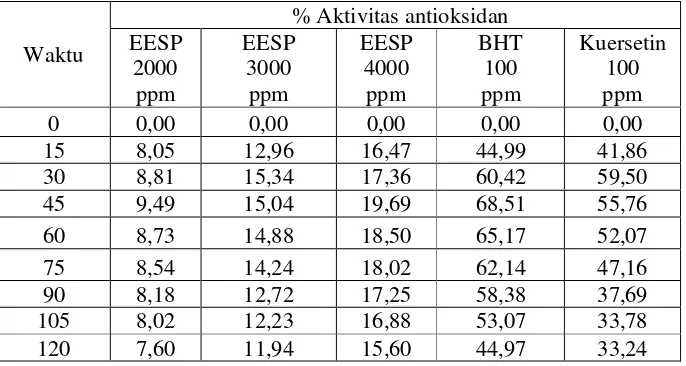
[image:48.612.131.476.399.580.2]Tabel 4.5 Persentase aktivitas antioksidan ekstrak etanol rumput laut coklat Sargassum polycystum C.A. Agardh dari berbagai konsentrasi
dengan metode β-karoten-asam linoleat
Waktu
% Aktivitas antioksidan EESP 2000 ppm EESP 3000 ppm EESP 4000 ppm BHT 100 ppm Kuersetin 100 ppm
0 0,00 0,00 0,00 0,00 0,00
15 8,05 12,96 16,47 44,99 41,86
30 8,81 15,34 17,36 60,42 59,50
45 9,49 15,04 19,69 68,51 55,76
60 8,73 14,88 18,50 65,17 52,07
75 8,54 14,24 18,02 62,14 47,16
90 8,18 12,72 17,25 58,38 37,69
105 8,02 12,23 16,88 53,07 33,78
120 7,60 11,94 15,60 44,97 33,24
Data persentase aktivitas antioksidan pada Tabel 4.3, 4.4, dan 4.5
terlihat bahwa persentase aktivitas antioksidan EESP > EEASP > ENSP.
Persentase aktivitas antioksidan pembanding butil hidroksitoluena (BHT) >
kuersetin (masing-masing dengan konsentrasi 100 ppm). Jika persentase
aktivitas antioksidan ekstrak dan pembanding dibandingkan maka diperoleh
aktivitas antioksidan BHT 100 ppm > kuersertin 100 ppm > EESP > EEASP >
ENSP. Jika dihubungkan dengan aktivitas antioksidan dari segi konsentrasi
maka konsentrasi EESP 4000 ppm > EESP 3000 ppm > EESP 2000 ppm.
Hubungan antara aktivitas antioksidan ENSP, butil hidroksitoluena
(BHT), dan kuersertin dengan konsentrasi yang berbeda dapat dilihat Gambar
[image:49.612.133.476.143.326.2]Gambar 4.1 Grafik persentase aktivitas antioksidan versus waktu ekstrak n-heksan rumput laut coklat Sargassum polycystum C.A. Agardh ENSP, BHT, dan kuersetin
Gambar 4.1 terlihat bahwa aktivitas antioksidan ekstrak n-heksan
rumput laut coklat dari tiga konsentrasi berbeda (2000, 3000, 4000 ppm).
Apabila dibandingkan dengan aktivitas pembanding maka BHT (100 ppm) >
kuersetin (100 ppm) > ENSP (4000 ppm) > ENSP (3000 ppm) > ENSP (2000
ppm).
Hubungan antara aktivitas antioksidan EEASP, butil hidroksitoluena
(BHT), dan kuersetin dengan konsentrasi yang berbeda dapat dilihat Gambar
4.2 berikut ini:
Gambar 4.2 Grafik persentase aktivitas antioksidan versus waktu ekstrak etilasetat rumput laut coklat Sargassum polycystum C.A. Agardh EEASP, BHT, dan kuersetin
0 5 10 15 20 25 30 35 40 45 50 55 60 65 70 75 80 85 90 95 100
0 15 30 45 60 75 90 105 120
ENSP 2000 ENSP 3000 ENSP 4000 0 5 10 15 20 25 30 35 40 45 50 55 60 65 70 75 80 85 90 95 100
0 15 30 45 60 75 90 105 120
[image:50.612.134.490.91.231.2] [image:50.6