PENGARUH DERAJAT DEASETILASI KITOSAN TERHADAP
KADAR PLUMBUM (Pb) DARAH DAN AKTIVITAS ENZIM
DELTA AMINOLEVULINIC ACID DEHYDRATASE ( -ALAD)
MENCIT ALBINO (
Mus musculus
L.)
TESIS
Oleh
SUHARSIH
057008003/BM
PENGARUH DERAJAT DEASETILASI KITOSAN TERHADAP
KADAR PLUMBUM (Pb) DARAH DAN AKTIVITAS ENZIM
DELTA AMINOLEVULINIC ACID DEHYDRATASE ( -ALAD)
MENCIT ALBINO (
Mus musculus
L.)
TESIS
Untuk Memperoleh Gelar Magister Kesehatan
dalam Program Studi Biomedik
pada Sekolah Pascasarjana Universitas Sumatera Utara
Oleh
SUHARSIH
057008003/BM
SEKOLAH PASCASARJANA
UNIVERSITAS SUMATERA UTARA
Judul Tesis : PENGARUH DERAJAT DEASETILASI
KITOSAN TERHADAP KADAR PLUMBUM (Pb) DARAH DAN AKTIVITAS ENZIM DELTA
AMINOLEVULINIC ACID DEHYDRATASE ( -ALAD) MENCIT ALBINO (Mus musculus L.) Nama Mahasiswa : Suharsih
Nomor Pokok : 057008003 Program Studi : Biomedik
Menyetujui, Komisi Pembimbing
( Dr. Ramlan Silaban, M.Si ) ( Dr. Harry Agusnar, M.Sc, M.Phil )
Ketua Anggota
Ketua Program Studi, Direktur,
Tanggal lulus : 12 Agustus 2008 Telah diuji pada
Tanggal : 12 Agustus 2008
PANITIA PENGUJI TESIS
Ketua : Dr. Ramlan Silaban, M.Si
Anggota : 1. Dr. Harry Agusnar, M.Sc, M.Phil
ABSTRAK
Pencemaran lingkungan oleh plumbum (Pb) antara lain diakibatkan oleh pertambangan, industri yang menggunakan Pb, dan asap kenderaan bermotor. Plumbum dapat mengganggu aktivitas enzim delta aminolevulinic acid dehydratase ( -ALAD), enzim yang berperan dalam biosintesa hemoglobin. Kitosan merupakan biopolimer alami hasil dari deasetilasi kitin, memiliki kemampuan untuk mengikat logam berat. Kemampuan kitosan dipengaruhi oleh derajat deasetilasi, berat molekul, dan viskositas.
Penelitian ini bertujuan untuk mengetahui pengaruh derajat deasetilasi kitosan terhadap kadar plumbum darah, aktivitas enzim -ALAD, dan kadar hemoglobin pada mencit yang telah dipapar plumbum.
Penelitian ini menggunakan 30 ekor mencit jantan strain BALBC yang dibagi menjadi 10 kelompok, masing-masing kelompok terdiri dari 3 ekor mencit. Kelompok K0 (kontrol aquades), K1 (kontrol Pb), K2 (kontrol asetat), K3 (kontrol kitosan), P1 (Pb asetat + kitosan A 1 %), P2 (Pb asetat + kitosan A 2 %), P3 (Pb asetat + kitosan B 1 %), P4 (Pb asetat + kitosan B 2 %), P5 (Pb asetat + kitosan C 1 %), dan P6 (Pb asetat + kitosan C 2 %). Perlakuan diberikan secara oral dengan menggunakan jarum gavage dengan volume pemberian 0,01 mL/g BB selama 14 hari. Data yang diperoleh dianalisis dengan uji anova satu arah dan jika terdapat perbedaan nyata dilanjutkan dengan uji BNT (Beda Nyata Terkecil).
Hasil penelitian menunjukkan bahwa kadar plumbum darah pada kelompok K1 (0,33 µg/100 mL) tidak berbeda nyata (p>0,05) dengan kelompok P1, P2, P3, P4, P5, dan P6, tetapi dari rata-rata kadar Pb darah pada kelompok perlakuan tersebut cenderung menurun. Aktivitas enzim -ALAD pada kelompok K3 (1,2 µmol PBG/jam/L eritrosit) meningkat dan berbeda nyata (p<0,05) dengan kelompok K0, K1, K2, P1, P2, P3, P4, dan P5. Aktivitas enzim -ALAD pada kelompok P6 lebih tinggi dan berbeda nyata (p<0,05) dengan kelompok P1, P3, dan P5. Kadar Hb darah pada kelompok K1 (12 g/dL) mengalami penurunan yang nyata (p<0,05) dibandingkan dengan semua kelompok perlakuan yang lain. Kadar Hb kelompok P6 mengalami peningkatan yang nyata dibandingkan dengan kelompok P1 dan P2.
ABSTRACT
Environmental lead pollution is caused by mining, industries which use lead, and vehicle exhaust. Lead inhibits of delta amino levulinic acid dehydratase ( -ALAD) activity, a cytosolic enzyme involved in haemoglobin biosynthesis. Chitosan is a natural biopolymer derived by deacetylation of chitin,and is known for its ability to bind heavy metals. The chelating capacity of chitosan is influenced by the degree of deacetylation (DD), the molecular weight (MW) and the viscosity of the chitosan compound used.
The aim of the present study is to know the effect of the degree of deacetylation on the blood lead concentration, the activity of -ALAD, and the haemoglobin content in the blood of mice exposed to lead.
This study used 30 BALBC male mice divided into 10 groups. Each group consisted of 3 mice.The groups were : K0 (aquadest control), K1 (Pb acetate control), K2 (acetic acid control), K3 (chitosan control), P1 (Pb + chitosan A 1%), P2 (Pb + chitosan A 2 %), P3 (Pb + chitosan B 1 %), P4 (Pb + chitosan B 2 %), P5 (Pb + chitosan C 1 %), P6 (Pb + chitosan C 2 %). The treatment was given orally by a
gavage needle at a volume 0,01 mL/g b.w. over 14 days. The data was analyzed with the one way Anova Test, and if significant results were found the LSD Test ( Least Significant Difference) wasa needed.
The results showed that the blood lead concentration in the K1 group (0,33 µg/100 mL) was not significant (p>0.05) as compared to groups P1, P2, P3, P4, P5, and P6, although in all cases the blood lead concentration was reduced. The activity of -ALAD in the K3 group (1,2 µmol PBG/hr/L erythrocyte) was increased significantly (p<0,05) as compared to groups K0, K1, K2, P1, P2, P3, P4, and P5. The activity of -ALAD in the P6 group was not different from K3, but was significantly higher (p<0,05) than groups P1, P3, and P5. The haemoglobin content in the K1 group (12 g/dL) was significantly decreased compared to other groups. The haemoglobin content in the P6 group was significantly increased compared to groups P1 and P2.
KATA PENGANTAR
Alhamdulillah, puji syukur kehadirat Allah SWT yang Maha Pengasih lagi
Maha Penyayang serta atas segala rahmat dan karuniaNya sehingga penulis dapat
menyelesaikan penelitian dengan judul “Pengaruh Derajat Deasetilasi Kitosan
terhadap Kadar Plumbum (Pb) Darah dan Aktivitas Enzim Delta Aminolevulinic
Acid Dehydratase ( -ALAD) Mencit Albino(Mus musculus L.)”.
Tesis ini merupakan salah satu syarat yang harus dilaksanakan penulis dalam
rangka memenuhi persyaratan untuk meraih gelar Magister Kesehatan (M.Kes) pada
Sekolah Pascasarjana Universitas Sumatera Utara.
Dengan selesainya tesis ini, maka perkenankanlah penulis mengucapkan
terima kasih yang sebesar-besarnya kepada :
Rektor Universitas Sumatera Utara, Bapak Prof. Chairuddin P. Lubis, DTM
& H, SpA(K) yang telah memberikan kesempatan kepada penulis untuk mengikuti
pendidikan di Sekolah Pascasarjana USU Medan.
Direktur Sekolah Pascasarjana USU Medan, Ibu Prof. Dr. Ir. T. Chairun Nisa
B.MSc., dan Ketua Program Studi Biomedik dr. Yahwardiah Siregar, PhD., atas
kesempatan dan fasilitas yang telah diberikan kepada penulis untuk mengikuti dan
Terimakasih yang tidak terhingga dan penghargaan yang setingi-tingginya
penulis sampaikan kepada Bapak Dr. Ramlan Silaban, M.Si (ketua komisi
pembimbing) dan Bapak Dr. Harry Agusnar, M.Sc. M.Phil, (anggota komisi
pembimbing) yang dengan penuh perhatian dan kesabaran telah mengorbankan waktu
untuk memberikan dorongan, bimbingan, semangat, bantuan, serta saran-saran yang
bermanfaat kepada Penulis mulai dari penyusunan proposal, persiapan penelitian
sampai pada penyelesaian tesis ini.
Terima kasih kepada komisi penguji Bapak Dr. Dwi Suryanto, M.Sc dan Ibu
Dr. Rumondang Bulan, M.Si yang telah bersedia dengan sabar membantu Penulis
dalam menyempurnakan, menguji, dan menilai tesis ini. Tak lupa terima kasih juga
Penulis sampaikan kepada semua dosen yang telah membimbing Penulis selama
mengikuti program magister ini.
Persembahan terima kasih tulus, rasa hormat dan sembah sujud kepada
ayahanda dan ibunda tercinta (H.Sarudji dan Hj.Tunam) yang telah membesarkan
dengan susah payah dengan penuh kasih sayang dan atas dukungan serta semangat
mereka inilah Penulis dapat menjalani pendidikan hingga pascasarjana. Semoga
ALLAH SWT mengampuni dan selalu merahmati kedua ayahanda dan ibunda
Penulis. Buat kakanda Siti Khadijah, kakanda Miswanto, S.SM., kakanda Syamsiah,
ST., kakanda Sulastri, kakanda Sriani, S.Pd., dan adinda Supriyanti serta
Terima kasih juga Penulis sampaikan kepada teman-teman : Emni
Purwonigsih, S.Si., T. M. Fauzi, S.Si., dr. T. Helvi Mardiani, dan dr. Dwi Rita
Anggraini, M.Kes., atas dorongan semangat sehingga tesis ini dapat selesai. Dan
kepada semua pihak yang telah membantu penyelesaian tesis ini, Penulis ucapkan
terima kasih.
Penulis menyadari atas ketidaksempurnaan tulisan ini. Oleh karena itu penulis
mengaharapkan kritik dan saran. Semoga tulisan ini bermanfaat bagi kita semua.
Medan, 12 Agustus 2008
Penulis,
(Suharsih)
RIWAYAT HIDUP
1. Nama : Suharsih
2. Tempat/Tanggal Lahir : Medan, 9 Juni 1975
3. Agama : Islam
4. Status : Belum Menikah
5. Alamat : Jl. Pancing V/46 Kelurahan Besar. Medan Labuhan
6. Telp/HP : 061-6852939/085261188796/081260001781
7. Pendidikan
SD Al-Washliyah 30 Medan : 1982-1988
M.Ts Proyek Depag Medan : 1988-1992
MAN-1 Medan : 1992-1995
Sarjana (S1) FMIPA USU : 1995-2002
Akta Mengajar IV UMN : 2004-2005
Sekolah Pascasarjana, Program Biomedik USU : 2005-2008
8. Riwayat Pekerjaan
Staf Pengajar di AAK Sari Mutiara Medan : 2002-2006
DAFTAR ISI
Halaman
ABSTRAK ... iv
ABSTRACT... v
KATA PENGANTAR ... vi
RIWAYAT HIDUP... ix
DAFTAR ISI... x
DAFTAR TABEL... xiii
DAFTAR GAMBAR ... xiv
DAFTAR LAMPIRAN... xv
BAB I. PENDAHULUAN ... 1
1.1. Latar Belakang ... 1
1.2. Perumusan Masalah ... 5
1.4. Tujuan Penelitian ... 7
1.5. Hipotesis... 7
1.6. Manfaat Penelitian ... 8
BAB II. TINJAUAN PUSTAKA... 9
2.1. Plumbum (Pb) ... 9
2.1.1. Keracunan Plumbum ... 9
2.1.2. Pengaruh Plumbum pada Sistem Peredaran Darah ... 11
2.1.3. Monitoring Plumbum dalam Tubuh Manusia ... 12
2.2. Aktivitas Enzim... 12
2.3. Biosintesis Hemoglobin ... 15
2.4. Bahan Pengkelat... 16
2.5. Kitosan ... 16
2.5.1. Sifat-sifat dan Penggunaan Kitosan ... 17
2.5.2. Derajat Deasetilasi Kitosan ... 19
2.5.3. Pengkelat kitosan dengan Ion-Ion Logam ... 20
BAB III. METODOLOGI PENELITIAN ... 21
3.1. Desain Penelitian... 21
3.2. Tempat dan Waktu Penelitian ... 21
3.3. Sampel Penelitian ... 21
3.4.2. Variabel Dependent ... 22
3.5. Rancangan Penelitian ... 22
3.6. Pelaksanaan Penelitian ... 23
3.6.1. Prosedur Penentuan Derajat Deasetilasi Kitosan ... 24
3.6.2. Pengambilan Sampel Darah ... 24
3.6.3. Pembuatan Larutan Pereaksi untuk Analisis Enzim -ALAD ... 24
3.7.4. Persentase Derajat Deasetilasi Kitosan... 29
4.2. Pembahasan... 36
BAB V. KESIMPULAN DAN SARAN... 40
5.1. Kesimpulan ... 40
5.2. Saran... 41
DAFTAR PUSTAKA ... 42
DAFTAR TABEL Nomor Judul Halaman 1. Tingkat Keracunan Pb di Darah dan Efeknya pada Anak-anak... 10
2. Pemanfaatan Kitosan pada Beberapa Industri……… 19
3. Hasil Uji Beda Nyata Terkecil Rata-Rata Aktivitas Enzim -ALAD pada Kelompok Perlakuan ... 33
DAFTAR GAMBAR
Nomor Judul Halaman
1. Bagan Kerangka Teori Pengaruh Kitosan terhadap Kadar
Pb Darah dan Aktivitas Enzim -ALAD ... 6
2. Diagram Alir Gangguan Timah Hitam (Pb) terhadap Biosintesis Hemoglobin... 14
3. Struktur Selulosa, Kitin, dan Kitosan ……… 17
4. Mekanisme Pengikatan Logam Berat oleh Kitosan... 18
5. Grafik Rata-Rata Kadar Pb Darah Mencit ……… 30
6. Grafik Rata-Rata Aktivitas Enzim -ALAD ………. 32
DAFTAR LAMPIRAN
Nomor Judul Halaman
1. Persetujuan Komisi Etik tentang Pelaksanaan
Penelitian Bidang Kesehatan... 47
2. Gambar Hasil Spektroskopi FT-IR Kitosan A... 48
3. Perhitungan Hasil Penentuan Derajat Deasetilasi Kitosan A... 49
4. Gambar Hasil Spektroskopi FT-IR Kitosan B... 50
5. Perhitungan Hasil Penentuan Derajat Deasetilasi Kitosan B….. 51
6. Gambar Hasil Spektroskopi FT-IR Kitosan C... 52
7. Perhitungan Hasil Penentuan Derajat Deasetilasi Kitosan C….. 53
10. Bagan Alir Penentuan Kadar Pb Darah………... 56
11. Bagan Alir Penentuan Hematokrit……… .. 57
BAB I
PENDAHULUAN
1.1. Latar Belakang
Polusi logam berat termasuk plumbum (Pb) merupakan masalah yang serius
di negara-negara maju maupun negara berkembang seperti Indonesia. Polusi
plumbum di lingkungan hidup biasanya berkaitan erat dengan proses pertambangan,
peleburan logam, industri yang menggunakan bahan baku plumbum (misalnya pabrik
cat, kabel, enamel, gelas, baterai dan pestisida), dan tidak kalah pentingnya, plumbum
juga dapat berasal dari asap kenderaan bermotor. Baku mutu udara untuk plumbum
adalah 0,06 µg/m3. Sedangkan dalam air minum, plumbum dapat berasal dari
kontaminasi pipa, solder dan kran air. Kandungan plumbum dalam air sebesar 15
mg/L dianggap sebagai konsentrasi yang aman untuk dikonsumsi. Dalam makanan,
plumbum berasal dari kontaminasi kaleng makanan dan minuman dan solder yang
bertimbal (Dharwiyanti, 2004; Nasution, 2004; Hariono, 2005).
Absorbsi plumbum dapat melalui berbagai cara misalnya saluran pernafasan,
pencernaan, dan permukaan kulit (Bartik, 1981). Plumbum merupakan jenis logam
berat yang bersifat toksik bagi tubuh manusia. Organ-organ tubuh yang menjadi
sasaran dari keracunan timbal adalah sistem peredaran darah, sistem saraf, sistem
Plumbum dalam darah pada kadar tertentu dapat berpengaruh terhadap
biosintesis heme pada beberapa tahap reaksi enzimatis. Plumbum berkemampuan
berikatan dengan gugus –SH dalam molekul protein dan menyebabkan hambatan
pada aktivitas kerja sistem enzim. Plumbum mengganggu sistem sintesis Hb dengan
menghambat konversi delta aminolevulinic acid (delta-ALA) menjadi forfobilinogen
dan juga menghambat korporasi dari Fe ke dalam protoforfirin IX untuk membentuk
Hb dengan menghambat enzim delta aminolevulinic acid dehydratase ( -ALAD) dan
feroketalase. Hal ini mengakibatkan meningkatnya ekskresi koproporfin dalam urin
dan delta –ALA (Jeffe, 1991; ATSDR, 1993; Akagi et al, 2000). Analisis biomedik yang dapat dilakukan untuk melihat efek toksik plumbum adalah dengan pemeriksaan
Pb darah dan urin, aktivitas enzim -ALAD, konsentrasi Hb dan nilai hematokrit
yang menurun (Shannon,1998).
1
Penelitian tentang efek plumbum terhadap aktivitas enzim -ALAD pada
hewan percobaan telah banyak dilakukan. Hasan & Seth (1981), telah melaporkan
bahwa pemberian Pb selama 14 hari pada tikus albino menyebabkan penurunan
aktivitas enzim δ- ALAD secara signifikan dibandingkan dengan kontrol. Idris (2004)
dalam penelitiannya pada ikan nila yang didedahkan di air yang mengandung
plumbum nitrat dengan berbagai konsentrasi selama 14 hari, mengakibatkan
penurunan aktivitas enzim -ALAD.
enzim -ALAD, kadar hematokrit, dan Hb secara signifikan dibandingkan dengan
kontrol dan Pb + ekstrak du-zhong. Soetopo (2005) melaporkan bahwa pemberian ekstrak limbah yang mengandung plumbum sebesar 0,32 μg dan 0,64 μg memberikan
efek toksik terhadap tikus.
Penelitian yang dilakukan Hariono (2005) menunjukkan bahwa pemberian
senyawa plumbum asetat yang merupakan senyawa anorganik sebanyak 0,5 g/kg
BB/oral/hari/tikus selama 16 minggu mengakibatkan anemia serta peningkatan
aktivitas enzim -ALAD yang belum diketahui mekanismenya. Di sisi lain pada
pemberian 1,5 mg senyawa plumbum organik/kg BB/hari selama 10 minggu akibat
yang ditimbulkan terjadinya peningkatan konsentrasi plumbum darah, penurunan
berat badan, tidak ada perbedaan aktivitas enzim -ALAD kelompok perlakuan
dengan kontrol (Hariono, 2006).
Untuk mengatasi permasalahan keracunan plumbum, dilakukan terapi dengan
bahan pengkelat (chelating agent). Bahan pengkelat dapat mengikat logam-logam transisi seperti plumbum (Pb). Bahan pengkelat mengikat logam plumbum dan
membentuk ikatan kompleks yang membuatnya bersifat hidrofilik, sehingga dapat
dikeluarkan bersama urin. Kadang-kadang dikeluarkan dalam bentuk garam dari
asam urat, asam hipourat, dan kreatinin. Untuk plumbum yang masuk melalui saluran
cerna dan tidak terabsorbsi di saluran cerna akan diekskresikan bersama feses
Bahan pengkelat komersil yang umum digunakan adalah golongan
aminopolikarboksil termasuk EDTA, N-hidroxy ethylene diamine triacetic acid
(HEDTA), diethylen triamin pentaacetic acid (DTPA), dan nitrilo triacetic acid
(NTA). EDTA merupakan asam amino sintetik yang pertama kali digunakan pada
keracunan logam berat. Polimer pengkelat juga dapat diperoleh dari bahan alami,
salah satunya yang berpotensi adalah kitosan (Sanghi, 2000), karena kitosan memiliki
kemampuan untuk mengikat logam dan membentuk kompleks logam-kitosan.
Kitosan merupakan bahan pengkelat ion yang sangat baik (Wan Ngah et al, 1998). Elektron dari nitrogen yang terdapat pada gugus amina dapat membentuk ikatan
kovalen dengan ion-ion logam transisi, kitosan sebagai donor elektron pada ion-ion
logam transisi (Guibal, 2004).
Kitosan polimer polikationik alami yang dapat berperan sebagai adsorben
terhadap logam berat dalam air limbah (Onsoyen & Skaugrud, 1990). Alimuniar
(1992), melaporkan bahwa kitosan dapat digunakan sebagai adsorben yang baik pada
beberapa logam berat, seperti: Hg, Zn, Pt, Ni, Ag, Co, Cd, Cu dan Cr dengan tujuan
untuk pengolahan air limbah. Gao et al (2000) telah mengkaji sifat penyerapan ion logam Pb dengan menggunakan kitosan manik dan dimasukkan ke dalam kolom mini
melalui ekstraksi fasa padat. Sedangkan Ahmad et al (2004) telah melaporkan penggunaan kitosan untuk mengabsorpsi limbah minyak yang dihasilkan dari pabrik
Kitosan zat non-toksik yang merupakan polisakarida alami yang terdiri dari
kopolimer glukosamin dan N-asetilglukosamin, dan dapat diperoleh dari deasetilasi kitin (Khan et al, 2002). Kitin adalah biopolimer alami terbesar kedua yang dapat ditemukan di alam setelah selulosa. Kitin dapat diperoleh dari arthropoda, jamur, dan
ragi (Fernandez-Kim, 2004).
Karakteristik kimia yang sangat penting sekali untuk interaksi kitosan–logam
adalah derajat deasetilasi (DD) dan berat molekular (MW) (Onsoyen & Skaugrud,
1990; Berger et al, 2003 ). Burke et al (2000) melaporkan bahwa kemampuan kitosan mengabsorpsi besi (III) atau ion ferri meningkat sejalan dengan peningkatan
derajat deasetilasi kitosan. Hasil percobaan Zhou et al., (2003) menunjukkan bahwa kapasitas serapan untuk urea dengan kitosan tembaga meningkat dengan peningkatan
derajat deasetilasi.
Berdasarkan uraian yang dikemukakan peneliti ingin mengetahui pengaruh
derajat deasetilasi kitosan terhadap kadar plumbum darah, aktivitas enzim -ALAD,
dan kadar hemoglobin pada mencit yang dipapar Pb.
1.2. Perumusan Masalah
Penelitian tentang pengaruh pemberian Pb terhadap aktivitas enzim δ-ALAD
dan karakteristik darah pada hewan percobaan telah banyak diteliti, dan diketahui
pula bahwa kitosan berpotensi sebagai pengkelat bagi logam berat seperti plumbum.
kitosan dengan berbagai derajat deasetilasi terhadap kadar Pb darah, aktivitas enzim
-ALAD dan kadar Hb secara in vivo.
3. Kerangka Teori
Plumbum dalam darah dapat mempengaruhi biosintesis heme diantaranya
dengan menghambat aktivitas enzim -ALAD di sitoplasma (WHO, 1997). Beberapa
hasil penelitian menunjukkan bahwa plumbum dapat menyebabkan penurunan
aktivitas enzim -ALAD dan anemia. Bahan pengkelat digunakan pada terapi
keracunan logam berat. Bahan pengkelat mengikat logam Pb dan membentuk ikatan
kompleks yang membuatnya bersifat hidrofilik sehingga mudah dikeluarkan bersama
urin.
Kitosan zat non toksik alami yang berpotensi sebagai bahan pengkelat karena
kemampuannya mengikat logam dan membentuk kompleks kitosan-logam.
Kemampuan kitosan mengikat logam dipengaruhi oleh bobot molekular (MW) dan
derajat deasetilasi (DD).
Plumbum
Saluran pencernaan
(intestine) feses
Hati (liver)
Darah
Ginjal
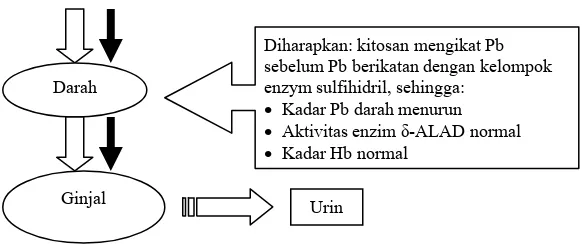
Diharapkan: kitosan mengikat Pb sebelum Pb berikatan dengan kelompok enzym sulfihidril, sehingga:
• Kadar Pb darah menurun
• Aktivitas enzim -ALAD normal
• Kadar Hb normal
Urin
Gambar 1. Bagan Kerangka Teori Pengaruh Kitosan terhadap Kadar Pb Darah dan Aktivitas Enzim -ALAD
1.4. Tujuan Penelitian
Tujuan umum penelitian ini adalah untuk mengetahui potensi kitosan sebagai
bahan pengkelat untuk mengatasi keracunan plumbum pada mencit jantan.
Tujuan khusus penelitian ini adalah:
a. Untuk mengetahui pengaruh pemberian kitosan dengan derajat deasetilasi yang
berbeda terhadap kadar Pb darah mencit jantan yang dipapar Pb.
b. Untuk mengetahui perbedaan aktivitas enzim -ALAD pada mencit yang dipapar
Pb asetat dengan Pb asetat + kitosan dengan derajat deasetilasi (DD) yang berbeda.
1.5. Hipotesis
Yang menjadi hipotesis pada penelitian ini adalah:
1. Ho1: tidak ada pengaruh derajat deasetilasi kitosan terhadap kadar Pb darah
mencit
Ha1: ada pengaruh derajat deasetilasi kitosan terhadap kadar Pb darah mencit
Ha2: ada pengaruh derajat deasetilasi kitosan terhadap aktivitas enzim -ALAD
3. Ho3: tidak ada pengaruh konsentrasi kitosan terhadap kadar Pb darah mencit
Ha3: ada pengaruh konsentrasi kitosan terhadap kadar Pb darah mencit
4. Ho4: tidak ada pengaruh konsentrasi kitosan terhadap aktivitas enzim -ALAD
Ha4: ada pengaruh konsentrasi kitosan terhadap aktivitas enzim -ALAD
1.6. Manfaat Penelitian
Hasil penelitian ini diharapkan dapat :
1. Memberikan informasi tentang pengaruh pemberian kitosan terhadap kadar
plumbum darah, aktivitas enzim -ALAD, dan kadar hemoglobin mencit
jantan.
2. Memberikan informasi pada masyarakat bagaimana upaya mengatasi
keracunan Pb.
3. Memberikan informasi khususnya kepada seluruh sivitas akademika
Universitas Sumatera Utara dan kepada masyarakat untuk mengembangkan
industri yang memanfaatkan potensi limbah udang, kepiting, dan sotong
BAB II
TINJAUAN PUSTAKA
2.1. Plumbum (Pb)
Timbal atau dalam keseharian lebih dikenal dengan nama timah hitam, dalam
bahasa ilmiahnya dinamakan plumbum. Logam ini disimbolkan dengan Pb. Plumbum termasuk ke dalam kelompok logam golongan IV-A pada Tabel Periodik unsur kimia.
Mempunyai nomor atom (NA) 82, dengan berat atom (BA) 207,2. Plumbum
merupakan logam yang bersifat lunak, mempunyai titik lebur 327,50C dan titik didih
1740 0C (Palar 2004; MSDS, 2005).
Plumbum dan persenyawaannya banyak digunakan dalam berbagai bidang.
Senyawa PbCrO digunakan dalam industri cat, senyawa Pb-silikat digunakan secara
luas sebagai salah satu bahan pengkilap keramik. Senyawa timbal oksida (PbO4)
digunakan dalam industri baterai. Dalam perkembangan industri kimia, dikenal pula
aditif yang dapat ditambahkan ke dalam bahan bakar kenderaan bermotor untuk anti
knocking yang berfungsi menaikkan angka oktan yaitu tetraetyllead (TEL)
(WHO,1977; Palar, 2004).
2.1.1. Keracunan Plumbum
Keracunan yang ditimbulkan oleh plumbum dapat terjadi karena masuknya
persenyawaan logam tersebut ke dalam tubuh. Saluran gastrointestinal dan respirasi
1981). Ukuran keracunan suatu zat ditentukan oleh kadar dan lamanya paparan.
Keracunan dibedakan menjadi keracunan akut dan keracunan kronis. Keracunan yang
disebabkan oleh timbal dalam tubuh mempengaruhi berbagai jaringan dan organ
tubuh (Palar, 2004).
Pada ginjal dapat menyebabkan aminoasiduria, fosfaturia, glukosuria,
nefropati dan fibrosis. Sistem gastrointestinal menyebabkan kolik dan konstipasi.
Sistem kardiovaskuler menyebabkan peningkatan permeabelitas pembuluh darah.
Sistem reproduksi dapat menyebabkan kematian janin waktu melahirkan pada wanita
dan hipospermi dan teratospermia pada pria. Sistem endokrin mengakibatkan
gangguan fungsi tiroid dan fungsi adrenal, dan sistem haemopoietik menyebabkan
anemia (Ellenhorn dan Barceloux, 1988).
Efek yang disebabkan oleh keracunan plumbum pada anak-anak adalah:
Tabel 1. Tingkat Keracunan Pb di Darah dan Efeknya pada Anak-anak
Kelompok Tingkat kadar Pb di darah Efek pada anak-anak
1 1-9 μg/dL Gangguan belajar
Plumbum memiliki 3 sifat biokimia yang penting, yang dapat menimbulkan
efek toksik pada manusia:
1. Plumbum merupakan logam yang bersifat elektropositif dengan afinitas yang
tinggi untuk kelompok enzim sulfhidril dan menghambat enzim sulfhidril
seperti enzim 5-aminolivolinic acid (ALAD, EC 4.2.1.24) dan ferroketalase
(EC 4.99.1.2) yang sangat penting pada sintesa haem.
2. Aktivitas divalensinya menyerupai kalsium dan aksinya sebagai competitive inhibitor di dalam daerah yang sangat penting seperti fosforilasi oksidatif mitokondria. Plumbum merusak sistem messenger yang diatur oleh kalsium
dengan demikian akan mempengaruhi fungsi endokrin dan neural.
3. Plumbum juga dapat mempengaruhi transkripsi DNA, yang berinteraksi
dengan ikatan protein asam nukleat yang memiliki kemampuan mengatur gen.
(Goering, 1993)
2.1.2. Pengaruh Plumbum pada Sistem Peredaran Darah
Kira-kira 90 % Pb yang masuk ke dalam sirkulasi darah menuju ke eritrosit,
ada juga yang ke albumin darah, α-globulin dan protein lain (Bartik, 1981). Plumbum
mempengaruhi sistem peredaran darah dengan berbagai cara :
1. Dengan memperlambat pematangan normal sel darah merah (eritrosit) dalam
sum-sum tulang, hal ini menyebabkan terjadinya anemia.
2. Mempengaruhi kelangsungan hidup sel darah merah. Sel darah merah yang diberi
kelemahan pergerakan. Selain itu juga memperlihatkan penghambatan Na-K-ATP
ase yang meningkatkan kehilangan kalium intraseluler. Pengaruh ini menjelaskan
bahwa kejadian anemia pada peristiwa keracunan timbal juga mempersingkat
waktu hidup sel darah merah.
3. Menghambat biosintesis hemoglobin dengan cara menghambat aktivitas enzim
-ALAD dan enzim ferroketalase (WHO, 1977)
2.1.3. Monitoring Plumbum dalam Tubuh Manusia
Untuk mengetahui seberapa besar kandungan timbal yang diabsorbsi, dapat
dilakukan dengan beberapa cara. Tiga cara yang umum dilakukan adalah:
1. Pengujian kadar koproporfirin dalam urin
2. Pengujian kadar ALA dalam urin
3. Pengujian kadar ALA dan aktivitas enzim -ALAD dalam darah
Pengujian kadar ALA dan aktivitas enzim -ALAD dalam darah biasanya
dipakai untuk mengetahui kandungan timbale pada orang yang terpapar timbale.
Pengukuran yang paling sensitif adalah pengukuran yang dilakukan terhadap
penurunan aktivitas enzim -ALAD (Palar, 2004).
2.2. Aktivitas Enzim
Enzim berperan penting dalam proses metabolisme yang terjadi dalam tubuh.
Aktivitas biologis enzim adalah sebagai biokatalis yang mengatur dan mempercepat
jumlah unit enzim yang mengkatalisis substrat dalam mikromolekul porfobilinogen
(PBG) per jam per liter eritrosit pada suhu 37 0C (Sadikin, 2002; Murray et al, 2003). Pada umumnya semua reaksi biokimia dikalisasi oleh enzim. Sebagian besar
reaksi biokimia sel-sel hidup akan terjadi dengan sangat lambat jika tidak dikatalisis
oleh enzim. Sifat enzim enzim yang paling bermakna adalah kemampuannya untuk
mengkatalisis suatu reaksi spesifik, dan pada hakekatnya tidak tidak mengkatalisis
reaksi lain. Dengan demikian kecepatan proses metabolisme spesifik dapat diatur oleh
enzim spesifik (Murray et al, 2003).
Dalam menjalankan tugasnya enzim-enzim sering membutuhkan logam atau
vitamin atau gabungan dari keduanya sebagai kofaktor dan aktivator. Logam berat
mempunyai kemampuan untuk berikatan dengan enzim dengan menggantikan fungsi
ion logam dari gugus enzim (Sadikin, 2002; Murray et al, 2003; Palar, 2004).
Pada enzim-enzim tertentu ada yang mengandung gugus sulfhidril (-SH)
sebagai pusat aktifnya. Enzim-enzim ini merupakan kelompok enzim yang paling
mudah terhalang daya kerjanya. Keadaan ini disebabkan gugus sulfhidril dengan
mudah berikatan dengan ion-ion logam berat yang masuk ke dalam tubuh. Akibat dari
ikatan yang terbentuk antara gugus –SH dengan ion logam berat, daya kerja yang
dimiliki enzim menjadi sangat berkurang atau sama sekali tidak dapat bekerja (Palar,
2004).
Enzim delta-aminolevulininic acid dehydratase ( -ALAD), enzim yang
gugus –SH. Senyawa Pb yang masuk dalam tubuh akan mengikat gugus aktif dari
ENZYMATIC METABOLITES AND ABNORMAL PRODUCTS
Gambar 2. Diagram Alir Gangguan Timah Hitam (Pb) terhadap Biosintesis Hemoglobin (WHO, 1977)
2.3. Biosintesis Hemoglobin
Hemoglobin merupakan protein konjugasi globulin dan heme (yaitu suatu
kompleks protoporfirin dengan besi). Biosintesis porfirin berasal dari derivat
Ko-enzim A dari asam suksinat pada Siklus Krebs dalam mitokondria dan asam amino
glisin. Hasil reaksi kondensasi antara suksinil Ko-enzim A dan glisin adalah asam
alfa amino beta ketoadipat yang dengan cepat dikarboksilasi menjadi asam delta
aminolevulenat. Sintesis asam delta-aminolevulenat terjadi di mitokondria.
Dalam sitoplasma 2 molekul delta-aminolevulenat dikatalisis oleh enzim
delta-aminolevulinic acid dehydratase membentuk 2 molekul air dan 1 molekul
porfobilinogen. Masih dalam sitoplasma, 4 unit porfobilinogen mengalami
kondensasi membentuk polimer siklik yaitu uroporfobilinogen. Ada 2 isomer
uroporfobilinogen, yaitu isomer tipe I dan isomer tipe III. Heme berasal dari isomer
tipe III. Uroporfobilinogen III diubah menjadi koproporfirinogen III. Reaksi ini
dikatalisis oleh uroporfirinogen dekarboksilase.
Koproporfirinogen III memasuki mitokondria, selanjutnya diubah menjadi
protoporfirinogen. Dari 15 kemungkinan isomer hanya satu yang dibentuk, yaitu
protoporfirinogen IX. Protoporfirinogen IX dioksidasi oleh enzim protoporfirinogen
oksidase menghasilkan protoporfirin IX. Oksidasi ini menghasilkan ikatan rangkap
terkonjugasi yang merupakan ciri porfirin. Tahap akhir pembentukan heme adalah
2.4. Bahan Pengkelat
Kelat berasal dari bahasa Yunani chele yang artinya capit (Sanghi, 2000). Bahan pengkelat dapat mengikat logam-logam transisi salah satu logam tersebut
adalah timbal (Pb). Pengkelat yang sering digunakan adalah pengkelat sintetik yaitu
EDTA.
Karakteristik yang penting dan ideal yang harus dimiliki pengkelat timbal adalah:
1. Dapat mengurangi efek toksik timbal pada sel target.
2. Dapat memperkecil atau mencegah malfungsi pada sel.
3. Menghilangkan efek negatif karena gangguan homeostasis dan penggunaan
dari elemen essensial yang menyusut.
4. Menghilangkan atau meminimalisir toksisitas intrinsik (Goyer et al,1995)
2.5. Kitosan
Kitosan merupakan polisakarida alami yang terdiri dari kopolimer glukosamin
dan N-acetylglukosamin, dan dapat diperoleh dari deasetilasi kitin (Khan et al, 2002). Kitin biopolimer alami terbesar kedua yang dapat ditemukan di alam setelah selulosa.
Kitin dapat diperoleh dari arthropoda, jamur, dan ragi (Fernandez-Kim, 2004), tetapi
sumber komersial yang penting adalah eksoskleton dari kepiting (Kim & Park, 2001).
Kitin dapat diisolasi dari cangkang kepiting dengan 2 tahap dasar, (1) pemisahan
protein (deproteinisasi) dan pemisahan calsium carbonat dan calsium phospat
Struktur kitin sangat mirip dengan selulosa yaitu ikatan yang terjadi antara
monomernya terangkai dengan ikatan glikosida pada posisi β-(1-4). Perbedaannya
dengan selulosa adalah gugus hidroksil yang terikat pada atom karbon yang kedua,
pada kitin diganti oleh gugus asetamida (NHCOCH2) sehingga kitin menjadi sebuah
polimer berunit N-asetilglukosamin Kitosan mempunyai rantai tidak linier dan
mempunyai rumus umum (C6H11NO4)n atau disebut sebagai (14)amino2deoksi
-D-glukosa (Fernandez-Kim,2004).
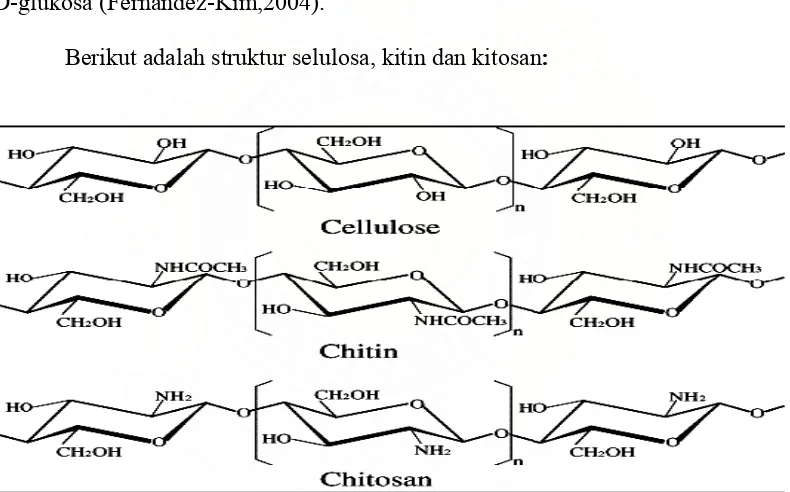
Berikut adalah struktur selulosa, kitin dan kitosan:
Gambar 3. Struktur Selulosa, Kitin, dan Kitosan (Fernandez-Kim,2004)
2.5.1. Sifat-sifat dan Penggunaan Kitosan
Kitosan bersifat polielektrolit kation yang dapat mengikat logam berat,
sehingga dapat berfungsi sebagai absorben terhadap logam berat dalam air limbah.
nitrogen dalam kitosan akan bereaksi dan mengikat logam dari persenyawaan limbah
cair. Kitosan yang tidak dapat larut dalam air akan menggumpalkan logam menjadi
flok-flok yang akan bersatu dan dapat dipisahkan dari air limbah. Kitosan dapat
bekerja sempurna jika dilarutkan dalam larutan asam (Marganof, 2003; Widodo et al, 2005). Proses pengikatan logam berat oleh kitosan dapat dilihat dalam Gambar 4
berikut.
Gambar 4. Mekanisme Pengikatan Logam Berat oleh Kitosan (Widodo et al, 2005)
Contoh di atas menggunakan logam Cu atau tembaga. Terjadi pengikatan Cu
oleh gugus N (nitrogen) dan O (oksigen). Logam Cu tersebut akan terikat atau
terserap, terkumpul dan terjadi flok-flok logam.
Kitosan juga bersifat hidrofilik, menahan air dalam strukturnya dan
membentuk gel secara spontan. Pembentukan gel berlangsung pada harga pH asam
dan sedikit asam, disebabkan sifat kationik kitosan. Viskositas gel kitosan meningkat
dengan meningkatnya derajat deasetilasi. Gel kitosan terdegradasi secara
berangsur-angsur, sebagaimana halnya kitosan melarut (Muzzarelli et al,1988).
Kitosan juga telah digunakan secara luas dalam bidang pengobatan,
bioteknologi, menjadi bahan yang penting dalam aplikasi farmasi, karena mempunyai
kemampuan biodegradasi dan biocompatibility dan rendah toksisitasnya ( Berger et al, 2004). Kitosan juga memperlihatkan aktivitas biologi seperti hypocholesterolemic, antimikroba, anti jamur (Rhoades & Roller 2000).
Tabel 2. Pemanfaatan Kitosan pada Beberapa Industri
Industri Manfaat
Industri pengolahan limbah Penyerap ion logam, koagulan, protein, asam amino, dan bahan pencelup
Industri makanan Pengawet, penstabil makanan, penstabil warna, bahan pengental, dll.
Industri kesehatan Penyembuh luka dan tulang, pengontrol kholesterol darah, kontak lensa, penghambat plag gigi, dll.
Industri pertanian Pupuk, pelindung biji, dll.
Kosmetik Pelembab (moisturizer), krem wajah, tangan dan bada, dll.
Bioteknologi Dapat immobolisasi enzim, chromatography, penyembuh sel, dll.
Sumber: Fernandez-Kim, 2004
2.5.2. Derajat Deasetilasi Kitosan
Berat molekul kitosan dan derajat deasetilasi berperan penting dalam proses
penyerapan. Pertambahan nilai derajat deasetilasi menyebabkan bertambahnya
Beberapa publikasi menyatakan bahwa derajat deasetilasi akan dapat
meningkatkan keupayaan dalam proses penyerap ion logam. Ini disebabkan
meningkatnya gugus amina bebas dan di dalam praktiknya berat molekul dan derajat
deasetilasi bertambah nilainya juga membawa pengaruh pada sifat fisik dan
fisikokimia pada porositas, viskositas, dan titik leburnya (Agusnar, 1990).
2.5.3. Pengkelat Kitosan dengan Ion-ion Logam
Kitosan memiliki reaktivitas yang tinggi untuk absorpsi dengan beberapa
mekanisme:
a. Kandungan yang tinggi pada gugus –OH membuatnya menjadi polimer yang
hidrofilik dan memberikan efek kelasi.
b. Kandungan gugus amina yang tinggi memberikan beban kation pada pH
asam.
c. Kelompok amina dapat mengikat logam kationik sehingga membuatnya
menjadi sepasang elektron (Inoue et al, 1993; Guibal, 2005)
Guibal 2004 (1984), menjelaskan bahwa interaksi antara ion-ion logam
dengan kitosan yaitu dengan menggunakan tembaga sulfat (CuSO4). Elektron dari
nitrogen yang terdapat pada gugus amina dapat mengakibatkan ikatan kovalen dative
dengan ion-ion logam transisi. Dimana kitosan sebagai donor elektron pada ion-ion
logam transisi. Kitosan memiliki kemampuan untuk mengikat logam dan membentuk
BAB III
METODOLOGI PENELITIAN
3.1.Desain Penelitian
Desain yang digunakan pada penelitian ini adalah studi experimental pada
mencit (Mus musculus L.) strain BALBC.
3.2.Tempat dan Waktu Penelitian
Penelitian ini dilaksanakan di Laboratorium Terpadu Fakultas Kedokteran
USU, Laboratorium Biokimia BPPV Regional I Medan, Laboratorium Bapedalda
Propsu (Badan Pengendalian Dampak Lingkungan Provinsi Sumatera Utara), dalam
waktu 12 minggu.
3.3. Sampel Penelitian
Hewan uji yang digunakan dalam penelitian ini adalah mencit jantan Mus musculus L., umur 6-7 minggu, dengan kisaran berat badan 30-45 g yang diperoleh dari Balai Penyidikan dan Pengujian Veteriner (BPPV) Medan. Sebelum perlakuan
mencit terlebih dahulu diaklimatisasi selama seminggu. Mencit dipelihara dalam
kandang yang diberi alas sekam dan anyaman kawat sebagai penutup. Pemberian
makan dan minum dilakukan setiap hari secara ad libitum. Pakan yang diberikan berupa pelet produksi PT. Charoen Pokphan Medan dan diberi minum air ledeng.
3.4. Variabel yang diteliti
3.4.1. Variabel independent
1. Pb asetat
2. Derajat deasetilasi (DD) kitosan
3. Dosis kitosan
3.4.2. Variabel dependent
1. Kadar Pb darah
2. Aktivitas enzim -ALAD
3. Kadar Hb
3.5. Rancangan Penelitian
Pada penelitian ini sampel terdiri dari 30 ekor mencit jantan yang dibagi
secara acak dalam 10 kelompok masing-masing 3 ekor tiap kelompok, dengan nama
kelompok K0, K1, K2, K3, P1, P2, P3, P4, P5,dan P6.
K0 = Kelompok kontrol aquades
K1 = Kelompok kontrol Pb yang diberi larutan Pb asetat 25 mg/kg BB
K2 = Kelompok kontrol asetat yang diberi larutan asam asetat 1 %
K3 = Kelompok kontrol kitosan yang diberi larutan kitosan
P1 = Kelompok perlakuan yang diberi larutan Pb asetat 25 mg/BB + kitosan A 1 %
P2 = Kelompok perlakuan yang diberi larutan Pb asetat 25 mg/BB + kitosan A 2 %
P3 = Kelompok perlakuan yang diberi larutan Pb asetat 25 mg/BB + kitosan B 1 %
P4 = Kelompok perlakuan yang diberi larutan Pb asetat 25 mg/BB + kitosan C 1 %
P5 = Kelompok perlakuan yang diberi larutan Pb asetat 25 mg/BB + kitosan C 2 %
Kitosan A = Kitosan dengan Derajat Deasetilasi 64 %
Kitosan B = Kitosan dengan Derajat Deasetilasi 65 %
Kitosan C = Kitosan dengan Derajat Deasetilasi 75 %
Kitosan yang digunakan adalah kitosan yang bersumber dari sotong yang mempunyai
berat molekul yang rendah.
Jumlah Ulangan Tiap Kelompok
Penentuan jumlah ulangan untuk tiap kelompok berdasarkan rumus dari
Federer (1963), yaitu :
( t- 1 ) ( n-1)≥ 15
t = jumlah perlakuan ; n = jumlah ulangan
Jumlah perlakuan dalam penelitian ini adalah 10, maka jumlah ulangan tiap
kelompok minimal 3.
3.6.Pelaksanaan Penelitian
Perlakuan dimulai dengan menimbang berat badan masing-masing mencit dan
diberi perlakuan sesuai dengan kelompok perlakuan. Bahan uji diberikan secara oral
dislokasi leher dan dibedah untuk diambil darahnya sebanyak 1 mL. Selanjutnya
dianalisa kadar Pb darah, aktivitas enzim -ALAD, hematokrit, dan kadar Hb.
3.6.1. Prosedur penentuan derajat deasetilasi kitosan
Dimasukkan masing-masing 200 mL larutan NaOH 50 % ke dalam beaker
glass A, B, dan C yang masing-masing telah berisi 10 g kitosan, diaduk dan kitosan
dibiarkan terendam dalam larutan NaOH tersebut selama masing-masing 2 hari (A), 3
hari (B), dan 4 hari (C). Kemudian disaring dan dibilas dengan aquades, dan
dibiarkan kering pada suhu kamar. Selanjutnya kitosan A, B, dan kitosan C tersebut
dipreparasi untuk mengukur derajat deasetilasinya dengan metode spektroskopi infra
merah. Derajat deasetilasi dihitung dengan metode ”baseline”. (Alimuniar & Zainuddin, 1998)
3.6.2. Pengambilan sampel darah
Pengambilan sampel darah dilakukan dari jantung sebanyak 1 mL dengan
menggunakan spuit, dimasukkan ke dalam tabung eppendorf yang telah berisi heparin
sebagai antikoagulan.
3.6.3. Pembuatan larutan pereaksi untuk analisis enzim -ALAD
Alat yang digunakan dalam pembuatan larutan pereaksi yaitu: timbangan
analitik; labu ukur 100 mL, pH meter, gelas piala 250 mL, batang pengaduk, gelas
Bahan kimia yang digunakan adalah: Na2HPO4.12H2O; NaH2PO4.2H2O,
-ALA; trikloro asetat (TCA), HgCl2, Triton X-100, p-dimethylaminobenzaldehyd,
asam asetat glacial, asam perklorat, aquades.
Cara kerja
a. Larutan triton x-100
Sebanyak 0,5 mL triton x-100 dicampur dengan 500 mL aquades.
b. Larutan buffer natrium fosfat 0,2 mol/L pH 6,4
Sebanyak 53,72 g Na2HPO4.12H2O dilarutkan dalam 500 mL aquades
(Larutan A). Sebanyak NaH2PO4.2H2O 23,4 g dilarutkan dalam 500 mL
aquades (Larutan B). Sebanyak 100 mL Larutan A dicampur dengan 168 mL
Larutan B, pH 6,4 disesuaikan dengan menambahkan asam atau basa dan
diukur dengan menggunakan pH meter.
c. Larutan -ALA 125 mmol/L
Sebanyak 209,5 mg -ALA dimasukkan ke dalam labu ukur 100 mL,
ditambahkan aquades hingga 100 mL, dikocok hingga homogen, dan
disimpan pada suhu 40C.
d. Larutan trikloro asetat (TCA) 60 g/L yang mengandung HgCl2 60
Sebanyak 15 g TCA dan 4 g HgCl2 dimasukkan ke dalam gelas piala dan
ditambah dengan aquades sampai volumenya 250 mL.
e. Larutan pereaksi Ehrlich
Sebanyak 2,0 g p-dimethylaminobenzaldehyd dilarutkan dalam 60 mL asam
asetat glasial dan ditambahkan 32 mL asam perklorat 70%. Sambil diaduk,
tambahkan asam asetat sampai tepat 100 mL (Wigfield & Farant, 1981).
3.6.4. Prosedur penentuan aktivitas enzim -ALAD
Alat yang digunakan dalam penentuan aktivitas enzim -ALAD adalah:
tabung ependorf , mikro pipet, inkubator, vorteks, sentrifugator dan spektrofotometer
. Bahan-bahan yang digunakan adalah: sampel darah, aquades, larutan triton
x-100, larutan buffer natrium fosfat 0,2 mol/L pH 6,4, larutan -ALA 125 mmol/L,
larutan trikloro asetat (TCA) 60 g/L yang mengandung HgCl2 60 mmol/L ,larutan
pereaksi ehrlich.
Cara kerja
Dipipet 20 μL sampel darah dengan mikropipet, dimasukkan dalam tabung
ependorf tambahkan 100 μL larutan Triton X-100 campur selama 15 detik dan
tempatkan campuran dalam ice-bath selama 3 menit untuk menyempurnakan lisis. Ke
dalam hemolisat ditambahkan 100 μL buffer natrium fosfat pH 6,4 dan 100 μL
larutan δ-Aminolevulinic acid kemudian diinkubasi selama 30 menit pada suhu 37
0
Inkubasi semua sampel selama 60 menit pada suhu 37 0C. Untuk mengakhiri inkubasi
hentikan reaksi dengan menambahkan 200 μL campuran larutan TCA merkuri
klorida. Sentrifugasi pada kecepatan 11500 rpm selama 5 menit pada eppendorf
microcentrifuge. Setelah disentrifugasi pindahkan 400 μL larutan supernatan ke
tabung lain dan tambahkan 400 μL pereaksi Ehrlich. Selanjutnya untuk blanko
ditambahkan 400 μL pereaksi Ehrlich dan 400 μL aquadest. Setelah 5 menit,
absorbansi diukur pada panjang gelombang 555 nm (Wigfield & Farant, 1981).
3.6.5. Prosedur penentuan kadar Pb dalam darah
Alat yang digunakan adalah gelas ukur 1,0 mL, tabung reaksi, hot plate, spektrofotometer serapan atom (Shimadzu AA-6200). Bahan yang digunakan adalah
sampel darah, larutan asam nitrat.
Cara kerja
Sebanyak 0,5 mL darah dimasukkan ke dalam tabung reaksi, kemudian
ditambahkan asam nitrat pekat ± 1mL. Selanjutnya dipanaskan secara perlahan-lahan
di atas hot plate sampai larutan berwarna kuning. Larutan dibiarkan sampai kering dengan baik di atas hot plate.Kemudian ditambahkan asam nitrat 13% sebanyak 10
mL. Kemudian larutan diukur dengan spektrofotometer serapan atom (Shimadzu AA-
6200) pada panjang gelombang 283,3 nm (Saraswati, 1998)
3.6.6. Prosedur penentuan hematokrit
Cara kerja
Sampel darah dimasukkan ke dalam pipet hematokrit hingga hampir penuh,
kedua ujung pipet ditutup dengan lilin dan kemudian disentrifuge pada kecepatan
16.000 rpm, selama 5 menit. Persentase hematokrit dibaca pada skala khusus.
3.6.7. Prosedur penentuan kadar hemoglobin
Kadar hemoglobin diukur dengan metode cyanmethemoglobin. Alat yang
digunakan: mikropipet, spektofotometer. Bahan yang digunakan: sampel darah,
reagen untuk menentukan konsentrasi hemoglobin (Biosystem Reagent & Instrumen)
Cara kerja
Preparasi reagen : satu mL reagen ditambah 49 mL aquades, diaduk dan
dimasukkan ke dalam botol cokelat,disimpan pada suhu 15-300C.
Dimasukkan 10 µL darah sampel ke dalam tabung A, 10 µL standard ke
dalam tabung B. Pada masing-masing tabung ditambahkan 2,5 mL larutan reagen.
Untuk blangko ke tabung C dimasukkan 2,5 mL larutan reagen.Setelah itu semua
tabung di vortex dan didiamkan selama 3 menit pada suhu ruang. Setelah 3 menit tiap
larutan dimasukkan ke dalam cuvet, larutan blangko dimasukkan ke dalam
spektrofotometer dan diatur absorbansinya 0,00 pada panjang gelombang 540 nm.
Kemudian dilanjutkan dengan pengukuran absorbansi standard dan sampel.
3.7. Variabel yang diamati
Keaktivan enzim dinyatakan dalam mikromolekul porfobilinogen (PBG) per
jam per liter eritrosit pada suhu 37 0C yang dihitung dengan rumus :
Absorbansi X 109,4 X 1,00 µmol PBG/jam/L eritrosit Hematokrit
3.7.2. Kadar Pb dalam darah
Kadar Pb dalam darah dinyatakan dalam µg/100 mL darah. Pada alat AAS
Shimadzu AA 6200, angka yang dibaca pada rekorder menunjukkan harga
konsentrasi. Sampel darah yang dianalisis kadar Pbnya sebanyak 0,5 ml. Pada saat
pengukuran,volume ditepatkan menjadi 1,0 ml, maka kadar Pb dalam darah adalah:
1 x konsentrasi yang dibaca (Saraswati, 1998). 0,5
3.7.3. Kadar Hb dalam darah
Untuk mendapatkan konsentrasi Hb maka dihitung dengan rumus :
C = A sampel x 37,5
C = konsentrasi
A = nilai absorbansi
3.7.4. Persentase derajat deasetilasi kitosan
Derajat deasetilasi dihitung dengan metode base line. Puncak tertinggi dicatat dari garis dasar yang dipilih. Nilai absorbansi dihitung dengan rumus :
P0 A = log
P
P = transmitansi pada puncak minimum
Nilai derajat N-asetilasi dapat dihitung dengan rumus :
% N- asetilasi = 1- (A gugus amida/A gugus hidroksil x 1/1,33) x 100 %
3.8. Analisis Data
Data yang diperoleh dianalisis dengan progam komputer SPSS 13. Dicari
apakah ada perbedaan kadar Pb darah, aktivitas enzim -ALAD, dan kadar Hb antara
kelompok perlakuan dengan kontrol dengan menggunakan uji Analisis Varian
(Anova). Jika dengan uji tersebut terdapat perbedaan yang nyata maka dilanjutkan
dengan uji LSD (Least Significant Difference) atau uji Beda Nyata Terkecil pada
tingkat kemaknaan p< 0,05.
BAB IV
HASIL DAN PEMBAHASAN
4.1. Hasil Penelitian
Dari hasil perhitungan penentuan derajat deasetilasi diperoleh nilai derajat
deasetilasi untuk Kitosan A adalah 64 %, Kitosan B 65 % dan Kitosan C 75 %.
4.1.1. Kadar Pb darah
Kadar Pb darah diukur untuk mengetahui pengaruh pemberian kitosan dengan
derajat deasetilasi 64 % (Kitosan A), 65 % (Kitosan B) dan 75% (Kitosan C) terhadap
penelitian yang telah dilakukan diperoleh rata-rata kadar Pb darah mencit yang dapat
dilihat pada Gambar 5 berikut.
Rata-Rata Kadar Pb Darah Mencit
Kadar Pb 0.14 0.33 0.02 0.03 0.04 0.11 0.06 0.02 0.003
K0 K1 K3 P1 P2 P3 P4 P5 P6
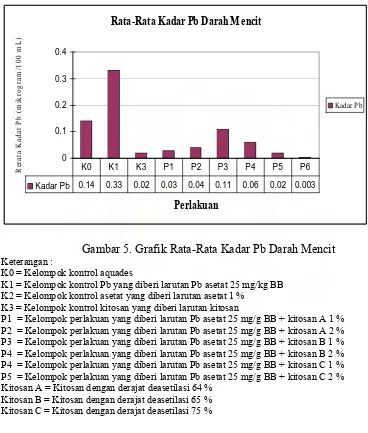
Gambar 5. Grafik Rata-Rata Kadar Pb Darah Mencit
Keterangan :
K0 = Kelompok kontrol aquades
K1 = Kelompok kontrol Pb yang diberi larutan Pb asetat 25 mg/kg BB K2 = Kelompok kontrol asetat yang diberi larutan asetat 1 %
30
K3 = Kelompok kontrol kitosan yang diberi larutan kitosan
P1 = Kelompok perlakuan yang diberi larutan Pb asetat 25 mg/g BB + kitosan A 1 % P2 = Kelompok perlakuan yang diberi larutan Pb asetat 25 mg/g BB + kitosan A 2 % P3 = Kelompok perlakuan yang diberi larutan Pb asetat 25 mg/g BB + kitosan B 1 % P4 = Kelompok perlakuan yang diberi larutan Pb asetat 25 mg/g BB + kitosan B 2 % P4 = Kelompok perlakuan yang diberi larutan Pb asetat 25 mg/g BB + kitosan C 1 % P5 = Kelompok perlakuan yang diberi larutan Pb asetat 25 mg/g BB + kitosan C 2 % Kitosan A = Kitosan dengan derajat deasetilasi 64 %
Kitosan B = Kitosan dengan derajat deasetilasi 65 % Kitosan C = Kitosan dengan derajat deasetilasi 75 %
Dari Gambar 5 di atas dapat dilihat rata-rata kadar Pb darah mencit pada
statistik dengan uji Anova satu arah diperoleh nilai p=0.6 (p>0,05) atau Ho1 dan Ho3
diterima yang berarti tidak ada perbedaan yang signifikan di antara kelompok
perlakuan hewan uji.Walaupun demikian jika dilihat dari rata-rata kadar Pb darah di
antara kelompok perlakuan terdapat kecendrungan terjadinya penurunan kadar Pb
darah mencit antara kelompok perlakuan K1 (kontrol Pb) dibandingkan dengan
kelompok perlakuan P1, P2, P3, P4, P5, dan P6.
4.1.2.Aktivitas Enzim -ALAD
Plumbum dapat mempengaruhi aktivitas enzim -ALAD,untuk mengetahui
pengaruh pemberian kitosan pada mencit yang diberi larutan Pb asetat secara oral
selama 14 hari terhadap aktivitas enzim tersebut telah dilakukan penelitian dan
diperoleh rata-rata aktivitas enzim -ALAD pada Gambar 6 berikut.
Rata-Rata Akivitas Enzim DALAD Mencit
Aktivitas enzim 0.63 0.72 0.66 1.2 0.33 0.55 0.43 0.61 0.49 0.9
K0 K1 K2 K3 P1 P2 P3 P4 P5 P6
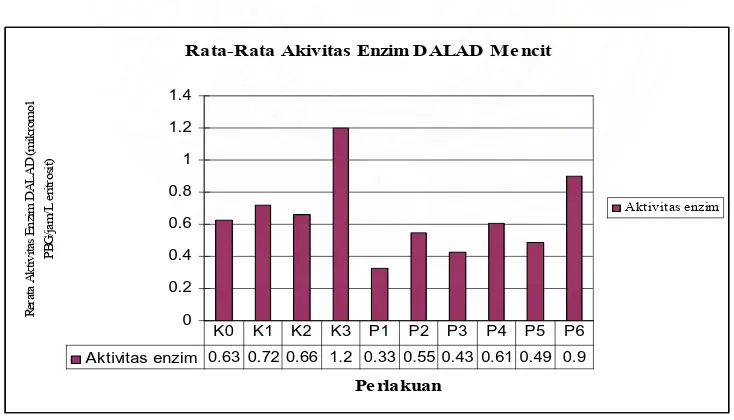
Gambar 6. Grafik Rata-Rata Aktivitas Enzim -ALAD
Keterangan :
K0 = Kelompok kontrol aquades
K2 = Kelompok kontrol asetat yang diberi larutan asetat 1 % K3 = Kelompok kontrol kitosan yang diberi larutan kitosan
P1 = Kelompok perlakuan yang diberi larutan Pb asetat 25 mg/g BB + kitosan A 1 % P2 = Kelompok perlakuan yang diberi larutan Pb asetat 25 mg/g BB + kitosan A 2 % P3 = Kelompok perlakuan yang diberi larutan Pb asetat 25 mg/g BB + kitosan B 1 % P4 = Kelompok perlakuan yang diberi larutan Pb asetat 25 mg/g BB + kitosan B 2 % P4 = Kelompok perlakuan yang diberi larutan Pb asetat 25 mg/g BB + kitosan C 1 % P5 = Kelompok perlakuan yang diberi larutan Pb asetat 25 mg/g BB + kitosan C 2 % Kitosan A = Kitosan dengan derajat deasetilasi 64 %
Kitosan B = Kitosan dengan derajat deasetilasi 65 % Kitosan C = Kitosan dengan derajat deasetilasi 75 %
Berdasarkan data dari Gambar 6 tersebut dapat dilihat bahwa pada kelompok
K3 (kontrol kitosan) memiliki aktivitas enzim -ALAD tertinggi dibandingkan
dengan kelompok perlakuan yang lain. Sedangkan kelompok P1 memiliki aktivitas
enzim -ALAD terendah dibandingkan dengan kelompok perlakuan yang lain.
Kelompok K1 (kontrol Pb) memiliki aktivitas enzim -ALAD lebih tinggi
dibandingkan dengan kelompok K0, K2, P1, P2, P3, P4, dan P5.
Berdasarkan hasil analisis statistik dengan uji anova satu arah diperoleh nilai
p=0.009 (p<0,05) atau Ho2 ditolak yang berarti ada pengaruh derajat deasetilasi
kitosan terhadap aktivitas enzim -ALAD. Kemudian untuk melihat perbedaan antar
kelompok perlakuan dilanjutkan dengan uji Beda Nyata Terkecil (Least Significant Difference), diperoleh perbedaan antar kelompok perlakuan seperti pada Tabel 3.
P4 ns ns ns * ns ns ns ns ns
P5 ns ns ns * ns ns ns ns *
P6 ns ns ns ns * ns * ns *
Keterangan : ns = tidak berbeda nyata * = berbeda nyata
Dari hasil uji BNT pada Tabel 3 tersebut aktivitas enzim -ALAD pada
kelompok K3 (kontrol kitosan) berbeda nyata (p<0,05) dengan semua kelompok
perlakuan (K0, K1, K2, P1, P2, P3, P4, P5) kecuali dengan kelompok P6. Sedangkan
kelompok P6 berbeda nyata dengan kelompok P1, P3, dan P5 yang berarti ada
pengaruh konsentrasi kitosan terhadap aktivitas enzim -ALAD (Ho4 ditolak).
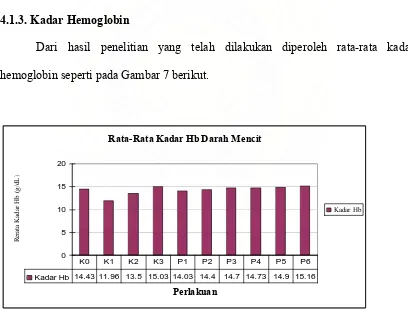
4.1.3. Kadar Hemoglobin
Dari hasil penelitian yang telah dilakukan diperoleh rata-rata kadar
hemoglobin seperti pada Gambar 7 berikut.
Rata-Rata Kadar Hb Darah Mencit
Kadar Hb 14.43 11.96 13.5 15.03 14.03 14.4 14.7 14.73 14.9 15.16
K0 K1 K2 K3 P1 P2 P3 P4 P5 P6
Gambar 7. Grafik Rata-Rata Kadar Hemoglobin Mencit
Keterangan :
K1 = Kelompok kontrol Pb yang diberi larutan Pb asetat 25 mg/kg BB K2 = Kelompok kontrol asetat yang diberi larutan asetat 1 %
K3 = Kelompok kontrol kitosan yang diberi larutan kitosan
P1 = Kelompok perlakuan yang diberi larutan Pb asetat 25 mg/g BB + kitosan A 1 % P2 = Kelompok perlakuan yang diberi larutan Pb asetat 25 mg/g BB + kitosan A 2 % P3 = Kelompok perlakuan yang diberi larutan Pb asetat 25 mg/g BB + kitosan B 1 % P4 = Kelompok perlakuan yang diberi larutan Pb asetat 25 mg/g BB + kitosan B 2 % P4 = Kelompok perlakuan yang diberi larutan Pb asetat 25 mg/g BB + kitosan C 1 % P5 = Kelompok perlakuan yang diberi larutan Pb asetat 25 mg/g BB + kitosan C 2 % Kitosan A = Kitosan dengan derajat deasetilasi 64 %
Kitosan B = Kitosan dengan derajat deasetilasi 65 % Kitosan C = Kitosan dengan derajat deasetilasi 75 %
Berdasarkan data dari Gambar 7 pada kelompok K1 (kontrol Pb) memiliki
kadar hemoglobin terendah (12 g/dL) dibandingkan dengan kelompok perlakuan yang
lain. Sedangkan kelompok P6 memiliki kadar hemoglobin tertinggi (15,2 g/dL)
dibandingkan dengan kelompok lain.
Berdasarkan hasil analisis statistik dengan uji anova satu arah diperoleh hasil
yang signifikan p=0.000 (p<0,05) di antara kelompok perlakuan. Untuk mengetahui
perbedaan antar kelompok perlakuan dilakukan uji Beda Nyata Terkecil dan
diperoleh hasil seperti pada Tabel 4 berikut.
Tabel 4. Hasil Uji Beda Nyata Terkecil Rata-Rata Kadar Hemoglobin
Berdasarkan hasil uji BNT pada Tabel 4 di atas dapat dilihat bahwa kelompok
K1 (kontrol Pb) berbeda nyata (p<0,05) dengan semua kelompok perlakuan (K0,
K2,K3, P1, P2, P3, P4, P5, dan P6) yaitu terjadi penurunan kadar hemoglobin. Begitu
juga dengan kelompok K2 (kontrol asetat) berbeda nyata dengan semua kelompok
perlakuan kecuali dengan kelompok P1 (Pb asetat + Kitosan A 1%).
Pada kelompok P1 kadar Hb lebih rendah dan berbeda nyata dari kelompok
P5 (Pb asetat + Kitosan C 1%), P6 (Pb asetat + Kitosan C 2 %), dan K3 (kontrol
kitosan) tetapi masih lebih tinggi dibandingkan dengan kelompok K1. Begitu juga
dengan kelompok P2 (Pb asetat + kitosan A 2%) lebih rendah dan berbeda nyata
dengan kelompok P6.
Pada kelompok P3 (Pb asetat + kitosan B 1 %) dan kelompok P4 (Pb asetat +
kitosan B 2%) tidak berbeda dengan kelompok K0, K3, P1, P2, P5, dan P6.
Pemberian kitosan dengan konsentrasi berbeda antara P1 dan P2, P3 dan P4, P5 dan
P6 tidak berpengaruh terhadap kadar Hb, tetapi kadar Hb meningkat sejalan dengan
kenaikan derajat deasetilasi kitosan yang diberikan.
4.2. Pembahasan
Berdasarkan hasil penelitian yang diperoleh pemberian larutan Pb asetat dapat
meningkatkan kadar Pb dalam darah hewan uji kelompok K1 (kontrol Pb) sebesar
0,33 µg/100 mL serta menunjukkan penurunan kadar hemoglobin darah (12 g/dL).
Hal ini sesuai dengan penelitian Sugiharto (2004), dan Hariono (2005) yang
hemoglobin darah tikus. Menurut Palar (2004), plumbum dapat menghambat proses
pengikatan heme dengan globin sehingga Hb yang terbentuk berkurang. Kadar Pb
dalam darah sebesar 0,5 µg/mL pada manusia dewasa dapat menurunkan sintesis Hb,
pada kadar 0,8 µg/mL dapat mengakibatkan anemia, sedangkan pada anak-anak
anemia dapat terjadi apabila dalam darah mengandung timbal pada kadar 0,7 µg/mL
(WHO, 1987 ).
Meskipun tidak terdapat perbedaan yang nyata kadar Pb darah di antara
kelompok perlakuan namun terdapat kecenderungan penurunan kadar Pb darah antara
kelompok kontrol Pb dengan kelompok perlakuan yang diberi kitosan (P1, P2, P3,
P4, P5, dan P6). Hal ini dapat dilihat dari kadar hemoglobin kelompok perlakuan.
Kecendrungan menurunnya kadar Pb darah pada kelompok perlakuan yang diberi
kitosan mengakibatkan peningkatan kadar hemoglobin seperti yang terlihat pada
Gambar 7. Terdapat peningkatan yang nyata kadar hemoglobin antara kelompok
kontrol Pb (K1) dengan semua kelompok perlakuan yang diberi kitosan (P1, P2, P3,
P4, P5, P6), serta terdapat perbedaan yang nyata kadar hemoglobin antara kelompok
perlakuan yang diberi kitosan derajat deasetilasi 64 % (P1 dan P2) dengan kadar
hemoglobin kelompok perlakuan yang diberi kitosan derajat deasetilasi 75 % (P5 dan
P6). Hal ini menunjukkan kemampuan kitosan sebagai pengkelat logam Pb.
Plumbum merupakan logam berat yang merupakan inhibitor enzim. Kerjanya
enzim yang paling mudah terhalang daya kerjanya, karena gugus –SH mudah
berikatan dengan ion-ion logam berat. Enzim-enzim pada sistem haemopoietik seperti
enzim delta aminolevulinic acid dehydratase ( -ALAD) yang berperan dalam
biosintesis hemoglobin adalah salah satu enzim yang mengandung gugus –SH,
sehingga daya kerjanya sangat dipengaruhi oleh plumbum. Interaksi antara plumbum
dengan gugus –SH enzim -ALAD mengakibatkan pembentukan intermediet
porphobilinogen dan kelanjutan dari proses pembentukan haem tidak dapat berlanjut
(terputus). Sehingga terjadi hambatan dalam sintesa hemoglobin (Saraswati, 1998;
Palar, 2004; Sudarmaji et al, 2006).
Logam berat seperti Pb selain dapat bereaksi dengan gugus –SH pada enzim
juga dapat bereaksi dengan gugus karboksilat (-COOH) dan gugus amina (-NH2).
Kitosan mengandung gugus amina dan hidroksil (-OH) sehingga menyebabkan
kitosan mempunyai reaktifitas kimia yang tinggi, bersifat polielektrolit kation
sehingga dapat berperan sebagai penukar ion (ion exchanger) dan dapat berperan
sebagai absorben terhadap logam berat dalam air limbah (Marganof, 2003).
Menurut Inoue et al (1993) Rorrer dan Hsien (1993), gugus hidroksil pada kitosan menyebabkan kitosan menjadi bersifat hidrofilik , dan gugus amina pada
rantai kitosan merupakan tempat pengkelat untuk ion logam. Maka dari sifat-sifat ini
kitosan mempunyai kemampuan untuk mengikat plumbum darah.
Kemampuan kitosan dalam mengkelat plumbum darah dapat dilihat dari
kitosan terutama pada kelompok P6 yang diberi kitosan derajat deasetilasi 75 %
konsentrasi 2 % mempunyai kadar Pb darah terendah (0,003 µg/100 mL). Juga dari
kadar hemoglobin darah terdapat perbedaan yang nyata kadar hemoglobin antara
kelompok perlakuan yang diberi kitosan derajat deasetilasi 64 % (P1 dan P2) dengan
kadar hemoglobin kelompok perlakuan yang diberi kitosan derajat deasetilasi 75 %
(P5 dan P6). Rendahnya kadar Pb darah serta tingginya kadar hemoglobin pada
kelompok P6 tersebut karena kemampuan kitosan dengan derajat deasetilasi 75 %,
konsentrasi 2 % dalam mengkelat Pb lebih tinggi dibandingkan dengan kitosan
derajat deasetilasi 64 % dan 65 %. Keadaan ini sesuai dengan yang dikemukakan
oleh Milot et al (1998), bahwa pertambahan nilai derajat deasetilasi dapat meningkatkan keupayaan dalam proses penyerapan ion logam, hal ini disebabkan
bertambahnya jumlah gugus amina bebas, serta konsentrasi larutan menyebabkan
viskositas menjadi tinggi yang penting untuk kekuatan ion.
Berdasarkan data pada Gambar 6 dan Tabel 3, kelompok K3 (kontrol kitosan)
memiliki aktivitas enzim -ALAD tertinggi (1,2 µmol PBG /jam/L eritrosit ) dan
berbeda nyata (p<0,05) dengan semua kelompok perlakuan (K0, K1, K2, P1, P2, P3,
P4, P5). Belum diketahui mekanisme yang menyebabkan kitosan dapat meningkatkan
aktivitas enzim -ALAD di darah. Pada kelompok K1 (kontrol Pb) memiliki aktivitas
enzim -ALAD lebih tinggi dibandingkan dengan kelompok K0, K2, P1, P2, P3, P4,
oleh Maes dan Gerber (1978), Fujita et al (1982), Kajimoto et al (1982) Hariono, 2005. Mekanisme kenaikan aktivitas enzim -ALAD ini juga belum diketahui.
Menurut Fujita et al (1982), peningkatan aktivitas enzim -ALAD yang terjadi di dalam darah manusia kemungkinan karena penghambatan yang berlebihan
oleh Pb terhadap aktivitas enzim -ALAD tersebut pada sel-sel sum-sum tulang
belakang selama pemaparan Pb.
Kelompok P6 (Pb asetat + kitosan derajat deasetilasi 75 % konsentrasi 2 %)
memiliki aktivitas enzim -ALAD 0, 9 µmol PBG /jam/l eritrosit berbeda nyata
dengan kelompok P5 (Pb asetat + kitosan derajat deasetilasi 75 % konsentrasi 1 %),
aktivitas enzim -ALAD 0,49 µmol PBG /jam/l eritrosit; kelompok P3 (Pb asetat +
kitosan derajat deasetilasi 65 % konsentrasi 1 %, aktivitas enzim -ALAD 0,43 µmol
PBG /jam/l eritrosit; dan kelompok P1 (Pb asetat + kitosan derajat deasetilasi 64 %
konsentrasi 1 %) aktivitas enzim -ALAD 0,33 µmol PBG /jam/l eritrosit ).
BAB V
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Dari hasil penelitian dapat diambil kesimpulan sebagai berikut :
a. Pemberian kitsan pada derajat deasetilasi 64%, 65%, dan 75 % dengan
konsentrasi1% dan 2% terhadap mencit yang dipapar Pb asetat dengan dosis 25
mg/ kg BB tidak menunjukkan perbedaan kadar Pb darah yang nyata.
b. Aktivitas enzim -ALAD pada kelompok K3 (kontrol kitosan) meningkat dan
berbeda nyata dengan kelompok K0, K1, K2, P1, P2, P3, P4 dan P5
c. Pemberian kitosan pada derajat deasetilasi 75% dengan konsentrasi 2%
(kelompok P6) terhadap mencit yang dipapar Pb asetat menunjukkan peningkatan
aktivitas enzim -ALAD dan berbeda nyata dengan kelompok P1, P2, dan P5.
d. Pemberian kitosan pada derajat deasetilasi 64%, 65%, dan 75 % dengan
konsentrasi 1% dan 2% terhadap mencit yang dipapar Pb asetat dengan dosis 25
mg/ kg BB meningkatkan kadar hemoglobin darah dan berbeda nyata dengan
kelompok K1 (kontrol Pb).
e. Kadar hemoglobin darah pada kelompok P6 meningkat dan berbeda nyata dengan
5.2. Saran
40 1. Perlu dilakukan penelitian yang sama dengan derajat deasetilasi yang lebih
tinggi (>75 % DD < 100 %) dan dengan jumlah hewan uji yang lebih banyak.
2. Perlu dilakukan penelitian yang sama dengan menggunakan bentuk kitosan
yang berbeda.
3. Perlu dilakukan pengukuran nilai viskositas larutan kitosan yang digunakan
selama perlakuan.
4. Perlu dilakukan penelitian lanjutan untuk mengetahui mekanisme penyerapan
plumbum oleh kitosan secara in vivo di dalam darah.
5. Perlu diperhatikan agar AAS yang digunakan untuk mengukur kadar Pb darah
DAFTAR PUSTAKA
Agusnar, H. 1990. Kitin dan Kitosan sebagai Fasa dalam Kromatografi Gas untuk Pemisahan Hidrokarbon. Tesis M.Sc. UKM
Ahmad, A.L., Sumathi, S., Hameed, B.H. 2004. Chitosan: A Natural Bioplolymer for the Adsorption of Residue from Oily Wastewater. Adsorption Science & Teechnology. 22:75.
Akagi, R., Nishitani, C., Harigae, H., Horie,Y., Garbaczewski,L., Hassoun,A., Marcelis,R., Versrtraeten, L., and Sassa, S. 2000. Molecular Analysis of Delta Aminolevulinate Dehydratase Deficiency in a Patient with an Unusual Late-Onset Porphyria. Blood. 96:3618
Alimuniar, A., Zainuddin, R. 1998. An Economical Technique for Producing, Advantage integration chitin and chitosan, London, Elvesier. p. 627.
A.T.S.D.R. (Agency for Toxic Substances and Disease Registry). 1993. Toxicological Profile for Lead, Update. Prepared by Clement International Corporation Under Contact No. 205-88-060 for ATSDR, U.S. Public Health Services, Atlanta, GA.
Bartik, M. 1981. Veterinary Toxicology. Elsevier Scientific Publishing Company, New York. pp.108-110.
Berger, J., Reist, M., Mayer, J.M., Felt, O., Peppas, N.A., and Gurny, R. 2004. Review Article.Structure and Interactions in Covalently and Ionically Crosslinked Chitosan Hydrogels for Biomedical Applications. European Journal of Pharmaceutics and Biopharmaceutics. 57:19-34.
Burke, A., Yilmaz, E. and Hasirci, N. 2002. Evaluation of Chitosan As a Potential Medical Iron (III) ion Adsorbent. Turk J Med Sci. 30:341-348.
Centers for Disease Control and Prevention. 2000. Recommendation for Blood Lead Screening of Young Children Enrolled in Medicaid: Targeting a Group at High Risk. MMWR. 49:1-13.
http:/www.pikiran-Ellenhorn, M.J and Barceloux, D.G.1988. Medical Toxicology: Diagnosis and Treatment of Human Poisoning. Elsevier Science Publishing Company, Inc. New York.
Federer,W.Y. 1963. Experimental Design Theory and Application. New York, Mac Millan. p.544.
Fernandez-Kim, S.O. 2004. Physicochemical and Functional Properties of Crawfish Chitosan as Effected by Different Processing Protocols. Thesis The Departement of Food Science. Seoul National University. pp.6-8; 28-29.
Fujita, H., Sato, K., and Sano, S. 1982. Increase in the Amount of Erythrocyte -Aminolevulinic Acid Dehydratase in Workers with Moderate Lead Exposure. Intl. Arch.of Occupational and Environmental Health. 50:287
Gao, Y., Lee, K.H., Oshima, M., and Motomizu, S. 2000. Adsorption Behavior of Metal Ions Cross-Linked Chitosan and the Determination of Oxoanions after Pretreatment with a Chitosan Column. Analytical Science.16:1303
Goering, P.L. 1993. Lead-Protein Interaction as a Basis for Lead Toxicity. Neurolotoxicology. 14:60.
Goyer, R.A., Cherian, MG., Jones, M.M., and Reigar, J.R. 1995. Role of Chelating Agent for Prevention, Intervention, and Treatment of Exposures to Toxic Metal. Environmental Health Prespective. 103:132
Guibal, E. 2004. Metal Ion Interaction with Chitosan A Review. Separation and Purification Technology. 38:43.
Guibal, E., Touraud, E., and Roussy, J. 2005. Chitosan Interaction with Metal Ions And Dyes : Dissolved-State Versus Solid-State Application. World J. Microbiol. Biotechnol. 21:913.
Hariono. 2005. Efek Pemberian Plumbum (Timah Hitam) Anorganik pada Tikus Putih (Rattus norvegicus). J.Sain Vet. 23:107-108
2006. Efek Pemberian Plumbum (Timah Hitam) Organik pada Tikus Putih (Rattus norvegicus). J.Sain Vet. 24:125-134