Lampiran 1
Skema Alur Pikir
1. Penggunaan jangka panjang obat kumur berbahan dasar kimia berefek samping menimbulkan diskolorisasi gigi, rasa kurang enak, ulserasi mukosa mulut, dan parestesi. Oleh karena itu masyarakat kini lebih memilih produk berbahan alami, salah satunya adalah obat kumur yang mengandung cengkeh. (Anggayanti NA dkk, 2013; Arinda A dkk, 2010; Pratama IKJ dkk, 2013; Bhowmik D dkk, 2012; Rani B dkk, 2012)
2. Cengkeh (Syzygium Aromaticum) adalah tanaman asli Indonesia dan sampai saat ini, sebagian besar kebutuhan cengkeh dunia (80%) masih dipasok oleh Indonesia, disusul oleh Madagaskar dan Tanzania. (Pratama IKJ dkk, 2013)
3. Cengkeh mempunyai kandungan kalsium (4%) dan fosfor (13%). Kandungan kalsium dan fosfor merupakan mineral penting dalam proses remineralisasi enamel. (Bhowmik dkk, 2012, Milind P dkk, 2011; Mittal M dkk, 2014; Pratama IKJ dkk, 2012; Susi dkk, 2014; Prasetyo EA, 2005) 4. Perendaman dalam larutan ekstrak cengkeh 1%, 5%, 10% selama 4 menit
dapat meningkatkan kekerasan enamel pada gigi yang terdemineralisasi secara signifikan karena kandungan kalsium dan fosfatnya (Alyaa HKA dkk, 2011)
5. Minyak cengkeh 0,05% dapat menghambat proses dekalsifikasi enamel oleh jus apel. Kandungan eugenol dan eugenil asetat yang terdapat dalam minyak cengkeh dipercaya dapat menghambat dekalsifikasi enamel meskipun diperlukan penelitian lebih lanjut. (Charu M. Marya dkk, 2012) 6. Minuman ringan seperti jus jeruk berpotensi menyebabkan penurunan
kekerasan enamel karena mempunyai kandungan asam yang tinggi (Lussi A dkk, 2008)
kekerasan enamel berkisar 270-360 VHN, sedangkan Cirano FR dkk melaporkan sebesar 398,41±24,74 VHN. (Gutierrez-Salazar MP dkk, 2003; Cirano FR dkk, 2003)
Permasalahan
1. Apakah terdapat pengaruh perendaman obat kumur cengkeh terhadap kekerasan permukaan enamel gigi yang telah direndam dalam jus jeruk kemasan?
2. Apakah terdapat pengaruh perendaman obat kumur cengkeh yang ditambahkan saliva buatan terhadap kekerasan permukaan enamel gigi yang telah direndam dalam jus jeruk kemasan ?
3. Bagaimanakah perbandingan kekerasan permukaan enamel antara perendaman obat kumur cengkeh dengan perendaman obat kumur cengkeh yang ditambah saliva buatan ?
Tujuan Penelitian
1. Mengetahui pengaruh perendaman obat kumur cengkeh terhadap kekerasan permukaan enamel gigi yang telah direndam dalam jus jeruk kemasan.
2. Mengetahui pengaruh obat kumur cengkeh yang ditambahkan saliva buatan terhadap kekerasan permukaan enamel gigi yang telah direndam dalam jus jeruk kemasan.
Manfaat Penelitian
a. Manfaat Teoritis
1. Sebagai data dan informasi mengenai efek perendaman dalam obat kumur mengandung ekstrak cengkeh terhadap kekerasan permukaan enamel gigi.
2. Sebagai bahan masukan untuk perkembangan ilmu pengetahuan kedokteran gigi, khususnya di bidang biologi oral.
b. Manfaat Praktis
1. Bagi peneliti, sebagai data untuk melakukan penelitian lanjutan mengenai efek ekstrak cengkeh terhadap kekerasan permukaan enamel gigi dalam larutan kumur.
Lampiran 2
II. Pengukuran Kekerasan Awal Enamel Gigi
Lampiran 3
PENGARUH OBAT KUMUR CENGKEH TERHADAP NILAI KEKERASAN ENAMEL SETELAH DIRENDAM DENGAN LARUTAN ASAM
LEMBAR PEMERIKSAAN
No Sampel :
PEMERIKSAAN GIGI
Regio Gigi : Kiri Kanan
Kriteria Inklusi Tanpa karies
Belum pernah direstorasi
Kriteria Eksklusi Karies
Erosi
Atrisi
Abrasi
Terdapat tambalan
Fraktur
Nekrosis
Kesimpulan Hasil Pemeriksaan :
Lampiran 4
LEMBARAN PENJELASAN KEPADA SUBJEK PENELITIAN
Selamat pagi,
Bersama ini saya, Novia adalah mahasiswa S1 semester 7 Fakultas Kedokteran Gigi, Universitas Sumatera Utara yang saat ini sedang mengerjakan skripsi di Departemen Biologi Oral FKG USU. Sehubungan dengan penulisan skripsi saya, saya akan mengadakan penelitian dengan judul “Pengaruh Obat Kumur
Cengkeh Terhadap Nilai Kekerasan Permukaan Enamel Gigi Yang Telah Di Demineralisasi”
Tujuan dari penelitian ini adalah untuk melihat pengaruh waktu perendaman berbeda obat kumur cengkeh terhadap kekerasan enamel gigi yang mengalami demineralisasi dan melihat waktu perendaman dalam obat kumur cengkeh yang paling berpengaruh terhadap kekerasan enamel gigi yang mengalami demineralisasi.
aquabidest, dan saliva buatan yang baru setiap hari. Setelah 1 minggu, diukur kekerasan enamel dengan micro vickers.
Sebanyak 32 sampel gigi premolar pertama atas permanen akan digunakan dalam penelitian ini dengan kriteria inklusi gigi premolar pertama atas permanen tanpa karies dan belum pernah direstorasi dan kriteria eksklusi gigi yang karies, mengalami erosi, atrisi, abarasi, terdapat tambalan, fraktur, dan nekrosis.
Data yang akan diperoleh nantinya akan kami simpan dengan baik dan dijamin kerahasiaannya, begitu juga ketika hasil penelitian ini kami publikasikan. Kesediaan Bapak/Ibu sangat kami hargai dan bukan merupakan paksaan. Bila Bapak/Ibu ingin meminta kembali sampel gigi sebelum kami lakukan penelitian, dapat mengajukan pada kami dan kami akan mengembalikan sampel gigi tersebut dalam keadaan utuh. Namun bila Bapak/Ibu meminta kembali sampel gigi setelah kami melakukan penelitian, maka sampel gigi yang akan kami kembalikan adalah dalam keadaan sudah diberikan perlakuan.
Sebagai tanda terima kasih atas partisipasi Bapak/Ibu dalam penelitian ini kami akan memberikan imbalan sebesar Rp 20.000,- untuk setiap sampel yang kami peroleh.
Bila ada hal yang kurang berkenan atau merasa terganggu kenyamaan, Bapak/Ibu dapat menghubungi saya, Novia (Tel. 087768778645) atau di Departemen Biologi Oral FKG USU untuk mendapat penjelasan.
Demikian informasi ini saya sampaikan. Atas bantuan, partisipasi dan kesediaan Bapak/Ibu, saya ucapkan terima kasih.
Peneliti,
Lampiran 5
SURAT PERNYATAAN PERSETUJUAN (INFORMED CONSENT)
Saya yang bertanda tangan di bawah ini:
Nama :
Umur :
Jenis Kelamin : L / P
Alamat :
Instansi :
Menyatakan telah membaca lembar penjelasan dan sudah mengerti serta bersedia untuk turut serta memberikan gigi sebagai sampel dalam penelitian atas nama Novia yang berjudul “Pengaruh Obat Kumur Cengkeh Terhadap Nilai
Kekerasan Permukaan Enamel Gigi Yang Telah Di Demineralisasi” dan
menyatakan tidak keberatan maupun melakukan tuntutan di kemudian hari.
Demikian pernyataan ini saya buat dalam keadaan sehat, penuh kesadaran dan tanpa paksaan dari pihak manapun.
Medan, 2016 Pembuat Pernyataan
Lampiran 10
Hasil uji normalitas SPSS
Hasil uji statistik SPSS T Berpasangan
Kelompok A1 (Perendaman obat kumur cengkeh 30 detik)
Kelompok A2 (Perendaman obat kumur cengkeh 1 menit)
Kelompok A3 (Perendaman obat kumur cengkeh 2 menit)
Kelompok A4 (Perendaman obat kumur cengkeh 4 menit)
Kelompok B1 (Perendaman obat kumur cengkeh + saliva buatan 30 detik)
Kelompok B2 (Perendaman obat kumur cengkeh + saliva buatan 1 menit)
Kelompok B3 (Perendaman obat kumur cengkeh + saliva buatan 2 menit)
Kelompok B4 (Perendaman obat kumur cengkeh + saliva buatan 4 menit)
Hasil uji statistik SPSS ANOVA
Perbandingan ∆ VHN jus jeruk kemasan dengan obat kumur cengkeh antar kelompok
Multiple Comparisons
Perbandingan antar kelompok Mean Difference (I-J)
Std. Error Sig. 95% Confidence Interval
Lower Bound Upper Bound
Kelompok A1
Kelompok A2 -2.11250 12.32093 1.000 -42.9184 38.6934
Kelompok A3 -5.90500 12.32093 1.000 -46.7109 34.9009
Kelompok A4 -37.22000 12.32093 .092 -78.0259 3.5859
Kelompok B1 116.34250* 12.32093 .000 75.5366 157.1484 Kelompok B2 111.64250* 12.32093 .000 70.8366 152.4484 Kelompok B3 109.46250* 12.32093 .000 68.6566 150.2684 Kelompok B4 110.28000* 12.32093 .000 69.4741 151.0859
Kelompok A2
Kelompok A1 2.11250 12.32093 1.000 -38.6934 42.9184 Kelompok A3 -3.79250 12.32093 1.000 -44.5984 37.0134 Kelompok A4 -35.10750 12.32093 .129 -75.9134 5.6984
Between Groups 125272.910 7 17896.130 58.944 .000
Within Groups 7286.657 24 303.611
Kelompok B1 118.45500* 12.32093 .000 77.6491 159.2609 Kelompok B2 113.75500* 12.32093 .000 72.9491 154.5609 Kelompok B3 111.57500* 12.32093 .000 70.7691 152.3809 Kelompok B4 112.39250* 12.32093 .000 71.5866 153.1984
Kelompok A3
Kelompok A1 5.90500 12.32093 1.000 -34.9009 46.7109 Kelompok A2 3.79250 12.32093 1.000 -37.0134 44.5984 Kelompok A4 -31.31500 12.32093 .226 -72.1209 9.4909 Kelompok B1 122.24750* 12.32093 .000 81.4416 163.0534 Kelompok B2 117.54750* 12.32093 .000 76.7416 158.3534 Kelompok B3 115.36750* 12.32093 .000 74.5616 156.1734 Kelompok B4 116.18500* 12.32093 .000 75.3791 156.9909
Kelompok A4
Kelompok A1 37.22000 12.32093 .092 -3.5859 78.0259 Kelompok A2 35.10750 12.32093 .129 -5.6984 75.9134 Kelompok A3 31.31500 12.32093 .226 -9.4909 72.1209 Kelompok B1 153.56250* 12.32093 .000 112.7566 194.3684 Kelompok B2 148.86250* 12.32093 .000 108.0566 189.6684 Kelompok B3 146.68250* 12.32093 .000 105.8766 187.4884 Kelompok B4 147.50000* 12.32093 .000 106.6941 188.3059
Kelompok B1
Kelompok A1 -116.34250* 12.32093 .000 -157.1484 -75.5366 Kelompok A2 -118.45500* 12.32093 .000 -159.2609 -77.6491 Kelompok A3 -122.24750* 12.32093 .000 -163.0534 -81.4416 Kelompok A4 -153.56250* 12.32093 .000 -194.3684 -112.7566 Kelompok B2 -4.70000 12.32093 1.000 -45.5059 36.1059 Kelompok B3 -6.88000 12.32093 .999 -47.6859 33.9259 Kelompok B4 -6.06250 12.32093 1.000 -46.8684 34.7434
Kelompok B2
Kelompok A1 -111.64250* 12.32093 .000 -152.4484 -70.8366 Kelompok A2 -113.75500* 12.32093 .000 -154.5609 -72.9491 Kelompok A3 -117.54750* 12.32093 .000 -158.3534 -76.7416 Kelompok A4 -148.86250* 12.32093 .000 -189.6684 -108.0566 Kelompok B1 4.70000 12.32093 1.000 -36.1059 45.5059 Kelompok B3 -2.18000 12.32093 1.000 -42.9859 38.6259 Kelompok B4 -1.36250 12.32093 1.000 -42.1684 39.4434
Kelompok B3
Kelompok A1 -109.46250* 12.32093 .000 -150.2684 -68.6566 Kelompok A2 -111.57500* 12.32093 .000 -152.3809 -70.7691 Kelompok A3 -115.36750* 12.32093 .000 -156.1734 -74.5616 Kelompok A4 -146.68250* 12.32093 .000 -187.4884 -105.8766 Kelompok B1 6.88000 12.32093 .999 -33.9259 47.6859 Kelompok B2 2.18000 12.32093 1.000 -38.6259 42.9859 Kelompok B4 .81750 12.32093 1.000 -39.9884 41.6234
Kelompok B4
Kelompok A1 -110.28000* 12.32093 .000 -151.0859 -69.4741 Kelompok A2 -112.39250* 12.32093 .000 -153.1984 -71.5866 Kelompok A3 -116.18500* 12.32093 .000 -156.9909 -75.3791 Kelompok A4 -147.50000* 12.32093 .000 -188.3059 -106.6941 Kelompok B1 6.06250 12.32093 1.000 -34.7434 46.8684
Kelompok B2 1.36250 12.32093 1.000 -39.4434 42.1684
DAFTAR PUSTAKA
1. Anggayanti NA, Adiatmika IPG, Adiputra N. Berkumur dengan teh hitam lebih efektif daripada chlorhexidine gluconate 0,2% untuk menurunkan akumulasi plak gigi. Jurnal PDGI 2013; 62(2): 35-40.
2. Arinda A, Rahardjo P, Triwardani A. Perbedaan efektivitas obat kumur yang mengandung cengkeh dengan obat kumur chlorhexidine gluconate 0,2% dalam menghambat pembentukan plak. Ortho Dent J 2010; 1(1): 22-4.
3. Pratama IKJ, Adi P, Prasetyaningrum N. Pengaruh larutan ekstrak bunga cengkeh (syzygium aromaticum) terhadap perubahan ph saliva buatan yang diinduksi streptococcus mutans secara in vitro. Jurnal PDGI 2013; 62(2): 35-40. 4. Bhowmik D, Kumar KPS, Yadav A, Srivastava S, Paswan S, Dutta AS. Recent
trends in indian traditional herbs syzygium aromaticum and its health benefits. J of Pharmacognosy and Phytochemistry 2012; 1(1): 14-21.
5. Rani B, Kacchawa GR, Yadav RK, Chauhan V, Maheshwari R. Phytochemical effectiveness of clove oil: a review. Int J of Res in Pharmacology and Pharmacotherapeutics 2012; 1(2): 230-3.
6. Milind P, Deepa K. Clove: a champion spice. IJRAP 2011; 2(1): 47-54.
7. Mittal M, Gupta N, Parashar P, Mehra V, Khatri M. Phytochemical evaluation and pharmacological activity of syzygium aromaticum: a comprehensive review. Int J Pharm Pharm Sci 2014; 6(8): 67-72.
8. Susi, Abidin T. Pengaruh buah belimbing wuluh (averrhoa bilimbi) terhadap pencegahan karies gigi dan perubahan terhadap email gigi (literatur review). In: Proceeding Book Regional Dental Meeting & Exhibition-VI 2014. Medan, 2014: 331-5.
9. Prasetyo EA. Keasaman minuman ringan menurunkan kekerasan permukaan gigi. Maj Ked Gigi (Dent J) 2005; 38(2): 60-3.
11. Marya CM, Satija G, Avinash J, Nagpal R, Kapoor R, Ahmad A. In vitro inhibitory effect of clove essential oil and its two active principles on tooth decalcification by apple juice. Int J Dent 2012: 1-6.
12. Tahmassebi JF, Duggal MS, Kotru GM, Curzon MEJ. Soft drinks and dental health: a review of the current literature. J Dent 2006; 34: 2-6.
13. Machado C, Lacefield W, Catledge A. Human enamel microhardness, elastic modulus and surface integrity after beverage contact. Braz Dent J 2008; 19(1): 68-72.
14. Lussi A, Jaeggi T. Erosion-diagnosis and risk factors. Clin Oral Invest 2008; 12(1): 7-9.
15. Gutierrez-Salazar MP, Reyes-Gasga J. Microhardness and chemical composition of human tooth. Mater Res 2003; 6(3): 371-2.
16. Cirano FR, Romito GA, Todescan JH. Determination of enamel and coronal dentin microhardness. Braz J Oral Sci 2003; 2(6): 258-63.
17. Towaha J. Manfaat eugenol cengkeh dalam berbagai industri di Indonesia. Perspektif 2012; 11(2): 80-4.
18. Chaiya A, Saraya S, Chuakul W, Temsirirkkul R. Screening for dental caries: preventive activities of medicinal plants against streptococcus mutans. J Phar Sci 2013; 40(1): 15-6.
19. Aneja KR, Joshi R. Antimicrobial activity of syzygium aromaticum and its bud oil against dental cares causing microorganisms. Haryana, India: Kurukshetra University, 2010: 4850-5.
20. Ali Hs, Kamal M, Mohamed SB. In vitro clove oil activity against periodontopathic bacteria. J Sc Tech 2009; 10(1): 1-7.
21. Widyaningtyas V, Rahayu YC, Barid I. Analisis peningkatan remineralisasi enamel gigi setelah direndam dalam susu kedelai murni menggunakan scanning electron microscope (SEM). Jurnal Pustaka Kesehatan 2014; 2(2): 258-62.
23. Berkovitz BKB, Holland GR, Moxham BJ. Oral anatomy, histology and embryology. 4th ed. Oxford: Mosby Elsevier, 2009: 105-8.
24. Bath-Balogh M, Fehrenbach MJ. Illustrated dental embryology, histology, and anatomy. 2nd ed. Missouri: Saunders Elsevier, 2006: 180-2, 185-6.
25. Pintauli S, Hamada T. Menuju gigi dan mulut sehat: pencegahan dan pemeliharaannya. Ed 1. Medan: USU Press, 2008: 21-3.
26. Fathilah AR, Rahim ZHA. The effect of beverages on the release of calcium from the enamel surface. Annal Dent Univ Malaya 2008; 15(1): 1-4.
27. Borjian A, Ferrari CCF, Anouf A, Touyz LZG. Pop-cola acids and tooth erosion: an in vitro, in vivo, electron-microscopic, and clinical report. Int J Dent 2010: 10-12.
28. Roberts MW, Wright JT. The dynamic process of demineralization and remineralization. J Prof Excel 2009; 7(7): 16-21.
29. Chuenarrom C, Benjakul P, Daosodsai P. Effect of indentation load and time on knoop and vickers microhardness tests of enamel and dentin. Material Res 2009; 12(4): 473-6.
30. Zanet CG, Fava M, Alves LAC. In vitro evaluation of the microhardness of bovine enamel exposed to acid solutions after bleaching. Braz Oral Res 2011; 25(6): 562-7.
31. Benjakul P, Prommontri P, Chuenarrom C, Leggat U. Effects of sour curry temperature with fermented shrimp paste on surface hardness of tooth enamel. Songklanakarin J Sci Technol 2011; 33(4): 419-23.
32. Seow WK, Thong KM. Erosive effects of common beverages on extracted premolar teeth. Aust Dent J 2005; 50(3): 173-8.
33. Schwarts GT. Enamel thickness and the helicoidal wear plane in modern human mandibular molars. Arch Oral Biol 2000; 45(5): 401-9.
35. Stewart E. Microindentation hardness testing.
36. Van der Voort GF. Microindentation hardness testing.
37. Nasution MI. Pengenalan gigi. Medan: USU Press, 2011: 71-5.
38. Farah CS, McIntosh L, McCullough MJ. Mouthwashes. Aust Prescr 2009; 32: 162-4.
39. Herdiyati Y, Gartika M, Kartikadewi N, Dewi FD. Differences in effectiveness of herbal, betel, leaves, and chlorhexidine mouthwash on plaque reduction in orphanage children. IJSR 2013; 4(4): 260-3.
40. Subramaniam P, Nandan N. Effect of xylitol, sodium fluoride and triclosan containing mouth rinse on streptococcus mutans. Contemp Clin Dent 2011; 2(4): 287-90.
41. Walters L. The effect of xylitol on the growth of three normal oral commensal or probiotic bacteria. Tesis. Amerika Serikat: Degree of Bachelor of Science Coastal Carolina University, 2011: 14-6.
42. Ogochukwu UNC, Sabinus OI. Effect of some preservatives on the aqueous stability of an oral rehydration salt solution intended for use in developing countries. Asian J Pharm Clin Res 2013; 6(2): 33-7.
43. Lalitha C, Rao PVVP. Antimicrobial efficacy of low level cosmetic preservatives. World J Pharmacy and Pharmaceutical Sci 2014; 3(2): 1688.
44. David P, Crowley PJ. Antimicrobial preservatives part two: choosing a preservatives. American Pharmaceutical Review 2012; 1-5.
45. Stanojevic D, Comic L, Stefanovic O, Sukdolak S. Antimicrobial effects of sodium benzoate, sodium nitrite and potassium sorbate and their synergistic action in vitro. Bulgarian J Agri Sci 2009; 15(4): 307-11.
47. Sulieman AME, Abdelrahman SE, Rahim AMA. Phytochemical analysis of local spearmint (mentha spicata) leaves and detection of the antimicrobial activity of its oil. J Microbiol Res 2011; 1(1): 1-4.
48. Sujana P, Sridhar Tm. Jothna P. Naidu CV. Antibacterial activity and phytochemical analysis of mentha piperita L. (peppermint)- an important multipurpose medicinal plant. American J Plant Sci 2013; 4: 78-82.
49. Singh R, Shushni MA, Belkheir A. Antibacterial and antioxidant activities of
mentha piperita L. Arabian J Chem 2015; 8: 322-8.
50. Soesilo D, Santoso RE, Diyatri I. Peranan sorbitol dalam mempertahankan kestabilan ph saliva pada proses pencegahan karies. Dent J (Maj Ked Gigi) 2005; 38(1): 25-8.
51. Almeida PDV, Gragio AMT, Machado MAN, Lima AAS, Azevedo LR. Saliva composition and functions: a comprehensive review. J Contemp Dent Pract 2008; 9(3): 2.
52. Supriyadi. Statistik kesehatan. Jakarta: Salemba Medika, 2014: 119.
53. Kim DK. Nanoindentation basic principle. .
2015)
54. Walangare KBA, Lumenta ASM, Wuwung JO, Sugiarso BA. Rancang bangun alat konversi air laut menjadi air minum dengan proses destilasi sederhana meggunakan pemanas elektrik. E-Jurnal Teknik Elektro dan Komputer 2013: 1. 55. Aziz T, Yuanita, Susanti. Ekstraksi eugenol dari daun salam india. Jurnal Teknik
Kimia 2010; 3(17): 19-21.
56. Tatang. Kegunaan unsur kalsium dan sejarah kalsium. smpsma.com/kegunaan-unsur-kalsium-dan-sejarah-kalsium.html (19 Maret 2016)
57. Hikmat. Pengertian unsur fosfor dan efeknya.
2016)
59. Pontefract H, J, Hughes J, Kemp K, Yates R, Newcombe RG, Addy M. The erosive effects of some mouthrinses on enamel. J Clin Periodontal 2001; 28: 319-24.
60. Frey S. What can change the ph of someone’s mouth
BAB 3
METODOLOGI PENELITIAN
3.1 Jenis Penelitian
Jenis penelitian ini adalah eksperimental laboratoris dengan rancangan penelitian pretest and posttest control group design.
3.2 Tempat dan Waktu Penelitian 3.2.1Tempat Penelitian
Penelitian ini dilakukan di Laboratorium Mikrobiologi Fakultas Matematika dan Ilmu Pengetahuan Alam USU untuk penggunaan inkubator dan Laboratorium Teknik Mesin Universitas Negeri Medan untuk pengukuran kekerasan enamel.
3.2.2 Waktu Penelitian
Penelitian ini dimulai dari bulan Januari sampai bulan April 2016 yang mencakup pengumpulan sampel, penelitian, pengumpulan data, pengolahan data dan hasil penelitian.
3.3 Sampel dan Besar Sampel 3.3.1Sampel Penelitian
3.3.2Besar Sampel
Dalam menghitung besar sampel penelitian eksperimental digunakan rumus Federer. Rumus besar sampel Federer yaitu:52
Dimana t = jumlah perlakuan dan r = jumlah sampel Penelitian ini menggunakan 8 kelompok perlakuan yaitu:
1. Kelompok A1: Perendaman dalam obat kumur cengkeh 30 detik setiap hari selama 1 minggu.
2. Kelompok A2: Perendaman dalam obat kumur cengkeh 1 menit setiap hari selama 1 minggu.
3. Kelompok A3: Perendaman dalam obat kumur cengkeh 2 menit setiap hari selama 1 minggu.
4. Kelompok A4: Perendaman dalam obat kumur cengkeh 4 menit setiap hari selama 1 minggu.
5. Kelompok B1: Perendaman dalam obat kumur cengkeh yang ditambah saliva buatan 30 detik setiap hari selama 1 minggu.
6. Kelompok B2: Perendaman dalam obat kumur cengkeh yang ditambah saliva buatan 1 menit setiap hari selama 1 minggu.
7. Kelompok B3: Perendaman dalam obat kumur cengkeh yang ditambah saliva buatan 2 menit setiap hari selama 1 minggu.
8. Kelompok B4: Perendaman dalam obat kumur cengkeh yang ditambah saliva buatan 4 menit setiap hari selama 1 minggu.
Dari perhitungan di atas, jumlah sampel minimal pada setiap perlakuan adalah 4 gigi premolar pertama maksila permanen. Dalam penelitian ini terdapat 8 perlakuan sehingga total sampel yang digunakan adalah sebanyak 32 buah.
3.4 Kriteria Sampel
Kriteria sampel penelitian ini adalah :
a. Kriteria Inklusi: Gigi premolar pertama maksila tanpa karies, dan tidak ada tambalan.
b. Kriteria Ekslusi: Gigi karies, mengalami erosi, atrisi dan abrasi, terdapat tambalan, terdapat fraktur, dan nekrosis.
3.5 Variabel Penelitian 3.5.1Variabel Bebas
1. Obat kumur cengkeh sediaan (volume 5 ml/ sampel)
2. Obat kumur cengkeh sediaan (volume 5 ml/sampel) yang ditambah saliva buatan (volume 3 ml/sampel)
3.5.2Variabel Terikat
Kekerasan permukaan enamel gigi
3.5.3Variabel Terkendali
1. Gigi yang digunakan yaitu gigi premolar pertama maksila permanen 2. Bahan demineralisasi yang digunakan yaitu jus jeruk kemasan (pH 3,6). 3. Alat ukur pH yaitu pH digital Hanna Meter
4. Lama perendaman jus jeruk kemasan 5 menit
5. Lama perendaman obat kumur cengkeh 30 detik, 1 menit, 2 menit, dan 4 menit setiap hari selama 1 minggu
6. Lama perendaman obat kumur cengkeh yang ditambah saliva buatan 30 detik, 1 menit, 2 menit, dan 4 menit setiap hari selama 1 minggu
8. Alat pengukur kekerasan yaitu Micro Vickers Hardness Tester 9. pH saliva buatan 6,8
10.Volume perendaman obat kumur cengkeh 5 ml 11.Volume perendaman jus jeruk kemasan 5 ml
12.Volume perendaman aquabidest selama 24 jam 5 ml
13.Volume pencampuran saliva buatan 3 ml ke dalam obat kumur cengkeh 5 ml
3.5.4Variabel Tidak Terkendali
1. Suhu ruangan
Variabel Terkendali
1. Sampel gigi premolar pertama maksila permanen 2. Bahan demineralisasi (jus jeruk kemasan dengan pH
3,6)
3. Alat ukur pH dengan pH digital Hanna Meter 4. Lama perendaman jus jeruk kemasan 5 menit
5. Lama perendaman obat kumur cengkeh 30 detik, 1 menit, dan 2 menit selama 1 minggu
6. Lama perendaman obat kumur cengkeh yang dicampur saliva buatan 30 detik, 1 menit, 2 menit, dan 4 menit setiap hari selama 1 minggu
7. Suhu inkubator 37°C
8. Alat pengukur kekerasan dengan Micro Vickers
Hardness Tester
9. pH saliva buatan 6,8
10.Volume perendaman obat kumur cengkeh 5 ml 11.Volume perendaman jus jeruk kemasan 5 ml
12.Volume perendaman aquabidest selama 24 jam 5 ml 13. Volume pencampuran saliva buatan 3 ml ke dalam
obat kumur cengkeh 5 ml
Variabel Tidak
1. Obat kumur cengkeh sediaan dengan volume 5 ml/ sampel
2. Obat kumur cengkeh sediaan (volume 5
ml/sampel) yang ditambah saliva buatan (volume 3 ml/sampel)
Variabel Terikat
3.6 Definisi Operasional Penelitian
1. Obat kumur cengkeh merupakan obat kumur sediaan yang sudah ada dipasaran produk PT.X dengan konsentrasi 0,35% minyak cengkeh dalam 200 ml.
2. Aquabidest adalah air destilasi murni yang telah melalui proses penyulingan 2 kali.
3. Saliva buatan yang digunakan adalah saliva yang dibuat dengan komposisi hampir sama dengan komposisi saliva asli yaitu kalsium (Ca), natriumklorida (NaCl), kalium thiosanat (KSCN), kalium klorida (KCL), natrium bikarbonat (NaHCO3), urea ((NH2)2CO), dan kalium dihidrogen fosfat (KH2PO4) yang diperoleh dari Universitas Indonesia dengan pH 6,8.
4. Kekerasan permukaan enamel adalah nilai ketahanan permukaan enamel terhadap suatu tekanan yang diperoleh dari pengukuran menggunakan alat uji kekerasan Vickers dalam satuan VHN (Vickers Hardness Number). Perbedaan nilai kekerasan dapat dihitung dengan rumus:
∆VHN = VHN setelah perlakuan – VHN sebelum perlakuan.
5. Gigi premolar pertama maksila permanen adalah gigi yang pada anatomi normal terletak pada urutan ke empat dihitung dari garis tengah wajah pada rahang atas baik kiri maupun kanan, memiliki 2 cusp yaitu cusp bukal dan cusp palatal, dan memiliki 2 saluran akar yang sudah dicabut untuk keperluan ortodonti.
6. Bahan demineralisasi adalah jus jeruk kemasan 350 ml dengan pH 3,6. 7. pH digital Hanna meter adalah alat untuk mengukur pH larutan.
8. Lama perendaman jus jeruk kemasan adalah waktu yang diperlukan untuk merendam sampel dalam jus jeruk kemasan, yaitu selama 5 menit.
9. Lama perendaman obat kumur cengkeh adalah waktu yang diperlukan untuk merendam sampel dalam obat kumur cengkeh, yaitu 30 detik, 1 menit, 2 menit, dan 4 menit setiap hari selama 1 minggu.
11.Inkubator adalah alat yang digunakan untuk menyamakan suhu aquabidest dengan suhu rongga mulut, yaitu sebesar 37°C. Inkubator yang digunakan adalah merek Fisher Scientific 630D Isotemp Incubator.
12. Micro Vickers Hardness Tester adalah alat penguji kekerasan suatu benda
dengan membuat indentasi pada permukaan gigi dengan beban 100 gram selama 15 detik. Pada penelitian ini Vickers hardness tester yang digunakan adalah jenis
Microhardness Tester FM-800 (Future Tech, Japan).
13.Volume perendaman obat kumur cengkeh adalah 5 ml/sampel. 14.Volume perendaman jus jeruk kemasan adalah 5 ml/sampel.
15.Volume perendaman aquabidest selama 24 jam adalah 5 ml/sampel.
16.Volume pencampuran saliva buatan ke dalam obat kumur cengkeh 3 ml/sampel.
17.Suhu ruangan adalah suhu ruangan pada saat dilakukan perendaman jus jeruk kemasan, perendaman obat kumur cengkeh, dan pengukuran kekerasan permukaan enamel gigi.
3.7 Alat dan Bahan Penelitian 3.7.1Alat-alat Penelitian
1. Micro Vickers Hardness Tester
2. pH digital Hanna meter
3. Fisher Scientific 630D Isotemp Incubator
4. Rotary grinder
5. Air blower (pus-pus)
6. Kertas tisu 7. Spuit 10 ml
8. Kertas pasir no.1200 9. Cetakan resin
10. Nail varnish
11.Spidol hitam
13. Beaker glass
14.Masker 15.Sarung tangan 16.Pinset
17.Spiritus 18. Stopwatch
19.Mikromotor 20. Carborundum disc
3.7.2Bahan-bahan Penelitian
1. Gigi premolar pertama maksila permanen 2. Jus jeruk kemasan
3. Aquabidest 4. Saliva buatan
5. Obat kumur cengkeh sediaan 6. Self-curing Resin
7. Wax
3.8 Prosedur Penelitian 3.8.1Persiapan Sampel
1. Gigi dibilas dengan aquabidest, lakukan pengulangan sebanyak 2 kali hingga permukaan gigi bersih.
2. Ambil gigi satu per satu dengan pinset, lalu keringkan dengan pus-pus. 3. Gigi dipotong menjadi 2 bagian pada batas cementoenamel junction, yaitu bagian antara mahkota dan akar menggunakan mikromotor dan carborundum disc.
4. Beri tanda berupa garis dari central developmental groove ke arah mesial maupun distal sebagai batas pelapisan wax.
5. Permukaan mahkota gigi yang akan tertanam resin dilapisi dengan nail
varnish pada bagian cementoenamel junction ke arah palatal, sedangkan pada bagian cementoenamel junction ke arah bukal dilapisi dengan wax. (Gambar 7A&7B).
6. Bagian mahkota sampel gigi yang tidak tertutupi wax kemudian ditanam dalam self curing resin sehingga gigi stabil pada basis resin, sedangkan bagian yang tertutupi wax tidak ditanam dalam self curing resin (Gambar 7C & 7D)
7. Permukaan bukal gigi diratakan menggunakan rotary grinder dengan kertas pasir no. 1200, dengan ketentuan enamel yang terbuang tidak sampai 100μm.
8. Permukaan gigi dicuci dengan aquabidest dan dikeringkan dengan air
blower (pus-pus).
3.8.2 Pengukuran Kekerasan Awal Enamel Gigi
1. Sampel gigi dijepit dengan permukaan bukal menghadap ke atas kemudian dijepit dengan alat penjepit pada meja Micro Vickers Hardness Tester.
2. Tentukan beban dan waktu indentasi yang digunakan yaitu sebesar 0,1 HV (100 gram) selama 15 detik.
3. Sampel diatur supaya tepat di tengah lensa objektif dan difokuskan dengan cara memutar pegangan yang ada pada kanan alat searah jarum jam.
4. Setelah pada lensa okuler terlihat gambar dalam keadaan fokus, sampel dipindahkan dengan menggeser ke arah kanan sehingga tepat berada di bawah
diamond penetrator, kemudian tombol penetrator ditekan.
5. Diamond penetrator turun yang ditandai dengan menyalanya lampu hijau.
6. Setelah 15 detik, diamond penetrator akan naik lalu ditunggu sampai lampu padam.
7. Sampel digeser kembali ke tempat lensa okuler dan difokuskan lagi, sehingga akan terlihat gambar belah ketupat yang merupakan bekas penekanan.
8. Panjang diagonal diukur dengan mikrometer yang ada di lensa okuler dan didapati kekerasan enamel gigi.
9. Setiap sampel dilakukan pengukuran kekerasan sebanyak 3 kali lalu diambil rata-ratanya yang merupakan kekerasan permukaan sampel.
Gambar 8. Microvickers
3.8.3Perendaman Jus Jeruk Kemasan dan Pembagian Kelompok
1. Pengukuran pH jus jeruk kemasan pada suhu ruang dengan pH digital
Hanna Meter.
2. Setiap sampel direndam dalam jus jeruk kemasan 5 ml selama 5 menit. 3. Pencucian sampel dengan aquabidest dan dikeringkan dengan tisu dan air
blower (pus-pus).
4. Pengukuran kekerasan setelah direndam dalam jus jeruk kemasan. Setiap sampel dilakukan pengukuran kekerasan sebanyak 3 kali lalu diambil rata-ratanya yang merupakan kekerasan permukaan sampel.
5. Pembagian sampel dalam 8 kelompok besar secara random dan tiap kelompok terdiri dari 4 sampel dengan perlakuan A1, A2, A3, A4, B1, B2, B3, dan B4.
3.8.4Perendaman Obat Kumur Cengkeh
1. Pengukuran pH obat kumur cengkeh dan obat kumur cengkeh yang ditambah saliva buatan pada suhu ruang dengan pH digital Hanna Meter.
2. Kelompok A direndam dalam obat kumur cengkeh 5 ml dengan waktu berbeda untuk setiap kelompok (A1= 30 detik, A2= 1 menit, A3= 2 menit, dan A4= 4 menit)
3. Kelompok B direndam dalam obat kumur cengkeh 5 ml yang ditambah saliva buatan 3 ml dengan waktu berbeda untuk setiap kelompok (B1= 30 detik, B2= 1 menit, B3= 2 menit, dan B4= 4 menit)
4. Pencucian sampel dengan aquabidest dan dikeringkan dengan tisu dan air
blower (pus-pus).
5. Setiap sampel direndam dalam 5 ml aquabidest selama 24 jam di dalam inkubator 37°C.
7. Pengukuran kekerasan setelah direndam dalam obat kumur cengkeh selama 1 minggu. Setiap sampel dilakukan pengukuran kekerasan sebanyak 3 kali lalu diambil rata-ratanya yang merupakan kekerasan permukaan sampel.
Gambar 9. Cara kerja microvickers
hardness tester.53
3.9 Pengolahan dan Analisis Data
Data dianalisis secara statistik dengan SPSS v.20 menggunakan analisis: a. Uji analisis T Berpasangan untuk melihat perubahan pada setiap kelompok pada saat sebelum dan setelah perendaman obat kumur cengkeh pada sampel.
BAB 4
HASIL PENELITIAN
Penelitian mengenai pengaruh obat kumur cengkeh terhadap nilai kekerasan enamel setelah perendaman larutan asam telah dilakukan dengan pengujian kekerasan enamel pada 32 gigi premolar pertama maksila yang dibagi secara random menjadi 8 kelompok perlakuan. Kelompok A1, A2, A3, dan A4 direndam dengan obat kumur cengkeh dengan waktu perendaman masing-masing kelompok 30 detik, 1 menit, 2 menit, dan 4 menit dan kelompok B1, B2, B3, dan B4 direndam dengan obat kumur cengkeh yang ditambah saliva buatan dengan waktu perendaman masing-masing kelompok 30 detik, 1 menit, 2 menit, dan 4 menit. Penelitian dilakukan selama 1 minggu. Sampel merupakan gigi yang telah diekstraksi untuk keperluan ortodonti yang diperoleh dari Puskesmas maupun praktik dokter gigi di sekitar Kotamadya Medan. Sampel dipilih berdasarkan kriteria inklusi dan eksklusi. Seluruh sampel direndam dalam jus jeruk kemasan dengan pH 3,6 sebelum direndam dalam obat kumur cengkeh. Masing-masing kelompok perlakuan dilakukan pengujian kekerasan enamel awal, setelah perendaman jus jeruk kemasan, dan setelah perendaman obat kumur cengkeh dengan menggunakan Microvickers hardness tester FM-800 (Future
Tech, Japan) dan angka yang dihasilkan adalah dalam satuan VHN (Vickers Hardness Number).
Tabel 2. Nilai rerata kekerasan permukaan enamel awal, setelah perendaman jus jeruk kemasan, dan setelah perendaman obat kumur cengkeh 30 detik, 1 menit, 2 menit, dan 4 menit.
Kelompok
n
Nilai kekerasan permukaan enamel (VHN)
Awal Jus Jeruk
Kemasan
Obat Kumur Cengkeh A1 (Obat kumur cengkeh
30 detik) 4 405,19±14,24 343,32±31,24 283,51±30,65
A2 (Obat kumur cengkeh
1 menit) 4 374,94±37,81 332,68±40,41 270,77±42,48
A3 (Obat kumur cengkeh
2 menit) 4 411,67±16,15 354,68±7,12 263,97±26,10
A4 (Obat kumur cengkeh
4 menit) 4 385,04±10,18 353,13±17,68 256,10±41,00
B1 (Obat kumur cengkeh
+ saliva buatan 30 detik) 4 381,08±16,49 343,53±9,66 400,07±3,00 B2 (Obat kumur cengkeh
+ saliva buatan 1 menit) 4 377,68±12,10 333,42±12,92 385,26±7,58 B3 (Obat kumur cengkeh
+ saliva buatan 2 menit) 4 390,11±33,04 351,55±34,62 401,20±25,67 B4 (Obat kumur cengkeh
+ saliva buatan 4 menit) 4 393,31±21,13 347,77±22,50 398,24±13,70
Hasil uji T berpasangan pada kelompok perendaman obat kumur cengkeh memperlihatkan penurunan kekerasan permukaan enamel yang signifikan (p<0,05) pada semua kelompok waktu (Tabel 3).
Tabel 3. Hasil uji T berpasangan penurunan nilai kekerasan permukaan enamel dari perendaman jus jeruk kemasan dengan perendaman obat kumur cengkeh.
*terdapat perbedaan signifikan pada p<0,05 Kelompok
waktu
Hasil uji T berpasangan pada kelompok obat kumur cengkeh yang ditambah saliva buatan memperlihatkan peningkatan kekerasan permukaan enamel yang signifikan (p<0,05) pada semua kelompok waktu (Tabel 4).
Tabel 4. Hasil uji T berpasangan peningkatan nilai kekerasan permukaan enamel dari perendaman jus jeruk kemasan dengan perendaman obat kumur cengkeh yang ditambah saliva buatan.
*terdapat perbedaan signifikan pada p<0,05
Tabel 5 memperlihatkan perbandingan nilai rerata kekerasan permukaan enamel yang direndam dalam obat kumur cengkeh dengan penambahan saliva buatan maupun tanpa penambahan saliva buatan yang diuji dengan uji statistik One Way ANOVA. Dalam melakukan perbandingan antar kelompok, digunakan data selisih nilai rerata kekerasan permukaan enamel setelah perendaman obat kumur cengkeh dengan nilai setelah perendaman jus jeruk kemasan (∆ VHN). Hasil uji statistik One
Way ANOVA yang membandingkan selisih nilai rerata kekerasan permukaan enamel
setelah perendaman obat kumur cengkeh, dengan dan tanpa ditambah saliva buatan menunjukkan perbedaan yang signifikan (p<0,05) pada semua kelompok waktu.
Kelompok waktu
Nilai kekerasan permukaan enamel (VHN)
Peningkat-Tabel 5. Hasil uji statistik One Way ANOVA perbedaan rerata kekerasan permukaan enamel setelah direndam dalam obat kumur cengkeh dengan penambahan saliva buatan maupun tanpa penambahan saliva buatan.
*terdapat perbedaan signifikan pada p<0,05.
Hasil uji Post Hoc (Tabel 6) yang membandingkan selisih kekerasan permukaan enamel setelah perendaman obat kumur cengkeh dengan dan tanpa saliva buatan menunjukkan perbedaan yang signifikan (p<0,05) pada setiap kelompok waktu. Dengan demikian maka hipotesa diterima (Hα diterima).
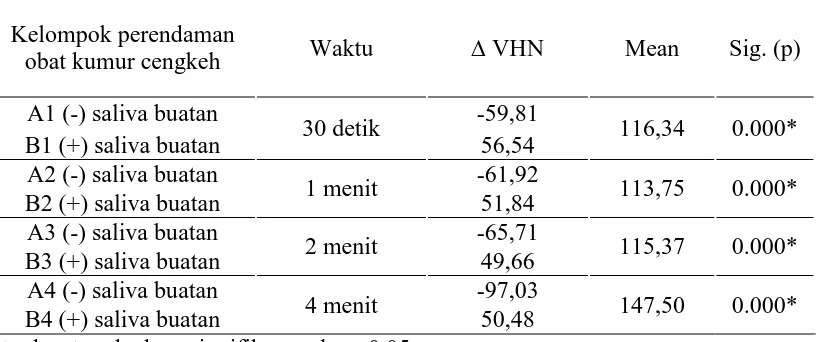
Tabel 6. Hasil uji statistik Post Hoc perbedaan rerata kekerasan permukaan enamel yang direndam dalam obat kumur cengkeh dengan penambahan saliva buatan maupun tanpa penambahan saliva buatan.
Kelompok perendaman
*terdapat perbedaan signifikan pada p<0,05.
Kelompok ∆ VHN Sig.
(p)
A1 (Perendaman obat kumur cengkeh 30 detik) -59,81
0.000*
A2 (Perendaman obat kumur cengkeh 1 menit) -61,92
A3 (Perendaman obat kumur cengkeh 2 menit) -65,71
A4 (Perendaman obat kumur cengkeh 4 menit) -97,03
BAB 5 PEMBAHASAN
Penelitian ini adalah penelitian eksperimental laboratoris mengenai pengaruh obat kumur cengkeh terhadap nilai kekerasan permukaan enamel setelah perendaman larutan asam yang diuji nilai kekerasannya dengan menggunakan alat Micro Vickers
Hardness Tester FM-800. Sebelum diukur nilai kekerasannya, sampel ditanam
terlebih dahulu dalam self-curing resin agar sampel tetap stabil saat dilakukan pengukuran. Dalam proses penanaman ke dalam resin, bagian mahkota sampel dilapisi terlebih dahulu dengan wax pada bagian central developmental groove ke arah bukal agar bagian bukal gigi terbebas dari resin saat proses penanaman sehingga tidak mempengaruhi hasil pengukuran kekerasan enamel pada bagian bukal.
Enamel merupakan lapisan terluar gigi dan merupakan bagian tubuh yang paling keras karena mengandung zat anorganik sebanyak 95-98%. Komponen mineral utama pada enamel adalah kalsium dan fosfat yang tersusun dalam hidroksiapatit (Ca10(PO4)6(OH)2). Meskipun enamel merupakan struktur yang sangat keras, namun enamel rentan terhadap demineralisasi. Demineralisasi dapat terjadi apabila enamel berada dalam suatu lingkungan pH di bawah 5,5. pH yang rendah akan meningkatkan konsentrasi ion hidrogen dan ion ini akan merusak hidroksiapatit enamel gigi. 3,8,9
dengan yang diilaporkan oleh Mettu S dkk di India (2015) dimana nilai kekerasan permukaan enamel yang diukur berkisar antara 389,04 VHN sampai 400,98 VHN.34
Cengkeh merupakan tanaman herbal yang memiliki banyak manfaat dalam bidang kesehatan karena mempunyai efek antivirus, antiseptik, analgesik, dan antifungal alami. Dalam cengkeh terkandung mineral seperti kalsium, fosfor, tembaga, zat besi, magnesium, dan mangan, dimana mineral kalsium dan fosfor merupakan mineral yang penting dalam proses remineralisasi gigi.3-5,7-9,17-21
masih membawa mineral (dalam hal ini kalsium dan fosfor) yang terdapat pada cengkeh sehingga remineralisasi dapat terjadi10 sedangkan pada penelitian ini ekstrak cengkeh yang digunakan dalam obat kumur adalah dalam bentuk minyak (minyak cengkeh yang mengandung eugenol). Secara teori, pembuatan minyak cengkeh menggunakan proses destilasi. Destilasi merupakan pemisahan 2 komponen/lebih berdasarkan perbedaan titik didih senyawanya, dimana zat yang memiliki titik didih lebih rendah akan menguap lebih dahulu, uap yang menguap kemudian akan didinginkan lalu mengembun dan menetes sebagai zat murni (ekstrak).54 Proses destilasi dalam pembuatan minyak cengkeh yang terkandung pada obat kumur ini menyebabkan eugenol pada cengkeh menguap dahulu (titik didih eugenol 253°C) karena mempunyai titik didih yang lebih rendah dari kalsium (1484°C) dan fosfor (280°C) sedangkan kalsium dan fosfor tidak turut menguap karena mempunyai titik didih yang berbeda.55-57 Proses ini menyebabkan kandungan kalsium dan fosfor pada cengkeh sangat sedikit atau bahkan tidak terkandung pada minyak cengkeh.4,6,7,11 Oleh karena itu peneliti menyarankan penelitian lanjutan mengenai penggunaan ekstrak cengkeh dalam bentuk ekstrak lain selain dalam bentuk minyak esensial dalam obat kumur.
Hasil penelitian juga menunjukkan bahwa semakin lama perendaman dalam obat kumur cengkeh, maka semakin besar pula penurunan kekerasan permukaan enamel (Tabel 4). Hal ini sesuai dengan penelitian Arief EP di Indonesia (2007) yang menyatakan kontak yang lama antara enamel dan larutan asam di sekitarnya akan mengakibatkan demineralisasi terjadi terus menerus, menyebabkan kehilangan sebagian dari prisma enamel, sehingga kekerasan permukaan enamel gigi akan semakin berkurang3,58 sehingga peneliti berpendapat bahwa lebih baik berkumur selama 30 detik sesuai anjuran pabrik agar efek demineralisasi lebih lanjut dapat dihindari.
digunakan oleh Marya CM dkk karena konsentrasi minyak cengkeh pada obat kumur ini lebih tinggi dibandingkan penelitian tersebut. Dengan adanya kandungan sodium benzoate sebagai pengawet dalam obat kumur cengkeh ini juga dapat menjadi salah satu alasan obat kumur cengkeh ini dibuat dengan pH rendah. Sodium benzoate berfungsi sebagai antibakteri dan pengawet. Diketahui sodium benzoate mempunyai efek pengawet yang maksimal seiring dengan menurunnya pH suatu larutan42-45 sehingga kemungkinan pabrik mengatur pH obat kumur cengkeh ini menjadi asam agar efek sodium benzoate sebagai pengawet dapat bekerja maksimal. Komposisi lain selain minyak cengkeh dan sodium benzoate yang terkandung dalam obat kumur cengkeh dalam penelitian ini diperuntukkan untuk antibakteri dan antimikroba 40,41,46-49
sehingga peneliti berasumsi bahwa obat kumur cengkeh ini dimaksimalkan untuk antibakteri saja namun tidak sebagai agen remineralisasi.
BAB 6
KESIMPULAN DAN SARAN
6.1 Kesimpulan
1. Terdapat penurunan kekerasan permukaan enamel yang signifikan (p<0,05)
pada gigi premolar pertama maksila permanen yang telah direndam obat kumur cengkeh setelah perendaman jus jeruk kemasan.
2. Terdapat peningkatan kekerasan permukaan enamel yang signifikan (p<0,05) pada gigi premolar pertama maksila permanen yang direndam obat kumur cengkeh yang ditambah saliva buatan setelah perendaman jus jeruk kemasan.
3. Terdapat perbedaan kekerasan permukaan enamel gigi yang telah direndam obat kumur cengkeh tanpa saliva buatan dengan obat kumur cengkeh yang ditambah saliva buatan.
6.2 Saran
1. Penelitian lanjutan mengenai penggunaan ekstrak cengkeh tidak dalam bentuk minyak esensial agar dapat memaksimalkan efeknya dalam remineralisasi enamel disamping efeknya sebagai antibakteri.
BAB 2
TINJAUAN PUSTAKA
2.1 Cengkeh
Cengkeh (Syzygium Aromaticum) adalah tanaman asli Indonesia yang berasal dari Maluku. Tanaman perkebunan ini menyebar di Indonesia sejak tahun 1870 dan kini sudah banyak dibudidayakan untuk diambil bunga dan minyaknya. Tanaman cengkeh dapat tumbuh dengan baik di daerah beriklim tropis.2 Indonesia merupakan negara penghasil cengkeh terbesar di dunia dengan kapasitas produksi sebesar 92.133 ton/tahun, disusul Madagaskar dan Tanzania dengan total produksi 1/6 total produksi cengkeh Indonesia yaitu sekitar 15.000 ton/tahun.3
Cengkeh adalah jenis tumbuhan perdu yang memiliki batang pohon yang besar dan berkayu keras. Pohon cengkeh dapat tumbuh hingga mencapai ketinggian 20 meter dan umumnya pohon cengkeh membutuhkan waktu sekitar 5 tahun untuk tumbuh dewasa dan siap dipanen. Daun cengkeh berwarna hijau berukuran 3-6 inci berbentuk bulat telur memanjang dengan bagian ujung dan pangkalnya menyudut. Bunga cengkeh yang muda berwarna keungu-unguan, kemudian berubah menjadi kuning kehijauan dan berwarna merah muda apabila sudah tua, sedangkan bunga cengkeh kering akan berwarna coklat kehitaman.4,5
2.1.1 Taksonomi Cengkeh
Berdasarkan ilmu taksonomi, cengkeh diklasifikasikan menjadi:4
• Kingdom : Plantae
• Subkingdom : Tracheobionta
• Filum : Angiosperma
• Kelas : Dicotyledonae
• Ordo : Myrtales
• Famili : Myrtaceae
• Genus : Syzygium
• Spesies : Syzygium aromaticum (L.)
2.1.2 Kandungan Cengkeh
United States Department of Agriculture (USDA) melaporkan bahwa dalam
100 gram cengkeh terkandung beberapa mineral seperti kalsium sebesar 44 mg, 0,231 mg tembaga, 1,28 mg zat besi, 60 mg magnesium, 0,256 mg mangan, dan 90 mg fosfor.4
Eugenol merupakan senyawa yang berperan dalam memberikan aroma khas menyegarkan dan pedas pada cengkeh, dan mempunyai efek analgesik, antiinflamasi, antimikroba, antiviral, antifungal, antiseptik, sehingga senyawa ini banyak dimanfaatkan dalam industri farmasi.6,7,17 Senyawa eugenol merupakan komponen utama yang terkandung dalam minyak cengkeh, dengan kandungan dapat mencapai 72-90%, kandungan lain pada minyak cengkeh antara lain:4,6,7,10
a. Asetil eugenol yang berfungsi sebagai antioksidan dan aktivitas antiplatelet; beta-kariofilen, asam krategolik, dan vanillin yang berfungsi sebagai agen antiinflamasi, antioksidan, dan antitumor.
b. Tannin seperti asam galatanat dan metil salisilat yang dapat meningkatkan ketahanan terhadap asam pada enamel gigi.
d. Triterpenoid seperti asam oleanolik yang berfungsi sebagai antimikroba dan antikanker.
2.1.3 Manfaat Cengkeh
Cengkeh merupakan tanaman herbal yang mempunyai banyak manfaat, dengan aroma khasnya yang harum dan sedikit pedas, cengkeh dapat digunakan untuk membuat lemari dan laci-laci menjadi harum. Kandungan kimia pada minyaknya yang sangat bermanfaat membuatnya banyak digunakan sebagai bumbu masakan dan obat berbagai masalah kesehatan sejak ribuan tahun yang lalu.4,5
Cengkeh mempunyai peran terapeutik dalam kondisi berikut:4,5-7,17-20
a. Anti-septik: minyak cengkeh dapat digunakan untuk mengurangi infeksi, luka, dan sakit akibat gigitan serangga.
b. Anti-fungal: cengkeh bermanfaat dalam mengurangi infeksi jamur seperti
athlete’s foot. Ali dkk di Dubai (2009) juga mengemukakan bahwa kandungan
eugenol yang ada pada cengkeh terbukti dapat menghambat perkembangan jamur
Candida albicans.
c. Anti-bakteria: minyak cengkeh dapat secara efektif membunuh bakteri infeksi pada kasus keracunan makanan. Chaiya A dkk di Thailand (2013) mengemukakan bahwa kandungan eugenol dalam obat kumur cengkeh dapat menghambat tumbuhnya bakteri Streptococcus mutans dan Streptococcus viridans yang dapat menyebabkan terjadinya plak gigi.
d. Anti-kasinogenik: asam oleanolik yang merupakan salah satu komponen dari etil asetat dalam ekstrak cengkeh berperan dalam aktivitas antitumor dengan menginduksi proses apoptosis.
e. Aktivitas antiplatelet: cengkeh dapat melancarkan peredaran darah karena kandungan eugenol dan asetil eugenol yang ada pada cengkeh dapat menghambat agregasi platelet.
g. Hipertensi: mengunyah cengkeh secara teratur setidaknya selama 6 minggu atau lebih dapat membantu mengurangi hipertensi.
h. Analgesik: serbuk cengkeh yang diaplikasikan pada gusi gigi yang sakit dapat mengurangi rasa sakit, selain itu dapat juga mengurangi sakit pada sakit telinga dan sakit kepala, dan sakit gigi.
i. Cengkeh dapat membantu dalam meredakan masalah pencernaan seperti muntah-muntah, diare, dan perut kembung.
j. Antioksidan: minyak cengkeh dapat berfungsi sebagai antioksidan yang kuat. USDA (United States Department of Agriculture) menetapkan skala yang bernama ORAC (Oxygen Radical Absorption Capacity), dimana semakin tinggi skor ORAC, semakin mampu bahan tersebut merusak radikal bebas, dan minyak cengkeh mempunyai skor ORAC tertinggi yaitu 10.786.875 disusul minyak thyme dengan skor 159.500, sehingga cengkeh dikenal sebagai sang juara dari seluruh bahan antioksidan. Selain dalam bidang kesehatan, cengkeh dapat juga dimanfaatkan untuk mengusir nyamuk dan ngengat. Dalam bidang industri pabrik, cengkeh digunakan sebagai bahan dalam pasta gigi, sabun, kosmetik, obat kumur, parfum, dan rokok. Cengkeh juga banyak dimanfaatkan sebagai bahan baku obat gosok balsam untuk mengurangi rasa sakit karena rematik, dan produk aroma terapi (Jirovets, 2010).17
2.1.4 Manfaat Cengkeh Terhadap Kekerasan Enamel
menunjukkan bahwa komponen mayor dalam cengkeh seperti eugenol dan asetil eugenol dalam minyak cengkeh 0,05% dapat menghambat dekalsifikasi enamel oleh jus apel dan menyebabkan terjadinya proses remineralisasi .11
2.2 Enamel
Gigi tersusun atas jaringan keras yang terdiri dari enamel, dentin, dan sementum. Enamel adalah lapisan terluar gigi yang menutupi seluruh mahkota gigi dan dibentuk oleh sel-sel yang disebut ameloblast. Enamel berwarna putih, namun enamel memiliki sifat translusen sehingga memungkinkan warna dentin yang sedikit kekuningan terlihat.22,23
Enamel terdiri atas 96% materi anorganik berupa mineral, 3% air, dan 1% materi organik. Komponen mineral utama pada enamel adalah kalsium dan fosfat yang tersusun dalam hidroksiapatit (Ca10(PO4)6(OH)2), sedangkan komponen organiknya adalah rod sheath dan protein-protein enamel.9,22,24 Enamel mengandung dua jenis protein yaitu amelogenin dan enamelin yang akan membantu dalam pembentukan kristal dengan mengikat kalsium dengan komponen hidroksiapatit yang lain.23
Kandungan mineral yang tinggi membuat enamel mempunyai sifat yang keras, bahkan merupakan jaringan yang paling keras pada tubuh manusia. Walaupun enamel merupakan struktur yang sangat keras, namun enamel bersifat semi-permeabel sehingga memungkinkan ion dan beberapa jenis cairan, bakteri, dan produk bakteri dalam rongga mulut berdifusi ke dalam enamel.21 Enamel tidak mempunyai sel, pembuluh darah, dan saraf sehingga tidak dapat memperbaharui dirinya jika rusak atau patah, tetapi dapat mengalami mineralisasi apabila mengalami kehilangan substansi enamel yang ringan.24
Secara mikroskopis, struktur dasar enamel adalah susunan prisma enamel atau
enamel rod. Prisma enamel tersusun pada enamel dengan dasarnya tegak lurus pada
yang keempat. Pada potongan melintang, prisma enamel tampak seperti lubang kunci dengan kepala dan ekor, sedangkan pada potongan memanjang tampak seperti persegi panjang. Prisma enamel merupakan massa kristal-kristal hidroksiapatit pada pola yang teroganisir.21,24
2.2.1Demineralisasi dan Remineralisasi
Demineralisasi enamel adalah lepasnya sebagian maupun seluruh mineral dalam hidroksiapatit enamel karena larut dalam asam.Kondisi demineralisasi enamel terjadi bila pH larutan disekeliling permukaan enamel lebih rendah dari 5,5, dimana dilaporkan bahwa pH kritis enamel gigi berada diantara 5,2 dan 5,5. Semakin rendah pH saliva, maka akan menyebabkan ion hidrogen semakin meningkat sehingga dapat merusak ikatan hidroksiapatit (Ca10(PO4)6(OH)2) pada enamel gigi. Adapun pengaruh pH terhadap koefisien laju reaksi menunjukkan, bahwa semakin kecil atau semakin asam media, maka semakin tinggi laju reaksi pelepasan ion kalsium dari enamel gigi.8,9,21
Demineralisasi dapat dibedakan menjadi demineralisasi yang disebabkan oleh karies dan demineralisasi non karies yang terdiri atas atrisi, abrasi, dan erosi.
Demineralisasi oleh karies disebabkan oleh asam yang berasal dari fermentasi karbohidrat oleh bakteri. Sedangkan demineralisasi non karies seperti pada erosi terjadi karena asam yang berasal dari makanan dan minuman, obat-obatan, asam lambung dan dari lingkungan pekerjaan yang berkontak langsung dengan gigi tanpa melibatkan aktifitas bakteri. Pada tahap awal, erosi kurang disadari oleh penderita sebab tidak terjadi perubahan warna dan bukan berbentuk lubang. Gejala awal erosi adalah suatu bercak putih yang secara mikroanatomi terlihat bulat, licin, dan mengkilap. Pada tahap lanjut, semakin banyak enamel hilang, permukaan gigi semakin licin dan mengkilap, serta permukaan yang membulat pada elemen gigi menjadi rata.25
Pada saat asam berkontak dengan enamel maka ion hidrogen pada larutan asam mulai melarutkan kristal enamel. Mula-mula, daerah selubung prisma (prisma sheath) melarut dan berlanjut ke inti prisma, membentuk permukaan dengan gambaran seperti sarang lebah. Kemudian asam yang tidak berionisasi (anion) berdifusi ke dalam daerah interprismatik pada enamel gigi dan melarutkan lebih lanjut mineral pada daerah bagian bawah permukaan enamel. Struktur prisma enamel menjadi irreguler diikuti dengan derajat hilangnya enamel yang bervariasi dari satu tempat ketempat lain.14
Reaksi kimia pelepasan ion kalsium dari enamel gigi dalam suasana asam ditunjukkan dengan persamaan reaksi sebagai berikut:26,27
Ca10(PO4)6(OH)2 10Ca2+ + 6PO43- + 2OH-
Padat Larut
Remineralisasi merupakan proses dimana ion mineral kalsium dan fosfat kembali membentuk kristal hidroksiapatit pada enamel. Kunci utama dalam proses remineralisasi adalah dengan mengembalikan pH rongga mulut ke tingkat yang lebih tinggi daripada pH kritis enamel gigi dan terdapat ion Ca2+ dan PO43- yang cukup pada rongga mulut.8,21,28
Remineralisasi dapat terjadi jika terdapat sebagian kristal yang terdemineralisasi sehingga kristal yang terdemineralisasi tersebut dapat kembali ke ukuran semula ketika terekspos dengan cairan yang mengandung ion Ca2+ dan PO43-. Ion kalsium dan fosfat akan menghambat proses penguraian hidroksiapatit dan menyebabkan terjadinya rebuilding atau pembangunan kembali sebagian kristal hidroksiapatit yang larut. Mikroporositas yang disebakan oleh karena minuman asam mengakibatkan enamel gigi memiliki energi tegangan permukaan yang tinggi sehingga memungkinkan mineral Ca2+ dan PO43- masuk ke dalam mikroporositas tersebut. Mikroporositas enamel yang terjadi akan terisi Ca2+ dan PO43- karena mikroporositas enamel hanya akan diisi dengan ion mineral yang memiliki jari-jari ionik yang sama dengan jari-jari ionik mineral yang hilang. Pergantian mineral pada mikroporositas enamel akan stabil hanya bila ion Ca2+ dan PO43- yang larut juga tergantikan dengan kedua ion tersebut.8,21
Remineralisasi enamel tidak selalu dapat terjadi, dalam prosesnya selalu dipengaruhi oleh banyak hal, seperti waktu perendaman, supersaturasi larutan terhadap gigi, laju endapan reaktan dan pH larutan. Jika faktor tersebut tidak memenuhi maka remineralisai enamel akan terhambat. Proses remineralisasi adalah proses penting yang memiliki pengaruh secara signifikan pada kekerasan dan kekuatan gigi.8,21,28,29
2.2.2 Kekerasan Enamel
permukaan luar enamel menuju ke dentin. Hal ini disebabkan kandungan mineral anorganik pada dentin dan sementum lebih rendah dari enamel.15,23
Penurunan kekerasan permukaan gigi membuat gigi lebih rentan terhadap erosi dan kehilangan mineral gigi.30 Kekerasan permukaan gigi dipengaruhi oleh beberapa faktor, yaitu tingkat keasaman, suhu, dan mineral pada makanan atau minuman: a. Mineral yang ada di dalam makanan atau minuman
Benjakul dkk di Thailand (2011) menunjukkan bahwa Kapi yang ditambahkan pada makanan sejenis kari yang berasal dari Thailand (Kangsom) dapat mengurangi erosi pada enamel. Kapi adalah udang yang telah difermentasi hingga berbentuk pasta yang mengandung kalsium cukup tinggi. Penelitian ini membuktikan bahwa mineral yang terkandung dalam makanan dan minuman dapat mempengaruhi kekerasan enamel.31
b. Tingkat keasaman makanan atau minuman
Semakin asam makanan dan minuman akan semakin berpotensi
mengakibatkan erosi gigi. Tahmassebi dkk di Inggris (2006) menunjukkan bahwa Makanan dan minuman yang memiliki pH di bawah pH kritis (5,5) dengan kuantitas asam yang tinggi dapat menyebabkan erosi gigi yang lebih progresif.30 Pernyataan ini didukung oleh Seow WK dan Thong KM di Australia (2005) yang menunjukkan bahwa minuman ringan, minuman olahraga, jus buah, serta minuman beralkohol dengan pH asam (<5,5) dapat menimbulkan erosi dan penurunan kekerasan enamel yang signifikan.32
c. Suhu makanan atau minuman
Machado C dkk di Amerika (2008) menunjukkan bahwa semakin tinggi temperatur jus jeruk dan minuman ringan, semakin besar efeknya pada erosi enamel.13
2.2.3Ketebalan Enamel
edge) ketebalan enamel sebesar 2 mm, gigi premolar (cusp) sebesar 2,3-2,5 mm, dan
gigi molar (cusp) sebesar 2,5-3 mm. Gigi premolar satu permanen memiliki ketebalan enamel sebesar 0,904 mm (dari puncak cusp lingual), 0,625 mm (dari puncak cusp
buccal), 0,95 mm (dari lingual occlusal), dan 0,68 mm (dari buccal occlusal).
Schwartz GT (2000) mendeskripsikan ketebalan enamel pada gigi premolar, molar 1, molar 2, dan molar 3 melalui tabel berikut.33
Tabel 1. Nilai rerata ketebalan enamel manusia pada rahang atas dan rahang bawah.33
Daerah pengukuran gigi
Rerata ketebalan enamel gigi (mm)
Molar 1 Molar 2 Molar 3 Premolar
Lingual cusp tips 1,77 1,80 1,81 0,90
Buccal cusp tips 1,98 2,05 2,26 0,62
Lingual occlusal 1,53 1,55 1,59 0,95
Buccal occlusal 1,91 1,81 1,96 0,68
2.2.4Alat Penguji Kekerasan Enamel
Kekerasan enamel umumnya diukur dengan menggunakan alat pengukur kekerasan mikro yaitu Knoop Hardness Tester dan Vickers Hardness Tester. Gutierrez-salazar MP dan Reyes-Gasga J melaporkan kekerasan enamel yang diukur berkisar 270-360 VHN (Vickers Hardness Number), Chuenarrom C dkk melaporkan kekerasan enamel berkisar dari 316-328 VHN, Mettu S dkk melaporkan kekerasan enamel berkisar 395.01±5.97 VHN, sedangkan Cirano FR dkk melaporkan sebesar 398,41±24,74 VHN. Variasi kekerasan enamel dapat terjadi karena faktor gambaran histologi gigi, komposisi kimiawi yang terkandung pada gigi, dan persiapan sampel.15,16,29,34
a. Metode Knoop
1000 gram. Indentor diamond Knoop menghasilkan indentasi kecil yang berbentuk belah ketupat yang elongasi dimana ratio antara diagonal yang panjang dibanding diagonal pendek adalah 7:1, yang diukur adalah panjang diagonal terbesar. Kemudian, daerah yang terjejas dibagi dengan beban yang diberikan sehingga menghasilkan Knoop Hardness Number (KHN).35,36
Gambar 3. Bentuk indentasi alat kekerasan Knoop36
b. Metode Vickers
Vickers hardness tester adalah salah satu alat yang digunakan untuk mengukur
nilai kekerasan enamel. Pengujian kekerasan Vickers dilakukan dengan membuat indentasi pada permukaan obyek yang diuji dengan indentor diamond yang berbentuk piramida dengan dasar persegi dan sudut 136o antara satu permukaan dengan permukaan yang berlawanan seperti di gambar 4. Beban yang diinginkan ditekan pada permukaan obyek selama 10 sampai 15 detik. Setelah itu, panjang kedua garis diagonal pada lekukan yang dihasilkan diukur di bawah mikroskop untuk mendapatkan nilai rata-ratanya.35,36 Kemudian, nilai kekerasan Vickers (HV) dapat dihitung dengan rumus:29
HV = 1,854 x F Petunjuk:
F= beban yang diterapkan
Pengujian kekerasan enamel menggunakan metode Vickers lebih banyak digunakan dibandingkan metode Knoop karena bentuk persegi yang dihasilkan oleh indentor Vickers lebih mudah diukur dan hasil juga lebih akurat. Perubahan kecil pada bentuk persegi yang dihasilkan oleh indentor dapat dideteksi dengan mudah, sementara lekukan yang dihasilkan oleh indentor Knoop berbentuk rhomboid sehingga pendeteksian kesalahan sulit dilakukan. Untuk menghindari bias nilai kekerasan sampel, beberapa indentasi harus dilakukan pada setiap sampel dan diambil nilai rata-ratanya.15,29
Gambar 4. Bentuk indentasi alat kekerasan Vickers35
2.3 Gigi Premolar Pertama Maksila Permanen
Gigi premolar pertama maksila permanen erupsi pada usia 10-11 tahun, dengan pembentukan akar yang lengkap pada usia 12-13. Gigi ini tumbuh di sebelah distal gigi kaninus maksila permanen dan merupakan gigi pengganti dari gigi molar pertama maksila sulung.Gigi ini berfungsi untuk membantu pengunyahan makanan.24
Gigi premolar pertama maksila memiliki dua cusp yang tajam, yaitu buccal
cusp dan palatal cusp. Buccal cusp lebih panjang 1 mm daripada palatal cusp.
premolar satu maksila mempunyai dua akar dan dua saluran akar. Pada gigi premolar satu maksila dengan satu radiks, saluran radiksnya tetap dua.24,37
Bukal D M Palatal
Oklusal
Mesial Distal
Gambar 5. Gigi premolar pertama maksila permanen kanan dilihat dari berbagai aspek24
2.4 Obat Kumur
Obat kumur merupakan larutan atau cairan yang digunakan untuk membilas rongga mulut dengan tujuan untuk menyingkirkan plak, menyegarkan mulut, membantu menyembuhkan inflamasi dan mencegah karies gigi. Obat kumur dapat digunakan sebagai tambahan dari pemeliharaan kebersihan mulut seperti sikat gigi dan flossing.38
Obat kumur pada umumnya terdiri dari 3 komponen utama, yaitu:38
a. Bahan aktif yang dipilih untuk meningkatkan kesehatan rongga mulut secara spesifik, seperti antikaries, antimikroba, atau untuk mengurangi plak.
c. Surfaktan untuk menjaga kestabilan struktur zat yang terkandung dalam larutan obat kumur.
Kandungan alkohol pada obat kumur berfungsi sebagai pelarut dan pengawet. Penelitian telah menunjukkan bahwa konsentrasi alkohol yang tinggi (diatas 20%) pada obat kumur dapat berefek pada keratosis, ulserasi mukosa, gingivitis, petechiae, bahkan resiko kanker mulut.38 Beberapa penelitian telah dilakukan untuk memverifikasi kelebihan obat kumur herbal, karena obat kumur herbal mengandung bahan alami yang disebut phytochemicals, bahan ini mempunyai efek antimikrobial dan antiinflamasi.39
Komposisi yang terdapat dalam obat kumur yang digunakan dalam penelitian ini adalah:
a. Air yang berfungsi sebagai pelarut.
b. Xylitol (5%) berfungsi untuk menekan jumlah bakteri patogen rongga mulut.40,41 c. Minyak cengkeh (0,35%) berfungsi sebagai antibakteri alami. Penelitian yang dilakukan oleh Chaiya A dkk di Thailand (2013), Aneja KR dkk di India (2010), dan Ali HS dkk di Dubai (2009) menunjukkan bahwa minyak cengkeh dapat menghambat tumbuhnya bakteri yang dapat menyebabkan terjadinya plak gigi, juga mengurangi bau mulut.18-20
d. Sodium benzoate berfungsi sebagai pengawet dan antibakteri. Sodium benzoate dapat bekerja maksimal pada suasana asam.42-45
e. Minyak mint berfungsi sebagai antibakteri dan antifungal alami. Penelitian yang dilakukan oleh Al-Sum BA et al (2013) di Saudi Arabia dan Sulieman AME et al (2011) di Sudan menunjukkan bahwa minyak mint dapat menghambat pertumbuhan jamur dan bakteri penyebab plak gigi.46,47
f. Minyak peppermint berfungsi sebagai antibakteri. Penelitian yang dilakukan oleh Surjana P dkk di India (2013) dan Singh R dkk di Libya (2011) menunjukkan bahwa minyak peppermint dapat menghambat pertumbuhan bakteri gram negatif dalam rongga mulut.48,49
2.5 Saliva
Saliva merupakan cairan mulut yang kompleks terdiri dari campuran sekresi kelenjar saliva mayor dan minor yang ada dalam rongga mulut. Saliva sebagian besar dihasilkan saat makan yang merupakan reaksi atas rangsangan yang berupa pengecapan dan pengunyahan makanan.50 Aliran saliva dapat menurunkan akumulasi plak pada permukaan gigi, menetralkan suasana asam, dan juga membantu mempertahankan kestabilan sistem buffer dalam rongga mulut.50 Laju alir saliva normal berkisar dari 1-3 ml/menit.51 Keberadaan saliva merupakan faktor penting dalam proses remineralisasi enamel, dimana difusi komponen saliva seperti kalsium dan fosfat dapat memperlambat proses kelarutan enamel dan meningkatkan remineralisasi gigi.50
2.6 Komposisi Saliva
Saliva terdiri dari 94-99,5% air, bahan organik, dan anorganik. Komponen organik dalam saliva yang utama adalah protein-protein seperti α-Amilase, musin, protein kaya prolin, musin, urea dan sialin. Urea dan sialin memegang peranan penting dalam meningkatkan pH biofilm setelah paparan dengan karbohidrat.51
Komponen anorganik saliva antara lain natrium (Na+), kalium (K+), magnesium (Mg2+), klor (Cl-), sulfat (SO42-), bikarbonat (HCO3-), kalsium (Ca2+), dan fosfat (PO4). Kadar kalsium dan fosfat dalam saliva sangat penting untuk remineralisasi enamel karena dapat mengisi kembali kristal hidroksiapatit yang telah terurai pada proses demineralisasi. Ion bikarbonat juga merupakan ion buffer terpenting dalam saliva yang menghasilkan 85% dari kapasitas buffer saliva.51
2.7 Landasan Teori
Enamel gigi yang terpapar dalam suasana asam melewati pH kritis enamel (5,5) akan mengalami demineralisasi. Demineralisasi enamel adalah lepasnya sebagian maupun seluruh mineral dalam hidroksiapatit akibat proses kimia. Semakin rendah pH atau semakin asam media, maka semakin tinggi laju reaksi pelepasan ion kalsium dari enamel gigi. pH saliva yang rendah juga akan menyebabkan ion hidrogen semakin meningkat sehingga dapat merusak ikatan hidroksiapatit (Ca10(PO4)6(OH)2) pada enamel gigi.2,8,9,21,28 Akhir-akhir ini semakin banyak masyarakat mengkonsumsi minuman ringan, salah satunya adalah jus jeruk kemasan. Minuman ringan seperti jus jeruk mempunyai pH <5,5 dan terbukti dapat menyebabkan erosi dan penurunan kekerasan pada enamel.12-14,32
Remineralisasi merupakan proses dimana ion kalsium dan fosfat kembali masuk kedalam kristal hidroksiapatit. Remineralisasi dapat terjadi jika terdapat sebagian kristal yang terdemineralisasi sehingga kristal yang terdemineralisasi tersebut dapat kembali ke ukuran semula ketika terekspos dengan cairan yang mengandung ion kalsium dan fosfat. Ion kalsium dan fosfat akan menghambat proses penguraian hidroksiapatit dan hal ini memungkinkan pembentukan kembali kristal apatit yang telah terpisah.3,8,9 Cengkeh (Syzygium Aromaticum) merupakan tanaman herbal asli Indonesia yang berasal dari Maluku. Cengkeh dilaporkan mempunyai kandungan kalsium dan fosfat, dimana kedua kandungan tersebut dapat berperan dalam meningkatkan kekerasan permukaan enamel.2,4,10 Keberadaan saliva juga merupakan faktor penting dalam proses remineralisasi enamel, dimana difusi komponen anorganik saliva seperti kalsium, fosfat, dan ion bikarbonat juga komponen organik seperti urea dan sialin dapat menurunkan kelarutan enamel dan meningkatkan remineralisasi gigi. Proses remineralisasi merupakan proses penting yang memiliki pengaruh pada kekerasan dan kekuatan gigi.8,21,28,29
alat pengukur kekerasan mikro yaitu Knoop Hardness Tester dan Vickers Hardness
Tester, namun pengukuran kekerasan permukaan enamel dengan metode Vickers
lebih banyak digunakan dibandingkan metode Knoop karena bentuk persegi yang dihasilkan oleh indentor Vickers lebih mudah diukur dan hasil juga lebih akurat. Perubahan kecil pada bentuk persegi yang dihasilkan oleh indentor dapat dideteksi dengan mudah, sementara lekukan yang dihasilkan oleh indentor Knoop berbentuk
2.8 Kerangka Konsep
Kekerasan enamel yang di demineralisasi Gigi premolar pertama maksila permanen
Enamel
Perbedaan kekerasan enamel