EFEKTIFITAS PENAMBAHAN GLUKOSAMIN HCL-KONDROITIN SULFAT TERHADAP PENURUNAN INTENSITAS NYERI DAN INDEKS
LEQUESNE PADA PASIEN OSTEOARTRITIS LUTUT YANG DIBERI NATRIUM DIKLOFENAK
PENELITIAN UJI KLINIS DI BAGIAN / SMF ILMU PENYAKIT DALAM FAKULTAS KEDOKTERAN USU/ RS H ADAM MALIK MEDAN
JANUARI 2009 – JUNI 2009
TESIS
OLEH
KURNIAKIN WALRISMAN SAHATA GIRSANG
DEPARTEMEN ILMU PENYAKIT DALAM
FAKULTAS KEDOKTERAN UNIVERSITAS SUMATERA UTARA RSUP H ADAM MALIK / RSUD DR PIRNGADI
DEWAN PENILAI
KATA PENGANTAR
Dengan segala kerendahan hati terlebih dahulu penulis
mengucapkan segala puji bagi kebesaran Allah SWT yang telah memberi
kekuatan & rahmatNya sehingga penulis dapat menyelesaikan tesis/ karya
ilmiah akhir ini dengan judul: Efektifitas Penambahan Glukosamin Hcl-Kondroitin Sulfat Terhadap Penurunan Intensitas Nyeri dan Indeks Lequesne pada Pasien Osteoartritis Lutut yang diberi Natrium Diklofenak”, yang merupakan persyaratan dalam menyelesaikan pendidikan dokter ahli dibidang Ilmu Penyakit Dalam pada Fakultas
Kedokteran Universitas Sumatera Utara.
Dengan selesainya karya tulis ini maka penulis ingin
menyampaikan rasa terimakasih dan hormat serta penghargaan yang
setinggi – tingginya kepada :
1. Dr. Sally Roseffi Nasution SpPD - KGH. Selaku Kepala
Departemen dan Dr Refli Hasan SpPD-SpJP Sebagai Sekretaris
Departemen Ilmu Penyakit Dalam FK – USU / RSUP H. Adam
Malik Medan yang telah memberikan kemudahan dan perhatian
yang besar terhadap pendidikan penulis.
2. Dr. Zulhelmi Bustami, SpPD-KGH sebagai Ketua Program Studi
Ilmu Penyakit Dalam dan Dr. Dharma Lindarto, SpPD-KEMD
sebagai Sekretaris Program Studi Ilmu Penyakit Dalam atas segala
perhatian dan bimbingan selama penulis menjalani pendidikan.
3. Seluruh staf Departemen Ilmu Penyakit Dalam FK USU / RSUD Dr.
pendidikan: Prof. Dr. OK. Moehad Sjah, SpPD-KR, Prof. Dr. Harun
Rasyid Lubis, SpPD-KGH, Prof. Dr. Habibah Hanum Nasution,
SpPD-Kpsi, Prof. Dr. Sutomo Kasiman, SpPD-KKV, Prof. Dr.
Lukman Hakim Zain, SpPD-KGEH, Prof. Dr. M Yusuf Nasution,
SpPD-KGH, Prof. Dr. Gontar A Siregar, SpPD-KGEH, Prof. Dr.
Harris Hasan, SpPD-SpJP(K),SpPD-KKV, Dr. Bethin Marpaung,
SpPD-KGEH, Dr. Sri M Sutadi SpPD-KGEH, Dr. Mabel Sihombing,
SpPD-KGEH, Dr. Abdurrahim Rasyid Lubis, SpPD-KGH, Dr
Alwinsyah Abidin, SpPD, Dr Juwita Sembiring, SpPD-KGEH, Dr
Umar Zein KPTI-DTM&H-MHA, Dr Yosia Ginting,
SpPD-KPTI, Dr EN Keliat SpPD-KP, Dr Blondina Marpaung SpPD-KR, Dr
Leonardo B Dairi SpPD-KGEH yang merupakan guru-guru saya
yang telah banyak memberikan arahan dan petunjuk kepada saya
selama mengikuti pendidikan.
4. Dr Armon Rahimi, SpPD, Dr Daud Ginting SpPD, Dr Tambar
Kembaren SpPD, Dr Saut Marpaung SpPD, Dr Mardianto, SpPD,
Dr Zuhrial SpPD, Dr Dasril Efendi SpPD, Dr Ilhamd SpPD, Dr
Calvin Damanik SpPD, Dr Zainal Safri SpPD, Dr Rahmat Isnanta,
SpPD, Dr Santi Safril, SpPD, Dr Dairion Gatot SpPD, Dr Jerahim
Tarigan SpPD, Dr Endang Sembiring SpPD, Dr Abraham SpPD, Dr
Soegiarto Gani SpPD, Dr Savita Handayani SpPD, Dr. Deske
Muhadi SpPD, Dr Franciscus Ginting SpPD sebagai dokter kepala
ruangan/ senior yang telah amat banyak membimbing saya selama
5. Direktur RSUD. Dr. Pimgadi dan RSUP. H. Adam Malik Medan,
Direktur RS PTP Tembakau Deli Medan yang telah memberi
kemudahan dan keizinan dalam menggunakan fasilitas / sarana
Rumah Sakit dalam menjalani pendidikan.
6. Direktur RS Sri Pamela Tebing Tinggi , Dr. Indra Lubisdan konsultan
bagian Penyakit Dalam Dr Nazrin B Sitompul yang telah memberi
kesempatan kepada penulis selama ditugaskan sebagai konsultan di
bagian Penyakit Dalam di RS Sri Pamela dalam rangka pendidikan
ini.
7. Para Sejawat PPDS Interna, perawat serta paramedis lainnya dan
seluruh karyawan /karyawati dilingkungan SMF / Departemen Ilmu
Penyakit Dalam RSUD Dr. Pirngadi Medan / RSUP H. Adam Malik
Medan / RS Sri Pamela atas kerjasama yang baik selama ini.
8. Para penderita rawat inap dan rawat jalan di SMF/Departemen Ilmu
Penyakit Dalam RSUD. Dr. Pirngadi dan RSUP. H. Adam Malik
Medan, karena tanpa mereka mustahil penulis dapat
menyelesaikan pendidikan ini.
9. Pada kesempatan ini pula izinkan saya mengucapkan terimakah
kepada Rektor USU dan Dekan Fakultas Kedokteran USU yang
telah memberikan kesempatan kepada penulis untuk mengikuti
pendidikan ini.
10. Khusus mengenai karya tulis ini, penulis mengucapkan terimakasih
yang sebesar – besarnya kepada Prof Dr. OK. Moehad Sjah
sekaligus sebagai pembimbing tesis, yang senantiasa tidak
henti-hentinya memberi semagat dan memberi kemudahan
seluas-luasnya selama penulis mengikuti pendidikan dan dalam
melaksanakan penelitian ini sampai selesai dan juga penulis
rasakan benar-benar dengan tulus membantu penulis
menyelesaikan penelitian dan karya tulis ini, hanya doa yang dapat
penulis berikan semoga kiranya Allah SWT memberikan kesehatan
dan membalas kebaikan beliau serta keluarga dengan surga-Nya.
Penulis juga mengucapkan terimakasih sebesar-besarnya dan
semoga tuhan memberkati kepada Dr. Blondina Marpaung
SpPD-KR yang telah meluangkan waktu dalam kesibukannya,
memberikan pengarahan dan memotivasi penulis, dan Dr. Deske
Muhadi SpPD yang banyak memotivasi penulis untuk mengikuti
pendidikan di bagian penyakit dalam dan membantu penulis dalam
menyelesaikan tulisan ini sampai selesai.
11. Kepada Drs Abdul Jalil Amri Arma, M.Kes yang telah memberikan
bantuan yang tulus kepada penulis khususnya dalam metodologi
penelitian ini.
Rasa hormat dan terimakasih yang setinggi – tingginya dan
setulusnya penulis tujukan kepada papa H. M. Amin Girsang dan mama
Hj. Sumentharia Sinaga yang saya kasihi, yang telah membesarkan,
mengasuh, mendidik dan menyekolahkan penulis, banyak berkorban serta
memberikan dorongan secara moril dan materil demi kemajuan penulis.
kedua orang tua saya, Kiranya Allah SWT selalu memberikan yang terbaik
bagi papa dan mama yang tercinta.
Kepada Ayah mertua H. Zainal Bahri Saragih dan Ibu mertua Hj.
Mandiah Sinaga (Alm) yang telah memberikan dorongan semangat dalam
menyelesaikan pendidikan ini, saya ucapkan terimakasih yang setulusnya,
kiranya Allah SWT selalu memberikan yang terbaik untuk kedua mertua
saya.
Khusus untuk istriku tercinta Sri Kunbestari Fitriani Saragih, sulit
rasanya memilih kata – kata yang tepat untuk menyampaikan rasa
terimakasih atas kesabaran, keikhlasan, dukungan, dorongan dan segala
pengorbanan yang telah diberikan selama ini, semoga apa yang kita capai
ini dapat memberikan kebahagian dan kesejahteraan bagi kita dan
semoga Allah SWT selalu meridhoi rumah tangga kita. Demikian juga
kepada buah hatiku yang kusayangi Azifah Syifa Girsang, Fadilah Salma
Girsang dan Nadirah Sihran Girsang, semoga apa yang kita jalani
bersama selama ini menjadi pendorong untuk mencapai cita – cita yang
lebih baik lagi.
Kepada Abang, Kakak dan Adikku dan seluruh anggota keluarga
yang telah banyak membantu, memberi semangat dan dorongan selama
pendidikan, terima kasihku yang tak terhingga untuk segalanya.
Akhimya izinkanlah penulis memohon maaf yang sebesar-besamya
atas kesalahan dan kekurangan selama mengikuti pendidikan ini, semoga
segala bantuan, dorongan dan petunjuk yang diberikan kepada penulis
ganda dari Allah SWT yang maha pengasih, maha pemurah dan maha
penyayang. Amin ya Rabbal Alamin.
Medan, Juli 2009.
Penulis,
D A F T A R I S I
Halaman
Kata pengantar ... i
Daftar isi ... vii
Daftar tabel dan gambar ... xi
Daftar singkatan ... xii
Abstrak ... xiv
BAB I : P E N D A H U L U A N ... 1
BAB II : TINJAUAN PUSTAKA 2.1. Osteoartritis ... 5
2.1.1. Patologi dan Patogenesis OA ... 5
2.1.2. Faktor Resiko OA ... 8
2.1.3. Manifestasi Klinis ... 10
2.1.4. Diagnosis ... 11
2.2. Nyeri Rematik ... 13
2.2.1. Mekanisme Nyeri ... 13
2.2.2. Pengukuran Nyeri ... 14
2.2.2.1. Visual Analogue Scale ... 15
2.3. Glukosamin Hcl dan Kondroitin Sulfat ... 15
2.3.1. Glukosamin Hcl ... 15
2.3.1.1. Biokimia ... 16
2.3.1.2. Efek Kesehatan ... 17
2.3.1.3. Penggunaan ... 17
2.3.2. Kondroitin Sulfat ... 18
2.3.2.1. Fungsi ... 19
2.3.2.2. Struktural ... 19
2.3.2.3. Regulasi ... 19
2.3.2.4. Penggunaan Medis ... 20
2.3.2.5. Farmakologi ... 20
2.3.2.6. Sumber ... 21
2.4. Pengobatan OA dengan Glukosamin dan Kondroitin Sulfat ... 21
2.5. Evaluasi Efek teraumatik OA Lutut... 25
BAB III : PENELITIAN SENDIRI 3.1. Latar Belakang... 27
3.2. Perumusan Masalah ... 30
3.3. Hipotesa ... 30
3.4. Tujuan Penelitian ... 31
3.5. Manfaat Penelitian ... ... 31
3.6. Kerangka Konsepsional ... 31
3.7. Bahan dan Cara 3.7.1. Desain Penelitian ... 31
3.7.2. Definisi operasional ………...………. 32
3.7.2.1. Osteoartritis lutut ………...… 32
3.7.2.2. Intensitas Nyeri ………..….. 32
3.7.2.3. Indeks Lequesne ………...…...………. 33
3.7.2.4. Kellgreen Lawrence .………..…………. 34
3.7.2.6. Lama Sakit ... 35
3.7.2.7. Berat Badan ... 35
3.7.2.8. Tinggi Badan ... 35
3.7.2.9. Indeks Massa Tubuh ... 35
3.7.3. Waktu dan Tempat Penelitian …….……….………. 36
3.7.4. Populasi Terjangkau ……….….………. 36
3.7.5. Kriteria Inklusi ………..………... 36
3.7.6. Kriteria Eksklusi ………..……… 36
3.7.7. Populasi dan Sampel ……..……… 37
3.7.8. Cara Penelitian ... 37
3.7.9. Analisa Data ... 38
3.7.10. Kerangka Operasional ... 39
BAB IV : HASIL DAN PEMBAHASAN 4.1. Hasil Penelitian ... 40
4.1.1. Karakteristik Subyek Penelitian ... 40
4.1.2. Efek Terapi Glukosamin Hcl-Kondroitin Sulfat terhadap nilai VAS ... 42
4.1.3. Efek Terapi Glukosamin Hcl-Kondroitin Sulfat terhadap nilai Indeks Lequesne... 43
4.1.4. Efek Terapi Glukosamin Hcl-Kondroitin Sulfat terhadap nilai VAS selama 3 bulan ... 44
4.1.5. Efek Terapi Glukosamin Hcl-Kondroitin Sulfat terhadap nilai Indeks Lequesne selama 3 bulan... 45
BAB V : KESIMPULAN DAN SARAN
5.1. K e s i m p u l a n ... 50
5.2. S a r a n ... 50
BAB VI : DAFTAR PUSTAKA ... 51
LAMPIRAN 1. Master Tabel ... 57
2. Persetujuan Komite Etik ... 59
3. Lembaran Penjelasan Kepada Subyek Penelitian ... 60
4. Formulir Persetujuan Setelah Penjelasan ... 61
5. Form Data Peserta Penelitian... 62
DAFTAR TABEL
Halaman T a b e l 1 : Data Karakteristik Sampel Studi Masing-Masing
Kelompok...41
T a b e l 2 : Perbandingan VAS Perlakuan dan kontrol dari minggu ke 2– 12...42
T a b e l 3 : Perbandingan LQ Perlakuan dan Kontrol dari minggu ke 2-12...43
DAFTAR GAMBAR Gambar 1 : Rumus Bangun Glukosamin ...16
Gambar 2 : Rumus Bangun Kondroitin Sulfat ...18
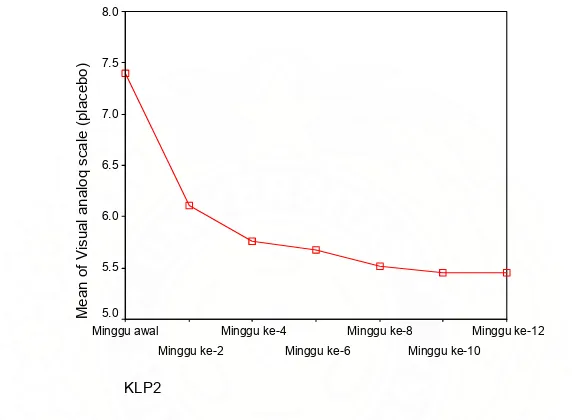
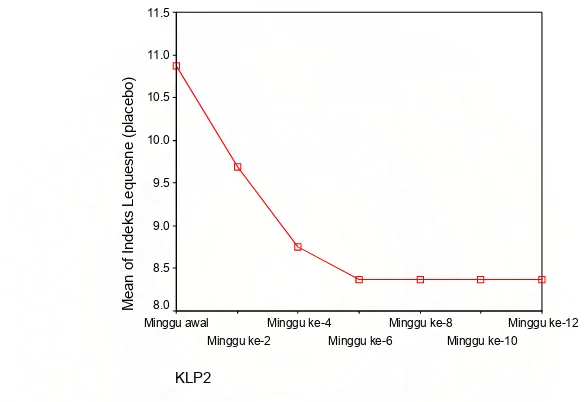
Gambar 3 : Rata-rata Nilai VAS Placebo selama 3 bulan...44
Gambar 4 : Rata-rata Nilai VAS Perlakuan selama 3 bulan...44
Gambar 5 : Rata-rata Nilai LQ Placebo selama 3 bulan...45
DAFTAR SINGKATAN
ACR : American College of Rheumatology
ARA : American Rheumatology Association
CM : Centi Meter
DMOADs : Disease modifying Osteoartritis Drugs
ECM : Extracellular matrix
EULAR : European League Against Rheumatism
FK : Fakultas Kedokteran
GAG : Glikosaminoglikan
GMP : Good Manufacturing Process
GNP : Gross National Product
IMT : Indeks Massa Tubuh
KG : Kilo Gram
LED : Laju Endap Darah
LQ : Indeks Lequesne
MMPs : Matriks Metalo Proteinases
mRNA : mesanger Ribo Nucleat Acid
NO : Nitric Oxide
NSAIDs : Non Steroid Anti Inflamation Drugs
OA : Osteoartritis
OA-SYSADOA : OsteoartritisSymptomatic Slow acting drugs for
SYSADOA : Symptomatic Slow Acting Drugs for
Osteoarthritis
RF : Reumatoid Faktor
TIMPs : Tissue Inhibitor Proteinases
USU : Unuversitas Sumatra Utara
VAS : Visual Analogue Scale
WHO : Word Health Organitation
Abstrak
Efektivitas Penambahan Glukosamin Hcl-Kondroitin Sulfat Terhadap Penurunan Intensitas Nyeri dan Indeks Lequesne pada Pasien Osteoartritis
Lutut yang diberi Natrium Diklofenak
Kurniakin WSG, OK Moehad sjah
Divisi Reumatologi, Departemen Penyakit Dalam
Fakultas Kedokteran Universitas Sumatera Utara – RSUP H Adam Malik , Medan
Latar Belakang:
Glukosamin HCL-Kondroitin Sulfat merupakan salah satu Disease Modifying Osteoartritis Drug (DMOD) dilaporkan efektif dalam menatalaksana osteoartritis lutut berdasarkan beberapa penelitian terakhir. Efektivitas obat ini dalam menurunkan intensitas nyeri dan perbaikan klinis masih diperdebatkan.
Tujuan:
Untuk mengetahui efektifitas pemberian Glukosamin HCL-Kondroitin Sulfat dalam menurunkan intensitas nyeri dan indeks Lequesne (klinis) pada pasien osteoartritis sendi lutut.
Metode :
32 pasien osteoartritis lutut dengan grade 2-3 dilakukan secara uji klinis dengan penilaian intensitas nyeri (Visual Analoque Scale) dan progresifitas penyakit (indeks lequesne) pada kelompok perlakuan dengan kelompok kontrol sebelum dan sesudah pemberian Glukosamin HCL-Kondroitin sulfat dengan dosis 1500/1200 mg selama 12 minggu. Setiap 2 minggu dimonitor efek samping obat dan dievaluasi intensitas nyeri dan indeks lequesne.
Hasil :
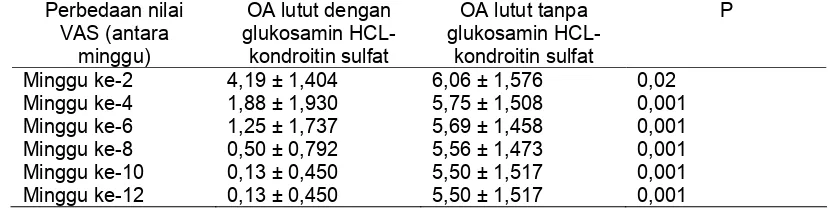
Didapatkan 32 pasien yang dibagi dalam dua kelompok, 16 pasien kelompok Glukosamin HCL-Kondroitin Sulfat (GKS) dan 16 pasien kelompok placebo. Satu pasien dari kelompok GKS dan satu pasien dari kelompok placebo drop out. Terdapat perbedaan bermakna dalam penurunan intensitas nyeri antara kelompok perlakuan dan kelompok placebo pada minggu ke dua sampai minggu ke dua belas pengobatan (4,34 ± 1,404 vs 6,11 ± 1,576 ; p=0,02; 1,99 ± 1,93 vs 5,76 ± 1,51; p=0,001; 1,25 ± 1,74 vs 5,68 ± 1,46; p=0,001; 0,47 ± 0,79 vs 5,52 ± 1,47; p=0,001; 0,11 ± 0,45 vs 5,46 ± 1,517, p=0,001; 0,11±0,45 vs 5,46 ±1,52; p=0,001) dan terdapat juga perbedaan bermakna dalam penurunan indeks lequesne antara kelompok perlakuan dan kelompok placebo pada minggu ke empat sampai minggu ke dua belas pengobatan (3,56 ± 1,896 vs 8,75 ± 4,420; p=0,001; 2,00 ± 1,731 vs 8,38 ± 4,241; p=0,001; 1,56 ± 1,315 vs 8,38 ± 4,241; p=0,001; 1,25 ± 1,438 vs 8,38 ± 4,241; p=0,001; 1,25 ±1,438 vs 8,38 ±4,241; p=0,001)
Kesimpulan :
Glukosamin HCL-Kondroitin Sulfat efektif dalam menurunkan intensitas nyeri dan indeks lequesne pada pasien osteoartritis lutut.
Abstract
Effectivity Glucosamine HCL- Chondroitin Sulfate in Reduced Intensity of Pain and Lequesne Index in Osteoarthtitis Genu With Sodium Diclovenac
Kurniakin WSG, OK Moehad Sjah
Rheumatology division, Internal Department Faculty of Medicine University of Sumatera Utara-H.Adam Malik Hospital
Medan.
Background:
Glucosamine HCL-Chondroitin Sulfate is Modifying osteoarthritis drug rises was reported efective in treatment osteoarthritis genu according to study. Effectivity of this drugs in reduced intencity of pain and recover symptoms was debated.
Aim :
To know effectivity glucosamine HCL-Chondroitin Sulfate in reduced intensity of pain and Lequesne index in osteoarthritis genu patient.
Method:
Thirty two osteoarthritis genu patients with grade 2-3 do the clinical trial with measure intensity of pain (visual analoque scale) and Lequesne index in case and control before and after gives glucosamine HCL-Chondroitin sulfate with doses 1500/1200 mg with duration 12 weeks. Every 2 weeks side effect of drugs monitored and evaluated tolerated of pain and Lequesne index.
Results:
Thirty two patients divided in two groups, 16 patients glucosamine HCL-Chondroitin sulfate group and 16 patients in placebo group. We found significant different in reduced intensity of pain between case group and placebo group in second week until twelveth week treatment (4,34 ± 1,404 vs 6,11 ± 1,576 ; p=0,02; 1,99 ± 1,93 vs 5,76 ± 1,51; p=0,001; 1,25 ± 1,74 vs 5,68 ± 1,46; p=0,001; 0,47 ± 0,79 vs 5,52 ± 1,47; p=0,001; 0,11 ± 0,45 vs 5,46 ± 1,517, p=0,001; 0,11±0,45 vs 5,46 ±1,52; p=0,001) and we found significant different in decreased lequesne index between case group and placebo group in fourth week until twelveth treatment.
Conclusions :
Glucosamine Hcl-Chondroitin sulfate effective in reduced intensity of pain and lequesne index in osteoarthritis genu.
BAB I PENDAHULUAN 1. Latar Belakang
Osteoartritis sampai saat ini masih merupakan salah satu penyakit
sendi sinovial terbanyak dijumpai dalam masyarakat, baik di Indonesia
atau belahan dunia lainnya, selain karena prevalensinya yang meningkat
juga karena masih banyaknya penderita osteoartritis yang belum
mendapatkan pengobatan yang memadai. Data dari WHO memperkirakan
10% dari penduduk berusia lebih dari 60 tahun terserang penyakit ini,
sedangkan pada penduduk Amerika Serikat berumur 25 sampai 75 tahun
diperkirakan 12,1% mempunyai tanda dan gejala klinik OA.1
Di Indonesia OA merupakan penyakit rematik yang paling banyak
dijumpai. Di kabupaten Malang dan Kotamadya Malang ditemukan
prevalensi sebesar 10,0% dan 13,5%.2 Sedangkan di poliklinik Sub bagian
Reumatologi FKUI/RSCM ditemukan pada 43,82% dari seluruh penderita
baru penyakit rematik yang berobat antara tahun 1991-1994.3
Dampak ekonomi, psikologi dan sosial dari OA sangat besar, tidak
hanya untuk penderita tetapi juga keluarga dan lingkungannya dan
diperkirakan biaya nasional untuk semua artritis sebesar 1% dari GNP
(Gross National Product). Di Australia biaya medik yang dikeluarkan
adalah sebesar USS 2.700/orang/tahun.4
Sendi penyangga berat tubuh seperti panggul dan lutut merupakan
sendi tersering terkena OA. Nyeri sendi berfluktuasi disertai
kekakuan sendi merupakan manifestasi penyakit ini. Mereka yang terkena
OA jenis ini hanya sebagian kecil (seperlima) yang mencari pengobatan.5,6
Osteoartritis seringkali dianggap sebagai penyakit usia lanjut dan
kerusakan sendi diakibatkan akibat proses menua. Oleh karenanya,
proses degenerasi sendi dianggap sebagai satu-satunya patologi yang
mendasarinya. Muncullah hipotesis wear and tear atau penggunaan yang
lama dan berlebihan menimbulkan keausan yang diikuti respon perbaikan.
Respon perbaikan tulang terlihat sebagai pembentukan osteofit. Namun
seiring dengan adanya berbagai bukti lain akan keterkaitan proses
inflamasi pada sinovium (sinovitis), maka patologi OA tidak hanya
didasarkan atas proses degeneratif semata, namun kombinasi
diantaranya yang terjadi bersamaan.7 Bukti inflamasi lebih nyata pada
flare up OA.8 Secara molekular, inflamasi dimulai oleh rangsangan, baik
akibat trauma maupun benda asing, yang akan merangsang makrofag
menghasilkan berbagai sitokin yang akan merangsang produksi dan
migrasi sel darah putih lainnya ke tempat inflamasi. Adanya respon
inflamasi memicu rangkaian enzimatik yang berakhir dengan kerusakan
rawan sendi sebagai target kerusakan pada patogenesis OA. 7,8
Dimana sitokin yang dikeluarkan oleh khondrosit dan
mengakibatkan kerusakan matriks rawan sendi atau oleh sel lain dalam
struktur sendi seperti sinoviosit, makrofag dan fibroblast. Keunikan
patogenesis OA adalah percepatan proses degenerasi yang lebih besar
dibandingkan proses anaboliknya. Perlambatan sintesis faktor anabolik
pada ECM (extra cellular matrix). Oleh karenanya manifestasi klinis OA
tidak hanya berupa nyeri, namun juga kekakuan sendi, gangguan
pergerakan , krepitus dan efusi sendi. 6,7
Penatalaksanaan OA saat ini lebih banyak ditujukan dalam
mengatasi rasa nyeri serta inflamasi dan perbaikan fungsi sendi yang
terkena (symptoms modification). Sementara structure modification lebih
sulit dicapai. Bila mengacu pada perubahan paradigma patogenesis OA,
maka sudah selayaknya diperhatikan bahwa OA melibatkan faktor
biomekanik dan biologik yang mengakibatkan rusaknya rawan sendi.9
Berbagai modalitas penatalaksanaan OA dapat dikelompokkan dalam tiga
kelompok besar, yaitu non farkologik, farkologik (analgetik, NSAIDs,
intra-artikuler steroid, berbagai rubefacients, symptomatic slow acting drugs in
OA-SYSADOA) dan pembedahan.10
Obat tersering yang diberikan dan bertujuan mengatasi rasa nyeri
adalah kelompok NSAIDs. Keterbatasan pemakaian NSAIDs tidak
terlepas dari efek samping terhadap sistim gastrointestinal, kardiovaskular
dan dampak buruk terhadap rawan sendi. Disamping itu NSAIDs tidak
mampu mengubah perjalanan alamiah penyakit OA. Sedangkan
penggunaan injeksi intraartikular memerlukan keterampilan dalam injeksi. 11
Berdasarkan keterangan diatas, sudah selayaknya dipahami
mekanisme kerusakan rawan sendi sebagai landasan baru dalam
pendekatan panatalaksanaan OA, dimana disease modifying OA drugs
memperlambat, menghambat atau bahkan merestorasi kerusakan yang
terjadi pada rawan sendi. Terminologi DMOAD bermula dari
khondroprotektor. Obat dalam kelompok ini seyogyanya memiliki dua efek
penting yaitu symptoms modifying effect dan structure modifying effect.12
Penelitian terhadap glukosamin sulfat dan kondroitin sulfat pada OA
telah banyak dilakukan dan efek perbaikan simptomatik dan struktural
BAB II
TINJAUAN PUSTAKA
2.1.OSTEOARTRITIS
Osteoartritis didefinisikan sebagai penyakit yang diakibatkan
kejadian biologik dan mekanik yang menyebabkan gangguan
keseimbangan antara proses degradasi dan sintesis dari kondrosit,
matriks ekstraseluler tulang rawan sendi dan tulang subkondral.1
2.1.1. Patologi dan patogenesis OA
Rawan sendi normal terdiri dari tulang rawan (kondrosit) dan
matriks tulang rawan. Matrik tulang rawan dibentuk oleh proteoglikan dan
serabut kologen. Proteoglikan tersusun atas inti protein dengan
glikosaminoglikan yang melekat pada inti protein tersebut. Glikosamiglikan
yang banyak menyusun matrik tulang rawan adalah kondroitin sulfat dan
keratan sulfat. Proteoglikan akan membentuk agregat bersama dengan
asam hialuronat dan agregat ini mempunyai kemampuan untuk mengisap
air sampai 50 kali volumenya, sehingga dapat mengembang dan berfungsi
sebagai bantalan. Kolagen yang menyusun matrik tulang rawan terutama
terdiri dari kolagen tipe II, IX dan XII. Kolagen ini tidak elastis dan
berfungsi untuk menahan agar proteoglikan tidak berkembang berlebihan. 14-16
Kondrosit adalah sel rawan sendi yang terbenam didalam matrik
rawan sendi. Fungsi kondrosit adalah untuk mensintesis matrik rawan
Dengan bertambahnya usia, terjadi perubahan pada rawan sendi,
glikosaminoglikan menjadi memendek, sehingga kemampuan proteoglikan
untuk menahan air menjadi berkurang. Akibatnya, fungsi rawan sendi
sebagai bantalan terhadap beban pada sendi akan berkurang. Selain itu
jaringan kolagen juga menjadi patah-patah yang mengakibatkan timbulnya
fisur pada rawan sendi. 14,15
Rawan sendi merupakan jaringan yang avaskukular. Nutrisi untuk
rawan sendi diperoleh dari cairan sendi dengan cara difusi. Beban yang
hilang timbul pada rawan sendi sangat baik untuk peredaran nutrisi dan
pembuangan hasil metabolisme dari rawan sendi. Osteoartritis terjadi
akibat kondrosit gagal mensintesis matriks yang berkualitas dan gagal
memelihara keseimbangan antara degradasi dan sintesis matriks
ekstraseluler. Perubahan kualitas matrik tersebut termasuk produksi
kolagen tipeI, III,VI dan X yang berlebihan dan sintesis proteoglikan yang
pendek. 14,15
Gangguan keseimbangan antara sintesis dan degradasi matriks
termasuk peningkatan produksi berbagai proteinase yang akan merusak
kolagen dan proteoglikan dan penurunan sintesis inhibitor proteinase yaitu
tissue inhibitor proteinases (TIMPs). Sintesis kondrosit abnormal ini
disebabkan oleh berbagai sitokin, mediator lipid (prostaglandin), radikal
bebas (NO, H202) dan konstituen matriks itu sendiri yaitu fragmen
fibronektin. Kondrosit yang teraktifasi ini memiliki kemampuan untuk
Proteinase yang banyak perperan pada kerusakan rawan sendi
adalah matriks metalo proteinases (MMPs), yang sampai saat ini telah
ditemukan minimal 18. Kerja MMPs akan dikontrol oleh TIMPs.
Keseimbangan antara MMPs dan TIMPs sangat penting untuk
menghindari kerusakan rawan sendi. MMPs merupakan salah satu kelas
enzim yang termasuk metaloproteinase. 14,15
MMPs diproduksi oleh kondrosit kemudian diaktifkan melalui
kaskade yang melibatkan proteinase serin (aktivator plasminogen,
plasminogen, plasmin), radikal bebas dan beberapa MMPs tipe membran.
Kaskade enzimatik ini dikontrol oleh berbagai inhibitor, termasuk TIMPs
dan inhibitor aktivator plasminogen. 14,15
Enzim lain yang turut merusak kolagen tipe II dan proteoglikan
adalah katepsin, yang bekerja pada pH rendah, proteinase haspartat dan
proteinase sistein yang disimpan didalam lisosom kondrosit. Hialuronidase
tidak terdapat didalam rawan sendi tetapi glikosidase lain turut berperan
merusak proteoglikan. 14,15
Selain kondrosit, sinoviosit juga berperan pada patogenesis
osteoartritis, terutama setelah terjadi sinovitis. Sinovisit yang mengalami
peradangan akan menghasilkan MMPs dan berbagai sitokin yang akan
dilepaskan kedalam rongga sendi dan merusak matriks rawan sendi serta
mengaktifkan kondrosit. Pada akhirnya tulang subkondral juga ikut
berperan, dimana osteoblas akan merangsang dan menghasilkan enzim
Berbagai sitokin turut berperan merangsang kondrosit untuk
menghasilkan enzim perusak rawan sendi. Sitokin yang terpenting adalah
IL-1 yang juga berperan menurunkan sintesis kolagen tipe II dan XI dan
meningkatkan sintesis kolagen tipe I dan III, sehingga menghasilkan
matriks rawan sendi yang bersifat buruk. 14-16
Oksidanitrat (NO) diketahui berperan pada penghambatan sintesis
glikosida minoglikan dan kolagen dan merangsang sintesis mRNA, MMP
dan protein yang berperan pada kematian kondrosit, tetapi NO juga
memiliki efek anabolik dan antikatabolik. 14-16
2.1.2. Faktor resiko Osteoatritis
Harus diingat bahwa masing-masing sendi mempunyai biomekanik,
cedera dan persentase gangguan yang berbeda, sehingga peran faktor
resiko tersebut untuk masing-masing OA tertentu berbeda. Secara garis
besar faktor resiko untuk timbulnya OA adalah seperti dibawah ini,
yaitu:17,18
a. Umur
Dari semua faktor resiko untuk timbulnya OA, faktor ketuaan adalah
yang terkuat. Prevalensi dan beratnya OA semakin meningkat
dengan bertambahnya umur. OA hampir tidak pernah pada
anak-anak, jarang pada umur dibawah 40 tahun dan sering pada umur di
atas 60 tahun. Akan tetapi harus diingat bahwa OA bukan akibat
ketuaan saja, perubahan tulang rawan sendi pada ketuaan berbada
b. Jenis kelamin
Wanita lebih sering terkena OA lutut dan OA banyak sendi, dan
lelaki lebih sering terkena OA paha, pergelangan tangan dan leher.
Secara keseluruhan, di bawah 45 tahun frekuensi OA kurang lebih
sama pada laki dan wanita, tetapi diatas 50 tahun (setelah
menopause) frekuensi OA lebih sering pada wanita dari pada pria.
Hal ini menunjukkan adanya peran hormonal pada patogenesa OA.
c. Suku bangsa
Prevalensi dan pola terkenanya sendi pada OA nampaknya
terdapat perbedaan diantara masing-masing suku bangsa.
d. Genetik
Faktor herediter juga berperan pada timbulnya OA misalnya, pada
ibu dari seorang wanita dengan OA pada sendi interfalang distal
terdapat 2 kali lebih sering OA pada sendi tersebut, dan
anak-anaknya perempuan cendrung mempunyai 3 kali lebih sering, dari
pada ibu dan anak perempuan dari wanita tanpa OA tersebut.
e. Kegemukan dan penyakit metabolik
Berat badan yang berlebih berkaitan dengan meningkatnya resiko
untuk timbulnya OA baik pada wanita atau pria. Kegemukan
ternyata tak hanya berkaitan dengan OA pada sendi yang
menanggung beban, tapi juga dengan OA sendi lain. Oleh karena
itu di samping faktor mekanis yang berperan, diduga terdapat faktor
metabolik yang berperan.
Pekerjaan berat maupun dengan pemakaian satu sendi yang terus
menerus berkaitan dengan peningkatan resiko OA tertentu. Beban
benturan yang berulang dapat menjadi suatu faktor penentu lokasi
pada orang-orang yang mempunyai predisposisi OA dan dapat
berkaitan dengan perkembangan dan beratnya OA.
g. Kelainan pertumbuhan
Kelainan kogenital dan pertumbuhan telah dikaitkan dengan
timbulnya OA pada usia muda.
h. Faktor lain
Tingginya kepadatan tulang dapat meningkatkan resiko timbulnya
OA, karena tulang yang lebih padat tak mampu membantu
mengurangi benturan beban yang diterima oleh tulang rawan sendi.
Akibatnya tulang rawan sendi menjadi lebih mudah robek. Merokok
menjadi faktor yang melindungi untuk timbulnya OA, meskipun
mekanismenya belum jelas.
2.1.3. Manifestasi klinis
Manifestasi klinis yang palin sering ialah nyeri sendi yang
mengganggu aktivitas. Awitan penyakit samar-samar, perjalanan penyakit
lambat. Nyeri sendi bervariasi dari ringan sampai berat, bertambah pada
aktivitas dan membaik jika istirahat. Terdapat kaku sendi pagi hari yang
biasanya kurang dari 30 menit. Sendi yang sering terkena ialah sendi
lutut, pinggul, kaki dan vertebra lumbosakral. Biasanya unilateral tanpa
manifestasi sistemik. Pada pemeriksaan jasmani didapatkan pembesaran
kapsul sendi serta tendo periartikular. Gerakan sendi terbatas dan
mungkin juga ditemukan instabilitas sendi dan locking pada waktu sendi
digerakkan. Krepitasi yang dirasakan pada gerakan pasif merupakan
akibat iregularitas rawan sendi yang berhadapan. Tanda ini terdapat pada
lebih dari 90% pasien lutut. Lebih dari 50% pasien OA lutut menunjukkan
malaligment sendi. Kadang terdapat tanda peradangan lokal berupa
panas dan pembengkakan jaringan lunak akibat efusi sendi.17-20
2.1.4. Diagnosis
Diagnosis OA biasanya sudah dapat ditegakkan berdasarkan
riwayat penyaki dan pemeriksaan jasmani. Pemeriksaan laboratorium rutin
hasilnya normal. Pemeriksan penunjang yang dapat membantu ialah
pemeriksaan radiologis. Kelainan radiologis yang tampak berupa osteofit
pada tepi sendi, penyempitan celah sendi yang asimetris, sklerosis
subkondral, kista subkhondral dan perubahan bentuk sendi. Untuk
penyeragaman diagnosis dipergunakan beberapa kriteria, yaitu: 17-20
a. Klinis:
1. nyeri sendi lutut dan 3 dari kriteria dibawah ini:
2. krepitus saat gerakan aktif
3. kaku sendi < 30 menit
4. umur > 50 tahun
5. pembesaran tulang sendi lutut
6. nyeri tekan tepi tulang
diagnosis OA jika: Bila ditemukan nyeri sendi serta osteofit dari
gambaran radiologik dan 3 dari kriteria 2-7. Sensitivitas 95% dan
spesifitas 69%.
b. Klinis dan radiologis:
1.nyeri sendi dan paling sedikit 1 dari 3 kriteria di bawah ini:
2.kaku sendi < 30 menit
3.umur > 50 tahun
4.krepitus pada gerakan sendi aktif
Diagnosis OA jika didapatkan butir 1 disertai osteofit pada
gambaran radiologik disertai kriteria 2,3 atau 4. Paling sedikit satu
kriteria 2-4 harus ditemuka.
Sensitivitas 91% dan spesifitas 86%.
c. Klinis dan laboratoris:
1.nyeri sendi di tambah adanya 5 dari kriteria dibawah ini:
2.usia > 50 tahun
3.kaku sendi < 30 menit
4.krepitus
5.nyeri tekan tepi tulang
6.pembesaran tulang
7.tidak teraba hangat pada sendi terkena
8.LED < 40 mm/jam
9.RF < 1:40
Diagnosis OA ditegakkan bila ditemukan nyeri sendi lutut diserrtai 5
dari kriteria 2-10.
Sensitivitas 92% dan spesifitas 75%.
2.2. Nyeri rematik 2.2.1. Mekanisme nyeri
Proses nyeri mulai stimulasi nociceptor oleh stimulus noxiuos
sampai terjadinya pengalaman subyektif nyeri adalah suatu seri kejadian
elektrik dan kimia yang bisa dikelompokkan menjadi 4 proses, yaitu:
transduksi, transmisi, modulasi dan persepsi.21
Secara singkat mekanisme nyeri dimulai dari stimulasi nosiseptor
oleh stimulus noxiuos pada jaringan, yang kemudian akan mengakibatkan
stimulasi nosiseptor dimana disini stimulus noxious tersebut akan dirubah
menjadi potensial aksi. Proses ini disebut transduksi atau aktivasi
reseptor. Selanjutnya potensial aksi tersebut akan ditransmisikan menuju
neuron susunan saraf pusat yang berhubungan dengan nyeri. Tahap
pertama transmisi adalah konduksi impuls dari neuron aferen primer ke
kornu dorsalis medula spinalis, pada kornu dorsalis ini neuron aferen
primer bersinap dengan neuron susunan sarap pusat. Dari sini jaringan
neuron tersebut akan naik keatas di medula spinalis menuju batang otak
dan talamus. Selanjutnya terjadi hubungan timbal balik antara talamus
dan pusat-pusat yang lebih tinggi di otak yang mengurusi respons
persepsi dan afektif yang berhubungan dengan nyeri. Tetapi rangsangan
nosiseptif tidak selalu menimbulkan persepsi nyeri dan sebaliknya
modulasi sinyal yang mampu mempengaruhi proses nyeri tersebut, tempat
modulasi sinyal yang paling diketahui adalah pada kornu dorsalis medula
spinalis. Proses terakhr adalah persepsi, dimana pesan nyeri di relai
menuju ke otak dan menghasilkan pengalaman yang tidak
menyenangkan.21
2.2.2. Pengukuran nyeri
Pengukuran nyeri seyogyanya dilakukan seobyektif mungkin dan
dapat menggunakan beberapa metode pengukuran dan terbanyak adalah
dengan kwesioner serta observasi pola prilaku terkait dengan rasa nyeri.
Katagori pengukuran nyeri beragam sekali namun yang termudah yaitu,
pengukuran nyeri dengan skala kategorikal, numerikal dan pendekatan
multidimensional. Masing-masing pendekatan pengukuran nyeri ini
memiliki kelebihan dan kekurangan masing-masing serta tingkat
obyektifitas-subyektifitas berbeda-beda dan area yang menjadi tujuan
pengukuran apakah sensorik saja, apakah mencakup afektif serta adakah
sifat evaluatif dari instrumen dimaksud.21,22
Pengukuran nyeri dapat merupakan pengukuran satu dimensional
saja atau pengukuran berdimensi ganda. Pada pengukuran satu
dimensional umumnya hanya mengukur pada satu aspek nyeri saja,
misalnya berapa berat rasa nyeri menggunakan pain rating scale yang
dapat berupa pengukuran kategorikal atau numerikal misalnya visula
analogue scale (VAS). 21,22
VAS adalah instrumen pengukuran nyeri yang paling banyak
dipakai dalam berbagai studi klinis dan diterapkan terhadap berbagai jenis
nyeri. Metode pengukuran ini sebagaimana yang dikembangkan oleh
Stevenson dan kawan-kawan dari pusat penanganan nyeri kanker di
Wisconsin. Terdiri dari satu garis lurus sepanjang 10 cm. Garis paling kiri
menunjukkan tidak ada rasa nyeri sama sekali, sedangkan garis paling
kanan menandakan rasa nyeri yang paling buruk. Kepada pasien
dimintakan untuk memberikan garis tegak lurus yang menandakan derajat
beratnya nyeri yang dirasakannya. Instrumen VAS ini tidak
menggambarkan jenis rasa nyeri yang dialami pasien.21,22
Pengukuran dengan VAS pada nilai di bawah 4 dikatakan sebagai
nyeri ringan; nilai 4-7 dinyatakan sebagai nyeri sedang dan di atas7
dianggap sebagai nyeri hebat.21
2.3. Glukosamin HCL dan kondroitin sulfat 2.3.1. Glukosamin HCL
Glukosamin (C6H13NO5) merupakan gula amino dan prekursor
penting dalam sintesis biokimia dari protein glikosilasi dan lipid.
Glukosamin ditemukan sebagai komponen utama dari rangka luar
krustasea, artropoda, dan cendawan. Glukosamin merupakan salah satu
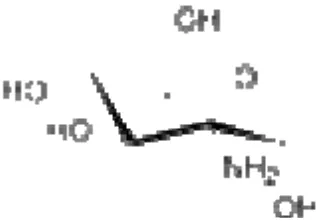
monosakarida yang banyak dijumpai (gambar-1).23,24
Dalam industri,
glukosamin diproduksi dengan cara hidrolisis rangka luar krustasea.
Glukosamin umumnya digunakan untuk meringankan gejala osteoartritis
Gambar-1. Rumus Bangun Glukosamin 2.3.1.1. Biokimia
Glukosamin pertama kali diidentifikasi oleh Dr. Georg Ledderhose
pada tahun 1876, tapi struktur stereokimia tidak sepenuhnya diketahui
sampai ditemukan oleh Walter Haworth pada tahun 1939.23,24
D-Glukosamin dibuat secara alami dalam bentuk glukosamin-6-fosfat, dan
merupakan prekursor biokimia dari semua gula yang mengandung
nitrogen.23 Glucosamine-6-phosphate dibuat dari fructose-6-phosphate
dan glutamine sebagai fase awal dari jalur biosintesis hexosamine.24
Produk akhir dari lintasan ini adalah UDP-N-asetilglukosamin
(UDP-GlcNAc), yang kemudian digunakan untuk membentuk glikosaminoglikan,
proteoglikan, dan glikolipid.
Pembentukan glukosamin-6-fosfat merupakan tahap awal untuk
menyintesis produk ini. Glukosamin merupakan komponen penting dalam
meregulasi produksi senyawa tersebut. Walaupun demikian, bagaimana
lintasan biosintesis heksoamin diregulasi dan bagaimana hal ini dapat
berpengaruh terhadap penyakit manusia masih belum terlalu jelas 25
2.3.1.2. Efek Kesehatan
Konsumsi glukosamin secara oral biasanya digunakan untuk
yang menyusun jaringan kartilago sendi, suplementasi glukosamin
diharapkan mampu membangun kembali jaringan kartilago dan
mengurangi resiko osteoartritis, walaupun efektivitasnya masih
diperdebatkan.26,27
2.3.1.3. Penggunaan
Glukosamin dapat diperoleh dari suplemen makanan. Dosis garam
glukosamin (dalam bentuk glukosamin sulfat atau glukosamin hidroklorida)
yang biasa dikonsumsi adalah sebesar 1,500 mg per hari.Umumnya,
glukosamin yang umum dijual merupakan glukosamin dalam bentuk
glukosamine sulfat dan glukosamin hidroklorida.26 Glukosamin umumnya
dijual bersama kombinasi dengan suplemen lain seperti kondroitin sulfat.
2.3.1.4. Keamanan
Berbagai studi klinis telah membuktikan bahwa glukosamin aman
untuk dikonsumsi. Walaupun demikian, isu alergi masih sering mengikuti
konsumsi glukosamin ini karena umumnya glukosamin diperoleh dari
cangkang kerang dan semacamnya (walaupun pada kenyataanya, bahan
alergen penyebab alergi ada di dalam daging kerang, bukan pada
cangkangnya).28 Sumber alternatif lain adalah penggunaan cendawan
pada fermentasi jagung. Beberapa sumber lain menyebutkan bahwa
konsumsi berlebih glukosamin berkontribusi pada diabetes. 25tapi
beberapa referensi lain menyangkal.29-31 Terlepas dari isu tersebut,
sebuah penelitian lain menunjukkan bahwa asupan glukosamin sesuai
dosis yang dianjurkan tidak berpengaruh terhadap intolerasi glukosa dan
2.3.2. Kondroitin Sulfat
Kondroitin yang lebih dikenal dengan nama Kondroitin sulfat adalah
glikosaminoglikan (GAG) tersulfatisasi yang tersusun atas rantai gula
bercabang (N-asetilgalaktosamin dan asam glukuronat). Ia biasanya
ditemukan menempel pada protein sebagai bagian dari senyawa
proteoglikan. Rantai kondrotin dapat memiliki lebih dari 100 gula individual
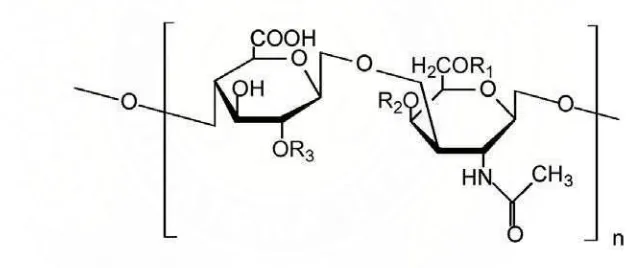
yang dapat tersulfatisasi di setiap bagian variable (gambar-2). Kondroitin
sulfat merupakan komponen struktural penting penyusun jaringan
kartilago dan berperan dalam meningkatkan ketahanannya terhadap
tekanan. Bersama dengan glukosamin, kondroitin sulfat digunakan secara
luas sebagai suplemen makanan untuk mencegah osteoartritis.36,37
Gambar-2. Struktur kimia Kondroitin Sulfat 2.3.2.1. Fungsi
Fungsi dari kondroitin sangat tergantung pada sifat proteoglikan
yang ditempelinya. Fungsi dari senyawa ini dapat dibedakan secara
struktural atau regulatoral. walaupun demikian, tidak tertutup kemungkikan
bahwa beberapa proteoglikan dapat memiliki kedua fungsi tersebut
2.3.2.2. Struktural
Kondroitin sulfat merupakan komponen mayor dari matriks
ekstraselular dan penting dalam mempertahankan kesatuan dari jaringan.
Fungsi ini merupakan karakteristik khusus dari proteoglikan agregat besar
seperti aggrekan, versikan, brevikan, dan neurokan. Sebagai bagian
aggrekan, kondroitin sulfat adalah komponen mayor penyusun kartilago.
Kondrotin sulfat yang bermuatan dapat menimbulkan gaya elektrostatik
yang mampu meningkatkan tahanan kartilago terhadap tekanan.
Kekurangan kondroitin sulfat dari jaringan kartilago merupakan penyebab
mayor dariosteoartritis. 36,37
2.3.2.3. Regulasi
Di dalam matriks ektraseluler, kondroitin sulfat dapat berinteraksi
dengan protein karena muatan negatifnya. Interaksi ini penting untuk
meregulasi jalur lalulintas aktivitas seluler. Di dalam jaringan saraf,
kondroitin sulfat meregulasi pertumbuhan dan perkembangan sistem saraf
dan respons sistem saraf terhadap cedera. 36,37
2.3.2.4. Penggunaan Medis
Kondroitin merupakan bahan yang umumnya dapat ditemukan di
dalam suplemen makanan. Ia juga biasa digunakan sebagai obat alternatif
untuk mengatasi osteoartritis dan juga diterima sebagai obat gejala
2.3.2.5. Farmakologi
Dosis oral dari kondroitin untuk digunakan di dalam uji klinis
manusia adalah 800–1,200 mg per hari. Kebanyakan kondroitin dibuat
dari jaringan kartilago sapi dan babi (trakea sapi dan telinga serta hidung
babi). Beberapa sumber lain seperti kartilago hiu, ikan dan unggas juga
digunakan. Dikarenakan kondroitin bukanlah substansi yang seragam dan
secara alami muncul dalam berbagai variasi dan bentuk, komposisi pasti
dari setiap suplemen dapat berbeda. Hal ini dapat disebabkan karena
perusahaan-perusahaan pembuat suplemen membuat produknya dengan
memenuhi Proses Manufaktor yang Baik (good manufacturing
Process/GMP) untuk makanan manusia, bukan dengan standar
pembuatan bagi industri farmasi sehingga produk yang dihasilkan juga
tidak memenuhi standar farmasi. Belum ada efek yang signifikan dari
overdosis kondroitin untuk pemakaian jangka panjang.39 European
League Against Rheumatism (EULAR) mengonfirmasi kondrotin sulfat
sebagai salah satu obat teraman untuk mengatsi osteoartritis.40
2.3.2.6. Sumber Kondroitin
Saat ini, belum ada sumber alami yang signifikan bagi kondroitin
sulfat mengingat banyaknya variasi bentuknya. Sumber kondroitin yang
signifikan dapat diperoleh dari suplemen makanan.
2.4. Pengobatan OA dengan glukosamin dan kondroitin sulfat Penatalaksanaan OA yang baik hingga saat ini belum memuaskan.
setidaknya untuk memperlambat proses patologi pada OA sampai saat ini
belum ditemukan. Belum ditemukan satu obatpun yang secara pasti dan
meyakinkan, yang dapat mempengaruhi kondrosit dalam memacu proses
sintesis rawan sendi sehingga kerusakan benar-benar diperbaiki dan
bukan proses remodeling yang justru dapat dianggap sebagai kegagalan
respon perbaikan sendi terhadap kerusakan rawan sendi. 14-16
Kondroprotektor sebagai modifying drugs untuk OA dibagi 2 yaitu
symptom modifying drugs dan structure modifying drugs. Kondroprotektor
yang sebenarnya adalah DMOADs , dan menurut Lequesne diartikan
sebagai simptom dan structure modifying drugs dan ditujukan tidak hanya
perlindungan terhadap rawan sendi namun lebih jauh lagi dalam
pencengahan, penghentian, perlambatan proses patologi OA dan
penyembuhan atau mengembalikan lesi rawan sendi. Dalam hal ini yang
dimaksud sebagai kondroprotektor tidak lain adalah symptom modifying
drugs atau sering dikenal sebagai symptomatic slow acting drugs for
osteoarthritis (SYSADOA) karena belum ada obat yang memenuhi kriteria
sebagai DMOADs. 14-16
Kelompok nutraceutical baik glukosamin, kondroitin sulfat atau
lainnya banyak dikembangkan dengan maksud mengurangi pemakaian
NSAID terutama mengatasi efek samping. Banyak tulisan yag menulis
tentang hal ini seperti Das AM, Kalbhen DA, MCAlindon TE, dll, dan telah
banyak publikasi dari tahun 1980 sampai saat ini yang membicarakan
manfaat klinis kondroprotektor ini. 14,41,42 Reginster dkk membuktikan untuk
mampu mempengaruhi struktur rawan sendi yaitu dengan didapatkannya
pengurangan penyempitan celah sendi secara radiologis dan efektifitas
simptomatik dibuktikan melalui pengukuran WOMAC. 14,43
Uebelhart D dkk dalam penelitianya membuktikan bahwa kondroitin
sulfat dapat mempengaruhi perjalanan alamiah OA pada manusia melalui
pembuktikan hambatan progresif OA secara radiologik. 14,44
Lee BF dalam penelitianya mendapatkan bahwa kondroitin sulfat
memberikan efek mengatasi rasa nyeri yang lebih baik dibandingkan
placebo dalam waktu pemberian 6 bulan tanpa adanya perbedaan efek
dosis. 14,45
Bourgeois P dkk dalam penelitianya mendapatkan bahwa
pemberian kondroitin sulfat 1200 mg sebagai dosis tunggal atau dosis
terbagi selama 3 bulan efektifitasnya terhadap parameter nyeri (VAS/
Visual Analogue Scale) dan indeks Lequesne’s tidak berbeda bermakna. 14,46
Kondroitin sulfat memiliki efek anti inflamasi dengan mekanisme
yang belum jelas, ia tidak menghambat isoform COX atau enzim
proteolitik, tetapi melalui hambatan in vitro pembentukan superoksida dan
enzim lisosoma pada hepar. 14,47
Mc Carty MF dkk menjelaskan mekanisme glukosamin sulfat dapat
memperbaiki rawan sendi dengan meningkatkan produksi HA oleh
sinovium seolah-olah seperti efek menyerupai hormon yang dipicu oleh
Ganu dkk membuktikan bahwa N-glycosylation akan menurunkan
kadar MMPs, nitric oxide, dan prostaglandi E2. 47
Kombinasi glukosamin sulfat dan kondroitin sulfat sering ditemukan
dalam berbagai sediaan nutraceutical yang beredar dipasaran. 14-16
Karel Pavelha dkk pada penelitan selama 3 tahun secara acak,
placebo kontrol, double-blind study, pemberian 1500 mg glukosamin sulfat
sekali sehari pada 202 penderita OA lutut (diagnosa berdasarkan kriteria
ACR) dengan menilai celah sendi secara radiografi, dan menilai gejala
dengan indeks Lequesne mendapatkan pengurangan progresifitas dan
gejala nyeri dan keterbatasan fungsi sendi pun terjadi perbaikan secara
bermakna dibandingkan dengan pemberian placebo. Mereka mengatakan
bahwa pengobatan jangka panjang dengan glukosamin sulfat akan
mengurangi atau memperlambat progresifitas OA lutut mungkin karena
terjadi modifikasi penyakit. 48
Bernard Mazieres dkk meneliti efikasi dan keamanan pemberian
kondroitin sulfat 1 gram perhari dibandingkan pemberian placebo, dengan
metode double blind randomized parallel group study selama pengobatan
3 bulan diikuti dengan 3 bulan periode post treatment pada penderita OA
femorotibial. Penilaian dengan memakai indeks Lequesne, nyeri waktu
aktifitas dan waktu istirahat, dan daily living pada 130 kasus (63 dengan
kondroitin sulfat dan 67 dengan placebo). Didapatkan hasil efikasi dan
tolarensi yang baik dibandingkan plasebo setelah 3 bulan pengobatan dan
Florent Richy dkk meneliti struktur dan efek simtomatik pemberian
glukosamin sulfat dan kondroitin sulfat minimal 2 minggu secara oral pada
OA lutut. Dengan metode komprehensive meta-analysis, terhadap efek
penyempitan celah sendi dan indeks Lequesne, VAS, mobility, keamanan
dan respon pengobatan. Dengan mengumpulkan semua penelitian,
clinical trial dan penelitian yang dilakukan atau dipublikasikan sejak
Januari 1980 sampai Maret 2002. Didapatkan hasil yang sangat bermakna
pada pemberian glukosamin sulfat untuk semua hasil, dan pemberian
kondroitin sulfat sangat efektif dengan penilaian indeks Lequesne, VAS,
dan mobility dan kedua preparat tersebut sangat aman dipakai. 42
Secara umum dapat dikatakan bahwa glukosamin adalah zat
pembentuk proteoglikan dan dibutuhkan untuk sintesis glukosaminoglikan,
dan sumber nutrisi untuk sintesis glikosaminoglikan dan proteoglikan dan
merupakan stimulan bagi kondrosit dan sebagai pemacu kondrosit dalam
produksi kolagen dan proteoglikan lebih banyak serta sebagai pengatur
metabolisme kartilage. 14-16,42,43,47,48
Secara umum dapat dikatan bahwa kondroitin adalah pembentuk
matriks proteoglikan suatu zat yang menunjukkan efikasi dalam
memperbaiki gejala OA dan merupakan zat anti inflamasi dan zat yang
dapat memperbaiki integritas dan elastisitas dari kartilage. Juga dapat
mempertahankan kesehatan cairan sinovial dan membantu menghambat
enzim yang melisis kartilage. 14,42,44-47,49
Kombinasi glukosamin-kondroitin akan menstimulir kondrosit dalam
memperbaiki integritas rawan sendi dan mempertahankan kesehatan
cairan sinovial, dan kombinasi ini sebagai substrat primer biosintesis
proteoglikan dan akan mencegah kerusakan dini pada rawan sendi dan
berperan juga dalam keseimbangan sintesis dan degradasi rawan
sendi.14-16,42-49
Penelitian tentang penggunaan kombinasi glukosamin sulfat dan
kondroitin sulfat pada pasien osteoartritis sendi lutut yang dilaporkan di
Medan sampai saat ini sepengetahuan penulis belum ada. Oleh karena itu
penulis tertarik melakukan penelitian mengenai pengaruh penggunaan
kombinasi glukosamin sulfat dan kondroitin sulfat pada pengobatan
osteoartritis.
2.5. Evaluasi efek terapeutik OA Lutut
Untuk mengetahui perkembangan klinis pada penelitian ini
menggunakan:17,20
• VAS: Penilaian nyeri dengan mengukur jarak dari titik nol ke garis
yang dicentangkan.
• Indeks Lequesne: mengukur berat ringannya OA sendi lutut dari
pengamatan pasien dengan menjumlah nilai dari nyeri, jarak
maksimium yang dapat ditempuh dengan berjalan dan aktivitas
BAB III
PENELITIAN SENDIRI 3.1. Latar Belakang
Salah satu penyakit sendi sinovial terbanyak dijumpai dalam
masyarakat, baik di Indonesia atau belahan dunia lainnya, adalah
osteoartritis (OA). WHO memperkirakan 10% dari penduduk berusia lebih
dari 60 tahun terserang penyakit ini, sedangkan pada penduduk Amerika
Serikat berumur 25 sampai 75 tahun diperkirakan 12,1% mempunyai
tanda dan gejala klinik OA.1
Di Indonesia OA merupakan penyakit rematik yang paling banyak
dijumpai. Di kabupaten Malang dan Kotamadya Malang ditemukan
prevalensi sebesar 10,0% dan 13,5%.2 Sedangkan di poliklinik Sub bagian
Reumatologi FKUI/RSCM ditemukan pada 43,82% dari seluruh penderita
baru penyakit rematik yang berobat antara tahun 1991-1994.3
Dampak ekonomi, psikologi dan sosial dari OA sangat besar, tidak
hanya untuk penderita tetapi juga keluarga dan lingkungannya.4
Sendi penyangga berat tubuh seperti panggul dan lutut merupakan
sendi tersering terkena OA. Nyeri sendi berfluktuasi disertai
pembengkakan sendi, efusi, berkurangnya lingkup gerak sendi dan
kekakuan sendi merupakan manifestasi penyakit ini. Mereka yang terkena
OA jenis ini hanya sebagian kecil (seperlima) yang mencari pengobatan.5,6
Osteoartritis seringkali dianggap sebagai penyakit usia lanjut dan
kerusakan sendi diakibatkan akibat proses menua. Oleh karenanya,
mendasarinya. Muncullah hipotesis wear and tear atau penggunaan yang
lama dan berlebihan menimbulkan keausan yang diikuti respon perbaikan.
Respon perbaikan tulang terlihat sebagai pembentukan osteofit. Namun
seiring dengan adanya berbagai bukti lain akan keterkaitan proses
inflamasi pada sinovium (sinovitis), maka patologi OA tidak hanya
didasarkan atas proses degeneratif semata, namun kombinasi
diantaranya yang terjadi bersamaan.7 Bukti inflamasi lebih nyata pada
flare up OA.8 Secara molekular, inflamasi dimulai oleh rangsangan, baik
akibat trauma maupun benda asing, yang akan merangsang makrofag
menghasilkan berbagai sitokin yang akan merangsang produksi dan
migrasi sel darah putih lainnya ke tempat inflamasi. Adanya respon
inflamasi memicu rangkaian enzimatik yang berakhir dengan kerusakan
rawan sendi sebagai target kerusakan pada patogenesis OA. 7,8
Dimana sitokin yang dikeluarkan oleh khondrosit dan
mengakibatkan kerusakan matriks rawan sendi atau oleh sel lain dalam
struktur sendi seperti sinoviosit, makrofag dan fibroblast. Keunikan
patogenesis OA adalah percepatan proses degenerasi yang lebih besar
dibandingkan proses anaboliknya. Perlambatan sintesis faktor anabolik
seperti kolagen tipe II dan agrecan menyebabkan ketidakseimbangan
pada ECM (extra cellular matrix). Oleh karenanya manifestasi klinis OA
tidak hanya berupa nyeri, namun juga kekakuan sendi, gangguan
pergerakan , krepitus dan efusi sendi. 6,7
Penatalaksanaan OA saat ini lebih banyak ditujukan dalam
terkena (symptoms modification). Sementara structure modification lebih
sulit dicapai. Bila mengacu pada perubahan paradigma patogenesis OA,
maka sudah selayaknya diperhatikan bahwa OA melibatkan faktor
biomekanik dan biologik yang mengakibatkan rusaknya rawan sendi.9
Berbagai modalitas penatalaksanaan OA dapat dikelompokkan dalam tiga
kelompok besar, yaitu non farkologik, farkologik (analgetik, NSAIDs,
intra-artikuler steroid, berbagai rubefacients, symptomatic slow acting drugs in
OA-SYSADOA) dan pembedahan.10
Obat tersering yang diberikan dan bertujuan mengatasi rasa nyeri
adalah kelompok NSAIDs. Keterbatasan pemakaian NSAIDs tidak
terlepas dari efek samping terhadap sistim gastrointestinal, kardiovaskular
dan dampak buruk terhadap rawan sendi. Disamping itu NSAIDs tidak
mampu mengubah perjalanan alamiah penyakit OA. Sedangkan
penggunaan injeksi intraartikular memerlukan keterampilan dalam
injeksi.11
Berdasarkan keterangan diatas, sudah selayaknya dipahami
mekanisme kerusakan rawan sendi sebagai landasan baru dalam
pendekatan panatalaksanaan OA, dimana disease modifying OA drugs
(DMOA) merupakan obat yang ditujukan untuk mencegah, memperlambat,
menghambat atau bahkan merestorasi kerusakan yang terjadi pada rawan
sendi. Terminologi DMOA bermula dari khondroprotektor. Obat dalam
kelompok ini seyogyanya memiliki dua efek penting yaitu symptoms
Berbagai penelitian lain terhadap glukosamin sulfat dan kondroitin
sulfat pada OA telah dilakukan. Efek perbaikan simptomatik dan struktural
diperlihatkan oleh kombinasi glukosamin sulfat dan chondroitin sulfat telah
diteliti Florent Richy dkk .13
Penelitian tentang penggunaan kombinasi glukosamin sulfat dan
kondroitin sulfat pada pasien osteoartritis sendi lutut yang dilaporkan di
Medan sampai saat ini sepengetahuan penulis belum ada. Oleh karena itu
penulis tertarik melakukan penelitian mengenai pengaruh penggunaan
kombinasi glukosamin sulfat dan kondroitin sulfat sebagai pengobatan
osteoartritis.
3.2. Perumusan Masalah
Apakah terdapat perbedaan penurunan intensitas nyeri dan indeks
Lequesne pada pasien osteoartritis sendi lutut setelah penambahan
12 minggu Glukosamin HCL-Kondroitin Sulfat dibandingkan dengan
kontrol (pasien osteoartritis sendi lutut dengan Natrium diklofenak
2x50mg dan Ranitidin 2x150 mg dengan placebo).
3.3. Hipotesa
Terdapat perbedaan rerata penurunan intensitas nyeri dan indeks
Lequesne pada pasien osteoartritis sendi lutut dengan
penambahan 12 minggu Glukosamin HCL-Kondroitin Sulfat
dibandingkan dengan kontrol.
3,4. Tujuan penelitian
Untuk mengetahui efektifitas penambahan Glukosamin
Lequesne pada pasien osteoartritis sendi lutut yang diberi natrium
diklofenak.
3.5. Manfaat penelitian
Dengan mengetahui penurunan intensitas nyeri dan indeks
Lequesne pada pasien osteoartritis sendi lutut yang menggunakan
Glukosamin HCL-Kondroitin Sulfat sehingga dapat menjadi salah
satu modalitas terapi dalam pengobatan osteoartritis sendi lutut.
3.6. Kerangka Konsepsional
OSTEOARTRITIS LUTUT KRITERIA INKLUSI
DAN EKSKLUSI
OA LUTUT GRADE 2 DAN 3 YANG MEMENUHI KRITERIA
PEMERIKSAAN VAS DAN INDEKS LEQUESNE
GLUKOSAMIN&KONDROITIN SULFAT KELOMPOK KONTROL PEMERIKSAAN VAS DAN INDEKS LEQUESNE
( DIBANDINGKAN) 3.7. BAHAN DAN CARA
3.7.1. Desain Penelitian
Penelitian dilakukan secara uji klinis acak sederhana tersamar
3.7.2. Definisi Operasional 3.7.2.1.Osteoartritis Lutut
Osteoartritis lutut ialah osteoartritits sendi lutut yang memenuhi
kriteria dari ”Criteria for classification of idiopathic OA of the knee”
dari American College of Rheumatology (ACR).
Klinis dan radiologis:
1. Nyeri sendi dan paling sedikit 1 dari3 kriteria dibawah ini:
2. Kaku sendi < 30 menit
3. Umur > 50 tahun
4. Krepitus pada gerakan sendi aktif
Diagnosis OA jika didapatkan butir 1 disertai osteofit pada
gambaran radiologik disertai kriteria 2,3 atau 4. Paling sedikit satu
kriteria 2-4 harus ditemukan.
Sensitivitas 91% dan spesifitas 86%
3.7.2.2. Intensitas Nyeri
Intensita nyeri dengan Visual Analogue Scale (VAS), dengan
membuat garis lurus sepanjang 10 cm dan berikan tanda 0 pada
ujung kiri garis dan 10 pada ujung kanan garis. Berikan penjelasan
pada titik nol menunjukkan tidak ada rasa nyeri sama sekali dan
sebaliknya pada titik 10 dan dintruksikan pada pasien untuk
membuat tanda ( I ) yang memotong rentang garis dengan skala
1-10 cm. Ukurlah dari titik 0 kearah tanda garis tersebut.
Penilaiannya: a. VAS <4 : nyeri ringan
c. VAS >7 : nyeri berat
3.7.2.3. Indeks Lequesne
Indeks Lequesne, nilai tersebut dijumlahkan dan dinyatakan
sebagai:
- Nilai 1-4 : ringan
- Nilai 5-7 : sedang
- Nilai 8-10 :berat
- Nilai >14 : ekstrim berat
3.7.2.4. Kellgreen Lawrence
Derajat osteoartritis lutut dinyatakan menurut skala derajat
Radiologis dari Kellgreen Lawrence, yaitu:
0= normal
1= kemungkinan osteofit
2= osteofit nyata dan kemungkinan penyempitan celah sendi
3= osteofit sedang dan multipel, penyempitan celah sendi
nyata, sedikit skerosis dan kemungkinan deformitas
4= osteofit besar, penyempitan celah sendi besar, sklerosis
berat dan deformitas nyata.
Pemeriksaan radiologik sendi lutut Anterior-Posterior dilakukan
dengan posisi weigt bearing (berdiri pada posisi menopang berat
badan) dan lateral dengan fleksi 45º. Bila derajat radiologik salah
satu sendi lutut lebih tinggi dari yang lain maka pasien
dimasukkan kedalam kelompok yang lebih tinggi. Pemeriksaan
dilakukan di Bagian Radiologi
3.7.2.5. Umur
Umur: dihitung saat pemeriksaan, menurut Kartu Tanda
Penduduk, apabila>6 bulan dibulatkan keatas dan apabila <6
3.7.2.6. Lama sakit
Lama sakit: dalam bulan, dihitung sejak peserta penelitian merasa
sakit di daerah lutut baik dalam keadaan istirahat maupun aktivitas
sampai diperiksa peneliti.
3.7.2.7. Berat badan
Berat badan: dalam kilogram (kg) diukur menggunakan timbangan
model ZT 120, peserta penelitian ditimbang tanpa alas kaki.
3.7.2.8. Tinggi badan
Tinggi badan: dalam centimeter (cm) diukur menggunakan
timbangan model ZT 120, peserta penelitian berdiri tegak tanpa
alas kaki.
3.7.2.9. Indeks masa tubuh
Indeks masa tubuh (IMT): dalam kg/m2 dihitung menggunakan
rumus:
Berat badan (kg)/ Tinggi Badan (m2 )
Katagori berat badan didasarkan hasil IMT dengan ketentuan dari
Centers for Disease Control and Preventions United States
Department of Health and Human Services, sebagai berikut:
1. IMT <20 kg/ m2 = BB Kurang
2. IMT >20-<25 kg/ m2 = BB Normal
3. IMT >25-<30 kg/ m2 = BB Lebih
3.7.3. Waktu dan Tempat Penelitian
Penelitian dilakukan mulai bulan Desember 2008 - Juni 2009 di
Poliklinik Reumatologi, serta Poliklinik Pria dan Wanita Bagian
Penyakit Dalam RSUP H. Adam Malik Medan dan RS Pirngadi.
3.7.4. Populasi Terjangkau
Penderita OA sendi lutut yang berobat jalan di RSUP H. Adam
Malik Medan dan RS Pirngadi.
3.7.5. Kriteria yang diikutkan dalam penelitian a. Usia diatas 18 tahun
b. Penderita OA lutut berdasarkan kriteria ARA pada tahun
2006.
c. Grade 1-3 berdasarkan klasifikasi Kellgren/Lawrence.
d. Bersedia mengikuti penelitian
3.7.6. Kriteria yang dikeluarkan dari penelitian a. Memakan dan memakai obat rematik
b. Variasi perubahan berat badan signifikan
c. Penderita penyakit serius
d. Menderita penyakit kaganasan, penyakit ginjal menahun,
hipertiroidisme Diabetes Melitus, hipertensi dan
kardiovaskuler selama periode tahun 2008-2009.
e. Mempunyai penyakit artritis lain selain osteoartritis
f. Gambaran radiografi OA lutut grade 4 tahun 2008-2009
h. Riwayat mendapat terapi injeksi kortikosteroid intra artikuler
< 12 minggu
3.7.7. Populasi dan Sampel
Perkiraan besar sampel Besar sampel dengan memakai rumus :64 2 (Z α + Z )S
n =
X1 – X2
Dimana :
Zα = nilai normal berdasarkan α = 0,05 dan Zα = 1,96 Z = nilai normal berdasarkan = 0,05 dan Z = 1,64 S = Simpangan Baku gabungan = 16
X1-X2 = 15
2 2
Jadi besar sampel dan kontrol masing-masing 15 orang 3.7.8 . Cara Penelitian
a) Penelitian ini mendapat persetujuan oleh komite etik penelitian
bidang kesehatan FK USU dan dilakukan skrining untuk kriteria
yang dimasukkan dan yang dikeluarkan, kemudian subyek
penelitian diminta untuk menandatangani persetujuan tertulis
(informed consent), setelah dilakukan pemeriksaan pendahuluan,
termasuk anamnesis, pemeriksaan fisik, pengukuran tinggi badan
dan berat badan, radiografi lutut, nilai VAS, Indeks Lequesne dan
pemeriksaan laboratorium rutin yang meliputi fungsi hati, kadar
gula darah, ureum, kreatinin, darah perifer lengkap dan CRP. (1,96+1,64)(16)
(15) n =
3,6 x 16
15
Data hasil pemeriksaan dicantumkan didalam kuesioner
penelitian.
b) Pada subyek mendapat Natrium Diklofenak 50 mg dan Ranitidin
150 mg dalam dua dosis dan Glukosamin HCL-Kondroitin Sulfat
1500/1200 mg/hari selama 3 bulan dan kontrol tidak mendapat
Glukosamin HCL-Kondroitin Sulfat
c) Evaluasi pemakaian tablet menggunakan sistim pill count yaitu
pasien diberi tablet untuk 2 minggu dan evaluasinya dengan cara
menghitung tablet yang tersisa.
d) Setelah 12 minggu pemakaian tablet, dilakukan pemeriksaan
terhadap subyek dan kontrol meliputi nilai VAS, Indeks Lequesne
dan laboratorium ulang fungsi hati, kadar gula darah, ureum,
kreatinin, darah perifer lengkap dan CRP.
e) Selama penelitian dilakukan pengamatan terhadap efek samping
yang dicatat didalam kuesioner.
3.7.9. Analisa Data
Penentuan normalisasi dari distribusi data ditentukan dengan Kolmogorov - Smirnov, untuk melihat hubungan antara jenis kelamin dan tingkat pendidikan dengan Glukosamin HCL-Kondroitin Sulfat digunakan uji Chi Square. Untuk melihat hubungan karakteristik penderita yang meliputi umur, indeks massa tubuh, dengan Glukosamin HCL-Kondroitin Sulfat digunakan uji t tidak berpasangan67
Untuk membandingkan penurunan gambaran radiografi
berdasarkan Kellgren/Lawrence, CRP, LED, VAS 1-7 dan LQ1-7
Sulfat dengan menggunakan uji t berpasangan bila data
terdistribusi normal dan uji wilcoxon bila data tidak terdistribusi
normal., dikatakan bermakna bila p <0,05. Analisa data dilakukan
dengan menggunakan perangkat lunak program SPSS versi 11,5.67
3.7.10. Kerangka Operasional
SUBJEK PENELITIAN :
Penderita OA lutut Dengan Glukosamin
HCL-Kondroitin Sulfat
- ANAMNESA
- PEMERIKSAAN FISIK
PEMERIKSAAN VAS DAN INDEKS LEQUESNE
- KRITERIA INKLUSI
- KRITERIA EKSKLUSI
PEMERIKSAAN VAS DAN INDEKS LEQUESNE
PENDERITA OA LUTUT
KONTROL :
Penderita OA lutut tanpa Glukosamin
BAB IV
HASIL DAN PEMBAHASAN
4.1. HASIL PENELITIAN
4.1.1. Karakteristik Subjek Penelitian
Penelitian dilakukan mulai bulan Desember 2008 sampai Juni 2009
di poliklinik Reumatologi, serta Poliklinik Pria dan Wanita Bagian Penyakit
Dalam RSUP H. Adam Malik Medan dan RS Pirngadi. Ada 34 orang yang
memenuhi kriteria diikutkan dalam penelitian, dari 34 orang kemudian
dikelompokkan menjadi dua kelompok terdiri dari 17 pasien osteoartritis
sendi lutut dengan pemberian 12 minggu Glukosamin HCL-Kondroitin
Sulfat dan 17 pasien osteoartritis sendi lutut tanpa pemberian Glukosamin
HCL-Kondroitin Sulfat.
Satu orang peserta perlakuan mengundurkan diri pada hari kedua
setelah mendapat terapi. Alasan pengunduran diri adalah gejala nyeri ulu
hati dan mual – mual yang dialami sehingga tidak ingin melanjutkan
penelitian. Dan satu orang peserta kontrol mengundurkan diri setelah hari
ketiga mendapat terapi. Alasan pengunduran diri adalah nyeri ulu hati dan
gatal diseluruh badan. Pada akhir penelitian, subjek berjumlah 16 orang
dari kelompok perlakuan dan 16 orang dari kelompok kontrol. Karakteristik
Tabel 1. Data karakteristik sampel studi masing – masing kelompok Osteoartritis sendi lutut
Variabel OA lutut dengan
Glukosamin HCL-Kondroitin Sulfat
Mean ± SD
OA lutut tanpa Glukosamin HCL-Berat Badan (Kg) LED Awal (mm/jam) VAS Awal (cm)
Analogue Scale; LQ = Indeks Lequesne (signifikan p<0,05)
Pada tabel 1 diperlihatkan data dasar seluruh penderita
Osteoartritis sendi lutut yang ikut penelitian. Peserta kelompok perlakuan
dengan jenis kelamin laki 3 orang (18,75%) dan 13 orang perempuan
(81,25%). Peserta kelompok placebo dengan jenis kelamin laki 1 orang
(6,25%)dan 15 orang perempuan (93,75%).
Rentang umur subjek yang ikut dalam penelitian adalah 42-82
tahun dengan usia rerata pada kelompok OA lutut dengan glukosamin
HCL-kondroitin sulfat 64,34 ± 8,84 tahun dan pada kelompok OA lutut
tanpa glukosamin 59,44 ± 9,32 tahun, dengan uji t berpasangan tidak
dijumpai perbedaan umur yang bermakna pada masing-masing kelompok
dengan p=0,137.
Rerata indeks massa tubuh antara kelompok OA lutut dengan
glukosamin HCL-kondroitin sulfat 26,74 ± 5,52 kg/m2 dengan kelompok
OA lutut tanpa glukosamin HCL-kondroitin sulfat 28,45 ± 5,01 kg/m2 , tidak
berbeda bermakna secara statistik dengan uji t berpasangan dengan