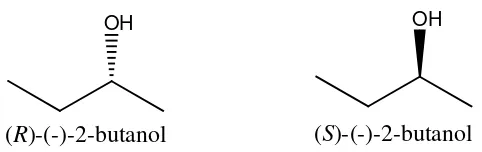1,2-DIMETIL-1,1,2,2-TETRAFENIL DISILANA SULFONAT MENGKATALISIS REAKSI ESTERIFIKASI
ASAM PALMITAT DENGAN 2-BUTANOL
SKRIPSI
RIZAL AGUS W. SIMANGUNSONG 080802042
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
1,2-DIMETIL-1,1,2,2-TETRAFENIL DISILANA SULFONAT MENGKATALISIS REAKSI ESTERIFIKASI
ASAM PALMITAT DENGAN 2-BUTANOL
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
RIZAL AGUS W. SIMANGUNSONG 080802042
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : 1,2-dimetil-1,1,2,2-tetrafenildisilana Sulfonat Mengkatalisis Reaksi Esterifikasi Asam Palmitat Dengan 2-Butanol ALAM (FMIPA) UNIVERSITAS SUMATERA UTARA
Disetujui Di Medan, 2014
Komisi Pembimbing :
Pembimbing 2 Pembimbing 1
( Dr. Nimpan Bangun, M.Sc.) (Prof. Dr. Seri Bima Sembiring, M.Sc.) Nip 195012221980031002 Nip 194907181976031001
Diketahui/Disetujui Oleh:
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
1,2-DIMETIL-1,1,2,2-TETRAFENIL DISILANA SULFONAT MENGKATALISIS REAKSI ESTERIFIKASI
ASAM PALMITAT DENGAN 2-BUTANOL
SKRIPSI
S
aya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.Medan, Juli 2014
PENGHARGAAN
Segala puji syukur penulis panjatkan kepada Tuhan Yesus Kristus atas segala berkat, kasih karuniaNya, sehingga penulis dapat menyelesaikan penelitian dan penyusunan skripsi ini sebagai salah satu persyaratan untuk meraih gelar Sarjana Sains bidang Kimia di Fakultas Matematika dan Ilmu Pengetahuan Alam (FMIPA) Universitas sumatera Utara.
Dengan segala kerendahan hati, penulis mengucapkan terima kasih yang sebesar-besarnya kepada bapak Prof. Dr. Seri Bima Sembiring selaku dosen pembimbing I dan kepada bapak Dr. Nimpan Bangun, M.Sc selaku dosen pembimbing II yang telah memberikan banyak bimbingan dan arahan kepada penulis sehingga penulis dapat menyelesaikan skripsi ini. Ibu Dr. Rumondang Bulan, M.S selaku ketua departemen dan Bapak Drs. Albert Pasaribu, M.Sc selaku sekretaris departemen kimia FMIPA USU. Kepada bapak Lamek Marpaung, M.Phill, Ph.D selaku dosen wali. Dan tak terkecuali kepada bapak Dr. Hamonangan Nainggolan, M.Sc, Bapak Dr. Minto Supeno, M.S, ibu Dra. Saur Lumban Raja, M.Si, Ibu Dra. Nurhaida Pasaribu, M.Si, ibu Dr. Andriayani, S.Pd, M.Si, selaku Staf Laboratorium kimia anorganik. Bapak dan ibu dosen serta staf pegawai departemen kimia FMIPA USU.
Terakhir Penulis menyampaikan penghargaan yang terdalam dan terima kasih yang sebesar-besarnya kepada kedua orang tuaku tercinta, ayahanda R.Simangunsong dan Ibunda E.Br. Silaban, atas semua cinta, doa yang selalu mengiringi langkah penulis, pengorbanan dan juga dukungan yang selalu diberikan. Juga penghargaan yang tulus kepada seluruh keluarga besar R. Simangunsong (Op.Monika), abang dan kak Monika, Lae dan kak Vincen, Abang dan kak Rapael, Adikku Roy simangunsong atas semua dukungan dan doa yang selalu diberikan dan keponakan tersayang Monika, christophel, Christian, Vincensius, Marinto, dan Rapael yang selalu menjadi sumber semangat buat penulis, semoga berkat dan kasih sayang Tuhan selalu menyertai kita.
Medan, Juli 2014 Penulis,
ABSTRAK
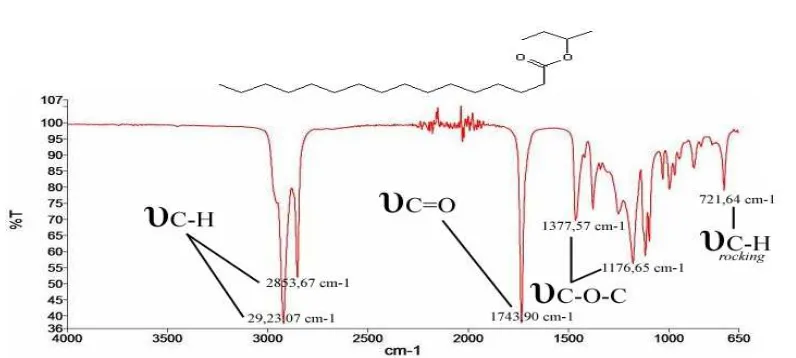
2-butil palmitat telah disintesis dengan mereaksikan asam palmitat dan 2-butanol pada suhu 100oC selama 10 jam dan pada suhu 150oC selama 15 jam dengan bantuan katalis 1,2-dimetil-1,1,2,2-tetrafenil disilan sulfonat dengan yield reaksi yang paling tinggi sebesar 48%. Spektrum FT-IR 2-butil palmitat menunjukkan pita serapan pada panjang gelombang 1743,90 cm-1 yang diberikan oleh vibrasi regangan gugus C=O ester dan pita serapan pada panjang gelombang 1377,57 cm-1 dan 1176,65 cm-1 yang diberikan oleh vibrasi regangan C-O yang berasal dari ester asam lemak. Spektrum 1
1,2-DIMETIL-1,1,2,2-TETRAFENIL DISILANE SULFONIC CATALYZED ESTERIFICATION REACTION BETWEEN PALMITIC ACID WITH
2-BUTANOL
ABSTRACT
DAFTAR ISI
BAB 1. PENDAHULUAN
1.1. Latar Belakang 1
BAB 2. TINJAUAN PUSTAKA
2.1. oleokimia 5
2.8.1.Katalis Homogen 13
2.8.2.Katalis Heterogen 13
2.8.3.Katalis Dengan Gugus asam sulfonat 14 2.8.4.Katalis Berbasis Ramah Lingkungan 14 BAB 3. METODOLOGI
3.1. Alat 16
3.2. Bahan 16
3.3. Prosedur Penelitian 17
4.3. Bagan Penelitian 18
BAB 4. HASIL DAN PEMBAHASAN
4.1. Reaksi Esterifikasi Asam Palmitat dengan 2-butanol 19 BAB 5. KESIMPULAN DAN SARAN
5.1. Kesimpulan 27
DAFTAR TABEL
DAFTAR GAMBAR
Halaman Gambar 1.1 Perkiraan struktur 1,2-dimetil-1,1,2,2-tetrafenil disilan sulfonat
2
Gambar 2.1 Struktur Trigliserida 6
Gambar 2.2 Reaksi Esterifikasi Asam Lemak Secara Umum 8 Gambar 2.3 Mekanisme reaksi esterifikasi as. lemak dengan katalis asam 8
Gambar 2.4 Bentuk isomer dari 2-butanol 10
Gambar 2.5 Reaksi Pada Permukaan Katalis Heterogen 13 Gambar 4.1 Reaksi Asam Plamitat dengan 2-butanol Menggunakan
Katalis Disilan Sulfonat 19 Gambar 4.2 Spektrum FT-IR 2-butil palmitat 21 Gambar 4.3 Spektrum 1H-NMR dari 2-butil palmitat (500 mHz, CDCl3) 22 Gambar 4.4 Expansi 1 Spektrum 1H-NMR dari 2-butil palmita
dari δ 0,84 ppm hingga δ 1,19 ppm (CDCl3) 23 Gambar 4.5 perkiraan saling tumpang tindih 2 puncak triplet A dan D 24 Gambar 4.6 Expansi 2 Spektrum 1H-NMR dari 2-butil palmitat
DAFTAR LAMPIRAN
Halaman
ABSTRAK
2-butil palmitat telah disintesis dengan mereaksikan asam palmitat dan 2-butanol pada suhu 100oC selama 10 jam dan pada suhu 150oC selama 15 jam dengan bantuan katalis 1,2-dimetil-1,1,2,2-tetrafenil disilan sulfonat dengan yield reaksi yang paling tinggi sebesar 48%. Spektrum FT-IR 2-butil palmitat menunjukkan pita serapan pada panjang gelombang 1743,90 cm-1 yang diberikan oleh vibrasi regangan gugus C=O ester dan pita serapan pada panjang gelombang 1377,57 cm-1 dan 1176,65 cm-1 yang diberikan oleh vibrasi regangan C-O yang berasal dari ester asam lemak. Spektrum 1
1,2-DIMETIL-1,1,2,2-TETRAFENIL DISILANE SULFONIC CATALYZED ESTERIFICATION REACTION BETWEEN PALMITIC ACID WITH
2-BUTANOL
ABSTRACT
BAB 1
PENDAHULUAN
1.1Latar Belakang
Katalis heterogen yang memiliki gugus asam telah digunakan secara luas dalam berbagai reaksi kimia karena memiliki banyak kelebihan dibandingkan dengan katalis homogen, antara lain aktivitas penggunaan ulang (reuseable activity) yang sangat baik, stabil pada suhu tinggi, mudah dipisahkan dari produk reaksi (Corma, A. 2008) dan rendah polusi terhadap lingkungan (Fang, L. 2013). Katalis heterogen seperti resin penukar ion, senyawa mesopori silika, dan senyawa yang mengandung gugus asam sulfonat telah digunakan untuk reaksi-reaksi seperti, alkilasi (Kouzu, M. 2011), hidrolisis (Zang, Q.Y. 2011), asilasi (Weerachhanchai, P. 2012), asetalisasi (Fang, L. 2013) dan reaksi esterifikasi (Boey, P.L. 2012., Zang, Q.Y. 2011., Lou, W.Y. 2008., Muylaert, I.2012., Kang, S.2013).
Keberadaan gugus sulfonat pada katalis heterogen mengakibatkan adanya 2 sifat yaitu sifat polar dan non-polar pada katalis tersebut. Seperti katalis Carbon nanotube yang di preparasi dengan asam sulfat (Yu, H. 2008) dan carbon-based sulfonated catalys hasil karbonasi-sebagian naptalin oleh asam sulfat (Kang, S.2013), kedua katalis ini dapat bercampur dengan baik dalam pelarut air dan pelarut organik. Ini memungkinkan dilakukannya reaksi antara pereaksi yang tidak saling bercampur tanpa menggunakan pelarut (Rajendran, A. 2011).
jarak dan minyak nabati lainnya dengan metanol, tetapi katalis ini tidak tahan pada suhu tinggi sehingga menurunkan kinerja reaksi
Manullang telah mensisntesis katalis 1,2-dimetil-1,1,2,2-tetrafenil disilan sulfonat. Katalis ini telah dipakai pada transesterifikasi crude palm oil (CPO) ber-ALB 8% dengan metanol pada suhu 140oC selama 6 jam dan menghasilkan ester total 96%. Katalis ini menunjukan bahwa tidak terjadi perubahan struktur setelah dilakukan reaksi pada suhu tinggi sehingga dapat digunakan kembali (Manullang, W. 2014).
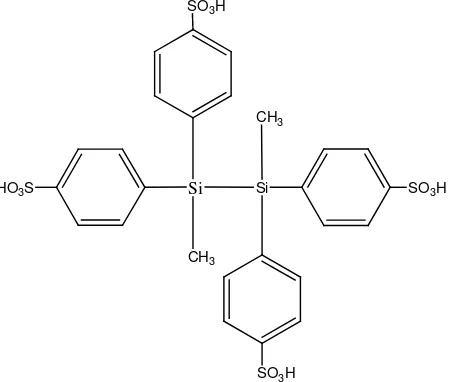
Dibawah diduga struktur katalis organo disilan sulfonat yang diperoleh dari hasil sulfonasi senyawa 1,2-dimetil-1,1,2,2-tetrafenildisilan dengan asetil sulfa seperti terlihat pada gambar 1.1 berikut.
Si Si
Gambar 1.1. Perkiraan struktur 1,2-dimetil-1,1,2,2-tetrafenil disilan sulfonat
Semua reaksi esterifikasi yang diuraikan diatas dilakukan dengan mereaksikan asam lemak dengan alcohol primer, namun esterifikasi asam lemak dengan alkohol sekunder masih sedikit dilaporkan.
dengan alkohol sekunder 2-butanol dengan bantuan katalis resin asam sulfonat pada suhu 120oC menghasilkan 64% ester total. Dari beberapa penelitian diatas, dilaporkan bahwa yield masih rendah dan dilakukan pada suhu rendah, hal ini dikarenakan katalis yang dipakai tidak tahan pada suhu tinggi sehingga mengganggu kinerja katalis.
Faktor halangan ruang yang besar menyebabkan reaksi esterifikasi asam karboksilat rantai panjang dengan alkohol sekunder sulit untuk dilakukan (Trimm, 2001). Reaksi pada suhu tinggi diharapkan dapat meningkatkan yield reaksi dan tentunya harus digunakan katalis yang tahan terhadap reaksi pada suhu tinggi. Oleh karena itu peneliti tertarik untuk mencoba menggunakan katalis asam 1,2-dimetil-1,1,2,2-tetrafenil disilan sulfonat untuk esterifikasi asam palmitat dengan 2-butanol, dimana katalis ini telah diketahui stabil pada suhu tinggi dan bersifat reuse yang baik.
1.2 Permasalahan
1. Apakah katalis asam 1,2-dimetil-1,1,2,2-tetrafenil disilan sulfonat dapat dipakai untuk reaksi esterifikasi asam palmitat dengan 2-butanol.
2. Apakah katalis tersebut masih dapat dipisahkan dari zat hasil reaksi.
1.3 Tujuan Penelitian
Memperoleh ester asam lemak melalui reaksi esterifikasi asam palmitat dengan 2-butanol menggunakan katalis asam 1,2-dimetil-1,1,2,2-tetrafenil disilan sulfonat dan memisahkan katalis dari campuran hasil reaksi.
1.4 Manfaat Penelitian
diperoleh informasi tambahan mengenai reaksi esterifikasi dengan menggunakan alkohol sekunder serta diusahakan untuk melakukan pemisahan yang baik terhadap katalis yang dipakai.
1.5 Lokasi Penelitian
Penelitian ini dilakukan di Laboratorium Anorganik FMIPA USU, Medan. Karakterisasi FT-IR dilakukan di laboratorium Terpadu LIDA USU, dan Analisa 1 H-NMR dilakukan di laboratorium LIPI serpong.
1.6 Metodologi Penelitian
BAB 2
TINJAUAN PUSTAKA
2.1 Oleokimia
Oleokimia pada dasarnya merupakan cabang ilmu kimia yang mempelajari trigliserida yang berasal dari minyak dan lemak menjadi asam lemak dan gliserin serta turunan asam lemak baik dalam bentuk ester, amida, sulfat, sulfonat, alkohol, alkoksi, maupun sabun. Oleokimia merupakan turunan gliserol dengan asam lemak yang berubah dalam bentuk turunannya yang digunakan baik sebagai surfaktan, deterjen, polimer, aditif, bahan bakar dan sebagainya. Bahan dasar oleokimia seperti gliserol, asam lemak, alkil asam lemak, amina asam lemak dan alkohol asam lemak dapat diperoleh dengan mengubah lipida baik yang berasal dari hewan maupun tumbuhan menjadi gliserol dan turunan asam lemak.
Sumber minyak dan lemak alami dapat berasal dari bahan nabati maupun hewani. Sumber minyak nabati diantaranya adalah minyak kelapa sawit, minyak kacang kedelai, minyak biji bunga matahari, minyak biji wijen, minyak jarak dan sebagainya. Sedangkan minyak dan lemak yang berasal dari hewan yaitu seperti minyak sapi, minyak domba, minyak babi, minyak ikan dan lain-lain. Minyak dan lemak tersebut sangat luas penggunaannya, baik sebagai bahan baku lemak dan minyak yang dapat dikonsumsi maupun sebagai bahan oleokimia (Richtler dan Knault, 1984).
pelumas, lilin. Penggunaan terbesar dari gliserol adalah industri farmasi dan kosmetika serta makanan (Richtler dan Knault, 1984).
2.2 Lipid, Lemak dan Minyak
Lipid adalah senyawa organik yang terjadi secara alami dan memiliki kelarutan yang terbatas dalam air dan dapat diisolasi dari tumbuhan atau hewan dengan cara ekstraksi dengan menggunakan pelarut non-polar. Lipid terbagi atas dua bagian besar yaitu lemak dan lilin, yang mana mengandung ikatan ester dan dapat dihidrolisis.
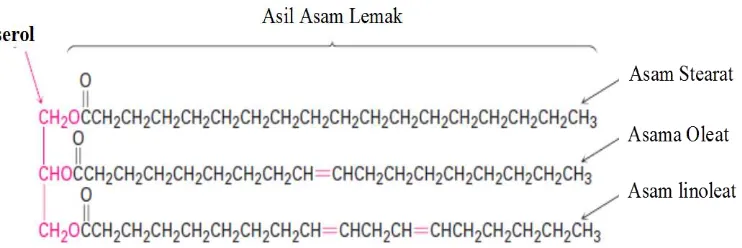
Lemak hewani dan minyak nabati terjadi secara alami dalam bentuk lipid. Meskipun keduanya berbeda, lemak hewani adalah padat dan minyak nabati adalah cair. Lemak dan minyak adalah trigliserida atau triasilgliserol atau triester dari gliserol dengan tiga buah karboksilat rantai panjang yang dinamakan asam lemak (McMurry, J. 2010)
Gambar 2.1. Struktur Trigliserida
2.3 Asam Lemak
Asam lemak tidak jenuh dapat dioksidasi menjadi beberapa jenis oksidator seperti HNO3, KmnO4, Ozon, dan senyawa peroksida. Asam oleat dapat dioksidasi menjadi azelat dan asam pelargonat sebagai hasil samping
CH3(CH2)7CH=CH(CH2)7COOH
O
HOOC(CH2)7COOH + CH3(CH2)7COOH
Asam oleat juga dapat mengalami reaksi hidroksilasi membentuk senyawa dialkohol (diol). (McMurry, J, 2012)
2.4 Esterifikasi
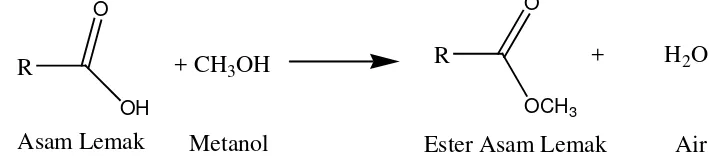
Esterifikasi adalah tahap konversi dari asam lemak bebas menjadi ester. Dengan cara mereaksikan minyak atau lemak dengan alkohol. Katalis-katalis yang cocok adalah asam kuat, dan karena ini, asam sulfat, asam sulfonat organik atau resin penukar kation asam kuat merupakan katalis-katalis yang biasa terpilih dalam praktek industrial (Soerawidjaja, 2005). Untuk mendorong agar reaksi bisa berlangsung ke konversi yang sempurna pada temperatur rendah (misalnya paling tinggi 120° C), reaktan metanol harus ditambahkan dalam jumlah yang sangat berlebih (biasanya lebih besar dari 10 kali perhitungan stoikiometrik) dan reaksi harus bebas air. Melalui kombinasi-kombinasi yang tepat dari kondisi-kondisi reaksi dan metode penyingkiran air, konversi sempurna asam-asam lemak ke ester metilnya dapat dituntaskan dalam waktu 1 sampai beberapa jam. Reaksi esterifikasi dari asam lemak menjadi metil ester adalah :
Asam Lemak Metanol Ester Asam Lemak
+ H2O
Air
Gambar. 2.2. Reaksi Esterifikasi Asam Lemak Secara Umum
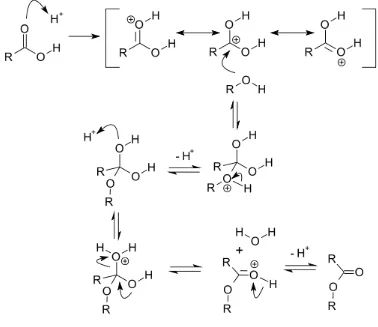
transesterfikasi. Namun sebelum produk esterifikasi diumpankan ke tahap transesterifikasi, air dan bagian terbesar katalis asam yang dikandungnya harus disingkirkan terlebih dahulu.
Gambar. 2.3 Mekanisme reaksi esterifikasi asam lemak dengan katalis asam Faktor-faktor yang mempengaruhi jalannya reaksi esterifikasi antara lain : 1. Suhu
Kecepatan reaksi dipengaruhi oleh suhu reaksi. Kecepatan reaksi akan meningkat sejalan dengan kenaikan suhu. Semakin tinggi suhu, berarti semakin banyak energi yang dapat digunakan oleh reaktan untuk mencapai energi aktivasi. Ini akan menyebabkan tumbukan terjadi lebih sering diantara molekul-molekul reaktan untuk kemudian melakukan reaksi sehingga kecepatan reaksi meningkat (Berrios, M. 2007)
2. Waktu reaksi
Namun jika kesetimbangan telah tercapai, tambahan waktu reaksi tidak akan mempengaruhi reaksi.
3. Katalis
Katalis berfungsi untuk mempercepat laju reaksi dengan menurunkan energi aktivasi reaksi namun tidak menggeser letak kesetimbangan. Tanpa katalis, reaksi transesterifikasi baru dapat berjalan pada suhu sekitar 250°C. Penambahan katalis bertujuan untuk mempercepat reaksi dan menurunkan kondisi operasi. Katalis yang dapat digunakan adalah katalis asam, basa, ataupun penukar ion. Dengan katalis basa reaksi dapat berjalan pada suhu kamar, sedangkan katalis asam pada umumnya memerlukan suhu reaksi diatas 100ºC.
4. Pengadukan
Pada reaksi transesterifikasi, reaktan-reaktan awalnya membentuk sistem cairan dua fasa. Reaksi dikendalikan oleh difusi diantara fase-fase yang berlangsung lambat. Seiring dengan terbentuknya metil ester, ia bertindak sebagai pelarut tunggal yang dipakai bersama oleh reaktan-reaktan dan sistem dengan fase tunggal pun terbentuk. Dampak pengadukan ini sangat signifikan selama reaksi sebagaimana sistem tunggal terbentuk, maka pengadukan menjadi tidak lagi mempunyai pengaruh yang signifikan. Pengadukan dilakukan dengan tujuan untuk mendapatkan campuran reaksi yang bagus. Pengadukan yang tepat akan mengurangi hambatan antar massa. Untuk reaksi heterogen, ini akan menyebabkan lebih banyak reaktan mencapai tahap reaksi.
2.5. 2-Butanol
2-butanol adalah salah satu jenis alkohol sekunder dengan rumus
2CH3, dimana alkohol ini sangat mudah terbakar, tak berwarna.
OH OH
(R)-(-)-2-butanol (S)-(-)-2-butanol
Gambar2.4 Bentuk isomer dari 2-butanol
2-butanol dapat terdehidrasi dengan adanya asam kuat membentuk alkena. Sifat kimia dan fisika 2-butanol dapat dilihat pada table 2.1 dibawah.
Table 2.1 Sifat Kimia dan Fisika 2-butanol
2.6 Asam Palmitat
Salah sat
heksadekanoat. Tumbuh-tumbuhan dari famili
nucifera) da
ini. Minyak kelapa bahkan mengandung hampir semuanya palmitat (92%). Minyak sawit mengandung sekitar 50% palmitat. Produk hewani juga banyak mengandung asam lemak ini (dari mentega, keju, susu, dan juga daging).
Sifat Fisika Dan Kimia
C4H10O
Kelarutan Dalam Air 290 g/L
1.67 kPa (20 °C)
nD) 1.3978 (20 °C)
Asam palmitat adal (CH3(CH2)14COOH). Pada suhu ruang, asam palmitat berwujud padat berwarna putih. Titik leburnya 63,1 °C.
Asam palmitat adalah produk awal dalam proses biosintesis asam lemak (lihat
artikel
berlangsung lebih lanjut.
Dalam industri, asam palmitat banyak dimanfaatkan dalam bidang kosmetika dan pewarnaan. Dari segi gizi, asam palmitat merupakan sumber kalori penting namun memiliki daya antioksidasi yang rendah (Rogers, B. 2001). Sifat Kimia dan fisika asam palmitat dapat dilihat pada Tabel 2.2 dibawah.
Tabel 2.2 Sifat Kimia dan Fisika Asam Palmitat
C16H32O2
256.42 g/mol
Penampilan Kristal putih
0.853 g/cm
Aerosil merupakan silikon dioksida murni yang diketahui dalam jumlah kecil dapat menyerap air yang cukup besar. Aerosil diperoleh melalui penguapan silikon tetraklorida yang dioksidasi dengan nyala suhu tinggi menggunakan H2 dan O2.
farmasi sebagai pengontrol reologi, cat, mantel, lem, sealant, plastik, film, serat, keramik dan pendukung katalisator (Wikipedia, 2011). Luas permukaan aerosil bervariasi yaitu dari 50 hingga 400 m2/g. Permukaan aerosil bersifat hidrofilik dan terus menyerap air (Pevzner,1973).
Aerosil juga telah digunakan pada reaksi karbonilasi sebanyak 3% dari jumlah metil oleat dan dilaporkan dapat meningkatkan hasil reaksi karbonilasi metil oleat dari < 20% menjadi 52,1% (Saragih, 2009).
2.8 Katalis
Katalis dapat mempercepat sebuah reaksi kimia, dengan cara membentuk ikatan dengan molekul reaktan dan memungkinkan bereaksi membentuk suatu produk yang kemudian dilepaskannya sedemikian rupa sehingga tersedia untuk reaksi selanjutnya.
Katalis adalah kunci utama trnsformasi kimia dalam industri. Kira-kira 85-90% produk kimia industri dibuat dengan proses katalitik (Chorkendorff, J.W dan Niemantsverdriet, 2003). Katalis dibagi menjadi dua yaitu katalis homogen dan katalis heterogen. Katalis homogen adalah katalis yang sefasa dengan pereaksi dalam reaksi yang dikatalisisnya. Sedangkan katalis heterogen adalh katalis yang ada dalam fasa yang berbeda dengan pereaksi dalam reaksi yang dikatalisisnya (Syukri, S. 1999) 2.8.1 Katalis Homogen
Cara kerja katalis homogeny umumnya melibatkan pembentukan senyawa kompleks antara yang bersifat tidak stabil dalam tahap-tahap reaksi. Katalis dengan reaktan membentuk kompleks antara yang mengakibatkan reaktan dalam kompleks menjadi aktif membentuk produk baru dan disertai dengan pelepasan katalisatornya (sugiyarto, K.H. 2003)
mengikuti kinetika reaksi katalitik (Crabtree, R. H, 2005), selain itu katalis mudah terdispersi secara efektif sehingga semua molekul katalis dapat berinteraksi dengan reaktan. Kerugian dari katalis homogen adalah sulit memisahkan katalis dari produk dan biayanya mahal. Selain itu dapat terjadi korosi dan hilangnya katalis pada perolehan kembali katalis yang juga menyebabkan pencemaran lingkungan (Gates, B.C, dkk. 1979)
2.8.2 Katalis Heterogen
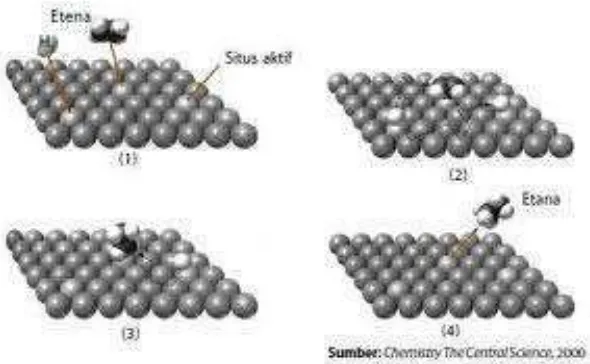
Pada katalis heterogen, umumnya berupa padatan. Proses katalisis berlangsung pada permukaan katalis dan memerlukan tekanan dan temperatur yang tinggi. Keuntungan dari katalis heterogen adalah mudah dipisahkan dari produk yang terlarut dalam medium reaksi. (Sleight, H. W, 1983). Contoh reaksi dari C2H2 + 2H2 –> C2H6 dengan menggunakan katalis heterogen Pd/Al2O3 telihat secara sederhana pada gambar
2.8.3 Katalis Dengan Gugus Asam Sulfonat
Katalis heterogen dengan gugus asam sulfonat
Seperti sudah diketahui bahwa katalis heterogen dapat mengatasi beberapa kelemahan yang diberikan oleh katalis homogen. Dengan adanya gugus asam sulfonat pada katalis heterogen akan meningkatkan nilai lebih dari pada katalis tersebut, antara lain memiliki kestabilan yang sangat tinggi dan dapat dengan mudah diregenerasi setelah proses reaksi berlangsung.
Resin penolik yang tersulfonasi telah digunakan untuk reaksi esterifikasi asam asetat dengan propanol dan reaksi aldol asimetrik (Muylaert, I. 2013). Senyawa mesopori carbon-coated yang tersulfonasi juga dapat digunakan untuk reaksi asetilasi (Fang, L. 2013., Canck, E.D. 2013).
2.8.4 Katalis Berbasis Ramah Lingkungan
BAB 3
METODE PENELITIAN
3.1. Alat
- Gelas Beaker 250 ml Pyrex
- Gelas Ukur 25 ml Pyrex
- Corong
- Termometer 360oC Boeco
- Autoclave
- Neraca Analitis Mettler PM 400
- Botol Akuades - Kertas Saring
- Hotplate stirer Cimarec
- Lemari Pendingin Gea
3.2. Bahan
- Asam Palmitat p.a E’Merck
- N-heksan p.a E’Merck
- 2-butanol p.a E’Merck
- Katalis
3.3 Prosedur Penelitian
3.4. Bagan Penelitian
0,0194 mol asam palmitat
dimasukkan ke dalam autoclave
ditambahkan 0,2 g katalis
ditambahkan 0,39 mol 2-butanol
dimasukkan pengaduk magnet
dipanaskan pada suhu 100oC selama 10 jam sambil diaduk
karakterisasi
didinginkan pada suhu -15oC selama 3 jam disaring dalam keadaan dingin
sisa asam palmitat
filtrat
dilarutkan dengan 20 ml n-heksan
fraksi terlarut
fraksi tidak terlarut
ditambah NaSO4 anhidrat disaring
BAB 4
HASIL DAN PEMBAHASAN
4.1 Reaksi Esterifikasi Asam Palmitat dengan 2-butanol
Reaksi antara asam palmitat dengan 2-butanol dengan bantuan katalis 1,2-dimetil-1,1,2,2-tetrafenil disilan sulfonat menghasilkan 2-butil palmitat seperti terlihat pada gambar 4.1 :
Gambar 4.1 Reaksi Asam Plamitat dengan 2-butanol Menggunakan Katalis Disilan Sulfonat
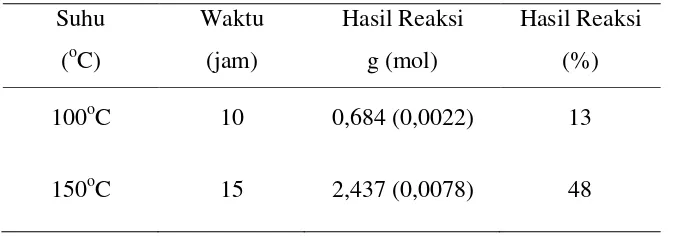
Reaksi esterifikasi ini dilakukan sebanyak 2 kali yaitu pada suhu 100oC selama 10 jam dan pada suhu 150oC selama 15 jam dan hasilnya dapat dilihat pada Tabel 4.1 dibawah ini :
Tabel 4.1 Hasil Reaksi Esterifikasi Asam Palmitat 0,0194 mol dengan 2-butanol 0,399 mol dengan variasi waktu dan suhu reaksi
Suhu
hidrokarbon rantai panjang dan didukung juga oleh pita serapan pada panjang gelombang 721,64 cm-1 yang merupakan vibrasi tekukan rocking dari C-H rantai panjang. Dan υC=O pada panjang gelombang 1743 cm-1 diberikan vibrasi regangan gugus C=O dari ester , dan pita serapan ini telah bergeser sebesar 44,5 cm-1dari υC=O asam lemak. Dan υC-O-C pada 1377,57 cm-1 dan 1176,65 cm-1 diberikan oleh vibrasi regangan gugus C-O yang berasal dari ester asam lemak. Hal ini mengindikasikan bahwa reaksi esterifikasi antara asam palmitat dengan 2-butanol menggunakan katalis asam 1,2-dimetil-1,1,2,2-tetrafenil disilan sulfonat telah berlangsung dan menghasilkan senyawa ester.
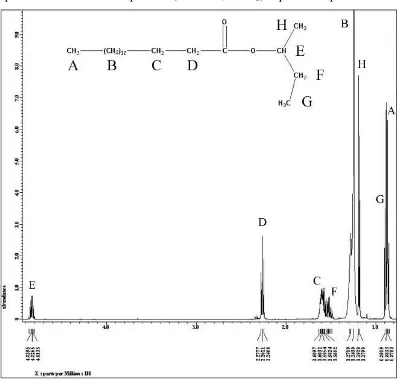
Spektrum 1H-NMR 2-butil palmitat (500 MHz, CDCl3) dapat dilihat pada Gambar 4.3.
Gambar 4.4 Expansi 1 Spektrum 1H-NMR dari 2-butil palmitat dari δ 0,84 ppm hingga δ 1,19 ppm (CDCl3)
Gambar. 4.5 perkiraan saling tumpang tindih 2 puncak triplet A dan G
Gambar 4.6 Expansi 2 Spektrum 1H-NMR dari 2-butil palmitat dari δ 1,2 ppm hingga δ 1,6 ppm (CDCl3)
Gambar 4.7 Expansi 1 Spektrum 1H-NMR dari 2-butil palmitat dari δ 2,2 ppm hingga δ 4,9 ppm (CDCl3)
BAB 5
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Dari hasil penelitian dapat disimpulkan bahwa reaksi esterifikasi asam palmitat dengan 2-butanol dengan menggunakan katalis 1,2-dimetil-1,1,2,2-tetrafenil disilan sulfonat menghasilkan produk ester asam lemak yaitu 2-butil palmitat, dan reaksi yang berlangsung dipengaruhi oleh suhu dan waktu reaksi. Hal ini dapat dilihat dari peningkatan hasil reaksi dengan peningkatan suhu dan waktu reaksi. Dan katalis yang telah digunakan masih dapat diperoleh dari campuran hasil reaksi.
5.2. Saran
DAFTAR PUSTAKA
Alonso, M. L., Christian, V. M., Maynor, A. C., Julio, M. S. 2006. Kinetics of the Fischer esterification of palm fatty acids with isopropanol and butyl-cellosolve. Ciencia y Tecnología, 24(2): 175-181, 2006
Boey, P. L., Ganesana, S., Maniamb, G. P. 2012. A new heterogeneous acid catalyst system for esterification of free fatty acid into methyl esters. Applied Catalyst A : General, 433-434 : 12-17
Clark, J.H. 2002. Handbook Of Green Chemistry And Technology. Newyork : Blackwell Science Ltd
Clark, J.H., 2002. Solid acids for green chemistry. Accounts of Chemical Research 35, 791–797.
Crabtree, R. 2005, The Organomettalic Chemistry of The Transition Metal. Fourth Edition. New Jersey : Willey-Interface
Chorkendorf, I dan Niemantsverdriet, J.W. 2003.Concept of Modern Katalysis and Kinetics. Weinheim : Willey-VCH GmbH & Co
Corma, A., Garcia, H. 2008.Top Catal. 8:31
Demirbas, A. 2009. Progress and recent trends in biodiesel fuel. Energy Conversion and management.
Fang, L., Zhang, K., Chen, L., Wu, P. 2013. Carbon-Coated Mesoporous Silica Functionalized With Sulfonic Acid Group and Its Application to acetalization. Chinese Journal of Catalyst 34. 932-941
Fang, L., Zhang, K., Chen, L., Wu, P. 2010. Sci China Chem, 53 : 1481
Freedman, B., Pryde.E.H., Mounts. T.L., 1984, Variables Affecting the Yields of Fatty Esters from Transesterfied Vegetable Oils.
Gates, B.C,;Katzer,J.R.;Schuit.G.C.A. 1979. Chemistry Of catalytic processes. New York : McGraw-Hill Company.
Kang, S., Ye, J., Chang, J. 2013.Recents Advance in Carbon-Based Sulfonated Catalyst : Preparation and Appliucation. International Review of Chemical Engineering.5:2
Kouzu, M., Nakagaito, A., Hidaka, J. S. 2010. Pre-Esterification Of FFA In Plant Oil Transesterified Into Biodiesel With The Help of Solid Acid Catalysis of Sulfonated Cation-Exchange Resin. Journal of Applied Catalysis A : General, 405 : 36-44
Lou, W.Y., Zong, M.H., Duan, Z.Q.2008.Effecient production of Biodiesel From High Free Fatty Acid-Containing Waste Oils Using Various Carbohidrated-derived Solid Acid Catalyst. Bioresource Technology 99. 8752-8758
McMurry, J. 2012. Organic Chemistry. Eight Edition. Canada : Brooks/ Cole Learning
Muylaert, L., Verberckmoes, A., Spileers, J., Demuynck, A., Peng, L. 2013.Synthesis of Sulfonated Mesoporous Phenolic Resin and Their Application in Esterification and Assymetric Aldol Reaction. Material Chemistry and Physics 138. 131-139
Perry, R.H. and Green, D.W., 1984, Perry’s Chemical Engineering Handbook, 6th ed, Mc Graw Hill Book Company, Inc, New York.
Rajendran, A., Karthikeyan, C. 2011.Silica Sulphuric Acid Catalized Fischer Esterification Reaction Under Solventless Condition : A novel Green Chemical Reaction. American Chemical Science Journal-1. 28-36
Richtler, H.J. and Knault, J. 1984. Challenges To A Mature Industry, Marketing Economics of Oleochemicals in Western Europe. J.am.oil.chem.soc.vol.61.
Sleight, H. W. 1983. Catalyst Design And Section, Applied, Industry Catalyst. New York : Academic Press
Sidabutar, A. 2011. Penggunaan Polistirena Sulfonat Sebagai Katalis Transesterifikasi Minyak Jarak Pagar (Jatropha Curcas) Berkadar Asam Lemak Bebas Tinggi. Skripsi. Medan : Departemen Kimia FMIPA USU.
Singh, M., Singh, S., Singh, R.S .,Chisti, Y., Banerjee, U.T. 2007. Transesterification of primary and secondary alcohols using Pseudomonas aeruginosa lipase. Bioresource Technology 99. 2116–2120
Soerawidjaja, Tatang H., 2005, Minyak-lemak dan produk-produk kimia lain dari kelapa, Handout kuliah Proses Industri Kimia, Program Studi Teknik Kimia : Institut Teknologi Bandung.
Syukri, S. 1999. Kimia Dasar. Jilid I. Bandung : Penerbit ITB
Trimm, D.L. 2001. The Regeneration Or Disposalof Deactivated Heterogeneous Catalyst. 153-160
Ullman’s. 2011. Encyclopedia of Industryal Chemistry. 7th Edition. New York : Willey-VCH. 700-7005
Weerachanchai, P., Tangshatitkuilchai, C. Tangshatitkuilchai, M. 2012. Effect of reaction condition on the catalytic esterification of bio-oil. Korean Journal of chemical enggenering, 29(2) : 182-189
Xin, N., Li, J., Yang, L., Lu, X., Xu, L. 2013. Catalytic Synthesis of Sec-Butyl Acetate on Sulfoacid Resin. International Journal of a advancements in research and technology, volume 2. 1-5.
Yu, H., Jin, Z., Li, F., Peng, H. 2008. Synthesis And Characterization Of Sulfonated Single-Walled Carbon Nanotube And Their Performance As Solid Acid Catalyst. Journal Solid State Chem, 181 : 432-438