PERTUMBUHAN DAN PRODUKSI KEDELAI (Glycine max (L.) Merrill)
TERHADAP PEMBERIAN FUNGI MIKORIZA ARBUSKULAR (FMA)
DAN KONSORSIUM MIKROBA
SKRIPSI
Oleh:
DINI OKTAVIANI 090301175
PROGRAM STUDI AGROEKOTEKNOLOGI FAKULTAS PERTANIAN
UNIVERSITAS SUMATERA UTARA MEDAN
PERTUMBUHAN DAN PRODUKSI KEDELAI (Glycine max (L.) Merrill)
TERHADAP PEMBERIAN FUNGI MIKORIZA ARBUSKULAR (FMA)
DAN KONSORSIUM MIKROBA
SKRIPSI
Oleh:
DINI OKTAVIANI
090301175/ AGROEKOTEKONOLOGI
Skripsi sebagai salah satu syarat untuk dapat memperoleh gelar sarjana di Fakultas Pertanian
Universitas Sumatera Utara
PROGRAM STUDI AGROEKOTEKNOLOGI FAKULTAS PERTANIAN
UNIVERSITAS SUMATERA UTARA MEDAN
Judul Penelitian : Pertumbuhan dan Produksi Kedelai (Glycine max (L.) Merrill) Terhadap Pemberian Fungi Mikoriza Arbuskular (FMA) dan Konsorsium Mikroba
Nama : Dini Oktaviani
Nim : 090301175
Program Studi : Agroekoteknologi
Minat : Budidaya Pertanian dan Perkebunan
Disetujui Oleh :
(Ir.Yaya Hasanah, MSi) (Ir. Asil Barus, MS)
Ketua Pembimbing Anggota Pembimbing
NIP. 19690110 200502 2 001 NIP. 19540424 198203 1 005
Diketahui Oleh :
(Ir. T Sabrina, M.Agr.Sc, Ph.D) Ketua Departemen NIP. 19640620 0199803 2 001
ABSTRAK
DINI OKTAVIANI: Pertumbuhan dan Produksi Kedelai terhadap Pemberian Fungi Mikoriza Arbuskular (FMA) dan Konsorsium Mikroba dibimbing oleh YAYA HASANAH dan ASIL BARUS.
Penggunaan pupuk kimia pada budidaya kedelai semakin tinggi. Untuk menekan penggunaan pupuk kimia secara terus menerus, pemanfaatan pupuk hayati pada budidaya kedelai dapat meningkatkan pertumbuhan dan produksi kedelai. Penelitian dilaksanakan di Jalan Setiabudi Kelurahan Simpang Selayang Kecamatan Medan Tuntungan pada April-Juli 2013, menggunakan rancangan acak kelompok faktorial dengan dua faktor yaitu pemberian FMA (0, 20, 40 g/tanaman) dan pemberian konsorsium mikroba (0, 5, 10, 15 g/kg benih). Parameter yang diamati adalah tinggi tanaman, diameter batang, bobot kering tajuk, bobot kering akar, kehijauan daun, total luas daun, derajat infeksi FMA, jumlah bintil akar, jumlah bintil akar efektif,bobot bintil akar, serapan hara N tajuk, serapan hara P tajuk, jumlah cabang produktif, jumlah polong per tanaman, jumlah polong berisi per tanaman, bobot kering biji per tanaman, bobot kering 100 biji, bobot kering biji per plot.
Hasil penelitian menunjukkan pemberian FMA meningkatkan tinggi tanaman, diameter batang, jumlah bintil akar, jumlah bintil akar efektif, derajat infeksi, jumlah cabang produktif, jumlah polong berisi per tanaman, bobot kering biji per tanaman, bobot kering 100 biji dan bobot biji per plot. Pemberian konsorsium mikroba meningkatkan tinggi tanaman, diameter batang, jumlah bintil akar, jumlah bintil akar efektif, kehijauan daun, total luas daun, derajat infeksi, jumlah cabang produktif, jumlah plong per tanaman, jumlah polong berisi per tanaman, bobot kering biji per tanaman dan bobot biji per plot. Interaksi kedua perlakuan meningkatkan bobot bintil akar dan jumlah bintil akar efektif.
ABSTRACT
DINI OKTAVIANI: Growth and Yield of Soybean to Addition of Arbuscular Mycorrhiza Fungi (AMF) and Addition of microbe Concortium, supervised by YAYA HASANAH and ASIL BARUS.
Using of chemical fertilizer is increasing for soybean plantation. The action to compress that situation, utilization of biological fertilizer aims to increase growth and yield of soybean. This research had been conducted at Jalan Setiabudi Kelurahan Simpang Selayang Kecamatan Medan Tuntungan on April-July 2013, using a factorial randomized block design with two factors. The factors were addition of AMF (0, 20, 40 g per plant) and addition of microbe concortium (0,5,10,15 g per kg of seed). Parameters observed were plant height, stem diameter, weight of dry shoot, weight of dry root, leaf greenness level, total of leaf area, analysis substance N of shoot, analysis substance P of shoot, infection degree AMF, number of nodules, number of effective nodules, weight of nodules, number of productive branches, number of pods per plant, number of filled pods per plant, dry seeds weight per plant, 100 seeds dry weight, and dry seeds weight per plot.
The result showed that addition of AMF increase plant height, stem diameter, infection degree AMF, number of nodules, number of effective nodules, number of productive branches, number of filled pods per plant, dry seeds weight per plant, 100 seeds dry weight, and dry seeds weight per plot. The addition of microbe concortium increase plant height, stem diameter, leaf greenness level, total of leaf area, infection degree AMF, number of nodules, number of effective nodules, number of productive branches, number of pods per plant, number of filled pods per plant, dry seeds weight per plant, and dry seeds weight per plot. Interaction both of treatment increase weight of nodules and number of effective nodules.
RIWAYAT HIDUP
Dini Oktaviani, lahir pada tanggal 25 Oktober 1991 di Bandung dari ibunda
Hj. Halimatussakdiyah dan ayahanda Alm.H.Ir.M.Udin, MT. Penulis merupakan
anak pertama dari tiga bersaudara.
Pendidikan formal yang pernah diperoleh penulis antara lain : tahun
1997-2003 menempuh pendidikan dasar di SD Percobaan Negeri; tahun 1997-2003-2006
menempuh pendidikan di SMP Negeri 1 Medan; tahun 2006-2009 menempuh
pendidikan di SMA Negeri 15 Medan dan terdaftar sebagai mahasiswa Fakultas
Pertanian Universitas Sumatera Utara Medan pada tahun 2009 melalui Seleksi
Penerimaan Mahasiswa Baru (SPMB). Penulis memilih minat Budidaya Pertanian
dan Perkebunan, Program Studi Agroekteknologi. Selama perkuliahan penulis
mendapatkan beasiswa peningkatan prestasi akademik (PPA) pada tahun 2010
sampai 2012.
Selama mengikuti perkuliahan, penulis aktif sebagai anggota Himpunan
Mahasiswa Agroekoteknologi (Himagrotek), sebagai asisten praktikum di
Laboratorium Fisiologi Tumbuhan (2010-2013) dan Laboratorium Teknologi
Budidaya Tanaman Pangan (2012-2013).
Penulis melaksanakan praktek kerja lapangan (PKL) di
PT. PD Paya Pinang Group, Laut Tador, Tebing Tinggi dari tanggal 9 Juli sampai 4
KATA PENGANTAR
Puji dan syukur penulis panjatkan kehadirat Allah SWT, atas rahmat dan
hidayah-Nya sehingga penulis dapat menyelesaikan skripsi yang berjudul
“Pertumbuhan dan Produksi Kedelai (Glycine max (L.) Merrill) Terhadap
Pemberian Fungi Mikoriza Arbuskular (FMA) dan Konsorsium Mikroba ”.
Penulisan skripsi ini merupakan salah satu syarat untuk mendapatkan gelar sarjana
di Fakultas Pertanian Program Studi Agroekoteknologi Universitas Sumatera Utara,
Medan.
Pada kesempatan ini, penulis menghanturkan terima kasih yang
sebesar-besarnya kepada kedua orang tua penulis yang telah berjuang membesarkan,
merawat, dan mendidik penulis selama ini. Penulis juga mengucapkan terima kasih
kepada Ibu Ir. Yaya Hasanah, MSi selaku ketua komisi pembimbing dan Bapak Ir.
Asil Barus, MS selaku anggota komisi pembimbing yang telah membimbing dan
memberikan berbagai saran yang berharga kepada penulis mulai dari penetapan
judul, melakukan penelitian sampai ujian akhir mengelar sarjana. Disamping itu,
penulis juga mengucapkan terima kasih kepada semua staf pengajar dan pegawai di
Program Studi Agroekoteknologi, semua teman-teman angkatan 2009 serta
adik-adik angkatan 2012 yang telah banyak membantu penulis dalam menyelesaikan
skripsi ini.
Semoga hasil skripsi ini bermanfaat bagi budidaya kedelai serta bermanfaat
bagi pihak yang membutuhkan.
Medan, November 2013
DAFTAR ISI
Fungi Mikoriza Arbuskular (FMA) ... 7
Konsorsium Mikroba ... 9
BAHAN DAN METODE PENELITIAN Tempat dan Waktu Penelitian ... 14
Penanaman Jagung sebagai Tanaman Inang ... 17
Pemberian Pupuk Organik Cair ... 17
Pemeliharaan ... 17
Panen Inokulan FMA ... 17
Penanaman Kedelai ... 18
Aplikasi FMA ... 18
Aplikasi Konsorsium mikroba ... 18
Penanaman Benih ... 18
Pemupukan N dan K ... 19
Penjarangan ... 19
Pemeliharaan Tanaman Penyiraman ... 19
Penyiangan ... 19
Pengendalian Hama dan Penyakit ... 19
Pengamatan Parameter ... 20
Tinggi tanaman (cm) ... 20
Diameter batang (mm) ... 20
Bobot kering akar (g) ... 20
Bobot kering tajuk(g) ... 20
Jumlah bintil akar (bintil) ... 20
Jumlah bintil akar efektif (bintil) ... 21
Bobot bintil akar (g) ... 21
Kehijauan daun (SPAD) ... 21
Total luas daun (cm²) ... 21
Derajat infeksi FMA(%) ... 21
Kandungan N tajuk tanaman ... 21
Kandungan P tajuk tanaman... 22
Jumlah cabang produktif (cabang) ... 22
Jumlah polong per tanaman sampel (polong) ... 22
DAFTAR PUSTAKA ... 65
DAFTAR TABEL
No. Hal.
1. Rataan tinggi tanaman (cm) 2-6 MST pada perlakuan pemberian
Fungi Mikoriza Arbuskular (FMA) dan pemberian konsorsium mikroba ... 24
2. Rataan diameter batang (mm) pada perlakuan pemberian Fungi
Mikoriza Arbuskular (FMA) dan pemberian konsorsium mikroba ... 28
3. Rataan bobot kering akar (g) pada perlakuan pemberian Fungi
Mikoriza Arbuskular (FMA) dan pemberian konsorsium mikroba ... 30
4. Rataan bobot kering tajuk (g) pada perlakuan pemberian Fungi
Mikoriza Arbuskular (FMA) dan pemberian konsorsium mikroba ... 31
5. Rataan jumlah bintil akar (bintil) pada perlakuan pemberian Fungi
Mikoriza Arbuskular (FMA) dan pemberian konsorsium mikroba ... 32
6. Rataan bobot bintil akar (g) pada perlakuan pemberian Fungi
Mikoriza Arbuskular (FMA) dan pemberian konsorsium mikroba ... 34
7. Rataan jumlah bintil akar efektif (bintil) pada perlakuan pemberian
Fungi Mikoriza Arbuskular (FMA) dan pemberian konsorsium mikroba ... 35
8. Rataan kehijauan daun pada perlakuan pemberian Fungi Mikoriza
Arbuskular (FMA) dan pemberian konsorsium mikroba ... 37
9. Rataan total luas daun (cm²) pada perlakuan pemberian Fungi
Mikoriza Arbuskular (FMA) dan pemberian konsorsium mikroba ... 38
10. Rataan derajat infeksi FMA (%)pada perlakuan pemberian Fungi
Mikoriza Arbuskular (FMA) dan pemberian konsorsium mikroba ... 39
11. Rataan kandungan N tajuk tanaman (%) pada perlakuan pemberian
Fungi Mikoriza Arbuskular (FMA) dan pemberian konsorsium mikroba ... 41
12. Rataan kandungan P tajuk tanaman (%) pada perlakuan pemberian
Fungi Mikoriza Arbuskular (FMA) dan pemberian konsorsium mikroba ... 42
13. Rataan jumlah cabang produktif (cabang) pada perlakuan pemberian
14. Rataan jumlah polong per tanaman sampel (polong) pada perlakuan pemberian Fungi Mikoriza Arbuskular (FMA) dan pemberian konsorsium mikroba ... 45
15. Rataan jumlah polong berisi per tanaman sampel (polong) pada
perlakuan pemberian Fungi Mikoriza Arbuskular (FMA) dan pemberian konsorsium mikroba ... 46
16. Rataan bobot kering biji per tanaman sampel (g) pada perlakuan
pemberian Fungi Mikoriza Arbuskular (FMA) dan pemberian konsorsium mikroba ... 48
17. Rataan bobot kering 100 biji (g) pada perlakuan pemberian Fungi
Mikoriza Arbuskular (FMA) dan pemberian konsorsium mikroba ... 50
18. Rataan bobot kering biji per plot (g) pada perlakuan pemberian Fungi
DAFTAR GAMBAR
No. Hal.
1. Grafik hubungan tinggi tanaman 2 MST dengan interaksi pemberian
FMA dan konsorsium mikroba ... 26
2. Grafik hubungan tinggi tanaman 6 MST dengan pemberian FMA ... 27
3. Grafik hubungan tinggi tanaman 6 MST dengan pemberian
konsorsium mikroba ... 27
4. Grafik hubungan diameter batang dengan pemberian FMA ... 29
5. Grafik hubungan diameter batang dengan pemberian konsorsium
mikroba ... 29
6. Grafik hubungan jumlah bintil akar dengan pemberian FMA ... 32
7. Grafik hubungan jumlah bintil akar dengan pemberian konsorsium
mikroba ... 33
8. Grafik hubungan bobot bintil akar dengan interaksi pemberian FMA
dan pemberian konsorsium mikroba ... 34
9. Grafik hubungan jumlah bintil akar efektif dengan interaksi
pemberian FMA dan konsorsium mikroba ... 36
10. Grafik hubungan kehijauan daun dengan pemberian konsorsium
mikroba ... 37
11. Grafik hubungan total luas daun dengan pemberian konsorsium
mikroba ... 38
12. Grafik hubungan derajat infeksi dengan pemberian FMA ... 40
13. Grafik hubungan derajat infeksi dengan pemberian konsorsium
mikroba ... 40
14. Grafik hubungan jumlah cabang produktif dengan pemberian FMA ... 43
15. Grafik hubungan jumlah cabang produktif dengan pemberian
konsorsium mikroba ... 44
16. Grafik hubungan jumlah polong per tanaman sampel dengan
17. Grafik hubungan jumlah polong berisi per tanaman sampel dengan pemberian FMA ... 47
18. Grafik hubungan jumlah polong berisi per tanaman dengan pemberian
konsorsium mikroba ... 47
19. Grafik hubungan bobot kering biji per tanaman sampel dengan
pemberian FMA ... 49
20. Grafik hubungan bobot kering biji per tanaman sampel dengan
pemberian konsorsium mikroba ... 49
21. Grafik hubungan bobot kering 100 biji dengan pemberian FMA ... 51
22. Grafik hubungan bobot kering biji per plot dengan pemberian FMA ... 52
23. Grafik hubungan bobot kering biji per plot dengan pemberian
DAFTAR LAMPIRAN
No. Hal.
1. Deskripsi tanaman kedelai varietas Grobogan ... 69
2. Bagan penanaman pada plot... 70
3. Bagan plot penelitian ... 71
4. Jadwal kegiatan pelaksanaan penelitian ... 72
5. Teknik pewarnaan untuk menghitung derajat infeksi FMA (%) ... 73
6. Data pengamatan tinggi tanaman 2 MST (cm) ... 74
7. Sidik ragam tinggi tanaman 2 MST ... 74
8. Data pengamatan tinggi tanaman 3 MST (cm) ... 75
9. Sidik ragam tinggi tanaman 3 MST ... 75
10. Data pengamatan tinggi tanaman 4 MST (cm) ... 76
11. Sidik ragam tinggi tanaman 4 MST ... 76
12. Data pengamatan tinggi tanaman 5 MST (cm) ... 77
13. Sidik ragam tinggi tanaman 5 MST ... 77
14. Data pengamatan tinggi tanaman 6 MST (cm) ... 78
15. Sidik ragam tinggi tanaman 6 MST ... 78
16. Data pengamatan diameter batang (mm) ... 79
17. Sidik ragam diameter batang ... 79
18. Data pengamatan bobot kering akar (g) ... 80
19. Sidik ragam bobot kering akar ... 80
20. Data pengamatan bobot kering tajuk (g) ... 81
21. Sidik ragam bobot kering tajuk ... 81
23. Sidik ragam jumlah bintil akar ... 82
24. Data pengamatan bobot bintil akar (g) ... 83
25. Sidik ragam bobot bintil akar ... 83
26. Data pengamatan jumlah bintil akar efektif (bintil) ... 84
27. Sidik ragam jumlah bintil akar efektif ... 84
28. Data pengamatan kehijauan daun... 85
29. Sidik ragam kehijauan daun ... 85
30. Data pengamatan total luas daun (cm2) ... 86
31. Sidik ragam total luas daun ... 86
32. Data pengamatan derajat infeksi FMA (%) ... 87
33. Sidik ragam derajat infeksi FMA ... 87
34. Data pengamatan jumlah cabang produktif (cabang) ... 88
35. Sidik ragam jumlah cabang produktif ... 88
36. Data pengamatan jumlah polong per tanaman sampel ... 89
37. Sidik ragam jumlah polong per tanaman sampel ... 89
38. Data pengamatan jumlah polong berisi per tanaman sampel ... 90
39. Sidik ragam jumlah polong berisi per tanaman sampel ... 90
40. Data pengamatan bobot kering biji per tanaman sampel ... 91
41. Sidik ragam bobot kering biji per tanaman sampel ... 91
42. Data pengamatan bobot kering 100 biji ... 92
43. Sidik ragam bobot kering 100 biji ... 92
44. Data pengamatan bobot kering biji per plot ... 93
45. Sidik ragam bobot kering biji per plot ... 93
47. Hasil analisis kandungan hara N dan P tajuk tanaman ... 95
ABSTRAK
DINI OKTAVIANI: Pertumbuhan dan Produksi Kedelai terhadap Pemberian Fungi Mikoriza Arbuskular (FMA) dan Konsorsium Mikroba dibimbing oleh YAYA HASANAH dan ASIL BARUS.
Penggunaan pupuk kimia pada budidaya kedelai semakin tinggi. Untuk menekan penggunaan pupuk kimia secara terus menerus, pemanfaatan pupuk hayati pada budidaya kedelai dapat meningkatkan pertumbuhan dan produksi kedelai. Penelitian dilaksanakan di Jalan Setiabudi Kelurahan Simpang Selayang Kecamatan Medan Tuntungan pada April-Juli 2013, menggunakan rancangan acak kelompok faktorial dengan dua faktor yaitu pemberian FMA (0, 20, 40 g/tanaman) dan pemberian konsorsium mikroba (0, 5, 10, 15 g/kg benih). Parameter yang diamati adalah tinggi tanaman, diameter batang, bobot kering tajuk, bobot kering akar, kehijauan daun, total luas daun, derajat infeksi FMA, jumlah bintil akar, jumlah bintil akar efektif,bobot bintil akar, serapan hara N tajuk, serapan hara P tajuk, jumlah cabang produktif, jumlah polong per tanaman, jumlah polong berisi per tanaman, bobot kering biji per tanaman, bobot kering 100 biji, bobot kering biji per plot.
Hasil penelitian menunjukkan pemberian FMA meningkatkan tinggi tanaman, diameter batang, jumlah bintil akar, jumlah bintil akar efektif, derajat infeksi, jumlah cabang produktif, jumlah polong berisi per tanaman, bobot kering biji per tanaman, bobot kering 100 biji dan bobot biji per plot. Pemberian konsorsium mikroba meningkatkan tinggi tanaman, diameter batang, jumlah bintil akar, jumlah bintil akar efektif, kehijauan daun, total luas daun, derajat infeksi, jumlah cabang produktif, jumlah plong per tanaman, jumlah polong berisi per tanaman, bobot kering biji per tanaman dan bobot biji per plot. Interaksi kedua perlakuan meningkatkan bobot bintil akar dan jumlah bintil akar efektif.
ABSTRACT
DINI OKTAVIANI: Growth and Yield of Soybean to Addition of Arbuscular Mycorrhiza Fungi (AMF) and Addition of microbe Concortium, supervised by YAYA HASANAH and ASIL BARUS.
Using of chemical fertilizer is increasing for soybean plantation. The action to compress that situation, utilization of biological fertilizer aims to increase growth and yield of soybean. This research had been conducted at Jalan Setiabudi Kelurahan Simpang Selayang Kecamatan Medan Tuntungan on April-July 2013, using a factorial randomized block design with two factors. The factors were addition of AMF (0, 20, 40 g per plant) and addition of microbe concortium (0,5,10,15 g per kg of seed). Parameters observed were plant height, stem diameter, weight of dry shoot, weight of dry root, leaf greenness level, total of leaf area, analysis substance N of shoot, analysis substance P of shoot, infection degree AMF, number of nodules, number of effective nodules, weight of nodules, number of productive branches, number of pods per plant, number of filled pods per plant, dry seeds weight per plant, 100 seeds dry weight, and dry seeds weight per plot.
The result showed that addition of AMF increase plant height, stem diameter, infection degree AMF, number of nodules, number of effective nodules, number of productive branches, number of filled pods per plant, dry seeds weight per plant, 100 seeds dry weight, and dry seeds weight per plot. The addition of microbe concortium increase plant height, stem diameter, leaf greenness level, total of leaf area, infection degree AMF, number of nodules, number of effective nodules, number of productive branches, number of pods per plant, number of filled pods per plant, dry seeds weight per plant, and dry seeds weight per plot. Interaction both of treatment increase weight of nodules and number of effective nodules.
PENDAHULUAN
Latar BelakangKedelai (Glycine max (L.) Merrill) termasuk komoditas pangan ketiga
terpenting setelah padi dan jagung bagi Indonesia. Tahu, tempe, kecap, dan tauco
adalah produk pangan yang dibuat dari kedelai untuk sumber protein nabati dalam
mendukung ketahanan pangan nasional. Produksi kedelai 2012 menurut Badan
Pusat Statistik (2012) diperkirakan sebesar 783,16 ribu ton biji kering atau
mengalami penurunan sebesar 68,13 ribu ton (8,00%) dibandingkan 2011.
Kebutuhan nasional kedelai dewasa ini telah mencapai 2,2 juta ton per tahun,
sementara produksi dalam negeri baru mampu memenuhi 35-40% dari total
kebutuhan (Badan Penelitian dan Pengembangan Pertanian, 2012).
Rendahnya produksi kedelai Indonesia dikarenakan mahalnya harga sarana
produksi, keterbatasan modal usaha tani, belum maksimalnya pengetahuan petani
dalam penggunaan teknologi produksi yang mendukung pertanian berkelanjutan,
semakin berkurangnya sumber daya lahan yang subur karena penggunaan pupuk
anorganik secara terus menerus, serta alih fungsi lahan (Jumrawati, 2008).
Pertumbuhan tanaman kedelai yang banyak mengandung protein
membutuhkan banyak unsur hara terutama N dan P. Untuk memenuhi kebutuhan
unsur hara tersebut diperlukan pupuk buatan yang membutuhkan biaya yang mahal.
Bahkan selain biaya yang tinggi, penggunaan pupuk buatan secara terus-menerus
dapat mengakibatkan pencemaran lingkungan dan menurunkan kesuburan tanah.
Oleh karena itu perlu diupayakan beberapa alternatif untuk memulihkan produksi
mikroorganisme tanah misalnya konsorsium mikroba dan Fungi Mikoriza
Arbuskular (FMA) (Bertham, 2007).
Konsorsium mikroba yang digunakan dalam penelitian ini merupakan
gabungan mikroorganisme yang berasosiasi membentuk kerja sama untuk
memfiksasi N, sebagai penyedia unsur hara agar tersedia bagi tanaman dan
sebagai biokontrol patogen akar. Selain Rhizobium sp., didalam konsorsium
mikroba yang digunakan terdiri dari Bacillus sp., Azospirillum sp.,
Pseudomonas sp.,dan Bakteri Endofitik (Ocrobactrum pseudogrigmonense) yang
berasal dari PT Bio Industri Nusantara, Balai Penelitian Tanah.
Menurut hasil penelitian Noertjahyani (2007) menyatakan bahwa
inokulasi konsorsium Bradyrhizobium japonicum dan Pseudomonas sp. sebanyak
12 g/kg benih dapat mempercepat keluarnya bunga kedelai dan meningkatkan
bobot 100 biji tanaman, tetapi tidak berpengaruh terhadap kandungan N dan P
pada tanaman kedelai. Pemberian takaran konsorsium yang semakin tinggi akan
mempercepat waktu berbunga.
Menurut hasil penelitian Musfal (2010) penambahan FMA pada tanaman
jagung sebanyak 20 g/tanaman dapat meningkatkan infeksi akar, serapan fosfat,
bobot kering tanaman dan hasil pipilan kering dan Zein (2004) dalam penelitian nya
dengan penggunaan FMA jenis Glomus manihotis pada kedelai dengan dosis
tertinggi 15 g/tanaman dapat meningkatkan serapan P tanaman dan jumlah biji per
polong tetapi tidak nyata meningkatkan bobot 100 biji, serapan hara N, bobot
kering biji dan jumlah polong berisi.
Rao (1994) dalam Zein (2004) menambahkan penggunaan bakteri
Fungi Mikoriza Arbuskular (FMA) sehingga koinokulasi keduanya dapat
menghasilkan bintil akar, pengambilan nutrien dan hasil panen lebih baik. Salah
satu pengaruh utama mikoriza dengan tanaman kedelai adalah pertukaran dan
pengambilan unsur hara terutama P, yang dapat meningkatkan bobot kering biji
kedelai.
Berdasarkan uraian diatas dalam upaya menghasilkan produksi kedelai
yang berkualias dengan meningkatkan penyerapan unsur hara, penulis tertarik
untuk melakukan penelitian tentang pertumbuhan dan produksi kedelai
(Glycine max (L.) Merill) terhadap pemberian Fungi Mikoriza Arbuskular (FMA)
dan konsorsium mikroba.
Tujuan Penelitian
Untuk mengetahui pertumbuhan dan produksi kedelai
(Glycine max (L.) Merrill) terhadap pemberian Fungi Mikoriza Arbuskular (FMA)
dan konsorsium mikroba serta interaksi keduanya.
Hipotesis Penelitian
Pemberian Fungi Mikoriza Arbuskular (FMA) dan konsorsium mikroba
serta interaksi keduanya dapat meningkatkan pertumbuhan dan produksi kedelai
(Glycine max (L.) Merrill).
Kegunaan Penelitian
Penelitian ini berguna untuk memperoleh gelar Sarjana di Fakultas
Pertanian Universitas Sumatera Utara dan diharapkan dapat pula berguna untuk
TINJAUAN PUSTAKA
Botani TanamanMenurut Van Steenis (2003), tanaman kedelai diklasifikasikan ke dalam
kingdom Plantae dengan divisi Spermatophyta. Kedelai merupakan tanaman berbiji
terbuka yaitu dengan subdivisi Angiospermae. Tanaman kedelai termasuk ke dalam
kelas Dicotyledonae, berordo Polypetales dengan famili Leguminosae. Genus
tanaman ini adalah Glycine dengan nama spesies dari tanaman ini adalah Glycine
max (L.) Merrill.
Tanaman kedelai memiliki sistem perakaran yang terdiri dari akar tunggang
yang terbentuk dari calon akar, sejumlah akar sekunder yang tersusun dalam empat
barisan sepanjang akar tunggang, cabang akar sekunder, dan cabang akar adventif
yang tumbuh dari bagian bawah hipokotil. Umumnya sistem perakaran tanaman
kedelai terdiri dari akar lateral yang berkembang 10-15 cm di atas akar tunggang
(Adie dan Krisnawati, 2007).
Tanaman kedelai berbatang pendek (30–100 cm), memiliki 3-6
percabangan, berbentuk tanaman perdu. Batang tanaman kedelai berkayu, biasanya
kaku dan tahan rebah. Menurut tipe pertumbuhannya, tanaman kedelai dapat
dibedakan menjadi determinate dan indeterminate. Pertanaman determinate
memiliki karakteristik tinggi tanaman pendek sampai sedang, ujung batang hampir
sama besar dengan batang tengah dan berbunga serentak sedangkan indeterminate
memiliki tinggi tanaman sedang sampai tinggi, ujung batang lebih kecil dari bagian
tengah, agak melilit dan beruas panjang, daun teratas lebih kecil dari daun bagian
tengah dan pembungaan secara bertahap mulai dari pangkal hingga ke bagian atas
Daun kedelai terbagi menjadi empat tipe, yaitu (1) kotiledon atau daun biji,
(2) dua helai daun primer sederhana, (3) daun bertiga, dan (4) profila. Daun primer
berbentuk oval dengan tangkai daun sepanjang 1-2 cm, terletak berseberangan pada
buku pertama diatas kotiledon. Bentuk daun kedelai adalah lancip, bulat dan
lonjong serta terdapat perpaduan bentuk daun misalnya antara lonjong dan lancip
(Adie dan Krisnawati 2007).
Berdasarkan Poelman and Sleper (1995) menyatakan kultivar kedelai
memiliki bunga bergerombol terdiri atas 3-15 bunga yang tersusun pada ketiak
daun. Bunga kedelai termasuk bunga sempurna yaitu bunga mempunyai alat jantan
dan betina. Penyerbukan terjadi pada saat mahkota bunga masih tertutup sehingga
kemungkinan perkawinan silang akan kecil.
Jumlah polong kedelai bervariasi mulai 2-20 dalam satu pembungaan dan
lebih dari 400 dalam satu tanaman. Pada umumnya berisi 2-3 biji per polong.
Polong masak berwarna kuning muda sampai kuning kelabu, coklat atau hitam.
Polong kedelai terbentuk pertama kali sekitar 7-10 hari setelah munculnya bunga
pertama (Ramadhani, 2011).
Somaatmadja, dkk (1999) menyatakan bentuk biji umumnya bulat telur.
Pembentukan protein dan lemak pada biji membutuhkan unsur hara terutama N dan
P. Adapun bobot 100 butir biji kedelai berkisar antara 5 sampai 30 gram. Adie dan
Krisnawati (2007) menambahkan pengelompokan ukuran biji di Indonesia
dikelompokkan yaitu berukuran besar (berat > 14g/100 biji), sedang (10-14g/100
Syarat Tumbuh Iklim
Kedelai dapat tumbuh baik di tempat pada daerah berhawa panas, di tempat
terbuka dengan curah hujan 100–400 mm3 per bulan. Oleh karena itu, kedelai
kebanyakan ditanam di daerah yang terletak kurang dari 400 m di atas permukaan
laut (Andrianto dan Indarto 2004).
Tanaman kedelai sebagian besar tumbuh di daerah yang beriklim tropis dan
subtropis. Suhu yang dikehendaki tanaman kedelai antara 21-340C, akan tetapi suhu
optimum bagi pertumbuhan tanaman kedelai 23-270C. Pada perkecambahan benih
kedelai memerlukan suhu yang cocok sekitar 300C (Prihatman, 2000).
Kedelai merupakan tanaman berhari pendek, yaitu tanaman cepat berbunga
apabila panjang hari 12 jam atau kurang, dan tanaman tidak mampu berbunga
apabila panjang hari melebihi 16 jam. Tanaman kedelai di Indonesia umumnya
berbunga pada umur 25-40 hari. Kelembaban udara yang optimal bagi tanaman
kedelai berkisar antara 75–90% selama periode tanaman tumbuh sampai fase
pengisian polong dan kelembaban udara rendah berkisar antara 60–75% pada waktu
pemasakan polong sampai panen (Sumarno dan Manshuri, 2007).
Tanah
Pada dasarnya kedelai mengkehendaki kondisi tanah yang tidak terlalu
basah, tetapi air tetap tersedia. Tanah yang baru pertama kali ditanam kedelai,
sebelumnya perlu diberi bakteri rhizobium (Hapsari dan Adie, 2010).
Kondisi lahan yang sesuai untuk pertanaman kedelai adalah tanah dengan
tekstur lempung, drainase baik, kedalaman lapisan lebih > 50cm, bahan organik
dengan topografi datar dan tanpa naungan, serta tidak ada pengaruh salinitas
(Mulyatri dan Firdaus, 2008).
Pupuk Hayati
Pupuk hayati didefinisikan sebagai inokulan berbahan aktif organisme hidup
yang berfungsi untuk menambat hara tertentu sehingga tersedia bagi tanaman.
Penyediaan hara ini dapat berlangsung simbiotis dan nonsimbiotis. Kelompok
mikroba simbiotis ini terutama meliputi bakteri bintil akar dan cendawan mikoriza.
Tumbuhnya kesadaran akan dampak negatif penggunaan pupuk buatan, maka
sebagian kecil petani beralih dari pertanian konvensional ke pertanian organik
(Simanungkalit, dkk, 2006).
Meningkatnya perhatian terhadap aplikasi pupuk hayati karena
kegunaannya yang dapat menyediakan sumber hara bagi tanaman, melindungi akar
dari gangguan hama dan penyakit, menstimulir sistem perakaran agar berkembang
sempurna sehingga memperpanjang usia akar, sebagai penawar racun beberapa
logam berat. Pada tanaman kedelai aplikasi pupuk hayati dapat menekan kebutuhan
pupuk nitrogen sampai 100%, fosfor 25-50% dan kalium 50% dari takaran anjuran
(Damanik, dkk, 2011).
Fungi Mikoriza Arbuskular (FMA)
Mikoriza merupakan struktur yang terbentuk karena asosiasi simbiosis
mutualisme antara cendawan tanah dengan akar tanaman tingkat tinggi. Adapun
manfaat mikoriza bagi perkembangan tanaman yang menjadi inangnya, yaitu
meningkatkan absorbsi hara dari dalam tanah, sebagai penghalang biologis terhadap
infeksi patogen akar, meningkatkan ketahanan inang terhadap kekeringan,
mendapatkan keuntungan nutrisi untuk keperluan hidupnya dari akar tanaman
(Noli, dkk, 2011).
Fungi Mikoriza Arbuskular (FMA) adalah salah satu tipe cendawan
mikoriza termasuk kedalam golongan endomikoriza. Karakteristik FMA
digambarkan sebagai berikut (a) sistem perakaran yang terinfeksi FMA tidak
membesar, (b) cendawan membentuk struktur lapisan hifa tipis dan tidak merata
pada permukaan akar, (c) hifa masuk ke dalam individu sel jaringan korteks
(Delvian, 2003).
Selain meningkatkan penyerapan unsur P telah diketahui bahwa mikoriza
juga meningkatkan penyerapan beberapa unsur mikro seperti Cu dan Zn. Pada
tanaman kedelai yang bermikoriza, penyerapan Cu dan Zn meningkat
(Islami dan Utomo, 1995). Hal yang serupa juga disampaikan oleh Salisburry and
Ross (1995) yang menyatakan bahwa manfaat mikoriza yang paling besar dalam
meningkatkan penyerapan ion yang biasanya berdifusi secara lambat menuju akar
atau yang dibutuhkan dalam jumlah banyak, terutama fosfat.
Mekanisme penyerapan hara P oleh akar yang bersimbiosis dengan
mikoriza, yaitu :
1. Kolonisasi mikoriza mengubah morfologi akar sedemikian rupa, sehingga
mengakibatkan pembesaran sistem akar untuk mengabsorpsi P.
2. Hifa dalam tanah mengabsorpsi P dan mengangkutnya ke akar-akar yang
dikolonisasi, dimana P ditransfer ke inang mikoriza.
3. Daerah akar bermikoriza tetap aktif dalam mengabsorpsi hara untuk jangka
Ketika fosfat di sekitar rambut akar sudah terkuras, maka hifa membantu menyerap
fosfat di tempat-tempat yang tidak dapat lagi dijangkau rambut akar
(Simanungkalit, dkk, 2006).
Faktor-faktor yang dapat mempengaruhi perkembangan mikoriza selain pH
tanah, kondisi tanah yang lain yang mempengaruhi adalah drainase, ketersediaan
bahan organik dan ketersediaan hara. Mikoriza akan dapat berkembang dengan baik
apabila tidak ada hambatan aerasi. Ketersediaan hara terutama nitrogen dan fosfat
yang rendah akan mendorong pertumbuhan mikoriza. Sebaliknya kandungan hara
yang terlalu rendah atau terlalu tinggi menghambat pertumbuhan mikoriza (Islami
dan Utomo, 1995).
Berdasarkan Hanum (2006) melaporkan bahwa pemanfaatan Fungi
Mikoriza Arbuskular (FMA) pada tanaman kedelai membantu meningkatkan
potensi sistem perakaran tanaman untuk mengabsorbsi air. Pada serapan hara P,
tanaman yang berasosiasi dengan mikoriza memperlihatkan peningkatan serapan
fosfor lebih tinggi pada kedelai dibandingkan tanpa mikoriza. Pemanfataan MVA
juga dapat meningkatkan bobot kering biji kedelai yang akhirnya akan memberikan
kontribusi positif bagi peningkatan produksi.
Konsorsium Mikroba
Dalam inokulan konsorsium mikroba terdiri dari gabungan
bermacam-macam mikroba yang dapat saling bersimbiosis dan bekerja sama dalam
memfiksasi dan menyediakan hara yang dibutuhkan tanaman. Mikroba yang
membantu fiksasi N dari udara adalah bakteri rhizobium, Bacillus sp. yang dapat
melarutkan fosfat dan sebagai biokontrol fungi patogen akar tanaman kedelai,
pencucian, Pseudomonas sp. yang dapat memacu pertumbuhan kecambah kedelai
dan mampu memproduksi fitohormon (IAA) dan bakteri endofitik yakni
Ocrobactrum pseudogrigmonense yang hidup didalam tanaman sebagai anti
patogen (Prihastuti, 2008).
Interaksi mikroba dengan tanaman di rizosfer dapat berupa hubungan yang
menguntungkan, netral, atau menggangu pertumbuhan tanaman. Plant Growth
Promoting Rhizobacteria (PGPR) atau Rizobakteri Pemacu Pertumbuhan Tanaman
(RPPT) berpotensi meningkatkan produktivitas dan pertumbuhan tanaman, seperti
dalam menghadapi hama dan penyakit; memproduksi fitohormon (biostimulant):
IAA (Indole Acetic Acid), sitokinin, giberellin dan penghambat produksi etilen,
dapat menambah luas permukaan akar-akar halus, meningkatkan ketersediaan
nutrisi bagi tanaman. Berbagai isolat Pseudomonas sp., Azospirillum sp.,
Azotobacter sp., Bacillus sp., dan Serratia sp. diketahui sebagai RPPT (Widodo,
2006).
Bakteri penambat nitrogen(Rhizobium) mempunyai kemampuan menambat
nitrogen bebas (N2) dari udara dan merubahnya menjadi amonia (NH3) yang akan
diubah menjadi asam amino yang akan digunakan oleh tanamanuntuk tumbuh dan
berkembang. Penambatan nitrogen secara biologis diperkirakanmenyumbang lebih
dari 170 juta ton nitrogen kebiosfer pertahun, 80% merupakan hasil dari simbiosis
antara bakteri Rhizobium dengan tanaman Leguminosae (Purwaningsih, 2004).
Penambatan nitrogen bebas oleh bakteri nodul diperantarai oleh enzimyang
diketahui sebagai nitrogenase. Dalam aktivitasnya, enzim nitrogenase peka
nodul akar, level oksigen diatur oleh haemoglobin khusus yaitu leghemoglobin
(Yurnalis, 2006).
Leghemoglobin berfungsi sebagai tempat absorbsi dan reduksi nitrogen,
pembawa elektron khusus dalam fiksasi nitrogen, dan pembawa dari oksigen.
Jumlah leghemoglobin di dalam bintil akar memiliki hubungan langsung dengan
jumlah nitrogen yang difiksasi yang berkorelasi positif. Rhizobium berasosiasi
dengan tanaman legum biasanya memfiksasi 100-300 kg nitrogen/ha dalam satu
musim tanam (Fitriani, 2007).
Pada tanaman kedelai menghasilkan bintil akar yang gepeng dan bulat
dengan daya hidup yang pendek. Bintil akar yang efektif dapat dilihat dari jaringan
bintil akar bagian tengah setelah dibelah berwarna merah, karena mengandung
legemoglobin dan letak bintil akar yang efektif cenderung mengumpul pada leher
akar (Islami dan Utomo, 1995).
Kelangsungan hidup rhizobium di dalam tanah sangat tergantung pada
kondisi tanah terutama pH, kelembaban, bahan organik, lamanya jarak (periode)
antara tanaman budidaya yang menjadi inangnya, serta bahan organik sebagai
sumber nutrisi. pH optimum bagi bakteri Rhizobium adalah sekitar 5,5-7,0. Hal
tersebut menunjukkan bahwa pada pH < 5,5 dan > 7,0 Rhizobium tidak dapat
berkembang atau berkembang dengan lambat sehingga kegiatan infeksi akan
terhenti (Risnawati, 2010).
Pembentukan bintil akar yang maksimal juga mmbutuhkan unsur P fosfor.
Ternyata unsur P yang diperlukan bagi pembentukan bintil akar lebih banyak
yang dipupuk dengan pupuk P, jumlah bintil akar akan meningkat
(Islami dan Utomo, 1995).
Hormon IAA atau yang dikenal sebagai auksin merupakan pemacu
pertumbuhan dan mengontrol berbagai proses fisiologi seperti pembelahan sel,
diferensiasi jaringan dan respons terhadap cahaya dan gravitasi. Bakteri penghasil
IAA mempunyai kemampuan membantu berbagai proses tersebut dengan
memasukkan IAA ke dalam bagian auksin tanaman. Akar merupakan organ
tanaman yang paling sensitive terhadap fluktuasi kadar IAA dan responsnya pada
peningkatan jumlah IAA eksogenous meluas dari pemanjangan akar primer,
pembentukan akar lateral dan akar liar, sampai penghentian pertumbuhan
(Widyawati, 2008).
Hasil penelitian Dewi, dkk (2012) mengatakan bahwa pemberian
konsorsium mikroba yang terdiri dari Rhizobium leguminosarum, Azotobacter
chroococcum, Azospirillum brasilense, Pseudomonas flurescens, Bacillus
megaterium serta Saccharomyces cerevisiae sebagai biofertilizer berpengaruh
terhadap pertumbuhan dan produktivitas kacang tanah (Arachis hypogaea L.)
dimana rata-rata tinggi tanaman tertinggi dan rata-rata berat kering tanaman
tertinggi dicapai dengan pemberian 15 ml biofertilizer sebanyak 1 kali, rata-rata
berat basah bintil akar tertinggi dicapai dengan pemberian 6 ml biofertilizer
sebanyak 1 kali, serta rata-rata berat kering polong tertinggi dan rata-rata berat
kering biji tertinggi dengan pemberian 6 ml biofertilizer sebanyak 2 kali.
Hanum (1997) dalam penelitiannya menyatakan bahwa FMA dan rhizobium
memiliki suatu sinergistik yang unik yakni FMA dapat menyumbangkan P untuk
rhizobium dapat dimanfaatkan untuk metabolisme tanaman inang. Inokulasi
Rhizobium dapat meningkatkan kolonisasi akar oleh jamur mikoriza. Inokulasi
ganda ini meningkatkan nodulasi, kolonisasi mikoriza dan kadar N dan P tanaman.
Sesuai dengan hasil penelitiannya bahwa Rhizobia strain USDA 110 memiliki
peranan dalam meningkatkan serapan N dan P tanaman, jumlah dan bobot kering
bintil akar, maka pertumbuhan tanaman baik vegetatif maupun produksi juga akan
meningkat.
BAHAN DAN METODE PENELITIAN
Tempat dan Waktu PenelitianPenelitian ini dilaksanakan di Lahan Masyarakat Jalan Setiabudi Kelurahan
Simpang Selayang Kecamatan Medan Tuntungan dengan ketinggian tempat ± 25 m
dpl, mulai bulan April sampai dengan Juli 2013.
Bahan dan Alat
Bahan yang digunakan dalam penelitian ini adalah benih kedelai
varietas Grobogan, benih jagung varietas P12, tryphan blue, KOH 10%, HCl 2%
konsorsium mikroba, mycorhiza fertilizer (mycofer), polibeg ukuran 45 x 30 cm,
pasir, pupuk organik cair Hyponex merah, plastik transparan, amplop serta bahan
yang lain yang mendukung penelitian.
Adapun alat yang digunakan adalah cangkul, gembor, meteran, pacak
sampel, handsprayer, selang air, jangka sorong, mikroskop, deck glass, preparat,
oven, gunting rumput, pisau, klorofilmeter, timbangan analitik, alat tulis dan alat
yang lain yang mendukung penelitian.
Metode Penelitian
Penelitian ini menggunakan metode Rancangan Acak Kelompok (RAK)
faktorial yang terdiri dua faktor perlakuan, yaitu:
Faktor I : Perlakuan inokulan FMA dengan 3 taraf yaitu :
M0 = Tanpa inokulan FMA
M1 = Inokulan FMA 20 gram/tanaman
M2 = Inokulan FMA 40 gram/tanaman
Faktor II : Perlakuan konsorsium mikroba dengan 4 taraf yaitu :
R1 = 5 gram / kg benih ( 0,81 g / 162 g benih)
R2 = 10 gram / kg benih ( 1,62 g / 162 g benih)
R3 = 15 gram / kg benih ( 2,43 g / 162 g benih)
Sehingga diperoleh 12 kombinasi perlakuan sebagai berikut :
M0R0 M1R0 M2R0
M0R1 M1R1 M2R1
M0R2 M1R2 M2R2
M0R3 M1R3 M2R3
Jumlah ulangan : 3 ulangan
Jumlah tanaman/plot : 50 tanaman
Jumlah tanaman/sampel : 5 tanaman
Jumlah sampel seluruhnya : 180 tanaman
Jumlah tanaman seluruhnya : 1800 tanaman
Luas Plot : 200 cm x 200 cm
Jarak Tanam : 40 cm x 20 cm
Data hasil penelitian dianalisis dengan menggunakan sidik ragam
berdasarkan model linier sebagai berikut :
Yijk = µ + ρi + αj + βk+ (αβ)jk+ εij
i = 1, 2, 3 j = 1, 2, 3 k = 1, 2, 3,4
Yij = Hasil pengamatan pada blok ke-i dengan perlakuan inokulasi FMA pada
taraf ke-j dan perlakuan konsorsium mikroba pada taraf ke-k
µ = Nilai tengah
ρi = Pengaruh ulangan pada taraf ke-i
βk = Pengaruh perlakuan konsorsium mikroba pada taraf ke-k
(αβ)jk = Pengaruhinteraksi pada dua perlakuan
εij = Galat pada blok ke-i dengan perlakuan inokulasi FMA pada taraf ke-j dan
perlakuan konsorsium mikroba pada taraf ke-k
Data hasil penelitian pada perlakuan yang berpengaruh nyata dilanjutkan
dengan Uji Beda Rataan berdasarkan Uji Jarak Berganda Duncan (DMRT) pada
PELAKSANAAN PENELITIAN
I. Perbanyakan Fungi Mikoriza Arbuskular (FMA)Persiapan Media Tanam
Media tanam berupa pasir yang dicuci dengan air mengalir untuk
membersihkan dari kotoran dan dilakukan pemisahan kerikil yang terdapat pada
pasir, kemudian dikeringkan selama 2-3 jam dan dimasukkan kedalam polibeg
berukuran 45 x 30 cm.
Inokulasi FMA
Inokulan FMA dalam bentuk mycofer sebanyak 5 gram/lubang tanam
ditanam pada media pasir dengan kedalaman 5 cm kemudian ditutup dengan pasir.
Penanaman Jagung sebagai Tanaman Inang
Benih jagung diletakkan diatas pasir yang telah diberikan inokulan FMA
kemudian ditutup kembali dengan pasir.
Pemberian Pupuk Organik Cair
Pupuk organik cair diaplikasikan 7 hari setelah tanam sebanyak 1
gram/liter air, diberikan 1 kali seminggu. Pupuk yang digunakan adalah pupuk
Hyponex merah.
Pemeliharaan
Dilakukan penyiraman secara intensif untuk menjaga kelembapan media
tanam yang dilakukan sesuai dengan kondisi lapang dan tidak terlalu basah.
Panen Inokulan FMA
Jagung sebagai tanaman inang FMA dapat dipanen setelah berumur 2 bulan
yang sudah dilakukan Trapping (pengeringan) selama 2 minggu, kemudian diuji
digunakan sebagai inokulan FMA. Akar tanaman jagung dicacah ± 0,5 cm dan
campuran cacahan akar dan media tanam pasir yang dijadikan inokulan FMA.
II. Penanaman Kedelai Persiapan Lahan
Areal pertanaman terlebih dahulu dibersihkan dari gulma. Kemudian lahan
diolah dan digemburkan menggunakan cangkul dengan kedalaman kira-kira 20 cm.
Kemudian dibuat plot-plot dengan ukuran 200 cm x 200 cm serta jarak antar plot 50
cm dan jarak antar blok 50 cm dan parit drainase sedalam 30 cm untuk menghindari
genangan air.
Aplikasi FMA
FMA diaplikasikan ke lubang tanam pada saat penanaman benih kedelai
dengan dosis sesuai dengan perlakuan.
Aplikasi Konsorsium Mikroba
Konsorsium mikroba diaplikasikan bersamaan dengan penanaman benih
kedelai dengan cara mencampurkan rhizobium dengan dosis 5 gram/kg benih, 10
gram/kg benih dan15 gram/kg benih pada pagi hari dan ditempat yang teduh.
Penanaman Benih
Dibuat lubang tanam secara tugal sedalam ± 5cm dengan jarak tanam
40 x 20 cm, terlebih dahulu dimasukkan FMA sesuai dosis perlakuan dan ditutup
selapis dengan tanah, kemudian dimasukkan 2 benih per lubang tanam yang telah
Pemupukan N dan K
Pemupukan urea dan KCl dilakukan pada saat tanam dengan cara larikan
pada semua tanaman. Pemupukan urea [CO(NH2)2]dengan dosis 25 kg/ha (10
g/plot) dan pemupukan KCl dengan dosis 100 kg/ha (40 g/plot).
Penjarangan
Penjarangan dilakukan pada 1 MST dengan cara menggunting tanaman
yang pertumbuhannya kurang baik dan meninggalkan 1 tanaman/lubang tanam.
Pemeliharaan Tanaman Penyiraman
Penyiraman dilakukan sesuai dengan kondisi lapangan. Penyiraman
dilakukan pagi atau sore hari yang dilakukan dengan menggunakan gembor.
Penyiangan
Penyiangan dilakukan apabila ditemukan gulma di areal penelitian.
Penyiangan dilakukan secara manual yaitu mencabut langsung dengan tangan untuk
menghindari persaingan dalam mendapatkan unsur hara dari dalam tanah.
Pengendalian Hama dan Penyakit
Pengendalian hama dilakukan dengan menyemprotkan pestisida organik
dengan bahan aktif azadirachtin, alkaloid, ricin, nikotin, poliferol, sitral, eygenol
dan annoanin. Hama yang menyerang adalah kepik polong, penggerek polong
kedelai dan wereng hijau kedelai. Penyemprotan dilakukan pada saat tanaman
berumur 6 MST dengan dosis 100 ml/1 L air.
Panen
Panen dilakukan dengan cara memotong 5 cm diatas pangkal batang utama
sudah menguning tetapi bukan karena serangan hama dan penyakit, batang
berwarna kuning agak kecoklatan, polongnya keras bila dipijit dan kulit polong
sudah berwarna kuning kecoklatan sebanyak 95%. Polong yang telah dipanen
dijemur dibawah sinar matahari selama 2-3 hari dan biji diambil dari polongnya.
Pengamatan Parameter Tinggi Tanaman (cm)
Tinggi tanaman diukur mulai dari pangkal batang sampai dengan titik
tumbuh menggunakan meteran dengan menggunakan patok sampel sebagai
penanda. Pengukuran tinggi tanaman dilakukan pada interval waktu 2 MST sampai
akhir fase vegetatif.
Diameter Batang (mm)
Diameter batang diukur pada bagian batang bawah pada ketinggian 1 cm di
atas permukaan tanah dengan menggunakan jangka sorong. Pengukuran dilakukan
pada akhir fase vegetatif.
Bobot Kering Akar (g)
Akar yang diukur adalah akar yang sudah dipisahkan dari tajuk dan
dibersihkan dari kotoran yang ada lalu diovenkan dengan suhu 80°C selama 24 jam
lalu ditimbang. Pengamatan ini dilakukan pada akhir fase vegetatif.
Bobot Kering Tajuk (g)
Bagian tajuk tanaman yang diukur dipisahkan dari akar dengan cara
memotong pada bagian pangkal; batang lalu tajuk dibersihkan dari kotoran yang
ada lalu diovenkan dengan suhu 80°C selama 24 jam lalu ditimbang. Pengamatan
Jumlah Bintil Akar (bintil)
Dihitung jumlah bintil akar pada sampel dekstruktif yang terbentuk di akar
tanaman kedelai. Pengamatan ini dilakukan pada akhir fase vegetatif.
Bobot Bintil Akar (g)
Bobot bintil akar dihitung pada saat akhir fase vegetatif tanaman dengan
cara menimbang bobot bintil akar setelah perhitungan jumlah bintil akar.
Jumlah Bintil Akar Efektif (bintil)
Jumlah bintil akar yang efektif dilakukan dengan cara membelah bintil akar.
Kriteria bintil akar efektif yakni jika dibelah bintil akar tersebut berwarna merah
jambu.
Kehijauan Daun (SPAD)
Kehijauan daun diukur dengan klorofilmeter tipe opti sciences CCM 200
dimana prinsip kerja dengan menggunakan panjang gelombang 653 nm untuk
mendeteksi kehijauan daun. Daun yang diuukur yakni daun pada bagian tengah
yang diambil sebanyak 5 sampel daun. Pengamatan dilakukan pada akhir fase
vegetatif.
Total Luas Daun (cm²)
Pengamatan total luas daun dihitung dengan menggunakan Leaf Area Meter
(LAM) dari seluruh daun tanaman destruktif pada saat fase akhir vegetatif.
Derajat Infeksi FMA (%)
Pengamatan derajat infeksi dilakukan pada saat akhir fase vegetatif. Akar
tanaman diteliti untuk mengetahui berapa persen FMA dapat menginfeksi akar
tanaman kedelai dengan metode panjang akar terkolonisasi. Tahapan kerja dapat
Kandungan N Tajuk Tanaman (%)
Kandungan hara dianalisis dengan cara mengukur kadar hara N tanaman
yang ditentukan dengan metode Kjeldahl. Pengukuran kadar hara dilakukan pada
akhir masa vegetatif.
Kandungan P Tajuk Tanaman (%)
Kandungan hara dianalisis dengan cara mengukur kadar hara P tanaman
yang ditentukan dengan metode pengabuan kering. Pengukuran kadar hara
dilakukan pada akhir masa vegetatif.
Jumlah Cabang Produktif (cabang)
Jumlah cabang yang dihitung adalah cabang yang produktif menghasilkan
polong. Pengamatan dilakukan pada saat menjelang panen.
Jumlah Polong Per Tanaman Sampel (polong)
Pengamatan dilakukan terhadap semua jumlah polong setiap tanaman
sampel dengan menghitung jumlah polong berisi dan jumlah polong hampa.
Pengamatan ini dilakukan pada saat panen.
Jumlah Polong Berisi Per Tanaman Sampel (polong)
Pengamatan dilakukan terhadap semua jumlah polong yang berisi setiap
tanaman sampel dengan menghitung jumlah polong berisi. Pengamatan ini
dilakukan pada saat panen.
Bobot Kering Biji per Tanaman Sampel (g)
Produksi biji per tanaman sampel dihitung dengan menimbang produksi biji
seluruh sampel tanaman kemudian dirata-ratakan. Biji yang ditimbang adalah biji
Bobot Kering 100 Biji (g)
Penimbangan dilakukan dengan menimbang 100 biji kedelai yang telah
dijemur di bawah sinar matahari selama 2-3 hari.
Bobot kering biji / tanaman
Jumlah biji / tanaman Bobot Kering Biji per Plot (g)
Produksi biji per plot dihitung dengan menimbang produksi seluruh
tanaman dari masing-masing plot. Biji yang ditimbang adalah biji yang telah
dijemur di bawah sinar matahari 2-3 hari.
HASIL DAN PEMBAHASAN
HasilTinggi Tanaman
Data hasil pengamatan dan sidik ragam dari tinggi tanaman pada 2 - 6 MST
dapat dilihat pada Lampiran 6 - 15. Hasil sidik ragam menunjukkan bahwa
pemberian FMA dan konsorsium mikroba berpengaruh nyata terhadap tinggi
tanaman 6 MST, sedangkan interaksi antara pemberian konsorsium mikroba dan
FMA berpengaruh nyata terhadap tinggi tanaman 2 MST.
Data rataan tinggi tanaman pada pemberian FMA dan konsorsium mikroba
dapat dilihat pada Tabel 1.
Tabel 1. Rataan tinggi tanaman pada pemberian FMA dan konsorsium mikroba
MST FMA
(g/tanaman)
Konsorsium mikroba (g/kg benih)
Rataan
Tabel 1 menunjukkan bahwa pada tanpa pemberian FMA, tinggi tanaman 2
MST meningkat seiring dengan bertambahnya dosis konsorsium mikroba sampai
10 g/kg benih dan menurun pada pemberian konsorsium mikroba15 g/kg benih.
Pada pemberian FMA 20 g/tanaman, tinggi tanaman 2 MST meningkat dengan
pemberian konsorsium mikroba 10 dan 15 g. Pada pemberian FMA 40 g/tanaman,
tinggi tanaman 2 MST meningkat dengan pemberian konsorsium mikroba 5 g/kg
benih dan menurun pada pemberian konsorsium mikroba 10 dan 15 g/kg benih.
Tabel 1 menunjukkan bahwa tanpa pemberian konsorsium mikroba, tinggi
tanaman 2 MST meningkat dengan pemberian FMA 20 g/tanaman dan menurun
dengan pemberian FMA 40 g/tanaman. Pada pemberian konsorsium mikroba 5
g/kg benih, tinggi tanaman menurun dengan pemberian FMA 20 g/tanaman dan
meningkat dengan pertambahan dosis FMA 40 g/tanaman. Pada pemberian
konsorsium 10 dan 15 g/kg benih, tinggi tanaman 2 MST meningkat pada
pemberian FMA 20 g/tanaman dan menurun dengan peningkatan dosis FMA
sampai 40 g/tanaman, dimana tinggi tanaman tertinggi terdapat pada pemberian
FMA 20 g/tanaman dan konsorsium mikroba 10 g/kg benih (13,22 cm) dan
terendah pada tanpa pemberian FMA dan tanpa pemberian konsorsium mikroba
(10,65 cm).
Tabel 1 menunjukkan bahwa peningkatan dosis FMA sampai 40 g/tanaman
menurunkan tinggi tanaman 6 MST dibandingkan dengan pemberian FMA 20
g/tanaman, dimana tinggi tanaman pada 6 MST tertinggi terdapat pada pemberian
FMA 20 g (52,78 cm) dan terendah pada pemberian FMA 0 g (48,57 cm).
Tabel 1 menunjukkan bahwa tinggi tanaman 6 MST menurun seiring
dengan pemberian konsorsium mikroba 5 g/kg benih, dimana tinggi tanaman 6
MST tertinggi terdapat pada pemberian konsorsium mikroba 5 g/kg benih
(52,70 cm) dan yang terendah pada tanpa pemberian konsorsium mikroba (47,14
cm).
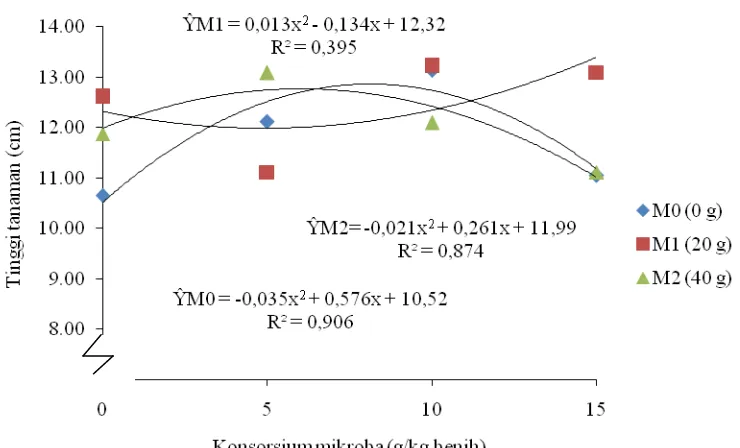
Grafik tinggi tanaman 2 MST dengan interaksi pemberian FMA dan
konsorsium mikroba dapat dilihat pada Gambar 1.
Gambar 1. Hubungan tinggi tanaman 2 MST dengan pemberian FMA dan konsorsium mikroba
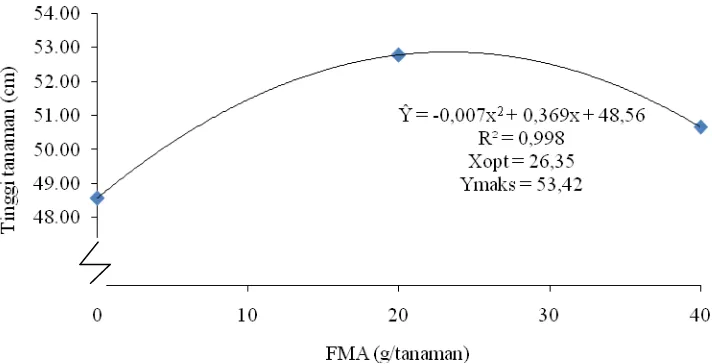
Grafik tinggi tanaman 6 MST dengan pemberian FMA dapat dilihat pada
Gambar 2. Hubungan tinggi tanaman 6 MST dengan pemberian FMA
Dari Gambar 2 dapat diketahui bahwa pemberian FMA terhadap tinggi
tanaman 6 MST menunjukkan hubungan kuadratik. Pada grafik dapat dilihat bahwa
pemberian FMA optimum adalah 26,35 g dengan tinggi tanaman maksimum yaitu
53,42 cm.
Grafik tinggi tanaman 6 MST dengan pemberian konsorsium mikroba dapat
dilihat pada Gambar 3.
Gambar 3. Hubungan tinggi tanaman 6 MST dengan pemberian konsorsium mikroba
Dari Gambar 3 dapat diketahui bahwa pemberian konsorsium mikroba
dapat dilihat bahwa pemberian konsorsium mikroba optimum adalah 8,89 g dengan
tinggi tanaman maksimum yaitu 53,13 cm.
Diameter Batang
Data hasil pengamatan dan sidik ragam dari diameter batang 6 MST dapat
dilihat pada Lampiran 16 dan 17. Hasil sidik ragam menunjukkan bahwa pemberian
FMA dan konsorsium mikroba berpengaruh nyata terhadap diameter batang,
sedangkan interaksi antara kedua perlakuan berpengaruh tidak nyata terhadap
diameter batang.
Data rataan diameter batang pada pemberian FMA dan konsorsium mikroba
dapat dilihat pada Tabel 2.
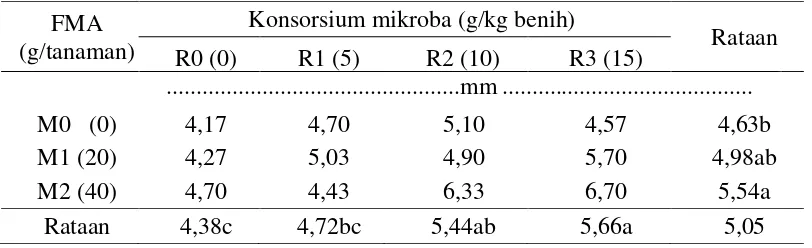
Tabel 2. Rataan diameter batang pada pemberian FMA dan konsorsium mikroba
FMA (g/tanaman)
Konsorsium mikroba (g/kg benih)
Rataan
Keterangan : Angka-angka yang diikuti huruf yang berbeda menunjukkan berbeda nyata menurut Uji Jarak Berganda Duncan pada taraf 5%
Tabel 2 menunjukkan bahwa peningkatan dosis FMA sampai 40
g/tanaman dapat meningkatkan diameter batang, dimana diameter batang tertinggi
terdapat pada pemberian FMA 40 g/tanaman (5,54 mm) dan terendah pada tanpa
pemberian FMA (4,63 mm).
Tabel 2 menunjukkan bahwa peningkatan dosis konsorsium mikroba sampai
15 g/kg benih dapat meningkatkan diameter batang, dimana diameter batang
tertinggi terdapat pada pemberian konsorsium mikroba 15 g/kg benih (5,66 mm)
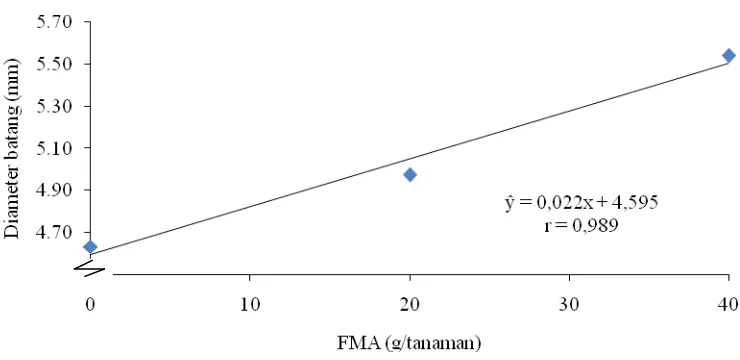
Grafik diameter batang dengan pemberian FMA dapat dilihat pada Gambar
4.
Gambar 4. Hubungan diameter batang 6 MST dengan pemberian FMA
Grafik diameter batang dengan pemberian konsorsium mikroba dapat dilihat
pada Gambar 5.
Gambar 5. Hubungan diameter batang dengan pemberian konsorsium mikroba
Bobot Kering Akar
Data hasil pengamatan dan sidik ragam dari bobot kering akar dapat dilihat
dan pemberian konsorsium mikroba serta interaksi antara keduanya berpengaruh
tidak nyata terhadap bobot kering akar.
Data rataan bobot kering akar pada pemberian FMA dan konsorsium
mikroba dapat dilihat pada Tabel 3.
Tabel 3. Rataan bobot kering akar pada pemberian FMA dan konsorsium mikroba
FMA (g/tanaman)
Konsorsium mikroba (g/kg benih)
Rataan
Tabel 3 menunjukkan bahwa bobot kering akar cenderung meningkat
seiring dengan pertambahan dosis FMA dan konsorsium mikroba, dimana bobot
kering akar tertinggi terdapat pada pemberian FMA 40 g/tanaman (1,45 g) dan
terendah pada tanpa pemberian FMA (1,21 g) dan bobot kering akar tertinggi
terdapat pada pemberian konsorsium mikroba 15 g/kg benih (1,63 g) dan terendah
pada tanpa pemberian konsorsium mikroba (1,06 g).
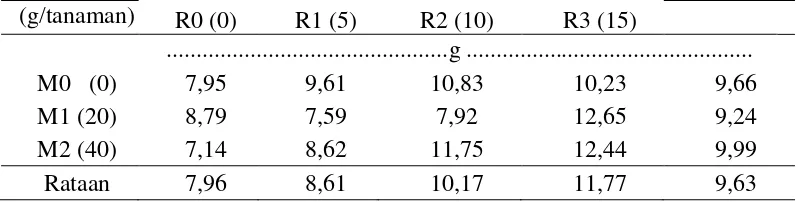
Bobot Kering Tajuk
Data hasil pengamatan dan sidik ragam dari bobot kering tajuk dapat dilihat
pada Lampiran 20 dan 21. Hasil sidik ragam menunjukkan bahwa pemberian FMA
dan pemberian konsorsium mikroba serta interaksi antara keduanya berpengaruh
tidak nyata terhadap bobot kering tajuk.
Data rataan bobot kering tajuk pada pemberian FMA dan konsorsium
mikroba dapat dilihat pada Tabel 4.
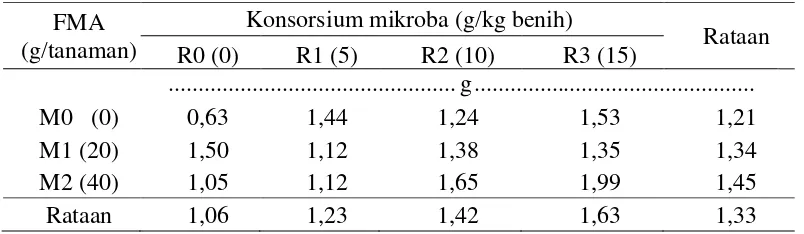
Tabel 4. Rataan bobot kering tajuk pada pemberian FMA dan konsorsium mikroba
(g/tanaman) R0 (0) R1 (5) R2 (10) R3 (15)
Tabel 4 menunjukkan bahwa bobot kering tajuk cenderung meningkat
seiring dengan penambahan dosis FMA dan konsorsium mikroba, dimana bobot
kering tajuk tertinggi terdapat pada pemberian FMA 40 g/tanaman (9,99 g) dan
terendah pada pemberian FMA 20 g/tanaman (9,24 g) dan bobot kering tajuk
tertinggi terdapat pada pemberian konsorsium mikroba 15 g/kg benih (11,17 g) dan
terendah pada tanpa pemberian konsorsium mikroba (7,96 g).
Jumlah Bintil Akar
Data hasil pengamatan dan sidik ragam dari jumlah bintil akar dapat dilihat
pada Lampiran 22 dan 23. Hasil sidik ragam menunjukkan bahwa pemberian FMA
dan konsorsium mikroba berpengaruh nyata terhadap jumlah bintil akar, sedangkan
interaksi antara kedua perlakuan berpengaruh tidak nyata terhadap jumlah bintil
akar.
Tabel 5 menunjukkan bahwa jumlah bintil akar meningkat seiring dengan
penambahan dosis FMA sampai 40 g/tanaman, dimana jumlah bintil akar tertinggi
terdapat pada pemberian FMA 40 g/tanaman (5,25 bintil) dan terendah pada tanpa
pemberian FMA (2,00 bintil).
Tabel 5 menunjukkan bahwa jumlah bintil akar meningkat seiring dengan
penambahan dosis konsorsium mikroba sampai 15 g/kg benih, dimana jumlah bintil
akar tertinggi terdapat pada pemberian konsorsium mikroba 15 g/kg benih (6,11
Data rataan jumlah bintil akar pada pemberian FMA dan konsorsium
mikroba dapat dilihat pada Tabel 5.
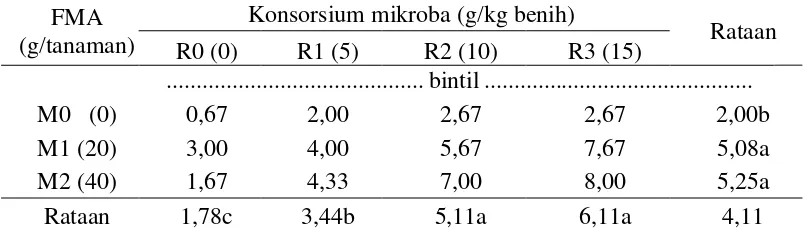
Tabel 5. Rataan jumlah bintil akar pada pemberian FMA dan konsorsium mikroba
FMA (g/tanaman)
Konsorsium mikroba (g/kg benih)
Rataan
R0 (0) R1 (5) R2 (10) R3 (15)
... bintil ...
M0 (0) 0,67 2,00 2,67 2,67 2,00b
M1 (20) 3,00 4,00 5,67 7,67 5,08a
M2 (40) 1,67 4,33 7,00 8,00 5,25a
Rataan 1,78c 3,44b 5,11a 6,11a 4,11
Keterangan : Angka-angka yang diikuti huruf yang berbeda menunjukkan berbeda nyata menurut Uji Jarak Berganda Duncan pada taraf 5%
Grafik jumlah bintil akar dengan pemberian FMA dapat dilihat pada
Gambar 6.
Gambar 6. Hubungan jumlah bintil akar dengan pemberian FMA
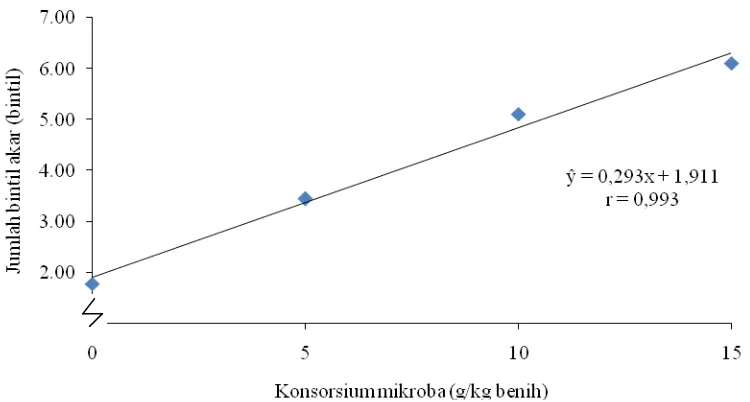
Dari Gambar 6 dapat diketahui bahwa pemberian FMA terhadap jumlah
bintil akar menunjukkan hubungan kuadratik.
Grafik jumlah bintil akar dengan pemberian konsorsium mikroba dapat
Gambar 7. Hubungan jumlah bintil akar dengan pemberian konsorsium mikroba
Bobot Bintil Akar
Data hasil pengamatan dan sidik ragam dari bobot bintil akar dapat dilihat
pada Lampiran 24 dan 25. Hasil sidik ragam menunjukkan bahwa interaksi antara
pemberian FMA dan konsorsium mikroba berpengaruh nyata terhadap bobot bintil
akar.
Tabel 6 menunjukkan bahwa pada tanpa pemberian FMA, pemberian FMA
20 g dan FMA 40 g/kg benih bobot bintil akar meningkat seiring dengan
penambahan dosis konsorsium mikroba sampai 15 g/kg benih.
Tabel 6 menunjukkan bahwa pada tanpa pemberian konsorsium mikroba
bobot bintil akar meningkat pada pemberian FMA 20 g/tanaman dan menurun pada
pemberian 40 g/tanaman. Pada pemberian konsorsium mikroba 5, 10 dan 15 g/kg
benih bobot bintil akar meningkat seiring pertambahan dosis FMA sampai 40
g/tanaman, dimana bobot bintil akar tertinggi terdapat pada interaksi perlakuan
FMA 40 g/tanaman dan konsorsium mikroba 15 g/kg benih (0,23 g) dan yang
Data rataan bobot bintil akar pada pemberian FMA dan konsorsium mikroba
dapat dilihat pada Tabel 6.
Tabel 6. Rataan bobot bintil akar pada pemberian FMA dan konsorsium mikroba
FMA (g/tanaman)
Konsorsium mikroba (g/kg benih)
Rataan
R0 (0) R1 (5) R2 (10) R3 (15)
... g ...
M0 (0) 0,01e 0,03de 0,03de 0,06cde 0,03
M1 (20) 0,04cde 0,09bcd 0,16ab 0,20a 0,13
M2 (40) 0,01e 0,11bc 0,21a 0,23a 0,14
Rataan 0,02 0,08 0,14 0,17 0,10
Keterangan : Angka-angka yang diikuti huruf yang berbeda menunjukkan berbeda nyata menurut Uji Jarak Berganda Duncan pada taraf 5%
Grafik bobot bintil akar dengan interaksi pemberian FMA dan konsorsium
mikroba dapat dilihat pada Gambar 8.
Gambar 8. Hubungan bobot bintil akar dengan pemberian FMA dan konsorsium mikroba
Jumlah Bintil Akar Efektif
Data hasil pengamatan dan sidik ragam dari jumlah bintil akar efektif dapat
pemberian FMA dan konsorsium mikroba berpengaruh nyata terhadap jumlah bintil
akar efektif.
Data rataan jumlah bintil akar efektif pada pemberian FMA dan konsorsium
mikroba dapat dilihat pada Tabel 7.
Tabel 7. Rataan jumlah bintil akar efektif pada pemberian FMA dan konsorsium mikroba
FMA (g/tanaman)
Konsorsium mikroba (g/kg benih)
Rataan
Keterangan : Angka-angka yang diikuti huruf yang berbeda menunjukkan berbeda nyata menurut Uji Jarak Berganda Duncan pada taraf 5%
Tabel 7 menunjukkan bahwa pada tanpa pemberian FMA jumlah bintil akar
efektif meningkat seiring dengan pertambahan dosis konsorsium mikroba sebanyak
10 g/kg benih dan tidak mengalami peningkatan pada pemberian konsorsium
mikroba 15 g/kg benih. Pada pemberian FMA 20 g dan 40 g/tanaman
jumlah bintil akar efektif meningkat seiring dengan peningkatan dosis konsorsium
mikroba sampai 15 g/kg benih.
Tabel 7 menunjukkan bahwa pada tanpa pemberian konsorsium mikroba
jumlah bintil akar efektif meningkat seiring dengan peningkatan dosis FMA sampai
40 g/tanaman. Pada pemberian konsorsium mikroba 5, 10 dan 15 g/kg benih jumlah
bintil akar juga meningkat seiring dengan peningkatan dosis FMA sampai 40
g/tanaman, dimana jumlah bintil akar efektif tertinggi terdapat pada interaksi
perlakuan FMA 40 g/tanaman dan konsorsium mikroba 15 g/kg benih (7,33 bintil)
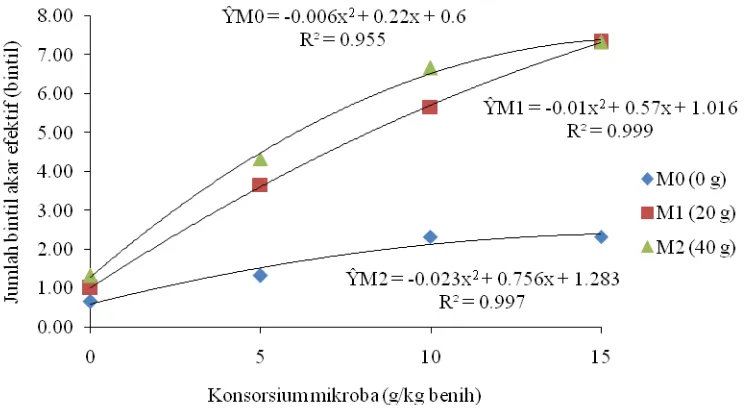
Grafik jumlah bintil akar efektif dengan interaksi pemberian FMA dan
konsorsium mikroba dapat dilihat pada Gambar 9.
Gambar 9. Hubungan jumlah bintil akar efektif dengan interaksi pemberian FMA dan konsorsium mikroba
Kehijauan Daun
Data hasil pengamatan dan sidik ragam dari kehijauan daun dapat dilihat
pada Lampiran 28 dan 29. Hasil sidik ragam menunjukkan bahwa pemberian
konsorsium mikroba berpengaruh nyata terhadap kehijauan daun, sedangkan
pemberian FMA dan interaksi antara pemberian konsorsium mikroba dan FMA
berpengaruh tidak nyata terhadap kehijauan daun.
Tabel 8 menunjukkan bahwa kehijauan daun meningkat seiring dengan
peningkatan dosis konsorsium mikroba sampai 15 g/kg benih, dimana kehijauan
daun tertinggi terdapat pada pemberian konsorsium mikroba 15 g/kg benih (29,16)
dan terendah pada tanpa pemberian konsorsium mikroba (22,73).
Data rataan kehijauan daun pada pemberian FMA dan konsorsium mikroba
Tabel 8. Rataan kehijauan daun pada pemberian FMA dan konsorsium mikroba
FMA (g/tanaman)
Konsorsium mikroba (g/kg benih)
Rataan
R0 (0) R1 (5) R2 (10) R3 (15)
... SPAD ...
M0 (0) 21.14 27.05 28.81 27.31 26.08
M1 (20) 21.78 26.01 26.51 31.68 26.50
M2 (40) 25.27 27.53 30.91 28.50 28.05
Rataan 22.73b 26.86a 28.74a 29.16a 26.87
Keterangan : Angka-angka yang diikuti huruf yang berbeda menunjukkan berbeda nyata menurut Uji Jarak Berganda Duncan pada taraf 5%
Grafik kehijauan daun dengan pemberian konsorsium mikroba dapat dilihat
pada Gambar 10.
Gambar 10. Hubungan kehijauan daun dengan pemberian konsorsium mikroba
Total Luas Daun
Data hasil pengamatan dan sidik ragam dari total luas daun dapat dilihat dari
Lampiran 30 dan 31. Hasil sidik ragam menunjukkan bahwa pemberian konsorsium
mikroba berpengaruh nyata terhadap total luas daun, sedangkan pemberian FMA
dan interaksi antara pemberian FMA dan konsorsium mikroba berpengaruh tidak
nyata terhadap total luas daun.
Data rataan total luas daun pada pemberian FMA dan konsorsium mikroba
Tabel 9. Rataan total luas daun pada pemberian FMA dan konsorsium mikroba
FMA (g/tanaman)
Konsorsium mikroba (g/kg benih)
Rataan
R0 (0) R1 (5) R2 (10) R3 (15)
... cm² ...
M0 (0) 755,46 1093,10 1171,09 1094,93 1028,64
M1 (20) 950,39 740,36 1088,31 1216,18 998,81
M2 (40) 832,95 1026,30 1402,68 1847,69 1277,41
Rataan 846,27c 953,25bc 1220,69ab 1386,26a 1101,62
Keterangan : Angka-angka yang diikuti huruf yang berbeda menunjukkan berbeda nyata menurut Uji Jarak Berganda Duncan pada taraf 5%
Tabel 9 menunjukkan bahwa total luas daun meningkat seiring dengan
peningkatan dosis konsorsium mikroba sampai 15 g/kg benih, dimana total luas
daun tertinggi terdapat pada pemberian konsorsium mikroba 15 g/kg benih
(1386,26 cm²) dan terendah pada tanpa pemberian konsorsium mikroba
(846,27 cm²).
Grafik total luas daun dengan pemberian konsorsium mikroba dapat dilihat
pada Gambar 11.
Gambar 11. Hubungan total luas daun dengan pemberian konsorsium mikroba
Data hasil pengamatan dan sidik ragam dari derajat infeksi FMA dapat
dilihat pada Lampiran 32 dan 33. Hasil sidik ragam menunjukkan bahwa pemberian
FMA dan konsorsium mikroba berpengaruh nyata terhadap derajat infeksi FMA,
sedangkan interaksi antara kedua perlakuan berpengaruh tida nyata terhadap derajat
infeksi FMA.
Tabel 10 menunjukkan bahwa bahwa derajat infeksi meningkat dengan
pemberian FMA 20 g/tanaman dan menurun pada pemberian FMA 40 g/tanaman,
dimana derajat infeksi tertinggi terdapat pada pemberian FMA 20 g/tanaman (55,00
%) dan terendah pada tanpa pemberian FMA (8,33%).
Tabel 10 menunjukkan bahwa derajat infeksi meningkat seiring dengan
penambahan dosis konsorsium mikroba sampai 15 g/kg benih, dimana derajat
infeksi tertinggi terdapat pada pemberian konsorsium mikroba 10 g/kg benih (41,11
%) dan terendah pada tanpa pemberian konsorsium mikroba (24,44 %),
Data rataan derajat infeksi FMA pada pemberian FMA dan konsorsium
mikroba dapat dilihat pada Tabel 10.
Tabel 10. Rataan derajat infeksi FMA pada pemberian FMA dan konsorsium mikroba
FMA (g/tanaman)
Konsorsium mikroba (g/kg benih)
Rataan
Keterangan : Angka-angka yang diikuti huruf yang berbeda menunjukkan berbeda nyata menurut Uji Jarak Berganda Duncan pada taraf 5%
Grafik derajat infeksi dengan pemberian FMA dapat dilihat pada
Gambar 12. Hubungan derajat infeksi dengan pemberian FMA
Dari Gambar 12 dapat diketahui bahwa pemberian FMA terhadap derajat
infeksi menunjukkan hubungan kuadratik. Pada grafik dapat dilihat bahwa
pemberian FMA optimum adalah 25,35 g dengan derajat infeksi maksimum yaitu
57,19%.
Grafik derajat infeksi dengan pemberian konsorsium mikroba dapat dilihat
pada Gambar 13.
Gambar 13. Hubungan derajat infeksi dengan pemberian konsorsium mikroba