SKRIPSI
PEMANFAATAN EKSTRAK ETANOL DAUN SRIKAYA (Annona reticulata L.) MENGGUNAKAN MATRIKS NATA DE COCO
DAN GEL DALAM PENYEMBUHAN LUKA SAYAT
OLEH:
ROGABE ULI PURBA NIM 081524060
PROGRAM EKSTENSI SARJANA FARMASI FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
PENGESAHAN SKRIPSI
PEMANFAATAN EKSTRAK ETANOL DAUN SRIKAYA (Annona reticulata L.) MENGGUNAKAN MATRIKS NATA DE COCO
DAN GEL DALAM PENYEMBUHAN LUKA SAYAT
Oleh :
ROGABE ULI PURBA NIM 081524060
Dipertahankan di hadapan Panitia Penguji Skipsi Fakultas Farmasi Universitas Sumatera Utara
Pada tanggal: Maret 2011
Disetujui Oleh:
Pembimbing I, Panitia Penguji,
KATA PENGHANTAR
Segala Puji dan syukur penulis ucapkan kehadirat Tuhan yang Maha
Kuasa yang telah melimpahkan kasih-Nya, sehingga penulis dapat melaksanakan
penelitian dan menyelesaikan penulisan skripsi ini dengan baik. Skripsi ini yang
merupakan salah satu syarat untuk memperoleh gelar sarjana farmasi pada
Fakultas FarmasiUniversitas Sumatera Utara.
Ucapan terima kasih dan penghargaan yang sebesar-besarnya kepada :
1. Ayahanda tercinta B.Purba dan Ibunda R.Hutasoit karena telah
memberikan kasih sayangnya yang melimpah kepada penulis dan
memberikan dukungan sehinggga penulis dapat menyelesaikan
pendidikan Sarjana Farmasi.
2. Bapak Dr Kasmirul Ramlan Sinaga. M.S.,Apt dan Dr. Marline
Nainggolan, M.S.,Apt selaku pembimbing yang telah memberikan
waktu, bimbingan, kesabaran dan petunjuk kepada penulis sehingga
dapat menyelesaikan penyusunan skripsi ini.
3. Kepada Laboratorium Fitokimia Ibu
Yang telah memberikan izin penggunaan fasilitas laboratorium kepada
penulis selama penelitian.
4. Bapak Prof. Dr. Sumadio Hadisahputera, Apt., yang telah memberikan
izin fasilitas sehingga penulis dapat menyelesaikan pendidikan.
5. Bapak Prof.Dr.Karsono, Apt., Bapak Prof Dr.M.Timbul Simanjuntak,
yang telah memberikan kritik saran dan arahan sehingga penulis dapat
menyelesaikan skripsi ini.
6. Mahasiswa ekstensi Farmasi 2008, teman farmasi regular dan
teman-teman baikku Siti Rizkya Putri, Rosfianita, Lastiur, Elwisda, Rosdiana,
Kak Vikha, Kak Wina dan teman-teman lainnya yang memberikan
semangat dan keceriaan sehinggga penulis dapat menyelesaikan
penelitian dan penulisan skripsi ini.
7. Rekan-rekan lain yang tidak dapat saya sebutkan satu persatu yang
memberikan dukungan, semangat, kritik dan saran kepada penulis
selama penelitian dan penulisan skripsi ini.
Penulis menyadari sepenuhnya bahwa penulisan skripsi ini masih
belum sempurna. Untuk itu dengan segala kerendahan hati penulis mengharapkan
saran dan kritik yang bersifat membangun demi kesempurnaan skripsi ini. Akhir
kata penulis berharap semoga skripsi ini dapat menjadi kontribusi yang
bermanfaat bagi ilmu pengetahuan khususnya dibidang farmasi.
Medan, Maret 2011
Penulis
ABSTRAK
Salah satu tumbuhan yang dapat digunakan sebagai obat luka adalah daun tumbuhan srikaya (Annona reticulata L.) famili Annonaceae. Tujuan penelitian ini adalah membuat ekstrak etanol daun srikaya menjadi sediaan dalam bentuk matriks nata de coco dan sediaan gel yang diuji terhadap luka sayat pada punggung kelinci.
Serbuk daun srikaya diekstraksi dengan pelarut etanol selama 5 hari, pisahkan, ampas di maserasi kembali selama 2 hari. Maserat yang diperoleh di uapkan dengan bantuan rotary evaporator. Ekstrak yang diperoleh diperangkapkan pada matriks nata de coco dengan cara merendam selama 24 jam kemudian di
freeze dryer. Selanjutnya ekstrak etanol di formulasi menjadi sediaan gel menggunakan HPMC sebagai dasar gel. Masing-masing ekstrak daun srikaya dalam bentuk matriks nata de coco dan sediaan gel di uji terhadap kelinci yang telah dibuat luka sayat sepanjang 2 cm dengan variasi konsentrasi 0,25%, 0,5% dan 0,75%. Untuk ekstrak yang diperangkapkan pada matriks nata de coco diberikan satu kali sehari, sebagai kontrol diberi matriks tanpa ekstrak sedangkan untuk sediaan gel diberi tiga kali sehari, sebagai kontrol diberi dasar gel, masing-masing kelompok dilakukan terhadap enam ekor kelinci dengan berat 1,5-2,0 kg. Terhadap daun srikaya dilakukan pemeriksaan karakterisasi simplisia. Hasil karakterisasi simplisia diperoleh kadar air 8,64%, kadar sari yang larut dalam air 12,53%, kadar sari larut dalam etanol 12,17%, kadar abu total 7,74% dan kadar abu tidak larut dalam asam 0,54%.
ABSTRACT
One of the plant has a healing effect for injury is Annona reticulata L., family Annonaceae. The aim of this research for making Annona reticulata etanol exract to be nata de coco matrix form and gel wich tested in to injury on back rabbits.
Annona reticulata simplex was extracted with etanol for 5 days, serparated, maceration recidue on back for 2 days. Maserat obtained in evavoration with the help rotary evavoration. The extract was trapped in nata de coco matrix with soaking for 24 hours, than the freeze dryer . Next, the extract was formulated to gel used HPMC. Each Annona reticulata extract form nata de coco matrix and gel were tested in to rabbits which injured with length 2 cm with 0,25%, 0,5% and 0,75% extract. For the extract which trapped on the nata de coco matrix were given once a day, as control given the matrix without extract, and for gel given three times a day, as control given the basic gel, each of group were done to 6 rabbits in weight 1,5 to 2,0 kg.
The characteristics of Annona reticulata simplex has been done. The simplex characteristics obtanained were as follow : The water content was 8,64%, the water-soluble was 12,53%, the ethanol-soluble was the total ash 7,74%, and the acid –soluble ash was 0,54%.
DAFTAR ISI
JUDUL ... i
HALAMAN PENGESAHAN ... ii
ABSTRAK ... iii
ABSTRACT ... iv
DAFTAR ISI ... v
DAFTAR TABEL ... viii
DAFTAR GAMBAR... ix
DAFTAR LAMPIRAN ... x
BAB I PENDAHULUAN 1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 3
1.5 Manfaat Penelitian... 4
BAB II TINJAUAN PUSTAKA 2.1 Uraian tumbuhan ... 5
2.1.1 Habitat ... 5
2.1.2 Morfologi tumbuhan ... 5
2.1.3 Sistematika tumbuhan ... 6
2.1.4 Nama daerah... 6
2.1.5 Kandungan kimia... 6
2.1.5 Khasiat tumbuhan ... 6
2.2 Ekstraksi ... 7
2.3 Gel ... 8
2.3.1 HPMC ... 10
2.3.2 Propilenglikol ... 11
2.3.3 Metilparaben... 12
2.4 Nata De Coco ... 13
2.5 Kulit ... 14
2.5.1 Fungsi kulit... 15
2.6 Absorbsi obat melalui kulit ... 16
2.7 Luka ... 17
2.8 Penyembuhan luka ... 18
BAB III METODOLOGI PENELITIAN 3.1 Alat-alat dan Bahan ... 21
3.1.1 Alat-alat yang digunakan ... 21
3.1.2 Bahan-bahan ... 21
3.2 Hewan Percobaan ... 21
3.3 Pengumpulan Sampel, Identifikasi dan Pengolahan Sampel ... 22
3.3.1 Pengumpulan sampel ... 22
3.3.2 Identifikasi tumbuhan ... 22
3.3.3 Pengolahan sampel ... 22
3.4 Pemeriksaan Karakteristik Simplisia ... 22
3.4.1 Pemeriksaan makroskopik ... 22
3.4.2 Penetapan kadar air ... 23
3.4.4 Penetapan kadar sari larut dalam etanol ... 24
3.4.5 Penetapan kadar abu total ... 24
3.4.6 Penetapan kadar abu yang tidak larut dalam asam ... 24
3.5 Pembuatan Ekstrak Etanol Daun Srikaya (EES) ... 24
3.6 Pembuatan Nata De Coco ... 25
3.6.1 Pembuatan bibit atau starter ... 25
3.6.2 Pembuatan nata de coco ... 25
3.7 Pembuatan Matriks Nata de coco ... 26
3.8 Pemerangkapan Ekstrak Dalam Matriks nata de coco ... 26
3.9 Pembuatan Sediaan Gel ... 26
3.10 Penentuan Mutu Fisik Sediaan Gel ... 27
3.10.1 Uji organoleptis... 28
3.10.2 Uji homogenitas ... 28
3.10.3 Penentuan pH sediaan ... 28
3.11 Pengujian Efek Penyembuhan Luka Sayat ... 28
3.12 Analisis Data ... 30
BAB IV HASIL DAN PEMBAHASAN 4.1 Hasil Pemeriksaan Karakteristik Simplisia dari Daun Srikaya ... 31
4.2 Hasil Pengeringan Nata De Coco Pemerangkapan dengan EES ... 32
4.3.1 Hasil pemeriksaan secara visual ... 32
4.3.2 Hasil uji organoleptis sediaan gel EES pada penyimpanan selama 28 hari ... 33
4.3.3 Hasil pengamatan pH ... 34
4.4 Hasil Uji Penyembuhan Luka Sayat ... 35
4.4.1 Hasil uji efek luka sayat EES yang diperangkapkan
pada matriks nata de coco dan kontrol... 35
4.4.2 Hasil uji efek penyembuhan luka sayat EES
pada sediaan gel dan kontrol ... 37
4.5 Hasil Analisis Variansi (ANAVA) ... 39
4.6 Hasil Uji Duncan ... 39
BAB V KESIMPULAN DAN SARAN
5.1 Kesimpulan ... 43
5.2 Saran ... 43
DAFTAR PUSTAKA
DAFTAR TABEL
Tabel Halaman
1. Formulasi sediaan gel dengan variasi konsentrasi
ekstrak daun srikaya ... 27
2. Hasil pemeriksaan karakteristik simplisia dari daun srikaya ... 31
3. Hasil pengeringan NDC dan pemerangkapan EES ... 32
4. Hasil pengamatan sediaan gel secara visual ... 33
5. Hasil pengamatan perubahan konsistensi, warna dan bau sediaan gel ... 34
6. Hasil pengukuran sediaan gel selama penyimpanan ... 34
7. Data rata-rata data perubahan panjang luka sayat (cm) hari ke 1–11 dengan menggunakan matriks nata ESS dan kontrol ... 35
8. Data rata-rata data perubahan panjang luka sayat (cm) hari ke 1–11 dengan menggunakan sediaan gel ESS dan kontrol ... 37
DAFTAR GAMBAR
Gambar Halaman
1. Struktur kimia HPMC ... 11
2. Struktur kimia propilenglikol ... 12
3. Struktur kimia metal paraben ... 12
4. Grafik hasil pengamatan pH sediaan gel selama 28 hari
penyimpanan ... 19
5. Grafik panjang luka rata-rata versus waktu (hari)
pada pemberian EES/NDC ... 21
6. Grafik panjang luka rata-rata versus waktu (hari)
DAFTAR LAMPIRAN
Lampiran
Halaman
1. Hasil identifikasi tumbuhan ... 46
2. Gambar tumbuhan dan daun segar dari srikaya ... 47
3. Gambar simplisia daun srikaya ... 48
4. Contoh perhitungan penetapan kadar air serbuk simplisia daun srikaya ... 49
5. Contoh perhitungan penetapan kadar sari yang larut dalam air serbuk simplisia daun srikaya ... 50
6. Contoh perhitungan penetapan kadar sari yang larut dalam etanol serbuk simplisia daun srikaya ... 51
7. Contoh perhitungan penetapan kadar abu total serbuk simplisia daun srikaya ... 52
8. Contoh perhitungan penetapan kadar abu yang tidak larut dalam asam serbuk simplisia daun srikaya ... 53
9. Berat NDC kering... 54
10.Data hasil pemerangkapan EES 0,25%, 0,5%, dan 0,75 ... 55
11.Gambar matriks nata de coco basah dan telah diperangkapkan dengan ekstrak etanol daun srikaya (EES) ... 56
12.Sediaan gel dengan variasi konsentrasi ekstrak daun srikaya ... 57
13.Bagan pembuatan nata de coco dan pemerangkapan EES ... 58
14.Bagan kerja penelitian ... 59
15.Bagan pembuatan sediaan gel EES ... 60
16.Data perubahan panjang luka sayat hari ke 1- 11 menggunakan matriks nata yang telah diperangkapkan dengan EES ... 61
18.Gambar perubahan panjang luka yang diobati dengan EES yang diperangkapkan dengan matriks NDC dan sediaan gel pada hari ke
-1 ... 63
19.Gambar perubahan panjang luka yang diobati dengan EES yang diperangkapkan dengan matriks NDC dan sediaan gel pada hari ke
-3 ... 64
20.Gambar perubahan panjang luka yang diobati dengan EES yang diperangkapkan dengan matriks NDC dan sediaan gel pada hari ke
-5 ... 6-5
21.Gambar perubahan panjang luka yang diobati dengan EES yang diperangkapkan dengan matriks NDC dan sediaan gel pada hari ke
-7 ... 66
22.Gambar perubahan panjang luka yang diobati dengan EES yang diperangkapkan dengan matriks NDC dan sediaan gel pada hari ke
-9 ... 67
23.Gambar perubahan panjang luka yang diobati dengan EES yang diperangkapkan dengan matriks NDC dan sediaan gel pada hari ke
-11 ... 68
24.Hasil analisis variansi (ANAVA) panjang (cm) luka sayat
menggunakan matrik NDC ... 69
25.Hasil uji Duncan terhadap rata-rata perubahan panjang luka sayat
dengan menggunakan matriks NDC ... 70
26.Hasil analisis variansi (ANAVA) panjang (cm) luka sayat
menggunakan sediaan gel ... 71
27.Hasil uji Duncan terhadap rata-rata perubahan panjang luka sayat
ABSTRAK
Salah satu tumbuhan yang dapat digunakan sebagai obat luka adalah daun tumbuhan srikaya (Annona reticulata L.) famili Annonaceae. Tujuan penelitian ini adalah membuat ekstrak etanol daun srikaya menjadi sediaan dalam bentuk matriks nata de coco dan sediaan gel yang diuji terhadap luka sayat pada punggung kelinci.
Serbuk daun srikaya diekstraksi dengan pelarut etanol selama 5 hari, pisahkan, ampas di maserasi kembali selama 2 hari. Maserat yang diperoleh di uapkan dengan bantuan rotary evaporator. Ekstrak yang diperoleh diperangkapkan pada matriks nata de coco dengan cara merendam selama 24 jam kemudian di
freeze dryer. Selanjutnya ekstrak etanol di formulasi menjadi sediaan gel menggunakan HPMC sebagai dasar gel. Masing-masing ekstrak daun srikaya dalam bentuk matriks nata de coco dan sediaan gel di uji terhadap kelinci yang telah dibuat luka sayat sepanjang 2 cm dengan variasi konsentrasi 0,25%, 0,5% dan 0,75%. Untuk ekstrak yang diperangkapkan pada matriks nata de coco diberikan satu kali sehari, sebagai kontrol diberi matriks tanpa ekstrak sedangkan untuk sediaan gel diberi tiga kali sehari, sebagai kontrol diberi dasar gel, masing-masing kelompok dilakukan terhadap enam ekor kelinci dengan berat 1,5-2,0 kg. Terhadap daun srikaya dilakukan pemeriksaan karakterisasi simplisia. Hasil karakterisasi simplisia diperoleh kadar air 8,64%, kadar sari yang larut dalam air 12,53%, kadar sari larut dalam etanol 12,17%, kadar abu total 7,74% dan kadar abu tidak larut dalam asam 0,54%.
ABSTRACT
One of the plant has a healing effect for injury is Annona reticulata L., family Annonaceae. The aim of this research for making Annona reticulata etanol exract to be nata de coco matrix form and gel wich tested in to injury on back rabbits.
Annona reticulata simplex was extracted with etanol for 5 days, serparated, maceration recidue on back for 2 days. Maserat obtained in evavoration with the help rotary evavoration. The extract was trapped in nata de coco matrix with soaking for 24 hours, than the freeze dryer . Next, the extract was formulated to gel used HPMC. Each Annona reticulata extract form nata de coco matrix and gel were tested in to rabbits which injured with length 2 cm with 0,25%, 0,5% and 0,75% extract. For the extract which trapped on the nata de coco matrix were given once a day, as control given the matrix without extract, and for gel given three times a day, as control given the basic gel, each of group were done to 6 rabbits in weight 1,5 to 2,0 kg.
The characteristics of Annona reticulata simplex has been done. The simplex characteristics obtanained were as follow : The water content was 8,64%, the water-soluble was 12,53%, the ethanol-soluble was the total ash 7,74%, and the acid –soluble ash was 0,54%.
BAB I
PENDAHULUAN
1.1 Latar Belakang
Sejak zaman dahulu masyarakat Indonesia mengenal dan memakai
tanaman berhasiat obat yang merupakan salah satu upaya dalam penanggulangan
masalah kesehatan. Pengetahuan tentang tanaman obat merupakan warisan
budidaya bangsa berdasarkan pengalaman turun temurun yang telah diwariskan
oleh generasi terdahulu kepada generasi berikutnya (Wijayakusuma, 1992).
Salah satu jenis tumbuhan obat yang diketahui berkhasiat bagi kesehatan
adalah daun srikaya (Annona reticulata L.). Daun tumbuhan srikaya mempunyai khasiat dalam pengobatan yaitu memperlancar pencernaan, mematangkan bisul,
mengatasi diare, mengobati luka, disentri, bekas gigitan nyamuk, pemakaian luar
untuk borok, kudis, penyakit kulit lain dan antelmentik. (Rukmana, 2002).
Penapisan fitokimia daun srikaya menunjukkan adanya golongan senyawa
flavonoid, tanin katekat, kuinon, saponin dan steroid/triterpenoid. (Anonim 2010).
Senyawa tanin berfungsi sebagai adstringen yang dapat menciutkan pori-pori kulit
membentuk jaringan baru dan anti bakteri. Saponin mempunyai kemampuan
sebagai antiseptik yang berfungsi membunuh pertumbuhan mikroorganisme.
Flavonoid berfungsi sebagai anti inflamasi, anti bakteri, anti alergi dan anti
oksidan (Simon dan Kerry, 2000).
Sjamsuhidajat (1997) mendefinisikan luka sebagai hilang atau rusaknya
sebagian jaringan tubuh. Terminologi luka yang dihubungkan dengan waktu dapat
baru contohnya luka sayat (luka insisi), dan luka kronis contohnya luka bakar.
Pada luka sayat yang berlangsung 3 fase yaitu fase inflamasi, fase proliferasi dan
maturasi (Anonim, 2010). Senyawa-senyawa yang biasa digunakan sebagai
antiinflamasi dan anti bakteri adalah senyawa steroid, senyawa flavonoid, tanin
dalam bentuk bebas dan kompleks tanin-protein (Simon dan Kerry, 2000).
Bahan pembawa yang digunakan untuk sediaan topikal akan memiliki
pengaruh yang sangat besar terhadap adsorbsi obat dan memiliki efek yang
menguntungkan jika dipilih secara tepat (Lachman, 1994).
Nata de coco sebagai salah satu bahan hasil proses fermentasi
menggunakan Acetobacter xylinum yang dapat digunakan sebagai penghantar obat untuk tujuan pelepasan obat (Piluharto, 2003). Keberadaan zat berkhasiat lebih
lama dalam tubuh sehingga pemakaian dosis dapat lebih dioptimalkan.
Bakteri Acetobacter xylinum dapat membentuk nata jika ditumbuhkan dalam air kelapa yang sudah diperkaya dengan karbon dan nitrogen melalui proses
yang terkontrol. Bahan tambahan yang diperlukan oleh bakteri antara lain
karbohidrat sederhana, sumber nitrogen dan asam asetat (Anonim, 2008).
Berdasarkan hasil penelitian yang dilakukan oleh Mariani (2010), matriks
nata de coco dapat digunakan sebagai bahan pembawa dalam sediaan farmasi
dengan tujuan pelepasan terkontrol.
Dipasaran obat luka telah banyak beredar dalam bentuk gel dan krim, dari
jenis sediaan tersebut bentuk gel lebih banyak digunakan karena rasa dingin di
kulit, mudah mengering membentuk lapisan film sehingga mudah dicuci (Suardi,
Berdasarkan uraian diatas, penulis tertarik untuk melakukan penelitian
pemanfaatan ekstrak etanol daun srikaya (EES) dalam penyembuhan luka dengan
menggunakan matriks nata de coco dan gel terhadap luka buatan pada punggung
kelinci.
1.2 Perumusan masalah
1. Apakah karakterisasi simplisia daun srikaya yang digunakan sesuai
dengan Materi Medika Indonesia, 1989.
2. Apakah ekstrak etanol daun srikaya dapat dibuat dalam bentuk matriks
nata de coco dan sediaan gel.
3. Apakah ekstrak etanol daun srikaya dalam bentuk matriks nata de coco
dan gel dapat menyembuhkan luka.
1.3 Hipotesis
1. Hasil karakterisasi simpisia daun srikaya sesuai dengan Materi Medika
Indonesia, 1989.
2. Ekstrak etanol daun srikaya dapat dibuat dalam bentuk matriks nata de
coco dan sediaan gel.
3. Terdapat efek penyembuhan luka ekstrak etanol daun srikaya dengan
menggunakan matriks nata de coco dengan sediaan gel.
1.4 Tujuan
Adapun tujuan penelitian ini adalah sebagai berikut :
1. Mengetahui karakterisasi simplisia daun srikaya apakah memenuhi syarat
(Materi Medika Indonesia,1989).
2. Mengetahui apakah ekstrak daun srikaya dapat diperangkapkan pada
3. Mengetahui berapa dosis dan lamanya waktu penyembuhan luka
menggunakan ekstrak etanol daun srikaya dalam bentuk matriks nata dan
sediaan gel.
1.5 Manfaat
Manfaat penelitian adalah untuk memperoleh sediaan matiks nata de coco
dan sediaan gel ekstrak daun srikaya yang nantinya dapat digunakan oleh
BAB II
TINJAUN PUSTAKA
2.1Uraian Tumbuhan
2.1.1 Habitat
Tumbuhan srikaya (Annona reticulata L.) adalah tumbuhan yang tumbuh di benua Amerika terutama kawasan Amerika Tengah dan Amerika Selatan dan
juga di Asia tropis diantaranya Thailand, Malasia dan Indonesia. Di Indonesia
terdapat di berbagai daerah yang umumnya ditanam di pekarangan, dibudidayakan
dan mempunyai tinggi 2-7 meter (Rukmana,2002).
2.1.2 Morfologi
Ciri-ciri morfologi tumbuhan srikaya sebagai berikut (Yuniarti T, 2008):
Batang : Batang gilik, percabangan simpodial, ujung rebah, kulit batang coklat
muda.
Daun : Daun srikaya bulat memanjang, ujung dan pangkal runcing, tepi rata,
panjang 6-17cm dan lebar 2,5-7,5 cm, tangkai daun pendek, tulang
daun menyirip, permukaan bawah agak kasar, permukaan daun
warnanya hijau, bagian bawah hijau kebiruan.
Bunga : Bunga tunggal, dalam berkas 1-2 berhadapan atau disamping daun,
dasar bentuk tugu (tinggi), benang sari berjumlah banyak.
Buahnya : Buahnya berbentuk bola atau kerucut, permukaan berbenjol–benjol,
warnanya hijau berserbuk putih, jika sudah masak anak buah akan
memisahkan diri satu dengan yang lainnya, daging buah berwarna
2.1.3 Sistematika Tumbuhan
Divisio : Spermatophyta
Sub division : Angiospermae
Kelas : Dycotyledonae
Bangsa : Ranunculales
Suku : Annonaceae
Marga : Annona
Jenis : Annona reticulata L.,
2.1.4 Nama Daerah
Nama daerah dari tumbuhan srikaya adalah sebagai berikut: Delima
bintang, serikaya (Sumatera), sarikaya, srikaya, serkaya (Jawa), sarikaya
(Kalimantan), sirikaya, delima srikaya (Sulawesi), atisi (Maluku). (Yuniarti T,
2008)
2.1.5 Kandungan kimia
Akar dan kulit srikaya mengandung senyawa flavonoid, borneol,
camphor, terpen dan alkaloid, disamping itu akarnya juga mengandung saponin,
tannin dan polifenol. Biji mengandung minyak, resin, dan bahan beracun yang
bersifat iritan. Buah mengandung asam amino, gula buah dan mucilago (Anonim
2010).
2.1.6 Khasiat Tumbuhan
Akar berkhasiat sebagai antiradang, antidepresi, daun berkhasiat sebagai
astringen, antelmentik, antiradang, mempercepat pematangan bisul, asbes, kudis,
dan insektisida. Kulit kayu berkhasiat astringen dan tonikum. Buah muda
berkhasiat sebagai disentri dan gangguan pencernaan.
2.2 Ekstraksi
Ekstraksi adalah kegiatan penarikan kandungan kimia yang dapat larut
sehingga terpisah dari bahan yang tidak dapat larut dengan pelarut cair. Senyawa
aktif yang terdapat dalam berbagai simplisia dapat digolongkan ke dalam
golongan minyak atsiri, alkaloid, flavonoid dan lain-lain. Diketahuinya senyawa
aktif yang dikandung oleh simplisia akan mempermudah pemilihan pelarut dan
cara ekstraksi yang tepat. Simplisia yang lunak seperti rimpang dan daun mudah
diserap oleh pelarut, karena itu pada proses ekstraksi tidak perlu diserbuk sampai
halus. Simplisia yang keras seperti biji, kulit kayu dan kulit akar susah diserap
oleh pelarut, karena itu perlu diserbuk sampai halus (Depkes, 2000).
Menurut Depkes (2000), ekstraksi dapat dilakukan dengan berbagai cara.
1. Maserasi
Maserasi adalah proses penyarian simplisia dengan cara perendaman
menggunakan pelarut dengan pengadukan pada temperatur kamar. Maserasi
yang dilakukan pengadukan secara terus menerus disebut maserasi kinetic
sedangkan yang dilakukan pengulangan penambahan pelarut setelah dilakukan
penyarian terhadap maserat pertama dan selanjutnya remaserasi.
2. Perkolasi
Perkolasi adalah ekstraksi dengan pelarut yang selalu baru sampai sempurna,
umumnya dilakukan pada temperatur ruangan. Prosesnya terdiri dari beberapa
tahapan, yaitu pengembangan bahan, maserasi antara, dan perkolasi sebenarnya
3. Refluks
Refluks adalah ekstraksi dengan pelarut pada temperatur titik didihnya selama
waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan adanya
pendingin balik. Umumnya dilakukan pengulangan proses pada residu pertama
sampai 3-5 kali sehingga dapat termasuk proses ekstraksi sempurna.
4. Sokletasi
Sokletasi adalah ekstraksi menggunakan pelarut yang selalu baru, umumnya
dilakukan menggunakan alat khusus, sehingga terjadi ekstraksi kontinu dengan
jumlah pelarut relatif konstan dan adanya pendingin balik.
5. Digesti
Digesti adalah maserasi dengan pengadukan kontinu pada temperatur yang
lebih tinggi dari temperatur ruangan, yaitu 40-500C. 6. Infuns
Infus adalah ekstraksi dengan pelarut air pada temperatur penangas air (bejana
infus tercelup dalam penangas air mendidih, temperatur terukur 96-980C) selama waktu tertentu biasanya 15-20 menit.
7. Dekok
Dekok adalah infus pada waktu yang lebih lama (> 30omenit) dan temperatur sampai titik didih air.
2.3 Gel
Gel didefenisikan sebagai suatu sistem setengah padat yang terdiri dari
suatu dispersi yang tersusun baik dari partikel anorganik yang kecil atau moleikul
organik yang besar dan saling diresapi cairan. Gel umumnya merupakan suatu
merupakan dispersi koloid mempunyai kekuatan yang disebabkan oleh jaringan
yang saling berikatan pada fase terdispersi. Makromoleikul pada sediaan gel
disebarkan keseluruh cairan sampai tidak terlihat ada batas diantaranya, disebut
dengan gel satu fase. Jika massa gel terdiri dari kelompok-kelompok partikel kecil
yang berbeda maka gel ini dikelompokkan dalam dua fase (Ansel 1989).
Polimer–polimer yang biasa digunakan untuk membuat gel–gel farmasetik
meliputi gom alam tragakan, pectin, karagen, agar, asam alginat, serta bahan–
bahan sintesis dan semi sintesis seperti metil selulosa, hidroksimetilselulosa,
karboksimetilselulosa, dan karbopol yang merupakan polimer vinil sintesis
dengan gugus karboksil yang terionisasi. Gel dibuat dengan proses peleburan atau
diperlukan suatu prosedur khusus berkenaan dengan sifat mengembang dari gel
(Lachman., dkk, 1994).
Dasar gel yang umum digunakan adalah gel hidrofobik dan hidrofilik.
1. Dasar gel hidrofobik
Dasar gel hidrofobik umumnya terdiri dari partikel-partikel anorganik.
Bila ditambahkan kedalam fase pendispersi, hanya sedikit sekali interaksi
antara kedua fase. Berbeda dengan hidrofilik, bahan hidrofobik tidak
secara spontan menyebar tetapi harus dirangsang dengan prosedur yang
khusus (Ansel, 1989).
2. Dasar gel hidrofilik umumnya terdiri dari moleikul organik dari fase
pendispersi. Istilah hidrofilik berarti suka pada pelarut (air). Umumnya
daya tarik menarik pada pelarut bahan-bahan hidrofilik kebalikan dari
tidak adanya daya tarik menarik dari bahan hidrofobik. Sistem koloid
lebih besar (Ansel, 1989). Gel hidrofilik umumnya mengandung
komponen bahan pengembang, air, humektan dan bahan pengawet
(Voigt,1994).
Keuntungan sediaan gel :
Beberapa keuntungan sediaan gel (Voight, 1994) adalah sebagai berikut:
• Kemampuan penyebarannya baik pada kulit
• Efek dingin, yang dijelaskan melalui penguapan lambat dari kulit
• Tidak ada penghambatan fungsi rambut secara fisiologis
• Kemudahan pencuciannya dengan air baik
• Pelepasan obatnya baik.
Tingginya kandungan air dalam sediaan gel dapat menyebabkan terjadinya
kontaminasi mikrobial, yang secara efektif dapat dihindari dengan penambahan
bahan pengawet. Untuk upaya stabilisasi dari segi mikrobial disamping
penggunaan bahan-bahan seperti balsam, khususnya untuk basis in sangat cocok
pemakaian metil dan propil paraben yang umumnya disatukan dalam bentuk
larutan pengawet. Upaya lain yang dilakukan adalah perlindungan terhadap
penguapan yaitu untuk menghindari masalah pengeringan. Oleh karena itu untuk
menyimpannya lebih baik menggunakan tube. Pengisian kedalam botol, meskipun
telah tertutup baik tetap tidak menjamin perlindungan yang memuaskan (voigt,
1994).
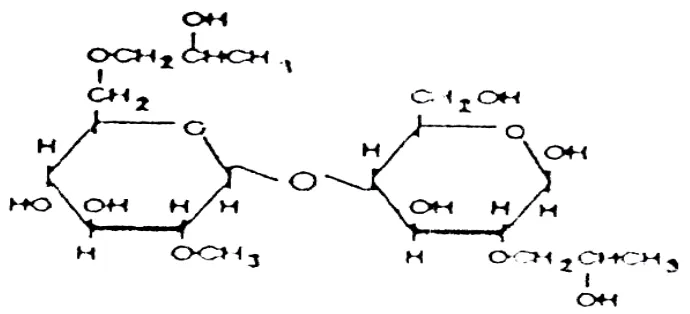
2.3.1 Hidroksi propil metilselulose (HPMC)
HPMC merupakan turunan dari metilselulosa yang memiliki ciri-ciri
serbuk atau butiran putih, tidak memiliki bau dan rasa. Sangat sukar larut dalam
menggumpal dan membentuk koloid. Mampu menjaga penguapan air sehingga
secara luas banyak digunakan. HPMC digunakan sebagai agen pengemulsi, agen
pensuspensi dan sebagai agen penstabil pada sediaan topikal seperti gel dan salep.
Sebagai koloid pelindung yang dapat mencegah tetesan air dan partikel dari
penggabungan atau agromerasi, sehingga menghambat pembentukan sedimen
(Rowe., dkk, 2005).
Gambar 1. Struktur kimia hidroksipropilmetilselulosa (HPMC) (Nisperos Carriedo dalam Krochta et al., 1994)
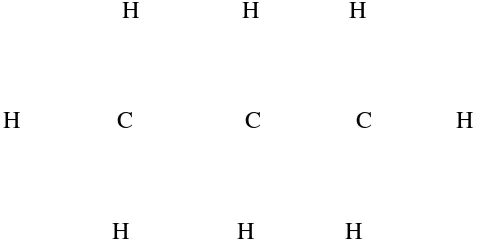
2.3.2 Propilen glikol
Propilen glikol banyak yang digunakan sebagai pelarut dan pembawa
dalam pembuatan sediaan farmasi dan kosmetik, khususnya untuk zat-zat yang
tidak stabil atau tidak dapat larut dalam air. Propilenglikol adalah cairan bening,
tidak berwarna kental dan hampir tdak berwarna, kental dan hampir tidak berbau.
Memiliki rasa manis sedikit tajam menyerupai gliserol. Dalam kondisi biasa
propilen glikol stabil dalam wadah yang tertutup baik, dan juga merupakan suatu
zat kimia yang stabil bila dicampur dengan gliserin, air dan alkohol.
klinis telah menunjukkan reaksi iritasi kulit pada permukaan propilen glikol
dibawah 10% dan dermatitis dibawah 2%. (Loden, 2009).
H H H
H C C C H
H H H
Gambar 2. Rumua bangun propilenglikol (Rowe.,dkk, 2005).
2.3.3 Metil paraben
Metil paraben memiliki ciri-ciri serbuk hablur halus, berwarna putih,
hampir tidak berwarna dan tidak mempunyai rasa kemudian agak membakar
diikuti rasa tebal (Depkes, 1979; Rowe.,dkk, 2005).
O OCH3
OH
Gambar 3. Rumus bangun Metil Paraben (Rowe., dkk, 2005)
Metil paraben banyak digunakan sebagai antimikroba dalam kosmetik,
prodak makanan dan formulasi farmasi dan baik digunakan dalam kombinasi
dengan antimikroba lain. Metil paraben meningkatkan aktivitas antimikroba
dengan panjangnya rantai alkil. Namun dapat menurunkan kelarutan terhadap air
meningkatkan kelarutan. Kemampuan pengawet metil paraben ditingkatkan
dengan penambahan propilenglikol (Rowe.,dkk, 2005).
2.4 Nata De Coco
Nata adalah produk hasil fermentasi menggunakan mikroba Acetobacter xylinum. Nata dapat dibuat dengan menggunakan bahan baku air kelapa, limbah air tahu, limbah industri nanas. Nata de coco adalah nata yang dibuat dengan
bahan baku air kelapa, sebenarnya tidak memiliki rasa, namun karena diolah
menjadi minuman dengan tambahan bahan-bahan perasa maka produk yang
dihasilkan mempunyai rasa yang enak (Suryani dkk, 2005). Nata de coco berasal
dari Filipina, kata coco berasal dari Cocos nucifera, nama latin dari kelapa. Sementara nama nata diambil dari nama tuan Nata yang telah berhasil
menciptakan nata de coco. Nata de coco memiliki bentuk padat, berwarna putih
seperti kolang-kaling dan terasa kenyal, yang mengandung air cukup banyak
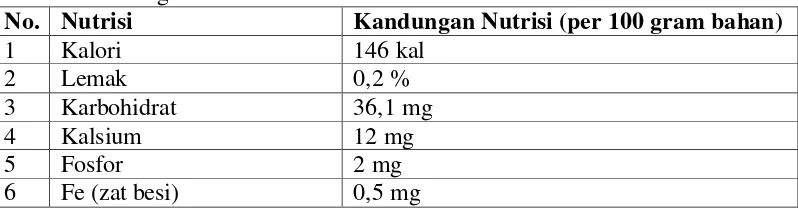
(80%), dan dapat disimpan lama. Nata de coco mengandung nilai nutrisi yang
cukup banyak (Warisno, 2004). Seperti terlihat pada Tabel 1 berikut:
Tabel 1. Kandungan nutrisi nata de coco
No. Nutrisi Kandungan Nutrisi (per 100 gram bahan)
1 Kalori 146 kal
Nata de coco adalah selulosa bakteri yang merupakan hasil sintesa dari
gula oleh bakteri pembentuk nata yaitu Acetobakter xylinum (Wahyudi, 2003). Bakteri Acetobacter xylinum dapat merubah gula sebesar 19% pada medium menjadi selulosa. Selulosa yang terbentuk dalam media tersebut berupa
Aktivitas pembuatan nata hanya terjadi pada kisaran pH antara 3,5-7,5. Sedangkan
pH optimum untuk pembentukan nata adalah 4. Suhu yang memungkinkan untuk
pembentukan nata adalah pada suhu kamar antara 28-32oC (Multazam, 2009).
Beberapa industri telah menggunakan selulosa bakteri, misalnya Sony
Corporation mengembangkan audio pembicara (Headphone) dengan
menggunakan selulosa bakteri. Pada awal 1980-an Johnson & Johnson
menggunakan selulosa bakteri sebagai pembawa obat dan perawatan luka.
Ajinomoto Co bersama dengan Mitsubishi Paper Mills di Jepang juga
mengembangkan selulosa bakteri untuk produk kertas (Brown, 1989).
2.5Kulit
Kulit merupakan organ besar yang berlapis-lapis, menutupi permukaan lebih
dari 20.000 cm2 yang mempunyai bermacam-macam fungsi dan kegunaan.
Merupakan jaringan pelindung yang lentur dan elastis, melindungi seluruh
permukaan tubuh dan mempunyai berat 5% dari berat total badan. Secara anatomi,
kulit terdiri dari banyak lapisan jaringan, tetapi pada umumnya kulit dibagi dalam
tiga lapisan jaringan yaitu: epidermis, dermis dan hipodermis (Lachman, dkk,
1994).
Lapisan epidermis terdiri atas :
1. Stratum korneum (lapisan tanduk)
Stratum korneum adalah lapisan kulit yang paling luar dan terdiri atas
beberapa sel yang mati, tidak berinti, dan protoplasmanya telah berubah
menjadi keratin (zat tanduk).
Stratum lusidum terdapat langsung di bawah stratum korneum, merupakan
lapisan sel tanpa inti.
3. Stratum granulosum
Statum granulosum merupakan 2 atau 3 lapis sel dengan sitoplasma
berbutir kasar dan terdapat inti sel diantaranya.
4. Statum granulosum terdiri atas beberapa sel berbentuk poligonal.
5. Stratum basalis terdiri atas sel–sel kubus yang tersusun vertikal dan
berbaris seperti pagar ( palisade ). (Acherman, 1987).
Dermis atau korium merupakan serabut kolagen yang bertanggung jawab
untuk sifat–sifat penting dari kulit. Dermis mengandung pembuluh darah,
pembuluh limfe, folikel rambut, kelenjar lemak, kelenjar keringat, otot dan
serabut saraf (Anief, 2000).
Lapisan sub kutan (hipodermis) merupakan lapisan kulit yang terdalam.
Lapisan ini terutamanya adalah lapisan adipose, yang memberikan bantalan dan
isolator panas (Anief 2000).
2.5.1 Fungsi kulit
Kulit menutupi dan melindungi permukaan tubuh dan bersambung dengan
selaput lender yang melapisi rongga-rongga dan lubang masuk. Kulit mempunyai
banyak fungsi yaitu di dalamnya tedapat ujung saraf peraba, membantu mengatur
suhu dan mengendalikan hilanggnya air dari tubuh, juga mempunyai sedikit
ekstori, sekretori dan absorbs (Pearce, 2004).
2.5.1 Kulit merupakan organ terbesar yang meliputi bagian luar dan dari seluruh
tubuh dan juga membentuk pelindung terhadap lingkungan. Bagian luar yang kuat
pada setiap bagian tubuh. Kulit mempertahankan karakterisasi fisiko kimia seperti
struktur, suhu, pH dan keseimbangan oksigen dan karbondioksida. Sifat asam dari
kulit ditemukan pertama sekali oleh Heus pada tahun 1882 dan kemudian
disahkan oleh Schade dan Marchionini pada tahun 1928, yang dianggap bahwa
keasaman digunakan sebagai pelindung dan menyebutnya sebagai “pelindung
asam” dan beberapa literature saat ini menyatakan bahwa pH permukaan kulit
sebahagian besar asam antara 5,4 dan 5,9.
Sebuah variasi permukaan pH kulit terjadi pada setiap orang karena tidak
semua permukaan kulit orang terkena kondisi yang sama seperti perbedaan cuaca.
Banyak penelitian mengatakan bahwa pH kulit alami adalah pada rata-rata 4,7 dan
sering dilaporkan bahwa pH kulit antara 5,0 dan 6,8, pH permukaan kulit tidak
hanya bervariasi di lokasi yang berbeda, tetapi dapat juga mempengaruhi profil
pH di stratum corneum. (Ansari.,dkk, 2009).
2.6Absorpsi Obat Melalui Kulit
Tujuan utama penggunaan obat topikal pada terapi adalah untuk menghasilkan
efek teraupetik pada tempat–tempat spesifik di jaringan epidermis dan dermis,
sedangkan obat–obat topikal tertentu seperti emoliens ( pelembab), antimikroba
dan deodorant terutama bekerja di permukaan kulit saja. Hal ini memerlukan
penetrasi difusi dari kulit atau absorbsi perkutan (Lachman, dkk., 1994).
Absorbsi obat melalui kulit umumnya disebabkan oleh penetrasi langsung
obat melalui stratum korneum yang terdiri dari kurang lebih 40% protein
(umumnya keratin) dan 40% air. Stratum korneum sebagai jaringan keratin
Jumlah obat dapat menyebrangi lapisan kulit tergantung pada konsentrasi
obat, kelarutannya dalam air. Bahan–bahan yang mempunyai sifat larut dalam
keduanya minyak dan air merupakan bahan yang baik untuk difusi melalui
stratum korneum seperti epidermis dan lapisan- lapisan kulit.
Penetrasi obat kedalam kulit dengan cara difusi adalah melalui :
a. Penetrasi transeluler (menyebrangi sel)
b. Penetrasi intraseluler (antarsel)
c. Penetrasi transappendageal yaitu melalui folikel rambut, keringat, dan
kelenjar lemak (Ansel, 1989).
Faktor-faktor yang mempengaruhi penetrasi kulit sangat bergantung dari
sifat fisika kimia obat dan juga bergantung pada zat pembawa, pH dan
konsentrasi. Perbedaan fisiologis melibatkan kondisi kulit yakni apakah kulit
dalam keadaan baik atau terluka, umur kulit, perbedaan spesies dan kelembaban
yang dikandung oleh kulit (Lachman, dkk., 1994).
2.7Luka
Luka merupakan rusaknya sebahagian dari jaringan tubuh. Luka sering sekali
terjadi dalam aktivitas sehari-hari. Berdasarkan penyebabnya luka dapat dibagi
atas karena zat kimia, luka termis dan luka mekanis. Pada luka mekanis
berdasarkan luka yang terjadi bervariasi bentuk dan dalamnya, sesuai dengan
benda yang mengenainya.
Terminologi luka yang dihubungkan dengan waktu penyembuhan dapat dibagi
menjadi :
• Luka akut : Luka dengan masa penyembuhan sesuai dengan konsep
baru, mendadak dan penyembuhannya sesuai dengan waktu yang
diperkirakan, contoh : Luka sayat, luka bakar, luka tusuk.
• Luka kronis : Luka yang mengalami kegagalan setelah penyembuhan,
dapat karena factor eksogen. Pada luka kronik luka gagal sembuh pada
waktu yang diperkirakan, tidak berespon baik terhadap terapi dan
punya tendensi untuk timbul kembali, contoh : ulkus dekubitus, ulkus
diabetic, ulkus venous dan lain-lain (Prabakti Yudhi, 2005).
2.8Penyembuhan Luka
Penyembuhan luka dipengaruhi oleh berbagai faktor, dan infeksi adalah sebab
yang paling penting dari penghambatan penyembuhan luka karena infeksi
mengakibatkan inflamasi dan dapat menyebabkan cidera jaringan. Rangsangan
eksogen dan endogen dapat menimbulkan kerusakan sel selanjutnya memicu
reaksi vaskuler kompleks pada jaringan ikat yang ada pembuluh darahnya. Reaksi
inflamasi berguna sebagai proteksi terhadap jaringan yang mengalami kerusakan
untuk tidak mengalami infeksi meluas tak terkendali. Proses inflamasi sangat
berhubungan erat dengan penyembuhan luka. Tanpa adanya inflamasi tidak akan
terjadi proses penyembuhan luka, luka akan tetap menjadi sumber nyeri sehingga
proses inflamasi dan penyembuhan luka akan cendrung menimbulkan nyeri.
(Anonim 2010)
Proses penyembuhan luka dibagi dalam tiga fase yaitu fase inflamasi
poliferasi dan penyudahan yang merupakan penyerupan kembali (remodeling)
1. Fase infamasi
Fase inflamasi berlangsung sejak terjadinya luka sampai hari
kelima. Pembuluh darah yang terputus pada luka menyebabkan
pendarahan, dan tubuh akan berusaha menghentikannya dengan
vasokontriksi. Pengerutan pembuluh yang terputus dan reaksi hemostatis.
Hemostatis tejadi karena trombosit yang keluar dari pembuluh darah saling
melengket dan bersamaan dengan jalan fibrin yang terbentuk membekukan
darah.
Sel mast dalam jaringan ikat menghasilkan serotonin dan histamin
yang meningkatkan fermiabilitas kapiler sehingga terjadi eksudasi cairan,
pembentukan sel radang disertai vasodilatasi setempat menyebabkan
pembengkakan.
2. Fase poliferasi
Fase poliferasi disebut juga fibroflasia karena yang menonjol adalah
proses poliferase fibrolas. Fase ini berakhir dari akhir fase inflamasi
sampai kira–kira akhir minggu ketiga. Pada fase ini serat kolagen yang
mempertahankan tepi luka.
3. Fase penyudahan
Pada fase ini terjadi proses pematangan yang terdiri dari penyerapan
kembali jaringan yang berlebih dan pembentukan jaringan baru, Fase ini
dapat berlangsung berbulan–bulan dan dinyatakan berakhir kalau semua
tanda radang sudah lenyap. Tubuh berusaha menormalkan kembali semua
yang menjadi abnormal karena proses penyembuhan (Sjamsuhidajat dan
Penyembuhan luka merupakan suatu proses penggantian jaringan yang
mati atau rusak dengan jaringan baru oleh tubuh dengan jalan regenerasi. Luka
dikatakan sembuh apabila permukaannya dapat bersatu kembali dan didapatkan
kekuatan jaringan yang mencapai normal. Setiap kejadian luka, mekanisme tubuh
akan mengupayakan mengembalikan komponen-komponen jaringan yang rusak
tersebut dengan membentuk struktur baru, dan fungsional sama dengan keadaan
sebelumnya. Proses penyembuhan tidak hanya terbatas pada proses regenarasi
yang bersifat lokal, tetapi juga sangat dipengaruhi oleh factor endogen seperti
umur, nutrisi, imunologi, pemakaian obat-obatan dan kondisi metabolik (Anonim
BAB III
METODOLOGI PENELITIAN
Metode yang digunakan dalam penelitian ini adalah metode eksperimental
meliputi penyiapan sampel, pemeriksaan karakterisasi simplisia, pembuatan
ekstrak, pembuatan nata de coco, pembuatan matriks nata, pemerangkapan ekstrak
ke dalam nata de coco, pembuatan sediaan gel dan pengujian efek penyembuhan
luka pada kelinci.
3.1 Alat dan Bahan
3.1.1 Alat-alat yang digunakan
Alat-alat yang digunakan dalam penelitian ini adalah alat- alat gelas
laboratorium, freeze dryer (Modulyo), inkubator (Gallenkamp), neraca analitik (Sartorius), neraca kasar (Ohaus), oven listrik (Fisher Scientific), penangas air
(Yenaco), pH indikator, rotary evaporator (Buchi, RE 111), pH meter, penangas air (Yenaco),
3.1.2 Bahan-bahan
Bahan yang digunakan dalam penelitian ini adalah daun tumbuhan srikaya
(Annona reticulata L.), air kelapa, akuades, asam asetat 25 %, etanol 80%, etanol 70%, gula pasir, HPMC 4000, lidokain® injeksi, NaOH, nipagin, propilenglikol,
stater (Acetobacter xylinum) dan urea.
3.2Hewan Percobaan
Hewan yang digunakan pada penelitian ini adalah kelinci dengan berat
badan 1,5-2 kg. Hewan dikarantina dalam kandang yang sesuai sebelum dan
3.3 Pengumpulan sampel, Identifikasi dan Pengolahan Sampel
3.3.1 Pengumpulan Sampel
Sampel yang digunakan adalah daun srikaya (Annona reticulata L.) yang masih segar, diperoleh dari Klumpang Kecamatan Hamparan Perak Deli Serdang.
Pengumpulan sampel dilakukan secara purposif yaitu tanpa membandingkan
dengan tumbuhan yang sama dari daerah lain.
3.3.2 Identifikasi Tumbuhan
Identifikasi tumbuhan dilakukan oleh Lembaga Ilmu Pengetahuan
Indonesia (LIPI) Pusat Penelitian dan Pengembangan Biologi, Bogor. Hasil
identifikasi tumbuhan dapat dilihat pada lampiran 1 halaman 46 .
3.3.3 Pengolahan Sampel
Daun srikaya yang telah dikumpulkan sebanyak 4 kg, dicuci bersih dengan
air mengalir, ditiriskan, dikeringkan di lemari pengering. Kemudian. daun
diserbuk dan disimpan di dalam wadah kering dan terlindung dari cahaya
matahari.
3.4 Pemeriksaan Karakterisasi Simplisia
Pemeriksaan karakteristik simplisia meliputi pemeriksaan makroskopik,
penetapan kadar air, penetapan kadar abu total, penetapan kadar abu tidak larut
dalam asam, penetapan kadar sari larut dalam air dan penetapan kadar sari larut
dalam etanol (Depkes, 1989).
3.4.1 Pemeriksaan makroskopik
Pemeriksaan makroskopik dilakukan terhadap simplisia meliputi warna,
bentuk, ukuran dan ketebalan. Gambar tumbuhan daun segar dapat dilihat pada
3.4.2 Penetapan Kadar Air
Penetapan kadar air dilakukan menurut metode Azeotropi (destilasi
toluen). Dimasukkan 200 ml toluen dan 2 ml air suling ke dalam labu alas bulat,
lalu didestilasi selama 2 jam. Setelah itu, toluen dibiarkan mendingin selama 30
menit, dan dibaca volume air pada tabung penerima dengan ketelitian 0,05 ml.
Kemudian ke dalam labu tersebut dimasukkan 5 g serbuk simplisia yang telah
ditimbang seksama, labu dipanaskan hati-hati selama 15 menit. Setelah toluen
mendidih, kecepatan tetesan diatur lebih kurang 2 tetes tiap detik sampai sebagian
besar air terdestilasi, kemudian kecepatan tetesan dinaikkan hingga 4 tetes tiap
detik. Setelah semua air terdestilasi, bagian dalam pendingin dibilas dengan
toluen. Destilasi dilanjutkan selama 5 menit, kemudian tabung penerima dibiarkan
mendingin pada suhu kamar. Setelah air dan toluen memisah sempurna, volume
air dibaca dengan ketelitian 0,05 ml. Selisih kedua volume air yang dibaca sesuai
dengan kandungan air yang terdapat dalam bahan yang diperiksa. (WHO, 1992).
3.4.3 Penetapan Kadar Sari Larut dalam Air
Sebanyak 5 g serbuk yang telah dikeringkan di udara, dimaserasi selama
24 jam dalam 100 ml air-kloroform (2,5 ml kloroform dalam air suling sampai 1
liter) dalam labu bersumbat sambil dikocok sesekali selama 6 jam pertama,
kemudian dibiarkan selama 18 jam, lalu disaring. Sejumlah 20 ml filtrat pertama
diuapkan sampai kering dalam cawan dangkal berdasar rata yang telah ditara dan
sisa dipanaskan pada suhu 105oC sampai bobot tetap. Kadar dalam persen sari yang larut dalam air dihitung terhadap bahan yang telah dikeringkan (Depkes,
3.4.4 Penetapan Kadar Sari Larut dalam Etanol
Sebanyak 5 g serbuk yang telah dikeringkan di udara, dimaserasi selama
24 jam dalam 100 ml etanol 95% dalam labu bersumbat sambil dikocok sesekali
selama 6 jam pertama, kemudian dibiarkan selama 18 jam. Kemudian disaring
cepat untuk menghindari penguapan etanol. Sejumlah 20 ml filtrat diuapkan
sampai kering dalam cawan dangkal berdasar rata yang telah ditara dan sisa
dipanaskan pada suhu 105oC sampai bobot tetap. Kadar dalam persen sari yang larut dalam etanol 95% dihitung terhadap bahan yang telah dikeringkan.
3.4.5 Penetapan Kadar Abu Total
Sebanyak 2 g serbuk yang telah dihaluskan dan ditimbang seksama
dimasukkan dalam krus porselin yang telah dipijar dan ditara, lalu diratakan. Krus
dipijarkan pada suhu 600ºC sampai arang habis, kemudian didinginkan dan
ditimbang sampai diperoleh bobot tetap. Kadar abu dihitung terhadap bahan yang
telah dikeringkan (Depkes, 1989).
3.4.6 Penetapan Kadar Abu Tidak Larut dalam Asam
Abu yang telah diperoleh dalam penetapan kadar abu total dididihkan
dalam 25 ml asam klorida 2 N selama 5 menit, bagian yang tidak larut dalam
asam dikumpulkan, disaring melalui kertas saring bebas abu kemudian dicuci
dengan air panas. Residu dan kertas saring dipijarkan pada suhu 600ºC sampai
bobot tetap, kemudian didinginkan dan ditimbang sampai bobot tetap. Kadar abu
tidak larut dalam asam dihitung terhadap bahan yang dikeringkan (Depkes, 1989).
3.5 Pembuatan Ekstrak Etanol Daun Srikaya (EES)
Pembuatan ekstrak dilakukan dengan cara maserasi menggunakan pelarut
wadah kaca berwarna gelap kemudian dimaserasi dengan pelarut etanol 80%
sampai seluruh serbuk terendam, ditutup dan disimpan pada suhu kamar selama 5
hari terlindung dari cahaya sambil sesekali diaduk, kemudian disaring sehingga
didapat maserat. Ampas dimaserasi kembali dengan etanol 80% selama 2 hari
menggunakan prosedur yang sama. Seluruh maserat digabungkan dan diuapkan
dengan bantuan alat rotary evaporator pada temperatur ± 400 C sampai diperoleh ekstrak yang agak kental, kemudian dipekatkan dengan freeze dryer pada suhu -400 C selama ± 24 jam. (Depkes, 1979). Bagan dapat dilihat pada lampiran 14 halaman 59.
3.6 Pembuatan Nata De Coco (NDC)
3.6.1 Pembuatan Bibit atau Stater
Sebanyak 2 liter air kelapa dibiarkan hingga kotorannya mengendap dan
disaring menggunakan kain kasa. Air kelapa ditambahkan urea sebanyak 10 g dan
gula pasir 400 g direbus di atas api yang besar hingga mendidih. Selama
perebusan, air kelapa diaduk. Setelah mendidih selama ± 15 menit, diangkat dan
didinginkan kemudian ditambahkan asam cuka 25 % hingga larutan ini memiliki
pH 4. Diaduk hingga larutan tercampur merata. Setelah dingin dimasukkan ke
dalam wadah yang steril, ditambahkan biakan murni sebanyak 400 ml. Ditutup
wadah dengan aluminium foil yang steril. Disimpan di ruang inkubasi dan
dibiarkan selama 1 minggu. Setelah 1 minggu, di permukaan media akan
terbentuk lapisan berwarna putih. Berarti stater sudah jadi dan siap digunakan
3.6.2 Pembuatan Nata De Coco
Sebanyak 1 liter air kelapa yang telah disaring dari pengotoran
ditambahkan urea sebanyak 5 g dan gula pasir 100 g kemudian direbus di atas api
yang besar hingga mendidih. Selama perebusan air kelapa diaduk. Setelah
mendidih selama ± 15 menit diangkat dan didinginkan. Setelah dingin
ditambahkan asam cuka 25 % hingga larutan ini memiliki pH 4. Masukkan larutan
ke dalam wadah yang telah disterilkan kemudian tambahkan biakan murni
sebanyak 100 ml. Ditutup wadah dengan aluminium foil yang steril dan disimpan
di ruang inkubasi selama 2 minggu (Warisno, 2004). Bagan dapat dilihat pada
lampiran halaman .
3.7 Pembuatan Matriks Nata
Nata de coco dicuci dengan NaOH 0,2 N kemudian dibilas dengan
akuades hingga bersih dan tiriskan. Nata de coco dipotong 2 x 3 x 1 cm kemudian
di freeze dryer sampai kering pada suhu -40oC selama ±24 jam. Kemudian nata ditimbang satu persatu.
3.8 Pemerangkapan ekstrak dalam matriks nata de coco
Masing-masing matriks nata de coco ditimbang kemudian direndam ke
dalam larutan EES 0,25%, EES 0,5% dan EES 0,75%. Masing-masing dibiarkan
selama 24 jam untuk memperoleh hasil perendaman optimal. Kemudian matriks
nata tersebut ditiriskan dan dikeringkan di freeze dryer selama ± 24 jam. Bagan dapat dilihat pada lampiran 13 halaman 58. Gambar dapat dilihat pada lamiran
halaman .
Pada pembuatan sediaan dengan konsentrasi ekstrak etanol daun srikaya
(EES) adalah 0,25%, 0,5% dan 0,75% sebagai basis gel digunakan HPMC 4000
yaitu dengan formula sebagai berikut:
HPMC 3,5
Propilenglikol 15
Metil paraben 0,18
Air suling sampai 100
m.f gel
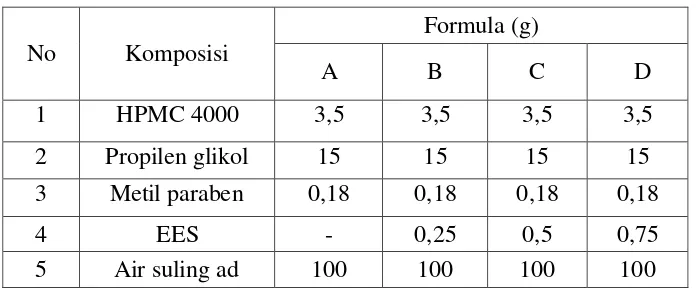
Tabel 1. Formulasi sediaan gel ekstrak etanol daun srikaya.
Keterangan:
Formula A: dasar gel EES; Formula B: gel EES 0,25%; Formula C: gel EES 0,5%; Formula D: gel EES 0,75% Cara Pembuatan :
HPMC dikembangkan ke dalam air panas sebanyak 20 kali beratnya
selama 15 menit. Setelah mengembang ditambahkan metil paraben yang telah
dilarutkan dalam propilenglikol. Dicukupkan dengan air suling dan digerus
homogen hingga diperoleh dasar gel. Ekstrak digerus dalam lumpang dengan
menambahkan etanol beberapa tetes sampai larut, lalu ditambahkan dengan dasar
No Komposisi
Formula (g)
A B C D
1 HPMC 4000 3,5 3,5 3,5 3,5
2 Propilen glikol 15 15 15 15
3 Metil paraben 0,18 0,18 0,18 0,18
4 EES - 0,25 0,5 0,75
gel dan diaduk hingga homogen (Suardi, dkk., 2008). Bagan pembuatan dapat
dilihat pada lampiran 15 halaman .
3.10 Penentuan Mutu Fisik Sediaan Gel
Penentuan mutu fisik sediaan gel daun srikaya dilakukan terhadap uji
organoleptis, homogenitas, penentuan pH sediaan yang dilakulkan selama 28 hari
dengan pengukuran setiap 4 hari (Herdiana, 2007; Farida, 2007).
3.10.1 Uji Organoleptis
Meliputi bentuk, warna, dan bau yang diamati secara visual.
3.10.2 Uji Homogenitas
Uji homogenitas dilakukan dengan cara menggunakan objek gelas.
Cara:
Sejumlah tertentu sediaan jika dioleskan pada sekeping kaca atau bahan
transparan lain yang cocok, sediaan harus menunjukkan susunan yang homogen
dan tidak terlihat adanya butir–butir yang kasar (Depkes, 1979).
3.10.3 Penentuan pH sediaan
Penentuan pH sediaan dilakukan dengan menggunakan pH meter
Cara :
Alat pH meter di kalibrasi menggunakan larutan dapar standar pH 4 dan
pH 7. Satu gram sediaan diencerkan dengan air suling hingga 10 ml. Elektroda pH
meter dicelupkan kedalam larutan yang diperiksa, pH meter dibiarkan bergerak
sampai menunjukkan posisi yang tetap. Angka yang ditunjukkan oleh pH meter
dicatat (Suardi, dkk, 2008).
Pengujian efek penyembuhan luka sayat terdiri atas 2 kelompok yaitu
kelompok 1 yang diberi EES yang diperangkapkan dengan matriks NDC
(kelompok A, B, C dan D) dan kelompok 2 yang diberi sediaan gel (kelompok E,
F, G dan H).
Kelompok 1 yang diberi matriks NDC
Kelompok A: Diberikan matriks (NDC)
Kelompok B: Diberikan EES konsentrasi 0,25%
Kelompok C: Diberikan EES konsentrasi 0,5%
Kelompok D: Diberikan EES konsentrasi 0,75%
Kelompok 2 yang diberi sediaan gel
Kelompok E: Diberikan dasar gel
Kelompok F: Diberikan gel EES konsentrasi 0,25%
Kelompok G: Diberikan gel EES konsentrasi 0,5%
Kelompok H: Diberikan gel EES konsentrasi 0,5%
Masing-masing kelompok dilakukan terhadap 6 ekor kelinci. Kelinci yang
digunakan adalah kelinci jantan dewasa dengan berat 1,5-2,0 kg.
Sebelum pengujian, bulu punggung kelinci dicukur dan dianestesi dengan
lidokain injeksi dosis 1 ml dan didesinfeksi menggunakan etanol 70%.
Selanjutnya dibuat sayatan sepanjang 2 cm dan kedalaman sampai subkutis (2
mm), luka sayatan dibersihkan, kemudian diberi perlakuan (Prabakti, 2005).
Untuk kelompok 1 diberikan 1 kali sehari dan ditutup dengan perekat. Untuk
kelompok 2 diberikan 3 kali sehari secara merata. Pengamatan dilakukan dengan
sembuh jika panjang luka mencapai nol setelah luka tertutup oleh jaringan baru.
Hasil dapat dilihat pada lampiran halaman .
3.12 Analisis Data
Data hasil pengujian efek EES matriks nata de coco dan sediaan gel
terhadap perubahan diameter rata-rata luka sayat dianalisis secara statistik
menggunakan metode ANAVA (Analisis Variasi ) dengan program Statistical
Product Services Solution (SPSS) dengan taraf kepercayaan 95 % dan dilanjutkan
dengan uji metode Duncan untuk mengetahui kelompok mana yang memiliki
pengaruh sama atau berbeda antara satu dengan yang lainnya. Hasil dapat dilihat
BAB IV
HASIL DAN PEMBAHASAN
Hasil identifikasi tumbuhan dilakukan oleh Pusat Penelitian dan
Pengembangan Biologi, Lembaga Ilmu Pengetahuan Indonesia (LIPI) adalah
tumbuhan daun srikaya (Anona reticulata L.) dari suku Annonaceae.
Ekstraksi dilakukan secara maserasi dengan pelarut etanol 80% untuk
menarik senyawa yang terdapat dalam simplisia. Hasil ekstraksi dari 750 g
diperoleh ekstrak etanol 90,5 g setelah di freezedryer.
4.1Hasil pemeriksaan karakteristik simplisia dari daun srikaya
Hasil karakterisasi dari simplisia dari daun srikaya terlihat pada tabel dan
hasil perhitungan dapat dilihat pada lampiran halaman.
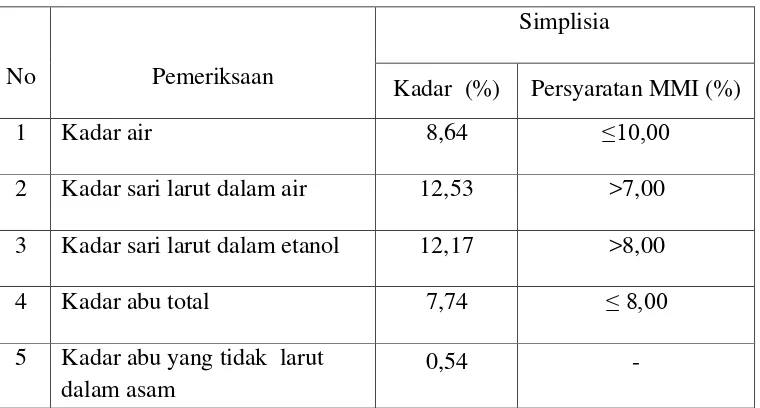
Tabel 2. Hasil pemeriksaan karakterisasi simplisia daun srikaya
(Annona reticulata L.)
No Pemeriksaan
Simplisia
Kadar (%) Persyaratan MMI (%)
1 Kadar air 8,64 ≤10,00
2 Kadar sari larut dalam air 12,53 >7,00
3 Kadar sari larut dalam etanol 12,17 >8,00
4 Kadar abu total 7,74 ≤ 8,00
5 Kadar abu yang tidak larut dalam asam
0,54 -
Penetapan kadar air dilakukan untuk mengetahui apakah simplisia
memenuhi persyaratan, karena air merupakan media yang baik untuk tumbuhnya
Penetapan kadar sari larut air adalah untuk mengetahui kadar senyawa yang
bersifat polar, sedang kadar sari larut dalam etanol dilakukan untuk mengetahui
senyawa yang terlarut dalam etanol, baik polar maupun non polar. Penetapan
kadar abu total dilakukan untuk mengetahui kadar senyawa anorganik dalam
simplisia, misalnya logam K, Ca, Na, Pb, Hg, silika, sedang penetapan kadar abu
tidak larut dalam asam dilakukan untuk mengetahui kadar senyawa yang tidak
larut dalam asam, misalnya silika, logam-logam berat seperti Pb, Hg.
4.2 Hasil Pengeringan Nata De Coco (NDC) dan Pemerangkapan Ekstrak
Tabel 3. Hasil pengeringan NDC dan pemerangkapan EES
No Berat NDC persegi panjang 2cmx3cmx1cm NDC
1. Berat kering rata-rata 0,0775 g
2. Berat rata-rata setelah pemerangkapan EES 0,25% 0,3926 g 3. Berat rata-rata setelah pemerangkapan EES 0,5% 0,3916 g 4. Berat rata-rata setelah pemerangkapan EES 0,75% 0,3918 g
Pada tabel di atas menunjukan bahwa NDC yang telah dikeringkan dapat
memerangkapkan ekstrak sebanyak 5 kali berat keringnya.
4.3 Hasil Pemeriksaan Gel
4.3.1 Hasil pemeriksaan secara visual
Hasil pemeriksaan homogenitas yang diamati secara visual
memperlihatkan bahwa semua sediaan homogen. Hasil formula sediaan gel dari
EES dilakukan terhadap sediaan yang baru dibuat, yang diamati secara visual,
Tabel 4. Hasil pengamatan sediaan gel secara visual
Formula Warna Bau Konsistensi
1 Bening khas HPMC Kental
Gel tanpa penambahan ekstrak berwarna bening sedangkan dengan
penambahan ekstrak dihasilkan sediaan gel berwarna kuning sampai coklat karena
ekstrak yang ditambahkan pada gel berwarna hijau coklat. Intensitas warna gel
bertambah dengan meningkatnya konsentrasi ekstrak yang ditambahkan. Bau khas
juga bertambah dengan meningkatnya konsentrasi ekstrak. Keempat formula yang
dibuat menghasilkan sediaan gel yang kental.
4.3.2 Hasil uji organoleptis sediaan gel EES pada penyimpanan selama 28 hari.
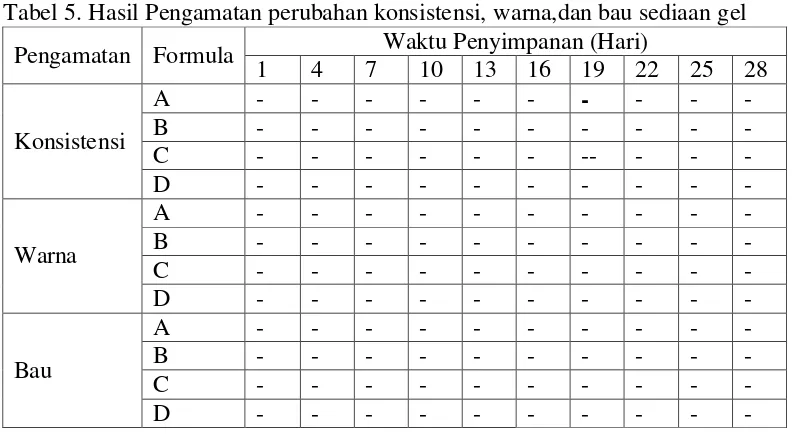
Tabel 5.Hasil Pengamatan perubahan konsistensi, warna,dan bau sediaan gel
Pengamatan Formula Waktu Penyimpanan (Hari)
Berdasarkan hasil pengamatan yang dilakukan terhadap sediaan gel EES
0,25%, 0,5% dan 0,75% dengan dasar gel tidak mengalami perubahan konsistensi,
warna maupun bau. Artinya bahwa sediaan gel yang dibuat stabil secara fisik.
4.3.3 Hasil pengamatan pH
Stabilitas gel juga dapat dilihat dari pH sediaan selama penyimpanan.
Hasil pengukuran pH sediaan gel EES dan hasil pengamatan selama
penyimpanan 28 hari pada tabel 6 gambar 4.
Tabel 6. Hasil pengukuran sediaan gel selama penyimpanan
Formula Waktu Penyimpanan (Hari)
1 4 7 10 13 16 19 22 25 28
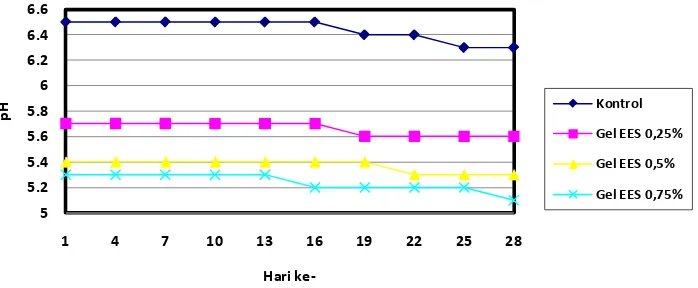
Gambar 4.Grafik hasil pengamatan pH sediaan gel selama 28 hari penyimpanan Berdasarkan pengukuran pH dari masing-masing formula, selama
pengamatan terjadi penurunan pH dan secara keseluruhan terlihat bahwa pH dari
sediaan gel EES menurun dengan bertambahnya waktu penyimpanan. Sediaan gel
untuk blanko tanpa penambahan EES juga mengalami penurunan pH. Hasil uji
menunjukkan pH sediaan tetap stabil pada penyimpanan karena masih berada
dalam range pH normal kulit yaitu 5,0-6,8 (Ansari, dkk., 2009).
4.4 Hasil Uji Penyembuhan Luka Sayat
Pengujian efek sediaan gel terhadap luka sayat pada kelinci, yaitu luka
dibuat sampai subkutis, yang ditunjukan oleh kerusakan seluruh bagian dermis.
Perubahan panjang luka sayat diukur sampai luka dinyatakan sembuh, dengan
interval waktu pengukuran 1 hari. Hasil dapat dilihat pada lampiran dan halaman
dan .
4.4.1 Hasil uji efek luka sayat ekstrak etanol daun srikaya yang diperangkapkan pada matriks nata de coco (EES/NDC).
Data pengamatan uji penyembuhan luka sayat EES 0,25%, 0,5% dan
0,75% yang diperangkapkan dalam matriks NDC dan juga kontrol dapat dilihat
pada tabel 7 dan hasil nya pada gambar 5 berikut:
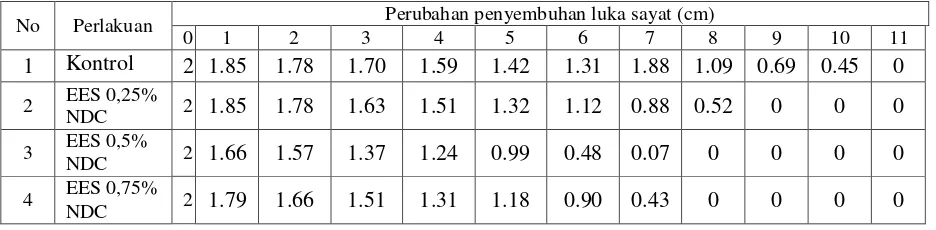
Tabel 7. Data rata-rata perubahan panjang luka sayat (cm) hari ke-1-11 dengan menggunakan EES/NDC.
No Perlakuan Perubahan penyembuhan luka sayat (cm)
0 1 2 3 4 5 6 7 8 9 10 11
Pada tabel di atas dapat dilihat adanya pengurangan panjang luka sayat
oleh masing-masing perlakuan. Dimana pada kontrol, pengurangan panjang luka
sayat pada hari ke-1 adalah 0,15 cm dan hari ke-11 0,45 cm. Data tersebut
menunjukkan bahwa pengurangan panjang luka sayat oleh matriks NDC sebagai
tidak mengandung zat berkhasiat dalam matriks NDC yang digunakan sebagai
bahan pembawa. Pada EES 0,25% NDC, pengurangan panjang luka sayat pada
hari ke-1 adalah 0,15 cm dan hari ke-9 adalah 0,52 cm. Hal ini menunjukkan
bahwa EES 0,25% NDC dapat menyembuhkan luka sayat lebih cepat dari pada
kontrol. Pada EES 0,75% NDC, pengurangan panjang luka sayat pada hari ke-1
adalah 0,21 cm dan hari ke-8 adalah 0,43 cm. Hal ini menunjukkan bahwa EES
0,75% NDC dapat menyembuhkan luka sayat lebih cepat daripada EES 0,25%
NDC dan kontrol. Pada EES 0,5% NDC, pengurangan panjang luka sayat pada
hari ke-1 adalah 0,34 cm dan hari ke-7 adalah 0,07 cm. Hal ini menunjukkan
bahwa EES 0,5% NDC dapat menyembuhkan luka sayat lebih cepat daripada EES
0,75% NDC, EES 0,25% NDC dan kontrol.
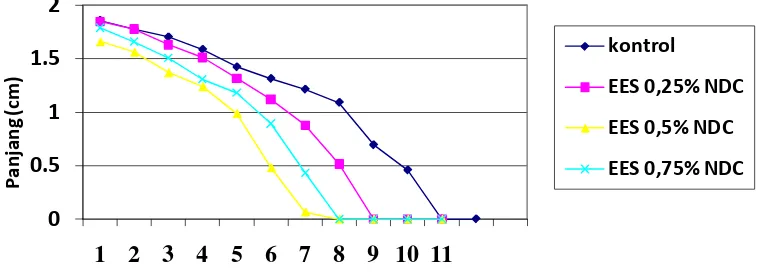
Gambar 5. Grafik panjang luka rata-rata versus waktu (hari) pada pemberian
EES/NDC
Pada grafik dapat dilihat bahwa kelompok kelinci yang paling cepat
sembuh adalah kelompok EES 0,5% NDC (C) pada hari ke-7 diameter luka sudah
0 (sembuh). Kelompok kelinci yang diberi EES 0,75% NDC (D) diameter
rata-rata luka sudah 0 pada hari ke 8. Kelompok kelinci yang diberi EES 0,25% NDC
(B) rata-rata hampir sembuh pada hari ke 9, Sedangkan kelompok kelinci yang
diberi matriks NDC atau kontrol (A) rata-rata pada hari 11 sembuh.
4.4.2 Hasil uji efek luka ekstrak etanol daun srikaya pada sediaan gel.
Data pengamatan uji penyembuhan luka sayat yang diberi EES 0,25%,
0,5% dan 0,75% yang diformulasi dalam sediaan gel dan juga kontrol dapat
dilihat pada tabel 8 dan hasil nya pada gambar 6 berikut:
Tabel 8. Data rata-rata perubahan panjang luka sayat (cm) hari ke 1-11 dengan menggunakan gel EES dan kontrol.
No Perlakuan Perubahan penyembuhan luka sayat (cm)
0 1 2 3 4 5 6 7 8 9 10 11
Pada tabel di atas dapat dilihat adanya pengurangan panjang luka sayat
oleh masing-masing perlakuan. Dimana pada kontrol, pengurangan panjang luka
sayat pada hari ke-1 adalah 0,1 cm dan hari ke-11 0,43 cm. Data tersebut
menunjukkan bahwa pengurangan panjang luka sayat oleh dasar gel sebagai
kontrol berlangsung lambat dengan waktu yang lama. Hal ini disebabkan karena
tidak ada zat berkhasiat dalam dasar gel yang digunakan sebagai bahan pembawa.
Pada gel ESS 0,25%, pengurangan panjang luka sayat pada hari ke-1 adalah 0,19
cm dan hari ke-9 adalah 0,5 cm. Hal ini menunjukan bahwa gel ESS 0,25% dapat
menyembuhkan luka sayat lebih cepat daripada kontrol. Pada gel EES 0,75%,
pengurangan panjang luka sayat pada hari ke-1 adalah 0,28 cm dan hari ke-8
menyembuhkan luka sayat lebih cepat daripada gel EES 0,25% dan kontrol. Pada
gel ESS 0,5%, pengurangan panjang luka sayat pada hari ke-1 adalah 0,34 cm dan
hari ke-6 adalah 0,51 cm. Hal ini menunjukkan bahwa gel EES 0,5% dapat
menyembuhkan luka sayat lebih cepat daripada gel EES 0,75%, gel EES 0,25%
dan kontrol.
Gambar 6. Grafik panjang luka rata-rata versus waktu (hari) pada pemberian gel.
Pada grafik dapat dilihat bahwa kelompok kelinci yang paling cepat
sembuh adalah kelompok yang diberi gel EES 0,5 % (G) pada hari ke 6 diameter
luka sudah 0 (sembuh). Kelompok kelinci yang diberi perlakuan gel EES 0,75%
(H) diameter rata-rata luka sudah 0 pada hari ke 7. Kelompok kelinci yang diberi
perlakuan gel EES 0,25% (F) rata-rata hampir sembuh pada hari ke 9, Sedangkan
kelompok kelinci yang diberi perlakuan dasar gel (E) rata-rata pada hari 11
sembuh.
Dari semua sediaan, bila dibandingkan antara matriks nata dengan sediaan
gel maka efek penyembuhan luka yang lebih cepat adalah EES 0,5% NDC (C)
sembuh pada hari ke-7 sedangkan pada gel EES 0,5% (G) sembuh pada hari ke 6.
contohnya gel mampu melekat pada permukaan tempat pemakaian dalam waktu
yang cukup lama sebelum sediaan ini dicuci atau dihilangkan (Lachman 1994).
Pada semua perlakuan EES dengan variasi konsentrasi yang
diperangkapkan dalam matriks nata de coco maupun dalam sediaan gel dapat
mempercepat penyembuhan luka sayat pada hewan percobaan. Pada EES yang
diperangkapkan dalam matriks NDC mempunyai efek penyembuhan luka sayat
lebih cepat yaitu konsentrasi 0,5% dengan waktu 7 hari. Begitu juga pada gel EES
yang mempunyai efek penyembuhan luka sayat lebih cepat yaitu konsentrasi 0,5%
dengan waktu 6 hari.
Kandungan senyawa kimia EES adalah tanin yang dapat berfungsi sebagai
adstringen yaitu menciutkan pori-pori kulit dan sebagai anti bakteri. Saponin
berfungsi sebagai antiseptik. Flavonoid berfungsi sebagai antiinflamasi,
antibakteri, anti oksidan. Steroid sebagai anti radang (Simon dan Kerry, 2000).
4.5 Hasil Analisis Variansi (ANAVA)
Berdasarkan hasil ANAVA, terdapat perbedaan secara signifikan (α ≤
0,05) terhadap penyembuhan luka sayat yang diberi dengan sediaan matriks nata
de coco dan sediaan gel pada hari ke 1-11. Ini menunjukkan bahwa kedua sediaan
tersebut mempunyai efek penyembukan luka. Hasil dapat dilihat pada lampiran
halaman dan lampiran halaman .
3.6 Hasil Uji Duncan
Untuk melihat kelompok perlakuan mana yang memiliki efek yang sama
atau berbeda dan efek terkecil sampai terbesar antara satu dengan yang lainnya,
dari hari ke 1-11. Hasil dapat dilihat pada lampiran 26 halaman dan lampiran 28
halaman .
Pada hari ke 1-3 EES 0,5% NDC (C) menunjukkan perbedaan yang
bermakana dengan EES 0,75% NDC (D), EES 0,25% NDC (B) dan matriks NDC
(A) tetapi EES 0,25% NDC (B) tidak berbeda secara signifikan dengan matriks
NDC (A). Pada pemberian sediaan gel menunjukkan bahwa gel EES 0,5% (G)
menunjukkan perbedaan yang bermakna dengan gel EES 0,75% (H), gel EES
0,25% (F) dan dasar gel (E).
Pada hari ke-4 EES 0,5% NDC (C) menunjukkan perbedaan yang
bermakna dengan EES 0,25% NDC (B) dan matriks NDC (A) tetapi EES 0,5%
NDC (C) tidak berbeda secara signifikan dengan EES 0,75% NDC (D) dan EES
0,25% NDC (B) tidak berbeda secara signifikan dengan matriks NDC (A). Pada
pemberian sediaan gel menunjukkan bahwa gel EES 0,5% (G) menunjukkan
perbedaan yang bermakna dengan gel EES 0,25% (F) dan dasar gel (E) tetapi gel
EES 0,5% (G) tidak berbeda secara signifikan dengan gel EES 0,75% (H). Gel
EES 0,75% (H) menunjukkan perbedaan yang bermakna pada dasar gel (E) tetapi
gel EES 0,75% (H) tidak berbeda secara signifikan dengan gel EES 0,25% (F)
(0,25%), gel EES 0,25% (F) tidak berbeda secara signifikan dengan gel E
(kontrol).
Pada hari ke-5 EES 0,5% NDC (C) menunjukkan perbedaan yang
bermakna dengan EES 0,75% NDC (D), EES 0,25% NDC (B) dan matriks NDC
(A), tetapi EES 0,75% NDC (D) tidak berbeda secara signifikan dengan EES
0,25% NDC (B) dan EES 0,25% NDC (B) tidak berbeda secara signifikan dengan