i
VALIDASI METODE SPEKTROFOTOMETRI ANALISIS
BILANGAN PEROKSIDA PADA MINYAK SAWIT DAN MINYAK
KELAPA DI PT FRISIAN FLAG INDONESIA
Tri Hayyu Majiida
DEPARTEMEN ILMU DAN TEKNOLOGI PANGAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR BOGOR
iii
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA*
Dengan ini saya menyatakan bahwa skripsi berjudul “Validasi Metode Spektrofotometri Analisis Bilangan Peroksida pada Minyak Sawit dan Minyak Kelapa di PT Frisian Flag Indonesia” adalah benar karya saya dengan arahan dari dosen pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tulisan ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, November 2013
ABSTRAK
TRI HAYYU MAJIIDA. Validasi Metode Spektrofotometri Analisis Bilangan Peroksida pada Minyak Sawit dan Minyak Kelapa di PT Frisian Flag Indonesia. Dibawah bimbingan SUGIYONO.
Validasi metode dilakukan untuk menjamin bahwa metode yang dilakukan sesuai peruntukkannya. Parameter yang digunakan dalam validasi metode spektrofotometri untuk analisis bilangan peroksida di Laboratorium Quality Control Departemen Kimia PT Frisian Flag Indonesia adalah linieritas, akurasi, presisi, batas deteksi instrumen, batas kuantitasi, dan stabilitas. Berdasarkan hasil pengujian didapatkan kurva kalibrasi dengan persamaan yang linier yakni y=0.591x + 0.004 dan koefisien korelasi sebesar 0.9999. Metode ini menghasilkan akurasi dengan persen perolehan kembali (recovery) sebesar 106.35%. Pengujian keseksamaan dilakukan dengan parameter keterulangan dan ketertiruan dan menghasilkan RSD yang memenuhi kriteria keterulangan dan ketertiruan. Nilai batas deteksi instrumen yang diperoleh sebesar 0.0192 mg/L, dan nilai batas kuantitasi yang diperoleh sebesar 0.0583 mg/L. Pengujian stabilitas larutan stok menunjukkan bahwa %diff larutan memenuhi kriteria diterimanya stabilitas yaitu berada pada kisaran -15% hingga 15%. Metode spektrofotometri untuk analisis bilangan peroksida ini telah memenuhi seluruh syarat keterterimaan sehingga metode ini valid dan dapat digunakan untuk analisis rutin sampel minyak nabati di Laboratorium Departemen Quality Control, PT Frisian Flag Indonesia plant Pasar Rebo.
v
ABSTRACT
TRI HAYYU MAJIIDA. Spectrophotometry Method Validation of Peroxide Value Analysis in Palm Oil and Coconut Oil in PT Frisian Flag Indonesia. Under supervision of SUGIYONO.
Method validation was performed to make sure that analysis method can be used for the intended purpose. The parameters used in the validation of spectrophotometric methods for the analysis of peroxide in the Quality Control Laboratory of the Department of Chemistry PT Frisian Flag Indonesia are linearity, accuracy, precision, the instrument detection limit, the limit of quantitation, and stability. As the results, the calibration curve had a linear equation y = 0.591x + 0.004 and correlation coefficient of 0.9999. This method had accuracy with recovery percentage at 106.35%. Precision including repeatability and reproducibility parameters had relative standard deviation that obtained a good repeatability and reproducibility conditions. The instrument detection limit was 0.0192 mg/L, and the limit of quantitation was 0.0583 mg/L. The stability of stock solvent was acquired the criteria %diff solvent in range -15% to -15%. Spectrophotometric method for the analysis of peroxide was in complianced with all terms acceptability so that this method was valid and can be used for routine analysis of samples of vegetable oils in the Laboratory Quality Control Department, PT Frisian Flag Indonesia Pasar Rebo plant.
i
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Teknologi Pertanian
pada
Departemen Ilmu dan Teknologi Pangan
VALIDASI METODE SPEKTROFOTOMETRI ANALISIS
BILANGAN PEROKSIDA PADA MINYAK SAWIT DAN MINYAK
KELAPA DI PT FRISIAN FLAG INDONESIA
Tri Hayyu Majiida
DEPARTEMEN ILMU DAN TEKNOLOGI PANGAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR BOGOR
iii
Judul Skripsi : Validasi Metode Spektrofotometri Analisis Bilangan Peroksida pada Minyak Sawit dan Minyak Kelapa di PT Frisian Flag Indonesia
Nama : Tri Hayyu Majiida NIM : F24090112
Disetujui oleh
Prof. Dr. Ir. Sugiyono, M.App.Sc Pembimbing
Diketahui oleh
Dr. Ir. Feri Kusnandar, M.Sc Ketua Departemen
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT atas segala karunia dan kemudahan yang diberikan kepada penulis sehingga skripsi ini berhasil diselesaikan. Skripsi ini merupakan hasil kegiatan magang yang penulis lakukan di PT Frisian Flag Indonesia. Kegiatan magang dilakukan selama empat bulan, dari Febuari hingga Mei 2013. Selama pelaksanaan magang dan penulisan skripsi ini, begitu banyak dukungan yang diberikan berbagai pihak, pada kesempatan ini penulis ingin menyampaikan rasa terima kasih kepada:
1. Bapak Prof. Dr. Ir. Sugiyono selaku pembimbing akademik yang selalu memberikan arahan dan dukungan kepada penulis.
2. Ibu Dr. Ir. Hanifah Nuryani Lioe dan Ibu Dr. Nancy Dewi Yuliana selaku dosen penguji, terima kasih atas seluruh ilmu yang diberikan.
3. Bapak Ramdani S. & Kelvin W. dari PT Frisian Flag Indonesia (FFI) selaku manajer QC dan Supervisor selama penulis melaksanakan magang, terima kasih telah memberikan kesempatan kepada penulis.
4. Keluarga tercinta, Ibu, kak Eda, kak Iya, abang Iqbal, Zac & Millie, serta Nyai&Datuk.
5. Seluruh dosen, staff, serta UPT Dept. ITP yang selalu memudahkan langkah selama di ITP.
6. Staf & Analis QC PT FFI, serta teman-teman PKL yang selalu membantu penulis: Diana, Olivia, Syarah, David, Ega, Selvi.
7. Sahabat-sahabat tercinta yang selalu mengingatkan dan memberikan dukungan lahir batin: Ayasho, Mila, Seno, Aca, Sobich, Iqbal, Ardy Brian, Putra, Chris, Fidil, Richard, Tika, Kyo, Aktris, DPPI Family, P3, pengurus Himitepa 2010-2012 dan semua keluarga ITP 46 yang menyenangkan dan selalu menjadi penyemangat untuk berangkat ke kampus.
8. Sahabat penulis dimanapun yang selalu memberi semangat : Satria, Ira, Nikko, Mudji, Novia, Nuril, Sonia, Devi.
Semoga karya ilmiah ini bermanfaat dan berkontribusi untuk kemajuan pangan Indonesia.
Bogor, Desember 2013
v
DAFTAR ISI
DAFTAR TABEL viii
DAFTAR GAMBAR viii
DAFTAR LAMPIRAN viii
PENDAHULUAN 1
Latar Belakang 1
Perumusan Masalah 2
Tujuan Penelitian 2
Manfaat Penelitian 2
METODE 3
Waktu dan Tempat Penelitian 3
Bahan 3
Alat 3
Tahapan Penelitian 3
HASIL DAN PEMBAHASAN 10
Uji Linieritas 10
Batas Deteksi Instrumen dan Batas Kuantitasi 11
Uji Kecermatan 12
Uji Keseksamaan 13
Stabilitas 18
SIMPULAN DAN SARAN 20
Simpulan 20
Saran 20
DAFTAR PUSTAKA 21
LAMPIRAN 23
DAFTAR TABEL
1 Rentang kriteria keterterimaan hasil recovery 8
2 Parameter uji, keterterimaan, serta hasil validasi 10
3 Hasil % recovery 12
4 Hasil uji keseksamaan dengan parameter keterulangan pada sampel
minyak sawit 13
5 Hasil uji keseksamaan dengan parameter keterulangan pada sampel
minyak kelapa 14
6 Hasil uji keseksamaan dengan parameter ketertiruan kadar bilangan peroksida yang dilakukan hari pertama pada sampel minyak sawit. 15 7 Hasil uji keseksamaan dengan parameter ketertiruan kadar bilangan
peroksida yang dilakukan pada hari ketiga sampel minyak sawit. 15 8 Hasil uji keseksamaan dengan parameter ketertiruan kadar bilangan
peroksida yang dilakukan hari keenam sampel minyak sawit. 15 9 Hasil uji keseksamaan dengan parameter ketertiruan kadar bilangan
peroksida yang dilakukan pada hari pertama sampel minyak kelapa. 16 10 Hasil uji keseksamaan dengan parameter ketertiruan kadar bilangan
peroksida yang dilakukan pada hari ketiga sampel minyak kelapa. 16 11 Hasil uji keseksamaan dengan parameter ketertiruan kadar bilangan
peroksida yang dilakukan pada hari keenam sampel minyak kelapa. 16 12 Hasil rerata, SD, dan RSD dari parameter ketertiruan intra-lab kadar
bilangan peroksida selama enam hari pada minyak sawit dan minyak
kelapa 18
13 Hasil pengukuran stabilitas larutan stok 18
DAFTAR GAMBAR
1 Diagram alir pengukuran bilangan peroksida dalam minyak dengan metode spektrofotometri (metode IDF 74A:1991 dengan modifikasi) 6 2 Kurva rerata linieritas standar FeCl3 menggunakan spektrofotometer 11
DAFTAR LAMPIRAN
1 Hasil pengukuran absorbansi larutan standar (uji linieritas) 23 2 Persamaan regresi linier kurva standar FeCl3 ulangan ke-1 hingga 6,
serta rerata persamaan kurva standar. 23
3 Perhitungan secara statistik simpangan baku regresi, intersep, dan
kemiringan 24
4 Penentuan limit deteksi instrument dan limit kuantitasi 24 5 Hasil pengukuran bilangan peroksida dan % recovery Anhydrous
Milk Fat untuk uji kecermatan 25
6 Hasil pengukuran bilangan peroksida minyak sawit untuk uji
keterulangan 25
7 Hasil pengukuran bilangan peroksida minyak kelapa untuk uji
vii
8 Contoh perhitungan bilangan peroksida 26
9 Hasil pengukuran bilangan peroksida minyak sawit hari pertama
untuk uji ketertiruan 26
10 Hasil pengukuran bilangan peroksida minyak sawit hari ketiga untuk
uji ketertiruan 27
11 Hasil pengukuran bilangan peroksida minyak sawit hari keenam
untuk uji ketertiruan 27
12 Hasil pengukuran bilangan peroksida minyak kelapa hari pertama
untuk uji ketertiruan 28
13 Hasil pengukuran bilangan peroksida minyak kelapa hari ketiga
untuk uji ketertiruan 28
14 Hasil pengukuran bilangan peroksida minyak kelapa hari keenam
untuk uji ketertiruan 28
15 Hasil pengukuran absorbansi, konsentrasi, serta %Diff larutan stok
PENDAHULUAN
Latar Belakang
Susu merupakan salah satu sumber gizi yang baik bagi manusia karena mengandung energi, protein, karbohidrat, lemak, mineral, vitamin, serta air sebagai bahan penyusun utama. Jika dipandang dari segi gizi, susu merupakan makanan yang hampir sempurna kandungan gizinya karena komposisi kandungan gizi yang terkandung dalam susu memiliki perbandingan yang sempurna sehingga susu mudah dicerna dan sangat baik untuk memenuhi kebutuhan gizi segala usia dari balita hingga lansia (Buckle et al 2007). Menurut Fox dan McSweeny (1992), kualitas produk susu yang baik dapat dicapai dengan melakukan pengendalian mutu secara kontinyu dan menyeluruh mulai dari bahan baku, mutu kemasan, label pengemas, mutu proses produksi, mutu produk antara (intermediate product) sampai produk akhir yang siap dipasarkan.
Salah satu parameter kualitas mutu yang penting dan penentu nilai ekonomis pada susu adalah lemak. Fungsi utama lemak pada produk susu adalah sebagai penyedia energi untuk bayi yang baru lahir. Lemak pada susu juga penting sebagai sumber asam lemak esensial (asam lemak yang tidak bisa disintesis oleh hewan/ manusia, khususnya asam linoleat, C18:2) dan sebagai pelarut vitamin larut
lemak, serta untuk flavor (Fox dan McSweeney 1992). Selain lemak hewani yang secara alami terdapat dalam susu, produsen susu, khususnya susu rekonstitusi, biasanya melakukan penambahan ataupun substitusi minyak nabati sebagai pengganti lemak susu ke dalam produk susu rekonstitusi. Penambahan minyak nabati tersebut memungkinkan konsumen mendapat asupan lemak tidak jenuh dari minyak nabati seperti minyak sawit yang baik untuk kesehatan (Saragih 2012).
Minyak nabati yang bersifat tidak jenuh (banyak memiliki ikatan rangkap) rentan mengalami oksidasi (Winarno 2002). Menurut Chung et al. (2004), oksidasi pada minyak nabati memiliki pengaruh langsung terhadap penerimaan konsumen dan berdampak buruk terhadap lemak, protein, karbohidrat, pigmen, dan vitamin larut lemak, menyebabkan perkembangan off-flavour pada produk, kehilangan nilai gizi produk, perubahan warna produk, dan adanya kemungkinan diproduksinya komponen beracun. Oksidasi minyak menghasilkan senyawa peroksida yang menyebabkan kerusakan dan penurunan mutu berupa terjadinya ketengikan pada minyak. Ukuran ketengikan dapat diketahui dengan menentukan bilangan peroksida, semakin tinggi jumlah bilangan peroksida maka semakin tinggi pula tingkat ketengikan minyak (ASA 2000). Menurut SNI No. 1-2902-1992, jumlah bilangan peroksida maksimum pada sampel minyak kelapa yang diterima sebesar 5.0 mg Oksigen/g sampel (BSN 1992).
2
adalah konfirmasi suatu metode pengujian dan pengadaan bukti bahwa syarat-syarat tertentu dari suatu metode telah dipenuhi. Validasi perlu dilakukan oleh laboratorium terhadap metode yang termasuk dalam kriteria berikut: 1. Metode non standar; 2. Metode yang dikembangkan sendiri; 3. Metode standar yang digunakan di luar lingkup yang dimaksud; 4. Metode standar yang dimodifikasi; 5. Metode standar untuk menegaskan dan mengonfirmasi bahwa metode tersebut sesuai dengan penggunaannya. Penentuan bilangan peroksida minyak sawit dan minyak kelapa menggunakan metode yang secara baku diperuntukkan untuk menentukan nilai bilangan peroksida anhydrous milk fat termasuk ke dalam kriteria metode standar yang telah dimodifikasi serta digunakan di luar lingkup yang dimaksud. Validasi perlu dilakukan untuk memastikan bahwa metode analisis yang dilakukan sudah sesuai peruntukkannya, serta menjamin hasil yang didapatkan dari analisis yang dilakukan dapat dipercaya.
Perumusan Masalah
Salah satu kegiatan yang dilakukan PT Frisian Flag Indonesia dalam menjamin mutu produk yang dihasilkan adalah analisis mutu kimia yang dilakukan di dalam laboratorium Quality Control. Kegiatan analisis yang dilakukan merujuk pada metode yang telah memenuhi standar dan diakui secara nasional/internasional. Metode analisis tersebut sebelumnya harus melalui tahapan validasi untuk menjamin keabsahan data yang dihasilkan selama metode dilakukan di dalam laboratorium Quality Control PT Frisian Flag Indonesia.
Tujuan Penelitian
Tujuan dari penelitian ini adalah melakukan validasi pengujian bilangan peroksida pada bahan baku berupa minyak sawit dan minyak kelapa dengan metode spektrofotometri agar kemudian metode ini dapat digunakan dalam laboratorium Quality Control PT Frisian Flag Indonesia dan dipercaya keabsahannya.
Manfaat Penelitian
3
METODE
Waktu dan Tempat Penelitian
Penelitian ini dilakukan selama 4 bulan, mulai dari 1 Februari 2013 sampai dengan 31 Mei 2013 di Laboratorium Kimia, Departemen Quality Control, PT Frisian Flag Indonesia, Jalan Raya Bogor KM.5, Pasar Rebo, Jakarta, 13160, Indonesia.
Bahan
Bahan-bahan yang digunakan pada analisis penentuan bilangan peroksida adalah sampel bahan baku minyak nabati berupa minyak sawit dan minyak kelapa, dan Anhydrous Milk Fat (AMF) yang dipesan khusus untuk ring test. Pereaksi-pereaksi yang digunakan berupa: campuran kloroform dan metanol kemurnian 99.8% (Baker Analyzed® A.C.S Reagent, Jerman) dengan perbandingan 70:30 ; FeCl2 (Baker Analyzed® Hydrate Reagent, Jerman) ; NH4SCN (Baker Analyzed®
Reagent, Jerman) ; serbuk besi(Baker Analyzed® Hydrate Reagent, Jerman); dan
HCl (Baker Analyzed® A.C.S Reagent, Jerman) 10 M, serta peroksida H2O2
(Baker Analyzed® A.C.S Reagent, Jerman) 30%.
Alat
Alat-alat yang digunakan pada analisis penentuan bilangan peroksida adalah: neraca analitik (Kern & Sohn, Jerman); pipet volumetrik (Baker®, Jerman); mikropipet (Thermo Scientific FinnpipetteTM Novus, USA); labu ukur 500, 100, dan 50 mL (Baker®, Jerman); labu ukur berwarna 50 dan 100 mL (Baker®, Jerman); serta spektrofotometer VIS (Hach tipe DR 2800-01B1, USA)
Tahapan Penelitian
Penelitian yang dilakukan terdiri atas penelitian pendahuluan dan penelitian utama. Penelitian pendahuluan mencakup analisis bilangan peroksida, kemudian dilakukan penelitian utama yaitu serangkaian proses validasi. Validasi yang dilakukan merupakan validasi parsial, sesuai kebutuhan laboratorium, parameter yang dikerjakan antara lain linieritas (linearity), kecermatan (accuracy), batas deteksi instrumen (instrument detection limit), batas kuantitasi (limit of quantitation), keseksamaan (precision), serta stabilitas (stability).
Penentuan Bilangan Peroksida
4
kemudian dapat mengompleks senyawa tiosianat dalam larutan ammonium tiosianat (NH4SCN) menjadi kompleks besi (III) tiosianat (FeSCN) yang
berwarna merah. Kepekatan senyawa besi (III) tiosianat dapat diukur absorbansinya secara optimal dengan spektrofotometer VIS pada panjang gelombang 500 nm (Dobarganes dan Velasco 2002). Menurut Shanta dan Decker (1994), metode penentuan bilangan peroksida dengan metode spektrofotometri berdasarkan standar IDF nomor 74A:1991 merupakan metode yang mudah, cepat, dan sensitif karena dapat mendeteksi konsentrasi senyawa peroksida hingga ketelitian 0.1 mgrek/kg sampel pada produk daging, unggas, susu, minyak nabati, hingga minyak ikan.
Pembuatan Larutan Amonium Tiosianat
Sebanyak 30 gram NH4SCN ditimbang dalam labu ukur 100 mL, dilarutkan
dan ditepatkan 100 mL dengan aquades. Pembuatan Larutan Stok Fe
Larutan stok Fedibuat dengan cara melarutkan 0.500 gram bubuk besi ke dalam 50 mL HCl 10 M, kemudian ke dalamnya ditambahkan 1-2 mL larutan hidrogen peroksida 30%. Larutan tersebut kemudian dipanaskan selama 5 menit untuk menghilangkan kelebihan peroksida. Larutan tersebut didinginkan hingga mencapai suhu kamar, kemudian ditepatkan dengan aquades dalam labu ukur 500 mL. Konsentrasi larutan ini sebesar 1 mg/mL atau 1000 g/L. Larutan stok Fe dengan konsentrasi 10 mg/L didapat dengan cara mengencerkan 1 mL larutan yang telah dibuat sebelumnya (konsentrasi 1000 g/L) dengan larutan campuran kloroform dan metanol ke dalam labu ukur 100 mL.
Untuk membuat serial larutan standar, ke dalam 5 labu ukur 50 mL masing-masing dipipet secara berurutan 0 mL, 5 mL, 10 mL, 15 mL, dan 20 mL larutan stok Fe 10 mg/L, ke dalamnya ditambahkan 0.25 mL larutan NH4SCN, dan
kemudian diencerkan dan ditepatkan dengan larutan campuran kloroform dan metanol. Serial larutan ini secara berturut-turut memiliki konsentrasi sebesar 0, 1, 2, 3, dan 4 mg/L. Setelah 5 menit, absorbansi masing-masing larutan diukur menggunakan spektrofotometer pada panjang gelombang 500 nm. Nilai korelasi minimal yang dapat diterima sebesar 0.999.
Pembuatan Larutan FeCl2
Sebanyak 0.35 gram FeCl2.4H2O dilarutkan ke dalam 100 mL aquades,
setelah itu ditambahkan 2 mL HCl 10 M.
Prosedur Analisis Bilangan Peroksida Sampel
Sebanyak 0.3 gram sampel dimasukkan ke dalam kuvet, ke dalamnya ditambahkan 10 mL campuran kloroform-metanol dan 0.05 mL larutan NH4SCN,
kemudian absorbansinnya diukur pada panjang gelombang 500 nm (E0). Sebanyak
0.05 mL larutan FeCl2 ditambahkan kemudian campuran tersebut dikocok.
Tunggu selama 5 menit kemudian absorbansinya diukur pada panjang gelombang 500 nm (E2). Campuran kloroform-metanol digunakan sebagai blanko.
Sebanyak 0.05 mL NH4SCN dan 0.05 mL FeCl2 ditambahkan ke dalam10
5 absorbansinya diukur pada panjang gelombang 500 nm (E1). Perbedaan
absorbansi (y) ditentukan dengan rumus :
y =E2-(E1+E0)
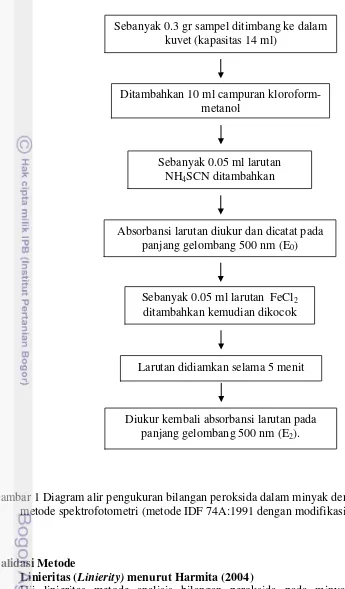
Perbedaan absorbansi sampel digunakan untuk menentukan konsentrasi Fe pada sampel berdasarkan kurva standar. Nilai perbedaan absorbansi kemudian dimasukkan ke dalam persamaan kurva standar ( y=a+bx ) dari serial larutan standar yang telah didapatkan sebelumnya untuk mengetahui konsentrasi Fe yang terbaca pada sampel. Konsentrasi sampel dari kurva standar (x) disebut juga m. Bilangan peroksida sampel (miligramekuivalen oksigen per kilogram) dapat ditentukan dengan rumus yang tertera di bawah ini, sedangkan diagram alir pengukuran kadar bilangan peroksida pada sampel dapat dilihat pada Gambar 1.
Keterangan :
m = konsentrasi Fe pada sampel (mg/L) mo = massa sampel (g)
55.84 = massa relatif Fe (g/mol) 1000 = faktor konversi ( 1000 g/kg)
6
Gambar 1 Diagram alir pengukuran bilangan peroksida dalam minyak dengan metode spektrofotometri (metode IDF 74A:1991 dengan modifikasi)
Validasi Metode
Linieritas (Linierity) menurut Harmita (2004)
Uji linieritas metode analisis bilangan peroksida pada minyak nabati menggunakan spektrofotometer dilakukan dengan melihat perolehan hasil kurva kalibrasi. Larutan standar FeCl3 dibuat pada konsentrasi berbeda yaitu 1 mg/L, 2
mg/L, 3 mg/L, 4 mg/L, ditambahkan ke dalamnya 0.25 mL larutan NH4SCN
hingga berwarna merah muda kemudian diukur absorbansinya pada panjang gelombang 500 nm. Masing-masing konsentrasi dibuat dan diukur absorbansinya sebanyak enam ulangan. Linieritas diukur dengan nilai R2 dari kurva hubungan
Sebanyak 0.3 gr sampel ditimbang ke dalam kuvet (kapasitas 14 ml)
Ditambahkan 10 ml campuran kloroform-metanol
Sebanyak 0.05 ml larutan NH4SCN ditambahkan
Absorbansi larutan diukur dan dicatat pada panjang gelombang 500 nm (E0)
Sebanyak 0.05 ml larutan FeCl2
ditambahkan kemudian dikocok
Larutan didiamkan selama 5 menit
7 antara absorbansi yang dibaca spektrofotometer (dengan blanko aquades) sebagai sumbu y, dan konsentrasi larutan standar sebagai sumbu x. Linieritas yang baik memiliki R2 ≥ ,97 SNI 2000) dan R2 ≥ ,99 A AC 1993). PT Frisian Flag Indonesia memiliki kriteria linieritas yang bisa diterima sebesar R2 ≥ 999
Batas Deteksi Instrumen (Instrument Detection Limit) dan Batas Kuantitasi (Limit of Quantitation) menurut ICH (2005)
Persamaan linier yang diperoleh dari uji linieritas selanjutnya digunakan untuk menghitung batas deteksi instrument (IDL) dan batas kuantitasi (LOQ). Menurut ICH (2005), batas deteksi (IDL) merupakan jumlah atau konsentrasi terkecil analit dalam contoh yang dapat dideteksi, namun tidak selalu kuantitatif sesuai dengan nilai sebenarnya. Batas kuantitasi merupakan parameter tes kuantitatif untuk senyawa berkadar rendah dalam matriks sampel, dan digunakan terutama untuk penentuan kotoran dan atau produk degradasi (ICH 2005). Berdasarkan ICH (2005), batas deteksi instrument dan batas kuantitasi ditentukan dari rerata kemiringan garis dan simpangan baku intersep kurva standar yang
LDI = Limit Detection of Instrument LOQ = Limit of Quantitation
Sa = Simpangan baku intersep
= rerata kemiringan garis kurva standar
Kecermatan (Accuracy) menurut Harmita (2004)
Uji kecermatan yang dilakukan pada penelitian ini dinyatakan dengan persen perolehan kembali (recovery) menggunakan sampel anhydrous milk fat (AMF) yang telah diketahui nilai benarnya. Menurut Codex (2007) AMF atau butteroil merupakan produk turunan dari susu, krim, atau mentega yang hampir seluruh kandungan air dan bahan non lemaknya dihilangkan. Secara spesifik menurut IDF standard 68A:1977, AMF harus mengandung sedikitnya 99.8% lemak susu dan dibuat dari krim atau mentega segar, serta tidak mengandung bahan tambahan lainnya (IDF 1977). AMF mengandung asam oleat sebesar 20-30% dari total asam lemak keseluruhan (Jensen 2002). AMF biasanya dikemas dalam kemasan 200 liter barel, dalam kemasan kedap berisi gas nitrogen, sehingga stabil dan dapat bertahan hingga satu tahun jika disimpan pada suhu 4oC. AMF berbentuk cair pada suhu di atas 36oC dan padat pada suhu di bawah 16oC (Bylund 1995).
8
perolehan kembali (recovery) dan menghitung akurasi anhydrous milk fat yang telah diketahui nilai benarnya (berdasarkan certificate of analysis).
Menurut Wood (1994), rentang kriteria keterterimaan hasil recovery pada setiap konsentrasi analit pada matriks dapat dilihat pada Tabel 1.
Tabel 1 Rentang kriteria keterterimaan hasil recovery Jumlah analit pada matrik
Keseksamaan (Precision) menurut Harmita (2004) dan EEC (2002). Keseksamaan adalah ukuran yang menunjukkan derajat kesesuaian antara hasil uji individual, diukur melalui penyebaran hasil individual dari rata-rata jika prosedur diterapkan secara berulang pada sampel-sampel yang diambil dari campuran yang homogen (Harmita 2004). Keseksamaan dapat dinyatakan sebagai keterulangan (repeatability) atau ketertiruan (reproducibility). Keterulangan adalah keseksamaan metode jika dilakukan berulang kali oleh analis yang sama pada kondisi sama dan dalam interval waktu yang pendek. Ketertiruan adalah keseksamaan metode jika dikerjakan pada kondisi yang berbeda. Analisis dilakukan terhadap sampel-sampel yang diduga identik yang dicuplik dari batch yang sama. Sampel yang digunakan dalam penelitian ini adalah minyak kelapa (Cocos nucifera), dan minyak sawit (Elaeis guineensis). Asam lemak dominan yang terdapat dalam minyak kelapa yaitu asam laurat dan asam miristat (Young 1983). Sedangkan asam lemak dominan dalam minyak sawit menurut Preeti et al. (2007) yaitu asam palmitat (43.45%), asam oleat (40.98%) dan asam linoleat (14.67%), sisanya asam stearat yaitu sebanyak 0.88% dari total asam lemak. Titik leleh minyak sawit yakni 31.38oC (Preeti et al. 2007).
9 RSD = Standar deviasi relatif
X = Nilai bilangan peroksida tiap ulangan
̅ = Rata-rata nilai bilangan peroksida sampel = jumlah ulangan
c = fraksi massa
Hasil yang didapat dari uji ketertiruan kemudian dapat diuji kembali sebagai parameter intra-laboratory reproducibility atau reprodusibilitas intra-lab. Menurut Directiva 2002/657/CE dari EEC (2002), untuk analisis yang dilakukan dibawah kondisi keterulangan (reproducibility), nilai RSD yang dihasilkan tidak boleh melebihi nilai RSD keterulangan yang telah ditentukan. RSD keterulangan didapatkan dari nilai RSD Horwitz dengan c adalah fraksi massa yang terbaca, dalam hal ini c= 10-6 karena fraksi massa yang digunakan adalah mg/kg, sehingga ditentukan nilai RSD keterulangan sebesar 16. Reprodusibilitas intra-lab juga menunjukkan kekuatan atau robustness suatu metode. Kekuatan atau robustness merupakan kapasitas metode analisis untuk tidak terpengaruh oleh adanya variasi parameter metode yang kecil. Menurut Harmita (2004), untuk memvalidasi kekuatan suatu metode perlu dibuat perubahan metodologi yang kecil dan terus menerus dan mengevaluasi respon analitik dan efek presisi dan akurasi.
Stabilitas Larutan Stok (Stability) menurut Chung et al. (2004)
Stabilitas larutan stok FeCl3 ditentukan dengan cara menghitung %diff
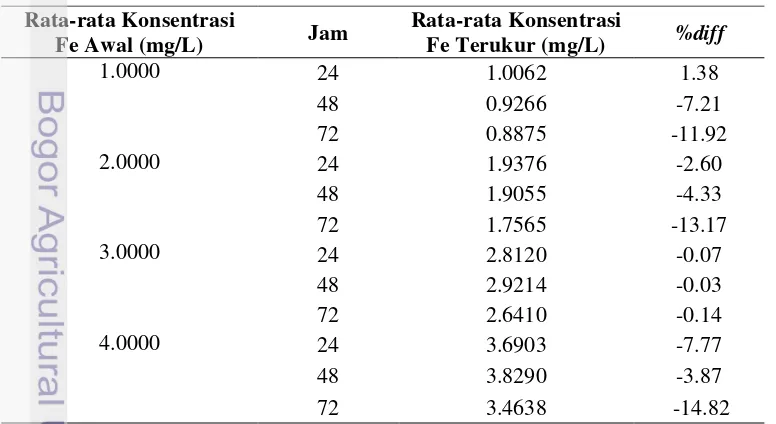
konsentrasi larutan (Chung et al. 2004). Pertama-tama konsentrasi larutan awal ditentukan dari absorbansi larutan standar. Kemudian ukur kembali absorbansi larutan pada saat selang waktu ke-24, 48, dan 72. Larutan dikatakan stabil jika % diff larutan berada pada kisaran -15% hingga 15%. Menurut Chung et al. (2004), persen diff larutan ditentukan dengan rumus sebagai berikut:
10
HASIL DAN PEMBAHASAN
Metode analisis bilangan peroksida yang dilakukan mengacu pada metode dalam standar International Dairy Federation nomor 74A:1991 untuk menentukan bilangan peroksida pada anhydrous milk fat (IDF 1991). Hal yang perlu diperhatikan dalam analisis bilangan peroksida menggunakan metode spektrofotometri menurut Shanta dan Decker (1994) adalah waktu inkubasi harus tepat selama 5 menit sebelum dilakukan pengukuran absorbansi larutan sampel yang telah ditambahkan seluruh reagen, karena intensitas warna larutan berubah seiring waktu. Sedangkan waktu optimum yang disarankan untuk menyelesaikan keseluruhan proses analisis adalah 10 menit (Hornero-Méndez et al. 2001). Perubahan warna terjadi karena ketidakstabilan FeCl2 ataupun karena oksidasi
lanjutan dari sampel (Jiang et al. 1992). Menurut Hornero-Méndez et al. (2001), metode IDF nomor 74A:1991 tidak memadai untuk dapat digunakan dalam menganalisis sampel yang memiliki kandungan karotenoid tinggi pada matriks lemak karena tumpang tindihnya spektrum cahaya fraksi karotenoid dan besi (III) tiosianat.
Secara umum, semakin rendah nilai bilangan peroksida, maka kualitas minyak semakin baik, akan tetapi nilai bilangan peroksida akan menurun seiring munculnya produk oksidasi sekunder dari minyak (Miller 2010). Peroksida merupakan produk utama autooksidasi yang dapat diukur dengan teknik berdasarkan pada kemampuannya mengoksidasi ion fero menjadi feri. Kandungannya diistilahkan dengan miliekuivalen oksigen per kg lemak, yaitu sejumlah oksigen yang diserap atau peroksida yang dibentuk untuk menghasilkan ketengikan dari berbagi macam komposisi minyak (Fennema 1985). Ringkasan hasil analisis selama dilakukannya validasi metode spektrofotometri dalam penentuan bilangan peroksida di PT Frisian Flag Indonesia disajikan pada Tabel 2.
Tabel 2 Parameter uji, keterterimaan, serta hasil validasi Parameter Uji Parameter
Akurasi Recovery 106.35% 80%-110%
Presisi RSDA memenuhi RSDA<0.67xRSDH
Batas Deteksi Instrumen IDL 0.0192 mg/L -
Batas Kuantitasi LOQ 0.0583 mg/L -
Stabilitas %Diff memenuhi (-15)% - 15%
Uji Linieritas
11 dilakukan dengan membuat larutan standar menggunakan larutan FeCl3 pada
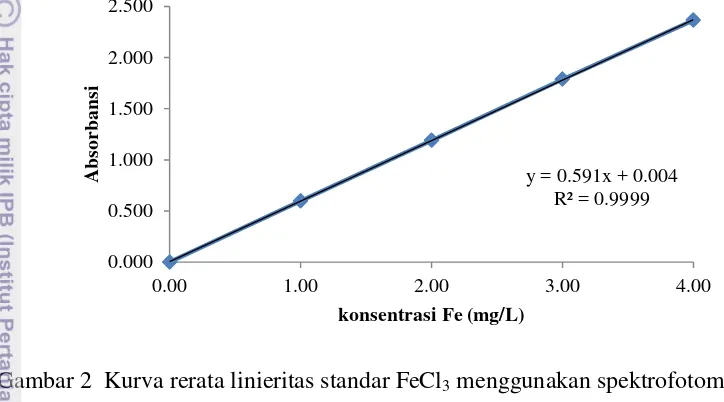
konsentrasi berbeda, yaitu 1 mg/L, 2 mg/L, 3 mg/L, dan 4 mg/L, dilakukan sebanyak enam kali ulangan. Linieritas pada analisis yang dilakukan diukur dengan nilai R2 dari kurva hubungan antara konsentrasi Fe3+ (sumbu x) dan absorbansi larutan yang terbaca oleh spektrofotometer (sumbu y). Hasil pengukuran dapat dilihat pada Lampiran 1, yang kemudian rerata hasil persamaannya diplotkan ke dalam sebuah kurva linieritas metode analisis pada Gambar 2.
Gambar 2 Kurva rerata linieritas standar FeCl3 menggunakan spektrofotometer
Berdasarkan kurva, diketahui rerata persamaan y= 0.591x+0.004, serta dihasilkan linieritas dengan R2 sebesar 0.9999. Nilai R2 yang dihasilkan telah memenuhi kriteria keterterimaan linieritas menurut SNI No. 19-17025-2008 tahun 2008 dan AOAC tahun 1993. Nilai R2 tersebut menunjukkan bahwa metode analisisis ini memiliki perbandingan yang proporsional karena telah memenuhi y y T F F I y ≥ 999
Batas Deteksi Instrumen dan Batas Kuantitasi
12
Berdasarkan hasil penghitungan, nilai batas deteksi instrumen yang diperoleh sebesar 0.0192 mg/L. Di bawah nilai tersebut instrumen tidak dapat membedakan sinyal antara blanko dan Fe3+. Nilai batas kuantitasi berdasarkan hasil penelitian adalah 0.0583 mg/L. Konsentrasi analit yang terukur di bawah nilai batas kuantitasi tidak dapat memberikan ketelitian dan ketepatan yang baik (ICH 2005). Hasil perhitungan batas deteksi dan batas kuantitasi selengkapnya tertera pada Lampiran 3 dan Lampiran 4.
Uji Kecermatan
Uji kecermatan yang dilakukan pada penelitian ini dinyatakan dengan menyatakan persen perolehan kembali (recovery) menggunakan sampel anhydrous milk fat (AMF) yang telah diketahui nilai benarnya. Uji ini dilakukan dengan cara mengukur nilai bilangan peroksida pada sampel AMF yang sama sebanyak enam kali. Data hasil pengukuran akurasi selengkapnya dapat dilihat pada Lampiran 5, sedangkan rangkuman hasil dapat dilihat pada Tabel 3.
Tabel 3 Hasil % recovery
Kecermatan dapat menunjukkan adanya galat sistematik yang dapat memengaruhi metode analisis. Galat sistematik dapat menyebabkan hasil analisis menjadi lebih besar atau lebih kecil. Beberapa contoh penyebab galat sistematik diantaranya adalah galat pada saat pengambilan contoh, kurva kalibrasi yang tidak linier, serta galat yang disebabkan oleh instrumen dan peralatan kaca yang digunakan (Harvey 2000). Rata-rata nilai bilangan peroksida (PoV) sampel yang terbaca pada enam kali ulangan analisis adalah sebesar 0.3187 mek O2/kg,
sedangkan nilai bilangan peroksida AMF yang sebenarnya tertera pada certificate of analysis adalah 0.3000 mek O2/kg, sehingga dihasilkan persen perolehan
13 Uji Keseksamaan
Keseksamaan adalah ukuran yang menunjukkan derajat kesesuaian antara hasil uji individual, diukur melalui penyebaran hasil individual dari rata-rata jika prosedur diterapkan secara berulang pada sampel yang diambil dari campuran yang homogen (Harmita 2004). Uji keseksamaan atau presisi pada penelitian dilakukan dengan parameter keterulangan (repeatability) dan ketertiruan (reproducibility) yang dinyatakan dalam bentuk nilai persen relatif standar deviasi (RSD). Uji ini dilakukan dengan cara mengukur nilai bilangan peroksida sampel sebanyak tujuh kali ulangan. Hasil uji dengan parameter keterulangan (repeatability) dapat dilihat pada Tabel 4 dan 5. Data selengkapnya dapat dilihat pada Lampiran 6 dan 7.
Tabel 4 Hasil uji keseksamaan dengan parameter keterulangan pada sampel minyak sawit
Ulangan PoV (mek O2/kg)
1 0.4792
2 0.4819
3 0.4781
4 0.4796
5 0.4754
6 0.4775
7 0.4850
Rata-rata 0.4795
SD 0.0031
RSD 0.6510
RSD Horwitz 2.2339
14
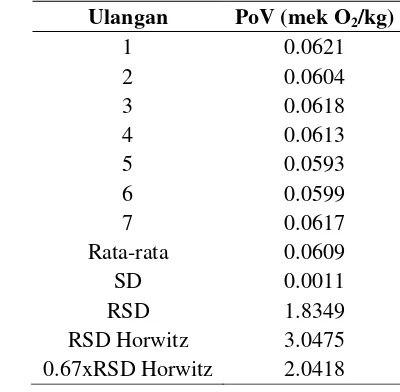
Tabel 5 Hasil uji keseksamaan dengan parameter keterulangan pada sampel minyak kelapa
Berdasarkan data yang didapat, metode spektrofotometri yang digunakan dikatakan memenuhi syarat keseksamaan dengan parameter keterulangan karena RSD analisis metode tersebut lebih kecil daripada 0.67 kali RSD Horwitz. Pada uji keseksamaan dengan parameter keterulangan dengan sampel minyak sawit didapatkan nilai RSD analisis sebesar 0.6510, nilai RSD Horwitz sebesar 2.2339 dan nilai 0.67 kali RSD Horwitz sebesar 1.4967. Hasil uji pada sampel minyak sawit tersebut memenuhi kriteria keseksamaan dengan parameter keterulangan yakni nilai RSD analisis yang didapat (0.6510) lebih kecil daripada nilai 0.67 kali RSD Horwitz (1.4967). Pada uji keseksamaan dengan parameter keterulangan dengan sampel minyak kelapa didapatkan nilai RSD analisis sebesar 1.8349, nilai RSD Horwitz sebesar 3.6035 dan nilai 0.67 kali RSD Horwitz sebesar 2.0418. Hasil uji sampel minyak kelapa tersebut memenuhi kriteria keseksamaan dengan parameter keterulangan yakni nilai RSD analisis yang didapat (1.8349) lebih kecil daripada nilai 0.67 kali RSD Horwitz (2.0418).
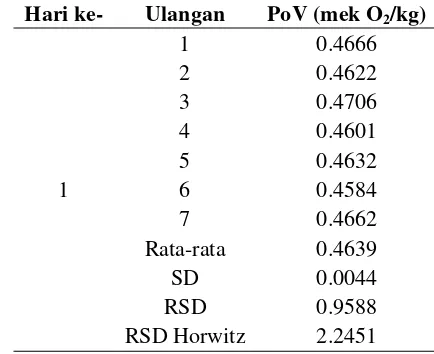
15 Tabel 6 Hasil uji keseksamaan dengan parameter ketertiruan kadar bilangan
peroksida yang dilakukan hari pertama pada sampel minyak sawit.
Hari ke- Ulangan PoV (mek O2/kg)
Tabel 7 Hasil uji keseksamaan dengan parameter ketertiruan kadar bilangan peroksida yang dilakukan pada hari ketiga sampel minyak sawit.
Hari ke- Ulangan PoV (mek O2/kg)
Tabel 8 Hasil uji keseksamaan dengan parameter ketertiruan kadar bilangan peroksida yang dilakukan hari keenam sampel minyak sawit.
16
Tabel 9 Hasil uji keseksamaan dengan parameter ketertiruan kadar bilangan peroksida yang dilakukan pada hari pertama sampel minyak kelapa.
Hari ke- Ulangan PoV (mek O2/kg)
Tabel 10 Hasil uji keseksamaan dengan parameter ketertiruan kadar bilangan peroksida yang dilakukan pada hari ketiga sampel minyak kelapa.
Hari ke- Ulangan PoV (mek O2/kg)
Tabel 11 Hasil uji keseksamaan dengan parameter ketertiruan kadar bilangan peroksida yang dilakukan pada hari keenam sampel minyak kelapa.
17 Pengolahan data yang dilakukan pada uji ketertiruan (repeatability) harus memenuhi syarat bahwa nilai RSD analisis metode lebih kecil daripada RSD Horwitz (Harmita 2004). Pada uji keseksamaan dengan parameter ketertiruan pengujian pada hari pertama dengan sampel minyak sawit didapatkan nilai RSD analisis sebesar 0.9588, sedangkan nilai RSD Horwitz sebesar 2.2451. Hasil uji pada sampel minyak sawit tersebut memenuhi kriteria keseksamaan dengan parameter keterulangan yakni nilai RSD analisis yang didapat (0.9588) lebih kecil daripada nilai RSD Horwitz (2.2451). Pengujian pada hari ketiga dengan sampel minyak sawit didapatkan nilai RSD analisis sebesar 1.3920, dan nilai RSD Horwitz sebesar 2.1909. Hasil uji pada sampel minyak sawit tersebut memenuhi kriteria keseksamaan dengan parameter keterulangan yakni nilai RSD analisis yang didapat (1.3920) lebih kecil daripada nilai RSD Horwitz (2.1909). Hasil uji keseksamaan minyak sawit dengan parameter ketertiruan pengujian pada hari keenam dengan sampel minyak sawit didapatkan nilai RSD analisis sebesar 0.8288, sedangkan nilai RSD Horwitz sebesar 2.1076. Hasil uji pada sampel minyak sawit tersebut memenuhi kriteria keseksamaan dengan parameter keterulangan yakni nilai RSD analisis yang didapat (0.8288) lebih kecil daripada nilai RSD Horwitz (2.1076).
Pada uji keseksamaan dengan parameter ketertiruan pengujian pada hari pertama dengan sampel minyak kelapa didapatkan nilai RSD analisis sebesar 1.2658, sedangkan nilai RSD Horwitz sebesar 2.5356. Hasil uji pada sampel minyak sawit tersebut memenuhi kriteria keseksamaan dengan parameter keterulangan yakni nilai RSD analisis yang didapat (1.2658) lebih kecil daripada nilai RSD Horwitz (2.5356). Pengujian pada hari ketiga dengan sampel minyak sawit didapatkan nilai RSD analisis sebesar 1.0461, dan nilai RSD Horwitz sebesar 2.3231. Hasil uji pada sampel minyak sawit tersebut memenuhi kriteria keseksamaan dengan parameter keterulangan yakni nilai RSD analisis yang didapat (1.0461) lebih kecil daripada nilai RSD Horwitz (2.3231). Hasil uji keseksamaan dengan parameter ketertiruan pengujian pada hari keenam dengan sampel minyak sawit didapatkan nilai RSD analisis sebesar 1.6633, sedangkan nilai RSD Horwitz sebesar 2.2532. Hasil uji pada sampel minyak sawit tersebut memenuhi kriteria keseksamaan dengan parameter keterulangan yakni nilai RSD analisis yang didapat (1.6633) lebih kecil daripada nilai RSD Horwitz (2.2532). Dari data di atas dapat dilihat bahwa nilai bilangan peroksida (peroxide value/PoV) meningkat seiring pertambahan waktu. Menurut Ankrah (1998), agar minyak kelapa memiliki umur simpan yang panjang, minyak harus disimpan dalam wadah tertutup rapat dan pada temperatur di bawah suhu kamar (kisaran 24-28oC). Hasil uji keseksamaan (presicion) menunjukkan hasil yang dapat diterima sesuai dengan standar penerimaan baik dari parameter keterulangan maupun ketertiruan, sehingga metode analisis ini dikatakan menghasilkan data yang seksama.
18
16. Berdasarkan hasil penelitian, nilai RSD analisis bilangan peroksida pada sampel minyak sawit yang didapat dari tiga kali pengukuran selama interval waktu enam hari yaitu sebesar 17.6319, sedangkan pada sampel minyak kelapa yaitu sebesar 30.5796, nilai tersebut tidak memenuhi syarat keterterimaan. Hal tersebut berarti hasil yang didapatkan tidak memenuhi keterterimaan presisi analitis jika dilakukan pada hari yang berbeda, dan tidak memenuhi kriteria kekuatan atau robustness.
Tabel 12 Hasil rerata, SD, dan RSD dari parameter ketertiruan intra-lab kadar bilangan peroksida selama enam hari pada minyak sawit dan minyak kelapa
Parameter Minyak sawit Minyak kelapa
Rerata PoV (mek O2/kg) pada
larutan standar dapat disimpan. Uji stabilitas larutan stok dilakukan dengan cara mengukur konsentrasi Fe3+ di dalam larutan stok FeCl3 yang disimpan dalam
lemari es (suhu 2-8 celcius) selama tiga hari berturut-turut. Mula-mula diukur konsentrasi Fe3+ pada jam ke-0, kemudian diukur lagi pada jam ke-24, 48, dan 72. Dari perbedaan konsentrasi kemudian didapatkan hasil %diff. Data hasil pengukuran kestabilan larutan standar dapat dilihat pada Tabel 13, sedangkan data perhitungan hasil pengukuran dapat dilihat selengkapnya pada Lampiran 15.
Tabel 13 Hasil pengukuran stabilitas larutan stok
20
SIMPULAN DAN SARAN
Simpulan
Pengujian linieritas dilakukan dengan cara membuat larutan standar FeCl3,
dan menghasilkan persamaan y= 0.591x + 0.004 dengan R2 sebesar 0.9999. Hasil tersebut memenuhi kriteria linieritas yang diterima yaitu R2≥0.999. Nilai batas deteksi instrumen (IDL) diperoleh sebesar 0.0192 mg/L, sedangkan nilai batas kuantitasi (LOQ) sebesar 0.0583 mg/L. Persen perolehan kembali (recovery) yang didapatkan dari hasil pengujian yaitu sebesar 106.32%, memenuhi syarat penerimaan akurasi yaitu recovery yang berkisar antara 80-110%. Pengujian keseksamaan dilakukan dengan parameter keterulangan dan ketertiruan, serta ketertiruan intra-lab. Hasil yang didapatkan untuk kedua sampel minyak sawitdan minyak kelapa memenuhi kriteria keterrulangan yakni nilai RSD analisis yang lebih kecil dari RSD Horwitz, serta memenuhi kriteria ketertiruan, yakni RSD analisisi lebih kecil dari 0.67 kali RSD Horwitz, sedangkan pada parameter ketertiruan intra-lab, nilai RSD analisis dari ulangan yang dilakukan tidak memenuhi syarat keterterimaan. Pengujian parameter ketertiruan intra-lab menunjukkan bahwa nilai RSD lebih kecil dari 16 sehingga menunjukkan tidak keterterimaan hasil presisis analitis pada hari yang berbeda. Stabilitas larutan stok yang diukur selama tiga hari pengukuran menunjukkan bahwa %diff larutan memenuhi kriteria diterimanya stabilitas yaitu berada pada kisaran -15% hingga 15%. Dengan demikian, dapat disimpulkan bahwa metode spektrofotometri yang digunakan untuk penetapan nilai bilangan peroksida ini memenuhi syarat keterterimaan yang telah ditetapkan sehingga metode ini valid dan dapat digunakan untuk analisis rutin sampel minyak nabati di Laboratorium Departemen QC PT Frisian Flag Indonesia, Plant Pasar Rebo.
Saran
21
DAFTAR PUSTAKA
Ankrah EK. 1998. Shelf life studies of oil samples of coconut (Cocos nucifera) in Ghana. Ghana Jnl Agric Sci 31:127-129.
Antolovich M, Prenzler PD, Patsalides E, McDonald S, Robards K. 2002. Methods for testing antioxidant activity. Analyst. 127:183-198
[AOAC] Association of Official Analytical Chemist. 1993. Official Method of The Association of Official Chemist. Virginia (US): AOAC Inc.
[ASA] American Soybean Association. 2000. Penentuan Bilangan Peroksida. Feed Quality Management Workshop, Ciawi.
[BSN] Badan Standarisasi Nasional. 1992. Minyak kelapa, SNI 01-2902-1992. Jakarta (ID): Badan Standarisasi Nasional.
________________________. 2008. Persyaratan umum kompetensi laboratorium pengujian dan laboratorium kalibrasi, SNI 19-17025-2008. Jakarta (ID): Badan Standarisasi Nasional.
Buckle RA, Edwards G, Fleet H, Wootton M. 2007. Ilmu Pangan. Jakarta (ID): UI Press.
Bylund G. 1995. Dairy Processing Handbook. Lund (SE): Tetra Pak Processing Systems AB.
Chung C C, Lee YC, Herman L, Xue-Ming Z. (ed). 2004. Analytical method validation and instrument performance verification. USA: A John Wiley & Sons, Inc
Chung HF, Colakoglu AS, Min DB. 2004. Relationship among headspace oxygen, peroxide value and conjungated diene content of soybean oil oxidation. Jnl of Food Sci 69(2):83-88.
[EEC] EUROPEAN ECONOMIC COMMUNITY. 2002. Commission decision executes the disposed in Directiva 2002/657/CE from council related to analytical methods performance and to results interpretation. Europ. Commun. Offic. J., v.657, 2002, p.L 221/8 – L 221/36.
Coupland JN, McClements DJ. 1996. Lipid oxidation in food emulsions. Trends in Food Sci and Tec 7(3):83–91.
Dobarganes MC, Velasco J. 2002. Analysis of lipid hydroperoxides. European J Lipid Sci Tec 104:420–428.
EURACHEM Guide. 1998. The Fitness for Purpose of Analytical Methods: a Laboratory Guide to Method Validation and Related Topics. EURACHEM: United Kingdom.
Fennema OR. 1985. Food Chemsitry. New York (US): Marcell Dekker, Inc. Fox PF, McSweeney PLH. 1992. Dairy Chemistry and Biochemistry. London
(GB): Blackie Academic & Professional.
Harmita. 2004. Petunjuk pelaksanaan metode validasi dan perhitungannya. Majalah Ilmu Kefarmasian 1(3): 117-135.
Harvey D. 2000. Modern Analytical Chemistry. Boston (US): McGraw-Hill. Hornero-Méndez D, Pérez-Gálvez A, Mínguez-Mosquera MI. 2001. A rapid
22
[IDF] International Dairy Federation. 1991. International Standard 74A, Method Determination of Peroxide Value in Anhydrous Milk Fat. Brussels (BE): International Dairy Federation, IDF.
______________________________. 1977. International Standard 68A, Anhydrous Milkfat, Anhydrous Butteroil or Anhydrous Butterfat, Butteroilor Butterfat, Ghee: Standards of Identity. Brussels (BE): International Dairy Federation, IDF.
[ICH] International Conference on Harmonization. 2005. Validation of Analytical Prosedures: Text and Methodology Q2(R1) [Diunduh 9 September 2013].
Tersedia pada :
http://www.ich.org/fileadmin/Public_Web_Site/ICH_Products/Guidelines/Qual ity/Q2_R1/Step4/Q2_R1__Guideline.pdf
Jensen RG. 2002. Invited review: The composition of bovine milk lipids: January 1995 to December 2000. Jnl of Dairy Sci. 85: 295-350.
Jiang Z, Hunt Y, Wolff S.P. 1992. Lipid oxidation. Anal. Biochem. 202:384-389. Miller M. 2010. Oxidation of food grade oils. Port Nelson (CA): Plant & Food
Research.
Preeti, Khetarpaul N, Jood S, Goyal R. 2007. Fatty acid composition and psycho-chemical characteristic of cooking oils and their blends. J Dairying Foods & H.S. 26(3/4):202-208.
Riuz A, Ayora-Canada MJ, Lendl B. 2001. Bead injection for surface enhanced Raman spectroscopy: automated on-line monitoring of substrate generation and application in quantitative analysis. Analyst. 126: 242–246.
Shanta NC, Decker EA. 1994. Rapid, sensitive, iron-based spectrophotometric methods for determination of peroxide values of food lipids. J of AOAC Int 77(2): 421-424.
Saragih F. Susu Kental Manis & Krimer Kental Manis. Food Rev Ind7(6).
Wood R. 1994. Proficiency testing and accreditation of food analysis laboratories. Conference on practical application of European legislation on foodstuffs. 1:55–65.
Winarno FG. 2002. Kimia Pangan dan Gizi. Jakarta (ID): PT. Gramedia Pustaka Utama.
23
LAMPIRAN
Lampiran 1 Hasil pengukuran absorbansi larutan standar (uji linieritas)
Konsentrasi
0 0.000 0.000 0.000 0.000 0.000 0.000 0.000
1 0.615 0.577 0.673 0.576 0.630 0.516 0.598
2 1.232 1.134 1.239 1.207 1.221 1.105 1.190
3 1.825 1.727 1.833 1.754 1.850 1.736 1.788
4 2.354 2.350 2.446 2.341 2.390 2.301 2.364
Lampiran 2 Persamaan regresi linier kurva standar FeCl3 ulangan ke-1 hingga 6,
24
Lampiran 3 Perhitungan secara statistik simpangan baku regresi, intersep, dan kemiringan
Lampiran 4 Penentuan limit deteksi instrument dan limit kuantitasi
IDL = 3.3 LOQ = 10
LDI = limit detection instrument LOQ = limit of quantitation Sa = Simpangan baku intersep
25 Lampiran 5 Hasil pengukuran bilangan peroksida dan % recoveryAnhydrous Milk
Fat untuk uji kecermatan
Lampiran 6 Hasil pengukuran bilangan peroksida minyak sawit untuk uji keterulangan
26
Lampiran 8 Contoh perhitungan bilangan peroksida
Contoh perhitungan bilangan peroksida pada minyak kelapa (lampiran 7)ulangan pertama.
Diketahui persamaan larutan standar: y = 0.582 x - 0.032 y = E2 - (E1+E0) = 0.031
x = m
V V
V
27 Lampiran 10 Hasil pengukuran bilangan peroksida minyak sawit hari ketiga untuk
uji ketertiruan
28
Lampiran 12 Hasil pengukuran bilangan peroksida minyak kelapa hari pertama untuk uji ketertiruan
Lampiran 13 Hasil pengukuran bilangan peroksida minyak kelapa hari ketiga untuk uji ketertiruan
29 Lampiran 15 Hasil pengukuran absorbansi, konsentrasi, serta %Diff larutan stok
selama 72 jam
Ulangan Absorbansi Konsentrasi %Diff
30
RIWAYAT HIDUP
Penulis memiliki nama lengkap Tri Hayyu Majiida. Lahir pada tanggal 2 Januari 1992 sebagai bungsu dari tiga bersaudara, anak pasangan Yusuf Helmi dan Widati ini menyelesaikan pendidikan dasar di SDN Pejaten Timur 07 Jakarta pada tahun 2003. Penulis menyelesaikan pendidikan menengah di SMPN 227 Jakarta pada 2006, dan SMAN 28 Jakarta pada tahun 2009. Pada tahun 2009 juga penulis diterima menjadi mahasiswi program studi S1 Ilmu dan Teknologi Pangan, Fakultas Teknologi Pertanian, Institut Pertanian Bogor melalui jalur Seleksi Nasional Masuk Perguruan Tinggi Negeri (SNMPTN).