PENGEMBANGAN METODE
KROMATOGRAFI CAIR KINERJA TINGGI PADA
PENETAPAN KADAR SIMVASTATIN TABLET
MENGGUNAKAN FASE GERAK ASETONITRIL : AIR
SKRIPSI
OLEH:
DIFA ANANDA
NIM 111524065
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
PENGEMBANGAN METODE
KROMATOGRAFI CAIR KINERJA TINGGI PADA
PENETAPAN KADAR SIMVASTATIN TABLET
MENGGUNAKAN FASE GERAK ASETONITRIL : AIR
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH: DIFA ANANDA
NIM 111524065
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
PENGESAHAN SKRIPSI
PENGEMBANGAN METODE
KROMATOGRAFI CAIR KINERJA TINGGI PADA
PENETAPAN KADAR SIMVASTATIN TABLET
MENGGUNAKAN FASE GERAK ASETONITRIL : AIR
OLEH: DIFA ANANDA
NIM 111524065
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: Juli 2014
Pembimbing I,
Drs. Fathur Rahman Harun, M.Si., Apt. NIP 195201041980031002
Pembimbing II,
Prof. Dr. rer.nat. E. De Lux Putra, SU., Apt.
NIP 195306191983031001
Panitia Penguji,
Prof. Dr. Siti Morin S, M.Sc., Apt. NIP 195008281976032002
Drs. Fathur Rahman Harun, M.Si., Apt. NIP 195201041980031002
Prof. Dr. Jansen Silalahi, M.App.Sc., Apt.
NIP 195006071979031001
Dra. Sudarmi, M.Si., Apt. NIP 195409101983032001
Medan, Juli 2014 Fakultas Farmasi
Universitas Sumatera Utara Dekan,
KATA PENGANTAR
Alhamdulillah, segala puji dan syukur kehadirat Allah SWT yang telah
melimpahkan rahmat, karunia dan ridhoNya, sehingga penulis dapat
menyelesaikan penelitian dan penyusunan skripsi yang berjudul “Pengembangan
Metode Kromatografi Cair Kinerja Tinggi Pada Penetapan Kadar Simvastatin
Tablet Menggunakan Fase Gerak Asetonitril : Air. Skripsi ini diajukan sebagai
salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara.
Pada kesempatan ini, penulis mengucapkan terima kasih yang tulus dan
ikhlas kepada Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan
Fakultas Farmasi Universitas Sumatera Utara yang telah memberikan fasilitas
sehingga penulis dapat menyelesaikan pendidikan. Bapak Drs. Fathur Rahman
Harun, M.Si., Apt., dan Bapak Prof. Dr. rer.nat. Effendy De Lux Putra, SU., Apt.,
selaku pembimbing yang telah memberikan waktu, bimbingan dan nasehat selama
penelitian hingga selesainya penyusunan skripsi ini. Ibu Prof. Dr. Siti M. Sinaga,
M.Sc., Apt., Ibu Dra. Sudarmi, M.Si., Apt., dan Bapak Prof. Dr. Jansen Silalahi,
M.App.Sc., Apt., selaku dosen penguji yang telah memberikan saran, arahan,
kritik, dan masukan kepada penulis dalam menyelesaikan skripsi ini. Bapak dan
Ibu staf pengajar Fakultas Farmasi USU Medan yang telah mendidik selama
perkuliahan.
Selain itu, penulis juga mengucapkan terima kasih dan penghargaan yang
tiada terhingga kepada Ayahanda Effendy A.S. dan Ibunda Adja Fauziah B.A
bagi kesuksesan penulis, juga kepada kakak, abang, dan teman-teman mahasiswa
Farmasi khususnya Farmasi Ekstensi 2011 yang selalu memberi doa, dorongan,
dan motivasi selama penulis melakukan penelitian.
Penulis menyadari bahwa penulisan skripsi ini masih belum sempurna,
sehingga penulis mengharapkan kritik dan saran yang membangun untuk
penyempurnaannya. Harapan saya semoga skripsi ini dapat bermanfaaat bagi ilmu
pengetahuan kefarmasian.
Medan, Juli 2014
Penulis,
Difa Ananda
PENGEMBANGAN METODE
KROMATOGRAFI CAIR KINERJA TINGGI PADA
PENETAPAN KADAR SIMVASTATIN TABLET
MENGGUNAKAN FASE GERAK ASETONITRIL : AIR
ABSTRAK
Simvastatin merupakan obat antihiperlidemia yang termasuk golongan penghambat HMC-CoA reduktase. Monografi sismvastatin tablet tidak terdapat pada Farmakope Indonesia edisi IV, tetapi pada USP 32 tahun 2009 penetapan kadar simvastatin dalam sediaan tablet ditentukan secara kromatografi cair kinerja tinggi (KCKT) dengan fase gerak asetonitril : buffer asetat dengan sistem isokratik, sedangkan pada penelitian sebelumnya menggunakan fase gerak asetonitril : air dengan sistem elusi gradien. Adapun kelemahan dari kedua metode tersebut adalah pemakaian buffer yang tidak ramah terhadap kolom dan pemakain sistem elusi gradien yang rumit. Tujuan penelitian ini adalah pengembangan metode penetapan kadar simvastatin tablet secara Kromatografi Cair Kinerja Tinggi (KCKT) yang lebih aman terhadap kolom dan relatif lebih mudah digunakan.
Penetapan kadar simvastatin tablet dilakukan dengan sampling purposif dengan menggunakan dua sediaan tablet generik dan dua sediaan tablet nama dagang. Penelitian ini menggunakan kolom Waters X-Bridge (250 x 4,6 mm) , fase gerak asetonitril : air berbagai perbandingan dengan sistem elusi isokratik, laju alir 1,5 ml/menit, suhu kolom 50ºC dan panjang gelombang 238 nm. Optimasi dilakukan dengan mengubah komposisi fase gerak asetonitril : air untuk mendapatkan hasil yang terbaik secara KCKT dengan parameter tailing factor, waktu retensi, nilai lempeng teori dan resolusi. Untuk menguji validitas metode ini, dilakukan uji validasi dengan parameter akurasi, presisi, batas deteksi dan batas kuantitasi.
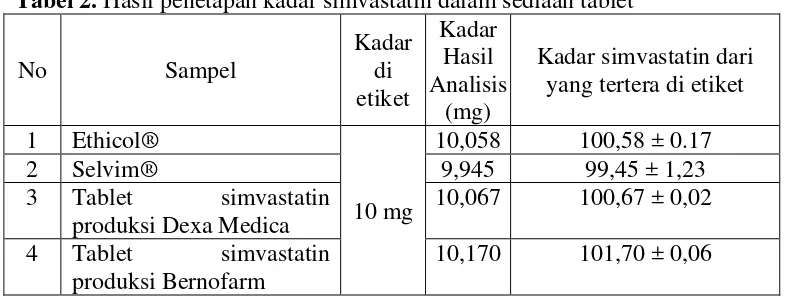
Hasil pengembangan metode dengan menggunakan sistem elusi isokratik diperoleh fase gerak yang paling baik dengan perbandingan asetonitril : air (80:20). Hasil uji validasi diperoleh % recovery 99,67%, presisi (RSD) 1,89%, ini menunjukkan bahwa metode ini memiliki akurasi dan presisi yang baik dengan batas deteksi (LOD) 2,314 µg/ml dan batas kuantitasi (LOQ) 7,713 µg/ml. Dari hasil penetapan kadar simvastatin dalam sediaan tablet diperoleh berturut-turut kadar dari yang tercantum di etiket untuk nama dagang Ethicol® 100,58 ± 0,17%, Selvim® 99,45 ± 1,23% dan dengan nama generik Dexa Medica 100,67 ± 0,02%, Bernofarm 101,70 ± 0,06%. Dapat disimpulkan bahwa semua sampel tablet simvastatin memenuhi persyaratan kadar menurut United Stated Pharmacopeia (USP) 32 tahun 2009 yaitu tidak kurang dari 90,0% dan tidak lebih dari 110,0% dari jumlah yang tertera pada etiket.
METHOD DEVELOPMENT HIGH PERFORMANCE LIQUID CHROMATOGRAPHY ASSAY OF SIMVASTATIN TABLETS IN USING
MOBILE PHASE ACETONITRILE : WATER ABSTRACT
Simvastatin is a drug that belonged to antihiperlidemia HMC-CoA reductase inhibitors. In the fourth edition of the Pharmacopoeia of Indonesia the sismvastatin’s tablet monograph is not available, but it is available in United States Pharmacopeia (USP) 32:2009. The assay of simvastatin tablet in the USP determined by high performance liquid chromatography (HPLC) using a mobile phase of acetonitrile: acetate buffer with an isocratic system, whereas in the previous study using a mobile phase of acetonitrile : water with gradient elution system. The limitation of both methods is the use of buffer that is not friendly to the column and the complication of gradient elution system usage. The purpose of this research is the development of HPLC assay method for simvastatin tablet where is more secure against column and relatively easy to use, this method is validated and is further applied to the determination of concentrations of simvastatin in tablet using generic and trade name as the sampels.
The Assay has been developed using a Waters X-Bridge column (250 x 4.6 mm), mobile phase of acetonitrile: water with isocratic elution system, a flow rate of 1.5 ml/min, column temperature 50ºC and a wavelength of 238 nm. In this study the optimation of this assay is done by changing the compotition of mobile phase to gain the best result of analysis. The validation parameters such as accuracy, precision, limit of detection and limit of quantitation is also performed.
This study shows the best result of simvastatin assay with a retention time of 2.7 minutes from isocratic elution system using acetonitrile : water (80:20) as the mobile phase. The validation test shows the % accuracy (recovery) and precision (RSD) of 99.67% and 1.89% respectively, indicating that the method has good accuracy and precision. The limits of detection (LOD) and limits of quantification (LOQ) is found to be 2.314 µg/ml and 7.713 µg/ml respectively. The determination using the developed procedure result concentration of simvastatin of 100.58 ± 0.17% for Ethicol®, 99.45 ± 1.23% for Selvim®, the 100.67 ± 0.02% for Simvastatin generic from Dexa Medica, 101.70 ± 0.06% for Simvastatin generic from Bernofarm. It can be concluded that all samples meet the requirement of the concentration of simvastatin in tablet according to the USP 32:2009, no less than 90.0% and not more than 110.0% of the amount listed on the label.
DAFTAR ISI
Halaman
JUDUL ... ... i
HALAMAN JUDUL ... ii
LEMBAR PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... v
ABSTRACT ... vi
DAFTAR ISI ... vii
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xvi
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 4
1.4 Tujuan Penelitian ... 4
1.5 Manfaat Penelitian ... 5
BAB II TINJAUAN PUSTAKA ... 6
2.1 Uraian Bahan ... 6
2.1.1 Sifat Fisiko Kimia Simvastatin ... 6
2.1.2 Mekanisme Kerja ... 6
2.1.3 Efek Samping ... 7
2.2.1 Sejarah Kromatografi ... 8
2.2.2 Pemakaian Kromatografi ... 8
2.2.3 Pembagian Kromatografi ... 9
2.3 Kromatografi Cair Kinerja Tinggi (KCKT) ... 9
2.3.1 Komponen Kromatografi Cair Kinerja Tinggi ... 11
2.3.2 Komponen KCKT ... 12
2.3.2.1 Wadah Fase Gerak ... 12
2.3.2.2 Pompa ... 13
2.3.2.3 Injektor ... 13
2.3.2.4 Kolom ... 15
2.3.2.5 Detektor ... 15
2.3.2.6 Alat Pengolah Data ... 16
2.3.2.7 Fase Gerak ... 16
2.3.2.8 Elusi Gradien dan Isokratik ... 17
2.3.2 Parameter penting dalam KCKT ... 12
2.3.3.1 Tinggi dan luas puncak ... 19
2.3.3.2 Waktu tambat ... 19
2.3.3.3 Faktor kapasitas ... 20
2.3.3.4 Selektifitas ... 20
2.3.3.5 Efisiensi kolom ... 21
2.3.3.6 Resolusi ... 21
2.3.3.7 Faktor asimetri ... 22
2.4 Penentuan Kadar Simvastatin Secara KCKT ... 23
2.5.1 Akurasi ... 24
2.5.2 Presisi ... 25
2.5.3 Spesifisitas ... 25
2.5.4 Batas Deteksi dan Batas Kuantitasi ... 25
2.5.5 Linearaitas ... 26
2.5.6 Rentang ... 27
2.5.7 Kekuatan ... 27
BAB III METODE PENELITIAN ... 28
3.1 Tempat dan Waktu Penelitian ... 28
3.2 Alat-alat ... 28
3.3 Bahan-bahan ... 28
3.4 Sampling Tablet Simvastatin ... 29
3.5 Prosedur Analisis ... 30
3.5.1 Penentuan Panjang Gelombang Maksimum ... 30
3.5.2 Pembuatan Pelarut ... 30
3.5.3 Penyiapan Alat KCKT ... 30
3.5.4 Optimasi Komposisi Fase Gerak ... 30
3.5.5 Analisis Kualitatif ... 31
3.5.6 Analisis Kuantitatif ... 31
3.5.6.1 Pembuatan Larutan Induk Baku I Simvastatin ... 31
3.5.6.2 Pembuatan Larutan Induk Baku II Simvastatin .. 31
3.5.6.3 Pembuatan Kurva Kalibrasi ... 32
3.5.6.4 Penetapan Kadar Simvastatin ... 32
3.6.1 Akurasi ... 33
3.6.1.1 Prosedur Akurasi ... 33
3.6.1.2 Pembuatan Kurva Kalibrasi untuk Akurasi ... 38
3.6.2 Presisi ... 39
3.6.3 Batas Deteksi dan Batas Kuantitasi ... 40
3.7 Analisis Data Secara Statistik ... 40
BAB IV HASIL DAN PEMBAHASAN ... 42
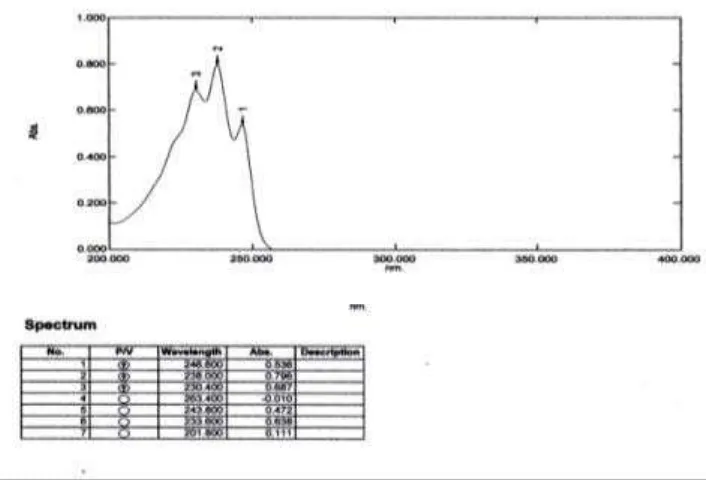
4.1 Panjang Gelombang Analisis ... 42
4.2 Optimasi Komposisi Fase Gerak ... 43
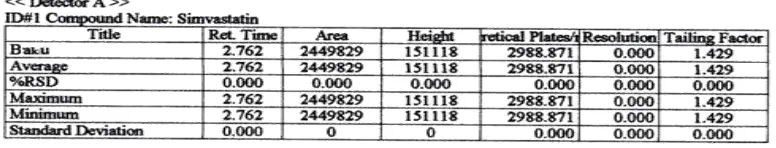
4.3 Analisa Kualitatif ... 46
4.4 Analisa Kuantitatif ... 49
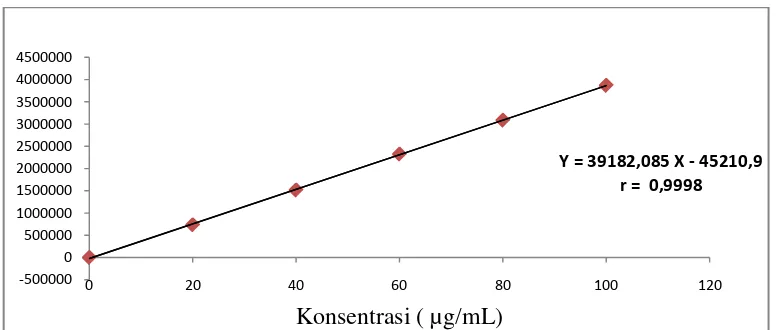
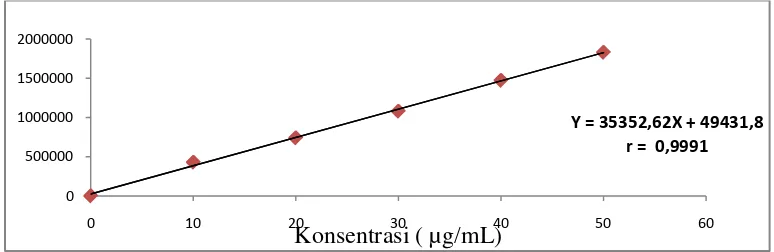
4.4.1 Kurva Kalibrasi ... 49
4.4.2 Kadar Analit pada Sampel yang Dianalisis ... 49
4.5 Hasil Uji Validasi ... 50
BAB V KESIMPULAN DAN SARAN ... 53
5.1 Kesimpulan ... 53
4.2 Saran ... 54
DAFTAR PUSTAKA ... 55
DAFTAR TABEL
Halaman
Tabel 1. Pengaruh Komposisi Fase Gerak Terhadap Parameter
Kromatogram ... 43
Tabel 2. Hasil Penetapan Kadar Simvastatin dalam Sediaan Tablet ... 50
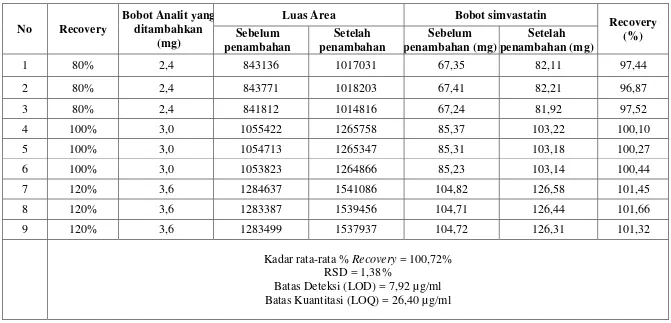
Tabel 3. Hasil Pengujian Validasi dengan Parameter Akurasi, Presisi, Batas Deteksi (LOD) dan Batas Kuantitasi (LOQ) Simvastatin Pada Tablet Simvastatin Produksi Bernofarm dengan Menggunakan
DAFTAR GAMBAR
Halaman
Gambar 1. Diagram Skematik Alat KCKT ... 11
Gambar 2. Tipe Injektor dan Katup Putaran ... 14
Gambar 3. Kurva serapan maksimum simvastatin BPFI dengan pelarut
Asetonitril : air (80:20) ... 42
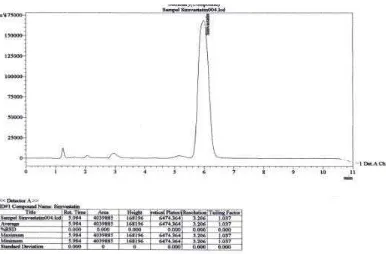
Gambar 4. Kromatogram Sampel Ethicol secara KCKT menggunakan Kolom Waters X-Bridge (250 x 4,6 mm) dengan perbandingan
Fase gerak asetonitril : air (40:60), laju alir 1,5ml/menit, volume penyuntikan 20 µL, panjang gelombang 238 nm dan suhu 50°C ... 44
Gambar 5. Kromatogram Sampel Ethicol secara KCKT menggunakan Kolom Waters X-Bridge (250 x 4,6 mm) dengan perbandingan
Fase gerak asetonitril : air (60:40), laju alir 1,5ml/menit, volume penyuntikan 20 µL, panjang gelombang 238 nm dan suhu 50°C ... 44
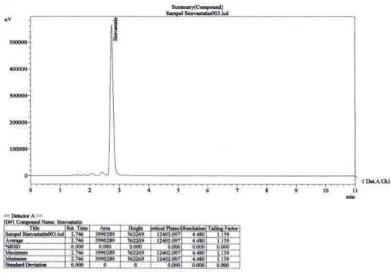
Gambar 6. Kromatogram larutan simvastatin sebelum spiking secara KCKT menggunakan Kolom Waters X-Bridge (250 x 4,6 mm) dengan perbandingan fase gerak asetonitril:air (80:20), laju alir volume penyuntikan 20 µL, panjang gelombang 238 nm dan suhu 50°C ... 45
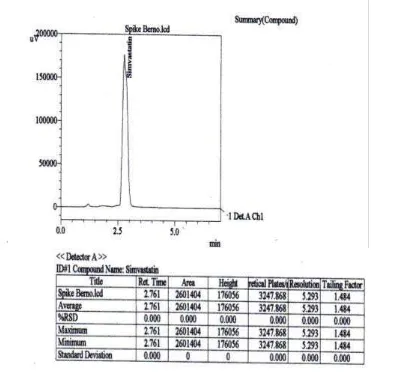
Gambar 7. Kromatogram larutan simvastatin sebelum spiking secara KCKT menggunakan Kolom Waters X-Bridge (250 x 4,6 mm) dengan perbandingan fase gerak asetonitril:air (80:20), laju alir volume penyuntikan 20 µL, panjang gelombang 238 nm dan suhu 50°C ... 47
Gambar 8. Kromatogram larutan simvastatin hasil spiking secara KCKT menggunakan Kolom Waters X-Bridge (250 x 4,6 mm) dengan perbandingan fase gerak asetonitril:air (80:20), laju alir volume penyuntikan 20 µL, panjang gelombang 238 nm dan suhu 50°C ... 47
Gambar 9. Kromatogram larutan baku seri simvastatin secara KCKT menggunakan Kolom Waters X-Bridge (250 x 4,6 mm) dengan perbandingan fase gerak asetonitril:air (80:20), laju alir
1,5 ml/menit, volume penyuntikan 20 µL, panjang gelombang
Gambar 10. Kurva Kalibrasi Baku Simvastatin ... 49
Gambar 11. Kurva Kalibrasi Baku Simvastatin untuk Validasi Metode ... 51
Gambar 12.Kromatogram penentuan kurva kalibrasi secara KCKT menggunakan kolom Waters X- Bridge (250 x 4,6 mm) dengan perbandingan fase gerak asetonitril : air (80:20), laju alir 1,5 ml/menit, volume penyuntikan 20 µL, penyuntikan
20 µL, panjang gelombang 238 nm dan suhu 50°C ... 57
Gambar 13.Kromatogram hasil penentuan kurva kalibrasi untuk sampel Ethicol menggunakan kolom Waters X-Bridge (250 x 4, mm) dengan perbandingan fase gerak asetonitril : air (80:20), laju alir 1,5ml/menit, volume penyuntikan 20 µL, penyuntikan
20 µL, panjang gelombang 238 nm dan suhu 50°C ... 59
Gambar 14. Kromatogram hasil penyuntikan sampel simvastatin Produksi Dexa Medica secara KCKT menggunakan kolom Waters X-Bridge (250 x 4,6 mm) dengan perbandingan Fase gerak asetonitril : air (80:20), laju alir 1,5ml/menit, volume penyuntikan 20 µL, penyuntikan 20 µL dan deteksi pada panjang gelombang 238 nm dan
suhu 50°C ... ... 61
Gambar 15. Kromatogram hasil penyuntikan Selvim secara KCKT menggunakan kolom Waters X-Bridge (250 x 4,6 mm) dengan perbandingan fase gerak asetonitril: air (80:20), laju alir 1,5ml / menit, volume penyuntikan 20 µL, penyuntikan 20 µL dan deteksi pada panjang gelombang
238 nm dan suhu 50°C ... 65
Gambar 16. Kromatogram hasil penyuntikan sampel tablet simvastatin Produksi Bernofarm secara KCKT menggunakan kolom Waters X-Bridge (250 x 4,6 mm) dengan
perbandingan fase gerak asetonitril: air (80:20), laju alir 1,5ml/menit, volume penyuntikan 20 µL, penyuntikan 20 µL dan deteksi pada panjang gelombang 238 nm dan
suhu 50°C ... ... 68
Gambar 17. Kromatogram hasil penyuntikan sampel Ethicol secara KCKT Menggunakan kolom Waters X-Bridge (250 x 4,6 mm)
Gambar 18. Kromatogram 1,2 dan 3 adalah sampel sebelum penambahan baku secara KCKT menggunakan kolom . Waters X-Bridge (250 x 4,6 mm) dengan perbandingan fase gerak asetonitril : air (80:20), laju alir 1,5ml/menit, volume penyuntikan dan deteksi
pada panjang gelombang 238 nm dan suhu 50°C ... 77
Gambar 19. Kromatogram 1,2 dan 3 adalah sampel sebelum penambahan baku secara KCKT menggunakan kolom . Waters X-Bridge (250 x 4,6 mm) dengan perbandingan fase gerak asetonitril : air (80:20), laju alir 1,5ml/menit, volume penyuntikan dan deteksi pada panjang gelombang 238 nm dan suhu 50°C ... 80
Gambar 20.Kromatogram hasil penentuan kurva kalibrasi untuk validasi Metode menggunakan kolom Waters X-Bridge (250 x 4,6 mm) dengan perbandingan fase gerak asetonitril : air (80:20), laju alir 1,5ml/menit, volume penyuntikan 20 µL, penyuntikan 20 µL, panjang gelombang 238 nm dan suhu 50°C ... 84
Gambar 21. Instrument KCKT (Shimadzu Prominence Series) ... 93
Gambar 22. Instrument Spektrofotometer (Shimadzu UV 1800) ... 93
Gambar 23. Heating Magnetic Stirrer (VELP) ... 94
Gambar 24. Alat Ultrasonic SONICA ... 94
Gambar 25. Pompa vakum (Boeco) ... 95
Gambar 26. Neraca Analitik Presica ... 95
Gambar 27. Micro Balance Mettler Toledo ... 96
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Gambar Kromatogram Penentuan Kurva Kalibrasi ... 57
Lampiran 2. Perhitungan Persamaan Regresi Simvastatin ... 58
Lampiran 3. Gambar kromatogram penentuan kurva kalibrasi untuk sampel Ethicol ... 59
Lampiran 4. Perhitungan persamaan kurva kalibrasi baku simvastatin Sampel Ethicol ... 60
Lampiran 5. Kromatogram Hasil Penyuntikan sampel Tablet Simvastatin Produksi Dexa Medica ... 61
Lampiran 6. Perhitungan Kadar Simvastatin Produksi Dexa Medica ... 62
Lampiran 7. Analisis Data Secara Statistik dari Hasil Penyuntikan Sampel Tablet Simvastatin Produksi Dexa Medica ... 63
Lampiran 8. Kromatogram Hasil Penyuntikan sampel Selvim ... 65
Lampiran 9. Perhitungan Kadar Tablet Selvim ... 66
Lampiran 10. Analisis Data Secara Statistik dari Hasil Penyuntikan Sampel Selvim ... 66
Lampiran 11. Kromatogram Hasil Penyuntikan sampel Tablet Simvastatin Produksi Bernofarm ... 68
Lampiran 12. Perhitungan Kadar Tablet Simvastatin Produksi Bernofarm ... 69
Lampiran 13. Analisis Data Secara Statistik dari Hasil Penyuntikan Sampel Tablet Simvastatin Produksi Bernofarm ... 69
Lampiran 14. Kromatogram Hasil Penyuntikan sampel Ethicol ... 71
Lampiran 15. Analisis Data Secara Statistik dari Hasil Penyuntikan Sampel Ethicol ... 72
Lampiran 16. Data Kadar Simvastatin dalam Sampel ... 74
Lampiran 17. Kromatogram Analisis Perolehan Kembali ... 75
Lampiran 19. Contoh Perhitungan untuk mencari Kadar Tablet Simvastatin
Generik (PT. Bernofarm) ... 82
Lampiran 20. Hasil Pengolahan Data Penetapan Kadar Simvastatin . ... 83
Lampiran 21. Gambar Kromatogram Penentuan Kurva Kalibrasi untuk Validasi Metode ... 84
Lampiran 22. Perhitungan Persamaan Regresi Recovery ... 85
Lampiran 23. Data Hasil Penyuntikkan Simvastatin Tablet Sebelum dan Sesudah Penambahan Analit ... 86
Lampiran 24. Data Perhitungan Batas Deteksi (LOD) dan Batas Kuantitasi (LOQ) ... 89
Lampiran 25. Tabel Distribusi t ... 90
Lampiran 26. Sertifikat Pengujian Baku Simvastatin ... 91
Lampiran 27. Spesifikasi Sampel ... 92
PENGEMBANGAN METODE
KROMATOGRAFI CAIR KINERJA TINGGI PADA
PENETAPAN KADAR SIMVASTATIN TABLET
MENGGUNAKAN FASE GERAK ASETONITRIL : AIR
ABSTRAK
Simvastatin merupakan obat antihiperlidemia yang termasuk golongan penghambat HMC-CoA reduktase. Monografi sismvastatin tablet tidak terdapat pada Farmakope Indonesia edisi IV, tetapi pada USP 32 tahun 2009 penetapan kadar simvastatin dalam sediaan tablet ditentukan secara kromatografi cair kinerja tinggi (KCKT) dengan fase gerak asetonitril : buffer asetat dengan sistem isokratik, sedangkan pada penelitian sebelumnya menggunakan fase gerak asetonitril : air dengan sistem elusi gradien. Adapun kelemahan dari kedua metode tersebut adalah pemakaian buffer yang tidak ramah terhadap kolom dan pemakain sistem elusi gradien yang rumit. Tujuan penelitian ini adalah pengembangan metode penetapan kadar simvastatin tablet secara Kromatografi Cair Kinerja Tinggi (KCKT) yang lebih aman terhadap kolom dan relatif lebih mudah digunakan.
Penetapan kadar simvastatin tablet dilakukan dengan sampling purposif dengan menggunakan dua sediaan tablet generik dan dua sediaan tablet nama dagang. Penelitian ini menggunakan kolom Waters X-Bridge (250 x 4,6 mm) , fase gerak asetonitril : air berbagai perbandingan dengan sistem elusi isokratik, laju alir 1,5 ml/menit, suhu kolom 50ºC dan panjang gelombang 238 nm. Optimasi dilakukan dengan mengubah komposisi fase gerak asetonitril : air untuk mendapatkan hasil yang terbaik secara KCKT dengan parameter tailing factor, waktu retensi, nilai lempeng teori dan resolusi. Untuk menguji validitas metode ini, dilakukan uji validasi dengan parameter akurasi, presisi, batas deteksi dan batas kuantitasi.
Hasil pengembangan metode dengan menggunakan sistem elusi isokratik diperoleh fase gerak yang paling baik dengan perbandingan asetonitril : air (80:20). Hasil uji validasi diperoleh % recovery 99,67%, presisi (RSD) 1,89%, ini menunjukkan bahwa metode ini memiliki akurasi dan presisi yang baik dengan batas deteksi (LOD) 2,314 µg/ml dan batas kuantitasi (LOQ) 7,713 µg/ml. Dari hasil penetapan kadar simvastatin dalam sediaan tablet diperoleh berturut-turut kadar dari yang tercantum di etiket untuk nama dagang Ethicol® 100,58 ± 0,17%, Selvim® 99,45 ± 1,23% dan dengan nama generik Dexa Medica 100,67 ± 0,02%, Bernofarm 101,70 ± 0,06%. Dapat disimpulkan bahwa semua sampel tablet simvastatin memenuhi persyaratan kadar menurut United Stated Pharmacopeia (USP) 32 tahun 2009 yaitu tidak kurang dari 90,0% dan tidak lebih dari 110,0% dari jumlah yang tertera pada etiket.
METHOD DEVELOPMENT HIGH PERFORMANCE LIQUID CHROMATOGRAPHY ASSAY OF SIMVASTATIN TABLETS IN USING
MOBILE PHASE ACETONITRILE : WATER ABSTRACT
Simvastatin is a drug that belonged to antihiperlidemia HMC-CoA reductase inhibitors. In the fourth edition of the Pharmacopoeia of Indonesia the sismvastatin’s tablet monograph is not available, but it is available in United States Pharmacopeia (USP) 32:2009. The assay of simvastatin tablet in the USP determined by high performance liquid chromatography (HPLC) using a mobile phase of acetonitrile: acetate buffer with an isocratic system, whereas in the previous study using a mobile phase of acetonitrile : water with gradient elution system. The limitation of both methods is the use of buffer that is not friendly to the column and the complication of gradient elution system usage. The purpose of this research is the development of HPLC assay method for simvastatin tablet where is more secure against column and relatively easy to use, this method is validated and is further applied to the determination of concentrations of simvastatin in tablet using generic and trade name as the sampels.
The Assay has been developed using a Waters X-Bridge column (250 x 4.6 mm), mobile phase of acetonitrile: water with isocratic elution system, a flow rate of 1.5 ml/min, column temperature 50ºC and a wavelength of 238 nm. In this study the optimation of this assay is done by changing the compotition of mobile phase to gain the best result of analysis. The validation parameters such as accuracy, precision, limit of detection and limit of quantitation is also performed.
This study shows the best result of simvastatin assay with a retention time of 2.7 minutes from isocratic elution system using acetonitrile : water (80:20) as the mobile phase. The validation test shows the % accuracy (recovery) and precision (RSD) of 99.67% and 1.89% respectively, indicating that the method has good accuracy and precision. The limits of detection (LOD) and limits of quantification (LOQ) is found to be 2.314 µg/ml and 7.713 µg/ml respectively. The determination using the developed procedure result concentration of simvastatin of 100.58 ± 0.17% for Ethicol®, 99.45 ± 1.23% for Selvim®, the 100.67 ± 0.02% for Simvastatin generic from Dexa Medica, 101.70 ± 0.06% for Simvastatin generic from Bernofarm. It can be concluded that all samples meet the requirement of the concentration of simvastatin in tablet according to the USP 32:2009, no less than 90.0% and not more than 110.0% of the amount listed on the label.
BAB I PENDAHULUAN
1.1Latar Belakang
Simvastatin merupakan obat antihiperlidemia yang bekerja dengan cara
menghambat enzim HMG-CoA reduktase. HMG-CoA merupakan pembentuk
kolesterol dengan bantuan katalis enzim HMG-CoA reduktase. Obat ini
mempunyai aktivitas menghambat pembentukan kolesterol atau mempromosikan
degradasi kolesterol sehingga dapat menurunkan kadar kolesterol dan serum
trigliserida dalam darah serta meningkatkan kadar HDL dalam darah (Yassin,
2007), namun kelebihan dosis dari simvastatin dapat menyebabkan myophaty
(Brenner dan Stevens, 2010).
Pada pembuatan obat, pemeriksaan kadar zat aktif merupakan persyaratan
yang harus dipenuhi untuk menjamin kualitas obat. Sediaan obat yang berkualitas
baik akan mendukung tercapainya efek terapeutik yang diharapkan. Salah satu
persyaratan mutu adalah kadar yang dikandung harus memenuhi persyaratan
kadar yang tercantum dalam literatur yang berlaku seperti Farmakope Indonesia
(Depkes RI, 1989).
Tablet simvastatin dalam perdagangan dijumpai dengan nama dagang dan
generik, dimana obat dengan nama generik harganya jauh lebih murah dibanding
dengan obat dengan nama dagang. Sementara masyarakat cenderung menilai
bahwa kualitas obat identik dengan harga yang lebih tinggi, obat yang lebih mahal
Monografi simvastatin tablet tidak terdapat pada Farmakope Indonesia
edisi IV, tetapi terdapat pada USP 32 tahun 2009 yaitu penetapan kadar
simvastatin dalam sediaan tablet secara kromatografi cair kinerja tinggi (KCKT)
menggunakan fase gerak asetonitril : buffer (65:35) dengan sistem elusi isokratik.
Pada penelitian sebelumnya telah dilakukan penetapan kadar simvastatin tablet
dengan menggunakan kolomPhenomenex ODS Luna (250 mm x 4,6 mm) pada
suhu 50ºC dengan laju alir 1,5 ml/menit pada panjang gelombang 238 nm secara
sistem elusi gradien. Metode tersebut menggunakan larutan buffer sebagai pelarut
pada perbandingan fase gerak asetonitril : air (40:60) yang dimulai pada menit ke
0 dan berakhir pada menit ke 10 dengan perbandingan fase gerak asetonitril : air
(100:0) menghasilkan waktu retensi diantara menit ke 9 sampai 10 (Guzik dkk,
2010).
Metode dengan prosedur tersebut di atas memiliki berbagai kelemahan,
seperti pemakaian larutan buffer bersamaan dengan asetonitril yang tidak ramah
terhadap kolom (USP, 2009) dan sistem elusi gradien yang lebih rumit dari sistem
isokratik (Guzik dkk, 2010). Sistem elusi isokratik lebih disukai karena komposisi
fase gerak tetap konstan selama pengujian, sehingga sistem dan kolom dalam
keadaan yang seimbang sepanjang waktu dan terjaga dari kemungkinan kerusakan
akibat terjadinya perubahan kimia yang cepat seperti pada sistem elusi gradien,
tetapi sistem gradien lebih banyak dipakai karena menghasilkan pemisahan yang
lebih baik (Anonim, 1997).
Berdasarkan hal diatas, peneliti tertarik untuk mengembangkan suatu
metoda penetapan kadar simvastatin dalam sediaan tablet yang lebih sederhana,
gerak asetonitril-air. Pengembangan metode tersebut dilakukan dengan
menggunakan metode elusi isokratik dengan berbagai perbandingan komposisi
fase gerak untuk memperoleh hasil yang optimal. Untuk menguji validitas dari
metode ini dilakukan pengujian antara lain uji akurasi dengan parameter
%recovery, uji presisi dengan parameter koefisien variasi (RSD), uji sensitifitas
dengan parameter limit deteksi (LOD) dan limit kuantitasi (LOQ), selanjutnya
metode yang tervalidasi ini diaplikasikan pada penetapan kadar simvastatin dalam
sediaan tablet dengan nama dagang dan nama generik yang beredar di pasaran.
1.2Perumusan Masalah
Adapun yang menjadi permasalahan dalam penelitian ini adalah:
1. Berapakah perbandingan komposisi fase gerak asetonitril : air yang
optimal (waktu elusi lebih cepat) dengan sistem elusi isokratik secara
KCKT pada penetapan kadar simvastatin dalam sediaan tablet dan
memenuhi uji persyaratan validasi metode?
2. Apakah kadar simvastatin dalam sediaan tablet baik nama dagang maupun
nama generik yang beredar dipasaran memenuhi persyaratan kadar
1.3Hipotesis
Hipotesis penelitian ini adalah:
1. Metode KCKT menggunakan fase gerak asetonitril : air dengan
perbandingan tertentu dan sistem elusi isokratik akan memberikan hasil
yang optimal untuk digunakan pada penetapan kadar simvastatin dalam
sediaan tablet memenuhi persyaratan uji validasi metode.
2. Kadar simvastatin dalam sediaan tablet baik nama dagang maupun nama
generik yang beredar dipasaran memenuhi persyaratan kadar menurut USP
32 tahun 2009.
1.4Tujuan Penelitian
Tujuan penelitian ini adalah:
1. Untuk menentukan perbandingan yang optimal dari fase gerak asetonitril :
air dengan sistem elusi isokratik pada penetapan kadar
simvastatintabletsecara KCKT dan menguji dari validitas metode tersebut.
2. Untuk mengetahui kesesuaian kadar simvastatin dalam sediaan tablet
nama dagang dan nama generik yang beredar dipasaran dengan
1.5Manfaat Penelitian
Penelitian ini dapat digunakan sebagai metode alternatif pada penetapan
kadar simvastatin dalam sediaan tablet secara KCKT untuk industri farmasi dan
BAB II
TINJAUAN PUSTAKA 2.1 Uraian Bahan
2.1.1 Sifat fisiko kimia simvastatin
Menurut Moffat, et al., (2004), sifat fisiko kimia simvastatin adalah
sebagai berikut:
Rumus struktur:
Gambar 1. Struktur Simvastatin Rumus Molekul : C25H38O5
Berat Molekul : 418,6
Titik Lebur : 135o sampai 138oC
Pemerian : Serbuk kristal putih
Kelarutan : Tidak larut dalam air, n-heksana, dan asam klorida;
larut dalam kloroform, dimetil sulfoksida, metanol,
2.1.2. Mekanisme kerja
Simvastatin merupakan obat antihiperlidemia yang strukturnya beranalog
dengan HMG-CoA reduktase sehingga dapat menghambat kerjanya. HMG-CoA
(3-hydroxy-3-methglutaryl coenzyme A) reduktase adalah suatu enzim yang
perubahan) dalam pembentukan kolesterol. Obat ini mempunyai aktivitas
menghambat pembentukan kolesterol atau mempromosikan degradasi kolesterol.
Aktivitas obat ini dapat menurunkan kadar kolesterol dan serum trigliserida dalam
darah serta meningkatkan kadar HDL dalam darah (Katzung, dkk., 2008).
HMG-CoA reduktase dapat mengubah HMG-CoA menjadi asam
mevalonat yang merupakan enzim dalam biosintesis kolesterol. Simvastatin
bekerja secara kompetitif menghambat enzim ini sehingga dapat mengurangi
biosintesis kolesterol di hati dan jumlah kolesterol yang dapat diubah menjadi
VLDL. Kejadian ini akan berujung kepada meningkatnya masukan
LDL-kolesterol di hati (Brenner dan Stevens, 2010).
Simvastatin berdaya menurunkan kadar Low Density Lipoprotein (LDL)
dan kolesterol total dalam 2-4 minggu. Kadar Very Low Density Lipoprotein
(VLDL) dan Trigliserida (TG) juga dapat diturunkan, sedangkan High Density
Lipoprotein (HDL) dinaikkan sedikit. Digunakan tersendiri atau dikombinasi
dengan damar. Khasiat menurunkan LDL-nya kuat, tetapi lebih lemah daripada
atorvastatin. DosisPermulaan 10 mg pada malam hari, bila perlu dinaikkan dengan
interval 4 minggu sampai maksimal 40 mg (Tan dan Rahardja, 2007).
2.1.3 Efek samping
Simvastatin umumnya dapat ditoleransi baik di tubuh, tetapi mungkin
dapat menimbulkan efek samping yang serius kepada sedikit orang. Efek samping
yang paling sering terjadi adalah masalah gastrointestinal, meliputi keram bagian
perut dan konstipasi. Efek samping yang jarang terjadi adalah hepatitis yang
disebabkan meningkatnya kadar enzim hepatik. Efek samping yang paling serius
2.2 Teori Kromatografi 2.2.1 Sejarah kromatografi
Kromatografi adalah suatu istilah umum yang digunakan untuk
bermacam-macam teknik pemisahan, yaitu berdasarkan absorbs sampel diantara suatu fase
gerak dan fase diam. Penemukromatografi adalah Tswett pada tahun 1903
mencoba memisahkan pigmen-pigmen dari daun dengan menggunakan suatu
kolom yang berisi kapur (CaSO4). Istilah kromatografi diciptakan Tswett untuk
melukiskan daerah-daerah yang berwarna yang bergerak kebawah kolom. Tswett
adalah yang pertama diakui sebagai penemu dan yang menjelaskan tentang proses
kromatografi (Johnson dan Stevenson, 1978).
2.2.2 Pemakaian kromatografi
Pemakaian untuk tujuan kualitatif mengungkapkan ada atau tidak adanya
senyawa tertentu dalam cuplikan. Pemakaian untuk tujuan kuantitatif
menunjukkan banyaknya masing-masing komponen campuran, sedangkan
pemakaian untuk tujuan preparatif untuk memperoleh komponen campuran
dalam jumlah memadai dalam keadaan murni (Gritter dkk, 1985).
2.2.3 Pembagian kromatografi
Kromatografi dapat dibedakan atas berbagai macam, tergantung pada
pengelompokannya. Berdasarkan pada mekanisme pemisahannya, kromatografi
dibedakan menjadi : (a) kromatografi adsorbsi; (b) kromatografi partisi; (c)
kromatografi pasangan ion; (d) kromatografi penukar ion; (e) kromatografi
eksklusi ukuran dan (f) kromatografi afinitas (Johnson dan Stevenson, 1978).
Berdasarkan pada alat yang digunakan, kromatografi dapat dibagi atas: (a)
kromatografi planar; (c) kromatografi cair kinerja tinggi (KCKT) dan (d)
kromatografi gas (KG) (Johnson dan Stevenson, 1978; Gandjar dan Rohman,
2007).
2.3 Kromatografi Cair Kinerja Tinggi (KCKT)
Kromatografi cair kinerja tinggi (KCKT) merupakan sistem pemisahan
dengan kecepatan dan efisiensi yang tinggi. Hal ini karena didukung oleh
kemajuan dalam teknologi kolom, sistem pompa tekanan tinggi, dan detektor yang
sangat sensitif dan beragam. KCKT mampu menganalisa berbagai cuplikan secara
kualitatif maupun kuantitatif, baik dalam komponen tunggal maupun campuran
(Ditjen POM, 1995). KCKT merupakan teknik pemisahan yang diterima secara
luas untuk analisis dan pemurnian senyawa tertentu dalam suatu sampel pada
sejumlah bidang antara lain; farmasi, lingkungan dan industri-industri makanan.
Kegunaan umum KCKT adalah untuk pemisahan sejumlah senyawa organik,
anorganik, maupun senyawa biologis, analisis ketidakmurnian (impurities) dan
analisis senyawa-senyawa yang tidak mudah menguap (nonvolatil). KCKT paling
sering digunakan untuk: menetapkan kadar senyawa-senyawa tertentu seperti
asam-asam amino, asam-asam nukleat dan protein-protein dalam cairan fisiologis,
menentukan kadar senyawa-senyawa aktif obat dan lain-lain.
Menurut De Lux Putra (2007), kelebihan KCKT antara lain:
a. Mampu memisahkan molekul-molekul dari suatu campuran. Resolusinya
baik.
b. Mudah melaksanakannya.
d. Dapat dihindari terjadinya dekomposisi/kerusakan bahan yang dianalisis.
e. Dapat digunakan bermacam-macam detektor.
f. Kolom dapat digunakan kembali.
g. Mudah melakukan rekoveri cuplikan.
h. Tekniknya tidak begitu tergantung pada keahlian operator dan
reprodusibilitasnya lebih baik.
i. Instrumennya memungkinan untuk bekerja secara automatis dan
kuantitatif.
j. Waktu analisis umumnya singkat.
k. Kromatografi cair preparatif memungkinkan dalam skala besar.
l. Ideal untuk molekul besar dan ion.
Keterbatasan metode KCKT adalah untuk identifikasi senyawa, kecuali
jika KCKT dihubungkan dengan spektrometer massa (MS). Keterbatasan lainnya
adalah jika sampelnya sangat kompleks, maka resolusi yang baik sulit diperoleh
(Munson, 1984).
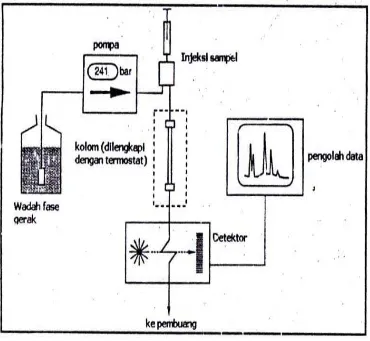
2.3.1 Komponen Kromatografi Cair Kinerja Tinggi
Instrumentasi KCKT terdiri atas wadah fase gerak, pompa, injektor,
kolom, detektor, dan pengolah data. Diagram skematik alat KCKT ditunjukkan
Gambar 1. Diagram Skematik Alat KCKT (Gandjar dan Rohman, 2009). 2.3.2 Komponen KCKT
2.3.2.1 Wadah fase gerak
Wadah fase gerak harus dapat memuat fase gerak untuk KCKT dalam
jumlah yang cukup untuk jalannya sistem secara terus menerus. Wadah fase
gerak dapat dilengkapi dengan sistem degassing terhubung dengan alat KCKT
serta saringan khusus untuk memisahkan fase gerak dari pengaruh lingkungan
(Kazakevich dan Lobrutto, 2007).
Wadah fase gerak harus bersih dari lembam (inert). Wadah pelarut kosong
ataupun labu laboratorium dapat digunakan sebagai wadah fase gerak. Wadah ini
sebelum digunakan harus dilakukan degassing (penghilangan gas) yang ada pada
fase gerak, sebab dengan adanya gas akan berkumpul dengan komponen lain
terutama di pompa dan detektor sehingga akan mengacaukan analisis. Pada saat
membuat pelarut untuk fase gerak, maka akan sangat dianjurkan untuk
menggunakan pelarut, buffer, dan reagen dengan kemurnian yang sangat tinggi,
dan lebih terpilih lagi jika pelarut-pelarut yang akan digunakan berderajat KCKT
(HPLC grade). Adanya pengotor dalam reagen dapat menyebabkan gangguan
pada sistem kromatografi. Adanya partikel yang kecil dapat berkumpul dalam
kolom atau dalam tabung sempit, sehingga dapat mengakibatkan suatu
kekosongan pada kolom atau tabung tersebut (Gandjar dan Rohman, 2009).
2.3.2.2 Pompa
Pompa yang cocok digunakan untuk KCKT adalah pompa yang
mempunyai syarat sebagaimana syarat pelarut yakni harus inert terhadap fase
gerak. Bahan yang umum dipakai untuk pompa adalah gelas, baja tahan karat,
teflon, dan batu nilam. Pompa yang digunakan sebaiknya mampu memberikan
tekanan sampai 5000 psi dan mampu mengalirkan fase gerak dengan kecepatan
alir 3 ml/menit (Gandjar dan Rohman, 2009).
Pompa harus menjamin tersedianya aliran fase gerak yang secara terus
menerus melewati sistem. Kebanyakan pompa modern memungkinkan untuk
mencampur berbagai fase gerak yang diambil dari wadah yang berbeda
(Kazakevich dan Lobrutto, 2007).
2.3.2.3 Injektor
Menurut Kazakevich dan Lobrutto (2007), larutan sampel masuk ke arus
kebanyakan injektor modern adalah autosampler, yang memungkinkan
pengaturan program untuk penginjekan larutan sampel dalam volume yang
berbeda. Larutan sampel diletakkan di dalam vial pada wadah autosampler.
Sedangkan untuk injektor konvensional terdiri dari 3 jenis, yaitu :
a. Hentikan aliran/stop flow: aliran dihentikan, injeksi dilakukan pada kinerja
atmosfir, sistem tertutup, dan aliran dilanjutkan lagi. Teknik ini bisa
digunakan karena difusi di dalam aliran kecil dan resolusi tidak
dipengaruhi.
b. Septum: injektor-injektor langsung ke aliran fase gerak umumnya sama
dengan yang digunakan pada kromatografi gas. Injektor ini dapat
digunakan pada kinerja sampai 60-70 atmosfir. Tetapi septum ini tidak
tahan dengan semua pelarut-pelarut kromatografi cair. Disamping itu,
partikel kecil dari septum yang terkoyak (akibat jarum injektor) dapat
menyebabkan penyumbatan.
c. Katup putaran (loop valve): tipe injektor ini umumnya digunakan untuk
menginjeksi volume lebih besar daripada 10 μl dan sekarang digunakan
dengan cara otomatis (dengan adaptor khusus, volume-volume lebih kecil
dapat diinjeksikan secara manual). Pada posisi Load, sampel loop
(cuplikan dalam putaran) diisi pada tekanan atmotsfir. Bila katup
difungsikan, maka cuplikan di dalam putaran akan bergerak ke dalam
Gambar 2. Tipe injektor dan katup putaran 2.3.2.4 Kolom
Kolom merupakan jantung dari sistem kromatografi cair kinerja tinggi
yang fungsinya adalah melakukan pemisahan analit dari campuran. Kolom adalah
tempat dimana fase gerak berkontak dengan fase diam, membentuk suatu
antarmuka dengan permukaan yang besar. Sebagian besar pengembangan kolom
akhir-akhir ini dititik beratkan pada cara untuk meningkatkan kontak antar muka
(Kazakevich dan Lobrutto, 2007).
Menurut Jhonson dan Stevenson (1978), kolom dapat dibagi menjadi dua
kelompok:
1. Kolom analitik: diameter khas adalah 2-6 mm. Panjang kolom tergantung
pada jenis kemasan. Untuk kemasan pelikel biasanya panjang kolom
50-100 cm. Untuk kemasan mikropartikel berpori, umumnya 10-30 cm.
2. Kolom preparatif: umumnya memiliki diameter 6 mm atau lebih besar dan
panjang kolom 25-100 cm.
Kolom umumnya dibuat dari stainless steel dan biasanya dioperasikan
pada temperatur kamar, tetapi bisa juga digunakan temperatur lebih tinggi,
terutama untuk kromatografi penukar ion dan kromatografi eksklusi. Kemasan
kolom tergantung pada mode KCKT yang digunakan.
2.3.2.5 Detektor
Suatu detektor dibutuhkan untuk mendeteksi adanya komponen cuplikan
dalam aliran yang keluar dari kolom. Detektor-detektor yang baik memiliki
sensitifitas yang tinggi, gangguan (noise) yang rendah, rentang respons linier yang
luas, dan memberi tanggapan/respon untuk semua tipe senyawa. Suatu kepekaan
yang rendah terhadap aliran dan fluktuasi temperatur sangat diinginkan, tetapi
tidak selalu dapat diperoleh (Johnson dan Stevenson, 1978).
Detektor yang paling banyak digunakan dalam kromatografi cair modern
kecepatan tinggi adalah detektor spektrofotometer UV 254 nm. Bermacam-macam
detektor dengan variasi panjang gelombang UV-Vis sekarang menjadi populer
karena mereka dapat digunakan untuk mendeteksi senyawa-senyawa dalam
rentang yang luas. Detektor indeks refraksi juga secara luas digunakan, terutama
dalam kromatografi eksklusi, tetapi umumnya kurang sensitif dari pada detektor
spektrofotometer UV. Detektor lainnya, antara lain: detektor fluometer, detektor
ionisasi nyala, detektor elektrokimia dan lain-lain juga telah digunakan (Johnson
2.3.2.6 Alat pengolah data
Alat pengumpul data seperti komputer, integrator dan rekorder
dihubungkan ke detektor. Alat ini mengukur sinyal elektronik yang dihasilkan
oleh detektor dan memplotkannya sebagai suatu kromatogram yang selanjutnya
dievaluasi oleh seorang analis (Gandjar dan Rohman, 2009).
2.3.2.7 Fase gerak
Fase gerak atau eluen biasanya terdiri atas campuran pelarut yang dapat
bercampur secara keseluruhan berperan dalam daya elusi dan daya resolusi. Daya
elusi dan resolusi ini ditentukan oleh polaritas keseluruhan pelarut, polaritas fase
diam, dan sifat komponen-komponen sampel (Gandjar dan Rohman, 2009).
Pada KCKT, susunan pelarut atau fase gerak merupakan salah satu hal
penting yang mempengaruhi proses pemisahan. Berbagai macam pelarut dipakai
dalam semua jenis KCKT, tetapi ada beberapa syarat fase gerak yang digunakan
dalam KCKT. Menurut Jhonson dan Stevenson (1978), kriteria fase gerak yang
ideal adalah sebagai berikut:
a. Murni, tanpa cemaran;
b. Tidak bereaksi dengan kemasan;
c. Sesuai dengan detektor;
d. Dapat melarutkan cuplikan;
e. Mempunyai viskositas rendah;
f. Memungkinkan memperoleh kembali cuplikan dengan mudah, jika diperlukan;
g. Harganya wajar.
Pada umumnya, pelarut dibuang setelah digunakan karena tata kerja
persyaratan pertama merupakan yang paling penting (Jhonson dan Stevenson,
1978).
2.3.2.8 Elusi isokratik dan gradien
Menurut Gritter, dkk., (1985), elusi pada kromatografi cair kinerja tinggi
dapat dibagi menjadi 2 sistem yaitu:
1. Sistem elusi isokratik
Pada sistem ini, elusi dilakukan dengan satu macam atau lebih fase gerak
dengan perbandingan tetap (komposisi fase gerak tetap selama elusi).
2. Sistem elusi gradien
Pada sistem ini, elusi dilakukan dengan perbandingan fase gerak yang
perbandingannya berubah-ubah dalam waktu tertentu (komposisi fase
gerak berubah-ubah selama elusi).
Analisis isokraktik sudah umum dipakai pada aplikasi quality control.
Kelemahan dari sistem ini adalah kapasitas puncak pada kromatogram yang
terbatas (jumlah puncak maksimum yang dapat diakomodasi pada kromatogram)
dan masalah pada sampel yang mempunyai polaritas yang berbeda, juga lambat
mengelusi (contohnya pada dimer) sangat sulit di hitung pada analisis dengan
sistem isokratik karena bentuk puncak yang sangat melebar dan waktu retensi
yang lama (Ahuja dan Dong, 2005).
Berlawanan dengan sistem isokratik, analisis dengan sistem gradien yang
memungkinkan untuk menaikkan kekuatan dari fase gerak selama proses elusi
sangat baik untuk sampel kompleks dan sampel yang mempunyai analit dengan
polaritas yang luas. Sistem gradien dapat digunakan untuk screening dengan hasil
yang baik untuk puncak yang keluar pada waktu-waktu awal elusi dan
memberikan puncak yang lebih tajam pada puncak yang keluar pada akhir elusi.
Kekurangannya adalah memerlukan peralatan yang lebih kompleks dan keahlian
yang lebih tinggi untuk mengembangkan metode serta kesulitan dalan mentransfer
metode (Ahuja dan Dong, 2005).
2.3.3 Parameter penting dalam KCKT 2.3.3.1 Tinggi dan luas puncak
Tinggi dan luas puncak berkaitan secara proporsional dengan kadar atau
jumlah analit tertentu yang terdapat dalam sampel (memiliki informasi
kuantitatif). Namun demikian, luas puncak lebih umum digunakan dalam
perhitungan kuantitatif karena lebih akurat/cermat daripada perhitungan
menggunakan tinggi puncak (Ahuja dan Dong, 2005). Hal ini dikarenakan luas
puncak relatif tidak banyak dipengaruhi oleh kondisi kromatografi, kecuali laju
alir. Sementara itu, tinggi puncak dipengaruhi oleh banyak faktor seperti misalnya
faktor tambat, suhu kolom serta cara injeksi sampel (Miller, 2005). Hal ini akan
menyebabkan tinggi puncak relatif labil selama analisis. Namun demikian tinggi
puncak masih dapat digunakan dalam perhitungan kuantitatif bila puncak analit
simetris (Meyer, 2004).
2.3.3.2 Waktu tambat
Periode waktu antara penyuntikan sampel dan puncak maksimum yang
terekam oleh detektor disebut sebagai waktu tambat.Waktu tambat dari suatu
komponen yang tidak ditahan oleh fase diam disebut sebagai waktu hampa/void
kolom. Jika fase gerak mengalir lebih lambat atau kolom semakin panjang, waktu
hampa dan waktu tambat akan semakin besar, dan sebaliknya bila fase gerak
mengalir lebih cepat atau kolom semakin pendek, maka waktu hampa dan waktu
tambat akan semakin kecil (Meyer, 2004).
2.3.3.3 Faktor kapasitas
Waktu tambat dipengaruhi oleh laju alir, ukuran kolom dan parameter
yang lain. Oleh karena itu, diperlukan suatu ukuran derajat tambatan dari analit
yang lebih independen yakni faktor kapasitas (Meyer, 2004). Dalam beberapa
literatur lain, faktor kapasitas juga disebut sebagai faktor tambat (k’). Idealnya,
analit yang sama jika diukur pada dua instrumen berbeda dengan ukuran kolom
yang berbeda namun memiliki fase diam dan fase gerakyang sama, maka faktor
tambat dari analit pada kedua sistem KCKT tersebut secara teoritis adalah sama
(Meyer, 2004). Faktor tambat yang disukai berada di antara nilai 1 hingga 10. Jika
nilai k’ terlalu kecil menunjukkan bahwa analit terlalu cepat melewati kolom
sehingga tidak terjadi interaksi dengan fase diam dan oleh karena itu tidak akan
muncul dalam kromatogram. Sebaliknya, nilai k’ yang terlalu besar
mengindikasikan waktu analisis akan panjang. Nilai k’ dari analit yang lebih besar
dari 10 akan menjadi masalah dalam analisis KCKT karena waktu analisis yang
terlalu panjang dan sensitifitas yang buruk sebagai akibat dari pelebaran puncak
yang berlebihan (Meyer, 2004).
2.3.3.4 Selektifitas
Proses pemisahan antara dua komponen dalam KCKT hanya
memungkinkan bila kedua komponen memiliki kecepatan yang berbeda dalam
memisahkan/membedakan analit yang berbeda dikenal sebagai selektifitas
(a).Selektifitas umumnya tergantung pada sifat analit itu sendiri, interaksinya
dengan permukaan fase diam serta jenis fase gerak yang digunakan. Nilai
selektifitas yang didapatkan dalam sistem KCKT harus lebih besar dari 1.
Selektifitas disebut juga sebagai faktor pemisahan atau tambatan relatif (Meyer,
2004).
2.3.3.5 Efisiensi kolom
Salah satu karakteristik sistem kromatografi yang paling penting adalah
efisiensi atau jumlah lempeng teoritis. Bilangan lempeng (N) yang tinggi
disyaratkan untuk pemisahan yang baik yang nilainya semakin kecilnya nilai H.
Istilah H merupakan tinggi ekivalen lempeng teoritis atau HETP (high equivalent
theoretical plate) yang mana merupakan panjang kolom yang dibutuhkan untuk
menghasilkan satu lempeng teoritis. Kolom yang baik akan mempunyai bilangan
lempeng yang tinggi dan nilai H yang rendah, untuk mencapai hal ini ada
beberapa faktor yang mendukung yaitu kolom yang dikemas dengan baik, kolom
yang lebih panjang, partikel fase diam yang lebih kecil, viskositas fase gerak yang
lebih rendah dan suhu yang lebih tinggi, molekul-molekul sampel yang lebih
kecil, dan pengaruh di luar kolom yang minimal (Gandjar dan Rohman, 2007).
2.3.3.6 Resolusi
Tingkat pemisahan komponen dalam suatu campuran dengan metode
kromatografi direfleksikan dalam kromatogram yang dihasilkan, untuk hasil
sempurna dari puncak lainnya. Resolusi adalah perbedaan waktu retensi 2
puncakyang saling berdekatan, dibagi dengan rata-rata lebar puncak, dengan
rumus sebagai berikut:
Keterangan:
t = waktu retensi puncak W = lebar puncak
Nilai Rs mendekati atau lebih dari 1,5 akan memberikan pemisahan yang baik
(Gandjar dan Rohman, 2007).
2.3.3.7 Faktor Asimetri
Adanya puncak yang asimetris dapat disebabkan oleh hal–hal berikut:
a. Ukuran sampel yang dianalisis terlalu besar. Jika sampel terlalu besar
maka fase gerak tidak mampu membawa solut dengan sempurna karenanya
terjadi pengekoran atau tailing.
b. Interaksi yang kuat antara solut dengan fase diam dapat menyebabkan
solut sukar terelusi sehingga dapat menyebabkan terbentuknya puncak
yang mengekor.
c. Adanya kontaminan dalam sampel yang dapat muncul terlebih dahulu
sehingga menimbulkan puncak mendahului (fronting) (Gandjar dan
Rohman, 2007).
2.4 Penentuan Kadar Simvastatin Secara KCKT
Menurut Abu-Nameh, et al., (2006) simvastatin tablet dapat ditentukan
kadarnya dengan metode KCKT menggunakan kolom C18 Hypersil, fase gerak
W2)
(W1
t1)
-2(t2
RS
asetonitril-buffer fosfat-metanol (5:3:1) dan dideteksi pada panjang gelombang
230 nm. Metode tersebut telah divalidasi dan memenuhi syarat linearitas, presisi,
akurasi, spesifisitas dan sensitivitas. Serta diperolehnya koefisien regresi sebesar
0,9995. Pada penelitian Guzik, et al., (2010) dilakukan perbandingan dan validasi
dua metode untuk analisis simvastatin dengan KCKT menggunakan campuran
pelarut yang berbeda yaitu asetonitril-air dan metanol-air dalam sistem elusi
gradien. Percobaan juga dilakukan pada beberapa jenis kolom dan temperatur
yang berbeda-beda. Parameter validasi memenuhi persyaratan untuk kedua
metode tersebut.
Pada penelitian Kumar dan Gowda (2012), dilakukan juga penetapan
kadar simvastatin dengan KCKT menggunakan campuran pelarut metanol-0,1%
asam ortofosfat di dalam air (10:90) pada panjang gelombang 238 nm. Waktu
retensi berada pada menit ke 3,106. Metode tersebut divalidasi dengan parameter
spesifisitas, linearitas, presisi, akurasi dan kekasaran. Dimana diperoleh %
recovery 97,45-98,32 % serta koefisien korelasi sebesar 0,9999.
2.5 Validasi Metode
Validasi metode dilakukan untuk menjamin bahwa metode analisis akurat,
spesifik, reprodusibel dan tahan pada kisaran analit yang di analisis. Suatu metode
analisis harus di validasi untuk verifikasi bahwa parameter-parameter kinerjanya
cukup mampu untuk mengatasi masalah dalam analisis. Parameter analisis yang
ditentukan pada vaidasi adalah akurasi, presisi, batas deteksi, batas kuantitasi,
spesifiksi, linieritas dan rentang, kekasaran (Ruggedness) dan ketahanan
2.5.1 Akurasi
Akurasi/kecermatan adalah ukuran yang menunjukkan derajat kedekatan
hasil analisis dengan kadar analit yang sebenarnya. Kecermatan dinyatakan
sebagai persen perolehan kembali (recovery). Akurasi/kecermatan dapat
ditentukan dengan dua metode, yakni spiked placebo recovery dan standard
addition method. Pada spiked placebo recovery atau metode simulasi, analit murni
ditambahkan (spiked) ke dalam campuran bahan pembawa sediaan farmasi, lalu
campuran tersebut dianalisis dan jumlah analit hasil analisis dibandingkan dengan
jumlah analit teoritis yang diharapkan. Jika plasebo tidak memungkinkan untuk
disiapkan, maka sejumlah analit yang telah diketahui konsentrasinya dapat
ditambahkan langsung ke dalam sediaan farmasi otentik. Metode ini dinamakan
metode standard addition method atau metode penambahan baku. Jumlah
keseluruhan analit kemudian diukur dan dibandingkan dengan jumlah teoritis,
yaitu jumlah analit yang murni berasal dari sediaan farmasi otentik tersebut,
ditambah dengan jumlah analit yg di-spiked ke dalam sediaan (Harmita, 2004).
2.5.2 Presisi
Presisi diekspresikan dengan standar deviasi atau standar deviasi relatif
(RSD) dari serangkaian data. Data untuk menguji presisi seringkali dikumpulkan
sebagai bagian dari kajian-kajian lain yang berkaitan dengan presisi seperti
linearitas atau akurasi. Biasnya replikasi 6-15 dilakukan pada sampel tunggal
untuk tiap-tiap konsentrasi. Pada pengujian dengan KCKT, nilai RSD antara 1-2%
sedangkan untuk senyawa-senyawa dengan kadar sekelumit RSD berkisar antara
5-15% (Gandjar dan Rohman, 2007).
2.5.3 Spesifitas
Penentuan spesifitas metode dapat diperoleh dengan dua jalan. Cara
pertama adalah dengan melakukan optimasi sehingga diperoleh senyawa yang
dituju terpisah secara sempurna dari senyawa-senyawa lain (resolusi senyawa
yang dituju > 1,5). Cara kedua untuk memperoleh spesifitas adalah dengan
menggunakan detektor selektif terutama untuk senyawa-senyawa yang terelusi
secara bersama-sama sebagai contoh detektor elektrokimia hanya akan
mendeteksi senyawa tertentu, sementara senyawa yang lainnya tidak terdeteksi.
Penggunaan detektor UV pada panjang gelombang yang spesifik juga merupakan
cara yang efektif untuk melakukan pengukuran selektifitas (Gandjar dan Rohman,
2007).
2.5.4 Batas Deteksi dan Batas Kuantitasi
Batas deteksi dan batas kuantitasi dapat ditentukan dengan 2 metode yakni
metode non instrumental visual dan metode perhitungan. Metode non instrumental
visual digunakan pada teknik kromatografi lapis tipis dan metode titrimetri.
Metode perhitungan didasarkan pada simpangan baku respon (SB) dan derajat
kemiringan/slope (b) dengan rumus perhitungan batas deteksi dan batas kuantitasi
sbb:
Batas deteksi (LOD) =
slope X SY x 3
Batas kuantitasi (LOQ) =
Simpangan baku respon dapat ditentukan berdasarkan simpangan baku blanko,
simpangan baku residual dari garis regresi atau simpangan baku intersep y pada
garis regresi (Gandjar dan Rohman, 2007).
2.5.5 Linearitas
Lineritas merupakan kemampuan suatu metode untuk memperoleh
hasil-hasil uji yang secara langsung proporsional dengan konsentrasi analit pada kisaran
yang diberikan. Linearitas suatu metode merupakan ukuran seberapa baik kurva
kalibrasi yang menghubungkan antara respon (y) dengan konsentrasi (x).
Linearitas dapat diukur dengan melakukan pengukuran tunggal pada konsentrasi
yang berbeda-beda. Data yang diperoleh selanjutnya diproses dengan metode
kuadrat terkecil, untuk selanjutnya dapat ditentukan nilai kemiringan (slope),
intersep, dan koefisien korelasinya (Gandjar dan Rohman, 2007).
2.5.6 Rentang
Rentang atau kisaran suatu metode didefinisikan sebagai konsentrasi
terendah dan tertinggi yang mana suatu metode analisis menunjukkan akurasi,
presisi, dan linearitas yang mencukupi. Kisaran-kisaran konsentrasi yang diuji
tergantung pada jenis metode dan kegunaannya (Gandjar dan Rohman, 2007).
2.5.7 Kekuatan
Kekuatan/ketahanan dievaluasi dengan melakukan variasi
parameter-parameter metode seperti persentase pelarut organik, pH, kekuatan ionik, suhu,
dan sebagainya. Suatu praktek yang baik untuk mengevaluasi ketahanan suatu
metode adalah dengan memvariasi parameter-parameter penting dalam suatu
metode secara sistematis lalu mengukur pengaruhnya pada pemisahan (Gandjar
BAB III
METODE PENELITIAN
3.1 Tempat dan Waktu Penelitian
Penelitian dilakukan di laboratorium Pengujian Balai Besar Pengawas
Obat dan Makanan di Medan pada bulan Maret 2013 sampai Juni 2013.
3.2 Alat–alat
Alat-alat yang digunakan dalam penelitian ini adalah seperangkat
instrumen KCKT lengkap (Shimadzu prominence series) dengan pompa
(LC-20AD),degasser (DGU- 20As), injektor (Rheodyne 7225i), kolom Waters
X-Bridge C18 (250mm x 4,6 mm), detektor UV/Vis (SPD-20A), Auto Sampler for
HPLC Shimadzu 20A HT, spektrofotometer UV-Vis (UV Probe 1800
Shimadzu), wadah fase gerak, sonifikator (SONICA), pompa vakum (Gast DOA -
P604-BN), neraca analitik (Mettler Toledo), membran filter PTFE 0,5 dan 0,2 µm,
cellulose nitrat membran filter 0,45µ m dan alat-alat gelas laboratorium.
3.3 Bahan-bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah simvastatin
(BPFI), metanol grade HPLC (Merck), asetonitril grade HPLC (Merck), aqua
bidestilata (PT.Ikapharmindo Putramas), tablet simvastatin 10 mg produksi Dexa
medica, tablet simvastatin 10 mg Produksi Bernofarm, tablet simvastatin 10 mg
3.4 Sampling Tablet Simvastatin
Pengambilan sampel secara purposif yaitu tanpa membandingkan antara
satu tempat dengan tempat lain, karena tempat pengambilan sampel dianggap
homogen (Sudjana, 2001). Menurut Torbeck (1997), proses sampling dilakukan
dengan menggunakan rumus:
1
+
= N
n
Keterangan:
n = jumlah sampel yang diteliti N = jumlah sampel dalam populasi
Sampel tablet simvastatin yang berhasil di data oleh peneliti dan beredar di
kota Medan berjumlah 10 sampel, yang terdiri dari 5 sampel dengan nama
dagang dan 5 sampel dengan nama generik. Sehingga perhitungannya
menjadi sebagai berikut:
� =√�+ 1
� =√10 + 1 = 4
maka jumlah sampel yang dipakai dalam penelitian ini adalah sebanyak 4 sampel
yang terdiri dari 2 sampel obat dengan nama dagang dan 2 sampel obat dengan
nama generik. Pengambilan sampel dengan nama dagang dimaksudkan untuk
mewakili harga dari yang termahal (Ethicol) dan yang termurah (Selvim),
sedangkan dalam pemilihan sampel dengan nama generik, dasar pertimbangannya
adalah produk yang sudah banyak beredar di apotik kota Medan (Dexa Medica)
3.5 Prosedur Analisis
3.5.1 Penentuan panjang gelombang maksimum
Pengukuran absorbansi maksimum simvastatin dilakukan dengan
membuat larutan simvastatin BPFI dalam pelarut asetonitril : air (80:20) dengan
konsentrasi 8,0 µg/ml. Larutan diukur pada rentang panjang gelombang 200-350
nm menggunakan spektrofotometer ultraviolet.
3.5.2 Pembuatan pelarut
Dicampurkan asetonitril dan air dengan komposisi yang disesuaikan
dengan perbandingan fase gerak yang di optimasi, kemudian diawaudarakan
selama ± 20 menit.
3.5.3 Penyiapan alat KCKT
Kolom yang digunakan Waters X-Bridge (250mm x 4,6 mm), dan detektor
UV-Vis. Pompa menggunakan mode aliran tetap dengan low-pressure gradient
system untuk memperoleh komposisi fase gerak yang konstan selama analisis.
Setelah alat KCKT dihidupkan, maka pompa dijalankan dan fase gerak dibiarkan
mengalir selama 30 menit sampai diperoleh garis alas yang datar yang
menandakan sistem tersebut telah stabil.
3.5.4 Optimasi komposisi fase gerak
Optimasi komposisi fase gerak dilakukan dengan menginjeksikan 20 µL
analit ke sistem KCKT. Kondisi pengukuran adalah metode isokratik dengan
perbandingan fase gerak asetonitril : air (40:60 ; 60:40 dan 80:20), laju alir 1,5
3.5.5 Analisis kualitatif
Larutan baku simvastatin diinjeksikan terlebih dahulu, dilanjutkan dengan
larutan sampel masing-masing sebanyak 20µl, dianalisis pada kondisi KCKT
dengan perbandingan fase gerak asetonitril : air yang terpilih dengan laju alir 1,5
ml/menit pada panjang gelombang 238 nm dan suhu 50ºC. Selanjutnya untuk
identifikasi, pada larutan sampel tersebut ditambahkan sejumlah tertentu larutan
simvastatin BPFI (spiking) kemudian diinjeksikan dan dianalisis kembali pada
kondisi KCKT yang sama. Diamati kembali luas area dan dibandingkan antara
kromatogram hasil spiking dengan kromatogram larutan sampel sebelum spiking.
Sampel dinyatakan mengandung simvastatin, jika terjadi peningkatan tinggi
puncak dan luas area pada kromatogram hasil spiking.
3.5.6 Analisis kuantitatif
3.5.6.1 Pembuatan larutan induk baku I simvastatin
Ditimbang secara seksama 10 mg simvastatin BPFI, dimasukkan ke dalam
labu tentukur 10 ml, dilarutkan dan diencerkan dengan fase gerak hingga garis
tanda, sehingga diperoleh larutan simvastatin BPFI dengan konsentrasi 1000
µg/ml.
3.5.6.2 Pembuatan larutan induk baku II simvastatin
Dipipet 5 ml dari larutan induk baku I ke dalam labu tentukur 10 ml.
Diencerkan dengan fase gerak hingga garis tanda, sehingga diperoleh larutan
dengan konsentrasi 100 µg/ml.
3.5.6.3 Pembuatan kurva kalibrasi
Dipipet masing-masing sebanyak 2,0ml; 4,0 ml; 6,0 ml dan 8,0 ml dari
hingga garis tanda, sehingga diperoleh larutan dengan konsentrasi 20 µg/ml, 60
µg/ml, 40 µg/ml, dan 80 µg/ml. Dikocok-kocok ± 5 menit lalu disaring dengan
membran filter PTFE 0,2µ m kemudian diawaudarakan selama ± 30 menit.
Masing-masing larutan diinjeksikan ke sistem KCKT dengan volume penyuntikan
20µ l diukur pada panjang gelombang 238nm dengan laju alir 1,5ml/menit dan
suhu 50ºC. Kemudian dihitung regrasi (y = ax + b), dimana y adalah luas area
puncak kromatogram dan x adalah konsentrasi baku yang disuntikkan.
3.5.6.4 Penetapan kadar simvastatin
Ditimbang dan diserbukkan 20 tablet simvastatin kemudian ditimbang
seksama sejumlah serbuk setara 10,0 mg simvastatin lalu dimasukkan ke dalam
labu tentukur 100 ml kemudian dilarutkan dan diencerkan dengan fase gerak
asetonitril : air (80:20) hingga garis tanda. Dari larutan tersebut di pipet 6,0 ml,
dimasukkan kedalam labu tentukur 10 ml lalu diencerkan dengan fase gerak
hingga garis tanda. Dikocok-kocok ±5 menit lalu disaring dengan membran filter
PTFE 0,2 µ m. Larutan sampel disuntuikkan ke dalam sistem KCKT. Konsentrasi
diperoleh dengan cara mensubtitusi luas area yang diperoleh kedalam persamaan
regresi. Sedangkan kadar dapat dihitung dengan rumus sebagai berikut:
Konsentrasi simvastatin per tablet (Cp) = Cs x V
Keterangan :
Cs = Konsentrasi simvastatin dari larutan yang diencerkan (µg/ml)
Cu = Konsentrasi larutan uji saat diinjeksi (µg/ml) Cp = Konsentrasi simvastatin per tablet (mg)
Ce = Konsentrasi simvastatin yang tertera pada etiket (mg) V = Volume awal larutan uji (ml)
x 100 (%)
=
Kadar simvastatin terhadap kadar yang tercantum di etiket
Cp x Bu
Ce x Br
Br = Bobot uji (mg)
Bu = Bobot rara-rata penimbangan 20 tablet (mg)
3.6 Validasi Metode 3.6.1 Akurasi
Ditimbang 20 tablet kemudian ditentukan pada rentang spesifik 80%,
100% dan 120% terhadap berat yang sama seperti pada penetapan kadar sampel
yaitu setara 10 mg simvastatin. Ditimbang serbuk yang mengandung 70% analit
dari rentang spesifik lalu dilakukan prosedur yang sama seperti pada penetapan
kadar sampel. Ditimbang lagi serbuk yang mengandung 70% analit rentang
spesifik dan 30% bahan baku lalu dilakukan prosedur yang sama seperti pada
penetapan kadar sampel. Dilakukan 3 kali replikasi untuk masing-masing rentang
spesifik tersebut.
3.6.1.1 Prosedur Akurasi
Berat 1 tablet simvastatin mengandung 10 mg simvastatin
Berat 20 tablet: 2526,6 mg
Rentang spesifik 80%, 100%, 120% dimana setiap rentang mengandung 70%
analit dan 30% baku pembanding
A. Perhitungan Pembuatan Larutan sampel + baku simvastatin 10 mg
1. Rentang 80%
80 % = 80/100 x 10 mg = 8 mg
- Berat analit 70 % = 70/100 x 8 mg = 5,6 mg
Berat sampel yang ditimbang = 5,6 ��
20 � 10 ��� 2,5266 � = 70,7448 mg
- Baku 30 %
Cara Pembuatan Larutan Sampel
Ditimbang serbuk sampel 70,7 mg setara dengan 5,6 mg simvastatin, lalu
dimasukkan kedalam labu tentukur 50 ml, dilarutkan dan dicukupkan dengan
asetonitril : air (80:20) hingga garis tanda sehingga diperoleh larutan dengan
konsentrasi 112 µg/ml, dikocok 5 menit kemudian disaring dengan kertas saring.
Dipipet 2 ml filtrat, dimasukkan kedalam labu tentukur 10 ml, dan dicukupkan
hingga garis tanda sehingga didapatkan konsentrasi 22,4 µg/ml. Dikocok 5 menit
lalu disaring dengan membran filter PTFE 0,45 µm. Disuntikkan sebanyak 20 µl
ke sistem KCKT dan dideteksi pada panjang gelombang 238 nm dengan
perbandingan fase gerak asetonitril : air (80:20), laju alir 1,5 ml/menit.
Dilakukan sebanyak 3 kali pengulangan.
Cara Pembuatan Larutan Sampel Ditambah Dengan Baku
Ditimbang 2,4 mg bahan baku dan 70,7 mg sampel kemudian dimasukkan
kedalam labu tentukur 50 ml, dilarutkan dan dicukupkan dengan asetonitril : air
(80:20) hingga garis tanda sehingga diperoleh larutan dengan konsentrasi 160
µg/ml, dikocok 5 menit kemudian disaring dengan kertas saring. Dipipet 2 ml
filtrat, dimasukkan kedalam labu tentukur 10 ml, dan dicukupkan hingga garis
tanda sehingga didapatkan konsentrasi 32 µg/ml. Dikocok 5 menit lalu disaring
dengan membran filter PTFE 0,45 µm. Disuntikkan sebanyak 20 µl ke sistem
KCKT dan dideteksi pada panjang gelombang 238 nm dengan perbandingan
fase gerak asetonitril : air (80:20), laju alir 1,5 ml/menit. Dilakukan sebanyak 3
2. Rentang 100 %
100 % = 100/100 x 10 mg = 10 mg
- Berat analit 70 % = 70/100 x 10 mg = 7 mg
Berat sampel yang ditimbang = 7 ��
20 � 10 ��� 2,5266 � = 88,4310
mg
- Baku 30 %
= 30/100 x 10 mg = 3 mg
Cara Pembuatan Larutan Sampel
Ditimbang serbuk sampel 88,4 mg setara dengan 7 mg simvastatin, lalu
dimasukkan kedalam labu tentukur 50 ml, dilarutkan dan dicukupkan dengan
asetonit