PENETAPAN KADAR ALPRAZOLAM DALAM SEDIAAN TABLET DENGAN NAMA DAGANG DAN GENERIK SECARA KROMATOGRAFI
CAIR KINERJA TINGGI SKRIPSI
OLEH:
MEIVA AMELIA LUBIS NIM 071501006
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
PENETAPAN KADAR ALPRAZOLAM DALAM SEDIAAN TABLET DENGAN NAMA DAGANG DAN GENERIK SECARA KROMATOGRAFI
CAIR KINERJA TINGGI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
MEIVA AMELIA LUBIS NIM 071501006
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
PENGESAHAN SKRIPSI
PENETAPAN KADAR ALPRAZOLAM DALAM SEDIAAN TABLET DENGAN NAMA DAGANG DAN GENERIK SECARA KROMATOGRAFI
CAIR KINERJA TINGGI
OLEH:
MEIVA AMELIA LUBIS NIM 071501006
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi
Universitas Sumatera Utara Pada tanggal: 6 Januari 2012
Pembimbing I, Panitia Penguji,
Prof. Dr. rer. nat. E. D. L. Putra, SU., Apt. Prof. Dr. Siti Morin Sinaga, M.Sc., Apt. NIP 195306191983031001
Pembimbing II, Prof. Dr. rer. nat. E. D. L. Putra, SU., Apt.
Drs. Fathur Rahman Harun, M.Si., Apt.
NIP 195201041980031002 Dra. Nurmadjuzita, M.Si., Apt.
Drs. Syafruddin, M.S., Apt.
Medan, 6 Januari 2011 Fakultas Farmasi Universitas Sumatera Utara
Dekan,
KATA PENGANTAR
Puji dan syukur kehadirat Tuhan Yang Maha Kuasa yang telah melimpahkan berkatNya, sehingga penulis dapat menyelesaikan skripsi dengan judul “Penetapan Kadar Alprazolam dalam Sediaan Tablet dengan Nama Dagang dan Generik secara Kromatografi Cair Kinerja Tinggi”. Skripsi ini diajukan sebagai salah satu syarat guna memperoleh gelar Sarjana Farmasi dari Fakultas Farmasi Universitas Sumatera Utara.
Kromatografi Cair Kinerja Tinggi (KCKT) merupakan metode yang sangat populer untuk menetapkan kadar senyawa obat baik dalam bentuk sediaan maupun dalam sampel hayati. Tujuan penelitian ini adalah melakukan pengembangan metode dengan menggunakan fase gerak metanol-air pada penetapan kadar alprazolam dalam tablet generik dan nama dagang. Hendaknya hasil penelitian ini menjadi masukan bagi industri obat dan BPOM tentang penetapan kadar Alprazolam pada sediaan tablet secara Kromatografi Cair Kinerja Tinngi (KCKT).
Penulis juga mengucapkan terima kasih yang tiada terhingga kepada Ayahanda Rajamin Lubis, Ibunda Elida, S.pd., Adik Rizka Syahfitri Lubis dan Rizky Syahfitri Lubis, Donatur Beasiswa Karya Salemba Empat, Kakak Pratania Villonensia, S.E., Lapharm+, Kak Mustika Furi, S.Farm. dan teman-teman lainnya serta semua keluarga yang tidak dapat disebutkan satu per satu, yang telah banyak memberikan doa dan dorongan serta bantuan moril dan materil kepada penulis selama menempuh pendidikan S-1 Farmasi.
Penulis menyadari bahwa tulisan ini masih memiliki banyak kekurangan, oleh karena itu dengan segala kerendahan hati penulis bersedia menerima kritik dan saran yang membangun pada skripsi ini. Semoga skripsi ini bermanfaat bagi
kita semua. Medan, Januari 2012
Penulis,
PENETAPAN KADAR ALPRAZOLAM DALAM SEDIAAN TABLET DENGAN NAMA DAGANG DAN GENERIK SECARA KROMATOGRAFI
CAIR KINERJA TINGGI ABSTRAK
Salah satu obat ansietas dan depresi yang terdapat di pasaran yang termasuk kelompok benzodiazepin adalah alprazolam. Penetapan kadar alprazolam dalam Farmakope Indonesia Edisi IV (1995) dan USP Edisi XXX (2007) ditentukan secara KCKT menggunakan fase gerak dapar posfat-asetonitril-P-tetrahidrofuran. Penggunaan dapar posfat dapat menyebabkan pengkristalan pada kolom. Tujuan penelitian ini adalah melakukan pengembangan metode dengan menggunakan fase gerak metanol-air pada penetapan kadar alprazolam dalam tablet generik dan nama dagang. Untuk menguji validitas metode ini dilakukan uji akurasi, presisi, batas deteksi (LOD) dan batas kuantitasi (LOQ).
Perbandingan fase gerak yang digunakan adalah metanol-air (90:10), perbandingan fase gerak ini diperoleh dari hasil optimasi yang dilakukan menggunakan kolom Luna 5µ C18 (250 x 4,60 mm i.d. 5 µm) dengan laju alir 1,5 ml/menit dan dideteksi pada panjang gelombang 254 nm.
Hasil identifikasi alprazolam diperoleh waktu retensi alprazolam dalam sediaan tablet adalah sama dengan waktu retensi alprazolam BPFI yaitu pada 2,07. Hasil penelitian menunjukkan kadar alprazolam dalam sediaan tablet Zypraz (PT Kalbe Farma) = 102,83 ± 1,82%, Alprazolam (PT Dexa Medica) = 98,61 ± 0,34%, Apazol (PT Dexa Medica) = 97,61 ± 0,26%, Alviz (PT Phapros) = 95,72 ± 0,81%, Atarax (PT Mersi) = 91,01 ± 0,74%. Ini memenuhi persyaratan umum dari sediaan tablet dalam Farmakope Indonesia Edisi IV (1995), yaitu mengandung alprazolam tidak kurang dari 90% dan tidak lebih dari 110% dari jumlah yang tertera pada etiket. Uji validasi yang dilakukan pada tablet Zypraz (PT Kalbe Farma) menunjukkan persen perolehan kembali sebesar 100,17%, Relatif Standar Deviasi (RSD) = 1,24%, Batas Deteksi (LOD) = 0,05 µg/ml dan Batas Kuantitasi (LOQ) = 0,18 µg/ml. Ini berarti metode memiliki ketepatan dan ketelitian yang baik.
DETERMINATION OF ALPRAZOLAM IN TABLET BY HIGH PERFORMANCE LIQUID CHROMATOGRAPHY
ABSTRACT
One of the others anxiety and depression medicine in the market which includes the benzodiazepines are alprazolam. Determination of alprazolam in Farmakope Indonesia 4th Edition (1995) and USP 30th Edition (2007) confirmed by HPLC use mobile phase of phosphate buffer-acetonitrile-P-tetrahydrofuran. Use of phosphate buffer can cause crystallization in the column. The purpose of this study for method development use mobile phase of methanol-water in determination of alprazolam in tablets of generic and trade names. The validity test of this method is performed test of the accuracy, the precision, the Limit of Detection (LOD) and the Limit of Quantitation (LOQ).
Comparison of mobile phase used methanol-water (90:10), this comparison of mobile phase obtained from the results of optimization were
performed use Luna 5μ C18 column (250 x 4.60 mm id 5 μm) with flow rate 1.5
ml/minute and detected at wavelength of 254 nm.
The results of identification alprazolam obtained the retention time of alprazolam tablets are same with the retention time of alprazolam BPFI at 2.07. The results show the alprazolam level in Zypraz tablets (PT Kalbe Farma) = 102.83 ± 1.82%, Alprazolam tablets (PT Dexa Medica) = 98.61 ± 0.34%, Apazol tablets (PT Dexa Medica) = 97.6058% ± 0.2579, Alviz tablets (PT Phapros) = 95.72 ± 0.81%, Atarax tablets (PT Mersi) = 91.01 ± 0.74%. These met the general requitments for tablet drugs in Farmakope Indonesia 4th Edition (1995), which is not less than alprazolam 90% and not more than 110% of the labeled amount. Validation test performed at the Zypraz tablets (PT Kalbe Farma) show the percent recovery 100.17%, the Relative Standard Deviation (RSD) = 1.24%, the Limit of Detection (LOD) = 0.05 µg/ml and the Limit of Quantitation (LOQ) = 0.18 µg/ml. It means the method has good accuracy and precision.
DAFTAR ISI
Halaman
HALAMAN JUDUL ... 1
LEMBAR PENGESAHAN ... 3
KATA PENGANTAR ... 4
ABSTRAK ... 6
ABSTRACT ... 7
DAFTAR ISI ... 8
DAFTAR TABEL ... 12
DAFTAR GAMBAR ... 13
DAFTAR LAMPIRAN ... 14
BAB I PENDAHULUAN ... 16
1.1 Latar Belakang ... 16
1.2 Perumusan Masalah ... 17
1.3 Hipotesis ... 18
1.4 Tujuan Penelitian ... 18
1.5 Manfaat Penelitian ... 18
BAB II TINJAUAN PUSTAKA ... 19
2.1 Alprazolam ... 19
2.1.1 Sifat Fisikokimia ... 19
2.1.2 Farmakologi ... 19
2.1.3 Bentuk Sediaan ... 20
2.2 Kromatografi ... 20
2.2.2 Puncak Asimetris ... 20
2.3 Kromatografi Cair Kinerja Tinggi (KCKT) ... 21
2.3.1 Cara Kerja KCKT ... 22
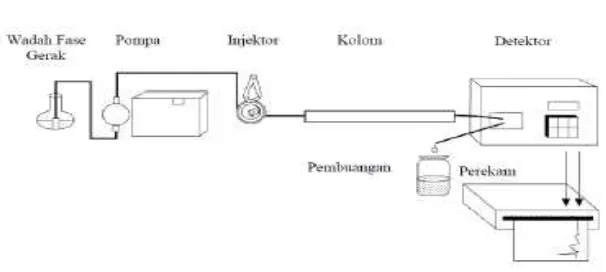
2.3.2 Komponen KCKT ... 23
2.3.3 Wadah Fase Gerak ... 23
2.3.4 Pompa ... 23
2.3.5 Injektor ... 24
2.3.6 Kolom ... 24
2.3.7 Detektor ... 25
2.3.8 Pengolahan Data ... 25
2.3.9 Fase Gerak ... 26
2.3.10 Elusi Gradien dan Isokratik ... 27
2.3.11 Jenis Pemisahan KCKT ... 27
2.4 Validasi Metode ... 27
2.4.1 Akurasi (Kecermatan) ... 28
2.4.2 Presisi (Keseksamaan) ... 28
2.4.3 Spesifisitas (Selektifitas) ... 28
2.4.4 Batas Deteksi dan Batas Kuantitasi ... 28
2.4.5 Linearitas ... 28
2.4.6 Rentang (Kisaran) ... 29
2.4.7 Kekuatan (Ketahanan) ... 29
2.4.8 Kekasaran (Ketangguhan) ... 29
BAB III METODE PENELITIAN ... 30
3.2 Alat ... 30
3.5.2.2 Penentuan Perbandingan Fase Gerak yang Optimum ... 31
3.5.3 Analisis Kualitatif Menggunakan KCKT ... 32
3.5.3.1 Uji Identifikasi Alprazolam Menggunakan KCKT
4.2 Analisa Kualitatif ... 39
4.3 Analisa Kuantitatif ... 41
4.3.1 Penentuan Kurva Kalibrasi ... 41
4.3.2 Penetapan Kadar Analit dalam Sampel yang Dianalisis ... 42
4.4 Hasil Uji Validasi ... 43
BAB V KESIMPULAN DAN SARAN ... 45
5.1 Kesimpulan ... 45
5.2 Saran ... 45
DAFTAR PUSTAKA ... 46
DAFTAR TABEL
Halaman Tabel 1. Pengaruh Komposisi Fase Gerak terhadap Parameter
Kromatogram ... 38 Tabel 2. Data Hasil Penyuntikan Larutan Alprazolam BPFI
Berdasarkan Luas Area ... 42 Tabel 3. Hasil Penetapan Kadar Alprazolam dalam Sediaan Tablet
dengan Nama Dagang dan Generik ... 42 Tabel 4. Hasil Pengujian Validasi, dengan parameter Akurasi, Presisi,
Batas Deteksi (LOD), Batas Kuantitasi (LOQ) Alprazolam pada tablet Zypraz (PT Kalbe Farma) dengan Menggunakan
DAFTAR GAMBAR
Halaman Gambar 1. Struktur Alprazolam ... 19 Gambar 2. Instrumen Dasar KCKT ... 23 Gambar 3. Kromatogram Alprazolam BPFI secara KCKT menggunakan
kolom Luna 5µ C18 (250 x 4,60 mm) dengan perbandingan fase gerak metanol-air (90:10) dan laju alir 1,5 ml/menit, volume penyuntikan 20 µl dan deteksi panjang gelombang
254 nm ... 39
Gambar 4. Kromatogram tablet Zypraz secara KCKT menggunakan kolom Luna 5µ C18 (250 x 4,60 mm) dengan perbandingan fase gerak metanol-air (90:10) dan laju alir 1,5 ml/menit, volume penyuntikan 20 µl dan deteksi panjang gelombang
254 nm ... 40
Gambar 5. Kurva kalibrasi Alprazolam BPFI menggunakan kolom Luna 5µ C18 (250 x 4,60 mm) dengan perbandingan fase gerak metanol-air (90:10) dan laju alir 1,5 ml/menit, volume penyuntikan 20 µl dan deteksi panjang gelombang 254 nm
... 41
Gambar 6. Alat KCKT Hitachi ... 116 Gambar 7. Alat Sonifikator Branson (1510) ... 117 Gambar 8. Pompa Vakum (Gast DO A-PG04-BN) dan Alat Penyaring
Fase Gerak ... 117
DAFTAR LAMPIRAN
Halaman Lampiran 1. Kromatogram Penyuntikan Alprazolam Baku untuk Mencari
Komposisi Fase Gerak Metanol-Air yang Optimum pada
Analasis ... 48 Lampiran 2. Kromatogram Larutan Alprazolam BPFI pada Pembuatan
Kurva Kalibrasi ... 50 Lampiran 3. Perhitungan Persamaan Regresi dari Kurva Kalibrasi
Alprazolam BPFI yang Diperoleh secara KCKT pada
Panjang Gelombang 254 nm ... 53
Lampiran 4. Perhitungan Recovery dengan Metode Adisi Standar ... 55 Lampiran 5. Kromatogram Hasil Recovery dari sampel Zypraz
(PT Kalbe Farma) ... 60
Lampiran 6. Hasil Pengujian Validasi, dengan parameter Akurasi, Presisi, Batas Deteksi (LOD), Batas Kuantitasi (LOQ) Alprazolam
pada Tablet Zypraz (PT Kalbe Farma) ... 72 Lampiran 7. Contoh Perhitungan % Recovery dengan Metode Adisi
Standar ... 73
Lampiran 8. Perhitungan Batas Deteksi (LOD) dan Batas kuantitasi (LOQ) Persamaan Regresi : Y = ax + b ... 74 Lampiran 9. Kromatogram dari Larutan tablet Zypraz (PT Kalbe Farma)
... 75 Lampiran 10. Kromatogram Spike dari Larutan tablet Zypraz
(PT Kalbe Farma) ... 79 Lampiran 11. Analisis Data Statistik untuk Mencari Kadar Sebenarnya
dari Penyuntikkan Larutan tablet Zypaz (PT Kalbe Farma)
... 80 Lampiran 12. Kromatogram dari larutan tablet Alprazolam
(PT Dexa Medica) ... 82 Lampiran 13. Analisis Data Statistik untuk Mencari Kadar Sebenarnya dari
Penyuntikkan Larutan tablet Alprazolam (PT Dexa Medica)
Lampiran 14. (Lanjutan) Analisis Data Statistik untuk Mencari Kadar
Sebenarnya dari Larutan tablet Alprazolam (PT Dexa Medica)
... 87
Lampiran 15. Kromatogram dari larutan tablet Apazol (PT Dexa Medica) ... 89
Lampiran 16. Analisis Data Statistik untuk Mencari Kadar Sebenarnya dari Penyuntikkan Larutan tablet Apazol (PT Dexa Medica) ... 93
Lampiran 17. (Lanjutan) Analisis Data Statistik untuk Mencari Kadar Sebenarnya dari Larutan tablet Apazol (PT Dexa Medica) ... 94
Lampiran 18. Kromatogram dari Larutan tablet Alviz (PT Pharos) ... 96
Lampiran 19. Analisis Data Statistik untuk Mencari Kadar Sebenarnya dari Penyuntikkan Larutan tablet Alviz (PT Pharos) ... 100
Lampiran 20. Kromatogram dari Larutan tablet Atarax (PT Mersi) ... 102
Lampiran 21. Analisis Data Statistik untuk Mencari Kadar Sebenarnya dari Penyuntikkan Larutan tablet Atarax (PT Mersi) ... 106
Lampiran 22. Perhitungan Penimbangan Sampel ... 108
Lampiran 23. Hasil Analisa Kadar Alprazolam dalam Sampel ... 109
Lampiran 24. Contoh Perhitungan untuk Mencari Kadar Alprazolam ... 111
Lampiran 25. Daftar Spesifikasi Sampel ... 112
Lampiran 26. Tabel Nilai Distribusi t ... 114
Lampiran 27. Sertifikat Alprazolam BPFI ... 115
Lampiran 28. Gambar alat KCKT (Hitachi) ... 116
PENETAPAN KADAR ALPRAZOLAM DALAM SEDIAAN TABLET DENGAN NAMA DAGANG DAN GENERIK SECARA KROMATOGRAFI
CAIR KINERJA TINGGI ABSTRAK
Salah satu obat ansietas dan depresi yang terdapat di pasaran yang termasuk kelompok benzodiazepin adalah alprazolam. Penetapan kadar alprazolam dalam Farmakope Indonesia Edisi IV (1995) dan USP Edisi XXX (2007) ditentukan secara KCKT menggunakan fase gerak dapar posfat-asetonitril-P-tetrahidrofuran. Penggunaan dapar posfat dapat menyebabkan pengkristalan pada kolom. Tujuan penelitian ini adalah melakukan pengembangan metode dengan menggunakan fase gerak metanol-air pada penetapan kadar alprazolam dalam tablet generik dan nama dagang. Untuk menguji validitas metode ini dilakukan uji akurasi, presisi, batas deteksi (LOD) dan batas kuantitasi (LOQ).
Perbandingan fase gerak yang digunakan adalah metanol-air (90:10), perbandingan fase gerak ini diperoleh dari hasil optimasi yang dilakukan menggunakan kolom Luna 5µ C18 (250 x 4,60 mm i.d. 5 µm) dengan laju alir 1,5 ml/menit dan dideteksi pada panjang gelombang 254 nm.
Hasil identifikasi alprazolam diperoleh waktu retensi alprazolam dalam sediaan tablet adalah sama dengan waktu retensi alprazolam BPFI yaitu pada 2,07. Hasil penelitian menunjukkan kadar alprazolam dalam sediaan tablet Zypraz (PT Kalbe Farma) = 102,83 ± 1,82%, Alprazolam (PT Dexa Medica) = 98,61 ± 0,34%, Apazol (PT Dexa Medica) = 97,61 ± 0,26%, Alviz (PT Phapros) = 95,72 ± 0,81%, Atarax (PT Mersi) = 91,01 ± 0,74%. Ini memenuhi persyaratan umum dari sediaan tablet dalam Farmakope Indonesia Edisi IV (1995), yaitu mengandung alprazolam tidak kurang dari 90% dan tidak lebih dari 110% dari jumlah yang tertera pada etiket. Uji validasi yang dilakukan pada tablet Zypraz (PT Kalbe Farma) menunjukkan persen perolehan kembali sebesar 100,17%, Relatif Standar Deviasi (RSD) = 1,24%, Batas Deteksi (LOD) = 0,05 µg/ml dan Batas Kuantitasi (LOQ) = 0,18 µg/ml. Ini berarti metode memiliki ketepatan dan ketelitian yang baik.
DETERMINATION OF ALPRAZOLAM IN TABLET BY HIGH PERFORMANCE LIQUID CHROMATOGRAPHY
ABSTRACT
One of the others anxiety and depression medicine in the market which includes the benzodiazepines are alprazolam. Determination of alprazolam in Farmakope Indonesia 4th Edition (1995) and USP 30th Edition (2007) confirmed by HPLC use mobile phase of phosphate buffer-acetonitrile-P-tetrahydrofuran. Use of phosphate buffer can cause crystallization in the column. The purpose of this study for method development use mobile phase of methanol-water in determination of alprazolam in tablets of generic and trade names. The validity test of this method is performed test of the accuracy, the precision, the Limit of Detection (LOD) and the Limit of Quantitation (LOQ).
Comparison of mobile phase used methanol-water (90:10), this comparison of mobile phase obtained from the results of optimization were
performed use Luna 5μ C18 column (250 x 4.60 mm id 5 μm) with flow rate 1.5
ml/minute and detected at wavelength of 254 nm.
The results of identification alprazolam obtained the retention time of alprazolam tablets are same with the retention time of alprazolam BPFI at 2.07. The results show the alprazolam level in Zypraz tablets (PT Kalbe Farma) = 102.83 ± 1.82%, Alprazolam tablets (PT Dexa Medica) = 98.61 ± 0.34%, Apazol tablets (PT Dexa Medica) = 97.6058% ± 0.2579, Alviz tablets (PT Phapros) = 95.72 ± 0.81%, Atarax tablets (PT Mersi) = 91.01 ± 0.74%. These met the general requitments for tablet drugs in Farmakope Indonesia 4th Edition (1995), which is not less than alprazolam 90% and not more than 110% of the labeled amount. Validation test performed at the Zypraz tablets (PT Kalbe Farma) show the percent recovery 100.17%, the Relative Standard Deviation (RSD) = 1.24%, the Limit of Detection (LOD) = 0.05 µg/ml and the Limit of Quantitation (LOQ) = 0.18 µg/ml. It means the method has good accuracy and precision.
BAB I PENDAHULUAN
1.1 Latar Belakang
Alprazolam merupakan kelompok obat benzodiazepin yang memiliki kerja pendek yang digunakan sebagai obat ansietas dan depresi. Ansietas merupakan perasaan khawatir atau ketakutan yang ditandai dengan gejala fisik seperti palpitasi, berkeringat, dan tanda-tanda stres lainnya (Tjay dan Rahardja, 2007).
Dalam perdagangan sediaan tablet alprazolam dijumpai dengan nama generik dan nama dagang dimana obat dengan nama generik harganya jauh lebih murah dibanding obat dengan nama dagang. Sementara masyarakat cenderung menilai bahwa kualitas obat identik dengan harga yang lebih tinggi, obat yang lebih mahal mutunya lebih baik daripada obat yang lebih murah harganya.
Dalam beberapa literatur penetapan kadar alprazolam dapat ditentukan secara KCKT menggunakan fase gerak dapar fosfat-asetonitril-P-tetrahidofuran (60:35:5), kolom 4,6 mm x 30 cm, detektor UV dengan panjang gelombang 254 nm (Ditjen POM, 1995); menggunakan fase gerak dapar fosfat-asetonitril-P-tetrahidofuran (60:35:5), kolom 4,6 mm x 10 cm, detektor UV dengan panjang gelombang 254 nm (USP, 2007); menggunakan fase gerak asetonitril-dapar fosfat (35:65), kolom C18 ODS (150 x 4,6 mm i.d. 5µm), detektor UV dengan panjang gelombang 240 nm (Moffat, dkk., 2005).
penyuntikan 20 µL. Akan tetapi, metode yang dilakukan tersebut belum divalidasi (Ashnagar, dkk., 2007).
Metode Kromatografi Cair Kinerja Tinggi (KCKT) merupakan metode yang sangat populer untuk menetapkan kadar senyawa obat baik dalam bentuk sediaan maupun dalam sampel hayati. Hal ini disebabkan karena KCKT merupakan metode yang memberikan sensitifitas yang tinggi. Selain itu, KCKT memiliki banyak keuntungan antara lain dapat digunakan untuk analisa suatu zat dalam jumlah kecil, waktu analisisnya relatif singkat, cukup sensitif dan selektif serta mudah dalam interpretasi yang diperoleh (Rohman dan Gandjar, 2007).
Persyaratan kadar untuk sediaan tablet Alprazolam, menurut Farmakope Indonesia Edisi IV yaitu mengandung Alprazolam tidak kurang dari 90,0% dan tidak lebih dari 110,0% dari jumlah yang tertera pada etiket (Ditjen POM, 1995).
Oleh karena itu, peneliti tertarik untuk menetapkan kadar alprazolam dalam sediaan tablet dengan nama dagang dan generik yang beredar di pasaran dan membandingkan hasil yang diperoleh dengan persyaratan yang tercantum dalam Farmakope Indonesia.
1.2 Perumusan Masalah
1. Apakah metode KCKT menggunakan fase gerak metanol-air dapat digunakan pada penetapan kadar alprazolam dalam sediaan tablet dan memberikan uji validasi metode yang memenuhi syarat?
1.3 Hipotesis
1. Metode KCKT dengan fase gerak metanol-air yang digunakan pada penetapan kadar alprazolam dalam sediaan tablet memenuhi persyaratan uji validasi metode.
2. Kadar alprazolam dalam sediaan tablet dengan nama dagang dan generik yang beredar di pasaran memenuhi persyaratan kadar yang ditetapkan Farmakope Indonesia edisi IV (1995).
1.4 Tujuan Penelitian
1. Menerapkan metode KCKT menggunakan fase gerak metanol-air dalam penetapan kadar alprazolam dalam sediaan tablet dan menguji validitas metode tersebut.
2. Mengetahui kesesuaian kadar tablet alprazolam dengan nama dagang dan generik yang beredar di pasaran dengan persyaratan kadar yang ditetapkan Farmakope Indonesia edisi IV (1995).
1.5 Manfaat Penelitian
1. Pengembangan ilmu bahwa penetapan kadar alprazolam dalam sediaan tablet dapat dilakukan dengan Kromatografi Cair Kinerja Tinggi (KCKT) menggunakan kolom C18 ODS (250 cm x 4,60 mm) dengan fase gerak metanol-air.
BAB II
TINJAUAN PUSTAKA
2.1 Alprazolam 2.1.1 Sifat fisikokimia Rumus struktur :
Gambar 1 Struktur Alprazolam
Nama Kimia :8-Kloro-1-metil-6-fenil-4H-s-triazolo[4,3-α] [1,4] benzodiazepina
Rumus Molekul : C17H13ClN Berat Molekul : 308,77
4
Pemerian : Serbuk hablur putih sampai hampir putih, melebur pada lebih kurang 2250
Kelarutan : Tidak larut dalam air, sukar larut dalam etil asetat, agak sukar larut dalam aseton, larut dalam metanol, mudah larut dalam kloroform (Ditjen POM, 1995).
.
2.1.2 Farmakologi
2.1.3 Bentuk Sediaan
Tablet 0,25 mg, 0,5 mg, 1 mg, 2 mg (Anonim, 2010).
2.2Kromatografi
Kromatografi pertama kali dikembangkan oleh ahli botani Rusia pada tahun 1903 yang bernama Michael Tswett untuk memisahkan pigmen warna dalam tanaman dengan cara perkolasi ekstrak petroleum eter dalam kolom gelas yang berisi kalsium karbonat. Saat ini kromatografi merupakan teknik pemisahan yang paling umum dan paling sering digunakan dalam bidang kimia analisis dan dapat dimanfaatkan untuk melalukan analisis, baik analisis kualitatif, analisis kuantitatif, atau preparatif dalam bidang farmasi, industri dan lain sebagainya. Kromatografi merupakan suatu teknik pemisahan yang menggunakan fase diam (stationary phase) dan fase gerak (mobile phase) (Rohman dan Gandjar, 2007).
2.2.1 Penggunaan Kromatografi
1. Pemakaian untuk tujuan kualitatif mengungkapkan ada atau tidak adanya senyawa tertentu dalam cuplikan
2. Pemakaian untuk tujuan kuantitatif menunjukkan banyaknya masing-masing komponen campuran
3. Pemakaian untuk tujuan preparatif untuk memperoleh komponen campuran dalam jumlah memadai dalam keadaan murni (Gritter, dkk., 1991).
2.2.2 Puncak Asimetris
Baik tinggi puncak maupun luasnya dapat dihubungkan dengan konsentrasi. Tinggi puncak mudah diukur, akan tetapi sangat dipengaruhi perubahan waktu retensi yang disebabkan oleh variasi suhu dan komposisi pelarut. Oleh karena itu, luas puncak dianggap merupakan parameter yang lebih akurat untuk pengukuran kuantitatif (Ditjen POM, 1995).
2.3 Kromatografi Cair Kinerja Tinggi (KCKT)
Kromatografi cair kinerja tinggi (KCKT) merupakan sistem pemisahan dengan kecepatan dan efisiensi yang tinggi. Hal ini karena didukung oleh kemajuan dalam teknologi kolom, sistem pompa tekanan tinggi, dan detektor yang sangat sensitif dan beragam. KCKT mampu menganalisa berbagai cuplikan secara kualitatif maupun kuantitatif, baik dalam komponen tunggal maupun campuran (Ditjen POM, 1995).
KCKT merupakan teknik pemisahan yang diterima secara luas untuk analisis dan pemurnian senyawa tertentu dalam suatu sampel pada sejumlah bidang antara lain: farmasi, lingkungan dan industri-industri makanan (Munson, 1991).
Kelebihan KCKT antara lain:
−Mampu memisahkan molekul-molekul dari suatu campuran −Resolusinya baik
−Mudah melaksanakannya
−Kecepatan analisis dan kepekaannya tinggi
−Dapat dihindari terjadinya dekomposisi/kerusakan bahan yang dianalisis −Dapat digunakan bermacam-macam detektor
−Kolom dapat digunakan kembali
−Tekniknya tidak begitu tergantung pada keahlian operator dan
reprodusibilitasnya lebih baik
−Instrumennya memungkinan untuk bekerja secara automatis dan kuantitatif −Waktu analisis umumnya singkat
−Kromatografi cair preparatif memungkinkan dalam skala besar
−Ideal untuk molekul besar dan ion (Munson, 1991).
2.3.1 Cara Kerja KCKT
2.3.2 Komponen KCKT
Gambar 4. Bagan alat KCKT
Gambar 2 Instrument Dasar KCKT 2.3.3 Wadah Fase Gerak
Wadah fase gerak harus bersih dan inert. Wadah pelarut kosong ataupun labu laboratorium dapat digunakan sebagai wadah fase gerak. Wadah ini biasanya dapat menampung fase gerak antara 1 sampai 2 liter pelarut. Fase gerak sebelum digunakan harus dilakukan degassing (penghilangan gas) yang ada pada fase gerak, sebab adanya gas akan berkumpul dengan komponen lain terutama dipompa dan detektor sehingga akan mengacaukan analisis (Rohman dan Gandjar, 2007).
2.3.4 Pompa
2.3.5 Injektor
Ada 3 jenis injektor, yakni syringe injector, loop valve dan automatic
injector (autosampler). Syringe injector merupakan bentuk injektor yang paling sederhana (Meyer, 2004).
Pada waktu sampel diinjeksikan ke dalam kolom, diharapkan agar aliran pelarut tidak mengganggu masuknya keseluruhan sampel ke dalam kolom. Sampel dapat langsung diinjeksikan ke dalam kolom (on column injection) atau digunakan katup injeksi (Meyer, 2004).
Katup putaran (loop valve), tipe injektor ini umumnya digunakan untuk menginjeksi volume lebih besar daripada 10 µl dan sekarang digunakan dengan cara otomatis (dengan adaptor khusus, volume-volume lebih kecil dapat diinjeksikan secara manual). Bila katup difungsikan, maka cuplikan di dalam putaran akan bergerak ke dalam kolom (Meyer, 2004).
Automatic injector atau disebut juga autosampler memiliki prinsip yang mirip, hanya saja sistem penyuntikannya bekerja secara otomatis (Meyer, 2004).
2.3.6 Kolom
Kolom adalah jantung kromatografi. Berhasil atau gagalnya suatu analisis tergantung pada pemilihan kolom dan kondisi percobaan yang sesuai. Kolom dapat dibagi menjadi dua kelompok :
b. Kolom preparatif : umumnya memiliki diameter 6 mm atau lebih besar dan panjang kolom 25 – 100 cm.
Kolom umumnya dibuat dari stainless steel dan biasanya dioperasikan pada temperatur kamar, tetapi bisa juga digunakan temperatur lebih tinggi, terutama untuk kromatografi penukar ion dan kromatografi eksklusi (Putra, 2007).
2.3.7 Detektor
Suatu detektor dibutuhkan untuk mendeteksi adanya komponen cuplikan dalam aliran yang keluar dari kolom. Detektor-detektor yang baik memiliki sensitifitas yang tinggi, gangguan (noise) yang rendah, kisar respons linier yang luas, dan memberi tanggapan/respon untuk semua tipe senyawa. Suatu kepekaan yang rendah terhadap aliran dan fluktuasi temperatur sangat diinginkan, tetapi tidak selalu dapat diperoleh (Johnson dan Stevenson, 1991).
Detektor yang paling banyak digunakan dalam kromatografi cair modern kecepatan tinggi adalah detektor spektrofotometer UV 254 nm. Bermacam-macam detektor dengan variasi panjang gelombang UV-Vis sekarang menjadi populer karena mereka dapat digunakan untuk mendeteksi senyawa-senyawa dalam rentang yang luas. Detektor lainnya, antara lain: detektor fluometer, detektor ionisasi nyala, detektor elektrokimia dan lain-lain juga telah digunakan (Johnson dan Stevenson, 1991).
2.3.8 Pengolahan Data
Guna kromatogram: 1. Kualitatif
Waktu retensi selalu konstan dalam setiap kondisi kromatografi yang sama dapat digunakan untuk identifikasi.
2. Kuantitatif
Luas puncak proporsional dengan jumlah sampel yang diinjeksikan dan dapat digunakan untuk menghitung konsentrasi (Johnson dan Stevenson, 1991).
2.3.9 Fase Gerak
Dalam kromatografi cair komposisi pelarut atau fase gerak adalah satu variabel yang mempengaruhi pemisahan. Terdapat keragaman yang luas dari fase gerak yang digunakan dalam semua mode KCKT, tetapi ada beberapa sifat-sifat yang diinginkan yang mana umumnya harus dipenuhi oleh semua fase gerak (Putra, 2007).
Fase gerak harus:
• Murni, tidak ada pencemar/kontaminan
• Tidak bereaksi dengan pengemas
• Sesuai dengan detektor • Melarutkan cuplikan
• Mempunyai viskositas rendah
• Tersedia diperdagangan dengan harga yang pantas (Putra, 2007).
2.3.10 Elusi Gradien dan Isokratik
Elusi pada KCKT dapat dibagi menjadi dua sistem yaitu:
1. Sistem elusi isokratik. Pada sistem ini, elusi dilakukan dengan satu macam atau lebih fase gerak dengan perbandingan tetap (komposisi fase gerak tetap selama elusi).
2. Sistem elusi gradien. Pada sistem ini, elusi dilakukan dengan campuran fase gerak yang perbandingannya berubah-ubah dalam waktu tertentu (komposisi fase gerak berubah-ubah selama elusi) (Putra, 2007).
2.3.11 Jenis Pemisahan Kromatografi Cair Kinerja Tinggi
Berdasarkan jenis fase gerak dan fase diamnya, jenis pemisahan KCKT dibedakan atas :
a. Kromatografi Fase Normal
Kromatografi dengan kolom yang fase diamnya bersifat polar, misalnya silika gel, alumina, sedangkan fase geraknya bersifat non polar seperti heksan.
b. Kromatografi Fase Terbalik
Pada kromatografi fase terbalik, fase diamnya bersifat non polar, yang banyak dipakai adalah oktadesilsilan (ODS atau C18) dan oktilsilan (C8). Sedangkan fase geraknya bersifat polar, seperti air, metanol dan asetonitril (Mulja dan Suharman, 1995).
2.4 Validasi metode
Validasi merupakan persyaratan mendasar yang diperlukan untuk menjamin kualitas dan hasil dari semua aplikasi analitik (Ermer, 2005).
Adapun karakteristik dalam validasi metode menurut USP (United States
batas deteksi, batas kuantitasi, linieritas, rentang/kisaran dan kekuatan/ketahanan dan kekasaran/ketangguhan.
2.4.1 Akurasi (Kecermatan)
Akurasi merupakan ketlitian metode analisis atau kedekatan antara nilai terukur dengan nilai sebenarnya. Akurasi dinyatakan dalam persen perolehan kembali (% recovery) (Harmita, 2004).
2.4.2 Presisi (Keseksamaan)
Presisi merupakan ukuran keterulangan metode analisis yang diperoleh dari beberapa kali pengukuran pada sampel yang sama dan biasanya diekspresikan sebagai Relatif Standar Deviasi (RSD) (Rohman dan Gandjar, 2007).
2.4.3 Spesifisitas (Selektifitas)
Spesifisitas/selektifitas adalah kemampuan untuk mengukur analit yang dituju secara tepat dan spesifik dengan adanya komponen lain dalam matriks sampel seperti ketidakmurnian, produk degradatif dan komponen matriks (Ermer, 2005).
2.4.4 Batas Deteksi dan Batas Kuantitasi
Batas deteksi adalah konsentrasi analit terendah dalam sampel yang masih dapat dideteksi, meskipun tidak selalu dapat dikuantifikasi. Sedangkan batas kuantitasi adalah konsentrasi analit terendah dalam sampel yang dapat ditentukan dengan presisi dan akurasi yang dapat diterima pada kondisi metode yang digunakan (USP XXX, 2007).
2.4.5 Linearitas
diberikan. Linieritas dapat ditentukan secara langsung dengan pengukuran sampel (analit) yang ditambahkan baku pada sekurang-kurangnya lima titik konsentrasi yang mencakup seluruh rentang konsentrasi kerja (Ermer, 2005).
2.4.6 Rentang (Kisaran)
Rentang/kisaran adalah konsentrasi terendah dan tertinggi yang mana suatu metode analitik menunjukkan akurasi, presisi dan linieritas yang dapat digunakan untuk menganalisis sampel (Ermer, 2005).
2.4.7 Kekuatan (Ketahanan)
Kekuatan/ketahanan merupakan pengujian kemampuan dari suatu metode untuk tidak terpengaruh oleh adanya perubahan parameter dalam melakukan metode analitik seperti persentase kandungan pelarut organik dalam fase gerak, pH larutan dapar, waktu pengekstraksian analit, komposisi pengekstraksi dan perbandingan konsentrasi fase gerak (Épshtein, 2004).
2.4.8 Kekasaran (Ketangguhan)
BAB III
METODE PENELITIAN
3.1 Tempat dan waktu penelitian
Penelitian dilakukan pada laboratorium penelitian Fakultas Farmasi Universitas Sumatera Utara pada bulan Juli sampai Oktober tahun 2011.
3.2 Alat-alat
Alat – alat yang digunakan dalam penelitian ini adalah seperangkat instrumen KCKT lengkap (Hitachi) dengan pompa, degasser (DGU 20 AS), injektor
Autosampler, kolom Luna Phenomenex C18 (250 x 4,60 mm), detektor UV, wadah fase gerak, vial khusus Autosampler, Sonifikator (Branson 1510), pompa vakum (Gast DOA-P604-BN), neraca analitik (Mettler Toledo), membrane filter
PTFE 0,5 µm dan 0,2 µm, cellulose nitrate membran filter 0,45 µm.
3.3 Bahan-bahan
Bahan-bahan yang digunakan adalah metanol grade for HPLC (E.Merck), dan akuabides (PT. Ikapharmindo Putramas), Alprazolam BPFI, tablet Alprazolam 0,5 mg (PT Dexa Medica), tablet Apazol 0,5 mg (PT Dexa Medica), tablet Atarax 0,5 mg (PT Mersi), tablet Zypraz 0,5 mg (PT Kalbe), tablet Alviz 0,5 mg (PT Pharos).
3.4 Pengambilan Sampel
0,5 mg (PT Dexa Medica), tablet Atarax 0,5 mg (PT MersiFarma TM), tablet Zypraz 0,5 mg (PT Kalbe), tablet Alviz 0,5 mg (PT Pharos).
3.5 Prosedur Penelitian
3.5.1 Pembuatan Fase Gerak
Metanol 500 ml di saring dengan menggunakan mebran filter PTFE 0,5 µm dan diawaudarakan selama 30 menit. Akuabides 500 ml di saring dengan menggunakan cellulose nitrate membran filter 0,45 µm dan diawaudarakan selama 30 menit.
3.5.2 Prosedur Analisis
3.5.2.1 Penyiapan Kromatografi Cair
Kinerja Tinggi
Masing - masing unit diatur, kolom yang digunakan C18 (250 x 4,60 mm), detektor UV-Vis dan dideteksi pada panjang gelombang 254 nm. Setelah alat KCKT dihidupkan, maka pompa dijalankan dan fase gerak dibiarkan mengalir selama 30 menit dengan laju alir 1,5 ml/menit sampai diperoleh garis alas yang datar, menandakan sistem tersebut telah stabil.
3.5.2.2Penentuan Perbandingan Fase Gerak Optimum
3.5.3 Analisis Kualitatif Menggunakan KCKT
3.5.3.1 Uji Identifikasi Alprazolam menggunakan KCKT
sebanyak 10 µg/ml ke dalam larutan sampel kemudian dianalisis pada kondisi KCKT yang sama. Luas area dan waktu retensi yang sama diamati kembali dan dibandingkan antara kromatogram hasil spiking dengan kromatogram larutan sampel sebelum spiking. Sampel dinyatakan mengandung alprazolam, jika terjadi peningkatan tinggi puncak dan luas area pada kromatogram hasil spiking dengan waktu retensi sama seperti pada kromatogram penyuntikan larutan alprazolam BPFI.
3.5.4 Analisis Kuantitatif
3.5.4.1 Pembuatan Larutan Induk Baku Alprazolam BPFI
Ditimbang seksama sejumlah 10,0 mg serbuk alprazolam BPFI, dimasukkan kedalam labu tentukur 50 ml, dilarutkan dan diencerkan dengan pelarut hingga garis tanda sehingga diperoleh larutan dengan konsentrasi 200 µg/ml (LIB I).
Dari LIB I dipipet 1 ml, lalu dimasukkan kedalam labu tentukur 50 ml dan diencerkan dengan pelarut dan dicukupkan hingga garis tanda sehingga diperoleh larutan dengan konsenterasi 4 µg/ml (LIB II)
3.5.4.2 Pembuatan Kurva Kalibrasi Alprazolam BPFI
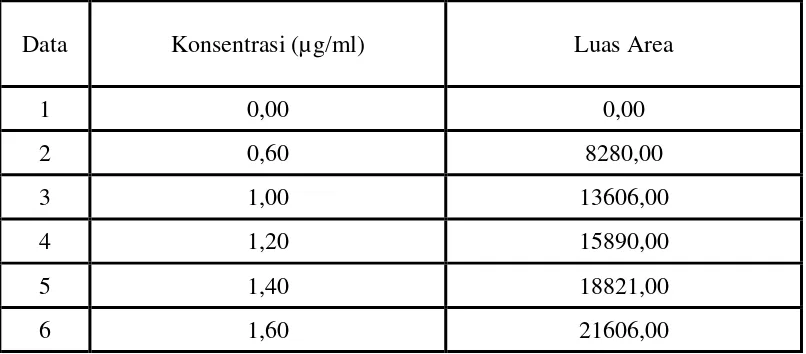
Dipipet LIB II sebanyak 1,5 ml, 2,5 ml, 3,0 ml, 3,5 ml, dan 4,0 ml, dimasukkan dalam labu tentukur 10 ml, diencerkan dengan pelarut hingga garis tanda. Kocok sehingga diperoleh konsentrasi 0,6 µg/ml, 1,0 µg/ml, 1,2 µg/ml, 1,4 µg/ml dan 1,6 µg/ml. Kemudian masing-masing larutan disaring dengan
Dari luas area yang diperoleh pada kromatogram dibuat kurva kalibrasi kemudian dihitung persamaan garis regresi dan faktor korelasinya.
3.5.4.3 Penetapan Kadar Sampel
Ditimbang 20 tablet untuk masing-masing jenis tablet, kemudian digerus sejumlah serbuk dan ditimbang seksama sejumlah tablet setara dengan ± 0,5 mg Alprazolam, lalu dimasukkan kedalam labu tentukur 50 ml, dilarutkan dan dicukupkan dengan pelarut hingga garis tanda sehingga diperoleh larutan dengan konsentrasi 10 µg/ml, dikocok ± 5 menit, kemudian disaring dengan kertas saring, ± 5 ml filtrat pertama dibuang. Dipipet 2,5 ml filtrat, dimasukkan kedalam labu tentukur 25 ml, dan dicukupkan hingga garis tanda sehingga diperoleh larutan dengan konsentrasi 1 µg/ml. Dikocok ± 5 menit lalu disaring dengan membran filter PTFE 0,2 µm. Diinjeksikan sebanyak 20 µl kesistem KCKT vial
autosampler dan dideteksi pada panjang gelombang 254 nm dengan perbandingan fase gerak metanol-air (90:10), laju alir 1,5 ml/menit. Dilakukan sebanyak 6 kali perlakuan untuk setiap sampel.
Kadar dapat dihitung dengan mensubtitusikan luas area sampel pada Y dari persamaan regresi : Y = ax + b
3.5.4.4 Analisis Data Penetapan Kadar Secara Statistik
Data perhitungan kadar dianalisis secara statistik menggunakan uji t. Menurut Harmita (2004), Rumus yang digunakan untuk menghitung Standar Deviasi (SD) adalah:
Kadar dapat dihitung dengan persamaan garis regresi dan untuk menentukan data diterima atau ditolak digunakan rumus:
t hitung
Dengan dasar penolakan apabila t hitung ≥ t tabel , pada taraf kepercayaan 99% dengan nilai α = 0,01, dk = n – 1.
Keterangan :
SD = Standar Deviasi
X = Kadar dalam Satu Perlakuan
X = Kadar Rata-Rata dalam Satu Sampel n = Jumlah Perlakuan
Menurut Wibisono (2005), untuk mencari kadar sebenarnya dapat digunakan rumus:
μ = Kadar sebenarnya
X = Kadar sampel n = Jumlah perlakuan t = Harga ttabel
dk= Derajad kebebasan
sesuai dengan derajat kepercayaan
3.5.5 Validasi Metode
3.5.5.1 Akurasi (Kecermatan)
Uji akurasi ditentukan dengan menggunakan metode penambahan baku (standard addition method), yakni ke dalam sampel ditambahkan larutan baku alprazolam 80%, 100%, 120% dari rata-rata kadar alprazolam yang terdapat pada sampel, kemudian dianalisis dengan perlakuan yang sama seperti pada penetapan kadar sampel (Épshtein, 2004).
Menurut Harmita (2004), hasil dinyatakan dalam persen perolehan kembali (% receovery). Persen perolehan kembali dapat dihitung dengan rumus:
% Perolehan kembali =
A
CF = konsentrasi total sampel yang diperoleh dari pengukuran (µg/g)
CA = konsentrasi sampel sebenarnya (µg/g) C*A = konsentrasi analit yang ditambahkan (µg/g)
3.5.5.2Presisi (Keseksamaan)
Menurut Rohman dan Gandjar (2007), presisi merupakan ukuran keterulangan metode analisis yang diperoleh dari beberapa kali pengukuran pada sampel yang sama dan biasanya diekspresikan sebagai Relatif Standar Deviasi (RSD) (Rohman dan Gandjar, 2007).
Nilai RSD dirumuskan dengan :
Sementara itu, nilai SD dihitung dengan :
X = nilai dari masing-masing pengukuran
X = rata-rata (mean) dari pengukuran n = banyaknya data
3.5.5.3 Batas Deteksi (LOD) dan Batas Kuantitasi (LOQ)
Menurut Ephstein (2004), Batas Deteksi (Limit Of Detection/ LOD) dan Batas Kuantitasi (Limit Of Quantitation/ LOQ) dapat dihitung dengan menggunakan rumus sebagai berikut :
BAB IV
HASIL DAN PEMBAHASAN
4.1 Penentuan komposisi fase gerak untuk mendapatkan kondisi kromatografi yang optimal
Perbandingan fase gerak dan laju alir yang digunakan pada penelitian ini merujuk pada literatur dari Ashnagar yaitu fase gerak metanol-air 90:10 dengan laju alir 1,5 ml/menit menggunakan C18 ODS
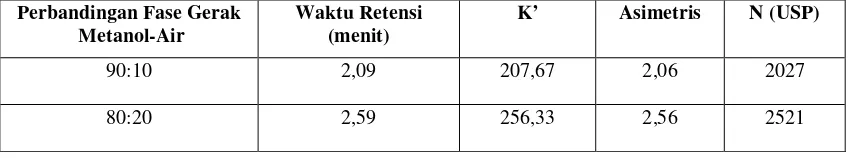
Pada awal penelitian ini dilakukan optimasi karena kolom yang digunakan berbeda dengan kolom yang digunakan oleh Ashnagar, dkk. Adapun perbandingan fase gerak yang dioptimasi adalah metanol-air dengan perbandingan 60:40, 70:30, 80:20, 90:10 pada laju alir 1,5 ml/menit, deteksi dilakukan pada panjang gelombang 254 nm. Dari hasil optimasi menggunakan kolom Luna 5µ C18 (250 x 4,60 mm) diperoleh perbandingan fase gerak yang terbaik yaitu pada perbandingan metanol-air 90:10. Pemilihan fase gerak yang terbaik ini didasarkan pada waktu retensi yang relatif singkat. Hubungan antara pengaruh komposisi fase gerak terhadap parameter kromatogram dapat dilihat pada Tabel 1 dibawah ini. Kromatogram dapat dilihat pada Lampiran 1.
(30 cm x 4,5 mm i.d 2-5µm), detektor UV dengan panjang gelombang 254 nm (Ashnagar, dkk., 2007).
Tabel 1 Pengaruh Komposisi Fase Gerak terhadap Parameter Kromatogram
Berdasarkan data diatas dapat dilihat bahwa, semakin besar konsentrasi metanol dalam fase gerak maka waktu retensi alprazolam akan semakin singkat. Hal ini dikarenakan kekuatan fase gerak (solvent strength), dimana pada kromatografi, konsentrasi metanol yang lebih besar akan mengakibatkan fase gerak semakin kuat sehingga proses elusi terjadi lebih cepat, maka waktu retensi analit menjadi lebih singkat (Synder and Kirkland, 1979).
4.2 Analisa Kualitatif
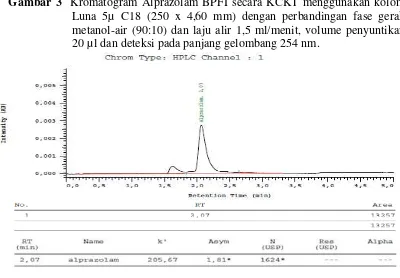
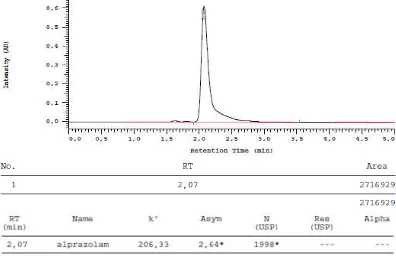
Dari hasil optimasi pada penentuan kondisi kromatografi yang terbaik untuk alprazolam diperoleh komposisi fase gerak metanol-air 90:10, laju alir 1,5 ml/menit. Dengan kondisi kromatogram ini, hasil uji identifikasi pada penyuntikan alprazolam BPFI diperoleh kromatogram dengan waktu retensi 2,09 dan waktu retensi ini hampir sama dengan waktu retensi sampel yang dianalisis yaitu pada menit ke-2,07. Kromatogram dapat dilihat pada Gambar 3 dan Gambar 4 dibawah ini.
70:30 3,74 373,00 - 2727
Gambar 3 Kromatogram Alprazolam BPFI secara KCKT menggunakan kolom Luna 5µ C18 (250 x 4,60 mm) dengan perbandingan fase gerak metanol-air (90:10) dan laju alir 1,5 ml/menit, volume penyuntikan 20 µl dan deteksi pada panjang gelombang 254 nm.
Gambar 4 Kromatogram tablet Zypraz secara KCKT menggunakan kolom Luna 5µ C18 (250 x 4,60 mm) dengan perbandingan fase gerak metanol-air (90:10) dan laju alir 1,5 ml/menit, volume penyuntikan 20 µl dan deteksi pada panjang gelombang 254 nm.
Meskipun waktu retensi yang ditunjukkan tidak sama persis, namun waktu retensi yang diamati pada kromatogram sampel dapat diterima sebagai waktu retensi alprazolam karena masih berada dalam rentang waktu retensi yang dapat diterima yaitu ± 5% dari waktu retensi BPFI.
Untuk mempertegas identifikasi dari semua sampel diperoleh waktu retensi alprazolam pada menit ke-2,07 dan setelah dilakukan metode spike juga diperoleh waktu retensi pada menit ke-2,07 dengan luas area yang meningkat. Ini menunjukkan bahwa semua tablet yang ditentukan mengandung alprazolam. Kromatogram spike dapat dilhat pada Lampiran 10.
yanag mengandung alprazolam dilakukan spiking yaitu menambahkan bahan baku kedalam sampel pada kondisi kromatografi yang sama. Hal ini dilakukan dengan cara: Pertama, dilakukan proses kromatografi sampel tanpa penambahan baku. Kedua, sampel dengan penambahan bahan baku dilakukan proses kromatografi. Pada puncak 2,07 terjadi peningkatan tinggi puncak/lebar puncak setelah penambahan baku dibandingkan tinggi puncak/lebar puncak sebelum penambahan baku, maka dapat diidentifikasi bahwa sampel mengandung alprazolam (Johnson dan Stevenson, 1991).
4.3 Analisis Kuantitatif
4.3.1 Penentuan Kurva Kalibrasi
Gambar 5 Kurva kalibrasi Alprazolam BPFI secara KCKT menggunakan kolom Luna 5µ C18 (250 x 4,60 mm) dengan perbandingan fase gerak metanol-air (90:10) dan laju alir 1,5 ml/menit, volume penyuntikan 20 µl dan deteksi pada panjang gelombang 254 nm.
Tabel 2 Data hasil penyuntikan larutan alprazolam BPFI berdasarkan Luas Area
4.3.2 Penetapan Kadar Analit dalam Sampel yang dianalisis
Hasil penetapan kadar alprazolam dalam sediaan tablet dengan nama dagang dan generik dapat dilihat pada Tabel 3 di bawah ini.
Tabel 3 Hasil penetapan kadar alprazolam dalam sediaan tablet dengan nama dagang dan generik
Sediaan tablet alprazolam dengan nama dagang dan generik yang ditentukan kadarnya berdasarkan luas area keseluruhannya memenuhi persyaratan yang ditetapkan Farmakope Indonesia edisi IV (1995) yaitu mengandung
Data Konsentrasi (µg/ml) Luas Area
1 0,00 0,00
Nama Sediaan Kadar Alprazolam (%)
alprazolam tidak kurang dari 90,0% dan tidak lebih dari 110,0% dari jumlah yang tertera pada etiket (Ditjen POM, 1995).
4.4 Hasil Uji Validasi
Pada penelitian ini dilakukan uji validasi metode dengan metode standar adisi terhadap sampel tablet Zypraz (PT Kalbe Farma) yang meliputi uji akurasi dengan parameter % recovery dan uji presisi dengan parameter RSD (Relative
Standard Deviasi), LOD (Limit of Detection) dan LOQ (Limit of Quantitation). Uji akurasi dengan parameter % recovery dilakukan dengan membuat tiga konsentrasi analit dengan rentang spesifik 80%, 100%, dan 120%, masing- masing dengan tiga replikasi dan setiap rentang spesifik mengandung 70% analit dan 30% baku pembanding (Harmita, 2004).
Data hasil uji validasi, parameter akurasi dan presisi alprazolam dengan metode adisi standar dapat dilihat pada Tabel 4.
Dari tabel di atas diperoleh hasil pengujian akurasi dengan kadar rata-rata
% recovery 100,17%, % recovery dapat diterima karena memenuhi syarat akurasi, bahwa rentang rata-rata % recovery ialah 98-102%. Maka dapat disimpulkan bahwa metode ini mempunyai akurasi yang baik (Epshtein, 2004).
Hasil uji presisi dengan parameter RSD (Relative Standard Deviasi) diperoleh 1,25%, persyaratan nilai RSD yang ditentukan adalah < 2%. Maka dapat disimpulkan bahwa metode analisis mempunyai presisi yang baik (Harmita, 2004).
Batas deteksi dan batas kuantitasi dihitung dari persamaan regresi yang diperoleh dalam kurva kalibrasi. Dari hasil perhitungan diperoleh nilai LOD 0,05 µg/ml dan nilai LOQ 0,17 µg/ml.
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Metode KCKT pada penetapan kadar alprazolam dalam tablet menggunakan kolom Luna 5µ C18 (250 x 4,60 mm) dengan fase gerak metanol-air (90:10), laju alir 1,5 ml/menit, panjang gelombang 254 nm memenuhi persyaratan uji validasi metode dengan parameter akurasi, presisi, batas deteksi dan batas kuantitasi.
Kadar alprazolam dengan nama dagang dan generik yang dianalisis dari lima sediaan tablet di pasaran dengan kondisi kromatografi yang terpilih diperoleh hasil yang memenuhi persyaratan kadar untuk sediaan tablet yaitu mengandung alprazolam tidak kurang dari 90,0% dan tidak lebih dari 110,0% dari jumlah yang tertera pada etiket.
5.2 Saran
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Metode KCKT pada penetapan kadar alprazolam dalam tablet menggunakan kolom Luna 5µ C18 (250 x 4,60 mm) dengan fase gerak metanol-air (90:10), laju alir 1,5 ml/menit, panjang gelombang 254 nm memenuhi persyaratan uji validasi metode dengan parameter akurasi, presisi, batas deteksi dan batas kuantitasi.
Kadar alprazolam dengan nama dagang dan generik yang dianalisis dari lima sediaan tablet di pasaran dengan kondisi kromatografi yang terpilih diperoleh hasil yang memenuhi persyaratan kadar untuk sediaan tablet yaitu mengandung alprazolam tidak kurang dari 90,0% dan tidak lebih dari 110,0% dari jumlah yang tertera pada etiket.
5.2 Saran
DAFTAR PUSTAKA
Anonim. (2010). ISO (Informasi Spesialite Obat Indonesia). Volume 45. Jakarta: Ikatan Sarjana Farmasi Indonesia. Hal. 421-425.
Ashnager, A., Kouchak, M., Soltani, M. dan Salimi, A. (2007). Invitro Evaluation of Some Different Brands of Alprazolam Tablets. E-Journal of Chemistry. 4 (4): 568-572.
Ditjen POM. (1995). Farmakope Indonesia Edisi ke IV. Jakarta: Departemen Kesehatan Republik Indonesia. Hal. 79-80.
Ermer, J. (2005). Method Validation in Pharmaceutical Analysis. Weinheim: Wiley-VCH Verlag GmbH & Co. KGaA. Hal. 3-5, 16.
Épshtein, N.A. (2004). Validation of HPLC Techniques for Pharmaceutical Analysis. Pharmaceutical Chemistry Journal 38(4): Pages 212 – 228. Ermer, J. (2005). Analytical Validation within the Pharmaceutical Environment.
In: Ermer, J., dan Miller, J.H McB., editors. Method Validation in Pharmaceutical Analysis. Weinhein: Wiley-VCH Verlag GmbH & Co. KgaA: hal. 54, 63-70,80,101.
Gritter, R. J, Bobbit, J. M, dan Schwarting, A. E. (1985). Pengantar Kromatografi. Edisi III. Terjemahan K. Padmawinata. Bandung: Penerbit ITB. Hal. 186.
Harmita. (2004). Petunjuk Pelaksanaan Validasi Metode dan Cara Perhitungannya. Majalah Ilmu Kefarmasian. I (3): 117-135.
Johnson, E. L. dan Stevenson, R. (1991). Dasar Kromatografi Cair. Terjemahan K. Padmawinata. Bandung: Penerbit ITB. Hal. 1-40.
Meyer, V.R. (2004). Practical High-Performance Liquid Chromatography. Fourth Edition. Chichester: John Wiley and Sons Inc. Page 4.
Moffat, A. C., Osselton, M. D. dan Widdop, B. (2005). Clarke’s Analysis Of Drug And Poisons. Thirth edition. London: Pharmaceutical Press. Electronic Version.
Munson, J. W. (1991). Analisis Farmasi Metode Modern. Terjemahan Harjana. Surabaya: Penerbit Air langga Univercity Press. Hal. 14-46.
Putra, E.D.L. (2007). Dasar-dasar Kromatografi Gas & Kromatografi Cair Kinerja Tinggi. Medan: Fakultas Farmasi USU. Hal. 88-91.
Rohman, A. dan Gandjar, I. G. (2007). Kimia Farmasi Analisis. Yogyakarta: Pustaka Pelajar. Hal. 378-390, 406, 456-473.
Synder, L., and Kirkland, J. (1979). Introduction to Modern Liquid Chromatography. 2th Edition. London: John Willey and Son. Hal.554. Sudjana. (2005). Metode Statistika. Edisi VI. Bandung: Tarsito. Hal. 93.
Tjay, T. H. dan Rahardja, K. (2007). Obat-Obat Penting Khasiat, Penggunaan, dan Efek-Efek Sampingnya. Edisi Keenam. Jakarta: PT. Elex Media Komputindo. Hal. 343, 365.
USP. (2007). The United States Pharmacopeia. 30th Edition. United States.
Electronic Version.
Lampiran 1 Kromatogram Penyuntikan Alprazolam Baku untuk Mencari Komposisi Fase Gerak Metanol-Air yang Optimum pada Analisis
Perbandingan Fase Gerak Metanol-Air (60:40) dengan Laju Alir 1,5 ml/menit
Perbandingan Fase Gerak Metanol-Air (80:20) dengan Laju Alir 1,5 ml/menit
v
Lampiran 2 Kromatogram Larutan Alprazolam BPFI pada Pembuatan Kurva Kalibrasi
A
C
D
E
Lampiran 3 Perhitungan Persamaan Regresi dari Kurva Kalibrasi Alprazolam BPFI yang Diperoleh secara KCKT pada Panjang Gelombang 254 nm
Data Hasil Penyuntikan Larutan Alprazolam BPFI Berdasarkan Luas Area
Konsenterasi (X) VS Luas Area (Y) untuk Alprazolam
Y = ax + b
= b =
= (12943,8333) – ( ) (0,9967) = 180,0156
Sehingga diperoleh persamaan regresi Y = 13203,9494X + 180,0156 No Konsentrasi (µg/ml) Luas Area
1 0 0
Untuk mencari hubungan kadar (X) dengan luas area (Y) digunakan pengujian koefisien korelasi (r)
Lampiran 4 Perhitungan Recovery dengan Metode Adisi Standar
Berat 1 tablet Alprazolam yang mengandung 0,5 mg Alprazolam
Rentang spesifik : 80%, 100% 120% dan setiap rentang mengandung 70% analit dan 30% baku pembanding.
Rentang 80% : Alprazolam = Analit 70% :
= mg = 280 µg
Serbuk sampel yang ditimbang setara 0,28 mg alprazolam = x 4490 mg = 125,72 mg
Baku Pembanding 30% :
= = 120 µg
Cara Pembuatan Larutan Sampel
Ditimbang serbuk sampel 125,72 mg setara dengan 0,4 mg Alprazolam, lalu dimasukkan kedalam labu tentukur 50 ml, dilarutkan dan dicukupkan dengan pelarut hingga garis tanda sehingga diperoleh larutan dengan konsentrasi 8 µg/ml, dikocok ± 5 menit, kemudian disaring dengan kertas saring, ± 5 ml filtrat pertama dibuang. Dipipet 2,5 ml filtrat, dimasukkan kedalam labu tentukur 25 ml, dan dicukupkan hingga garis tanda sehingga diperoleh larutan dengan konsentrasi 0,8 µg/ml. Dikocok ± 5 menit lalu disaring dengan membran filter PTFE 0,2 µm. Diinjeksikan sebanyak 20 µl kesistem KCKT vial autosampler dan dideteksi pada panjang gelombang 254 nm dengan perbandingan fase gerak metanol-air (90:10), laju alir 1,5 ml/menit. Dilakukan sebanyak 3 kali perlakuan.
Cara Pembuatan Larutan Sampel ditambah dengan BPFI
Lalu dipipet 1 ml dimasukkan dalam labu 50 ml yang sudah berisi serbuk sampel, larutkan dan cukupkan sampai garis tanda. Kemudian dipipet 2,5 ml dimasukkan dalam labu 25 ml, larutkan dan cukupkan sampai garis tanda. Dikocok ± 5 menit lalu disaring dengan membran filter PTFE 0,2 µm. Diinjeksikan sebanyak 20 µl kesistem KCKT vial autosampler dan dideteksi pada panjang gelombang 254 nm dengan perbandingan fase gerak metanol-air (90:10), laju alir 1,5 ml/menit. Dilakukan sebanyak 3 kali perlakuan.
Konsentrasi Bahan Baku =
Konsentrasi Bahan Baku =
Pipet 1 ml ke labu 50 ml =
Serbuk sampel yang ditimbang setara 0,35 mg alprazolam =
Baku pembanding 30% :
= g = 150 µg
Cara Pembuatan Larutan Sampel
dan dicukupkan hingga garis tanda sehingga diperoleh larutan dengan konsentrasi 1 µg/ml. Dikocok ± 5 menit lalu disaring dengan membran filter PTFE 0,2 µm. Diinjeksikan sebanyak 20 µl kesistem KCKT vial autosampler dan dideteksi pada panjang gelombang 254 nm dengan perbandingan fase gerak metanol-air (90:10), laju alir 1,5 ml/menit. Dilakukan sebanyak 3 kali perlakuan.
Cara Pembuatan Larutan Sampel ditambah dengan BPFI
Ditimbang 50 mg serbuk BPFI masukkan dalam labu 50 ml, larutkan dan cukupkan sampai garis tanda, lalu pipet 7,5 ml dan masukkan ke dalam labu 50 ml. Lalu dipipet 1 ml dimasukkan dalam labu 50 ml yang sudah berisi serbuk sampel, larutkan dan cukupkan sampai garis tanda. Kemudian dipipet 2,5 ml dimasukkan dalam labu 25 ml, larutkan dan cukupkan sampai garis tanda. Dikocok ± 5 menit lalu disaring dengan membran filter PTFE 0,2 µm. Diinjeksikan sebanyak 20 µl kesistem KCKT vial autosampler dan dideteksi pada panjang gelombang 254 nm dengan perbandingan fase gerak metanol-air (90:10), laju alir 1,5 ml/menit. Dilakukan sebanyak 3 kali perlakuan.
Konsentrasi Bahan Baku = Konsentrasi Bahan Baku =
Pipet 1 ml ke labu 50 ml =
Baku pembanding 30% :
= g = 180 µg/ml
Cara Pembuatan Larutan Sampel
Ditimbang serbuk sampel 188,58 mg setara dengan 0,5 mg Alprazolam, lalu dimasukkan kedalam labu tentukur 50 ml, dilarutkan dan dicukupkan dengan pelarut hingga garis tanda sehingga diperoleh larutan dengan konsentrasi 12 µg/ml, dikocok ± 5 menit, kemudian disaring dengan kertas saring, ± 5 ml filtrat pertama dibuang. Dipipet 2,5 ml filtrat, dimasukkan kedalam labu tentukur 25 ml, dan dicukupkan hingga garis tanda sehingga diperoleh larutan dengan konsentrasi 1,2 µg/ml. Dikocok ± 5 menit lalu disaring dengan membran filter PTFE 0,2 µm. Diinjeksikan sebanyak 20 µl kesistem KCKT vial autosampler dan dideteksi pada panjang gelombang 254 nm dengan perbandingan fase gerak metanol-air (90:10), laju alir 1,5 ml/menit. Dilakukan sebanyak 3 kali perlakuan.
Cara Pembuatan Larutan Sampel ditambah dengan BPFI
Ditimbang 50 mg serbuk BPFI masukkan dalam labu 50 ml, larutkan dan cukupkan sampai garis tanda, lalu pipet 9 ml dan masukkan ke dalam labu 50 ml. Lalu dipipet 1 ml dimasukkan dalam labu 50 ml yang sudah berisi serbuk sampel, larutkan dan cukupkan sampai garis tanda. Kemudian dipipet 2,5 ml dimasukkan dalam labu 25 ml, larutkan dan cukupkan sampai garis tanda. Dikocok ± 5 menit lalu disaring dengan membran filter PTFE 0,2 µm. Diinjeksikan sebanyak 20 µl kesistem KCKT vial autosampler dan dideteksi pada panjang gelombang 254 nm dengan perbandingan fase gerak metanol-air (90:10), laju alir 1,5 ml/menit. Dilakukan sebanyak 3 kali perlakuan.
Pipet 1 ml ke labu 50 ml = = 12 µg/ml
Lampiran 5 Kromatogram Hasil Recovery dari Sampel Alprazolam
A
C
A
C
A
C
A
C
A
C
A
C
Lampiran 6 Hasil Pengujian Validasi, dengan parameter Akurasi, Presisi, Batas Deteksi (LOD), Batas Kuantitasi (LOQ) Alprazolam pada Tablet Zypraz (PT Kalbe Farma) dengan Menggunakan Metode Adisi Standar
Luas Area Konsentrasi ( µg/ml ) Recovery ( % )
Sebelum
Penambahan penambahan Sesudah penambahan Sebelum Penambahan Setelah
Lampiran 7 Contoh Perhitungan % Recovery dengan Metode Adisi Standar % Recovery =
Keterangan :
A = Konsentrasi sampel setelah penambahan analit B = Konsentrasi sampel sebelum penambahan analit
% Recovery =
Lampiran 8 Perhitungan Batas Deteksi (LOD) dan Batas Kuantitasi (LOQ) Persamaan Regresi : Y = ax + b
Y = 13203,9494x + 180,0156
No Konsentrasi
Lampiran 9 Kromatogram dari Larutan Tablet Zypraz (PT Kalbe Farma)
A
Lampiran 10 Kromatogram Spike dari Larutan Tablet Zypraz (PT Kalbe Farma)
C
E
Lampiaran 10 Kromatogram Spike dari larutan tablet Zypraz (PT Kalbe Farma)
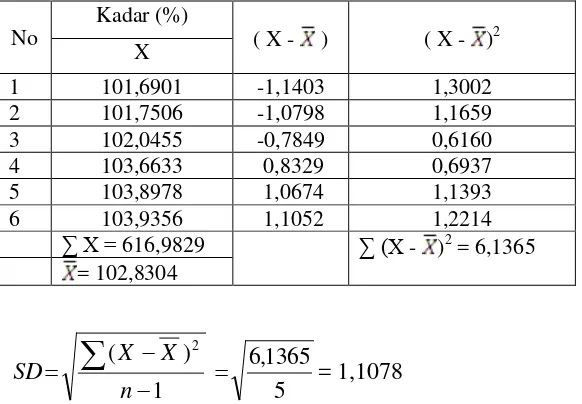
Lampiran 11 Analisis Data Statistik untuk Mencari Kadar Sebenarnya dari Penyuntikkan Larutan tablet Zypraz (PT Kalbe Farma)
No Kadar (%) ( X - ) ( X - )2
Dasar penolakan data apabila t = 4,0321
Semua data diterima
µ = X ± t(1-1/2α)dk
n SD x
= 102,8304 ± 4,0321 x 6 1078 , 1
Lampiran 12 Kromatogram dari larutan tablet Alprazolam (PT Dexa Medica)
A
C
E
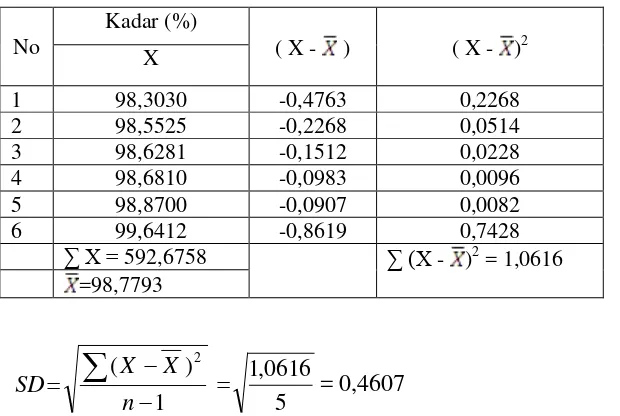
Lampiran 13 Analisis Data Statistik untuk Mencari Kadar Sebenarnya dari Penyuntikkan Larutan tablet Alprazolam (PT Dexa Medica)
No
Dasar penolakan data apabila t = 4,0321
Lampiran 14 (Lanjutan) Analisis Data Statistik Larutan tablet Alprazolam (PT Dexa medica)
Untuk itu dihitung kembali dengan cara yang sama tanpa mengikutsertakan data ke-6
Dasar penolakan data apabila t = 4,0321
Semua data diterima.
Jadi kadar sebenarnya terletak antara :
= 98,6069 ± 4,0321 x 6 2063 , 0
Lampiran 15 Kromatogram dari larutan tablet Apazol (PT Dexa Medica)
A
C
E
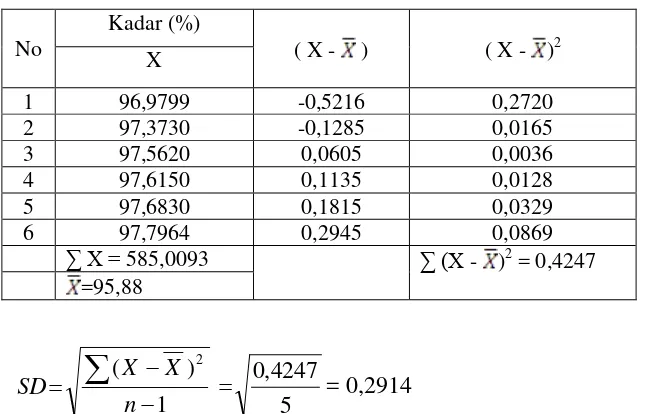
Lampiran 16 Analisis Data Statistik untuk Mencari Kadar Sebenarnya dari Penyuntikkan Larutan Apazol (PT Dexa Medica)
No
Dasar penolakan data apabila t = 4,0321
Lampiran 17 (Lanjutan) Analisis Data Statistik Larutan tablet Apazol (PT Dexa Medica)
Untuk itu dihitung kembali dengan cara yang sama tanpa mengikutsertakan data ke-1.
Dasar penolakan data apabila t = 4,0321
Semua data diterima.
µ = X ± t(1-1/2α)dk
n SD x
= 97,6058 ± 4,0321 x 6 1567 , 0
Lampiran 18 Kromatogram dari larutan tablet Alviz (PT Pharos)
A
C
E
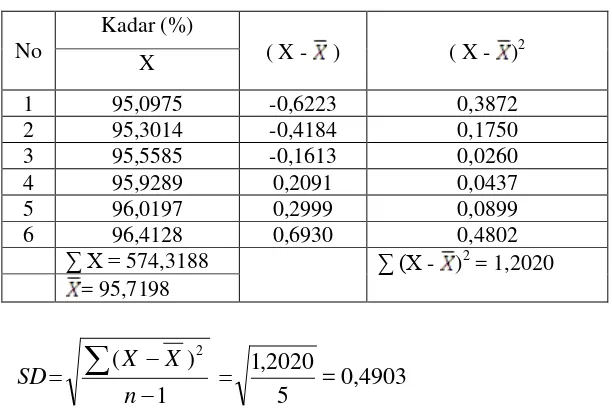
Lampiran 19 Analisis Data Statistik untuk Mencari Kadar Sebenarnya dari Penyuntikkan Larutan tablet Alviz (PT Pharos)
1
Semua data diterima.
Jadi kadar sebenarnya terletak antara :
µ = X ± t(1-1/2α)dk
n SD x
= 95,7198 ± 4,0321 x 6 4903 , 0
Lampiran 20 Kromatogram dari larutan tablet Atarax (PT Mersi)
A
C
E
Lampiran 21 Analisis Data Statistik untuk Mencari Kadar Sebenarnya dari Penyuntikkan Larutan tablet Atarax (PT Mersi)
1
Semua data diterima.
Jadi kadar sebenarnya terletak antara :
µ = X ± t(1-1/2α)dk
n SD x
= 91,0120 ± 4,0321 x 5 4516 , 0
Lampiran 22 Perhitungan Penimbangan sampel
Berat 20 tablet = 4490 mg
Kandungan Alprazolam di etiket = 0,5 mg Dibuat larutan uji dengan konsentrasi Alprazolam 1 µg/ml Ditimbang serbuk sampel setara dengan Alprazolam 0,5 mg
Berat penimbangan sampel =
=
= 224,5 mg
Sampel yang sudah ditimbang ( 224,5 mg) dimasukkan ke dalam labu tentukur 50 ml dilarutkan dan dicukupkan dengan pelarut sampai garis tanda.
Kadar larutan uji =
= 10 µg/ml
Lalu dipipet 2,5 ml dari larutan uji dimasukkan ke dalam labu tentukur 25 ml dilarutkan dan dicukupkan dengan pelarut sampai garis tanda. Sehingga didapat konsentrasi 1 µg/ml.
Konsentrasi =
Lampiran 23 Hasil Analisa Kadar Alprazolam dalam sampel
1. Hasil analisa Kadar Alprazolam dalam tablet Zypraz (PT Kalbe Farma) Berat
2. Hasil analisa Kadar Alprazolam dalam tablet Alprazolam (PT Dexa Medica) Berat
3. Hasil analisa Kadar Alprazolam dalam tablet Apazol (PT Dexa Medica) Berat
Luas Area Konsentrasi Teoritis ( µg/ml )
5. Hasil analisa Kadar Alprazolam dalam tablet Atarax (PT Mersi) Berat
Penimbangan ( mg )
Berat Setara
( mg ) Luas Area
Konsentrasi Teoritis ( µg/ml )
Konsentrasi Perolehan ( µg/ ml )
Lampiran 24 Contoh perhitungan untuk mencari kadar Aprazolam Perhitungan kadar sampel
Y = 13203,9494X + 180,0156 Luas Puncak = 13630
X =
= 1,0186 µg/ml Kadar =
Lampiran 25 Daftar Spesifikasi Sampel 1. Zypraz
Komposisi : Tiap tablet mengandung : ®
Alprazolam 0,5 mg
No Batch : 230073 Produsen : PT Kalbe Farma
No. Pendaftaran : DPL0111632810B1 Tgl. Kadaluwarsa : Oktober 2013 2. Alprazolam
Komposisi : Tiap tablet mengandung : ®
Alprazolam 0,5 mg No. Batch : 4112258
Produsen : PT Dexa Medica No. Pendaftaran : GPL0405036610B1 Tgl. Kadaluwarsa : Desember 2013 3. Apazol
Komposisi : Tiap tablet mengandung : ®
Alprazolam 0,5 mg
No. Batch : 4112259
Produsen : PT Dexa Medica No. Pendaftaran : DPL0105030010B1 Tgl. Kadaluwarsa : Desember 2013 4. Atarax
Komposisi : Tiap tablet mengandung : ®
No. Batch : 10397
Produsen : PT MersiFarma TM No. Pendaftaran : DPL0133303417A1 Tgl. Kadaluwarsa : Oktober 2014 5. Alviz
Komposisi : Tiap tablet mengandung : ®
Alprazolam 0,5 mg
No. Batch : COM5520 Produsen : PT Pharos
Lampiran 28 Gamba Alat KCKT (Hitachi)
Lampiran 29 Gambar Sonifikator (Branson 1510) dan Penyaring
Gambar 7 Sonifikator (Branson 1510)
Gambar Penyaring
Gambar 9 Sonifikator Kudos