PENETAPAN KADAR IBUPROFEN DALAM SEDIAAN
TABLET DENGAN NAMA DAGANG DAN GENERIK
SECARA KROMATOGRAFI CAIR KINERJA TINGGI
(KCKT)
SKRIPSI
OLEH: SITTI HIDAYATI
NIM 050814053
PROGRAM EKSTENSI SARJANA FARMASI FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
PENETAPAN KADAR IBUPROFEN DALAM SEDIAAN
TABLET DENGAN NAMA DAGANG DAN GENERIK
SECARA KROMATOGRAFI CAIR KINERJA TINGGI
(KCKT)
SKRIPSI
Diajukan untuk Melengkapi Salah Satu Syarat untuk Memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH :
SITTI HIDAYATI
NIM 050814053
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
LEMBAR PENGESAHAN
PENETAPAN KADAR IBUPROFEN DALAM
SEDIAAN TABLET DENGAN NAMA DAGANG DAN
GENERIK SECARA KROMATOGRAFI CAIR
KINERJA TINGGI (KCKT)
Diajukan Oleh: SITTI HIDAYATI
NIM 050814053
Medan, 18 April 2012
Disetujui Oleh: Disahkan Oleh:
Pembimbing I, Dekan,
Prof. Dr. rer. nat. Effendy De Lux Putra, SU., Apt. Prof. Dr. Sumadio Hadisahputra, Apt.
NIP 195306191983031001 NIP 195311281983031002
Pembimbing II,
KATA PENGANTAR
Puji dan syukur kehadirat Allah SWT yang telah melimpahkan nikmat,
rahmat, karunia dan ridhoNya, sehingga penulis dapat menyelesaikan skripsi yang
berjudul “Penetapan Kadar Ibuprofen Dalam Sediaan Tablet Dengan Nama
Dagang Dan Generik Secara Kromatografi Cair Kinerja Tinggi (KCKT)”. Skripsi
ini diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi
pada Fakultas Farmasi Universitas Sumatera Utara.
Pada kesempatan ini penulis mengucapkan banyak terima kasih kepada
Bapak Prof. Dr. Sumadio Hadisahputra, Apt., sebagai Dekan Fakultas Farmasi.
Bapak Prof. Dr. rer. Nat. Effendy De Lux Putra, SU., Apt. dan Bapak Drs.
Muchlisyam, MSi., Apt. selaku dosen pembimbing yang telah memberikan waktu,
bimbingan dan nasehat selama melakukan penelitian hingga selesainya
penyusunan skripsi ini.
Ucapan terima kasih yang tulus dan tiada terhingga untuk keluarga
tercinta, Ayahanda H.M. Junaidi (Alm) dan Ibunda Hj. Rosdiawati , Kakanda
Fatimah Dora (Almh) dan Suami, Kakanda M.Dini Hari dan istri, Kakanda Ridha
Aulia dan istri, Adinda Aidil Dianullah dan Harratullisan, Suami tercinta Darwin
Koto, Anak-anak tersayang Aisyah Anis Ulya dan Dziban Al-Hasan atas do’a,
perhatian, pengertian, kepercayaan dan dukungan yang diberikan baik moril
maupun materil yang tiada hentinya demi suksesnya penulis.
Penulis mengucapkan terima kasih sebesar-besarnya kepada Ibu Prof. Dr.
Siti Morin Sinaga, M.Sc., Apt., Ibu Dra. Sudarmi, M.Si., Apt., dan Ibu Dra. Tuty
Roida Pardede, M.Si., Apt., selaku dosen penguji yang telah memberikan saran
dan kritikan kepada penulis hingga selesainya penulisan skripsi ini. Penulis juga
sebagai dosen penasehat akademik penulis, beserta seluruh staf pengajar Fakultas
Farmasi USU Medan yang telah mendidik penulis dan seluruh rekan-rekan
mahasiswa Fakultas Farmasi Universitas Sumatera Utara, teristimewa buat
rekan-rekan Farmasi Ekstensi angkatan 2005 yang telah memberikan bantuan, saran, dan
semangat kepada penulis.
Penulis menyadari bahwa skripsi ini masih jauh dari kata sempurna. Untuk
itu penulis dengan kerendahan hati bersedia menerima kritikan dan saran yang
membangun dari kesempurnaan skripsi ini.
Medan, Juni 2012 Penulis,
PENETAPAN KADAR IBUPROFEN DALAM SEDIAAN
TABLET DENGAN NAMA DAGANG DAN GENERIK
SECARA KROMATOGRAFI CAIR KINERJA TINGGI
(KCKT)
ABSTRAKIbuprofen merupakan obat AINS derivat asam propionat yang diperkenalkan pertama kali di banyak negara. Obat ini bersifat analgesik dengan daya anti-inflamasi tidak terlalu kuat. Efek analgesiknya sama seperti aspirin. Efek anti-inflamasinya terlihat dengan dosis 1200-2400 mg sehari. Absorpsi ibuprofen cepat melalui lambung dan kadar maksimum dalam plasma dicapai setelah 1-2 jam. Efek samping terhadap saluran cerna lebih ringan dibandingkan dengan aspirin.
Tujuan penelitian adalah modifikasi penetapan kadar ibuprofen dalam tablet yang beredar di pasaran secara KCKT menggunakan kolom C18 (250 mm x 4,60 mm), fase gerak metanol-air, laju alir 1,0 ml/menit, dan deteksi dilakukan pada panjang gelombang 265 nm.
Berdasarkan hasil uji linieritas dari kurva kalibrasi diperoleh koefisien korelasi 0,9998 dengan persamaan regresi Y=107,4434X+68,6309. Dari hasil uji validasi metode yang digunakan memberikan hasil akurasi dan presisi yang dapat diterima dengan persen perolehan kembali Ibuprofen = 100,83% (RSD = 0,4363%). Dengan batas deteksi (LOD) = 2,9327 µg/ml. Batas kuantitasi (LOQ) = 9,7757 µg/ml.
Hasil penetapan kadar dari keenam sampel nama dagang dan generik, memenuhi persyaratan kadar yang ditetapkan Farmakope Indonesia edisi IV (1995) yaitu tidak kurang dari 90,0 % dan tidak lebih dari 110,0 % dari jumlah yang tertera pada etiket.
DETERMINATION IBUPROFEN IN THE PREPARATION OF
TABLET WITH TRADE NAME AND GENERIC WITH HIGH
PERFORMANCE LIQUID CHROMATOGRAPHY (HPLC)
ABSTRACTIbuprofen is propionate acid derivate AINS drugs. This drug is analgesic with no strong anti inflammation effects. Its analgesic effect is same to aspirin. Its anti inflammation effect is appear on dosage of 1200 – 2400 mg per day. Absorption of ibuprofen is quick through gastric and the maximum content in plasma is achieved after 1 – 2 hours. Side effects to gastric lower of aspirin.
Research target is modification the determination of ibuprofen in tablet by reversed phase with HPLC had been done, using column C18 (250 mm x 4.60 mm), methanol-water as mobile phase, flow rate 1,0 ml/minute, and detection at wafelength 265 nm.
Based on the linearity test obtained from the calibration curve correlation coefficient of 0.9998 with the regression equation Y = 107.4434 X + 68.6309. From the results of the validation test methods used give results of accuracy and precision that can be accepted with ibuprofen percent recovery = 100.83% (RSD = 0.4363%). With a limit of detection (LOD) = 2.9327 µg / ml. Limit of quantitation (LOQ) = 9,7757 µg / ml.
The results of the determination of levels of the six samples with the trade name and generic, meet the requirements specified levels of Indonesian Pharmacopoeia IV edition (1995) of not less than 90.0% and not more than 110.0% of the amount listed on the label.
PENETAPAN KADAR IBUPROFEN DALAM SEDIAAN
TABLET DENGAN NAMA DAGANG DAN GENERIK
SECARA KROMATOGRAFI CAIR KINERJA TINGGI
(KCKT)
ABSTRAKIbuprofen merupakan obat AINS derivat asam propionat yang diperkenalkan pertama kali di banyak negara. Obat ini bersifat analgesik dengan daya anti-inflamasi tidak terlalu kuat. Efek analgesiknya sama seperti aspirin. Efek anti-inflamasinya terlihat dengan dosis 1200-2400 mg sehari. Absorpsi ibuprofen cepat melalui lambung dan kadar maksimum dalam plasma dicapai setelah 1-2 jam. Efek samping terhadap saluran cerna lebih ringan dibandingkan dengan aspirin.
Tujuan penelitian adalah modifikasi penetapan kadar ibuprofen dalam tablet yang beredar di pasaran secara KCKT menggunakan kolom C18 (250 mm x 4,60 mm), fase gerak metanol-air, laju alir 1,0 ml/menit, dan deteksi dilakukan pada panjang gelombang 265 nm.
Berdasarkan hasil uji linieritas dari kurva kalibrasi diperoleh koefisien korelasi 0,9998 dengan persamaan regresi Y=107,4434X+68,6309. Dari hasil uji validasi metode yang digunakan memberikan hasil akurasi dan presisi yang dapat diterima dengan persen perolehan kembali Ibuprofen = 100,83% (RSD = 0,4363%). Dengan batas deteksi (LOD) = 2,9327 µg/ml. Batas kuantitasi (LOQ) = 9,7757 µg/ml.
Hasil penetapan kadar dari keenam sampel nama dagang dan generik, memenuhi persyaratan kadar yang ditetapkan Farmakope Indonesia edisi IV (1995) yaitu tidak kurang dari 90,0 % dan tidak lebih dari 110,0 % dari jumlah yang tertera pada etiket.
DETERMINATION IBUPROFEN IN THE PREPARATION OF
TABLET WITH TRADE NAME AND GENERIC WITH HIGH
PERFORMANCE LIQUID CHROMATOGRAPHY (HPLC)
ABSTRACTIbuprofen is propionate acid derivate AINS drugs. This drug is analgesic with no strong anti inflammation effects. Its analgesic effect is same to aspirin. Its anti inflammation effect is appear on dosage of 1200 – 2400 mg per day. Absorption of ibuprofen is quick through gastric and the maximum content in plasma is achieved after 1 – 2 hours. Side effects to gastric lower of aspirin.
Research target is modification the determination of ibuprofen in tablet by reversed phase with HPLC had been done, using column C18 (250 mm x 4.60 mm), methanol-water as mobile phase, flow rate 1,0 ml/minute, and detection at wafelength 265 nm.
Based on the linearity test obtained from the calibration curve correlation coefficient of 0.9998 with the regression equation Y = 107.4434 X + 68.6309. From the results of the validation test methods used give results of accuracy and precision that can be accepted with ibuprofen percent recovery = 100.83% (RSD = 0.4363%). With a limit of detection (LOD) = 2.9327 µg / ml. Limit of quantitation (LOQ) = 9,7757 µg / ml.
The results of the determination of levels of the six samples with the trade name and generic, meet the requirements specified levels of Indonesian Pharmacopoeia IV edition (1995) of not less than 90.0% and not more than 110.0% of the amount listed on the label.
BAB I
PENDAHULUAN
1.1Latar Belakang
Obat analgesik antipiretik serta obat anti-inflamasi non steroid atau
nonsteroidal anti-inflammatory drug (NSAID) merupakan salah satu kelompok
obat yang banyak diresepkan dan juga digunakan tanpa resep dokter.
Ibuprofen merupakan obat NSAID derivat asam propionat yang
diperkenalkan pertama kali di banyak negara. Obat ini bersifat analgesik dengan
daya anti-inflamasi tidak terlalu kuat. Efek analgesiknya sama seperti aspirin.
Efek anti-inflamasinya terlihat dengan dosis 1200-2400 mg sehari. Absorpsi
ibuprofen cepat melalui lambung dan kadar maksimum dalam plasma dicapai
setelah 1-2 jam. Efek samping terhadap saluran cerna lebih ringan dibandingkan
dengan aspirin (Wilmana dan Sulistia, 1995).
Dalam perdagangan sediaan tablet ibuprofen dijumpai dengan nama
dagang dan nama generik. Obat generik harganya jauh lebih murah daripada obat
dengan nama dagang. Sementara masyarakat cenderung menilai bahwa kualitas
obat identik dengan harganya, dengan anggapan obat yang lebih mahal, mutunya
lebih baik daripada obat yang murah harganya (Depkes, 1989).
Ibuprofen dapat ditentukan kadarnya dengan Kromatografi Cair Kinerja
Tinggi (KCKT), Spektrofotometri UV dan Alkalimetri.
dalam sediaan tablet dilakukan secara Kromatografi Cair Kinerja Tinggi (KCKT)
menggunakan fase gerak larutan 4,0 g asam kloroasetat P dalam 400 ml air, atur
hingga pH 3,0 dengan amonium hidroksida P, tambahkan 600 ml asetonitril P,
saring dan awaudarakan. KCKT dilengkapi dengan detektor 254 nm dan kolom
4,6 mm x 25 cm berisi bahan pengisi L1. Laju aliran lebih kurang 2,0 ml per
menit (Ditjen POM, 1995).
Menurut Battu dan Reddy (2009), penentuan kadar ibuprofen dalam
sediaan tablet di lakukan secara KCKT menggunakan fase gerak Asetonitril :
Buffer fosfat dengan perbandingan 60:40 dan pH diatur hingga 7,0. Menggunakan
detector UV pada panjang gelombang 260 nm dan kolom oktadesilsilan (C18, 5µ,
150 mm x 4,6 mm). Laju aliran 0,8 ml/menit. Berdasarkan hasil uji linieritas dari
kurva kalibrasi yang dibuat sebanyak 6 konsentrasi yaitu 20, 40, 60, 80, 100 dan
120 µg/ml diperoleh koefisien korelasi 0,998 dengan persamaan regresi
Y=0,0061X+0,002. Batas Deteksi (LOD) 10 µg/ml dan Batas Kuantitasi (LOQ)
25 µg/ml. Dari hasil uji validasi metode memberikan hasil akurasi dan presisi
dengan persen perolehan kembali Ibuprofen = 96,01% (RSD = 0,580%).
Ibuprofen sangat mudah larut dalam metanol, aseton dan kloroform.
Praktis tidak larut dalam air. Berdasarkan kelarutan dalam metanol, maka
dilakukan modifikasi penentuan kadar ibuprofen secara KCKT dengan fase gerak
metanol-air.
Alasan memilih metode KCKT karena metode ini mampu memisahkan
molekul-molekul dari suatu campuran, resolusinya baik, mudah
bermacam-macam detektor, kolom dapat digunakan kembali, waktu analisis
umumnya singkat, ideal untuk molekul besar dan kecil dan mudah memperoleh
kembali cuplikan (De Lux Putra, 2007).
Berdasarkan hal tersebut di atas, peneliti melakukan modifikasi penetapan
kadar ibuprofen tablet menggunakan KCKT dengan kolom Luna 5µ m C18 (250 x
4,60 mm), dengan berbagai perbandingan fase gerak metanol – air dan laju alir 1
ml/menit.
1.2 Perumusan Masalah
1. Berapakah perbandingan metanol-air yang tepat untuk fase gerak pada
penetapan kadar Ibuprofen baku secara KCKT?
2. Apakah metode KCKT dengan fase gerak metanol - air dapat diterapkan
pada penetapan kadar ibuprofen dalam sediaan tablet dan memberikan uji
validasi metode yang memenuhi syarat?
3. Apakah ibuprofen dalam sediaan tablet dengan nama dagang dan generik
memenuhi persyaratan kadar yang ditetapkan Farmakope Indonesia edisi
IV (1995)?
1.3 Hipotesis
1. Metanol-air yang tepat untuk fase gerak pada penetapan kadar ibuprofen
baku secara KCKT dalam perbandingan tertentu dapat ditentukan.
2. Metode KCKT dengan fase gerak metanol – air dapat diterapkan pada
penetapan kadar ibuprofen dalam sediaan tablet dan memberikan uji
3. Kadar ibuprofen dalam sediaan tablet dengan nama dagang dan generik
memenuhi persyaratan kadar yang ditetapkan Farmakope Indonesia edisi
IV (1995).
1.4 Tujuan Penelitian
1. Mengetahui perbandingan metanol-air yang tepat untuk fase gerak pada
penetapan kadar Ibuprofen baku secara KCKT.
2. Menerapkan metode KCKT pada penetapan kadar ibuprofen dalam
sediaan tablet dengan fase gerak metanol - air dan melakukan uji validasi
dari metode tersebut.
3. Mengetahui kesesuaian kadar tablet ibuprofen dengan nama dagang dan
generik dengan persyaratan kadar menurut Farmakope Indonesia edisi IV
(1995).
1.5 Manfaat Penelitian
Sebagai metode analisa kuantitatif baru bagi industri farmasi pada
BAB II
TINJAUAN PUSTAKA
2.1 Ibuprofen
2.1.1 Sifat Fisikokimia
Menurut Ditjen POM (1995), sifat fisikokimia dari Ibuprofen adalah
sebagai berikut :
Rumus Struktur :
Gambar 1. Struktur Ibuprofen
Nama Kimia : asam 2-(4-isobutil-fenil)-propionat
Rumus Molekul : C13H18O2
Berat Molekul : 206,28
Pemerian : Serbuk hablur, putih hingga hamper putih, berbau khas
lemah.
Kelarutan : Praktis tidak larut dalam air; Sangat mudah larut dalam
etanol, dalam metanol, dalam aseton dan dalam kloroform;
Sukar larut dalam etil asetat.
2.2Kromatografi
Kromatografi merupakan suatu proses pemisahan yang mana analit-analit
dalam sampel terdistribusi antara 2 fase, yaitu fase diam dan fase gerak. Fase
dalam bentuk cairan yang dilapiskan pada pendukung padat atau dilapiskan pada
dinding kolom. Fase gerak dapat berupa gas atau cairan. Jika gas digunakan
sebagai fase gerak, maka prosesnya dikenal sebagai kromatografi gas. Dalam
kromatografi cair dan kromatografi lapis tipis, fase gerak yang digunakan selalu
cair (Rohman, 2009).
2.2.1 Pemakaian Kromatografi
1. Pemakaian untuk tujuan kualitatif mengungkapkan ada atau tidak adanya
senyawa tertentu dalam cuplikan
2. Pemakaian untuk tujuan kuantitatif menunjukkan banyaknya masing-masing
komponen campuran.
3. Pemakaian untuk tujuan preparatif untuk memperoleh komponen campuran
dalam jumlah memadai dalam keadaan murni (Gritter, dkk., 1991).
2.2.2 Analisa Kualitatif dan Kuantitatif
a. Analisis Kualitatif
Ada 3 pendekatan untuk analisa kualitatif yakni:
1. Perbandingan antara retensi solut yang tidak diketahui dengan data retensi
baku yang sesuai (senyawa yang diketahui) pada kondisi yang sama.
2. Dengan cara spiking.
Untuk kromatografi yang melibatkan kolom, spiking dilakukan dengan
menambah sampel yang mengandung senyawa tertentu yang akan diselidiki
dengan senyawa baku pada kondisi kromatografi yang sama. Hal ini dilakukan
dengan cara: pertama, dilakukan proses kromatografi sampel yang tidak di
spiking. Kedua, sampel yang telah di-spiking dengan senyawa baku dilakukan
senyawa yang diselidiki terjadi peningkatan tinggi puncak/luas puncak setelah
di-spiking dibandingkan dengan tinggi puncak/luas puncak yang tidak
dilakukan spiking maka dapat diidentifikasi bahwa sampel mengandung
senyawa yang kita selidiki.
3. Menggabungkan alat kromatografi dengan spektrometer massa.
Pada pemisahan dengan menggunakan kolom kromatografi, cara ini akan
memberikan informasi data spektra massa solut dengan waktu retensi tertentu.
Spektra solut yang tidak diketahui dapat dibandingkan dengan spektra yang
ada di data base komputer yang diinterpretasi sendiri. Cara ini dapat dilakukan
untuk solut yang belum ada baku murninya (Rohman, 2009)
b. Analisis Kuantitatif
Untuk menjamin kondisi yang digunakan dalam analisis kuantitatif stabil
dan reprodusibel, baik pada penyiapan sampel atau proses kromatografi, berikut
beberapa syarat yang harus dipenuhi dalam analisis kuantitatif:
1. Analit (solut) harus telah diketahui dan terpisah sempurna dari
komponen-komponen lain dalam kromatogram
2. Baku dengan kemurnian yang tinggi dan telah diketahui harus tersedia
3. Prosedur kalibrasi yang sudah diketahui harus digunakan (Rohman, 2009)
Menurut Jhonson dan Stevenson (1991), untuk kromatografi yang
melibatkan kolom, kuantifikasi dapat dilakukan dengan luas puncak atau
tinggipuncak. Tinggi puncak atau luas puncak berbanding langsung dengan
banyaknya solut yang dikromatografi, jika dilakukan pada kisaran detektor yang
linier
Metode yang paling sederhana untuk pengukuran kuantitatif adalah
dengan tinggi puncak. Tinggi puncak diukur sebagai jarak dari garis dasar ke
puncak maksimum seperti puncak 1, 2, dan 3 pada Gambar 2 . Presisinya lebih
baik daripada mengukur luas puncak, terutama pada puncak-puncak yang sempit.
Namun tinggi puncak sangat sensitif terhadap perubahan-perubahan kecil dalam
cara penginjeksian dan dalam kondisi-kondisi operasi.
Gambar 2. Pengukuran tinggi puncak
Metode tinggi puncak hanya digunakan jika perubahan tinggi puncak
linier dengan konsentrasi analit. Kesalahan akan terjadi jika metode ini digunakan
pada puncak yang mengalami penyimpangan (asimetris) atau jika kolom
mengalami kelebihan muatan.
2. Metode luas puncak
Suatu teknik untuk mengukur luas puncak adalah dengan mengukur luas
puncak sebagai hasil kali tinggi puncak dan lebar pada setengah tinggi (L=
HW1/2). Cara kerjanya cepat dan sederhana yaitu dengan membuat garis dasar
puncak, tentukan setengah-tinggi, lalu ukur tinggi dan lebar pada setengah-tinggi.
Pengukuran luas puncak dapat dilihat pada Gambar 3 berikut ini:
Gambar 3. Pengukuran Luas Puncak
Baik tinggi puncak maupun luasnya dapat dihubungkan dengan
konsentrasi. Tinggi puncak mudah diukur, akan tetapi sangat dipengaruhi
perubahan waktu retensi yang disebabkan oleh variasi suhu dan komposisi
pelarut. Oleh karena itu, luas puncak dianggap merupakan parameter yang lebih
akurat untuk pengukuran kuantitatif (Ditjen POM, 1995).
2.3 Kromatografi Cair Kinerja Tinggi (KCKT)
Kromatografi Cair Kinerja Tinggi (KCKT) merupakan sistem pemisahan
dengan kecepatan dan efisiensi yang tinggi karena didukung oleh kemajuan dalam
teknologi kolom, sistem pompa tekanan tinggi, dan detektor yang sangat sensitif
dan beragam sehingga mampu menganalisis berbagai cuplikan secara kualitatif
maupun kuantitatif, baik dalam komponen tunggal maupun campuran (Ditjen
POM, 1995).
Saat ini, KCKT merupakan teknik pemisahan yang diterima secara luas
untuk analisis dan pemurnian senyawa tertentu dalam suatu sampel pada sejumlah
bidang, antara lain : farmasi, lingkungan, bioteknologi, polimer, dan
industri-industri makanan. KCKT biasanya dilakukan pada suhu kamar. Jadi, untuk zat –
zat yang labil pada pemanasan atau tidak menguap merupakan pilihan yang logis
(Gandjar dan Rohman, 2007).
2.4 Jenis Pemisahan Kromatografi Cair Kinerja Tinggi
Berdasarkan jenis fase gerak dan fase diamnya, jenis pemisahan KCKT
dibedakan atas :
Kromatografi dengan kolom yang fase diamnya bersifat polar, misalnya silika
gel, alumina, sedangkan fase geraknya bersifat non polar seperti heksan.
b. Kromatografi Fase Terbalik
Pada kromatografi fase terbalik, fase diamnya bersifat non polar, yang banyak
dipakai adalah oktadesilsilan (ODS atau C18) dan oktilsilan (C8). Sedangkan
fase geraknya bersifat polar, seperti air, metanol dan asetonitril (Mulja dan
Suharman, 1995).
2.5 Cara Kerja KCKT
Kromatografi merupakan teknik yang mana solut atau zat-zat terlarut
terpisah oleh perbedaan kecepatan elusi, dikarenakan solut-solut ini melewati
suatu kolom kromatografi. Pemisahan solut-solut ini diatur oleh distribusi dalam
fase gerak dan fase diam. Penggunaan kromatografi cair membutuhkan
penggabungan secara tepat dari berbagai macam kondisi operasional seperti jenis
kolom, fase gerak, panjang dan diameter kolom, kecepatan alir fase gerak, suhu
kolom, dan ukuran sampel (Rohman, 2009).
2.5.1 Komponen KCKT
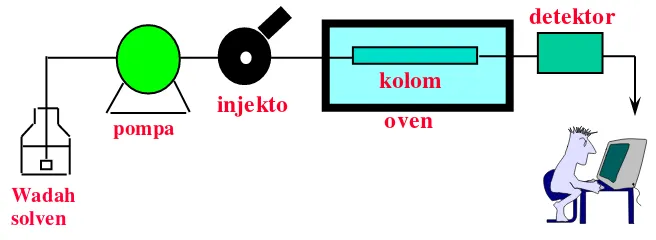
Gambar 4. Bagan alat KCKT
2.5.2 Wadah Fase Gerak pompa
injekto
kolom
oven
detektor
Wadah solven
Wadah fase gerak harus bersih dan lembam (inert). Wadah pelarut kosong
ataupun labu laboratorium dapat digunakan sebagai wadah fase gerak. Wadah ini
biasanya dapat menampung fase gerak antara 1 sampai 2 liter pelarut. Fase gerak
sebelum digunakan harus dilakukan degassing (penghilangan gas) yang ada pada
fase gerak, sebab adanya gas akan berkumpul dengan komponen lain terutama
dipompa dan detektor sehingga akan mengacaukan analisis (Rohman, 2009).
2.5.3 Pompa
Pompa yang cocok digunakan untuk KCKT adalah pompa yang
mempunyai syarat sebagaimana syarat wadah pelarut yakni : pompa harus inert
terhadap fase gerak. Bahan yang umum dipakai untuk pompa adalah gelas, baja
tahan karat, teflon, dan batu nilam. Pompa yang digunakan sebaiknya mampu
memberikan tekanan sampai 5000 psi dan mampu mengalirkan fase gerak
dengankecepatan alir 3 ml/menit. Untuk tujuan preparatif, pompa yang digunakan
harus mampu mengalirkan fase gerak dengan kecepatan 20 ml/ menit (Rohman,
2009).
2.5.4 Injektor
Menurut Meyer (2004), ada 3 jenis injektor, yakni syringe injector, loop
valve dan automatic injector (autosampler). Syringe injector merupakan bentuk
injektor yang paling sederhana.
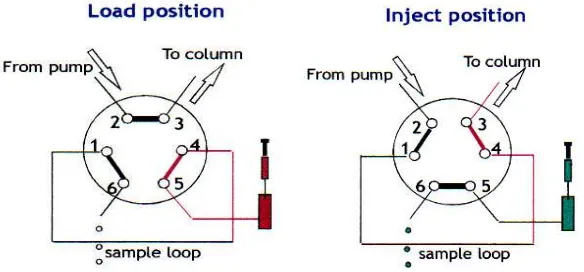
Katup putaran (loop valve) ditunjukkan secara skematik dalam Gambar 5,
tipe injektor ini umumnya digunakan untuk menginjeksi volume lebih besar
daripada 10 µl dan sekarang digunakan dengan cara otomatis (dengan adaptor
khusus, volume-volume lebih kecil dapat diinjeksikan secara manual). Pada posisi
katup difungsikan, maka cuplikan di dalam putaran akan bergerak ke dalam
kolom.
Gambar 5. Tipe injektor katup putaran
Automatic injector atau disebut juga autosampler memiliki prinsip yang
mirip, hanya saja sistem penyuntikannya bekerja secara otomatis (Meyer, 2004).
2.5.6 Kolom
Kolom merupakan jantung kromatografi. Keberhasilan atau kegagalan
analisis bergantung pada pemilihan kolom dan kondisi kerja yang tepat. Kolom
dapat dibagi menjadi dua kelompok :
a. Kolom analitik : garis tengah dalam 2 – 6 nm. Panjang bergantung pada
jenis kemasan,untuk kemasan pelikel biasanya panjang kolom 50 – 100
cm. Untuk kemasan mikropartikel berpori, biasanya 10 – 30 cm;
b. Kolom preparatif : umumnya bergaris tengah 6 mm atau lebih besar dan
panjang kolom 25 – 100 cm.
Kolom umumnya dibuat dari stainless steel dan biasanya dioperasikan pada
temperatur kamar, tetapi bisa juga digunakan temperatur lebih tinggi, terutama
untuk kromatografi penukar ion dan kromatografi eksklusi. Kemasan kolom
tergantung pada mode KCKT yang digunakan (Johnson dan Stevenson, 1991).
Suatu detektor dibutuhkan untuk mendeteksi adanya komponen cuplikan
dalam aliran yang keluar dari kolom. Detektor-detektor yang baik memiliki
sensitifitas yang tinggi, gangguan (noise) yang rendah, kisar respons linier yang
luas, dan memberi tanggapan/respon untuk semua tipe senyawa. Suatu kepekaan
yang rendah terhadap aliran dan fluktuasi temperatur sangat diinginkan, tetapi
tidak selalu dapat diperoleh.
Detektor yang paling banyak digunakan dalam kromatografi cair modern
kecepatan tinggi adalah detektor spektrofotometer UV 254 nm.
Bermacam-macam detektor dengan variasi panjang gelombang UV-Vis sekarang menjadi
populer karena mereka dapat digunakan untuk mendeteksi senyawa-senyawa
dalam rentang yang luas. Detektor indeks refraksi juga secara luas digunakan,
terutama dalam kromatografi eksklusi, tetapi umumnya kurang sensitif dari pada
detektor spektrofotometer UV. Detektor lainnya, antara lain: detektor fluometer,
detektor ionisasi nyala, detektor elektrokimia dan lain-lain juga telah digunakan
(Gandjar dan Rohman, 2007).
2.5.8 Pengolahan Data
Komponen yang terelusi mengalir ke detektor dan dicatat sebagai
puncak-puncak yang secara keseluruhan disebut sebagai kromatogram. Alat pengumpul
data seperti komputer, integrator dan rekorder dihubungkan ke detektor. Alat ini
akan mengukur sinyal elektronik yang dihasilkan oleh detektor dan
memplotkannya sebagai suatu kromatogram yang selanjutnya dapat dievaluasi
oleh seorang analis (Gandjar dan Rohman, 2007).
Validasi adalah suatu tindakan terhadap parameter tertentu pada prosedur
penetapan yang dipakai untuk membuktikan bahwa parameter tersebut memenuhi
persyaratan untuk penggunaannya (WHO, 1992).
Menurut United States Pharmacopeia (2007), validasi metode dilakukan
untuk menjamin bahwa metode analisis akurat, spesifik, reprodusibel dan tahan
pada kisaran analit yang akan dianalisis. Suatu metode analis harus divalidasi
untuk verifikasi bahwa parameter-parameter kinerjanya cukup mampu untuk
mengatasi masalah dalam analisis. Parameter analisis yang ditentukan pada
validasi adalah akurasi, presisi, batas deteksi, batas kuantitasi, spesifisitas,
linieritas dan rentang, kekasaran (Ruggedness) dan ketahanan (Robutness).
Akurasi/kecermatan adalah kedekatan antara nilai hasil uji yang diperoleh
lewat metode analitik dengan nilai sebenarnya. Akurasi dinyatakan dalam persen
perolehan kembali (%recovery). Akurasi dapat ditentukan dengan dua metode,
yakni spiked-placebo recovery dan standard addition method (Harmita, 2004).
Presisi merupakan ukuran kedekatan antar serangkaian hasil analisis yang
diperoleh dari beberapa kali pengukuran pada sampel homogen yang sama.
Biasanya diekspresikan sebagai relatif standar deviasi (RSD) dari sejumlah
sampel yang berbeda secara signifikan secara statistik (Gandjar dan Rohman,
2007).
Batas deteksi (Limit Of Detection, LOD) didefinisikan sebagai konsentrasi
analit terendah dalam sampel yang masih dapat dideteksi, meskipun tidak selalu
dapat dikuantifikasi (Gandjar dan Rohman, 2007).
Batas kuantitasi (Limit Of Quantitation, LOQ) didefinisikan sebagai
dan akurasi yang dapat diterima pada kondisi operasional metode yang digunakan
BAB III
METODE PENELITIAN
3.1 Waktu dan Tempat Penelitian
Penelitian dilakukan di Laboratorium Penelitian Fakultas Farmasi
Universitas Sumatera Utara pada bulan April sampai Juli 2011.
3.2 Alat-alat
Alat-alat yang digunakan dalam penelitian ini adalah satu unit alat KCKT
lengkap (Hitachi) dengan pompa (L-2130), degasser (DGU 20 AS), injektor
Autosampler L-2200, kolom Luna 5µm C18 (250 mm x 4,60 mm), detektor
UV-Vis L-2420, wadah fase gerak, vial khusus Autosampler, Sonifikator (Branson
1510), pompa vakum (Gast DOA - P604 – BN), neraca analitik (Mettler Toledo),
membran filter Poli Tetra Fluoro Etilen (PTFE) 0,5 µm dan 0,2, cellulose nitrat
membran filter 0,45 µ m.
3.3 Bahan-bahan
Bahan-bahan yang digunakan dalam penelitian yaitu metanol HPLC
Solvent (Merck), aquabidestilata (PT. Ikapharmindo Putramas), Ibuprofen baku
pabrik (PT. Kimia Farma), Tablet generik Ibuprofen 200 mg (PT. Aditama Raya
Farmindo), Ibuprofen 200 mg (PT. Phapros), Tablet proris 200 mg (PT. Pharos),
Tablet generik Ibuprofen 400 mg (PT. Indofarma), Ibuprofen 400 mg (PT. Phyto
3.4 Pengambilan Sampel
Pengambilan sampel secara purposif yaitu tanpa membandingkan antara
satu tempat dengan tempat yang lain, karena tempat pengambilan sampel
dianggap homogen. Sampel yang digunakan adalah tablet generik Ibuprofen 200
mg (PT. Aditama Raya Farmindo), Ibuprofen 200 mg (PT. Phapros), Tablet proris
200 mg (PT. Pharos), Tablet generik Ibuprofen 400 mg (PT. Indofarma),
Ibuprofen 400 mg (PT. Phyto Kemo Agung Farma), Tablet Ostarin 400 mg (PT.
Otto).
3.5 Prosedur Penelitian
3.5.1 Penyiapan Bahan
3.5.1.1 Pembuatan Fase Gerak Metanol – Air
Metanol 500 ml disaring dengan menggunakan membran filter PTFE 0,5
µm dan diawaudarakan selama 20 menit.
Akuabidestilata 500 ml disaring dengan menggunakan cellulose nitrat membran
filter 0,45 µ m dan diawaudarakan selama 20 menit.
3.5.1.2 Pembuatan Pelarut
Metanol disaring dengan menggunakan membran filter PTFE 0,5 µm dan
diawaudarakan selama 20 menit.
Campuran metanol-air dengan perbandingan 40:60, lalu disaring dengan
3.5.1.3 Pembuatan Larutan Induk Baku Ibuprofen Baku Pabrik (PT. Kimia
Farma)
Sejumlah 50 mg Baku Ibuprofen ditimbang seksama, dimasukkan kedalam
labu tentukur 50 ml, ditambah pelarut aduk hingga homogen,lalu dicukupkan
sampai garis tanda, maka diperoleh larutan dengan konsentrasi 1000 mcg/ml
(LIB).
3.5.2 Prosedur Analisis
3.5.2.1 Penyiapan Alat Kromatografi Cair Kinerja Tinggi
Masing-masing unit diatur, kolom yang digunakan Luna 5 µ m C18 (250 x
4,60 mm), detektor UV/Vis, dengan laju alir 1 ml/menit, dideteksi pada panjang
gelombang 265 nm.
Setelah alat KCKT dihidupkan, maka pompa dijalankan dan fase gerak
dibiarkan mengalir selama 60 menit sampai diperoleh garis alas yang datar,
menandakan sistem tersebut telah stabil.
3.5.2.2 Penentuan Perbandingan Fase Gerak
Dipipet 0,2 ml Larutan Induk Baku Ibuprofen dan masukkan dalam labu
tentukur 10 ml, dicukupkan dengan pelarut hingga garis tanda, kocok sehingga
diperoleh larutan Ibuprofen dengan konsentrasi 20 mcg/ml, disaring dengan
membran filter PTFE 0,2 µl dan diawaudarakan selama 20 menit, kemudian
diinjeksikan ke dalam sistem KCKT menggunakan vial autosampler sebanyak 10
dan (60:40), laju alir 1 ml/menit dan dideteksi pada panjang gelombang 265 nm.
Kemudian dipilih perbandingan fase gerak yang memberikan data yang terbaik.
3.5.2.3 Analisis Kualitatif Ibuprofen Menggunakan KCKT
3.5.23.1 Menentukan Waktu Tambat Ibuprofen Baku Pabrik (PT. Kimia
Farma)
Larutan Induk Baku Ibuprofen dipipet 0,2 ml masukkan dalam labu 10 ml,
dikocok dengan pelarut hingga homogen dan dicukupkan sampai garis tanda.
Maka diperoleh larutan Ibuprofen dengan konsentrasi 20 mcg/ml.
Larutan disaring dengan membran filter PTFE 0,2 µl dan diawaudarakan
selama 20 menit, diinjeksikan ke dalam sistem KCKT menggunakan vial
autosampler sebanyak 10 µl menggunakan perbandingan fase gerak dan laju alir
yang memberikan pemisahan yang terbaik, kemudian dicatat masing-masing
waktu tambatnya.
3.5.2.3.2 Identifikasi Sampel
Larutan sampel Ibuprofen sediaan tablet dengan konsentrasi 60 mcg/ml,
disuntikkan kesistem KCKT menggunakan vial autosampler sebanyak 10 µl pada
kondisi kromatogafi yang sama dengan baku. Kemudian waktu tambat
masing-masing tablet dibandingkan dengan waktu tambat Ibuprofen baku. Apabila waktu
tambat sampel hampir sama dengan waktu tambat Baku, maka sampel tablet
3.5.2.4 Analisis Kuantitatif Ibuprofen Menggunakan KCKT
3.5.2.4.1 Pembuatan Kurva Kalibrasi Ibuprofen Baku
Larutan Induk Baku Ibuprofen dipipet sebanyak 0,4 ml, 0,6 ml, 0,8 ml,
1 ml dan 1,2 ml, dimasukkan dalam labu tentukur 10 ml, diencerkan dengan fase
gerak, kocok hingga homogen dan dicukupkan sampai garis tanda. Maka
diperoleh konsentrasi 40 mcg/ml, 60 mcg/ml, 80 mcg/ml, 100 mcg/ml, dan 120
mcg/ml. Kemudian masing-masing larutan disaring dengan membran filter PTFE
0,2 µm dan diawaudarakan selama 20 menit, diinjeksikan kesistem KCKT
menggunakan vial autosampler sebanyak 10 µl pada kondisi kromatogafi yang
sama dengan Baku, dengan laju alir 1 ml/menit dan dideteksi pada panjang
gelombang 265 nm. Selanjutnya dari luas area yang diperoleh dibuat kurva
kalibrasi, dihitung persamaan regresi dan faktor korelasinya.
3.5.2.4.2 Penetapan Kadar Sampel
Ditimbang 20 tablet yang mengandung Ibuprofen kemudian digerus,
ditimbang sejumlah serbuk tablet setara dengan 50 mg Ibuprofen (sebanyak 6 kali
perlakuan), (perhitungan penimbangan sampel ada pada Lampiran 28 Hal. 89).
Masing-masing dimasukkan kedalam labu tentukur 50 ml, dilarutkan dengan
pelarut sampai garis tanda. Maka diperoleh larutan dengan konsentrasi 1000
mcg/ml, kemudian saring dengan kertas saring, 10% filtrat pertama dibuang. Dari
keenam larutan masing-masing dipipet 0,6 ml dimasukkan kedalam labu tentukur
10 ml, diencerkan dengan pelarut sampai garis tanda. Maka diperoleh larutan
dengan konsentrasi 60 mcg/ml Ibuprofen. Masing-masing larutan tersebut
kemudian diinjeksikan ke sistem KCKT menggunakan vial autosampler sebanyak
10 µl. dideteksi pada panjang gelombang 265 nm dengan laju aliran 1 ml/menit
dan dihitung kadarnya.
Kadar dapat dihitung dengan mensubtitusikan luas area sampel pada Y
dari persamaan regresi : Y = aX + b.
3.5.3 Penentuan Uji Validasi
3.5.3.1 Uji Akurasi
Uji akurasi dengan parameter persen perolehan kembali (% Recovery)
dilakukan secara Standard Addition Method dengan membuat konsentrasi analit
Ibuprofen 60 mcg/ml dan baku pembanding 20 mcg/ml, perlakuan sama dengan
perlakuan sampel.
Menurut WHO (1992) persen perolehan kembali dapat dihitung dengan
rumus:
% Perolehan kembali x100% C
B A−
=
Keterangan :
A = Konsentrasi sampel yang diperoleh setelah penambahan bahan baku
B = Konsentrasi sampel sebelum penambahan bahan baku
C = Konsentrasi baku yang ditambahkan
3.5.3.2 Uji Presisi
Menurut Rohman (2007), uji presisi ditentukan dengan parameter Relatif
Standar Deviasi (RSD) dengan rumus:
x100%
X SD
Keterangan:
RSD = Standar Deviasi Relatif (%)
SD = Standar deviasi
X = Kadar rata-rata sampel
3.5.3.3 Penentuan Batas Deteksi (LOD) dan Batas Kuantitasi (LOQ)
Menurut WHO (1992), untuk menentukan batas deteksi (LOD) dan batas
kuantitasi (LOQ) digunakan rumus:
2 ) ( 2 − − = n Yi Y SB Slope SB x
LOD=3
Slope
SB x
LOQ=10
Keterangan:
SB = Simpangan baku
LOD = Batas Deteksi
LOQ = Batas Kuantitasi
3.5.3.4 Analisis Data Secara Statistik
Untuk menghitung Standar Deviasi (SD) digunakan rumus:
1 ) ( − − =
∑
n X X SD Keterangan:SD = Standar deviasi
X = Kadar rata-rata sampel
n = Jumlah perlakuan
Kadar dapat dihitung dengan persamaan garis regresi dan untuk
menentukan data diterima atau ditolak digunakan rumus:
t hitung
n SD
X X
/ − =
Dengan dasar penolakan apabila t hitung ≥ t tabel
Untuk mencari kadar sebenarnya dengan α = 0,01, dk = n - 1, dapat digunakan
rumus:
n
SD x t
X (1 1/2α)dk
µ
= ± −Keterangan:
μ = Kadar sebenarnya X = Kadar sampel
n = Jumlah perlakuan
t = Suatu harga tergantung pada derajad kebebasan dan tingkat
kepercayaan
dk = Derajat kebebasan
BAB IV
HASIL DAN PEMBAHASAN
4.1 Penentuan Kondisi Kromatografi untuk Mendapatkan Hasil Analisis yang Optimum
4.1.1 Penentuan Perbandingan Fase Gerak
Pada awal penentuan perbandingan fase gerak di lakukan dengan cara
menyuntikkan larutan 20 mcg/ml Ibuprofen kedalam sistem KCKT dengan variasi
perbandingan fase gerak Metanol - Air (40:60), (50:50) dan (60:40), dideteksi
pada panjang gelombang 265 nm, dengan laju alir 1 ml/menit. Adapun parameter
yang perlu diperhatikan yaitu theoretical plate, tailing factor, resolusi dan waktu
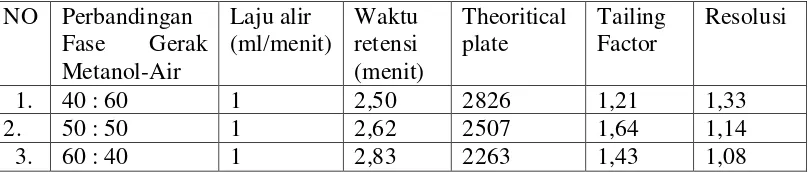
[image:33.595.112.517.429.516.2]retensi. Hasil orientasi dapat dilihat pada Tabel 1 dan Lampiran 4 Hal. 23.
Tabel 1. Hasil optimasi perbandingan fase gerak Metanol-Air
NO Perbandingan Fase Gerak Metanol-Air
Laju alir (ml/menit)
Waktu retensi (menit)
Theoritical plate
Tailing Factor
Resolusi
1. 40 : 60 1 2,50 2826 1,21 1,33
2. 50 : 50 1 2,62 2507 1,64 1,14
3. 60 : 40 1 2,83 2263 1,43 1,08
Dari tabel diatas dapat dilihat perbandingan fase gerak yang terbaik adalah
40 : 60, karena memberikan theoretical plate yang lebih tinggi dan tailing factor
yang lebih kecil, serta memberikan waktu retensi yang lebih cepat.
Menurut Rohman (2009), theoretical plate yang tinggi disyaratkan untuk
pemisahan yang baik. Kolom yang baik akan mempunyai theoretical plate yang
tinggi. Selain itu kinerja kromatografi yang baik adalah jika kromatogram
kromatogram mengalami pengekoran (tailing). Semakin besar harga TF maka
kolom yang di pakai semakin kurang efisien.
Selanjutnya kondisi kromatogram terpilih ini digunakan untuk identifikasi
dan analisis kuantitatif.
4.2Uji Identifikasi Ibuprofen Menggunakan KCKT
Hasil uji identifikasi Ibuprofen pada penyuntikan dengan konsentrasi 60
mcg/ml diperoleh kromatogram dengan waktu retensi 2,50 menit dan laju alir 1
ml/menit, kromatogram dapat dilihat pada Gambar 6 dibawah ini. Waktu retensi
yang diperoleh dari pengujian Baku dibandingkan dengan waktu retensi yang
[image:34.595.121.451.359.516.2]diperoleh dari sampel.
Gambar 6. Kromatogram hasil penyuntikan larutan 60 mcg/ml Baku (PT.Kimia Farma), dengan perbandingan metanol-air (40:60), laju alir 1 ml/ menit
No Nama RT Area k’ Asym N
(USP)
Res (USP)
Alpha
1 ibuprofen 2,50 6221 260.00 1.22 2833 --- ---
Hasil pengujian untuk sampel diperoleh waktu tambat yang hampir sama
dengan Ibuprofen Baku yaitu rata-rata 2,49 dapat di lihat pada Gambar 2. Dapat
diambil kesimpulan bahwa sampel mengandung Ibuprofen.
Penentuan linieritas kurva kalibrasi Ibuprofen Baku Pabrik (PT. Kimia
Farma) ditentukan berdasarkan luas puncak pada konsentrasi 40, 60, 80, 100, dan
120 mcg/ml, diperoleh hubungan yang linier dengan koefisien korelasi (r) =
0,9998 dan persamaan regrasi Y = 107,4434 X + 68,6309. Kurva kalibrasi
ibuprofen dapat dilihat pada Gambar 7 dibawah ini:
Gambar 7. Kurva Kalibrasi Ibuprofen Baku Pabrik (PT. Kimia Farma)
4.4 Penetapan Kadar Sampel
Analisis kuantitatif dapat ditentukan berdasarkan luas puncak dan tinggi
puncak. Pengukuran luas puncak tidak banyak dipengaruhi oleh kondisi
kromatografi dibandingkan dengan tinggi puncak, kecuali laju alir. Oleh karena
itu, pengukuran luas puncak merupakan pilihan yang terbaik dalam analisis
kuantitatif secara KCKT (Johnson dan Stevenson, 1991).
Kadar dapat dihitung dengan mensubtitusikan luas puncak pada Y dari
persamaan regresi Y=107,4434X +68,6309
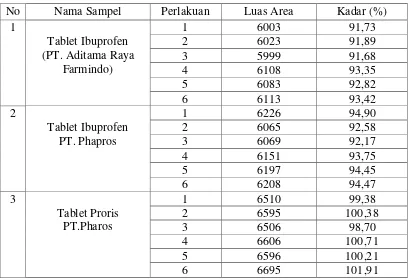
Hasil pengolahan data dari sediaan ibuprofen yang terdapat di
Tabel 2. Hasil pengolahan data kadar Ibuprofen 200 mg dalam sediaan tablet
No Nama Sampel Perlakuan Luas Area Kadar (%)
[image:36.595.108.518.109.389.2]1
Tablet Ibuprofen (PT. Aditama Raya
Farmindo)
1 6003 91,73
2 6023 91,89
3 5999 91,68
4 6108 93,35
5 6083 92,82
6 6113 93,42
2
Tablet Ibuprofen PT. Phapros
1 6226 94,90
2 6065 92,58
3 6069 92,17
4 6151 93,75
5 6197 94,45
6 6208 94,47
3
Tablet Proris PT.Pharos
1 6510 99,38
2 6595 100,38
3 6506 98,70
4 6606 100,71
5 6596 100,21
6 6695 101,91
Tabel 3. Hasil pengolahan data kadar Ibuprofen 400 mg dalam sediaan tablet
No Nama Sampel Perlakuan Luas Area Kadar (%)
1
Tablet Ibuprofen (PT. Indofarma)
1 6221 94,61
2 6117 93,13
3 6287 95,75
4 6198 94,64
5 6157 93,62
6 6226 94,94
2
Tablet Ibuprofen (PT. Phyto Kemo Agung Farma)
1 6753 103.13
2 6940 105,58
3 6721 102,63
4 6695 101,68
5 6808 103,55
6 6842 104,20
3
Tablet Ostarin PT.Otto
1 6264 95,62
2 6259 95,28
3 6410 98,00
4 6258 95,27
5 6362 96,87
Berdasarkan data pada Tabel 2 dan Tabel 3 yang diolah menggunakan
perhitungan statistik diperoleh kadar Ibuprofen dalam sediaan tablet dengan nama
dagang dan generik seperti pada Tabel 4 dan Tabel 5 di bawah ini.
Tabel 4. Hasil penetapan kadar Ibuprofen 200 mg dalam sediaan tablet
No Tablet
Rentang Kadar Ibuprofen tablet (%)
1. Ibuprofen (PT.Aditama Raya Farmindo) 92,48 ± 1,33
2. Ibuprofen (PT. Phapros) 93,72± 1,83
3. Proris (PT.Pharos) 100,22± 1,82
Tabel 5. Hasil penetapan kadar Ibuprofen 400 mg dalam sediaan tablet
No Tablet
Rentang Kadar Ibuprofen tablet (%)
1. Ibuprofen (PT.Indofarma) 94,44 ± 1,54
2. Ibuprofen (PT. Phyto Kemo Agung Farma) 103,46± 2,21
3. Ostarin (PT.Otto) 96,45± 2,02
Dari tabel di atas terlihat bahwa dari keenam sampel yang diteliti
semuanya memenuhi persyaratan kadar yang tertera dalam FI edisi IV (1995)
yaitu mengandung Ibuprofen tidak kurang dari 90,0% dan tidak lebih dari 110,0%
dari jumlah yang tertera pada etiket.
4.5 Hasil Uji Validasi
Pada penelitian ini dilakukan uji validasi metode, dengan metode
penambahan bahan baku (Standard Addition Method) terhadap sampel tablet
persen perolehan kembali (% recovery) dan uji presisi dengan parameter RSD
(Relatif Standar Deviasi), batas deteksi (LOD) dan batas kuantitasi (LOQ).
Uji akurasi dengan parameter persen perolehan kembali dilakukan dengan
menambahkan larutan baku pada analit. Konsentrasi larutan baku yang
ditambahkan adalah 20 mcg/ml, dimana konsentrasi tersebut jumlahnya diatas
batas kuantitasi (LOQ) yang diperoleh pada penelitian ini yaitu 9,775 mcg/ml.
Larutan di buat sebanyak 6 replikasi. Data hasil pengujian perolehan kembali
tablet ibuprofen (PT. Kimia Farma) dengan metode penambahan bahan baku
[image:38.595.113.516.384.630.2](Standar Addition Method) dapat dilihat pada Tabel 6 di bawah ini.
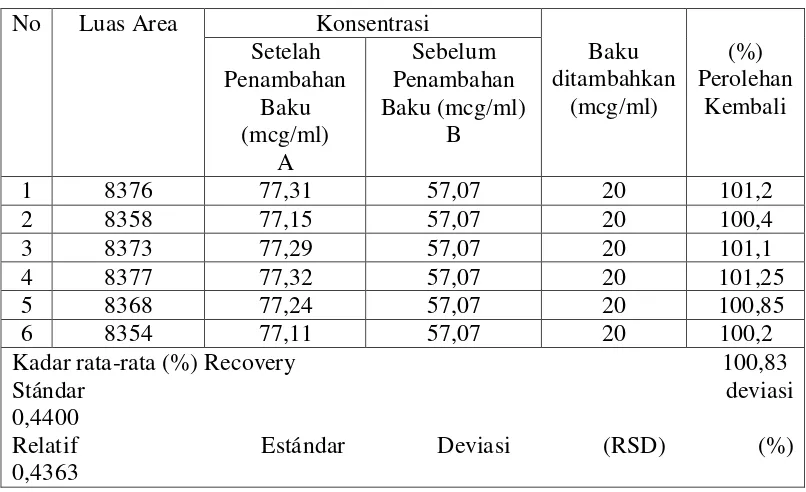
Tabel 6. Data hasil perolehan kembali Ibuprofen dengan metode penambahan
bahan baku (Standard Addition Method)
No Luas Area Konsentrasi
Baku ditambahkan (mcg/ml) (%) Perolehan Kembali Setelah Penambahan Baku (mcg/ml) A Sebelum Penambahan Baku (mcg/ml) B
1 8376 77,31 57,07 20 101,2
2 8358 77,15 57,07 20 100,4
3 8373 77,29 57,07 20 101,1
4 8377 77,32 57,07 20 101,25
5 8368 77,24 57,07 20 100,85
6 8354 77,11 57,07 20 100,2
Kadar rata-rata (%) Recovery 100,83
Stándar deviasi
0,4400
Relatif Estándar Deviasi (RSD) (%) 0,4363
Dari data di atas diperoleh persen perolehan kembali Ibuprofen 100,83 %
dengan Relatif Standar Deviasi (RSD) 0,4363 %. Nilai RSD yang diizinkan
adalah ≤ 2% dan batas rata – rata yang diperoleh adalah 98 – 102 %. Maka dapat
akurasi dan presisi yang memenuhi syarat (WHO, 1992). Batas deteksi (LOD) dan
batas kuantitasi (LOQ) yang diperoleh dari penelitian ini sebesar 2,9327 mcg/ml
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
1. Perbandingan metanol-air yang tepat untuk fase gerak pada penetapan kadar
ibuprofen baku secara KCKT adalah 40:60.
2. Metode kromatografi cair kinerja tinggi dengan fase gerak metanol-air
(40:60) dapat diterapkan pada penetapan kadar ibuprofen dalam sediaan
tablet dan memberikan uji validasi metode yang memenuhi syarat.
3. Hasil penetapan kadar ibuprofen dari keenam sampel dalam sediaan tablet
dengan nama dagang dan generik, semuanya memenuhi persyaratan kadar
yang tertera dalam FI edisi IV (1995).
5.2 Saran
Disarankan agar dilakukan penelitian lebih lanjut kadar ibuprofen dengan
DAFTAR PUSTAKA
Battu, P.R. and Reddy, M.S. (2009). RP-HPLC Method for Simultaneous Estimation of Paracetamol and Ibuprofen in Tablets. Asian J. Research Chem. AJRC All right reserved. Jan.-March, 2009. ISSN 0974-4169. Hal. 70-72.
De Lux Putra, E. (2007). Dasar-dasar Kromatografi Cair Kinerja Tinggi. Diktat. Medan: Fakultas Farmasi USU. Hal. 2.
Depkes. (1989). Informasi Tentang Obat Generik. Pusat Penyuluhan Kesehatan Masyarakat. Majalah Ilmu Kesehatan. Vol II. Hal 83
Ditjen POM. 1995). Farmakope Indonesia. Edisi IV. Jakarta: Departemen Kesehatan RI. Hal. 74.
Gandjar, I.G. dan Rohman, A. (2007). Kimia Farmasi Analisis. Yogyakarta: Penerbit Pustaka Pelajar. Hal. 378-388, 393-394, 463-472.
Gritter, R.J. Bobbit, J.M. and Swharting, A.E. (1991). Introduction to Chromatogarphy. Penterjemah: Kosasih Padmawinata. Pengantar Kromatografi. Edisi II. Bandung: Penerbit ITB. Hal. 186.
Harmita. (2004). Petunjuk Pelaksanaan Validasi Metode dan Cara Perhitungannya. Majalah Ilmu Kefarmasian. Vol I(3). Hal 117-135.
Johnson, E.L. dan Stevenson, R. (1991). Dasar Kromatografi Cair. Penterjemah: Kosasih Padmawinata. Bandung: Penerbit ITB. Hal 4-6, 236.
Meyer, V.R. (2004). Practical High-Performance Liquid Chromatography.
Fourth Edition. Chichester: John Wiley and Sons Inc. Page 4.
Mulja, M. dan Suharman. (1995). Analisis Instrumental. Surabaya: Airlangga University Press. Hal 159, 238-250.
Rohman, A. (2009). Kromatografi Untuk Analisis Obat. Edisi Pertama. Yogyakarta: Graha Ilmu. Hal. 225-226.
United States Pharmacopoeia. (2007). The National Formulary. 30th Edition . The United States Pharmacopoeial Convention. Page 3324-3325.
WHO. (1992). The International Pharmacopeia. Edisi ke-empat. Electronic Version Geneva: World Health Organization. Hal. 98.
Farmakologi dan Terapi. Editor: Sulistia Gan Gunawan. Edisi 5. Jakarta: Departemen Farmakologi dan Terapeutik Fak. Kedokteran UI. Hal. 230. Lampiran 1. Gambar alat KCKT, vial Autosampler,alat penyaring dan neraca
analitik
[image:42.595.113.504.147.642.2]
Gambar 8. Alat KCKT (Hitachi) Gambar 9. Vial
Autosampler
Gambar 10. Pompa Vakum (Gast DO A-PG04-BN) Gambar 11. Neraca analitik
[image:42.595.113.370.153.367.2]Lampiran 2. Gambar Sonifikator
Gambar 12. Sonifikator (Branson 1510)
Lampiran 3. Kromatogram dari Larutan Ibuprofen Baku untuk Mencari Perbandingan Fase Gerak Metanol-Air yang Optimal untuk Analisis
A
No Nama RT Area k’ Asym N (USP) Res(USP) 1 Ibuprofen 2.50 2248 260.00 1.21* 2826* ---
Perbandingan fase gerak metanol-air (40:60) dengan laju alir 1 ml/menit.
B
No Nama RT Area k’ Asym N (USP) Res(USP) 1 Ibuprofen 2.62 2253 280.00 1.64* 2507* ---
Perbandingan fase gerak metanol-air (50:50) dengan laju alir 1 ml/menit.
C
No Nama RT Area k’ Asym N (USP) Res(USP) 1 Ibuprofen 2.86 2246 290.00 1.43* 2263* ---
Lampiran 4. Kromatogram dari Larutan Ibuprofen Baku konsentrasi 40 mcg/ml pada pembuatan kurva kalibrasi
A
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.50 4453 260.00 1.21 * 2830* ---
B
No Nama RT Area k’ Asym N (USP)
C
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.50 4471 260.00 1.21* 2833* ---
D
No Nama RT Area k’ Asym N (USP)
E
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.50 4490 260.00 1.21* 2830* ---
F
No Nama RT Area k’ Asym N(USP) Res
1 Ibuprofen 2.50 4488 260.00 1.21* 2833* ---
Lampiran 5. Kromatogram dari Larutan Ibuprofen Baku konsentrasi 60 mcg/ml pada pembuatan kurva kalibrasi
A
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.50 6695 263.00 1.24* 2853* ---
B
No Nama RT Area k’ Asym N (USP)
C
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.50 6506 263.00 1.24* 2850* ---
D
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.50 6330 263.00 1.24* 2851* ---
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.50 6542 263.00 1.24* 2853* ---
F
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.50 6485 263.00 1.24* 2851* ---
Lampiran 6. Kromatogram dari Larutan Ibuprofen Baku konsentrasi 80 mcg/ml pada pembuatan kurva kalibrasi
A
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.50 8694 262.00 1.20* 2830* ---
B
No Nama RT Area k’ Asym N (USP)
C
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.50 8803 262.00 1.20* 2830* ---
D
No Nama RT Area k’ Asym N (USP)
E
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.50 8638 262.00 1.20* 2833* ---
F
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.50 8774 262.00 1.20* 2830* ---
Lampiran 7. Kromatogram dari Larutan Ibuprofen Baku konsentrasi 100 mcg/ml pada pembuatan kurva kalibrasi
A
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.50 10559 261.00 1.22* 2826* ---
B
No Nama RT Area k’ Asym N (USP)
C
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.50 10682 261.00 1.22* 2828* ---
D
No Nama RT Area k’ Asym N (USP)
E
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.50 10772 261.00 1.22* 2826* ---
F
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.50 10993 261.00 1.22* 2826* ---
Lampiran 8. Kromatogram dari Larutan Ibuprofen Baku konsentrasi 120 mcg/ml pada pembuatan kurva kalibrasi
A
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.50 13058 265.00 1.24* 2830* ---
B
No Nama RT Area k’ Asym N (USP)
C
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.50 13021 265.00 1.24* 2833* ---
D
No Nama RT Area k’ Asym N (USP)
E
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.50 12968 265.00 1.24* 2830* ---
F
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.50 12983 265.00 1.24* 2831* ---
Lampiran 9. Perhitungan persamaan regresi dari kurva kalibrasi Ibuprofen
No X
(mcg/ml))
Y (Area/A)
X2 Y2 X x Y
1 0 0,0000 0,0000 0,0000 0,0000
2 40 4479,0000 1600,0000 20061441,0000 179160,0000 3 60 6520,6666 3600,0000 42519092,9084 391239,9960 4 80 8710,5000 6400,0000 75872810,2500 696840,0000 5 100 10665,1666 10000,0000 113745778,6058 1066516,6600 6 120 13013,8333 14400,0000 169359857,1602 1561659,9960
∑ 400 43389,1665 36000,0000 421558979,9243 3895416,6520
Rata2 66,6667 7231,5278 6000,0000 70259829,9874 649236,1087
b aX Y= +
(
) ( )( )
( )
2( )
2X X n Y X XY n a Σ − Σ Σ Σ − Σ =
(
)
(
)
(
) ( )
2400 36000 6 1665 , 43389 400 6520 , 3895416 6 − − =
=107,4434
aX Y b= −
=7231,5278−
(
107,4434)(
66,6667)
=68,6309
(
) ( )( )
( ) ( )
[
2 2]
[
( )
2( )
2]
Y Y n X X n Y X XY n r Σ − Σ Σ − Σ Σ Σ − Σ =
(
) ( )(
)
(
) ( )
[
2]
[
(
) (
)
2]
1665 , 43389 9243 , 421558979 6 400 36000 6 1665 , 43389 400 6520 , 3895416 6 − − − = r 9998 , 0 = r
Jadi Persamaannya didapat :
Lampiran 10. Perhitungan Batas Deteksi (LOD) dan Batas Kuantitasi (LOQ) Ibuprofen
No X
(mcg/ml)
Y (Area/A)
Yi Y-Yi (Y-Yi)2
1 0 0 68,6309 -68,6309 4710,2004
2 40 4479,0000 4366,3669 112,6331 12686,2152
3 60 6520,6666 6515,2349 5,4317 29,5033
4 80 8710,5000 8664,1029 46,3971 2152,6908
5 100 10665,1666 10812,9709 -147,8043 21846,1111 6 120 13013,8333 12961,8389 51,9944 2703,4176
∑ 44128,1384 2 ) ( 2 − − =
∑
n Yi Y SB 2 6 ) 1384 , 44128 ( − = SB 0335 , 105 = SB Slope SB xLOD=3
4434 , 107 0335 , 105 3x LOD= 9327 , 2 = LOD mcg/ml Slope SB x
LOQ=10
Lampiran 11. Kromatogram Hasil Penyuntikkan dari Larutan Tablet Ibuprofen 200 mg (PT. Aditama Raya Farmindo).
A
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.49 6003 260.00 1.24* 2635* ---
B
No Nama RT Area k’ Asym N (USP)
C
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.49 5999 260.00 1.24* 2833* ---
D
No Nama RT Area k’ Asym N (USP)
E
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.49 6083 260.00 1.24* 2833* ---
F
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.49 6113 260.00 1.24* 2836* ---
Lampiran 12. Analisis Data Statistik untuk Mencari Kadar Sebenarnya dari
Penyuntikan Larutan Tablet Ibuprofen 200 mg (PT. Aditama Raya Farmindo)
No Luas Area X/Kadar (%) (X-Xrata) (X-Xrata)2
1 6003 91,73 -0,75 0,5625
2 6023 91,89 -0,59 0,3481
3 5999 91,68 -0,8 0,64
4 6108 93,35 0,87 0,7569
5 6083 92,82 0,34 0,1156
6 6113 93,42 0,94 0,8836
∑X 554,89 3,3067
Xrata 92,48
1 ) ( 2 − − =
∑
n X X SD 5 3067 , 3= = 0,8132
Pada interval kepercayaan 99% dengan nilai α = 0,01, dk = n – 1 = 6 – 1 = 5 Diperoleh t tabel = 4,0321
Dasar penolakan data apabila t hitung≥ t tabel
t hitung =
n SD X X / −
t hitung data 1 =
6 / 8132 , 0 75 , 0 = 2,2590
t hitung data 2 =
6 / 8132 , 0 59 , 0 = 1,7771
t hitung data 3 =
6 / 8132 , 0 8 , 0 = 2,4096
t hitung data 4 =
6 / 8132 , 0 87 , 0 = 2,6204
t hitung data 5 =
6 / 8132 , 0 34 , 0 = 1,0240
t hitung data 6 =
6 / 8132 , 0 94 , 0
= 2,8313 (semua data diterima)
Jadi kadar sebenarnya terletak antara :
= 92,48 ± 4,0321 x 6 8132 , 0
Lampiran 13. Kromatogram Hasil Penyuntikkan dari Larutan Tablet Ibuprofen 200 mg (PT. Phapros).
A
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.49 6226 263.00 1.22* 2828* ---
B
No Nama RT Area k’ Asym N (USP)
C
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.49 6069 263.00 1.22* 2630* ---
D
No Nama RT Area k’ Asym N (USP)
E
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.49 6197 263.00 1.22* 2626* ---
F
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.49 6208 263.00 1.22* 2628* ---
Lampiran14. Analisis data statistik untuk mencari kadar sebenarnya dari penyuntikkan larutan tablet Ibuprofen 200 mg (PT. Phapros)
1 ) ( 2 − − =
∑
n X X SD 5 1908 , 6= = 1,1127
Pada interval kepercayaan 99% dengan nilai α = 0,01, dk = n – 1 = 6 – 1 = 5 Diperoleh t tabel = 4,0321
Dasar penolakan data apabila t hitung≥ t tabel
t hitung =
n SD X X / −
t hitung data 1 =
6 / 1127 , 1 18 , 1 = 2,5979
t hitung data 2 =
6 / 1127 , 1 14 , 1 = 2,5099
t hitung data 3 =
6 / 1127 , 1 55 , 1 = 3,4125
t hitung data 4 =
6 / 1127 , 1 03 , 0 = 0,0660
t hitung data 5 =
6 / 1127 , 1 73 , 0 = 1,6072
t hitung data 6 =
6 / 1127 , 1 75 , 0
= 1,6512 (semua data diterima)
Jadi kadar sebenarnya terletak antara :
µ = X ± t(1-1/2α)dk x n SD
= 93,72 ± 4,0321 x 6 1127 , 1
No Luas Area X/Kadar(%) (X-Xrata) (X-Xrata)2
1 6226 94,90 1,18 1,3924
2 6065 92,58 -1,14 1,2996
3 6069 92,17 1,55 2,4025
4 6151 93,75 0,03 0,0009
5 6197 94,45 0,73 0,5329
6 6208 94,47 0,75 0,5625
∑X 562,32 6,1908
Lampiran 15. Kromatogram Hasil Penyuntikkan dari Larutan Tablet Proris 200 mg (PT. Pharos).
A
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.49 6510 261.00 1.22* 2828* ---
B
No Nama RT Area k’ Asym N (USP)
C
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.49 6506 261.00 1.22* 2630* ---
D
No Nama RT Area k’ Asym N (USP)
E
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.49 6596 261.00 1.22* 2628* ---
F
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.49 6695 261.00 1.22* 2630* ---
Lampiran16. Analisis data statistik untuk mencari kadar sebenarnya dari penyuntikkan larutan tablet Proris 200 mg (PT. Phapros)
1 ) ( 2 − − =
∑
n X X SD 5 1379 , 6= = 1,1079
Pada interval kepercayaan 99% dengan nilai α = 0,01, dk = n – 1 = 6 – 1 = 5 Diperoleh t tabel = 4,0321
Dasar penolakan data apabila t hitung≥ t tabel
t hitung =
n SD X X / −
t hitung data 1 =
6 / 1079 , 1 84 , 0 = 1,8571
t hitung data 2 =
6 / 1079 , 1 16 , 0 = 0,3537
t hitung data 3 =
6 / 1079 , 1 52 , 1 = 3,3606
t hitung data 4 =
6 / 1079 , 1 49 , 0 = 1,0833
t hitung data 5 =
6 / 1079 , 1 01 , 0 = 0,0221
t hitung data 6 =
6 / 1079 , 1 69 , 1
= 3,7364 (semua data diterima)
Jadi kadar sebenarnya terletak antara :
µ = X ± t(1-1/2α)dk x n SD
= 100,22 ± 4,0321 x 6 1079 , 1
No Luas Area X/Kadar (%) (X-Xrata) (X-Xrata)2
1 6510 99,38 -0,84 0,7056
2 6595 100,38 0,16 0,0256
3 6506 98,70 -1,52 2,3104
4 6606 100,71 0,49 0,2401
5 6596 100,21 -0,01 0,0001
6 6695 101,91 1,69 2,8561
∑X 601,29 6,1379
Lampiran 17. Kromatogram Hasil Penyuntikkan dari Larutan Tablet Ibuprofen 400 mg (PT. Indofarma).
A
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.49 6221 260.00 1.24* 2831* ---
B
No Nama RT Area k’ Asym N (USP)
C
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.49 6287 260.00 1.24* 2830* ---
D
No Nama RT Area k’ Asym N (USP)
E
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.49 6157 260.00 1.24* 2831* ---
F
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.49 6226 260.00 1.24* 2831* ---
Lampiran18. Analisis data statistik untuk mencari kadar sebenarnya dari penyuntikkan larutan tablet Ibuprofen 400 mg (PT. Indofarma)
1 ) ( 2 − − =
∑
n X X SD 5 4235 , 4= = 0,9405
Pada interval kepercayaan 99% dengan nilai α = 0,01, dk = n – 1 = 6 – 1 = 5 Diperoleh t tabel = 4,0321
Dasar penolakan data apabila t hitung≥ t tabel
t hitung =
n SD X X / −
t hitung data 1 =
6 / 9405 , 0 17 , 0 = 0,4428
t hitung data 2 =
6 / 9405 , 0 31 , 1 = 3,4123
t hitung data 3 =
6 / 9405 , 0 31 , 1 = 3,4123
t hitung data 4 =
6 / 9405 , 0 2 , 0 = 0,5200
t hitung data 5 =
6 / 9405 , 0 82 , 0 = 2,1359
t hitung data 6 =
6 / 9405 , 0 5 , 0
= 1,3024 (semua data diterima)
Jadi kadar sebenarnya terletak antara :
µ = X ± t(1-1/2α)dk x n SD
No Luas Area X/Kadar (%) (X-Xrata) (X-Xrata)2
1 6221 94,61 0,17 0,0289
2 6117 93,13 -1,31 1,7161
3 6287 95,75 1,31 1,7161
4 6198 94,64 0,2 0,004
5 6157 93,62 -0,82 0,6724
6 6226 94,94 0,5 0,25
∑X 566,69 4,4235
= 94,44 ± 4,0321 x 6 9405 , 0
Lampiran 19. Kromatogram Hasil Penyuntikkan dari Larutan Tablet Ibuprofen 400 mg (PT. Phyto Kemo Agung Farma).
A
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.49 6753 261.00 1.22* 2833* ---
B
No Nama RT Area k’ Asym N (USP)
C
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.49 6721 261.00 1.22* 2834* ---
D
No Nama RT Area k’ Asym N (USP)
E
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.49 6808 261.00 1.22* 2835* ---
F
No Nama RT Area k’ Asym N (USP)
Res (USP) 1 Ibuprofen 2.49 6842 261.00 1.22* 2833* ---
Lampiran 20. Analisis data statistik untuk mencari kadar sebenarnya dari penyuntikkan larutan tablet Ibuprofen 400 mg (PT. Phyto Kemo Agung Farma)
1 ) ( 2 − − =
∑
n X X SD 5 0163 , 9= = 1,3428
Pada interval kepercayaan 99% dengan nilai α = 0,01, dk = n – 1 = 6 – 1 = 5 Diperoleh t tabel = 4,0321
Dasar penolakan data apabila t hitung≥ t tabel
t hitung =
n SD X X / −
t hitung data 1 =
6 / 3428 , 1 33 , 0 = 0,6019
t hitung data 2 =
6 / 3428 , 1 12 , 2 = 3,8672
t hitung data 3 =
6 / 3428 , 1 83 , 0 = 1,5140
t hitung data 4 =
6 / 3428 , 1 78 , 1 = 3,1010
t hitung data 5 =
6 / 3428 , 1 09 , 0 = 0,1641
t hitung data 6 =
6 / 3428 , 1 74 , 0
= 1,3498 (Semua data diterima)
Jadi kadar sebenarnya terletak antara :
µ = X ± t(1-1/2α)dk x n SD
No Luas Area X/Kadar (%) (X-Xrata) (X-Xrata)2
1 6753 103,1