PENETAPAN KADAR GLISERIL GUAIAKOLAT
DALAM SEDIAAN TABLET
SECARA SPEKTROFOTOMETRI ULTRA VIOLET
TUGAS AKHIR
OLEH:
ISTIMEWA
BAKO
NIM 102410069
PROGRAM STUDI DIPLOMA III
ANALIS FARMASI DAN MAKANAN
FAKULTAS FARMASI
KATA PENGANTAR
Puji syukur penulis ucapkan kehadirat Allah SWT atas segala limpahan rahmat dan karunia-Nya yang telah memberikan pengetahuan, kekuatan, kesehatan dan kesempatan kepada penulis sehingga penulis dapat menyelesaikan tugas akhir
yang berjudul ”Penetapan Kadar Gliseril Guaiakolat Dalam Sediaan Tablet Secara Spektrofotometri Ultra Violet”. Tugas akhir ini disusun untuk memenuhi salahsatu
syarat untuk menyelesaikan Program Studi Diploma III Analis Farmasi Dan Makanan di Fakultas Farmasi Universitas Sumatera Utara.
Penulis menyadari sepenuhnya bahwa tanpa bantuan dari berbagai pihak,
penulis tidak akan dapat menyelesaikan tugas akhir ini sebagaimana mestinya. Untuk itu penulis mengucapkan terima kasih yang sebesar–besarnya kepada berbagai pihak antara lain:
1. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., sebagaiDekan Fakultas Farmasi Universitas Sumatera Utara.
2. Bapak Prof. Dr. Jansen Silalahi, M.App.Sc., Apt., sebagai Ketua Program Studi Diploma III Analis Farmasi dan makanan Fakultas Farmasi Universitas Sumatera Utara.
3. Bapak Dr. Kasmirul Ramlan Sinaga, M.S., Apt., selaku Dosen Pembimbing, yang telah membimbing dan mengarahkan penulis dalam pembuatan tugas akhir
4. Bapak Drs. Panal Sitorus, M.Si., Apt., sebagai Dosen Penasehat Akademis yang telah memberikan nasehat dan pengarahan kepada penulis dalam hal akademis
setiap semester.
5. Bapak Kepala Manager industri PT KIMIA FARMA (PERSERO) Tbk. PLANT MEDAN beserta stafnya yang telah membantu dan menyediakan fasilitas kepada
penulis selama melakukan Praktek Kerja Lapangan.
6. Bapak Drs. Beben Budiman, Apt., selaku Plant Manager PT Kimia Farma
(Persero) Tbk. Plant Medan.
7. Bapak Heru Khoerudin, S.Si., Apt., selaku koordinator pembimbing praktek kerja lapangan yang telah membimbing dan memberikan saran serta petunjuk
selama pelaksanaan PKL di PT KimiaFarma (Persero) Tbk Medan.
8. Bapak dan Ibu dosen staf pengajar Fakultas Farmasi Universitas Sumatera Utara atas semua ilmu, didikan dan bimbingan kepada penulis selama di perguruan
tinggi ini.
9. Staf administrasi Fakultas Farmasi yang telah membantu kemudahan
administrasi selama ini.
10.Ibunda tercinta serta seluruh keluarga yang telah memberikan doa restu dan motivasi hingga Tugas Akhir ini selesai.
11.Sahabat–sahabat yang satu kelompok dalam Praktek Kerja Lapangan yaitu Muhammad Asro, Elis Suryani dan Eva Lina Olivia yang telah saling membantu
dalam praktek kerja lapangan.
namanya satu per satu, terima kasih buat kebersamaan dan semangatnya selama ini, serta masukan dalam penyusunan tugas akhir ini.
13.Serta pihak-pihak yang telah ikut membantu penulis namun tidak dapat disebutkan namanya satu per satu.
Penulis menyadari sepenuhnya bahwa tugas akhir ini masih terdapat
kekurangan, serta dalam penulisan maupun penyajian dalam tulisan ini masih jauh dari kesempurnaan. Oleh karena itu dengan segala kerendahan hati penulis
menerima serta sangat mengharapkan saran dan kritik yang sifatnya membangun demi kesempurnaan tugas akhir ini.
Akhir kata semoga Allah SWT melimpahkan rahmat dan karunia–Nya
kepada kita semua dan harapan penulis semoga tugas akhir ini dapat memberikan manfaat bagi kita semua. Amin.
Medan, 23 Agustus 2013
Penulis,
PENETAPAN KADAR GLISERILGUAIAKOLAT DALAM SEDIAAN TABLET SECARA SPEKTROFOTOMETRI ULTRA VIOLET
ABSTRAK
Gliseril guaiakolat (guaifenesin) adalah derivat guaiakol yang banyak digunakan sebagai ekspektoran dalam berbagai jenis sediaan obat batuk. Dalam perdagangan, biasanya tablet Gliseril Guaiakolat diformulasikan dalam bentuk sediaan tablet dengan dosis, 50 mg atau 100 mg untuk setiap tablet. Tujuan pemeriksaan ini adalah untuk mengetahui apakah kadar gliseril guaiakolat dalam formulasi sediaan tablet hasil produksi PT. Kimia Farma Tbk. Plant Medan memenuhi syarat seperti yang tertera pada Farmakope Indonesia Edisi IV.
Penentuan kadar gliseril guaiakolat dilakukan dengan menggunakan metode spektrofotometri UV dengan panjang gelombang maksimum 274 nm. Percobaan ini dilakukan sebanyak 2 kali pengukuran untuk masing-masing batch. Hasil yang diperoleh menunjukkan bahwa kadar rata-rata gliseril guaiakolat dalam tablet dari batch 30096 T, 30097 T, dan 30098 T yang diproduksi PT.Kimia Farma Tbk. Plant Medan masing-masing sebesar 103,69%, 99,79%, dan 97,33%. Farmakope Indonesia Edisi ke-IV memberi persyaratan kadar tablet gliseril guaiakolat, yaitu tidak kurang dari 90,0% dan tidak lebih dari 110,0% dari jumlah yang tertera pada etiket, sehingga hasil penentuan kadar yang dilakukan memenuhi persyaratan.
GUAIACOLATE GLYCERYL ASSAY IN TABLET DOSAGE BY SPECTROPHOTOMETRY UV
ABSTRACT
Glyceryl guaiacolate ( guaifenesin ) is guaiacol derivatives are widely used as an expectorant in cough medicines different types of preparations . In the trade, usually Glyceryl guaiacolate tablet formulated in tablet dosage forms with dose , 50 mg or 100 mg for each tablet . The purpose of this examination is to determine whether the levels of glyceryl guaiacolate in tablet dosage formulations produced by PT. Kimia Farma Tbk . Plant Field qualifies as shown on Indonesian Pharmacopoeia Edition IV.
Determination of glyceryl guaiacolate done using UV spectrophotometric method with a maximum wacelength of 274 nm. This experiment is done as much as 2 times mewasurement.
Determination of glyceryl guaiacolate done using UV spectrophotometric method with a maximum wavelength of 274 nm. This experiment is done as much as 2 times measurements for each batch.
The results showed that the average levels of glyceryl guaiacolate in tablets of batch 30096 T , 30097 T , and T 30 098 produced PT.Kimia Farma Tbk. Plant Medan respectively 103.69 %, 99.79 %, and 97.33 %. Indonesian Pharmacopoeia Fourth Edition gives glyceryl guaiacolate tablet content requirements, is not less than 90.0 % and not more than 110.0 % of the amount listed on the label, so that the determination of which do meet the requirement.
DAFTAR ISI
2.8 Metode Penetapan Kadar Secara Spektrofotometri Ultra Violet(UV) ... 15
BAB III METODE PENGUJIAN ... 20
3.1 Tempat Pelaksanaan Penetapan kadar ... 20
3.2 Alat ... 20
3.3 Bahan ... 20
3.4.2 Pengambilan Sampel Uji ... 21
3.4.3 Larutan Standar ... 21
3.4.4 Larutan Uji ... 21
3.5Cara Penetapan Kadar ... 21
BAB IV HASIL DAN PEMBAHASAN ... 24
4.1 Hasil ... 24
4.2 Pembahasan ... 24
BAB V KESIMPULAN DAN SARAN ... 26
5.1 Kesimpulan ... 26
5.2 Saran ... 26
DAFTAR PUSTAKA ... 27
LAMPIRAN ... 29
Perhitungan Penetapan Kadar ... 29
PENETAPAN KADAR GLISERILGUAIAKOLAT DALAM SEDIAAN TABLET SECARA SPEKTROFOTOMETRI ULTRA VIOLET
ABSTRAK
Gliseril guaiakolat (guaifenesin) adalah derivat guaiakol yang banyak digunakan sebagai ekspektoran dalam berbagai jenis sediaan obat batuk. Dalam perdagangan, biasanya tablet Gliseril Guaiakolat diformulasikan dalam bentuk sediaan tablet dengan dosis, 50 mg atau 100 mg untuk setiap tablet. Tujuan pemeriksaan ini adalah untuk mengetahui apakah kadar gliseril guaiakolat dalam formulasi sediaan tablet hasil produksi PT. Kimia Farma Tbk. Plant Medan memenuhi syarat seperti yang tertera pada Farmakope Indonesia Edisi IV.
Penentuan kadar gliseril guaiakolat dilakukan dengan menggunakan metode spektrofotometri UV dengan panjang gelombang maksimum 274 nm. Percobaan ini dilakukan sebanyak 2 kali pengukuran untuk masing-masing batch. Hasil yang diperoleh menunjukkan bahwa kadar rata-rata gliseril guaiakolat dalam tablet dari batch 30096 T, 30097 T, dan 30098 T yang diproduksi PT.Kimia Farma Tbk. Plant Medan masing-masing sebesar 103,69%, 99,79%, dan 97,33%. Farmakope Indonesia Edisi ke-IV memberi persyaratan kadar tablet gliseril guaiakolat, yaitu tidak kurang dari 90,0% dan tidak lebih dari 110,0% dari jumlah yang tertera pada etiket, sehingga hasil penentuan kadar yang dilakukan memenuhi persyaratan.
GUAIACOLATE GLYCERYL ASSAY IN TABLET DOSAGE BY SPECTROPHOTOMETRY UV
ABSTRACT
Glyceryl guaiacolate ( guaifenesin ) is guaiacol derivatives are widely used as an expectorant in cough medicines different types of preparations . In the trade, usually Glyceryl guaiacolate tablet formulated in tablet dosage forms with dose , 50 mg or 100 mg for each tablet . The purpose of this examination is to determine whether the levels of glyceryl guaiacolate in tablet dosage formulations produced by PT. Kimia Farma Tbk . Plant Field qualifies as shown on Indonesian Pharmacopoeia Edition IV.
Determination of glyceryl guaiacolate done using UV spectrophotometric method with a maximum wacelength of 274 nm. This experiment is done as much as 2 times mewasurement.
Determination of glyceryl guaiacolate done using UV spectrophotometric method with a maximum wavelength of 274 nm. This experiment is done as much as 2 times measurements for each batch.
The results showed that the average levels of glyceryl guaiacolate in tablets of batch 30096 T , 30097 T , and T 30 098 produced PT.Kimia Farma Tbk. Plant Medan respectively 103.69 %, 99.79 %, and 97.33 %. Indonesian Pharmacopoeia Fourth Edition gives glyceryl guaiacolate tablet content requirements, is not less than 90.0 % and not more than 110.0 % of the amount listed on the label, so that the determination of which do meet the requirement.
BAB I PENDAHULUAN
1.1 Latar Belakang
Batuk adalah suatu refleks fisiologis protektif yang berfungsi untuk
mengeluarkan dan membersihkan saluran pernapasan dari dahak, debu, zat–zat perangsang asing dan unsur–unsur infeksi. Orang sehat hampir tidak batuk sama
sekali, berkat mekanisme pembersihan dari bulu getar (Cilia) di dinding bronchi, yang berfungsi menggerakkan dahak keluar dari paru–paru menuju batang tenggorokan. Cilia ini juga membantu menghindarkan masuknya zat–zat asing ke
saluran napas (Tan dan Raharjo, 2007).
Data analitik zat aktif mencakup data kualitatif, data kuantitatif, dan kemurnian dari zat berkhasiat. Untuk penetapan kualitatif biasanya digunakan
reaksi warna, kromatografi lapis tipis, spectrum serapan inframerah, dan reaksi lainnya. Penetapan kadar zat aktif biasanya dilakukan dengan metode titrasi,
spektrofotometri, kromatografi gas, kromatografi cair kinerja tinggi (KCKT), dan sebagainya. Analisis ini merupakan bagian penting dalam praformulasi, untuk menetapkan identitas dan kadar zat aktif (Siregar, 2010).
Dalam perdagangan, biasanya tablet gliseril guaiakolat diformulasikan dalam bentuk sediaan tablet dengan dosis, 50 mg atau 100 mg untuk setiap tablet.
Pengawasan terhadap tablet gliseril guaiakolat perlu dilakukan karena jika tidak memenuhi syarat dapat membahayakan konsumen. Oleh karena itu, zat
berkhasiat gliseril guaiakolat sediaan tablet sangat penting untuk diperiksa apakah telah memenuhi syarat atau tidak, sehingga penulis tertarik untuk mengambil tugas akhir dengan judul ”Penetapan Kadar Gliseril Guaiakolat Dalam Sediaan
Tablet Secara Spektrofotometri Ultraviolet”.
Dalam Farmakope Indonesia Edisi III, metode spektrofotometri ultraviolet
(UV) digunakan untuk mendapatkan kadar senyawa obat dalam jumlah yang cukup banyak. Penetapan kadar gliseril guaiakolat dilakukan dengan metode spektrofotometri ultraviolet (UV), karena analisis dengan spektrofotometri UV
cepat, teliti, peka, dan penyiapan sampelnya mudah. Metode ini biasanya
berdasarkan pada nilai suatu obat, cara untuk mendapatkan kadar sampel
adalah dengan menggunakan perbandingan absorbansi sampel dengan absorbansi baku (Rohman,2007).
1.2 Tujuan dan Manfaat 1.2.1 Tujuan
Untuk mengetahui apakah kadar gliseril guaiakolat yang digunakan dalam formulasi sediaan tablet yang dihasilkan oleh PT Kimia Farma Tbk. Plant Medan memenuhi syarat seperti yang tertera pada Farmakope Indonesia Edisi IV.
Untuk menambah pengetahuan dan keterampilan, khususnya tentang penetapan kadar gliseril guaiakolat sebagai zat aktif menggunakan metode
BAB II
TINJAUAN PUSTAKA
2.1Obat
Obat adalah zat aktif berasal dari nabati, hewani, kimiawi alam maupun
sintesis dalam dosis atau kadar tertentu dapat dipergunakan untuk preventif (profilaksis), rehabilitasi, terapi, diagnosa terhadap suatu keadaan penyakit pada
manusia maupun hewan. Namun zat aktif tersebut tidak dapat dipergunakan begitu saja sebagai obat, terlebih dahulu harus dibuat dalam bentuk sediaan seperti pil, tablet, kapsul, sirup, suspensi, supositoria, salep dan lain-lain (Jas,2007).
Meskipun obat dapat menyembuhkan penyakit, tetapi masih banyak juga orang yang menderita akibat keracunan obat. Oleh karena itu, dapat dikatakan bahwa obat dapat bersifat sebagai obat dan dapat juga bersifat sebagai racun. Obat
itu bersifat sebagai obat apabila tepat digunakan dalam pengobatan suatu penyakit dengan dosis dan waktu yang tepat. Jadi, apabila obat salah digunakan dalam
pengobatan atau dengan dosis yang berlebihan maka akan menimbulkan keracunan, sedangkan bila dosisnya kecil maka kita tidak akan memperoleh penyembuhan (Anief,1991).
Bahan baku obat adalah semua bahan,baik yang berkhasiat (zat aktif) maupun tidak berkhasiat (zat Nonaktif/eksipien), yang berubah maupun tidak
Menurut Dirjen POM(2006), bahan (zat) aktif adalah tiap bahan atau campuran bahan yang akan digunakan dalam pembuatan sediaan farmasi dan
apabila digunakan dalam pembuatan obat menjadi zat aktif obat tersebut. Dalam arti lain, bahan (zat) aktif adalah bahan yang ditujukan untuk menciptakan khasiat farmakologi atau efek langsung lain dalam diagnosis, penyembuhan, peredaan,
pengobatan atau pencegahan penyakit, atau untuk mempengaruhi struktur dan fungsi tubuh.
2.2 Tablet
Tablet merupakan bahan obat dalam bentuk sediaan padat yang biasanya
dibuat dengan penambahan bahan tambahan farmasetika yang sesuai. Tablet dapat berbeda-beda ukuran, bentuk, berat, kekerasan, ketebalan, daya hancur, dan aspek lainnya tergantung pada cara pemakaian tablet dan metode pembuatannya.
Umumnya tablet digunakan pada pemberian obat secara oral (Ansel, 1989). Untuk membuat tablet diperlukan bahan tambahan berupa:
a. Bahan pengisi (diluent)
Bahan pengisi adalah suatu zat inert secara farmakologis yang ditambahkan ke dalam suatu formulasi sediaan tablet, bertujuan untuk penyesuaian bobot,
ukuran tablet sesuai yang dipersyaratkan, untuk membantu kemudahan dalam pembuatan tablet, dan meningkatkan mutu sediaan tablet. Berikut ini beberapa
b. Bahan pengikat (binder)
Bahan pengikat ditambahkan ke dalam formulasi tablet untuk menambah
kohesivitas serbuk sehingga memberi ikatan yang penting untuk membentuk granul yang dibawah pengempaan akan membentuk suatu massa kohesif atau kompak yang disebut tablet. Beberapa jenis pengikat yang sering digunakan:
pati 5-10%, pati pragelatinisasi 0,5%, starch 1500, gelatin 2-10%, sukrosa 50-75%, akasia 10-25%, polivinilpirolidon 3-15% (Siregar, 2010).
c. Bahan penghancur (disintegrator)
Bahan ini dimaksudkan agar tablet dapat hancur dalam saluran cerna. Zat-zat yang digunakan seperti: amilum kering, gelatin, agar-agar, natrium alginat.
d. Bahan pelicin (lubricant)
Bahan ini dimaksudkan agar tablet tidak lekat pada cetakan. Zat-zat yang digunakan seperti: talcum, magnesii stearat, asam stearat.
Dalam pembuatan tablet, zat berkhasiat dan bahan tambahan, kecuali bahan pelicin dibuat granul (butiran kasar), karena serbuk yang halus tidak mengisi
cetakan dengan baik. Dengan dibuat granul akan terjadi free flowing, mengisi cetakan secara tetap dan dapat dihindari tablet menjadi capping (retak) (Anief, 1987).
2.3Cara Pembuatan Tablet
2. Serbuk biasanya tidak memiliki sifat lubrikasi dan dintegrasi yang dipersyaratkan untuk pentabletan.
3. Serbuk pada umumnya tidak atau kurang memiliki sifat mengalir bebas (Siregar, 2010).
Untuk itu zat aktif mula-mula harus mengalami praperlakuan, baik tunggal
ataupun dalam kombinasi dengan eksipien untuk membentuk granul yang memberi kemungkinan untuk dikempa. Proses ini disebut sebagai granulasi.
Granulasi adalah setiap proses membesarkan ukuran partikel-partikel kecil dengan mengumpulkannya bersama-sama menjadi agregat yang lebih besar dan permanen untuk membuatnya mengalir bebas yang serupa dengan pasir kering (Siregar,
2010).
Terdapat 3 metode pembuatan tablet kompresi yaitu: 1. Granulasi Basah
Metode granulasi basah merupakan yang terluas digunakan orang dalam memproduksi tablet kompresi. Langkah-langkah yang diperlukan dalam
pembuatan tablet dengan metode ini dapat dibagi sebagai berikut: menimbang dan mencampur bahan-bahan, pembuatan granulasi basah, pengayakan adonan lembab menjadi granul, pengeringan, pengayakan kering, pencampuran bahan pelicin,
pembuatan tablet dengan kompresi.
Penimbangan dan pencampuran: Bahan aktif, pengisi, dan bahan
dan dicampur, diaduk baik, biasanya dengan menggunakan mesin pencampur serbuk atau mikser.
Pembuatan granulasi basah. Hal ini dapat dilakukan dengan menambahkan cairan pengikat ke dalam campuran serbuk, melewatkan adonan yang lembab melalui ayakan yang ukuran nya sesuai kebutuhan, granul yang
dihasilkan melalui pengayakan ini dikeringkan, lalu diayak kembali dengan ayakan yang ukurannya lebih kecil supaya mengurangi ukuran granul berikut nya.
Unsur pengikat dalam tablet juga membantu merekatkan granul satu dengan lainnya, menjaga kesatuan tablet setelah dikompresi. Bahan pengikat yang digunakan adalah 10-20% cairan dari tepung jagung, 25-50% larutan glukosa,
molase, macam-macam gom alam (seperti akasia) derivat selulosa (metilselulosa, karboksimetilselulosa dan selulosa mikrokristal), gelatin, dan povidon. Bila diinginkan warna dan rasa dapat ditambahkan ke dalam bahan pengikat sehingga
terjadi granulasi dengan warna dan rasa yang diinginkan.
Penyaringan adonan lembab menjadi granul. Pada umumnya granulasi
basah ditekan melalui ayakan nomor 6 atau 8. Dibuat granul dengan menekankan pada alat yang dibuat berlubang-lubang.
Pengeringan granul. Kebanyakan granul dikeringkan dalam kabinet
pengering dengan sistem sirkulasi udara dan pengendalian temperatur. Untuk metode terbaru untuk pengeringan sekarang ini yaitu fluidization disalurkan ke
Penyaringan kering. Setelah dikeringkan, granul dilewatkan melalui ayakan dengan lubang lebih kecil daripada yang biasa dipakai untuk pengayakan
granulasi asli. Ukuran granul dihaluskan tergantung pada ukuran punch yang akan dipakai dan tablet yang akan diproduksi. Semakin kecil tablet yang akan diproduksi semakin halus granul yang dipakai, biasa nya menggunakan ayakan
ukuran 12-20.
Pelinciriran atau lubrikasi. Jumlah pelincir yang dipakai pada pembuatan
tablet mulai dari 0,1% berat granul sampai 5%. Manfaat pelincir dalam pembuatan tablet kompresi; mempercepat aliran granul dalam corong kedalam rongga cetakan, mencegah melekat nya granul pada punch dan cetakan,
mengurangi gesekan antara tablet dan dinding cetakan ketika tablet dilemparkan dari mesin dan memberikan rupa yang bagus pada tablet yang sudah jadi.
Pencetakan tablet. Mesin tablet berputar (rotary) dengan kecepatan tinggi
mempunyai banyak punch dan die (cetakan) dapat menyisihkan mesin tablet tunggal, karena punch berputar secara terus menerus maka pencetakan tablet
berlangsung secara terus menerus pula. Mesin tablet tunggal biasanya berkapasitas 100 tablet per menit sedangkan mesin tablet rotary dengan 16 tempat (16 set punch dan die) dapat memproduksi 1150 tablet per menit (Ansel, 1989).
2. Granulasi Kering
Tujuan metode granulasi kering adalah untuk memperoleh granul yang
aktif tidak dapat mengalir bebas dan dosis efektif zat aktif terlalu besar untuk kempa langsung (Siregar, 2010). Dalam metode ini, baik bahan aktif maupun
pengisi harus memiliki sifat kohesif supaya masa yang jumlah nya besar dapat dibentuk. Metode ini khususnya untuk bahan-bahan yang tidak dapat diolah dengan metode granulasi basah, karena kepekaannya terhadap uap air atau karena
untuk mengeringkannya diperlukan temperatur yang tinggi (Ansel, 1989). 3. Kompresi Langsung
Beberapa granul bahan kimia seperti kalium klorida, kalium iodida, amonium klorida, dan metenamin, memiliki sifat mudah mengalir sebagai mana juga sifat-sifat kohesifnya yang memungkinkan untuk langsung dikompresi dalam
mesin tablet tanpa memerlukan metode granulasi basah atau kering. Pada waktu sekarang ini penggunaan pengencer yang dikeringkan dengan penyemprotan, meluas kepada formula-formula tablet tertentu daripada dengan serbuk pengisi
biasa, kualitas yang diinginkan untuk tablet kompresi langsung dan sejumlah produk-produk lainnya banyak diproduksi dengan cara ini.
Capping atau keretakan dari tablet disebabkan oleh beberapa faktor dan tidak terbatas pada tablet yang dibuat dengan pengkompresian langsung saja. Misalnya bila punch tidak bersih sekali dan tidak halus sekali dapat menghasilkan
tablet yang terlepas bagian atasnya sebagaimana juga dengan cetakan (die) yang sudah tua dan tidak sempurna. Tekanan yang terlalu besar pada pengempaan dapat
dan perlu supaya pengisian rongga cetakan wajar. Tetapi kelebihan dari serbuk halus ini dapat juga berperan menjadi capping bila sejumlah besar udara
terperangkap dalam tablet, keadaan seperti ini disebut laminating (Ansel, 1989). 2.4 Syarat-Syarat Tablet
Menurut Farmakope Indonesia Edisi IV dan sumber-sumber lainnya, tablet
harus memenuhi persyaratan sebagai berikut:
A. Keseragaman Bobot
Tablet harus memenuhi uji keseragaman bobot untuk menjamin keseragaman bobot tiap tablet yang dibuat. Tablet yang bobotnya seragam diharapkan memiliki kandungan bahan obat yang sama, sehingga mempunyai efek terapi
yang sama. B. Kekerasan
Tablet harus memiliki kekuatan atau kekerasan agar dapat bertahan terhadap
berbagai guncangan pada saat pengepakan dan pengangkutan. Uji ini dilakukan dengan menggunakan alat yang disebut Hardness Tester. Tablet diletakkan
diantara alat penekan punch dan dijepit dengan memutar sekrup pengatur sampai tanda lampu menyala, lalu ditekan tombol sehingga tablet pecah. Tekanan dapat ditunjukkan melalui skala yang tertera. Umumnya kekuatan
tablet berkisar 4-8 kg.
C. Kerenyahan
Uji ini menggunakan alat yang disebut Roche Friabilator yang terdiri dari sebuah tabung yang berputar, kearah radial disambungkan sebuah bilah
lengkung. Tablet dimasukkan ke dalam drum tersebut, dihidupkan alat maka drum berputar dan tablet bergulir jatuh sampai pada putaran berikutnya dipegang kembali oleh bilah. Pemutaran dilakukan 100 kali dengan persyaratan
tablet tidak boleh kehilangan berat lebih dari 0,8%.
D. Waktu Hancur
Uji ini dimaksudkan untuk mengetahui kesesuaian batas waktu hancur yang tertera dalam masing-masing monografi, kecuali pada etiket dinyatakan bahwa tablet dirancang untuk pelepasan kandungan obat secara bertahap dalam jangka
waktu tertentu atau melepaskan obat dalam dua periode berbeda atau lebih dengan jarak waktu yang jelas diantara periode pelepasan tersebut. Uji waktu hancur tidak menyatakan bahwa sediaan atau bahan aktifnya terlarut sempurna.
Interval waktu hancur yaitu 5-30 menit. Sediaan dinyatakan hancur sempurna bila tidak ada sisa sediaan yang tidak larut tertinggal pada kasa.
E. Penetapan Kadar Zat Berkhasiat
Penetapan kadar ini dilakukan untuk mengetahui apakah tablet tersebut memenuhi syarat sesuai dengan etiket. Bila kadar obat tersebut tidak
memenuhi syarat, berarti obat tersebut tidak memiliki efek terapi yang baik dan tidak layak dikonsumsi. Penetapan kadar dilakukan dengan menggunakan
F. Disolusi
Disolusi adalah proses pemindahan molekul obat dari bentuk padat kedalam
larutan pada suatu medium. Uji ini digunakan untuk mengetahui kesesuaian dengan persyaratan disolusi yang tertera dalam monografi pada sediaan tablet kecuali pada etiket dinyatakan bahwa tablet harus dikunyah atau tidak
memerlukan uji disolusi.
2.5 Batuk
Batuk merupakan gejala yang mungkin paling umum yang bisa timbul
pada penyakit tenggorokan sampai penyakit cabang tenggorokan. Batuk bisa kering atau berlendir/berdahak (Irianto, 2004).
Batuk adalah suatu refleks fisiologis protektif yang berfungsi untuk
mengeluarkan dan membersihkan saluran pernapasan dari dahak, debu, zat–zat perangsang asing dan unsur–unsur infeksi. Orang sehat hampir tidak batuk sama
sekali, berkat mekanisme pembersihan dari bulu getar di dinding bronchi, yang berfungsi menggerakkan dahak keluar dari paru–paru menuju batang tenggorokan. Cilia ini juga membantu menghindarkan masuknya zat–zat asing ke
saluran napas (Tjay dan Raharjo, 2007).
Batuk juga bisa dipicu oleh stimulasi reseptor–reseptor yang terdapat di
sumsum lanjutan (medula oblogata), yang kemudian mengkoordinir serangkaian proses yang menjurus ke respon batuk (Tan dan Raharjo, 2007).
Menurut Anif (2000), obat yang digunakan untuk mengobati penyakit batuk dibagi dalam dua golongan besar, yaitu:
1. Ekspektoransia, yaitu mempertinggi sekresi dari saluran pernapasan dan atau
mencairkan riak sehingga mudah dikeluarkan.
2. Zat–zat pereda batuk (antitusif), yaitu zat–zat ini mengerem rangsangan batuk,
dan titik kerjanya dapat sentral dan perifer.
Bagi Mutschler (1991), jenis dua golongan besar di atas dibagi lagi. Ekspektoran dibagi atas: Sekretolitika (meniggikan sekresi bronchus dan dengan
demikian mengencerkan lendir), Mukolitika (mengubah sifat fisikokimia sekret, terutama viskositasnya diturunkan), Sekretomotorika (menyebabkan gerakan secret dan batuk, untuk mengeluarkan sekret tersebut), sedangkan sifat kerja
antitusif dibagi atas: penekanan pusat batuk (serabut sensorik /rangsang batuk) dan penekan reseptor batuk (serabut motorik/pendorong batuk).
2.6 Ekspektoran
Pengertian ekspektoran menurut Sartono (2005) adalah obat yang bekerja
dengan cara meningkatkan jumlah cairan sehingga lendir menjadi encer, dan juga merangsang pengeluaran lendir dari saluran napas.
Belum ada data yang membuktikan evektivitas ekspektoran dengan dosis yang umum digunakan. Mekanisme kerjanya diduga berdasarkan stimulasi mukosa
lambung dan selanjutnya secara refleks merangsang sekresi kelenjar saluran napas lewat nervus vagus, sehingga menurunkan viskositas dan mempermudah pengeluaran dahak.
2.7 Gliseril Guaiakolat (Dirjen POM, 1995) OH OCH2CHCH2
OCH3
3-(o-Metoksifenoksi)-1,2-propanadiol [93-14-1]
Rumus molekul : C10H14O
Berat molekul : 198,22
Pemerian : serbuk hablur, putih sampai agak keabu–abu khas lemah, rasa
pahit.
Kelarutan : larut dalam air, dalam etanol, dalam kloroform, dan dalam propilen glikol, agak sukar larut dalam gliserin.
2.7.1 Indikasi
Gliseril guaiakolat selain bekerja sebagai ekspektoran, juga meningkatkan
pembersihan mukosilier (Sartono, 2005). Obat generik Gliseril guaiakolat termasuk dalam jenis obat batuk basah, yaitu obat batuk untuk batuk yang memiliki ciri
berlendir, dahak mudah dikeluarkan, terasa ringan, dan tidak begitu sering intensitas
batuknya. Khasiat obat ini adalah mengeluarkan lendir di kerongkongan agar jalan
napas terbebas dari zat-zat asing (Widodo, 2004).
2.7.2 Farmakologi
Guaifenesin (gliseril guaiakolat) adalah derivat guaiakol yang banyak digunakan sebagai ekspektoran dalam berbagai jenis sediaan batuk. Pada dosiss
tinggi bekerja merelaksasi otot (Tan danRaharjo, 2007).
Penggunaan gliseril guaiakolat ini hanya didasarkan tradisi dan kesan
subyektif pasien dan dokter. Belum ada bukti bahwa obat bermanfaat pada dosis yang diberikan. Efek samping yang mungkin timbul dengan dosis besar, berupa kantuk, mual, dan muntah (Setiabudy, 2007).
2.8 Metode Penetapan Kadar Secara Spektroforometri Ultra Violet (UV) Spektroforometer UV-Vis adalah pengukuran intensitas sinar ultraviolet dan cahaya tampak yang diabsorbsi oleh sampel. Sinar ultraviolet dan cahaya tampak memiliki energi yang cukup untuk mempromosikan elektron pada kulit terluar ke tingkat energi yang lebih tinggi (Dachriyanus, 2004).
hanya sedikit informasi tentang struktur yang bisa didapatkan dari spektrum ini. Tetapi spektrum ini sangat berguna untuk pengukuran secara kuantitatif.
Konsentrasi dari senyawa (analit) di dalam larutan bisa ditentukan dengan mengukur absorban pada panjang gelombang tertentu dengan menggunakan hukum Lambert-Beer. Sinar ultraviolet berada pada panjang gelombang 200-400
nm(Dachriyanus, 2004).
Penggunaan utama spektrofotometri UV-Vis adalah dalam analisis
kuantitatif, yaitu dengan cara membandingkan absorban sampel terhadap absorban larutan standar yang konsentrasinya diketahui, diukur pada kondisi yang sama (Satiadarma, 2004).
Apabila dalam alur radiasi spektrofotometer terdapat senyawa yang mengabsorpsi radiasi, akan terjadi pengurangan kekuatan radiasi yang mencapai detektor. Parameter kekuatan energi radiasi khas yang diabsorpsi oleh molekul
adalah absorban (A) yang dalam batas konsentrasi rendah nilainya sebanding dengan konsentrasi zat yang mengabsorpsi radiasi. Penentuan kadar senyawa
organik yang mengabsorpsi radiasi UV-Vis penggunaannya cukup luas. Konsentrasi kerja larutan analit umumnya 10-20 μg/ml, tetapi untuk senyawa yang nilai absorptivitasnya besar dapat diukur pada konsentrasi yang lebih rendah
(Satiadarma, 2004).
Instrumen Spektrofotometer UV pada dasarnya terdiri atas lima komponen pokok,
1. Sumber energi radiasi
Sumber energi radiasi yang biasa digunakan adalah sebuah lampu pijar
dengan kawat terbuat dari wolfram (Day dan Underwood, 2002). Lampu deuterium, lampu pijar tugsten dan lampu halogen yang biasa dipakai sebagai sumber radiasi untuk daerah ultraviolet (Satiadarma, 2004).
2. Monokromator
Cara kerjanya seperti prinsip prisma yaitu bila seberkas cahaya menembus
antar muka antara dua media yang berbeda misalnya udara dan kaca, terjadilah pembengkokan, yang disebut pembiasan (refraksi), jauhnya pembengkokan ini bergantung pada indeks bias kaca. Indeks bias ini berbeda–beda menurut
panjang gelombang cahaya. Akibat bervariasinya indeks bias dengan panjang gelombang itu, prisma mampu mendispersikan atau menebarkan berkas cahaya putih menjadi suatu spektrum warna (Day dan Underwood, 2002).
Monokromator digunakan untuk memperoleh sumber sinar yang monokromatis. Alatnya berupa prisma ataupun grating. Untuk mengarahkan
sinar monokromatis yang diinginkan dari hasil penguraian ini dapat digunakan celah (Khopkar, 1990).
Bahan prisma untuk instrumen spektrofotometer visibel adalah dari prisma
kaca, sedangkan kuarsa merupakan bahan prisma untuk instrumen spektrofotometer ultraviolet, inframerah dekat, dan visibel (Day dan
3. Sel (wadah sampel/kuvet)
Sel haruslah meneruskan energi radiasi dalam daerah spektral yang
diinginkan, jadi digunakan sel kaca untuk visibel, sedangkan sel kuarsa atau kaca silika untuk daerah ultraviolet (Day dan Underwood, 2002). Sel yang biasa digunakan berbentuk persegi, tetapi bentuk silinder juga dapat digunakan.
Kuvet/sel yang tertutup harus digunakan untuk pelarut organik (Khopkar, 1990).
4. Detektor
Peran detektor adalah memberikan respon terhadap cahaya pada berbagai panjang gelombang (Khopkar, 1990). Detektor adalah alat yang menerima
sinyal dalam bentuk radiasi elektromagnetik, mengubah dan meneruskannya dalam bentuk sinyal listrik kerangkaian sistem penguat elektronika. Dengan demikian sinyal radiasi yang terdeteksi itu dapat diukur kekuatannya
(Satiadarma, 2004). Secara umum, detektor fotolistrik digunakan dalam daerah tampak dan ultraviolet, detektor fotolistrik yang paling sederhana adalah
tabung foto (Day dan Underwood, 2002). 5. Penguat dan pembacaan
Sebuah resistor beban yang besar yang seri dengan sebuah tabung foto
diberi daya radiasi yang disuplai ke katoda mengalir arus sebesar 1μA (10-6 A) dalam rangkaian, jika resistor mempunyai nilai sebesar 1 MΩ (106), menurut
voltmeter itu akan menjadi bagian dari rangkaian, dengan membangun suatu cabang pararel terhadap resistor, karena resistansi sebuah voltmeter yang khas
sangat rendah bila dibandingkan 106 ohm, maka sebagian besar sekali dari arus itu akan mengabaikan resistansi yang besar dan mengalir lewat voltmeter, dan voltase melintasi resistor, meskipun diukur dengan benar, adanya tidak lagi 1V,
tetapi barangkali hanya beberapa milivolt, sehingga spektrofotometer UV menggunakan sebuah penguat (amplifier) dengan resistansi masukan yang
tinggi sehingga rangkaian tabung foto tidak terserap habis.
Voltase pada tahanan beban digunakan untuk mengendalikan suatu rangkaian yang menarik dayanya dari suatu sumber bebas yang mempunyai
BAB III
METODE PENGUJIAN
3.1 Tempat Pelaksanaan Penetapan kadar
Penetapan kadar ini dilakukan di Ruang Laboratorium yang terdapat di
Industi PT. Kimia Farma (Persero) Tbk. Plant Medan yang beralamat di Jl. TanjungMorawa Km.9 No. 59 Medan.
3.2 Alat
Alat-alat yang digunakan adalah kertas perkamen, spatula, timbangan analitik eletrik, labu tentukur 100 ml dan 50 ml, beker gelas, gelas ukur, pipet
tetes, pipet volum 2 ml, Ultrasonic digital, seperangkat alat Spektofotometri UV-Visible Merk Agilent Type 8453 E.
3.3 Bahan
Bahan-bahan yang digunakan adalah aquadem bebas CO2, gliseril guaiakolat Baku Pembanding Farmakope Indonesia (BPFI), tablet gliseril
guaiakolat.
3.4 Pembuatan Larutan Pereaksi 3.4.1 Pengencer
Pengencer dengan menggunakan larutan aquadem bebas CO2 dibuat dengan cara aquadem dipanaskan hingga mendidih kemudian di ultrasonic untuk
3.4.2 Pengambilan Sampel Uji
Dari 3 batch diambil masing-masing dari batch sebanyak 10 tablet,
dihitung bobot masing-masing tablet dan diperoleh bobot rata-ratanya yaitu sebesar: 303,7 mg, 299,5 mg dan 298,3 mg.
3.4.3 Larutan Standar
Ditimbang seksama 100 mg gliseril guaiakolat Baku Pembanding Farmakope Indonesia, dimasukkan ke dalam labu tentukur 100 ml, ditambahkan
aquadem bebas CO2 50 ml, lalu dilarutkan dengan menggunakan alat Ultrasonic
digital selama 15 menit, ditambahkan dengan pengencer sampai garis tanda batas. Kemudian dipipet 2 ml, dimasukkan ke dalam labu tentukur 50 ml, lalu
ditambahkan dengan aquadem bebas CO2 sampai garis tanda batas (larutan A). 3.4.4 Larutan Uji
Sampel digerus sampai halus dari 10 tablet gliseril guaikolat (1 batch)
yang telah dihitung bobot rata-ratanya, timbang bobot sampel setara dengan bobot rata-rata penimbangan, dimasukkan ke dalam labu tentukur 100 ml, ditambahkan
aquadem bebas CO2 50 ml, lalu dilarutkan dengan menggunakan alat Ultrasonic
digital selama 15 menit, ditambahkan dengan pengencer sampai garis tanda. Kemudian dipipet 2 ml, dimasukkan ke dalam labu tentukur 50 ml, lalu
ditambahkan dengan aquadem bebas CO2 sampai garis tanda (larutan B).
3.5 Cara Penetapan Kadar
2. Klik program Spektofotometri Ultra Violet (UV) yang terdapat di komputer. 3. Klik menu Quantification, masukkan panjang gelombang maksimum (274
nm) serta jarak batas atas dan batas bawah panjang gelombang (200 nm dan 400 nm).
4. Ketik rentang area pengukuran, kemudian klik ok.
5. Tunggu selama 15 menit sampai mesin stabil.
6. Ukur larutan pengencer (blanko) terlebih dahulu, isikan ke dalam kuvet.
7. Klik blank, lalu spektrum keluar.
8. Ukur larutan standar (larutan A), isikan kedalam kuvet.
9. Klik standard, lalu procosed spektrum standard dan calibration keluar, serta
6 buah absorbansi keluar di dalam tabel, dalam perhitungan kadar digunakan absorbansi rata-ratanya.
10. Keluarkan kuvet dari tempat pengukuran dan bilas.
11. Ukur larutan uji (larutan B), isikan kedalam kuvet.
12. Klik sampel, lalu overhaid sample spectra keluar, serta 2 buah absorbansi
keluar di dalam tabel, dalam perhitungan kadar digunakan absorbansi rata-ratanya.
Perhitungan penetapan kadar dapat dilakukan dengan menggunakan rumus sebagai berikut:
C =
Dosis
Keterangan:
C : Kadar gliseril guaiakolat BPFI dalam g per ml
Au : Serapan larutan uji
As : Serapan larutan baku Ws : Berat baku pembanding
Wr : Berat sampel rata-rata Wu : Berat uji
BAB IV
HASIL DAN PEMBAHASAN 4.1 Hasil
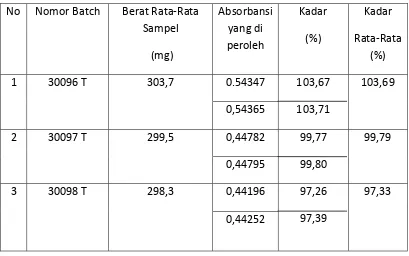
Dari pengujian kadar gliseril guaiakolat secara spektrofotometri UV diperoleh kadar rata-rata gliseril guaiakolat sebagai berikut ( Tabel 1 ).
Tabel 1:
Penetapan kadar secara spektrofotometri ultraviolet merupakan salah satu prosedur tetap metode yang digunakan sebagai penetapan kadar untuk produk
satu bentuk uji dalam rangka pemastian mutu produk tablet yang dikonsumsi oleh masyarakat. Dari hasil percobaan penetapan kadar gliseril guaiakolat dalam
sediaan tablet dengan menggunakan spektrofotometri UV, diketahui kadar rata-ratanya sebagai berikut:
1. Batch 30096 T: 103,69%
2. Batch 30097 T: 99,79% 3. Batch 30098 T: 97,33%
Menurut Farmakope Indonesia Edisi ke-IV, rentang kadar yang diperbolehkan untuk gliseril guaiakolat adalah tidak kurang dari 90,0% dan tidak lebih dari 110,0% dari jumlah yang tertera pada etiket. Maka kadar gliseril
guaiakolat dalam sediaan tablet PT Kimia Farma (Persero) Tbk Plant Medan memenuhi persyaratan.
Perbedaaan kadar dapat terjadi karena masing-masing tablet yang
ditimbang tidak tepat sama, sehingga perhitungan kadar memperoleh hasil yang berbeda. Selain itu, perbedaan kadar dapat terjadi apabila sampel yang digunakan
tidak tercampur homogen. Menurut Farmakope Indonesia Edisi IV, tablet harus memenuhi uji keseragaman bobot untuk menjamin keseragaman bobot tiap tablet yang dibuat. Tablet yang bobotnya seragam diharapkan memiliki kandungan
bahan obat yang sama, sehingga mempunyai efek terapi yang sama. Selain uji keseragaman bobot yang dimaksudkan untuk mengetahui keseragaman sediaaan,
merata. Penyimpangan yang terjadi dapat mempengaruhi dosis bahan obat tiap tablet (Martin, dkk., 1983).
Menurut Farmakope Indonesia Edisi IV, tablet gliseril guaiakolat ditetapkan dengan metode KCKT (Kromatografi Cair Kinerja Tinggi). Namun penetapan kadar tablet gliseril guaiakolat pada industri PT Kimia Farma Tbk.
BAB V
KESIMPULAN DAN SARAN 5.1 Kesimpulan
Penetapan kadar gliseril guaiakolat dalam sediaan tablet yang diproduksi PT Kimia Farma Tbk Plant Medan memenuhi persyaratan yang tertera pada
Farmakope Indonesia Edisi ke-IV, yaitu tidak kurang dari 90,0% dan tidak lebih dari 110,0% dari jumlah yang tertera pada etiket.
5.2 Saran
Pada penetapan kadar gliseril guaiakolat ini, hanya berasal dari satu pabrik industri obat saja, maka diharapkan kepada penulis selanjutnya untuk
DAFTAR PUSTAKA
Anif, M. (1991). Apa yang Perlu Diketahui Tentang Obat. Yogyakarta: Gajah Mada University Press. Hal. 3.
Anif, M. (2000). Prinsip Umum Dan Dasar Farmakologi. Yogyakarta: Gajah Mada University Press. Hal.77, 78.
Anief. (1987). Ilmu Meracik Obat. Yogyakarta: Gajah Mada University Press. Hal. 211.
Ansel, H. C. (1989). Pengatar Bentuk sediaan Farmasi.Edisi 4. Jakarta: UI Press. Hal. 244-255, 261-272.
Dachriyanus. (2004). Analisis Struktur Senyawa Organik Secara Spektroskopi. Padang: Andalas University Press. Hal. 1, 7, 8.
Day, R.A. dan Underwood, A.L. (2002). Analisis Kimia Kuantitatif. Edisi Keenam. Penerjemah: A. Hadyana Pudjaatmaka. Jakarta: Erlangga. Hal. 397–404.
Dirjen, POM. (2006), Cara Pembuatan Obat yang Baik. Jakarta: Badan POM. Hal. 5, 77, 98, 237.
Dirjen POM. (1995). Farmakope Indonesia. Edisi Ke IV. Jakarta: Departemen Kesehatan RI. Hal. 421, 422.
Irianto, K. (2004). Struktur Dan Fungsi Tubuh Manusia Untuk Para Medis. Bandung: Yrama Widya. Hal. 219.
Jas, A. (2007). Perihal Obat dengan Berbagai Jenis Dan Bentuk Sediaannya. Medan: USU Press. Hal. 2, 3.
Khopkar, S.M. (1990). Konsep Dasar Kimia Analitik. Penerjemah: Saptorahardjo, A. Jakarta: UI Press. Hal. 215, 216, 217.
Martin, A., Swarbriek J., Cammarata, A. (1983). Farmasi Fisik, Dasar-Dasar Kimia Fisika Dalam Ilmu Farmaset. Diterjemahkan Oleh Yoshita. Edisi 3. Jakarta: Universitas Indonesia Press. Hal. 845-848.
Mutschler, E. (1991). Dinamika Obat Farmakologi dan Toksikologi. Bandung: Penerbit ITB. Hal. 191, 518.
Rohman, A. (2007). Kimia Farmasi Analisis. Yogyakarta: Pustaka Pelajar. Hal. 242, 245, 246.
Sartono. (2005). Obat dan Anak. Bandung: Penerbit ITB. Hal. 12.
Satiadarma, K. (2004). Asas Pengembangan Prosedur Analisis. Surabaya: Airlangga University Press. Hal. 87-90, 94-97.
Setiabudy, R. (2007). Farmakologi Dan Terapi. Edisi Lima. Jakarta: Penerbit FK UI. Hal. 531.
Siregar, C.J.P. (2010). Teknologi Farmasi Sediaan Tablet: Dasar–Dasar Praktis. Jakarta: EGC. Hal. 15, 16, 123, 145, 161, 605, 647.
Tan, H.T., dan Raharjo, K. (2007). Obat-Obat Penting Edisi Enam cetakan pertama. Jakarta: Penerbit PT. Elex Media Komputindo. Hal.1, 661, 665. Widodo, R. (2004). Panduan Keluarga Memilih Dan Menggunakan Obat.
LAMPIRAN
Lampiran 1
PerhitunganPenetapan Kadar Gliseril GuaiakolatDi Dalam Tablet Kadar gliseril guaiakolat dihitung dengan rumus sebagai berikut:
C =
Dosis
Keterangan:
C : Kadar gliseril guaiakolat BPFI dalam g per ml
Au : Serapan Larutan Uji As : Serapan Larutan Baku Ws : Berat Baku Pembanding
Wr : Berat Sampel Rata-Rata Wu : Berat Uji
St BPFI : Kadar standarBaku Pembanding Farmakope Indonesia
Diketahui: Batch 30096 T Au1 : 0,54347
Wr : 303,7 mg Batch 30097 T
Au1 : 0.44789 Au2 : 0.44795 As : 0,44596
Wr : 299,5 mg Batch 30098 T
Au1 : 0,44196 Au2 : 0,44252 As : 0,45159
Wr : 298,3 mg Ws : 100 mg Wu : 300 mg
St BPFI: 99.98%
Kadar Batch 30096 T1
:
= 103,67%
100
Kadar Batch 30096 T2
:
= 103,71%
Kadar Batch 30097 T1
:
= 99,77%
100
Kadar Batch 30097 T2
:
= 99,80%
100
Kadar rata-rata batch 30097 T yang diperoleh: (99,77 + 99,80) = 99,79 %2
Kadar Batch 30098 T1
:
= 97,26%
100
Kadar Batch 30098 T2
:
= 97,39%
100
Kadar rata-rata batch 30098 T yang diperoleh:(97,26 + 97,39) = 97,33 % 2
Lampiran 2