PENETAPAN KADAR CAMPURAN ISONIAZID DAN VITAMIN B6 DALAM SEDIAAN TABLET SECARA SPEKTROFOTOMETRI ULTRAVIOLET DENGAN PERHITUNGAN
MULTIKOMPONEN DAN PERSAMAAN MATRIKS
OLEH
WARDAH KUMALA SARI NIM 071524081
PROGRAM EKSTENSI SARJANA FARMASI FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
PENETAPAN KADAR CAMPURAN ISONIAZID DAN VITAMIN B6 DALAM SEDIAAN TABLET SECARA SPEKTROFOTOMETRI ULTRAVIOLET DENGAN PERHITUNGAN
MULTIKOMPONEN DAN PERSAMAAN MATRIKS
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH
WARDAH KUMALA SARI NIM 071524081
PROGRAM EKSTENSI SARJANA FARMASI FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
PENGESAHAN SKRIPSI
PENETAPAN KADAR CAMPURAN ISONIAZID DAN VITAMIN B6
DALAM SEDIAAN TABLET SECARA SPEKTROFOTOMETRI ULTRAVIOLET DENGAN PERHITUNGAN MULTIKOMPONEN
DAN PERSAMAAN MATRIKS
OLEH
WARDAH KUMALA SARI NIM 071524081
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi
Universitas Sumatera Utara Pada Tanggal Maret 2011
Pembimbing I, Panitia Penguji,
Drs. Muchlisyam, M.Si., Apt Drs.Chairul A.Dalimunthe,M.Sc.,Apt NIP 195006221980011001 NIP 194907061980021001
Pembimbing II, Drs. Muchlisyam, M.Si., Apt NIP 195006221980011001
Drs. Fathur Rahman Harun, M.Si., Apt Dra. Sudarmi, M.Si., Apt NIP 195201041980031002 NIP 195409101983032001
Drs. Maralaut Batubara, M.Phill.,Apt NIP 195101311976031001
Dekan
KATA PENGANTAR
Puji syukur saya ucapkan kepada Allah SWT yang telah memberikan
rahmat dan nikmat-Nya kepada saya sehingga saya dapat menyelesaikan skipsi ini
dengan baik, serta sholawat dan salam tidak lupa saya ucapkan pada junjungan
kita Nabi Besar Muhammad SAW yang telah membawa kita dari alam yang gelap
gulita ke alam yang terang benderang dengan penuh dengan ilmu pengetahuan,
semoga di yaumil akhir kelak kita mendapat syafa’atnya Amin.
Penulisan skripsi ini merupakan salah satu tugas dan kewajiban bagi setiap
mahasiswa khususnya di Fakultas Farmasi Universitas Sumatera Utara sebagai
syarat untuk meraih gelar Sarjana Farmasi.
Saya menyadari dalam penulisan skripsi ini banyak mengalami kesulitan
dan hambatan. Namun berkat bimbingan dan arahan dari berbagai pihak, maka
penelitian ini dapat terselesaikan. Untuk itu pada kesempatan ini saya ingin
berterima kasih kepada:
1. Bapak Prof. Dr. Sumandio Hadisaputra, Apt selaku Dekan Fakultas
Farmasi.
2. Bapak /Ibu staf pengajar Fakultas Farmasi USU yang telah mendidik
penulis selama dalam perkuliahan.
3. Ibu Dra. Siti Nurbaya, Apt selaku Penasehat Akademik penulis yang telah
memberikan bimbingan kepada penulis selama ini.
4. Bapak Drs. Muchlisyam, M.Si., Apt selaku pembimbing I, yang telah
banyak memberi saya banyak arahan dan bimbingan dalam penyusunan
5. Bapak Drs. Fathur Rahman Harun, M.Si., Apt selaku pembimbing II yang
telah banyak memberikan petunjuk dan arahan-arahan dari awal hingga
skripsi ini selesai dengan baik.
6. Asisten Laboratorium Kimia Farmasi Kuanlitatif, teman-teman penulis
angkatan ekstensi 2007, senior, junior serta seluruh pegawai Fakultas
Farmasi Universitas Sumatera Utara yang tidak dapat disebutkan satu
persatu disini yang telah banyak membantu penulis.
7. Teristimewa kepada Ayahanda H. Hasanuddin Thariq dan Ibunda Hj.
Habsyah yang senantiasa mendo’akan saya sepanjang waktu dan
memberikan bantuan moril dan materil sehingga saya dapat menyelesaikan
pendidikan dengan baik.
8. Abangda M. Reza Pahlevi, S.Hi., Ahmad Hafidzullah Amin, S.Hi., M.A.,
kakanda Fatmawati, S.Pdi., Nurhartatik Khairiyah, S.Pd dan adinda
tersayang Maulana Putra Jauhari yang selalu memberikan semangat pada
saya.
Saya menyadari penyusunan skripsi ini tidak terlepas dari
kesalahan-kesalahan. Kesalahan yang terdapat dari isi skripsi ataupun dari segi tata bahasa,
saya harapkan kritik dan saran yang membanngun agar skripsi ini dapat
bermanfaat dan dapat memperkaya khazanah ilmu pengetahuan.
Medan, Maret 2011
Penulis
PENETAPAN KADAR CAMPURAN ISONIAZID DAN VITAMIN B6
DALAM SEDIAAN TABLET SECARA SPEKTROFOTOMETRI ULTRAVIOLET DENGAN PERHITUNGAN MULTIKOMPONEN
DAN PERSAMAAN MATRIKS
ABSTRAK
Isoniazid merupakan obat yang cukup efektif dalam pengobatan tuberkulosis. Dalam perdagangan Isoniazid sering dikombinasi dengan Vitamin B6 yang bertujuan untuk mencegah efek samping dari Isoniazid berupa neuritis
perifer. Kombinasi bahan aktif tersebut dapat menimbulkan masalah dalam analisis kuantitatif untuk kontrol kualitas sediaan. Pada penelitian ini dilakukan penetapan kadar sediaan tablet kombinasi Isoniazid dan Vitamin B6 secara
spektrofotometri Ultraviolet dengan perhitungan multikomponen dan persamaan matriks mempergunakan pelarut HCl 0,1N yang diukur serapannya pada panjang gelombang maksimum masing-masing komponen yaitu INH 266 nm dan Vitamin B6 290 nm.
Diperoleh kadar INH untuk tablet Pehadoxin® (PT. Phapros) sebesar 103,11% ± 1,54, tablet Niacifort – 6® (PT. Ikapharmindo Putramas) 97,62% ± 0,95, dan tablet Beniazid® (PT. Rocella) 99,86% ± 0,26 dan kadar Vitamin B6
untuk tablet Pehadoxin® (PT. Phapros) sebesar 101,91% ± 2,78, tablet Niacifort – 6® (PT. Ikapharmindo Putramas) 103,90% ± 1,62, dan tablet Beniazid® (PT. Rocella) 97,73% ± 1,61. Hal ini menunjukkan bahwa sediaan tablet bernama dagang yang dianalisis memenuhi persyaratan kadar yang tercantum dalam Farmakope Indonesia edisi IV (1995) yaitu mengandung tidak kurang dari 90,0% dan tidak lebih dari 110,0% dari jumlah yang tertera pada etiket untuk Isoniazid, dan untuk Piridoksin Hidroklorida, mengandung tidak kurang dari 95,0% dan tidak lebih dari 115,0% dari jumlah yang tertera pada etiket.
Uji validasi metode dilakukan dengan membuat 3 konsentrasi analit dengan rentang spesifik 80%, 100% dan 120%, masing-masing dengan 3 replikasi. Hasil persen recovery didapat untuk Isoniazid; Kadar rata-rata 97,43%, Standar Deviasi (SD) 2,61 dan Relatif Standar Deviasi (RSD) 2,68% dan untuk Vitamin B6; Kadar rata-rata 98,93%, Standar Deviasi (SD) 1,06 dan Relatif
Standar Deviasi (RSD) 1,07%. Nilai RSD yang diperoleh telah memenuhi syarat RSD yaitu 5-15% untuk senyawa-senyawa dengan kadar sekelumit. Dari hasil penelitian disimpulkan metode Spektrofotometri Ultraviolet secara perhitungan persamaan multikomponen dan matriks memberikan ketepatan dan ketelitian yang baik.
MIXED LEVEL OF DETERMINATION OF INH AND VITAMIN B6 IN THE TABLET BY ULTRAVIOLET SPECTROPHOTOMETRY WITH
MULTICOMPONENT CALCULATION AND MATRIX EQUATION
ABSTRACT
Isoniazid is a drug that is effective in the treatment of tuberculosis. In trading Isoniazid is often combined with Vitamin B6 which aims to prevent side effects of Isoniazid in the form of peripheral neuritis. The combination of active ingredients that can cause problems in quantitative analysis for quality control preparations. In this research, determination of the combination tablet Vitamin B6 and Isoniazid by Ultraviolet spectrophotometry with multicomponent calculation and use the matrix equation use HCl 0.1 N as measured at a wavelength of maximum absorbance of each component such as INH and Vitamin B6 266 nm, 290 nm.
Retrieved levels of INH for Pehadoxin ® tablets (PT. Phapros) amounted to 103.11% ± 1.54, tablet Niacifort - 6 ® (PT Ikapharmindo Putramas) 97.62% ± 0.95, and tablets Beniazid ® (PT. Rocella ) 99.86% ± 0.26 and levels of vitamin B6 for Pehadoxin ® tablet (PT. Phapros) amounted to 101.91% ± 2.78, tablet Niacifort - 6 ® (PT Ikapharmindo Putramas) 103.90% ± 1, 62, and tablet Beniazid ® (PT Rocella) 97.73% ± 1.61. This indicates that the tablets were analyzed trade name meets the requirements stated in the levels of Indonesian Pharmacopoeia IV edition (1995) which contains not less than 90.0% and not more than 110.0% of the amount listed on the label to Isoniazid, and to pyridoxine Hydrochloride, containing not less than 95.0% and not more than 115.0% of the amount listed on the label.
Test method validation is done by creating 3 concentration of the analyte with a specific range of 80%, 100% and 120%, respectively with 3 replication. Results per cent recovery obtained for Isoniazid; levels on average 97.43%, Standard Deviation (SD) 2.61 and Relative Standard Deviation (RSD) 2.68% and for vitamin B6; levels on average 98.93%, Standard deviation (SD) 1.06 and Relative Standard Deviation (RSD) 1.07%. RSD values obtained in compliance with the requirements of 5-15% RSD for the compounds with trace levels. The final conclusion Ultraviolet Spectrophotometric method for the calculation of multicomponent and matrix equations provide good accuracy and precision.
DAFTAR ISI
HALAMAN
JUDUL ... i
LEMBAR PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
BAB I : PENDAHULUAN ...
1
1
1.1 Latar Belakang ... 11.2 Perumusan Masalah ... 2
1.3 Hipotesis ... 3
1.4. Tujuan ... 3
BAB II : TINJAUAN PUSTAKA ... 4
2.1 Uraian Bahan ... 4
2.1.1 ISONIAZIDE (INH) ... 4
2.1.1.1 Sifat Fisikokimia ... 4
2.1.1.2 Kegunaan ... 5
2.1.1.3 Efek Samping ... 5
2.1.1.5 Farmakologi ... 5
2.1.2 VITAMIN B6 ... 6
2.1.2.1 Sifat Fisikokimia ... 6
2.1.2.2 Kegunaan ... 7
2.1.2.3 Efek Samping ... 7
2.1.2.4 Dosis ... 7
2.1.2.5 Farmakologi ... 7
2.2 Spektrofotometri Ultraviolet... 7
2.2.1 Teori Spektrofotometri Ultraviolet ... 7
2.2.2 Hukum Lambert Beer ... 9
2.2.3 Penggunaan Spektrofotometri Ultraviolet ... 10
2.2.4 Peralatan untuk Spektrofotometri ... 15
2.3 Validasi ... 16
BAB III : METODOLOGI PENELITIAN ... 19
3.1 Lokasi Penelitian ... 19
3.2 Metode Penelitian ... 19
3.3 Alat ... 19
3.4 Bahan ... 19
3.5 Metode Pengambilan Sampel ... 19
3.6 Pembuatan Pereaksi ... 20
3.6.1 Pembuatan Pelarut HCl 0,1 N ... 20
3.7 Pembuatan Larutan Induk Baku BPFI ... 20
3.7.1 Pembuatan Larutan Induk Baku Isoniazid BPFI ... 20
3.8 Penentuan Panjang Gelombang Maksimum ... 21
3.8.1 Penentuan Panjang Gelombang Maksimum Isoniazid BPFI ... 21
3.8.2 Penentuan Panjang Gelombang Maksimum Vitamin B6 BPFI ... 21
3.9 Pembuatan Kurva Serapan Gabungan (Overlay) Isoniazid BPFI dan Vitamin B6 ... 21
3.10 Penentuan Absorptivitas (α) ... 21
3.10.1
Penentuan Absorptivitas (α) Isoniazid BPFI
21
3.10.2 Penentuan Absorptivitas (α) Vitamin B6 BPFI ... 22
3.11 Penetapan Kadar Sampel ... 22
3.12 Uji Validasi Metode Analisis ... 24
3.12.1 Uji Akurasi ... 24
3.12.2 Penentuan Uji Presisi ... 25
3.12.3 Analisis Data Secara Statistik ... 25
BAB IV : HASIL DAN PEMBAHASAN ... 27
4.1 Penentuan Panjang Gelombang Maksimum ... 27
4.2 Kurva Serapan Gabungan (Overlay) Isoniazid BPFI dan Vitamin B6 (10:1) ... 30
4.3 Penentuan Absorbtivitas (α) Isoniazid BPFI dan Vitamin B6 ... 31
4.4 Penetapan Kadar Sampel ... 32
4.5.1 Penentuan Uji Akurasi dengan Parameter Persen Recovery Menggunakan Metode Penambahan Baku
(Standard Addition Method) ... 33
3.5.2 Penentuan Uji Presisi dengan Parameter Relatif Standar Deviasi (RSD) ... 35
BAB V KESIMPULAN DAN SARAN ... 36
5.1 Kesimpulan ... 36
5.2 Saran ... 36
DAFTAR PUSTAKA ... 37
DAFTAR TABEL
Tabel 1. Data absorptivitas Isoniazid (20 µ g/ml) dan Vitamin B6
(2 µ g/ml) secara persamaan multikomponen ... 31 Tabel 2. Data absorptivitas Isoniazid (20 µ g/ml) dan Vitamin B6
(2 µ g/ml) secara matriks ... 31 Tabel 3. Hasil penetapan kadar Isoniazid dalam sediaan tablet ... 32 Tabel 4. Hasil penetapan kadar VitaminB6 dalam sediaan tablet ... 32
Tabel 5. Hasil pengujian persen recovery Isoniazid dalam tablet Pehadoxin® (PT. Phapros) dengan metode penambahan baku
(standard addition method) ... 34 Tabel 6. Hasil pengujian persen recovery Vitamin B6 dalam tablet
Pehadoxin® (PT. Phapros) dengan metode penambahan baku
DAFTAR GAMBAR
Gambar 1. Kurva serapan Isoniazid BPFI, konsentrasi 10 µ g/ml dalam
larutan HCl 0,1 N. Panjang gelombang maksimum 266 nm ... ... … 28 Gambar 2. Kurva serapan Vitamin B6 BPFI, konsentrasi 8 µ g/ml dalam
larutan HCl 0,1 N. Panjang gelombang maksimum 290 nm... 29 Gambar 3. Kurva serapan gabungan (overlay) Isoniazid BPFI dan
DAFTAR LAMPIRAN
Halaman Lampiran 1. Data absorptivitas ... 39 Lampiran 2. Perhitungan Konsentrasi Pengukuran Isoniazid dan Vitamin B6 ... .... 40
Lampiran 3. Perhitungan Absorptivitas (α) secara Persamaan Multikomponen....41
Lampiran 4. Perhitungan Absorptivitas (α) secara Matriks ... .. 42 Lampiran 5. Contoh Perhitungan Penimbangan Sampel ... .. 43 Lampiran 6. Hasil Pengukuran Absorbansi Campuran Isoniazid dan
Vitamin B6dalam sediaan tablet diukur pada λ 266 nm dan
λ 290 nm . ... ... 44 Lampiran 7. Analisis Data Statisik untuk Menghitung Kadar
Isoniazid dan Vitamin B6 dalam sampel ... ... 47
Lampiran 8. Data Hasil Penetapan Kadar Isoniazid dan Vitamin B6
dalam Sediaan Tablet Pehadoxin® (PT. Phapros) Secara
Perhitungan Multikomponen dan Matriks ... ... 49 Lampiran 9. Data Hasil Penetapan Kadar Isoniazid dan Vitamin B6 dalam
Sediaan Tablet Niacifort – 6® (PT. Ikapharmindo Putramas)
Secara Perhitungan Multikomponen dan Matriks ... ... 50 Lampiran 10. Data Hasil Penetapan Kadar Isoniazid dan Vitamin B6
dalam Sediaan Tablet Beniazid® (PT. Rocella) Secara
Perhitungan Multikomponen dan Matriks ... ... 51 Lampiran 11. Contoh Perhitungan Sampel Uji Akurasi dengan Parameter
Persen Recovery Menggunakan Metode Penambahan Baku
(Standard Addition Method) ... ... 52 Lampiran 12. Hasil Uji Akurasi dengan Parameter Persen Recovery pada
Sampel Tablet Pehadoxin® (PT. Phapros) ... ... 56
Lampiran 13. Data Hasil Persen Recovery Isoniazid dan Vitamin B6 pada
Sampel Tablet Pehadoxin® (PT. Phapros) dengan Metode
Lampiran 14. Contoh Perhitungan Persen Recovery Isoniazid dan Vitamin B6
pada Sampel Tablet Pehadoxin® (PT. Phapros) dengan
Metode Penambahan Baku (Standard Addition Method).... 60 Lampiran 15. Analisis Data Uji Presisi pada Tablet Pehadoxin®
(PT. Phapros) ... ... 61 Lampiran 16. Analisis Data Uji Presisi pada tablet Niacifort – 6®
(PT. Ikapharmindo Putramas) ... ... 63 Lampiran 17. Analisis Data Uji Presisi pada tablet Beniazid (PT. Rocella) ... 66 Lampiran 18. Analisis Data Uji Presisi Hasil Persen Recovery Isoniazid
Dan Vitamin B6 dalam Sampel Tablet Pehadoxin®
(PT. Phapros) dengan Metode Penambahan Baku
(Standard Addition Method ) ... 68
Lampiran 19. Daftar Spesifikasi Sampel ... 74 Lampiran 20. Nilai Distribusi t ... ... 75 Lampiran 21. Perhitungan Membuat HCl 0,1N ... 76 Lampiran 22. Gambar Sampel Kombinasi Isoniazid 100 mg dan
Vitamin B6 10 mg dalam sediaan tablet ... .... 77
PENETAPAN KADAR CAMPURAN ISONIAZID DAN VITAMIN B6
DALAM SEDIAAN TABLET SECARA SPEKTROFOTOMETRI ULTRAVIOLET DENGAN PERHITUNGAN MULTIKOMPONEN
DAN PERSAMAAN MATRIKS
ABSTRAK
Isoniazid merupakan obat yang cukup efektif dalam pengobatan tuberkulosis. Dalam perdagangan Isoniazid sering dikombinasi dengan Vitamin B6 yang bertujuan untuk mencegah efek samping dari Isoniazid berupa neuritis
perifer. Kombinasi bahan aktif tersebut dapat menimbulkan masalah dalam analisis kuantitatif untuk kontrol kualitas sediaan. Pada penelitian ini dilakukan penetapan kadar sediaan tablet kombinasi Isoniazid dan Vitamin B6 secara
spektrofotometri Ultraviolet dengan perhitungan multikomponen dan persamaan matriks mempergunakan pelarut HCl 0,1N yang diukur serapannya pada panjang gelombang maksimum masing-masing komponen yaitu INH 266 nm dan Vitamin B6 290 nm.
Diperoleh kadar INH untuk tablet Pehadoxin® (PT. Phapros) sebesar 103,11% ± 1,54, tablet Niacifort – 6® (PT. Ikapharmindo Putramas) 97,62% ± 0,95, dan tablet Beniazid® (PT. Rocella) 99,86% ± 0,26 dan kadar Vitamin B6
untuk tablet Pehadoxin® (PT. Phapros) sebesar 101,91% ± 2,78, tablet Niacifort – 6® (PT. Ikapharmindo Putramas) 103,90% ± 1,62, dan tablet Beniazid® (PT. Rocella) 97,73% ± 1,61. Hal ini menunjukkan bahwa sediaan tablet bernama dagang yang dianalisis memenuhi persyaratan kadar yang tercantum dalam Farmakope Indonesia edisi IV (1995) yaitu mengandung tidak kurang dari 90,0% dan tidak lebih dari 110,0% dari jumlah yang tertera pada etiket untuk Isoniazid, dan untuk Piridoksin Hidroklorida, mengandung tidak kurang dari 95,0% dan tidak lebih dari 115,0% dari jumlah yang tertera pada etiket.
Uji validasi metode dilakukan dengan membuat 3 konsentrasi analit dengan rentang spesifik 80%, 100% dan 120%, masing-masing dengan 3 replikasi. Hasil persen recovery didapat untuk Isoniazid; Kadar rata-rata 97,43%, Standar Deviasi (SD) 2,61 dan Relatif Standar Deviasi (RSD) 2,68% dan untuk Vitamin B6; Kadar rata-rata 98,93%, Standar Deviasi (SD) 1,06 dan Relatif
Standar Deviasi (RSD) 1,07%. Nilai RSD yang diperoleh telah memenuhi syarat RSD yaitu 5-15% untuk senyawa-senyawa dengan kadar sekelumit. Dari hasil penelitian disimpulkan metode Spektrofotometri Ultraviolet secara perhitungan persamaan multikomponen dan matriks memberikan ketepatan dan ketelitian yang baik.
MIXED LEVEL OF DETERMINATION OF INH AND VITAMIN B6 IN THE TABLET BY ULTRAVIOLET SPECTROPHOTOMETRY WITH
MULTICOMPONENT CALCULATION AND MATRIX EQUATION
ABSTRACT
Isoniazid is a drug that is effective in the treatment of tuberculosis. In trading Isoniazid is often combined with Vitamin B6 which aims to prevent side effects of Isoniazid in the form of peripheral neuritis. The combination of active ingredients that can cause problems in quantitative analysis for quality control preparations. In this research, determination of the combination tablet Vitamin B6 and Isoniazid by Ultraviolet spectrophotometry with multicomponent calculation and use the matrix equation use HCl 0.1 N as measured at a wavelength of maximum absorbance of each component such as INH and Vitamin B6 266 nm, 290 nm.
Retrieved levels of INH for Pehadoxin ® tablets (PT. Phapros) amounted to 103.11% ± 1.54, tablet Niacifort - 6 ® (PT Ikapharmindo Putramas) 97.62% ± 0.95, and tablets Beniazid ® (PT. Rocella ) 99.86% ± 0.26 and levels of vitamin B6 for Pehadoxin ® tablet (PT. Phapros) amounted to 101.91% ± 2.78, tablet Niacifort - 6 ® (PT Ikapharmindo Putramas) 103.90% ± 1, 62, and tablet Beniazid ® (PT Rocella) 97.73% ± 1.61. This indicates that the tablets were analyzed trade name meets the requirements stated in the levels of Indonesian Pharmacopoeia IV edition (1995) which contains not less than 90.0% and not more than 110.0% of the amount listed on the label to Isoniazid, and to pyridoxine Hydrochloride, containing not less than 95.0% and not more than 115.0% of the amount listed on the label.
Test method validation is done by creating 3 concentration of the analyte with a specific range of 80%, 100% and 120%, respectively with 3 replication. Results per cent recovery obtained for Isoniazid; levels on average 97.43%, Standard Deviation (SD) 2.61 and Relative Standard Deviation (RSD) 2.68% and for vitamin B6; levels on average 98.93%, Standard deviation (SD) 1.06 and Relative Standard Deviation (RSD) 1.07%. RSD values obtained in compliance with the requirements of 5-15% RSD for the compounds with trace levels. The final conclusion Ultraviolet Spectrophotometric method for the calculation of multicomponent and matrix equations provide good accuracy and precision.
BAB I PENDAHULUAN
1.1Latar Belakang
Isoniazid diperkenalkan pada tahun 1952 sebagai obat yang cukup efektif
dalam pengobatan tuberkulosis dan sebagian besar penderita dapat disembuhkan
dengan obat ini (Katzung, 1998). Piridoksin HCl (Vitamin B6) ditemukan pada
tahun 1938 dalam bentuk kristal dari kulit beras maupun dari ragi (Schunack,
1998). Isoniazid dalam perdagangan sering dikombinasi dengan Vitamin B6 yang
bertujuan untuk mencegah efek samping dari Isoniazid yang berupa neuritis
perifer.
Kombinasi bahan aktif tersebut dapat menimbulkan masalah dalam
analisis kuantitatif untuk kontrol kualitas sediaan. Masalah ini disebabkan oleh
senyawa yang terkandung mempunyai sifat fisiko kimia yang hampir sama, atau
profil kurva serapan masing-masing komponen saling tumpang tindih pada daerah
tertentu sehingga serapan yang diperoleh merupakan jumlah serapan dari
masing-masing komponen tersebut.. Isoniazid dan Vitamin B6 memiliki struktur molekul
kimia yang mengandung gugus kromofor dan ausokrom.
Dalam USP 30 (2007) dan Farmakope Indonesia edisi IV (1995)
monografi sediaan tablet kombinasi Isoniazid dan Vitamin B6 belum
dicantumkan. Penetapan kadar tablet Isoniazid bentuk tunggal dapat ditentukan
dengan metode Kromatografi Cair Kinerja Tinggi (USP 30, 2007; DitJen POM,
1995), titrasi Nitrimetri (DitJen POM, 1979), titrasi Bromometri (DitJen POM,
Vitamin B6 bentuk tunggal adalah dengan metode titrasi bebas air dan
spektrofotometri UV.
Menurut Moffat (1986) Isoniazid dapat diidentifikasi secara
spektrofotometri ultraviolet dalam larutan asam dan mempunyai serapan
maksimum pada panjang gelombang 266 nm dengan A = 390a dan dalam larutan 11
basa mempunyai serapan maksimum pada panjang gelombang 298 nm sedangkan
Vitamin B6 dapat diidentifikasi dalam asam mempunyai serapan maksimum pada
panjang gelombang 290 nm dengan A = 523a dan dalam larutan buffer phospat 11
pH 6,88 mempunyai serapan maksimum pada panjang gelombang 254 nm dengan
1 1
A = 219° atau pada panjang gelombang 324 nm dengan A = 426°. 11
Berdasarkan uraian diatas maka penulis tertarik untuk menetapkan kadar
campuran Isoniazid dan Vitamin B6 dalam sediaan tablet dengan menggunakan
metode spektrofotometri ultraviolet dengan perhitungan multikomponen dan
persamaan matriks. Metode Spektrofotometri Ultraviolet memiliki beberapa
keuntungan antara lain kepekaan yang tinggi, selektifitas yang tinggi, ketelitian
yang baik, mudah dilakukan, cepat pengerjaannya dan dapat digunakan untuk
menentukan senyawa multikomponen (Munson, 1991).
Untuk menguji validasi metode, dilakukan uji akurasi (ketepatan) dengan
parameter persen recovery dengan metode penambahan baku (standard addition
method) dan uji presisi (ketelitian) dengan parameter Relatif Standar Deviasi
(RSD).
1.2Perumusan Masalah
1. Apakah kombinasi Isoniazid dan Vitamin B6 dalam bentuk sediaan tablet
perhitungan multikomponen dan persamaan matriks yang memenuhi uji
validasi metode?
2. Apakah kadar kombinasi Isoniazid dan Vitamin B6 dalam bentuk sediaan
tablet yang beredar dipasaran memenuhi persyaratan kadar yang
ditetapkan Farmakope Indonesia Edisi IV?
1.3Hipotesis
1. Metode Spektrofotometri Ultraviolet dapat digunakan untuk menetapkan
kadar kombinasi Isoniazid dan vitamin B6 dalam bentuk sediaan tablet dan
memenuhi uji validasi metode.
2. Kadar kombinasi Isoniazid dan Vitamin B6 dalam bentuk sediaan tablet yang
terdapat dipasaran memenuhi persyaratan kadar yang ditetapkan Farmakope
Indonesia Edisi IV.
1.4Tujuan
Tujuan dari penelitian ini adalah:
1. Untuk menentukan validasi spektrofotometri ultraviolet pada penetapan
kadar tablet kombinasi Isoniazid dan Vitamin B6.
2. Untuk menentukan kesesuaian kadar kombinasi Isoniazid dan Vitamin B6
yang terdapat dipasaran dengan persyaratan kadar yang ditetapkan
BAB II
TINJAUAN PUSTAKA 2.1 Uraian Bahan
2.1.1 ISONIAZIDE (INH) 2.1.1.1 Sifat Fisikokimia
Rumus Struktur :
Rumus Molekul : C6H7N3O
Berat Molekul : 137,14
Nama Kimia : Asam Isonikotinat Hidrazida
Kandungan : Tidak kurang dari 98% dan tidak lebih dari 102,0%
C6H7N3O, dihitung terhadap zat yang telah
dikeringkan.
Pemerian : Hablur putih atau tidak berwarna atau serbuk hablur
putih; tidak berbau, perlahan – lahan dipengaruhi oleh
udara dan cahaya.
Kelarutan : Mudah larut dalam air; agak sukar larut dalam etanol;
sukar larut dalam kloroform dan dalam eter.
pH : Antara 6,0 dan 7,5
Baku Pembanding : Sebelum digunakan lakukan pengeringan pada suhu
2.1.1.2 Kegunaan
Isoniazid berkhasiat tuberkulostatis paling kuat terhadap M. Tuberculosis
(dalam fase istirahat) dan bersifat bakterisid terhadap basil yang sedang tumbuh
pesat (Tjay, T.H. dan Rahardja, K., 2002)
2.1.1.3 Efek Samping
Mual, muntah, anoreksia, letih, malaise, lemah, gangguan saluran
pencernaan lain, neuritis perifer (paling sering terjadi dengan dosis
5mg/kgBB/hari), neuritis optikus, reaksi hipersensitivitas, demam, ruam, ikterus,
diskrasia darah, psikosis, kejang, sakit kepala, mengantuk, pusing, mulut kering,
gangguan BAK, kekurangan vitamin B6, hiperglikemia, asidosis metabolik,
ginekomastia, gejala reumatik, gejala mirip Systemic Lupus Erythematosus.
2.1.1.4 Dosis
Oral/i.m. dewasa dan anak-anak 1 dd 4-8 mg/kg/hari sehari atau 1 dd
300-400 mg. Profilaksis 5-10 mg/kg/hari. (Tjay, T.H. dan Rahardja, K., 2002).
2.1.1.5 Farmakologi
Isoniazid menghambat sintesis dari mycolic acid yang merupakan
komponen penting dari dinding sel mikobakteri. Resorpsinya dari usus sangat
cepat; difusinya kedalam jaringan dan cairan tubuh baik sekali, bahkan menembus
jaringan yang sudah mengeras. Didalam hati INH diasetilasi oleh enzim
asetiltransferase menjadi metabolit inaktif. PP-nya ringan sekali, plasma – t½ nya
antara 1 dan 4 jam tergantung pada kecepatan asetilasi. Eksresinya terutama
melalui ginjal (75-95% dalam 24 jam) dan sebagian besar sebagai asetilisoniazid.
2.1.2 VITAMIN B6
2.1.2.1 Sifat Fisikokimia
Rumus Struktur :
Rumus Molekul : C8H11NO3.HCI
Berat Molekul : 205,64
Nama Kimia : Piridoksol hidroklorida
Pyridoxini Hydrochloridum
Kandungan : Tidak kurang dari 98% dan tidak lebih dari 102,0%
C8H11NO3.HCI, dihitung terhadap zat yang telah
dikeringkan.
Pemeriaan : Hablur atau serbuk hablur putih atau hampir putih;
stabil di udara; secara perlahan-lahan dipengaruhi oleh
cahaya matahari.
Kelarutan : Mudah larut dalam air; sukar larut dalam etanol; tidak
larut dalam eter
pH : lebih kurang 3
Baku Pembanding : Sebelum digunakan lakukan pengeringan dalam
hampa udara diatas silika gel p selama 4 jam.
2.1.2.2 Kegunaan
Vitamin B6 selain untuk mencegah dan mengobati defisiensi vitamin B6
dengan gejala berupa kelainan kulit (dermatitis), peradangan lendir mulut dan
lidah- kelainan susunan syaraf pusat dan gangguan eritopoetik berupa anemia
hipokrom mikrositer, juga diberikan bersama vitamin B lainnya.
2.1.2.3 Efek Samping
Jarang terjadi dan berupa reaksi alergi. Penggunaan lama dari 500mg/hari
dapat mencetuskan ataxia (jalan limbung) dan neuropati serius (Tjay, T.H. dan
Rahardja, K., 2002).
2.1.2.4 Dosis
Oral selama terapi dengan antagonis-piridoksin 10-100mg (HCl) sehari,
profilaksis 2-10mg (Tjay, T.H. dan Rahardja, K., 2002).
2.1.2.5 Farmakologi
Didalam hati Vitamin B6 dengan bantuan ko-faktor riboflavin dan
magnesium diubah menjadi zat aktifnya piridoksal-5-fosfat (P5P). Zat ini
berperan penting sebagai ko-enzim pada metabolisme protein dan asam-asam
amino (Tjay, T.H. dan Rahardja, K., 2002).
2.2 Spektrofotometri Ultraviolet
2.2.1 Teori Spektrofotometri Ultraviolet
Spektrofotometer sesuai dengan namanya adalah alat yang terdiri dari
spektrometer dan fotometer. Spektrometer menghasilkan radiasi dengan panjang
gelombang tertentu dan fotometer adalah alat pengukur intensitas cahaya yang
mengukur energi secara relatif jika energi tersebut ditransmisikan, direfleksikan
atau diemisikan sebagai fungsi dari panjang gelombang (Khopkar,1990).
Spektrofotometri serapan merupakan pengukuran suatu interaksi antara
radiasi elektromagnetik dan molekul atau atom dari suatu zat kimia. Teknik yang
sering digunakan dalam analisis farmasi meliputi spektrofotometri ultraviolet,
cahaya tampak, infra merah dan serapan atom. Jangkauan panjang gelombang
untuk daerah ultraviolet adalah 190-380 nm, daerah cahaya tampak 380-780 nm,
daerah infra merah dekat 780-3000 nm, dan daerah infra merah 2,5-40 µm atau
4000-250 cm-1 ( Ditjen POM, 1995).
Radiasi ultraviolet dan sinar tampak diabsorpsi oleh molekul organik
aromatik, molekul yang mengandung elektron-π terkonyugasi dan atau atom yang
mengandung elektron-n, menyebabkan transisi elektron di orbital terluarnya dari
tingkat energi elektron dasar ke tingkat energi elektron tereksitasi lebih tinggi.
Besarnya serapan radiasi tersebut sebanding dengan banyaknya molekul analit
yang mengabsorpsi sehingga dapat digunakan untuk analisis kuantitatif
(Satiadarma, 2004).
Panjang gelombang cahaya ultraviolet dan cahaya tampak bergantung
pada mudahnya promosi elektron, dimana molekul-molekul yang memerlukan
lebih banyak energi untuk promosi elektron, akan menyerap pada panjang
gelombang yang lebih pendek sedangkan molekul yang memerlukan energi lebih
sedikit akan menyerap pada panjang gelombang yang lebih panjang. Senyawa
yang menyerap cahaya dalam daerah tampak mempunyai elektron yang lebih
mudah dipromosikan daripada senyawa yang menyerap pada panjang gelombang
Gugus fungsi yang menyerap radiasi di daerah ultraviolet dekat dan daerah
tampak disebut kromofor dan hampir semua kromofor mempunyai ikatan tak
jenuh. Pada kromofor jenis ini transisi terjadi dari π → π*, yang menyerap pada
λmax kecil dari 200 nm (tidak terkonyugasi), misalnya pada >C=C< dan -C≡C-.
Khromofor ini merupakan tipe transisi dari sistem yang mengandung elektron π
pada orbital molekulnya. Untuk senyawa yang mempunyai sistem konyugasi,
perbedaan energi antara keadaan dasar dan keadaan tereksitasi menjadi lebih kecil
sehingga penyerapan terjadi pada panjang gelombang yang lebih besar.
Gugus fungsi seperti –OH, -NH2 dan –Cl yang mempunyai
elektron-elektron valensi bukan ikatan disebut auksokrom yang tidak menyerap radiasi
pada panjang gelombang lebih besar dari 200 nm, tetapi menyerap kuat pada
daerah ultraviolet jauh. Bila suatu auksokrom terikat pada suatu kromofor, maka
pita serapan kromofor bergeser ke panjang gelombang yang lebih panjang (efek
batokrom) dengan intensitas yang lebih kuat. Efek hipsokrom adalah suatu
pergeseran pita serapan ke panjang gelombang lebih pendek, yang sering kali
terjadi bila muatan positif dimasukkan ke dalam molekul dan bila pelarut berubah
dari non polar ke pelarut polar (Noerdin, 1985; Dachriyanus, 2004).
2.2.2 Hukum Lambert Beer
Menurut Hukum Lambert, serapan berbanding lurus terhadap ketebalan sel
yang disinari. Menurut Hukum Beer, yang hanya berlaku untuk cahaya
monokromatik dan larutan yang sangat encer, serapan berbanding lurus dengan
konsentrasi (banyak molekul zat). Kedua pernyataan ini dapat dijadikan satu
dalam Hukum Lambert-Beer, sehingga diperoleh bahwa serapan berbanding lurus
A = a . b . C
Dimana: A = serapan (tanpa dimensi)
a = absorptivitas (l g-1 cm-1)
b = ketebalan sel (cm)
C = konsentrasi(g. l-1)
Jadi dengan Hukum Lambert-Beer konsentrasi dapat dihitung dari
ketebalan sel dan serapan. Absorptivitas merupakan suatu tetapan dan spesifik
untuk setiap molekul pada panjang gelombang dan pelarut tertentu.
Menurut Roth dan Blaschke (1981), absorptivitas spesifik juga sering
digunakan sebagai ganti absorptivitas. Harga ini memberikan serapan larutan 1%
(b/v) dengan ketebalan sel 1 cm, sehingga dapat diperoleh persamaan:
A = A . b . C 11
Dimana: A = absorptivitas spesifik (ml g11 -1 cm-1)
b = ketebalan sel (cm)
C = konsentrasi senyawa terlarut (g/100 ml larutan)
2.2.3 Penggunaan Spektrofotometri Ultraviolet
Pada umumnya spektrofotometri ultraviolet dalam analisis senyawa
organik digunakan untuk:
1. Menentukan jenis kromofor, ikatan rangkap yang terkonyugasi dan
auksokrom dari suatu senyawa organik
2. Menjelaskan informasi dari struktur berdasarkan panjang gelombang serapan
maksimum suatu senyawa
3. Mampu menganalisis senyawa organik secara kuantitatif dengan
Analisis kualitatif
Kegunaan spektrofotometri ultraviolet dalam analisis kualitatif sangat
terbatas, karena rentang daerah radiasi yang relatif sempit hanya dapat
mengakomodasi sedikit sekali puncak absorpsi maksimum dan minimum, karena
itu identifikasi senyawa yang tidak diketahui, tidak memungkinkan.
Penggunaannya terbatas pada konfirmasi identitas dengan menggunakan
parameter panjang gelombang puncak absorpsi maksimum, λmax, nilai
absorptivitas, a, nilai absorptivitas molar, ε, atau nilai ekstingsi, A1%, 1 cm, yang
spesifik untuk suatu senyawa yang dilarutkan dalam suatu pelarut dan pH tertentu
(Satiadarma, 2002).
Analisis Kuantitatif
Penggunaan utama spektrofotometri ultraviolet adalah dalam analisis
kuantitatif. Apabila dalam alur spektrofotometer terdapat senyawa yang
mengabsorpsi radiasi, akan terjadi pengurangan kekuatan radiasi yang mencapai
detektor. Parameter kekuatan energi radiasi khas yang diabsorpsi oleh molekul
adalah absorban (A) yang dalam batas konsentrasi rendah nilainya sebanding
dengan banyaknya molekul yang mengabsorpsi radiasi dan merupakan dasar
analisis kuantitatif. Penentuan kadar senyawa organik yang mempunyai gugus
khromofor dan mengabsorpsi radiasi ultraviolet-sinar tampak, penggunaannya
cukup luas. Konsentrasi kerja larutan analit umumnya 10 sampai 20 µg/ml, tetapi
untuk senyawa yang nilai absorptivitasnya besar dapat diukur pada konsentrasi
yang lebih rendah. Senyawa yang tidak mengabsorpsi radiasi ultraviolet-sinar
apabila ada reaksi kimia yang dapat mengubahnya menjadi khromofor atau dapat
disambungkan dengan suatu pereaksi khromofor (Satiadarma, 2004).
Analisis kuantitatif dengan metode Spektrofotometri UV dapat
digolongkan atas beberapa pelaksanaan pekerjaan, yaitu;
1. Analisis kuantitatif zat tunggal (analisis satu komponen)
a. Metode Regresi
Analisis kuantitatif dengan metode regresi yaitu dengan menggunakan
persamaan garis regresi yang didasarkan pada harga serapan dan konsentrasi
standar yang dibuat dalam beberapa konsentrasi, paling sedikit menggunakan 5
rentang konsentrasi yang meningkat yang dapat memberikan serapan yang linier,
kemudian diplot menghasilkan suatu kurva yang disebut dengan kurva kalibrasi.
Konsentrasi suatu sampel dapat dihitung berdasarkan kurva tersebut.
b. Metode Pendekatan
Analisis kuantitatif dengan cara ini dilakukan dengan membandingkan
serapan standar yang konsentrasinya diketahui dengan serapan sampel. Syarat
cara pendekatan yaitu serapan sampel tidak jauh berbeda dengan serapan baku
pembanding. Konsentrasi sampel (Cs) dihitung dengan rumus:
AP = a. b. Cp / As = a. b. Cs
Keterangan:
Ap = Absorbansi baku pembanding
As = Absorbansi sampel
Cp = Konsentrasi baku pembanding
2. Analisis Kuantitatif Campuran Dua Macam Komponen atau Lebih
Analisis campuran dua atau lebih bahan kadang-kadang ditentukan secara
simultan dalam sekali pengamatan tanpa dipisahkan. Hal ini didasarkan pada
asumsi bahwa absorbansi total dari campuran komponen merupakan jumlah
serapan masing-masing komponen tersebut.
Ada tiga kemungkinan analisis campuran dua komponen atau lebih, yaitu;
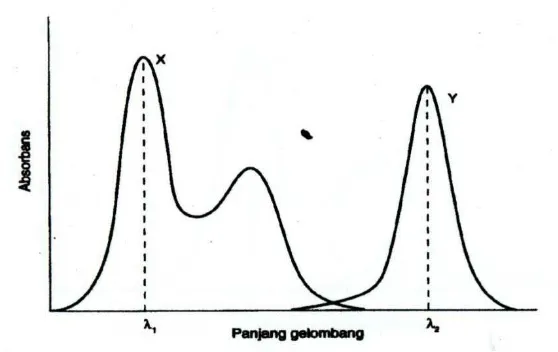
a. Spektrum tanpa tumpang tindih (Overlap)
Spektrum tidak saling tumpang tindih memungkinkan untuk menemukan
suatu panjang gelombang dimana X menyerap dan Y tidak menyerap, serta
panjang gelombang serapan maksimum dimana Y menyerap dan X tidak
menyerap (Gambar 1). Komponen X dan Y masing-masing diukur pada λ1 dan
[image:30.596.182.461.416.592.2]λ2.
Gambar 1. Spektrum absorpsi senyawa X dan Y (tidak ada tumpang tindih
pada pada kedua panjang gelombang yang digunakan)
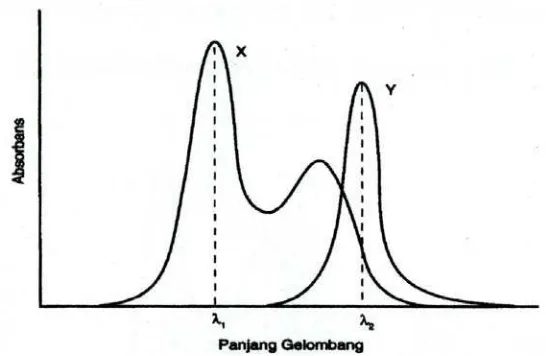
b. Spektrum tumpang tindih satu arah
Spektrum dari X dan Y tumpang tindih satu arah (Gambar 2). Y tidak
mengganggu pengukuran X pada λ1 tetapi X menyerap cukup banyak bersama
sederhana. Konsentrasi X ditetapkan langsung dari serapan larutan pada λ1.
Kemudian serapan yang diberikan oleh konsentrasi X pada λ2 dihitung dari
absorptivitas molar X pada λ2 yang sebelumnya telah diketahui. Serapan ini
dikurangkan dari serapan terukur larutan pada λ2 sehingga diperoleh serapan
yang disebabkan oleh komponen Y. Kemudian konsentrasi Y dapat dihitung
[image:31.596.184.457.254.432.2]dengan cara yang biasa.
Gambar 2. Spektrum absorbs senyawa X dan Y (tumpang tindih satu arah, X
dapat diukur tanpa gangguan Y, tetapi X mengganggu pada pengukuran langsung dari Y).
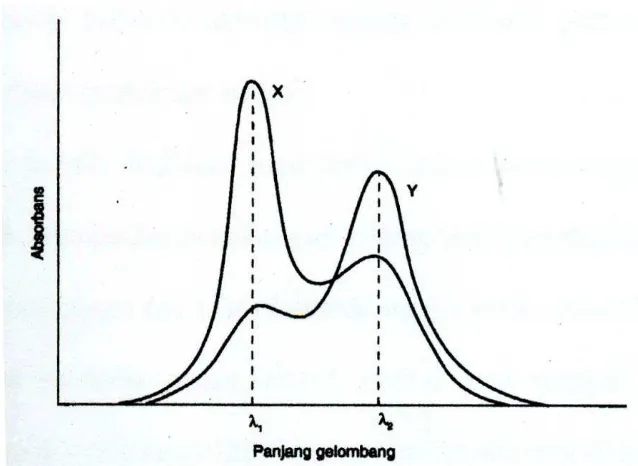
c. Spektrum tumpang tindih dua arah
Spektrum dari X dan Y saling tumpang tindih dua arah (Gambar 3), pada
keadaan ini tidak ada panjang gelombang serapan maksimum dimana X dan Y
menyerap tanpa gangguan. Maka perlu penyelesaian dua persamaan dengan
dua variabel yang tidak diketahui. Hal ini karena serapan total dari campuran
beberapa komponen merupakan jumlah serapan masing-masing komponen
tersebut. Sehingga konsentrasi X dan Y yang belum diketahui dalam kedua
persamaan dapat diukur dengan mudah. Dengan ditentukan bila nilai-nilai
komponen X dan Y pada kedua panjang gelombang itu. Pada perinsipnya
persamaan-persamaan dapat disusun untuk berbagai komponen, asal nilai
absorbansi diukur pada panjang gelombang yang sama banyak dengan
[image:32.596.161.480.197.430.2]komponen itu.
Gambar 3. Spektrum absorbsi X dan Y (tumpang tindih dua arah. Tidak ada
panjang gelombang dimana masing-masing senyawa dapat diukur tanpa mengalami gangguan oleh yang lainnya)
(Day and Underwood, 1999)
2.2.4 Peralatan Untuk Spektrofotometri
Spektrofotometer adalah alat untuk mengukur transmitans atau serapan
suatu sampel sebagai fungsi panjang gelombang. Alat ini terdiri dari spektrometer
yang menghasilkan sinar dari spektrum dengan panjang gelombang tertentu dan
fotometer sebagai alat pengukur intensitas cahaya yang ditransmisikan atau yang
diabsorpsi (Khopkar, 1990; Day and Underwood, 1999).
Unsur-unsur terpenting suatu spektrofotometer ditunjukkan secara skematik dalam
Keterangan Gambar :
1. Suatu sumber energi radiasi yang berkesinambungan yang meliputi daerah
spektrum, dimana instrumen itu dirancang untuk beroperasi.
2. Monokromator, yang merupakan suatu alat untuk mengisolasi suatu berkas
sempit cahaya pada panjang gelombang tertentu dari spektrum luas yang
dipancarkan oleh sumber.
3. Kuvet sebagai wadah untuk sampel.
4. Detektor yang merupakan suatu transducer yang mengubah energi radiasi
menjadi isyarat listrik sehingga dapat mendeteksi sinyal yang dipancarkan.
5. Suatu amplifier (penguat) dan rangkaian yang berkaitan yang membuat
isyarat listrik dapat untuk diamati.
6. Sistem pembacaan yang memperlihatkan besarnya isyarat listrik.
(Day and Underwood, 1999)
2.3 Validasi
Validasi adalah suatu tindakan penilaian terhadap parameter tertentu pada
prosedur penetapan yang dipakai untuk membuktikan bahwa parameter tersebut
memenuhi persyaratan untuk penggunaannya (Harmita, 2004).
Sumber Monokromator Kuvet Detektor
Penguat
Pembacaan, pengamatan Bagian optik
Bagian listrik
1 2 3 4
5
Parameter analisis yang ditentukan pada validasi adalah akurasi, presisi,
kespesifikan, limit deteksi, limit kuantitasi, kelinieran dan rentang.
Akurasi (kecermatan) adalah ukuran yang menunjukkan derajat kedekatan
hasil analisis dengan kadar analit sebenarnya. Akurasi dinyatakan sebagai persen
perolehan kembali (recovery) analit yang ditambahkan dan dapat ditentukan
melalui dua cara yaitu metode simulasi (spiked placebo recovery) dan metode
penambahan bahan baku (standard addition method). Dalam metode simulasi,
sejumlah analit bahan murni (senyawa pembanding kimia) ditambahkan kedalam
campuran bahan sediaan farmasi (plasebo), lalu campuran tersebut dianalisis dan
hasilnya dibandingkan dengan kadar standar yang ditambahkan (kadar
sebenarnya). Dalam metode adisi (penambahan bahan baku), sejumlah sampel
yang dianalisis ditambah analit dengan konsentrasi tertentu (biasanya 80% sampai
120% dari kadar analit yang diperkirakan), dicampur dan dianalisis kembali.
Selisih kedua hasil dibandingkan dengan kadar yang sebenarnya (hasil yang
diharapkan). Dalam kedua metode tersebut, persen perolehan kembali dinyatakan
sebagai rasio antara hasil yang diperoleh dengan hasil yang sebenarnya.
% perolehan kembali = * x100% c
c c
A A f −
Keterangan: c f = Konsentrasi sampel yang diperoleh setelah penambahan
larutan baku
A
c = Konsentrasi sampel sebelum penambahan larutan baku
*
A
c = Konsentrasi baku yang ditambahkan
Presisi (keseksamaan) adalah derajat kesesuain diantara masing-masing
yang diambil dari satu sampel homogen. Presisi dinyatakan sebagai deviasi
standar atau deviasi standar relative (RSD). Presisi dapat diartikan pula sebagai
derajat reprodusibilitas (ketertiruan) atau repeatabilitas (keterulangan)
(satiadarma, 2004; WHO, 1992). Nilai RSD antara 1-2% biasanya dipersyaratkan
untuk senyawa-senyawa aktif dalam jumlah yang banyak, sedangkan untuk
senyawa-senyawa dengan kadar sekelumit RSD berkisar antara 5-15% (Rohman,
2007).
Batas deteksi adalah nilai parameter, yaitu konsentrasi analit terendah
yang dapat dideteksi yang masih memberikan respon signifikan dibandingkan
dengan blanko. Batas deteksi dapat dihitung dengan rumus sebagai berikut:
Batas deteksi =
slope SB x
3
Batas kuantitasi adalah jumlah analit terkecil dalam sampel yang masih
dapat diukur dalam kondisi percobaan yang sama dan memenuhi kriteria ceermat
dan seksama. Batas Kuantitasi =
slope SB x
10
Kelinieran suatu metode analisis adalah kemampuan untuk menunjukkan
bahwa nilai hasil uji langsung atau setelah diolah secara secara matematika,
proporsional dengan konsentrasi analitt dalam sampel dalam batas rentang
BAB III
METODOLOGI PENELITIAN 3.1Lokasi Penelitian
Penelitian dilakukan di Laboratorium Kimia Farmasi Kuantitatif Fakultas
Farmasi Unuversitas Sumatera Utara.
3.2Metode Penelitian
Metode yang digunakan dalam penelitian ini adalah metode eksperimental.
3.3Alat
Alat-alat yang digunakan adalah spektrofotometer ultraviolet/visibel (UV
mini 1240 Shimadzu), neraca Listrik (Boeco Germany), oven dan alat-alat gelas.
3.4Bahan
Bahan – bahan yang digunakan adalah Isoniazid Baku Pembanding
Farmakope Indonesia (BPFI), Vitamin B6 BPFI, Asam Klorida (Merck), aquadest,
tablet Pehadoxin® (PT. Phapros), tablet Niacifort – 6® (PT. Ikapharmindo
Putramas), tablet Beniazid® (PT. Rocella).
3.5Metode Pengambilan Sampel
Sampel yang digunakan adalah tablet kombinasi Isoniazid dan Vitamin B6
dengan nama dagang dengan komposisi Isoniazid 100mg dan Vitamin B6 10mg
(10:1). Teknik pengambilan sampel dilakukan dengan cara sampling purposif dan
diasumsikan semua nama dagang yang dijual adalah homogen. Pemilihan cara
pengambilan ini didasarkan atas pertimbangan bahwa populasi sampel adalah
3.6Pembuatan Pereaksi
3.6.1 Pembuatan pelarut HCl 0,1N
Diencerkan 8,5 ml HCl 37% dengan 1 liter akuadest (DitJen POM, 1979).
3.7Pembuatan Larutan Induk Baku BPFI
3.7.1 Pembuatan Larutan Induk Baku Isoniazid BPFI
Ditimbang dengan seksama 50mg Isoniazid BPFI kemudian dimasukkan
kedalam labu tentukur 50ml, dilarutkan dengan HCl 0,1N hingga larut,
dicukupkan volume dengan HCl 0,1N sampai 50ml (LIB I).
Konsentrasi LIB I : x g mg g ml
ml mg / 1000 / 1000 50 50 µ µ =
Dari larutan LIB I dipipet 5ml dimasukkan kedalam labu tentukur 50ml,
diencerkan dengan HCl 0,1N sampai garis tanda (LIB II).
Konsentrasi LIB II : x g ml g ml
ml ml / 100 / 1000 50 5 µ µ =
3.7.2 Pembuatan larutan induk baku Vitamin B6 BPFI
Ditimbang dengan seksama 50mg Vitamin B6 BPFI kemudian dimasukkan
kedalam labu tentukur 50ml, dilarutkan dengan HCl 0,1N hingga larut,
dicukupkan volume dengan HCl 0,1N sampai 50ml (LIB I).
Konsentrasi LIB I : x g mg g ml
ml mg / 1000 / 1000 50 50 µ µ =
Dari larutan LIB I dipipet 2,5ml dimasukkan kedalam labu tentukur 50ml,
diencerkan dengan HCl0,1 N sampai garis tanda (LIB II).
Konsentrasi LIB II : x g ml g ml
3.8Penentuan Panjang Gelombang Maksimum
3.8.1 Penentuan Panjang Gelombang Maksimum Isoniazid BPFI
Dipipet sebanyak 2,5ml LIB II Isoniazid BPFI, dimasukkan ke dalam labu
tentukur 25ml, dicukupkan volume dengan HCl 0,1N sampai 25ml, diperoleh
kadar 10µg/ml. Diukur serapannya pada λ 200 – 350nm sehingga diperoleh
panjang gelombang maksimum (Hasil pengukuran dapat dilihat pada gambar 1
dihalaman 27)
3.8.2 Penentuan Panjang Gelombang Maksimum Vitamin B6 BPFI
Dipipet sebanyak 4ml LIB II vitamin B6 BPFI, dimasukkan ke dalam labu
tentukur 25ml, dicukupkan volume dengan HCl 0,1N sampai 25ml, diperoleh
kadar 8µg/ml. Diukur serapannya pada λ 200 – 350nm sehingga diperoleh
panjang gelombang maksimum (Hasil pengukuran dapat dilihat pada gambar 2
dihalaman 29)
3.9Pembuatan Kurva Serapan Gabungan (Overlay) Isoniazid BPFI dan Vitamin B6 BPFI (10:1)
Larutan Isoniazid BPFI dan Vitamin B6 BPFI dibuat dengan konsentrasi
masing 20µg/ml dan 2µg/ml (10:1). Kemudian diukur serapan
masing-masing pada rentang panjang gelombang 240-310nm. Kurva serapan yang
diperoleh masing-masing dibuat dengan cara overlay pada kerangka yang sama
(Hasil pengukuran dapat dilihat pada gambar 3 dihalaman 30).
3.10 Penentuan Absorptivitas (α)
3.10.1 Penentuan Absorptivitas (α) Isoniazid BPFI
Larutan Induk Baku II Isoniazid BPFI (100µg/ml), dipipet sebanyak 5ml
garis tanda, konsentrasi larutan menjadi 20µg/ml. Diukur serapannya pada λmax
Isoniazid dan pada λmax Vitamin B6 dengan menggunakan larutan HCl 0,1N
sebagai blanko.
3.10.2 Penentuan Absoptivitas (α) Vitamin B6 BPFI
Larutan Induk Baku II Vitamin B6 BPFI (50 µg/ml) dipipet sebanyak 1ml,
dimasukkan ke dalam labu tentukur 25 ml, dicukupkan volume dengan HCl 0,1N
sampai garis tanda, konsentrasi larutan menjadi 2µg/ml. Diukur serapan pada
λmax Isoniazid dan pada λmax Vitamin B6 dengan menggunakan larutan HCl
0,1N sebagai blanko.
3.11 Penetapan Kadar Sampel
Sejumlah 20 tablet ditimbang seksama dan diserbukkan homogen.
Sejumlah serbuk timbang seksama setara 50mg Isoniazid dan 5mg Vitamin B6,
Masing-masing dimasukkan ke dalam labu tentukur 100ml dilarutkan dengan HCl
0,1N, dicukupkan dengan HCl 0,1N sampai garis tanda dan disaring, 10ml filtrat
pertama dibuang, filtrat selanjutnya ditampung (konsentrasi teoritis Isoniazid
500µg/ml dan Vitamin B6 50µg/ml).
Filtrat ini dipipet 1ml dimasukkan ke dalam labu tentukur 25ml diencerkan
dengan HCl 0,1N sampai garis tanda, diperoleh konsentrasi teoritis Isoniazid
20µg/ml dan Vitamin B6 2µg/ml. Kemudian diukur serapannya pada λmax
Isoniazid dan pada λmax Vitamin B6 dengan menggunakan larutan HCl 0,1N
sebagai blanko. Perlakuan diulang sebanyak 6 kali.
Kadar dapat dihitung menggunakan persamaan multikomponen dan secara
- Persamaan multikomponen: ) 2 ... ... ... . . . . ) 1 ... ... ... . . . . 2 2 2 1 1 1 y y x x y x y y x x y x C b a C b a A A A C b a C b a A A A + = + = + = + = λ λ λ λ λ λ Keterangan: 1 λ
A = Absorbansi senyawa campuran pada panjang gelombang pertama
2
λ
A = Absorbansi senyawa campuran pada panjang gelombang kedua
x
a = Absorptivitas bahan berkhasiat pertama
y
a = Absorptivitas bahan berkhasiat kedua
b = Tebal kuvet (1cm)
x
C = Konsentrasi bahan berkhasiat pertama
y
C = Konsentrasi bahan berkhasiat kedua
- Matriks:
[
]
[ ]
b b b b b b b b b b b b y x y x A x A x Y y x y x y A y A X " " ' ' " "' ' ' " " ' ' "' " ' ' ε ε ε ε ε ε ε ε ε ε ε ε = =Keterangan:
[ ]
X = Konsentrasi bahan berkhasiat 1[ ]
Y = Konsentrasi bahan berkhasiat 2'
A = Absorbansi pada panjang gelombang maksimum x
"
A = Absorbansi pada panjang gelombang maksimum y
b x
'
ε = Absorptivitas x pada panjang gelombang maksimum x
b x
"
ε = Absorptivitas x pada panjang gelombang maksimum y
b y
'
ε = Absorptivitas y pada panjang gelombang maksimum x
b y
"
ε = Absorptivitas y pada panjang gelombang maksimum y
3.12 Uji Validasi Metode Analisis
Berdasarkan WHO (1992) Validasi adalah suatu tindakan penilaian
terhadap parameter tertentu pada prosedur penetapan yang dipakai untuk
membuktikan bahwa parameter tersebut memenuhi persyaratan untuk
penggunaannya.
Uji validasi yang dilakukan pada penelitian ini adalah uji akurasi dengan
parameter % perolehan kembali menggunakan metode penambahan baku
(standard addition method) dan uji presisi dengan parameter Relatif Standar
Deviasi (WHO, 1992).
3.12.1 Uji Akurasi
Uji akurasi dengan parameter persen perolehan kembali (recovery)
dilakukan secara metode penambahan baku (standard addition method) dengan
membuat 3 konsentrasi analit dengan rentang spesifik 80, 100 dan 120%,
30% baku pembanding kemudian dianalisis dengan perlakuan yang sama seperti
pada penetapan kadar sampel.
Menurut WHO (1992), perolehan kembali dapat dihitung dengan rumus
sebagai berikut:
% perolehan kembali = * x100% c
c c
A A f −
Keterangan: c f = Konsentrasi sampel yang diperoleh setelah penambahan
larutan baku
A
c = Konsentrasi sampel sebelum penambahan larutan baku
*
A
c = Konsentrasi baku yang ditambahkan
3.12.2 Penentuan Uji Presisi
Uji presisi (ketelitian) ditentukan dengan parameter Relatif Standar
Deviasi (RSD) dengan rumus:
% 100 x X SD
RSD= (Day, Jr. R.A. 1989)
Keterangan: RSD = Relatif standar deviasi
SD = Standar deviasi
X = Kadar rata-rata sampel
3.12.3 Analisis Data Secara Statistik
Untuk menghitung standar deviasi dapat digunakan rumus:
( )
1
2
− −
=
∑
n X X
SD (Day, Jr. R.A. 1989 & Basset, J. et.al. 1994)
Keterangan: SD = Standar deviasi
X = Kadar rata-rata sampel
n = Jumlah perlakuan
Menelaah apakah semua data yang diperoleh dapat diterima atau ditolak
dengan melihat t hitung dan t tabel.
(
)
n SD
X X th
/
−
= (Basset, J. et. al. 1994)
Keterangan: t h = t hitung
SD = Standar deviasi
X = Kadar sampel
X = Kadar rata-rata sampel
n = Jumlah perlakuan
Data diterima jika: -t tabel < t hitung < t tabel
Data ditolak jika: -t tabel > t hitung > t tabel
Untuk mencari kadar sebenarnya dengan kepercayaan 99%, nilai α = 0,01;
dk = n – 1 dapat menggunakan rumus:
( )
n SD x t
X 1/2α,dk
µ = ± (Basset, J. et. Al. 1994)
Keterangan: μ = Interval kepercayaan
X = Kadar rata-rata sampel
dk = Derajat kebebasan (n-1)
(1/2α)
t = Harga t tabel sesuai dk (n-1)
BAB IV
HASIL DAN PEMBAHASAN
4.1 Penentuan Panjang Gelombang Maksimum
Hasil pengukuran yang maksimum dari masing-masing komponen;
Isoniazid dan Vitamin B6 diperoleh pada pengukuran di panjang gelombang yang
memberikan serapan maksimum pada masing-masing komponen dengan
konsentrasi INH BPFI 10µg/ml dan Vitamin B6 BPFI 8µg/ml dan kurva serapan
dari masing-masing komponen dapat dilihat pada gambar 1 dan 2.
Gambar 1. Kurva serapan Isoniazid BPFI, konsentrasi 10µ g/ml dalam larutan
Gambar 2. Kurva serapan Vitamin B6 BPFI, konsentrasi 8µg/ml dalam larutan
HCl 0,1N. Panjang gelombang maksimum 290nm.
Dari hasil penentuan panjang gelombang maksimum dalam pelarut HCl
0,1N secara spektrofotometri ultraviolet pada gambar 1 dan 2 diperoleh serapan
maksimum larutan Isoniazid BPFI pada panjang gelombang 266nm & 215nm, dan
larutan Vitamin B6 BPFI pada panjang gelombang 290nm.
Menurut Moffat (1986), Isoniazid dalam larutan asam memberikan
serapan maksimum pada panjang gelombang 266nm dengan A = 390a dan dalam 11
larutan basa memberikan serapan maksimum pada panjang gelombang 298nm
sedangkan Vitamin B6 dalam asam memberikan serapan maksimum pada panjang
gelombang 290nm dengan A = 523a dan dalam larutan buffer phospat pH 6,88 11
memberikan serapan maksimum pada panjang gelombang 254nm dengan A = 11
219a atau pada panjang gelombang 324nm dengan A = 426a. 11
Karena pelarut yang digunakan adalah larutan asam maka pengukuran
selanjutnya akan dilakukan pada λmaksimum INH 266nm karena pada λ 215nm
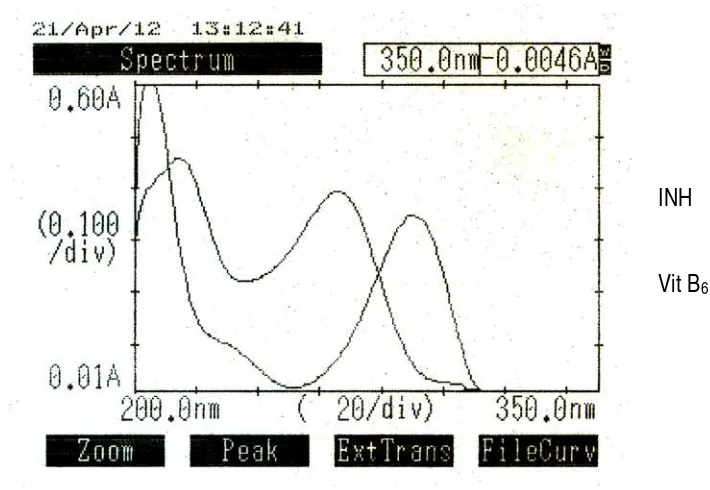
[image:46.596.172.453.85.301.2]4.2 Pembuatan Kurva Serapan Gabungan (overlay) Isoniazid BPFI dan Vitamin B6 BPFI (10:1)
Larutan Isoniazid BPFI dan Vitamin B6 BPFI dibuat dengan konsentrasi
20µg/ml dan 2µg/ml. Perbandingan konsentrasi yang dibuat sesuai dengan
perbandingan zat berkhasiat yang terdapat dalam sediaan tablet. Kemudian diukur
serapannya pada rentang panjang gelombang 240 – 310nm. Kurva serapan
masing-masing dibuat dengan cara overlay pada kerangka yang sama. Diperoleh
kedua spektra saling tumpang tindih dimana spektra absorpsi Isoniazid
mempengaruhi spektra absorpsi Vitamin B6 dan spektra absorpsi Vitamin B6 juga
mempengaruhi spektra absorpsi Isoniazid sehingga serapan yang terukur pada
panjang gelombang maksimum Isoniazid merupakan serapan Isoniazid dan
Vitamin B6. Begitu juga sebaliknya serapan yang terukur pada panjang gelombang
maksimum Vitamin B6 merupakan serapan Isoniazid dan Vitamin B6. Kurva
serapan dapat dilihat pada gambar 3.
Gambar 3. Kurva serapan gabungan (overlay) Isoniazid BPFI dan Vitamin B6
BPFI (10:1)
INH
[image:47.596.152.507.469.714.2]4.3 Penentuan Absorbtivitas (α) Isoniazid BPFI dan Vitamin B6 BPFI
Penentuan absorbtivitas dari masing-masing komponen dengan mengukur
serapan Isoniazid BPFI dengan konsentrasi 20µg/ml dan Vitamin B6 BPFI 2µg/ml
pada panjang gelombang 266nm dan 290nm.
Absorptivitas (α) secara persamaan multikomponen diperoleh dengan
membagi harga serapan dengan konsentrasi (α = A / b x C), sedangkan
absorptivitas (α) secara matriks diperoleh dengan menggunakan persamaan
C x b x A ( cm)
% 1 1
α
= .
Hasil perhitungan absorptivitas secara persamaan multikomponen dapat
dilihat pada tabel 1 dibawah ini dan contoh perhitungan dapat dilihat pada
lampiran 3 dihalaman . Sedangkan secara matriks dapat dilihat pada tabel 2
[image:48.596.110.514.442.571.2]dibawah ini dan contoh perhitungan pada lampiran 4 dihalaman .
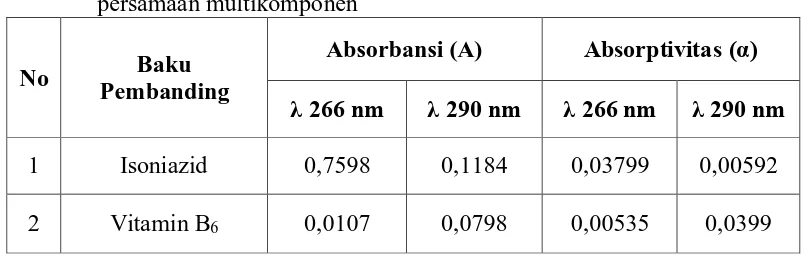
Tabel 1. Data absorptivitas Isoniazid (20 µg/ml) dan Vitamin B6 (2 µg/ml) secara
persamaan multikomponen
No Baku
Pembanding
Absorbansi (A) Absorptivitas (α)
λ 266 nm λ 290 nm λ 266 nm λ 290 nm
1 Isoniazid 0,7598 0,1184 0,03799 0,00592
2 Vitamin B6 0,0107 0,0798 0,00535 0,0399
Tabel 2. Data absorptivitas Isoniazid (20 µg/ml) dan Vitamin B6 (2 µg/ml) secara
matriks
No Baku
Pembanding
Absorbansi (A) Absorptivitas (α)
λ 266 nm λ 290 nm λ 266 nm λ 290 nm
1 Isoniazid 0,7598 0,1184 379,9 59,2
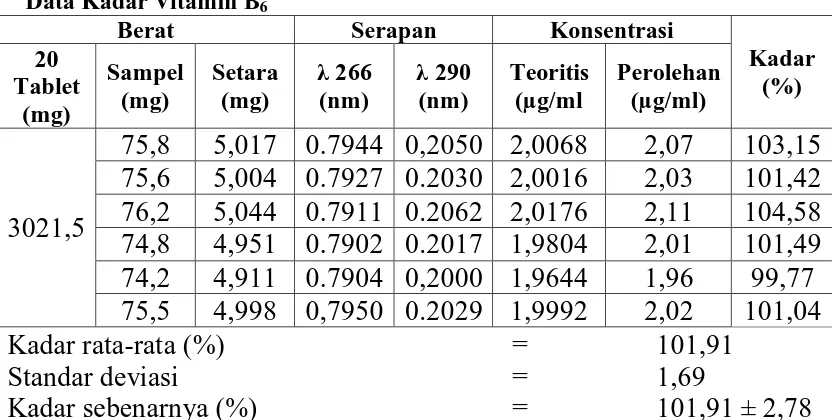
[image:48.596.112.513.595.731.2]4.4 Penetapan Kadar Sampel
Dari hasil penetapan kadar campuran Isoniazid dan Vitamin B6 secara
perhitungan persamaan multikomponen dan matriks diperoleh kadar yang tidak
[image:49.596.114.512.208.363.2]berbeda.
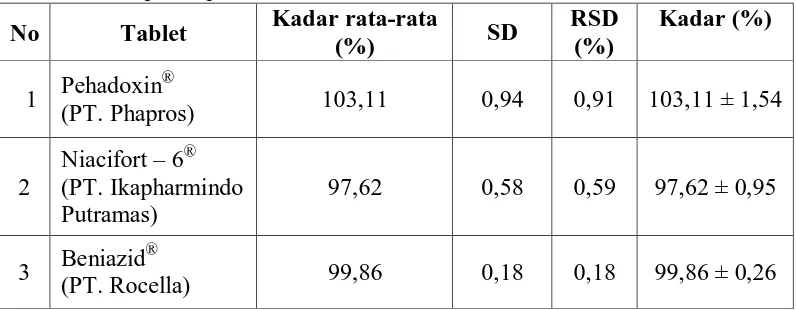
Tabel 3. Hasil penetapan kadar Isoniazid dalam sediaan tablet No Tablet Kadar rata-rata
(%) SD
RSD (%)
Kadar (%)
1 Pehadoxin
®
(PT. Phapros) 103,11 0,94 0,91 103,11 ± 1,54
2
Niacifort – 6® (PT. Ikapharmindo Putramas)
97,62 0,58 0,59 97,62 ± 0,95
3 Beniazid
®
(PT. Rocella) 99,86 0,18 0,18 99,86 ± 0,26
Tabel 4. Hasil penetapan kadar VitaminB6 dalam sediaan tablet No Tablet Kadar rata-rata
(%) SD
RSD (%)
Kadar (%)
1 Pehadoxin
®
(PT. Phapros) 101,91 1,69 1,66 101,91 ± 2,78
2
Niacifort – 6® (PT. Ikapharmindo Putramas)
103,90 0,79 0,76 103,90 ± 1,62
3 Beniazid
®
(PT. Rocella) 97,73 0,98 1,00 97,73 ± 1,61
Berdasarkan tabel diatas semua sediaan tablet yang dianalisis memenuhi
persyaratan kadar yang tercantum dalam Farmakope Indonesia edisi IV (1995)
yaitu mengandung tidak kurang dari 90,0% dan tidak lebih dari 110,0% dari
jumlah yang tertera pada etiket untuk Isoniazid, dan untuk VitaminB6,
mengandung tidak kurang dari 95,0% dan tidak lebih dari 115,0% dari jumlah
4.5 Pengujian Validasi Metode Meliputi Akurasi dan Presisi
Menurut WHO (1992) Uji validasi metode antara lain meliputi akurasi,
presisi, spesifitas, linearitas dan rentang, Batas deteksi dan batas kuantitasi,
ketangguhan dan kekuatan. Namun tidak selamanya parameter untuk
mengevaluasi validasi metode diuji (Rohman, 2007).
Dalam penelitian ini uji validasi metode yang dilakukan adalah akurasi
dengan parameter persen recovery menggunakan metode penambahan baku
(standard addition method) dan presisi dengan parameter Relatif Standar Deviasi
(RSD) dalam sediaan tablet Pehadoxin® (PT. Phapros).
4.5.1 Penentuan Uji Akurasi dengan Parameter Persen Recovery Menggunakan Metode Penambahan Baku (Standard Addition Method)
Uji akurasi dapat ditentukan dengan dua cara yaitu metode simulasi (spike-
placebo recovery) dan metode penambahan baku (standard addition method)
(WHO, 1992). Dalam penelitian ini peneliti menggunakan metode penambahan
baku (standard addition method) dengan parameter persen recovery terhadap
sampel tablet Pehadoxin® (PT. Phapros) karena sampel mengandung bahan
penyusun tablet (matriks) yang tidak diketahui komposisinya.
Uji akurasi dilakukan dengan membuat 3 konsentrasi analit dengan
rentang spesifik 80, 100 dan 120%, masing-masing dengan 3 replikasi dan setiap
rentang spesifik mengandung 70% analit dan 30% baku pembanding (Indrayanto
dan Yuwono, 2003).
Diperoleh data hasil pengujian persen recovery Isoniazid dan Vitamin B6
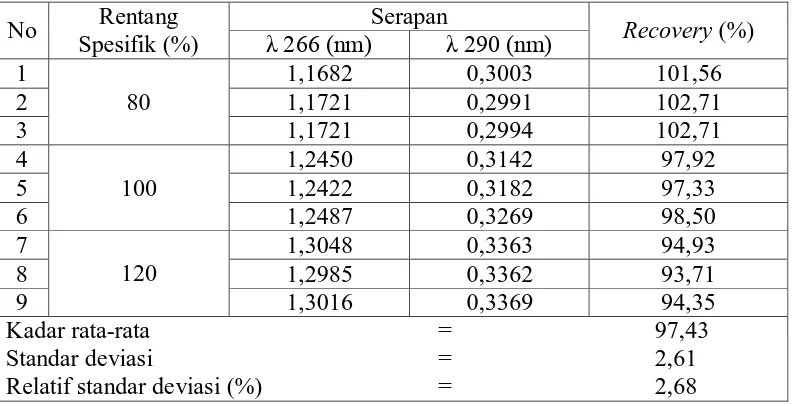
Tabel 5. Hasil pengujian persen recovery Isoniazid dalam tablet Pehadoxin® (PT. Phapros) dengan metode penambahan baku (standard addition method)
No Rentang Spesifik (%)
Serapan
Recovery (%) λ 266 (nm) λ 290 (nm)
1
80
1,1682 0,3003 101,56
2 1,1721 0,2991 102,71
3 1,1721 0,2994 102,71
4
100
1,2450 0,3142 97,92
5 1,2422 0,3182 97,33
6 1,2487 0,3269 98,50
7
120
1,3048 0,3363 94,93
8 1,2985 0,3362 93,71
9 1,3016 0,3369 94,35
Kadar rata-rata = 97,43
Standar deviasi = 2,61
Relatif standar deviasi (%) = 2,68
Tabel 6. Hasil pengujian persen recovery Vitamin B6 dalam tablet Pehadoxin®
(PT. Phapros) dengan metode penambahan baku (standard addition
method)
No Rentang Spesifik (%)
Serapan
Recovery (%) λ 266 (nm) λ 290 (nm)
1
80
1,1682 0,3003 103,12
2 1,1721 0,2991 98,96
3 1,1721 0,2994 100,00
4
100
1,2450 0,3142 97,50
5 1,2422 0,3182 96,67
6 1,2487 0,3269 113,33
7
120
1,3048 0,3363 97,86
8 1,2985 0,3362 99,28
9 1,3016 0,3369 100,00
Kadar rata-rata = 98,93
Standar deviasi = 1,06
Relatif standar deviasi (%) = 1,07
Dari hasil penelitian ini didapatkan kadar rata-rata persen recovery, untuk
Isoniazid 97,43% dan Vitamin B6 98,93%. Hasil persen recovery ini memenuhi
persyaratan uji akurasi sehingga dapat disimpulkan bahwa metode analisis yang
[image:51.596.114.513.367.581.2]4.5.2 Penentuan Uji Presisi dengan Parameter Relatif Standar Deviasi (RSD)
Presisi merupakan ukuran keterulangan metode analisis dan biasanya
diekspresikan sebagai simpangan baku relatif. Presisi seringkali diekspresikan
dengan SD atau standar deviasi dan RSD atau standar deviasi relatif dari
serangkaian data. (Rohman, 2007).
Adapun uji presisi ini dilakukan pada sampel tablet Pehadoxin® (PT.
Phapros) dan hasil yang diperoleh untuk Isoniazid diperoleh Standar Deviasi (SD)
2,61 dan Relatif Standar Deviasi (RSD) 2,68% sedangkan untuk Vitamin B6
Standar Deviasi (SD) 1,06 dan Relatif Standar Deviasi (RSD) 1,07%.
Nilai Relatif Standar Deviasi (RSD) yang diperoleh dari pengukuran
sediaan tablet yang dianalisis telah memenuhi syarat RSD yaitu 5-15% untuk
senyawa-senyawa dengan kadar sekelumit (Rohman, 2007). Dapat disimpulkan
bahwa metode yang digunakan memenuhi persyaratan uji validasi metode
sehingga dapat digunakan untuk penetapan kadar kombinasi Isoniazid dan
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
1. Metode spektrofotometri ultraviolet dapat digunakan untuk penetapan
kadar tablet kombinasi Isoniazid dan Vitamin B6 dan memenuhi uji
validasi metode dengan parameter akurasi dan presisi.
2. Sediaan tablet kombinasi bernama dagang yang dianalisis memenuhi
persyaratan kadar yang tercantum dalam Farmakope Indonesia edisi IV
(1995).
5.2 Saran
1. Disarankan kepada peneliti selanjutnya untuk melakukan penetapan kadar
Isoniazid dan Vitamin B6 dalam bentuk campuran dengan menggunakan
DAFTAR PUSTAKA
Basset, J., et.al. (1994). Vogel’s Textbook of Quantitative Inorganic Analysis
Including elementary Instrumental Analysis. 4th Ed. Alih bahasa, A.
Hadyana P., L. Setiono. Penerbit E.G.C. Jakarta.
Dachriyanus (2004). Analisis Struktur Senyawa Organik Secara Spektrofotometri. Andalas University Press. Padang.
Day, R.A dan Underwood, A.L. (1981). Analisa Kimia Kuantitatif. Edisi keempat. Penerjemah : Soendoro, R. Penerbit Erlangga. Jakarta.
Ditjen POM. (1972). Farmakope Indonesia. Edisi kedua. Departemen Kesehatan RI. Jakarta.
Ditjen POM. (1979). Farmakope Indonesia. Edisi ketiga. Departemen Kesehatan RI. Jakarta.
Ditjen POM. (1995). Farmakope Indonesia. Edisi keempat. Departemen Kesehatan RI. Jakarta.
Fessenden dan Fessenden. (1992). Kimia Organik. Jilid II. Edisi ketiga. Penerjemah: Pudjaatmaka, A.H. Penerbit Erlangga. Jakarta.
Harmita. (2004). Petunjuk Pelaksanaan Validasi metode dan Cara Perhitungannya. Review Artikel. Majalah Ilmu Kefarmasian. Vol.1 (3).
Harris, D.C. (1995). Quantitative Chemical Analysis. Fourth edition. W.H. Freeman and company. New York.
Holme, D. J., and Peck, H. (1983). Analytical Biochemistry. Longman Inc. London.
Indrayanto & Yuwono. (2003). Encyclopedia of Chromatography. Suplemen.
Katzung, B.G. (1998). Farmakologi Dasar dan Klinik. Penerjemah dan Editor Bagian Farmakologi Fakultas Kedokteran Universitas Airlangga. Penerbit Salemba Medika. Jakarta.
Khopkar, S.M., (1990). Konsep Dasar Kimia Analitik. Penerjemah A. Saptoraharjo. Cetakan Pertama. Penerbit Universitas Indonesia. Jakarta.
Moffat, A.C., et al. (1986). Clarke’s Isolation and Identification of Drug. Second Edition. The Pharmaceutical Press. London.
Noerdin, D. (1985). Elusidasi Struktur Senyawa Organik Dengan Cara
Spektroskopi Ultralembayung dan Inframerah. Penerbit Angkasa.
Bandung.
Rohman, A. (2007). Kimia Farmasi Analisis. Penerbit Pustaka Pelajar. Jakarta.
Roth, J.H., and Blaschke, G. (1998). Analisis Farmasi. Penerjemah: Kisman, dkk. Cetakan Ketiga. Penerbit UGM Press. Yogyakarta.
Satiadarma, K., dkk. (2004). Asas Pengembangan Prosedur Analisis. Cetakan Pertama. Airlangga Universitry Press. Surabaya.
Schunack, W., Mayer, K., dan Haake, M. (1998). Senyawa Obat. Penerbit Gajahmada University Press. Yogyakarta.
Sudjana. (1996). Metode Statistika. Edisi kelima. Penerbit Tarsito. Bandung.
Tjay, T.H dan Raharjo, K. (2002). Obat-obat Penting. Penerbit PT Elek Media Komputindo. Jakarta
USP Pharmacopeia. (2007). The National Formulary. 30th Edition. The United State Pharmacopeia Convention.
WHO, 1992. Validation of Analytical Procedures Used in the Examination of
Gambar

Dokumen terkait
VARSE memenuhi persyaratan yang ditetapkan oleh Farmakope Indonesia Edisi IV yaitu tablet piridoksin mengandung piridoksin hidroklorida dengan kadar 97,59 %, tidak kurang dari 95,00
PENETAPAN KADAR RIFAMPISIN DAN ISONIAZID DALAM SEDIAAN TABLET SECARA MULTIKOMPONEN DENGAN METODE.. SPEKTROFOTOMETRI ULTRAVIOLET
Persyaratan tablet tunggal untuk deksametason dan deksklorfeniramin maleat dalam3. Farmakope Indonesia edisi V (2014) adalah mengandung tidak kurang
yang terdapat dalam tablet memenuhi persyaratan yang ditetapkan Farmakope. Indonesia Edisi IV atau tidak, sehingga dapat dengan
Penetapan Kadar Triprolidina Hidroklorida dan Pseudoefedrina Hidroklorida dalam Tablet Anti Influenza Secara Spektrofotometri Derivatif.. Majalah
Penetapan Kadar Rifampisin dan Isoniazid dalam Sediaan Tablet Secara Multikomponen dengan Metode Spektrofotometri Ultraviolet.. Medan: Fakultas Farmasi, Universitas Sumatera
Kadar piroksikam dalam sediaan kapsul dengan nama dagang dan generik yang beredar dipasaran memenuhi persyaratan kadar yang ditetapkan Farmakope Indonesia Edisi V tahun 2014b.
Berdasarkan hasil pengujian didapatkan sampel tablet metronidazole 500 mg OGB dan bermerek dagang memenuhi persyaratan parameter uji Farmakope Indonesia edisi IV