PEMANFAATAN EKSTRAK BUAH SENDUDUK
(Melastoma malabathricum L.) SEBAGAI
PEWARNA TABLET
SKRIPSI
OLEH:
NURMALAHAYATI NIM 111524096
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
PEMANFAATAN EKSTRAK BUAH SENDUDUK
(Melastoma malabathricum L.) SEBAGAI
PEWARNA TABLET
SKRIPSI
Diajukan untuk Melengkapi Salah Satu Syarat untuk Memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
NURMALAHAYATI NIM 111524096
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
PEMANFAATAN EKSTRAK BUAH SENDUDUK
(Melastoma malabathricum L.) SEBAGAI
PEWARNA TABLET
OLEH:
NURMALAHAYATI NIM 111524096
Dipertahankan di hadapan Panitia Penguji skripsi Fakultas Farmasi Universitas Sumatra Utara
Pada tanggal: 28 April 2014
Disetujui oleh:
Pembimbing I, Panitia Penguji:
Drs. Agusmal Dalimunthe, M.S., Apt. Dra. Juanita Tanuwijaya, M.Si.,Apt. NIP 195406081983031005 NIP 195111021977102001
Pembimbing II, Drs. Agusmal Dalimunthe, M.S., Apt. NIP 195406081983031005
Dra. Suwarti Aris, M.Si., Apt. Dra. Herawaty Ginting, M.Si., Apt. NIP 195107231982032001 NIP 195112231980032002
Dra. Fat Aminah, M.Sc., Apt. NIP 195011171980022001
Medan, Juni 2014 Fakultas Farmasi
KATA PENGANTAR
Puji dan syukur marilah kita panjatkan kehadirat Allah SWT karena atas petunjuk, limpahan rahmat dan karuniaNYAlah, sehingga penulis dapat menyelesaikan skripsi ini yang berjudul “ Pemanfaatan Ekstrak Buah Senduduk (Melastoma malabathricum L.) Sebagai Pewarna dalam Sediaan Tablet”. Skripsi ini diajukan sebagai salah satu syarat untuk memperoleh gelar sarjana farmasi pada Fakultas Farmasi Universitas Sumatra Utara.
Pewarna alami adalah zat warna alami (pigmen) yang diperoleh dari tumbuh-tumbuhan dan hewan. Zat warna ini telah digunakan sejak dulu dan umumnya dianggap lebih aman dari zar warna sintetis. Antosianin merupakan salah satu pewarna alami penghasil warna merah, orange, ungu dan biru yang banyak terdapat pada bunga dan buah-buahan. Buah senduduk berwarna ungu kemerahan yang menandakan adanya kandungan antosianin, yang bisa digunakan sebagai sumber pewarna alami. Oleh karena itu sehingga penelitian ini dilakukan. Pada penelitian ini zat warna merah buah senduduk digunakan sebagai pewarna dalam sediaan tablet dan memberikan hasil yang bagus sehingga zat warna ini dapat digunakan sebagai pewarna yang baik dan aman.
ponakan-ponakan saya (Auria Natasya, Alifa dan Zahira) yang selalu setia memberi do’a, dorongan dan semangat kepada penulis dari pertama sampai skripsi ini selesai.
Pada kesempatan ini penulis juga mengucapkan terima kasih yang tulus kepada Bapak Prof. Dr. Sumadio Hadisahputra, Apt. selaku Dekan Fakultas Farmasi USU Medan yang telah memberikan fasilitas sehingga penulis dapat menyelesaikan pendidikan. Bapak Drs. Agusmal Dalimunthe, M.S., Apt. dan Ibu Dra. Suwati Aris, M.Si., Apt. selaku pembimbing yang telah memberikan waktu, bimbingan dan nasehat selama penelitian hingga selesainya penyusunan skripsi ini. Ibu Dra. Tuty Roida Pardede, M.Si., Apt. selaku penasehat akademik yang telah memberikan bimbingan kepada penulis selama masa perkuliahan. Ibu Dra. Juanita Tanuwijaya, M.Si., Apt., Ibu Dra. Herawaty Ginting, M.Si., Apt. dan Ibu Dra. Fat Aminah, M.Sc., Apt. selaku dosen penguji yang telah memberikan kritik, saran dan arahan kepada penulis dalam menyelesaikan skripsi ini. Ibu Kepala Laboratorium Farmakognosi dan Ibu Kepala Laboratorium Teknologi Sediaan Farmasi II Fakultas Farmasi USU yang telah memberikan bantuan dan fasilitas selama penulis melakukan penelitian.
Penulis menyadari sepenuhnya bahwa penulisan skripsi ini masih belum sempurna. Untuk itu dengan segala kerendahan hati penulis mengharapkan kritik dan saran yang bersifat membangun demi kesempurnaan skripsi ini. Akhir kata penulis berharap semoga skripsi ini dapat menjadi kontribusi yang bermanfaat bagi ilmu pengetahuan khususnya dibidang farmasi.
Medan, 28 April 2014 Penulis,
PEMANFAATAN EKSTRAK BUAH SENDUDUK (Melastoma
malabathricum L.) SEBAGAI PEWARNA TABLET
ABSTRAK
Pewarna alami adalah zat warna alami (pigmen) yang diperoleh dari tumbuh-tumbuhan dan hewan. Zat warna ini telah digunakan sejak dulu dan umumnya dianggap lebih aman daripada zat warna sintetis. Antosianin merupakan salah satu pewarna alami penghasil warna merah, orange, ungu dan biru yang banyak terdapat pada bunga dan buah-buahan. Buah senduduk (Melastoma malabathricum L.) berwarna ungu kemerahan yang menandakan adanya kandungan antosianin, sehingga bisa digunakan sebagai sumber pewarna alami. Tujuan dari penelitian ini adalah untuk mengetahui bahwa ekstrak buah senduduk dapat di gunakan sebagai bahan pewarna tablet dan untuk mengetahui konsentrasi ekstrak buah senduduk yang dapat menghasilkan warna terbaik.
Dalam penelitian ini dilakukan karakterisasi simplisia, skrining fitokimia, ekstraksi zat warna dari buah senduduk, yang dilakukan dengan metode perendaman menggunakan etanol 96% yang mengandung asam asetat 1%. Zat warna buah senduduk diformulasi menjadi pewarna dalam sediaan tablet dengan metode granulasi basah yang dibuat dengan empat konsentrasi yaitu 2, 3, 4 dan 5%. Selanjutnya dilakukan uji preformulasi tablet, pencetakan tablet, evaluasi tablet dan uji organoleptik untuk analisis warna dengan metode Hedonik menggunakan 30 panelis.
Hasil pemeriksaan karakterisasi simplisia buah senduduk yang diperoleh yaitu kadar air 6,65%, kadar sari yang larut dalam air 24,42%, kadar sari yang larut dalam etanol 20,64%, kadar abu total 1,51% dan Kadar abu yang tidak larut dalam asam yaitu 0,48%, dan hasil karakterisasi dari simplisia buah senduduk ini memenuhi persyaratan yang tercantum dalam MMI, edisi IV. Hasil skrining fitokimia serbuk simplisia menunjukkan adanya kandungan flavonoid, glikosida, tanin dan steroid/triterpenoid. Hasil penguapan ekstraks zat warna buah senduduk diperoleh ekstrak kental dengan persen rendemen 9,25%. Pembuatan tablet dengan bobot 300 mg dan diameter 11 mm, memenuhi persyaratan uji preformulasi dan evaluasi tablet. Hasil uji organoleptik diperoleh nilai warna untuk formula F1 (2%) = 7,26, F2 (3%) = 6,8, F3 (4%) = 6,26 dan F4 (5%) = 4,86. Berdasarkan nilai warna yang diperoleh, maka dapat disimpulkan bahwa ekstrak buah senduduk dapat digunakan sebagai pewarna dalam sediaan tablet dan formula F1 (2%) merupakan formula yang paling disukai panelis dan dinyatakan sebagai konsentrasi yang paling baik untuk pewarna tablet.
THE ULITIZATION OF EXTRACT SENDUDUK FRUIT (Melastoma
malabathricum L.) AS TABLETS COLORING AGENT
ABSTRACT
Natural dyes are natural colorants (pigments) obtained from plant, animal or mineral sources. The dyes has been used since old times and are generally considered safer than synthetic dyes. Anthocyanin is a natural dye color-red, orange, purple and blue are found in many flowers and fruits. Senduduk Fruit (Melastoma malabathricum L.) reddish purple color indicating the presence of anthocyanin content, so that it can be used as a source of natural dyes. The purpose of this research was to find out that senduduk fruit extract can be used as tablets coloring agent and to determine the concentration of fruit senduduk extract that can produce the best colors.
In this research, characterization of simplicia, phytochemistry screening, extraction dyes of senduduk fruits performed by maceration method using 96% ethanol containing 1% acetic acid, the dye senduduk fruit formulated into be coloring agent tablets by wet granulation method are made with four concentrations of 2, 3, 4 and 5%. The next performed preformulasi test, scoreded tablets, evaluation tablet and organoleptic test for the analysis of colored by Hedonic method using 30 panelists.
The characteristics of the simplicia senduduk fruit were 6.65% water content, 24.42% water soluble extract content, 20.64% ethanol soluble extract content, 1.51% ashes content and 0.48% acid dissoluble ashes and characterization of senduduk fruit meets the requirements listed in the MMI, edition IV. The result of the phytochemistry screening showsed the presence of flavonoids, glycosides, tannins and steroids/triterpenoids. The results of the dye extract evaporation senduduk fruit obtained concentrated extract with percent yield of 9.25%. Preparation of tablets with a weight of 300 mg and a diameter of 11 mm, meet the requirements of the preformulation test and evaluation tablets. The organoleptic test results obtained the color values for the formulation F1 (2%) = 7.26, F2 (3%) = 6.8, F3 (4%) and F4 = 6.26 (5%) = 4.86. Based on the color values was obtained, it could be concluded that senduduk fruit extracts could be used as tablet coloring agent and formulation F1 (2%) was the most preferred by panelists and expressed as the best concentration for tablets coloring agent.
DAFTAR ISI
Halaman
JUDUL ... i
LEMBAR PENGESAHAN ... ii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xiii
DAFTAR GAMBAR ... xiv
DAFTAR LAMPIRAN ... xv
BAB I PENDAHULUAN ... 1
1.1Latar Belakang ... 1
1.2Perumusan Masalah ... 3
1.3Hipotesis ... 3
1.4Tujuan Penelitian ... 4
1.5Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Uraian Tumbuhan ... 5
2.1.1 Sistematika tumbuhan ... 5
2.1.4 Morfologi tumbuhan ... 6
2.1.5 Kandungan senduduk ... 6
2.1.6 Kegunaan senduduk ... 7
2.1.7 Pewarna alami ... 7
2.1.8 Antosianin ... 8
2.1.9 Ekstraksi ... 9
2.2 Uraian Sediaan Tablet ... 11
2.2.1 Defenisi tablet ... 11
2.2.2 Bentuk tablet ... 12
2.2.3 Bahan pewarna obat ... 13
2.2.4 Metode pembuatan sediaan tablet ... 14
2.3.Uji Penilaian Organoleptik ... 16
2.3.1 Uji kesukaan ... 16
2.3.2 Panel ... 17
BAB III METODE PENELITIAN ... 19
3.1 Alat dan Bahan ... 19
3.1.1 Alat ... 19
3.1.2 Bahan ... 19
3.2 Penyiapan Sampel ... 20
3.2.1 Pengambilan sampel ... 20
3.2.2 Identifikasi sampel ... 20
3.2.3 Pengolahan sampel ... 20
3.3.1 Pereaksi asam klorida 5% ... 21
3.3.2 Pereaksi bouchardat ... 21
3.3.3 Pereaksi dragendorff ... 21
3.3.4 Pereaksi mayer ... 21
3.3.5 Pereaksi molish ... 21
3.3.6 Pereaksi timbal (II) asetat 0,4 M ... 22
3.3.7 Pereaksi kloralhidrat ... 22
3.3.8 Pereaksi asam klorida 2 N ... 22
3.3.9 Pereaksi besi (III) klorida 1% ... 22
3.3.10 Pereaksi liebermann-burchard ... 22
3.4 Skrining Fitokimia Serbuk Simplisia ... 22
3.4.1 Pemeriksaan alkaloida ... 22
3.4.2 Pemeriksaan flavonoida ... 23
3.4.3 Pemeriksaan tanin ... 24
3.4.4 Pemeriksaan glikosida ... 24
3.4.5 Pemeriksaan saponin ... 25
3.4.6 Pemeriksaan steroida/triterpenoida ... 25
3.5 Karakterisasi Simplisia ... 25
3.5.1 Pemeriksaan makroskopik ... 25
3.5.2 Pemeriksaan mikroskopik ... 26
3.5.3 Penetapan kadar air simplisia ... 26
3.5.6 Penetapan kadar abu total ... 27
3.5.7 Penetapan kadar abu tidak larut asam ... 28
3.6 Pembuatan Ekstrak ... 28
3.7 Pembuatan Tablet ... 29
3.7.1 Formula tablet parasetamol ... 29
3.7.2 Pembuatan tablet parasetamol ... 30
3.8 Uji Preformulasi ... 31
3.8.1 Sudut diam granul ... 31
3.8.2 Penentuan waktu alir granul ... 32
3.8.3 Penentuan indeks tap ... 32
3.9 Proses Pencetakan Tablet ... 33
3.10 Evaluasi Tablet ... 33
3.10.1 Keseragaman bobot ... 33
3.10.2 Kekerasan tablet ... 34
3.10.3 Friabilitas ... 34
3.10.4 Waktu hancur ... 34
3.11 Tes Hedonik (kesukaan warna) ... 35
BAB IV HASIL DAN PEMBAHASAN ... 36
4.1 Hasil Identifikasi Tumbuhan ... 36
4.2 Skrining Fitokimia Simplisia ... 36
4.3 Karakterisasi Simplisia ... 36
4.4 Hasil Ekstraksi Buah Senduduk ... 38
4.6 Hasil Evaluasi Tablet ... 41
4.7 Tes Hedonik ... 46
BAB V KESIMPULAN DAN SARAN ... 47
5.1 Kesimpulan ... 47
5.2 Saran ... 47
DAFTAR PUSTAKA ... 48
DAFTAR TABEL
Tabel Halaman
3.1 Formula tablet parasetamol ... 30
3.2 Persyaratan keseragaman bobot ... 33
4.1 Hasil skrining fitokimia simplisia ... 36
4.2 Hasil karakterisasi simplisia ... 38
4.3 Uji preformulasi dari lima formula ... 38
4.4 Hasil keseragaman bobot tablet ... 41
DAFTAR GAMBAR
Gambar Halaman
4.1 Histogram uji waktu alir granul ... 39
4.2 Histogram uji sudut diam granul ... 40
4.3 Histogram uji indeks tap granul ... 40
4.4 Histogram uji keragaman bobot tablet ... 42
4.5 Histogram uji waktu hancur tablet ... 43
4.6 Histogram uji kekerasan tablet ... 44
4.7 Histogram uji friabilitas tablet ... 45
DAFTAR LAMPIRAN
Lampiran Halaman
1. Hasil determinasi tumbuhan ... 51
2. Tumbuhan dan buah senduduk (Melastoma malabathricum L) .... 52
3. Mikroskopik simplisia ... 53
4. Ekstrak buah senduduk . ... 54
5. Gambar sediaan tablet ... 55
6. Perhitungan penetapan karakteristik simplisia ... 56
7. Pembuatan ekstrak buah senduduk ... 61
8. Pembuatan tablet parasetamol dengan zat warna buah senduduk 62
9. Perhitungan persen randemen ekstrak buah senduduk ... 63
10. Contoh perhitungan bahan tablet ... 64
11. Hasil uji preformulasi ... 66
12. Hasil evaluasi tablet ... 67
13. Kuwisioner uji kesukaan warna ... 68
14. Hasil pengamatan warna ... 70
PEMANFAATAN EKSTRAK BUAH SENDUDUK (Melastoma
malabathricum L.) SEBAGAI PEWARNA TABLET
ABSTRAK
Pewarna alami adalah zat warna alami (pigmen) yang diperoleh dari tumbuh-tumbuhan dan hewan. Zat warna ini telah digunakan sejak dulu dan umumnya dianggap lebih aman daripada zat warna sintetis. Antosianin merupakan salah satu pewarna alami penghasil warna merah, orange, ungu dan biru yang banyak terdapat pada bunga dan buah-buahan. Buah senduduk (Melastoma malabathricum L.) berwarna ungu kemerahan yang menandakan adanya kandungan antosianin, sehingga bisa digunakan sebagai sumber pewarna alami. Tujuan dari penelitian ini adalah untuk mengetahui bahwa ekstrak buah senduduk dapat di gunakan sebagai bahan pewarna tablet dan untuk mengetahui konsentrasi ekstrak buah senduduk yang dapat menghasilkan warna terbaik.
Dalam penelitian ini dilakukan karakterisasi simplisia, skrining fitokimia, ekstraksi zat warna dari buah senduduk, yang dilakukan dengan metode perendaman menggunakan etanol 96% yang mengandung asam asetat 1%. Zat warna buah senduduk diformulasi menjadi pewarna dalam sediaan tablet dengan metode granulasi basah yang dibuat dengan empat konsentrasi yaitu 2, 3, 4 dan 5%. Selanjutnya dilakukan uji preformulasi tablet, pencetakan tablet, evaluasi tablet dan uji organoleptik untuk analisis warna dengan metode Hedonik menggunakan 30 panelis.
Hasil pemeriksaan karakterisasi simplisia buah senduduk yang diperoleh yaitu kadar air 6,65%, kadar sari yang larut dalam air 24,42%, kadar sari yang larut dalam etanol 20,64%, kadar abu total 1,51% dan Kadar abu yang tidak larut dalam asam yaitu 0,48%, dan hasil karakterisasi dari simplisia buah senduduk ini memenuhi persyaratan yang tercantum dalam MMI, edisi IV. Hasil skrining fitokimia serbuk simplisia menunjukkan adanya kandungan flavonoid, glikosida, tanin dan steroid/triterpenoid. Hasil penguapan ekstraks zat warna buah senduduk diperoleh ekstrak kental dengan persen rendemen 9,25%. Pembuatan tablet dengan bobot 300 mg dan diameter 11 mm, memenuhi persyaratan uji preformulasi dan evaluasi tablet. Hasil uji organoleptik diperoleh nilai warna untuk formula F1 (2%) = 7,26, F2 (3%) = 6,8, F3 (4%) = 6,26 dan F4 (5%) = 4,86. Berdasarkan nilai warna yang diperoleh, maka dapat disimpulkan bahwa ekstrak buah senduduk dapat digunakan sebagai pewarna dalam sediaan tablet dan formula F1 (2%) merupakan formula yang paling disukai panelis dan dinyatakan sebagai konsentrasi yang paling baik untuk pewarna tablet.
THE ULITIZATION OF EXTRACT SENDUDUK FRUIT (Melastoma
malabathricum L.) AS TABLETS COLORING AGENT
ABSTRACT
Natural dyes are natural colorants (pigments) obtained from plant, animal or mineral sources. The dyes has been used since old times and are generally considered safer than synthetic dyes. Anthocyanin is a natural dye color-red, orange, purple and blue are found in many flowers and fruits. Senduduk Fruit (Melastoma malabathricum L.) reddish purple color indicating the presence of anthocyanin content, so that it can be used as a source of natural dyes. The purpose of this research was to find out that senduduk fruit extract can be used as tablets coloring agent and to determine the concentration of fruit senduduk extract that can produce the best colors.
In this research, characterization of simplicia, phytochemistry screening, extraction dyes of senduduk fruits performed by maceration method using 96% ethanol containing 1% acetic acid, the dye senduduk fruit formulated into be coloring agent tablets by wet granulation method are made with four concentrations of 2, 3, 4 and 5%. The next performed preformulasi test, scoreded tablets, evaluation tablet and organoleptic test for the analysis of colored by Hedonic method using 30 panelists.
The characteristics of the simplicia senduduk fruit were 6.65% water content, 24.42% water soluble extract content, 20.64% ethanol soluble extract content, 1.51% ashes content and 0.48% acid dissoluble ashes and characterization of senduduk fruit meets the requirements listed in the MMI, edition IV. The result of the phytochemistry screening showsed the presence of flavonoids, glycosides, tannins and steroids/triterpenoids. The results of the dye extract evaporation senduduk fruit obtained concentrated extract with percent yield of 9.25%. Preparation of tablets with a weight of 300 mg and a diameter of 11 mm, meet the requirements of the preformulation test and evaluation tablets. The organoleptic test results obtained the color values for the formulation F1 (2%) = 7.26, F2 (3%) = 6.8, F3 (4%) and F4 = 6.26 (5%) = 4.86. Based on the color values was obtained, it could be concluded that senduduk fruit extracts could be used as tablet coloring agent and formulation F1 (2%) was the most preferred by panelists and expressed as the best concentration for tablets coloring agent.
BAB I PENDAHULUAN
1.1Latar Belakang
Pewarna alami adalah zat warna alami (pigmen) yang diperoleh dari tumbuh-tumbuhan dan hewan. Zat warna ini telah di gunakan sejak dulu dan umumnya dianggap lebih aman dari pada zat warna sintetis, pewarna alami dan pewarna identik alami tergolong dalam uncertified color additives karena tidak memerlukan sertifikat kemurnian kimiawi, (Anonim1, 2009).
Zat pewarna yang berasal dari bahan alami yang sudah dikenal dan sering digunakan oleh masyarakat antara lain adalah kurkumin, karotenoid, klorofil dan antosianin. Antosianin merupakan salah satu pewarna alami yang menghasilkan warna merah, orange, ungu dan biru. Banyak terdapat pada bunga dan buah-buahan, seperti bunga mawar, pacar air, kembang sepatu, bunga tasbih/kana, krisan, pelargonium, aster dan buah apel, chery, anggur, strawberi, juga terdapat pada buah manggis dan umbi ubi jalar (Saati dan Hidayat, 2006).
Menurut Sentra informasi IPTEK (2009), buah senduduk (Melastoma
malabathricum Linn) berwarna ungu kemerahan yang menandakan adanya
kandungan antosianin. Sehingga buah senduduk dapat dijadikan sebagai sumber pewarna alami.
menanam, buah senduduk ini bisa dimakan dan meninggalkan warna ungu kemerahan pada lidah setelah memakannya, selain bisa dimakan, buah senduduk bisa digunakan untuk menyembuhkan luka (Anonim2, 2010).
Bahan pewarna sering digunakan untuk makanan, obat-obatan, dan kosmetika. Zat pewarna alami kini telah banyak digantikan dengan pewarna sintetik yang memberikan lebih banyak kisaran warna yang telah dibakukan. Sebagian besar pewarna yang diizinkan untuk digunakan, sudah dipakai sebagai pewarna makanan dan sediaan obat-obatan, juga digunakan sebagai zat diagnostik, desinfektan dan, zat dalam proses pengobatan. Dan sering digunakan sebagai pewarna pada tablet dan gelatin pada kapsul (Anonim 3. 2008).
Departemen Kesehatan RI (2012) mengungkapkan bahwa penggunaan pewarna sintetis secara berkesinambungan dapat menyebabkan kerusakan pada organ hati. Melihat efek samping dari pewarna sintetis yang berbahaya dan didukung gaya hidup back to nature maka masyarakat beralih menggunakan pewarna alami yang aman dikonsumsi.
Sediaan tablet merupakan jenis sediaan yang paling banyak diproduksi dan juga banyak mengalami perkembangan dalam formulasinya. Beberapa keuntungan sediaan tablet adalah sediaan lebih kompak, dosisnya tepat, mudah pengemasannya dan penggunaannya lebih praktis di banding sediaan yang lain (Banker dan Anderson, 1994).
memberi identitas pada produk sehingga memudahkan identifikasi produk. Kedua, pewarna dapat membantu meminimalkan kemungkinan terjadinya kesimpang siuran selama proses produksi. Ketiga, penambahan pewarna pada tablet untuk nilai estetik atau nilai pemasarannya. Bahan pewarna tidak mempunyai aktifitas terapetik, dan tidak dapat meningkatkan bioavailabilitas atau stabilitas produk (Siregar dan Wikarsa, 2010).
Berdasarkan uraian di atas, maka penulis berkeinginan untuk memanfaatkan pewarna alami yang berasal dari buah senduduk untuk digunakan sebagai pewarna pada sediaan tablet.
1.2 Perumusan Masalah
Berdasarkan uraian diatas maka perumusan masalah pada penelitian ini adalah:
a. Apakah ekstrak buah senduduk dapat digunakan sebagai pewarna dalam sediaan tablet.
b. Berapakah konsentrasi ekstrak buah senduduk yang menghasilkan warna terbaik.
1.3 Hipotesis
Berdasarkan perumusan masalah diatas, maka dibuat hipotesis sebagai berikut:
a. Ekstrak buah senduduk dapat digunakan sebagai pewarna dalam sediaan tablet.
1.4 Tujuan Penelitian
Tujuan dari penelitian ini adalah sebagai berikut:
a. Untuk mengetahui bahwa ekstrak buah senduduk dapat di gunakan sebagai pewarna dalam sediaan tablet.
b. Untuk mengetahui konsentrasi ekstrak buah senduduk yang dapat menghasilkan warna terbaik.
1.5 Manfaat penelitian
Manfaat dari penelitian ini adalah sebagai berikut:
a. Memberikan informasi bahwa buah senduduk dapat digunakan sebagai pewarna alami untuk sediaan tablet.
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan 2.1.1 Sistematika Tumbuhan Divisi : Spermatophyta Sub divisi : Angiospermae Kelas : Dicotyledoneae Bangsa : Myrtales
Suku : Melastomataceae Marga : Melastoma
Jenis : Melastoma malabathricum L 2.1.2 Sinonim
Nama lain dari senduduk (Melastoma malabathricum L) adalah Melastoma affine G. Don., Melastoma polyanthum BI (Ditjen POM, 1995). 2.1.3 Nama Daerah
2.1.4 Morfologi Tumbuhan
Tumbuhan senduduk (Melastoma malabathricum L.) tumbuh liar pada tempat-tempat yang mendapat cukup sinar matahari, seperti di lereng gunung, semak belukar, lapangan yang tidak terlalu gersang, atau di daerah objek wisata sebagai tanaman hias dan dapat tumbuh sampai ketinggian 1.650 m di atas permukaan air laut. Perdu, tegak, tinggi 0,5-4 m, banyak bercabang, bersisik, berambut. Daun tunggal, bertangkai, letak berhadapan silang. Helai daun bundar telur, memanjang sampai lonjong, ujung lancip, pangkal membulat, tepi rata, permukaan berambut pendek yang jarang dan kaku sehingga teraba kasar. Berbunga majmuk keluar diujung cabang, warna ungu kemerahan. Buah masak akan merekah dan terbagi atas beberapa bagian, warnanya ungu tua kemerahan. Biji kecil warnanya coklat. Buahnya dapat dimakan, sedangkan daun muda dapat dimakan sebagai lalap atau disayur. Perbanyakan dengan biji ( Dalimartha, 2000).
2.1.5 Kandungan Senduduk
Menurut Departemen Kesehatan RI 1995, tumbuhan senduduk (Melastoma malabathricum Linn) mengandung senyawa flavonoid, tanin,, steroida/triterpenoida.
Kandungan kimia tumbuhan senduduk yang sudah diketahui antara lain saponin, flavonoid dan tanin ( Arief, 2011).
2.1.6 Kegunaan Senduduk
Tanaman ini berkhasiat sebagai penurun panas, penghilang rasa sakit, peluruh urine, penghilang bengkak, pelancar aliran darah, dan penghenti pendarahan (hemostatik) (Arief, 2009).
Menurut Sentra informasi IPTEK (2009) Buah senggani dapat dijadikan sebagai sumber pewarna alami.
2.1.7 Pewarna Alami
Pewarna telah lama digunakan pada makanan untuk meningkatkan cita rasanya. Pada mulanya zat warna yang digunakan adalah zat warna alami dari tumbuhan dan hewan. Pewarna alami sebenarnya tidak semahal yang diperkirakan masyarakat dan pembuatannya juga sangat mudah. Bahan-bahan yang dapat digunakan sebagai pewarna ditumbuk, dapat pula menggunakan blender atau penumbuk biasa dengan sedikit ditambah air, lalu diperas dan disaring dengan alat penyaring (Saati dan Hidayat, 2006).
Menurut Saati dan Hidayat, (2006) beberapa contoh pewarna alami yang biasa digunakan untuk mewarnai makanan yaitu:
1. Karoten, memberikan warna jingga sampai merah. Dapat diperoleh dari wortel, pepaya dan sebagainya.
2. Biksin, memberikan warna kuning seperti mentega. Biksin diperoleh dari biji pohon Bixa orellana yang terdapat didaerah tropis.
4. Klorofil, memberikan warna hijau dan diperoleh dari daun. Banyak digunakan untuk makanan dan saat ini mulai digunakan pada berbagai produk kesehatan. Pigmen klorofil banyak terdapat pada dedaunan seperti daun suji, daun pandan, daun katuk dan sebagainya. Dedaunan tersebut sebagai penghasil warna hijau untuk berbagai jenis kue jajanan pasar. Selain menghasilkan warna hijau yang cantik, juga memiliki aroma yang khas.
5. Antosianin, memberikan warna merah, orange, ungu dan biru. Banyak terdapat pada bunga dan buah-buahan seperti bunga mawar, pacar air, kembang sepatu, bunga tasbih, anggur, buah apel, stroberi, buah manggis dan lain-lain.
6. Kurkumin, berasal dari kunyit sebagai salah satu bumbu dapur dan memberikan warna kuning.
2.1.8 Antosianin
Antosianin juga tidak stabil pada suhu yang tinggi, sehingga larutan sebaiknya disimpan di tempat gelap dan suhu dingin (Harborne, 1996).
2.1.9 Ekstraksi
Ekstraksi adalah kegiatan penarikan kandungan kimia yang dapat larut sehingga terpisah dari bahan yang tidak dapat larut dengan pelarut cair. Simplisia yang diekstrak mengandung senyawa aktif yang dapat larut dan senyawa yang tidak dapat larut seperti serat, karbohidrat, protein dan lain-lain. Menurut Ditjen POM (2000), ada beberapa metode ekstraksi yang sering digunakan dalam berbagai penelitian antara lain yaitu:
A. Cara dingin 1. Maserasi
Maserasi adalah proses penyarian simplisia dengan cara perendaman menggunakan pelarut dengan sesekali pengadukan pada temperatur kamar. Maserasi yang dilakukan pengadukan secara terus-menerus disebut maserasi kinetik sedangkan yang dilakukan pengulangan penambahan pelarut setelah dilakukan penyaringan terhadap maserat pertama dan seterusnya disebut remaserasi.
2. Perkolasi
ekstrak) terus menerus sampai diperoleh perkolat yang jumlahnya 1-5 kali bahan.
B. Cara panas 1. Refluks
Refluks adalah proses penyarian simplisia dengan menggunakan alat pada terperatur titik didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan adanya pendingin balik.
2. Digesti
Digesti adalah proses penyarian dengan pengadukan kontinu pada temperatur lebih tinggi dari pada temperatur ruangan, yaitu secara umum dilakukan pada temperatur 40o-50oC.
3. Sokletasi
Sokletasi adalah proses penyarian dengan menggunakan pelarut yang selalu baru, dilakukan dengan menggunakan alat soklet sehingga menjadi ekstraksi kontinu dengan pelarut relatif konstan dengan adanya pendingin balik.
4. Infudasi
Infudasi adalah proses penyarian dengan menggunakan pelarut air pada temperatur 90oC selama 15 menit.
5. Dekoktasi
2.2 Uraian Sediaan Tablet 2.2.1 Defenisi tablet
Defenisi tablet menurut Farmakope Indonesia edisi III adalah sediaan padat kompak, dibuat secara kempa cetak, dalam bentuk tabung pipih atau sirkuler, kedua permukaannya rata atau cembung, mengandung satu jenis obat atau lebih, dengan atau tanpa bahan tambahan. Bahan tambahan yang dapat berfungsi sebagai bahan pengisi, bahan pengembang, bahan pengikat, bahan pelicin, bahan pembasah atau bahan lain yang cocok.
Tablet merupakan jenis sediaan yang banyak di gunakan sampai sekarang karena memberikan dosis yang tepat pada pemakaiannya, mudah pemakaiannya, mudah pengemasannya, stabilitas kimia dan aktifitas fisiologis dari bahan-bahan obat cukup baik (Banker dan Anderson, 1994).
Menurut Banker dan Anderson (1994), tablet yang dinyatakan baik harus memenuhi syarat, yaitu:
a. Memiliki kemampuan atau daya tahan terhadap pengaruh mekanis selama proses produksi, pengemasan dan distribusi.
b. Bebas dari kerusakan seperti pecah pada permukaan dari sisi-sisi tablet c. Dapat menjamin kestabilan fisik maupun kimia dari zat berkhasiat yang
terkandung didalamnya.
d. Dapat membebaskan zat berkhasiat dengan baik sehingga memberikan efek pengobatan seperti yang dikehendaki.
(yang meningkatkan mutu sediaan tablet, kelancaran sifat aliran bebas, sifat kohesifitas, kecepatan disintegrasi, dan sifat antilekat) dan dibuat dengan mengempa campuran serbuk dalam mesin tablet. Definisi lain tablet kempa adalah unit bentuk sediaan solid, dibuat dengan mengempa suatu campuran serbuk yang mengandung zat aktif dengan atau tanpa bahan tanbahan atau bahan tertentu yang dipilih guna membantu dalam proses pembuatan dan untuk menciptakan sifat-sifat sediaan tablet yang dikehendaki (Siregar dan Wikarsa, 2010).
2.2.2 Bentuk tablet
Tablet terdapat dalam berbagai ragam bentuk, ukuran, bobot, kekerasan, ketebalan, dan dalam aspek lain, tergantung pada penggunaan yang dimaksudkan dan metode penggunaannya. Tablet biasanya berbentuk bundar dengan permukaan datar, atau konveks. Bentuk khusus seperti kaplet, segitiga, lonjong, empat segi, dan segi enam (heksagonal) dikembangkan oleh beberapa pabrik untuk membedakan produknya terhadap produk pabrik lainnya. Tablet dapat dihasilkan dalam berbagai bentuk, dengan membuat punch dan lubang kempa (lesung tablet) cetakan yang didesain secara khusus. Misalnya jika
punch kurang konkaf makin datar tablet yang dihasilkan. Sebaliknya punch
yang semakin konkaf, semakin lebih konveks tablet yang dihasilkan.
Tablet adalah sediaan solid mengandung zat aktif yang dapat diberikan secara oral dan ditelan, tablet yang hanya ditempatkan dirongga mulut tanpa ditelan, tablet oral yang dikunyah dulu lalu ditelan, atau hanya dikulum/dihisap (Siregar dan Wikarsa, 2010).
2.2.3 Bahan pewarna obat
Bahan pewarna pada dasarnya jenis yang digunakan pada produk obat adalah sama dengan jenis bahan pewarna yang digunakan pada makanan. Dengan demikian semua jenis bahan pewarna yang diizinkan digunakan pada makanan, diizinkan pula untuk digunakan dalam produk obat, pada umumnya digunakan untuk sediaan-sediaan sirup, tablet dan tablet salut.
Penggunaan bahan pewarna dalam obat konsentrasinya relatif sangat kecil apabila dibandingkan penggunaannya dalam makanan. Dilain pihak penggunaan obat itu sendiri mempunyai dosis dan aturan pakai yang tepat. Dengan demikian bahan pewarna dalam obat yang dikonsumsi oleh manusia jumlahnya sangat kecil dan hampir tidak berarti. Yang perlu diperhatikan adalah bahwa penggunaan bahan pewarna harus dilakukan secara tepat, yang ditinjau dari aspek proses teknologi produksi yang berpengaruh pada penampilan tablet (Anonim4, 1984).
Ada 2 cara penambahan zat pewarna yaitu: Cara Basah
Bahan warna dilarutkan dalam larutan bahan pengikat, kemudian ditambahkan kedalam serbuk yang akan digranulasi.
Cara Kering
Bahan warna dicampurkan dalam keadaan kering ke dalam campuran serbuk, kemudian baru ditambahkan bahan pengikat. Konsentrasi zat pewarna yang biasa dipakai 0.33% (Soekemi, 1987).
2.2.4 Metode pembuatan sediaan tablet
Metode pembuatan tablet didasarkan pada sifat fisika kimia dari bahan obat, seperti stabilitas dari bahan aktif dalam panas atau terhadap air, bentuk partikel bahan aktif dan sebagainya.
Metode pembuatan sediaan tablet yaitu: 1. Cetak Lansung
Cetak lansung adalah pencetakan bahan obat atau campuran bahan obat, bahan pembantu tanpa proses pengolahan awal. Cara ini hanya dilakukan untuk bahan-bahan tertentu saja yang berbentuk Kristal/butir-butir granul yang mempunyai sifat-sifat yang diperlukan untuk membuat tablet yang baik.
lansung, seperti ammonium bromida, ammonium klorida, kalium bromida, kalium klorida, natrium bromida, natrium klorida dan heksamin (Voigt, 1995). 2. Granulasi Kering
Granulasi kering disebut juga slugging atau prekompresi. Cara ini sangat tepat untuk tabletasi zat-zat yang peka suhu atau bahan obat yang tidak stabil dengan adanya air.
Obat dan bahan pembantu pada mulanya dicetak dulu, artinya mula-mula dibuat tablet yang cukup besar, yang massanya tidak tertentu. Selanjutnya dilakukan penghancuran tablet dengan proses penggranul kering, atau dalam hal yang sederhana dilakukan atas sebuah ayakan. Granulat yang dihasilkan kemudian decetak dengan takaran yang dikehendaki (Voigt, 1995).
3. Granulasi Basah
Pada tehnik ini juga memerlukan langkah-langkah pengayakan, pencampuran dan pengeringan. Pada granulasi basah, granul dibentuk dengan suatu bahan pengikat. Teknik ini membutuhkan larutan, suspensi atau bubur yang mengandung pengikat yang biasanya ditambahkan ke campuran serbuk. Cara penambahan bahan pengikat tergantung pada kelarutannya dan tergantung pada komponen campuran. Karena massa hanya sampai konsistensi lembab, bukan basah seperti pasta, maka bahan pengikat yang ditambahkan tidak boleh berlebihan (Banker dan Anderson, 1994).
granul lebih kompak, meningkatkan luas permukaan untuk memudahkan pengeringan.
Proses pengeringan diperlukan oleh seluruh cara granulasi basah untuk menghilangkan pelarut yang dipakai pada pembentukan gumpalan-gumpalan granul dan untuk mengurangi kelembaban sampai pada tingkat yang optimum (Banker dan Anderson, 1994).
2.3. Uji Penilaian Organoleptik 2.3.1 Uji Kesukaan
Uji kesukaan juga disebut uji hedonik. Dalam uji hedonik panelis dimintakan tanggapan pribadinya tentang kesukaan atau sebaliknya ketidak sukaan. Disamping panelis mengemukakan tanggapan senang, suka atau kebalikannya, mereka juga mengemukakan tingkat kesukaannya. tingka-tingkat kesukaan ini disebut skala hedonik. Misalnya dalam hal suka, dapat mempunyai skala hedonik seperti: amat sangat suka, sangat suka, suka dan agak suka. Sebaliknya jika tanggapan itu tidak suka, dapat mempunyai skala hedonik seperti: amat sangat tidak suka, sangat tidak suka, tidak suka dan agak tidak suka. Kemudian skala hedonik ini ditrasformasikan menjadi skala nomerik untuk dilakukan perhitungan berdasarkan tingkat kesukaan panelis (Soekarto, 1985).
2.3.2 Panelis
BAB III
METODE PENELITIAN
Penelitian ini menggunakan metode experimental. Penelitian ini meliputi tahapan penelitian yaitu identifikasi sampel, penyiapan sampel, skrining fitokimia, karakterisasi simplisia, pembuatan ekstrak, pembuatan sediaan tablet, uji preformulasi tablet, evaluasi tablet dan uji kesukaan warna (tes hedonik). Penelitian ini dilakukan di Laboratorium Farmakognosi dan Laboratorium Teknologi Sediaan Tablet Fakultas Farmasi USU Medan.
3.1 Alat dan Bahan 3.1.1 Alat-alat
Alat-alat yang digunakan dalam penelitian ini adalah alat-alat gelas laboratorium, lemari pengering, neraca listrik (Vibra), seperangkat alat destilasi penetapan kadar air, rotary evaporator, blender (National), mikroskop (Olympus), penangas air, mortir dan stamfer, mesin cetak tablet singel punch,
Hardness tester (copley), Friabilator (copley), Disintegration Tester (Copley)
stopwatch, termometer, hair drayer, ayakan, cawan porselen, beaker glas,
aluminium foil dan kertas saring. 3.1.2 Bahan
3.2 Penyiapan Sampel
Penyiapan sampel meliputi pengambilan sampel, identifikasi sampel, dan pengolahan sampel.
3.2.1 Pengambilan sampel
Pengambilan sampel dilakukan secara purposif, yaitu tanpa membandingkan dengan tumbuhan yang sama dari daerah lain. Bagian yang digunakan adalah buah senduduk masak yang berwarna hitam keunguan yang diambil dari Desa Saree, Kecamatan Jantho, Kabupaten Aceh Besar, Provinsi Nanggroe Aceh Darussalam.
3.2.2 Identifikasi sampel
Identifikasi tumbuhan dilakukan di laboratorium Herbarium Bogoriensi, Bidang Botani Pusat Penelitian Biologi-LIPI. Hasil dapat dilihat pada Lampiran 1, di halaman 48
3.2.3 Pengolahan sampel
3.3 Pembuatan Pereaksi
3.3.1 Pereaksi asam klorida 5%
Sebanyak 135 ml asam klorida pekat diencerkan dengan air suling hingga 1 liter (Ditjen POM, 1979).
3.3.2 Pereaksi bouchardat
Empat g kalium iodida dilarutkan dalam air suling secukupnya, ditambahkan 2 g iodium, dan ditambahkan air suling hingga 100 ml (Ditjen POM, 1989).
3.3.3 Pereaksi dragendorff
Delapan g bismuth (III) nitrat dilarutkan dalam 20 ml asam nitrat pekat. Pada wadah lain ditimbang 27,2 g kalium iodida lalu dilarutkan dalam 50 ml air suling. Campurkan kedua larutan dan diamkan sampai memisah sempurna. Ambil larutan jernih dan encerkan dengan air suling hingga 100 ml (Ditjen POM, 1989).
3.3.4 Pereaksi mayer
Sebanyak 1,4 g raksa (II) klorida dilarutkan dalam air suling hingga 60 ml. pada wadah lain ditimbang sebanyak 5 g kalium iodida lalu dilarutkan dalam 10 ml air suling. Keduanya dicampur dan ditambahkan air suling hingga 100 ml (Ditjen POM, 1989).
3.3.5 Pereaksi molish
3.3.6 Pereaksi timbal (II) asetat 0,4 M
Sebanyak 15,17 g timbal (II) asetat dilarutkan dalam air suling bebas karbondioksida hingga 100 ml (Ditjen POM, 1989).
3.3.7 Pereaksi kloralhidrat
Sebanyak 50 g kloralhidrat dilarutkan dalam 20 ml air suling (Ditjen POM, 1989).
3.3.8 Pereaksi asam klorida 2 N
Sebanyak 17 ml asam klorida pekat diencerkan dengan air suling hingga 100 ml (Ditjen POM, 1979).
3.3.9 Pereaksi besi (III) klorida 1%
Satu g besi (III) klorida dilarutkan dalam air suling hingga 100 ml (Ditjen POM, 1979).
3.3.10 Pereaksi liebermann-burchard
Sebanyak 2 bagian asam asetat anhidrat dicampur dengan satu bagian asam sulfat pekat (Ditjen POM, 1979).
3.4 Skrining Fitokimia Serbuk Simplisia
Skrining fitokimia serbuk simplisia meliputi pemeriksaan alkaloida, pemeriksaan flavonoida, pemeriksaan tanin, pemeriksaan glikosida, pemeriksaan saponin, pemeriksaan steroid/triterpenoid.
3.4.1 Pemeriksaan alkaloida
Filtrat dipakai untuk percobaan berikut:
• Filtrat sebanyak 3 tetes ditambahkan 2 tetes larutan pereaksi Mayer akan terbentuk endapan berwarna putih atau putih kekuningan
• Filtrat sebanyak 3 tetes ditambahkan 2 tetes larutan pereaksi Bouchardat akan terbentuk endapan berwarna coklat kemerahan sampai coklat kehitaman
• Filtrat sebanyak 3 tetes ditambahkan 2 tetes larutan pereaksi Dragendorf akan terbentuk endapan berwarna kuning jingga
Alkaloida dinyatakan positif jika terjadi endapan atau terjadi endapan paling sedikit dua dari tiga percobaan di atas (Ditjen POM, 1995).
3.4.2 Pemeriksaan flavonoida
Sebanyak 0,5 g serbuk simplisia disari dengan 10 ml metanol lalu direfluks selama 10 menit, disaring panas-panas melalui kertas saring berlipat, filtrat diencerkan dengan 10 ml air suling. Setelah dingin ditambah 5 ml petroleum benzen, dikocok hati-hati, lalu didiamkan sebentar. Lapisan metanol diambil, diuapkan pada temperatur 40oC. Sisanya dilarutkan dalam 5 ml etil asetat, disaring. Filtratnya digunakan untuk uji flavonoid.
Filtrat dipakai untuk percobaan berikut:
b. Sebanyak 1 ml filtrat diuapkan hingga kering, sisanya dilarutkan dalam 1-2 ml etanol 96%, ditambahkan 0,1 g magnesium dan 10 ml asam klorida pekat, terjadi warna merah jingga sampai warna merah ungu menunjukkan adanya flavonoid. (Ditjen POM, 1995).
3.4.3 Pemeriksaan tanin
Sebanyak 0,5 g serbuk simplisia disari dengan 10 ml air suling selama 15 menit kemudian disaring, filtratnya diencerkan dengan air suling sampai hampir tidak berwarna. Diambil 2 ml filtrat dan ditambahkan 1-2 tetes pereaksi besi (III) klorida 1%. Jika terjadi warna biru kehitaman atau hijau kehitaman menunjukkan adanya tanin (Farnsworth, 1966).
3.4.4 Pemeriksaan glikosida
cincin berwarna ungu pada batas cairan, reaksi ini menunjukkan adanya ikatan gula (Ditjen POM, 1995).
3.4.5 Pemeriksaan saponin
Sebanyak 0,5 g serbuk simplisia dimasukkan ke dalam tabung reaksi dan ditambahkan 10 ml air suling panas, didinginkan kemudian dikocok kuat-kuat selama 10 detik, timbul busa yang mantap tidak kurang dari 10 menit setinggi 1-10 cm. Ditambahkan 1 tetes larutan asam klorida 2 N, bila buih tidak hilang menunjukkan adanya saponin (Ditjen POM, 1995).
3.4.6 Pemeriksaan steroida/triterpenoida
Sebanyak 1 g serbuk simplisia dimaserasi dengan 20 ml eter selama 2 jam, lalu disaring. Filtrat diuapkan dalam cawan penguap. Pada sisa dalam cawan penguap ditambahkan 2 tetes asam asetat anhidrat dan 1 tetes asam sulfat pekat. Timbul warna ungu dan merah kemudian berubah menjadi hijau kebiruan menunjukkan adanya steroida triterpenoida (Harborne, 1987).
3.5 Pemeriksaan Karakterisasi Simplisia
Pemeriksaan karakterisasi simplisia meliputi pemeriksaan makroskopik dan mikroskopik, penetapan kadar air, penetapan kadar sari yang larut dalam air, penetapan kadar sari yang larut dalam etanol, penetapan kadar abu total, dan penetapan kadar abu tidak larut asam (Ditjen POM, 1995).
3.5.1 Pemeriksaan makroskopik
3.5.2 Pemeriksaan mikroskopik
Pemeriksaan mikroskopik terhadap serbuk simplisia dilakukan dengan cara meneteskan kloralhidrat diatas kaca objek, kemudian diatasnya diletakkan serbuk simplisia lalu ditutup dengan kaca penutup dan dilihat dibawah mikroskop.
3.5.3 Penetapan kadar air simplisia
Penetapan kadar air dilakukan dengan metode Azeotripi (destilasi toluene). Alat terdiri dari labu alas 500 ml, alat penampung, pendingin, tabung penyambung dan tabung penerima.
3.5.4 Penetapan kadar sari yang larut dalam air
Sebanyak 5 g serbuk yang telah dikeringkan di udara, dimaserasi selama 24 jam dalam 100 ml air kloroform (2,5 ml kloroform dalam air suling 1000 ml) dalam labu bersumbat sambil sesekali dikocok selama 6 jam pertama, dibiarkan selama 18 jam, kemudian disaring. Diuapkan 20 ml filtrat sampai kering dalam cawan penguap yang berdasar rata yang telah dipanaskan dan ditara. Sisa dipanaskan pada suhu 1050C sampai bobot tetap. Kadar dalam persen sari yang larut dalam air dihitung terhadap bahan yang telah dikeringkan diudara (Ditjen POM, 1995).
3.5.5 Penetapan kadar sari yang larut dalam etanol
Sebanyak 5 g serbuk yang telah dikeringkan diudara, dimaserasi selama 24 jam dalam etanol 96% dalam labu bersumbat sambil sesekali dikocok selama 6 jam pertama, dibiarkan selama 18 jam, kemudian disaring. diuapkan 20 ml filtrat sampai kering dalam cawan penguap yang berdasar rata yang telah dipanaskan dan ditara. Sisa dipanaskan pada suhu 105oC sampai bobot tetap. Kadar dalam persen sari yang larut dalam etanol (96%) dihitung terhadap bahan yang telah dikeringkan diudara (Ditjen POM, 1995).
3.5.6 Penetapan kadar abu total
ditimbang sampai diperoleh bobot tetap. Kadar abu dihitung terhadap bahan yang telah dikeringkan diudara (Ditjen POM, 1995).
3.5.7 Penetapan kadar abu tidak larut asam
Abu yang telah diperoleh dalam penetapan abu didihkan dengan 25 ml asam klorida encer selama 5 menit, bagian yang tidak larut dalam asam dikumpulkan, disaring dengan kertas masir atau kertas saring bebas abu, cuci dengan air panas, dipijarkan sampai bobot tetap, kemudian dinginkan dan ditimbang. Kadar abu yang tidak larut dalam asam dihitung terhadap bobot yang dikeringkan diudara (Ditjen POM, 1995).
3.6 Pembuatan Ekstrak
Buat ekstrak dari serbuk kering simplisia dengan cara maserasi menggunakan pelarut yang sesuai. Gunakan pelarut yang dapat menyari sebagian besar metabolit sekunder yang terkandung dalam serbuk simplisia. Jika tidak dinyatakan lain gunakan etanol 70%.
Masukkan satu bagian serbuk kering simplisia ke dalam maserator, tambahkan 10 bagian pelarut. Rendam selama 6 jam pertama sambil sekali-kali diaduk, kemudian diamkan selama 18 jam. Pisahkan maserat dengan cara filtrasi. Ulangi proses penyarian sekurang-kurangnya dua kali dengan jenis dan jumlah pelarut yang sama. Kumpulkan semua maserat, kemudian uapkan dengan penguap tekanan rendah hingga diperoleh ekstrak kental.
Pembuatan ekstrak bisa dilakukan dengan cara lain seperti perkolasi, sokletasi dan metode lain sebagainya (Ditjen POM, 2010).
Pembuatan ekstrak buah senduduk dilakukan dengan metode maserasi, Prosudur pembuatan ekstrak sebagai berikut: sebanyak 200,017 g Serbuk simplisia dimasukkan ke dalam wadah kemudian direndam dengan pelarut etanol 96% yang mengandung asam asetat 1% sebanyak 2000 ml (perbandingan sampel dan pelarut l:10) lalu ditutup dan disimpan pada suhu ruangan. Dimaserasi selama 24 jam sambil sekali-kali diaduk selama 6 jam pertama. Setelah 24 jam maserat disaring, kemudian dimaserasi lagi dengan penambahan pelarut yang baru, Dilakukan perlakuan yang sama. Kemudian Seluruh filtrat digabungkan dan diuapkan menggunakan rotary evaporator pada temperatur ± 40oC sampai diperoleh ekstrak kental, kemudian dipekatkan dengan freeze dryer selama ± 24 jam.
3.7 Pembuatan tablet
Formula tablet parasetamol dapat dilihat pada Tabel 2.1 dibawah ini: Tabel 3. 1 Formula tablet parasetamol
Bahan tambahan Formula
F1 F2 F3 F4 F5
Konsentrasi zat warna buah senduduk 2% 3% 4% 5% - Zat warna buah senduduk (g) 0,6 0,9 1,2 1,5 -
Parasetamol (g) 12 12 12 12 12
Amilum manihot (g) 1,5 1,5 1,5 1,5 1,5
Talkum (g) 0,3 0,3 0,3 0,3 0,3
Mg stearat (g) 0,3 0,3 0,3 0,3 0,3
Manitol (g) 3 3 3 3 3
Mucilago amili 10% (g) 6 6 6 6 6
Laktosa (g) 6,3 6 5,7 5,4 6,9
Berat 100 tablet (g) 30 30 30 30 30
3.7.2 Pembuatan tablet parasetamol dengan zat warna buah senduduk Pembuatan tablet parasetamol dengan zat warna buah senduduk dilakukan dengan cara:
2. Pembuatan mucilago amili 10%
Cawan porselen dan batang pengaduk ditara, ditimbang mucilago amili, lalu disuspensikan dengan aquades, selanjutnya dipanaskan pada api kecil sambil diaduk-aduk hingga diperoleh massa yang transparan, didinginkan dan dicek beratnya, kekurangan berat di cukupkan dengan aquades panas, dan kelebihan berat diuapkan kembali, ditimbang lagi, hingga diperoleh massa yang sesuai (massa 2).
3. Massa 2 ditambahkan sedikit demi sedikit ke massa 1, sambil digerus hingga diperoleh massa yang kompak, lalu digranulasi dengan ayakan mesh 12.
4. Granulasi dikeringkan pada suhu 40o-60o C pada lemari pengering. 5. Setelah kering, granulat diayak lagi dengan ayakan mesh 14 dan dicek
kembali beratnya.
6. Ditambahkan Mg-stearat, talkum dan bahan pengembang luar. 7. Massa granul diuji preformulasi dan dicetak menjadi tablet. 3.8 Uji preformulasi
Uji preformulasi yang dilakukan adalah penentuan sudut diam granul, penentuan waktu alir granul, penentuan indeks tap.
3.8.1 Sudut diam granul
Penentuan sudut diam granul dilakukan dengan cara:
penutup bawah corong dibuka dan dibiarkan granul mengalir melalui corong dan ditentukan besar sudut diamnya dengan rumus sebagai berikut:
Rumus untuk mengukur sudut diam : Tg Ө = 2�
�
Ө = sudut diam
H = tinggi tumpukan granul (cm) D = diameter tumpukan granul (cm) Syarat: 20° < θ < 40° (Cartensen, 1977). 3.8.2 Penentuan waktu alir granul
Penentuan waktu alir granul dilakukan dengan cara:
Ditimbang 100 g granul, kemudian dimasukkan ke dalam corong yang telah dirangkai kemudian permukaannya diratakan. Penutup bawah dibuka bersamaam dengan dihidupkan stopwatch. Stopwatch dihentikan tepat pada saat granul habis melewati corong dan dicatat waktu alirnya. Persyaratan dari waktu alir granul yaitu lebih kecil dari 10 detik (Voigt, 1995).
3.8.3 Penentuan indeks tap
Penentuan indeks tap dilakukan dengan cara:
Indeks tap dapat dihitung dengan rumus: Indeks tap = �1−�2
�1 x100% Keterangan :
V1 = volume sebelum hentakan V2 = volume setelah hentakan Syarat indeks tap lebih kecil dari 20% (Voigt, 1995). 3.9 Proses Pencetakan Tablet
Proses pencetakan tablet yaitu massa granul dicetak menjadi tablet dengan berat 300 mg dan diameter penampang 11 mm.
3.10 Evaluasi Tablet
Evaluasi tablet yang dilakukan adalah keseragaman bobot, kekerasan tablet, friabilitas, dan waktu hancur.
3.10.1 Keseragaman bobot
Penetapan keseragaman bobot dilakukan dengan cara:
Ditimbang 20 tablet, hitung bobot rata-rata tiap tablet, lalu ditimbang tablet satu persatu.
Deviasi = Bobot tablet−bobot rata−rata
Bobot rata−rata x 100%
Tabel 3.2 Persyaratan keseragaman bobot
Bobot rata-rata Penyimpangan terhadap bobot rata-rata
A B
Persyaratan tidak boleh lebih dari 2 tablet yang masing-masing bobotnya menyimpang dari bobot rata-rata dari harga yang ditetapkan pada kolom A dan tidak boleh satu tablet yang menyimpang dari bobot rata-rata dari harga yang ditetapkan pada kolom B.
Jika tidak mencukupi 20 tablet, dapat digunakan 10 tablet dengan persyaratan: Tidak satu tabletpun yang bobotnya menyimpang lebih besar dari bobot rata-rata yang ditetapkan pada kolom A dan kolom B (Ditjen POM, 1979).
3.10.2 Kekerasan tablet Alat: Hardness Tester (Copley)
3.10.3 Friabilitas
Alat: Friabilator (Copley)
Cara: Ditimbang 20 tablet yang telah dibersihkan dari debu, dicatat beratnya (a gram). Tablet dimasukkan ke dalam alat friabilator, lalu alat dijalankan selama 4 menit (100 kali putaran). Setelah batas waktu yang ditentukan tablet dikeluarkan dan dibersihkan dari debu, lalu ditimbang beratnya (b gram). Friabilitas (F) = (a – b)/a x 100%.
(Sharma, et al., 2011). 3.10.4 Waktu hancur
Alat: Disintegration Tester (Copley)
Cara: Pengujian dilakukan terhadap 6 tablet. Dimasukkan 1 tablet pada masing–masing tabung dari keranjang dan masukkan satu cakram pada tiap-tiap tabung kemudian alat dijalankan. Digunakan air dengan suhu 37˚±2˚C sebagai media kecuali dinyatakan menggunakan cairan lain dalam masing-masing monografi. Pada akhir batas waktu seperti yang tertera pada monografi, angkat keranjang dan amati keenam tablet. Semua tablet harus hancur sempurna. Bila satu tablet atau dua tablet tidak hancur sempurna, ulangi pengujian dengan 12 tablet lainnya.
Persyaratannya: tidak kurang 16 dari 18 tablet yang diuji harus hancur sempurna (Ditjen POM, 1979).
3.11 Tes Hedonik (kesukaan warna)
menceklis pada angka 9 bila amat sangat suka, 8 bila sangat suka, 7 bila suka, 6 bila agak suka, 5 bila netral, 4 bila agak tidak suka, 3 bila tidak suka, 2 bila sangat tidak suka, dan 1 bila amat sangat tidak suka (BSN, 2006).
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Identifikasi Tumbuhan
Tumbuhan yang digunakan diidentifikasi di Herbarium Bogoriense Pusat Penelitian Biologi-LIPI Bogor. Hasil identifikasi tumbuhan yang diteliti adalah buah senduduk (Melastoma malabathricum L.), suku Melastomataceae. 4.2 Skrining Fitokimia Simplisia
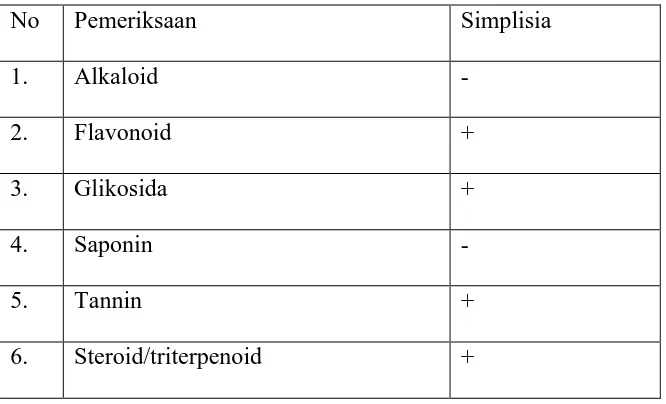
Hasil skrining fitokimia serbuk simplisia menunjukkan adanya kandungan flavonoid, glikosida, tanin dan steroid/triterpenoid. Hasil pemeriksaan skrining fitokimia dapat dilihat dari Tabel 4.1 di bawah ini:
Tabel 4.1 Hasil Pemeriksaan Skrining Fitokimia Simplisia
No Pemeriksaan Simplisia
1. Alkaloid -
2. Flavonoid +
3. Glikosida +
4. Saponin -
5. Tannin +
6. Steroid/triterpenoid +
4.3 Karakterisasi Simplisia
Hasil pemeriksaaan makroskopik dari buah senduduk segar menunjukkan: bakal buah terdiri dari 5 ruas yang dihubungkan oleh tabung kelopak, buah buni, berbentuk periuk, buah masak akan merekah dan terbagi atas beberapa bagian, tidak beraturan, pada daging buah terdapat biji berwarna coklat, buahnya kecil dengan ukuran garis rentang lebih kurang 1,3 cm, berwarna ungu kemerahan (gelap), dengan rasa sepat-sepat manis.
Hasil pemeriksaan mikroskopik simplisia terdapat endokarpium yang terdiri dari lapisan sel batu dengan bentuk berombak, dan mengandung zat warna (pigmen). Mesokarpium yang terdiri dari sel-sel parenkhim, pada bagian ini juga terdapat serabut sklerenkhim yang kecil dan pendek. Epikarpium merupakan epidermis kulit buah. Hasil dapat dilihat pada Lampiran 3, halaman 54.
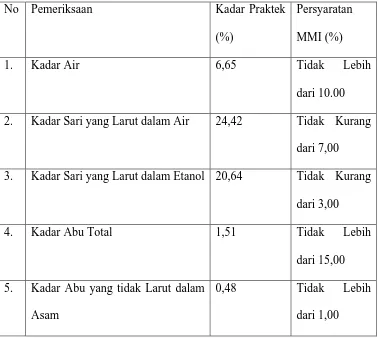
gambaran mengenai besarnya bahan-bahan terlarut atau merupakan bagian yang dimanfaatkan dari simplisia. Dan semua hasil pemeriksaan karakteristik dari simplisia memenuhi persyaratan yang tercantum di Materia Medika Indonesia. Hasil pemeriksaan kadar simplisia buah senduduk dan persyaratan MMI dapat dilihat pada Tabel 4.2 berikut ini:
Tabel 3.2 Hasil Karakterisasi Simplisia Buah Senduduk
No Pemeriksaan Kadar Praktek
(%)
Persyaratan MMI (%)
1. Kadar Air 6,65 Tidak Lebih
dari 10.00
2. Kadar Sari yang Larut dalam Air 24,42 Tidak Kurang dari 7,00
3. Kadar Sari yang Larut dalam Etanol 20,64 Tidak Kurang dari 3,00
4. Kadar Abu Total 1,51 Tidak Lebih
dari 15,00 5. Kadar Abu yang tidak Larut dalam
Asam
0,48 Tidak Lebih
dari 1,00
4.4 Hasil Ekstraksi Buah Senduduk
menggunakan rotary evaporator, selanjutnya di freeze dryer diperoleh ekstrak kental sebesar 18,495 g dengan persen rendemen 9,25%.
4.5 Hasil Uji Preformulasi
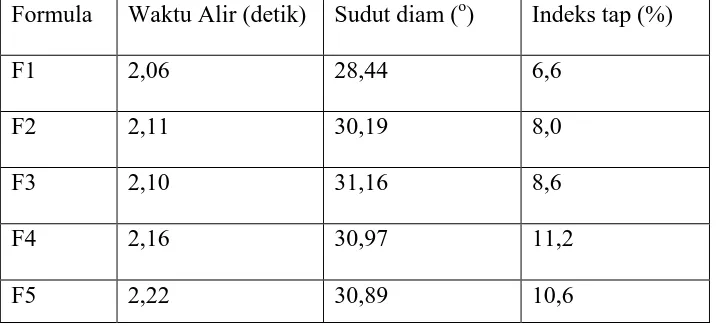
Hasil uji preformulasi dari lima formula yaitu waktu alir, indeks tab dan sudut diam memenuhi persyaratan. Hasil waktu alir, indeks tab dan sudut diam dapat dilihat pada Tabel 4.3 berikut ini:
Tabel 4.3 Uji preformulasi dari 5 formula
Formula Waktu Alir (detik) Sudut diam (o) Indeks tap (%) dapat dilihat pada Gambar 4.1, 4.2, dan 4.3 berikut ini:
Berdasarkan Gambar di atas dapat dilihat bahwa kelima formula memenuhi persyaratan waktu alir, dimana persyaratannya yaitu lebih kecil dari 10 detik dan F1 memiliki waktu alir yang paling baik diantara kelima formula. Sifat aliran yang baik merupakan hal penting untuk pengisian yang seragam kedalam lubang cetak mesin tablet (lesung tablet) dan untuk memudahkan gerakan granul pada saat pencetakan.
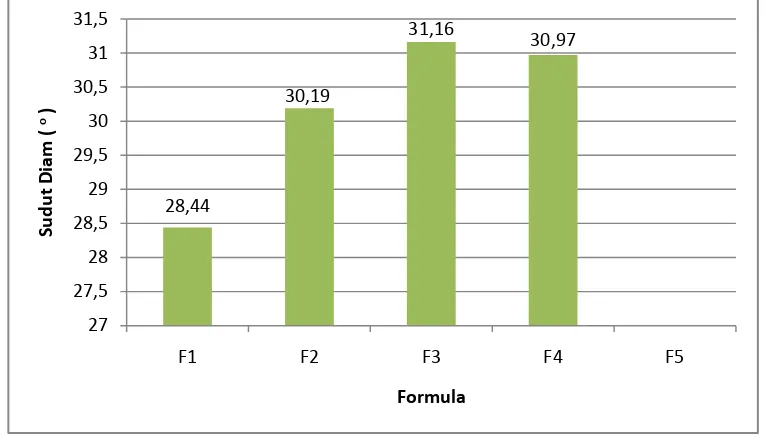
Gambar 4.2 Histogram uji sudut diam granul
Sudut diam dari kelima formula tersebut memenuhi persyaratan sudut diam. Banker dan Anderson (1994), menyatakan nilai sudut diam granul berkisar antara 25o sampai 45o,dengan nilai yang rendah menunjukkan sifat karakterisasi waktu alir yang lebih baik.
Gambar 4.3 Histogram uji indeks tap granul
Dari Gambar 4.3 di atas diperoleh nilai indeks tap yang bervariasi, tetapi masih memenuhi persyaratan indeks tap, dimana persyaratannya yaitu lebih kecil dari 20% (Voight, 1995). Hal ini disebabkan jumlah bahan pengikat yang digunakan pada tiap formula berbeda sehingga menghasilkan konsistensi granul basah yang berbeda, dan indeks tap granul yang diperoleh juga berbeda pada kelima formula. Semakin kecil nilai dari indeks tap granul, maka penyusutan volume yang terjadi akan semakin tinggi.
4.6 Hasil Evaluasi Tablet
Evaluasi tablet meliputi keseragaman bobot, kekerasan tablet, friabilitas tablet dan waktu hancur tablet. Hasil evaluasi keseragaman bobot tablet dapat dilihat pada Tabel 4.4 berikut ini:
Tabel 4.4 Hasil keseragaman bobot tablet
Hasil uji keseragaman bobot tablet dapat dilihat pada Gambar 4.4 di bawah ini:
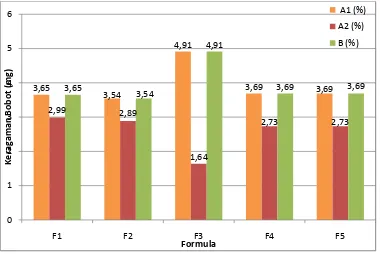
Gambar 4.4 Histogram uji keragaman bobot tablet
Keragaman bobot kelima formula ini memenuhi persyaratan Farmakope Indonesia Edisi III, dimana tidak lebih dari dua tablet yang masing-masing bobotnya menyimpang dari bobot rata-rata dari harga yang ditetapkan
dari kolom A1 (7,5%) dan tidak ada satu tablet yang menyimpang dari bobot rata-rata dari harga yang ditetapkan pada kolom B (10%).
Hasil evaluasi waktu hancur, kekerasan dan friabilitas tablet dapat dilihat pada Tabel 4.5 berikut ini:
Tabel 4.5 Hasil evaluasi waktu hancur, kekerasan dan friabilitas
Formula Keterangan Uji
Waktu Hancur (menit) Kekerasan (kg) Fiabilitas (%)
F1 5,57 4,76 1,98
F2 5,03 4,48 2,24
F3 5,17 5,12 3,44
F4 4,65 4,79 2,06
F5 6,19 5,16 2,89
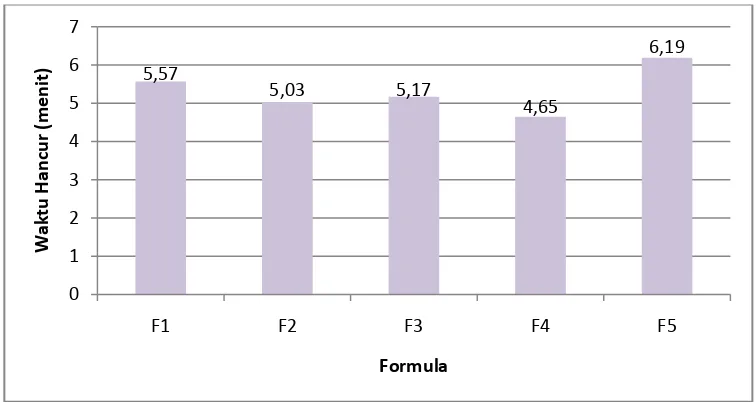
Hasil evaluasi waktu hancur, kekerasan dan friabilitas dapat dilihat pada Gambar 4.5, 4.6 dan 4.7 berikut ini:
Berdasarkan Gambar 4.5 di atas dapat dilihat bahwa kelima formula memenuhi persyaratan waktu hancur yang tercantum pada Farmakope Indonesia Edisi III yaitu tidak lebih dari 15 menit.
Gambar 4.6 Histogram uji kekerasan tablet
Berdasarkan gambar 4.6 diatas dapat dilihat bahwa uji kekerasan pada kelima sediaan tablet mempunyai kekerasan yang berbeda tetapi masih dalam rentang memenuhi persyaratan. Dimana menurut (Parrott,1971), persyaratan untuk kekerasan tablet yaitu 4 – 8 kg. Menurut Siregar (2010) kekerasan tergantung pada bobot bahan dan celah antara pons atas dan pons bawah pada waktu pengempakan. Jika volume bahan atau jarak antara pons bervariasi, kekerasan juga bervariasi.
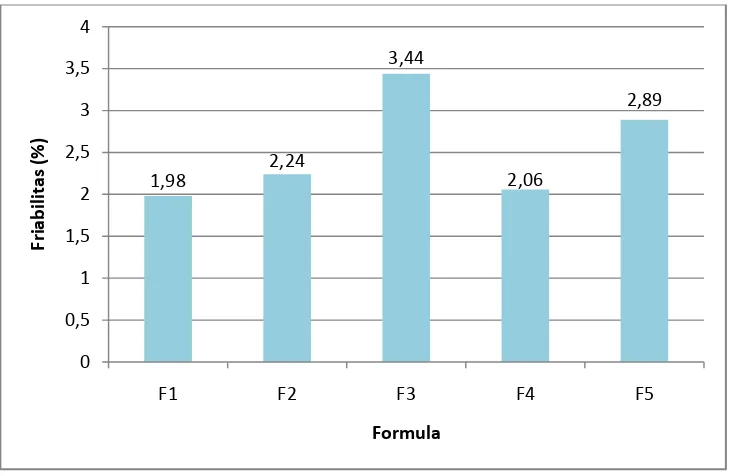
Gambar 4.7 Histogram uji friabilitas tablet
Berdasarkan gambar 4.7 diatas maka dapat disimpulkan bahwa hasil uji friabilitas pada kelima sediaan tablet semuanya menunjukkan tidak memenuhi persyaratan. Menurut siregar (2010) yang menyatakan bahwa persyaratan friabilitas yaitu maksimum 1% untuk tablet konvensional. walaupun kelima formula tablet diatas tidak memenuhi persyaratan uji friabilitas, namun kelima formula tablet tersebut masih memenuhi persyaratan, karena uji friabilitas bukan merupakan salah satu uji yang dipersyaratkan dalam Farmakope Indonesia.
3.7 Tes Hedonik (kesukaan warna)
Tes hedonik adalah uji yang dilakukan untuk mengukur tingkat kesukaan panelis terhadap produk. Tujuannya adalah untuk mengetahui formula dengan konsentrasi berapa yang paling disukai panelis. Hasil uji
Gambar 4.8 Histogram hasil tes hedonik
Berdasarkan Gambar 4.8 di atas dapat dilihat bahwa nilai kesukaan warna yang paling tinggi terdapat pada formula F1 yaitu konsentrasi 2%, dibandingkan dengan F2 = (konsentrasi 3%) F3 = (konsentrasi 4%) dan F4 = (konsentrasi 5%). Hal menunjukkan bahwa F1 menghasilkan warna yang lebih baik dan paling disukai panelis.
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
1. Zat warna merah buah senduduk (Melastoma malabathricum L.) yang diekstraksi dapat digunakan sebagai pewarna tablet.
2. Konsentrasi zat warna merah buah senduduk yang paling disukai panelis sebagai pewarna tablet adalah konsentrasi 2%.
5.2 Saran
DAFTAR PUSTAKA
Anonim.(1984). Bahan Pewarna, Bahan Pengawet, dan Bahan Tambahan
dalam Makanan, Obat dan Kosmetika. Publishing Sains dan
Teknologi Lembaga Penelitian USU. Medan. Hal. 32.
Anonim. (2008). Pewarna Kosmetik Sintetik :
@.Html Diakses pada tanggal: 12 Desember 2013.
Anonim. (2009). Pewarna Alami dan Sintesis : /2009/05/ pewarna-alami.html. Diakses pada tanggal : 2 April 2010. Anonim. (2010). Pokok senduduk
Diakses pada tanggal : 2 April 2010.
Abu-izza., Khawla, A.L., Vincent, H.L., Jee, L.P., Graham D.S., dan Matthew, K. (2009). Fast Dissolving Tablet. Dalam: Bhupendra G Prajapati and Nayan Ratnakar. A Review On Recent Patents On Fast Dissolving Drug Delivery System. International Journal of PharmTech Research. 1(3): 790-798.
Arief Hariana. (2011). Tumbuhan Obat dan Khasiatnya. Seri 3. cetakan 6. Jakarta: Penebar Swadaya. Hal.65.
Banker, G.S, dan Anderson N.R. (1994). Tablet. Dalam: Teori dan Praktek
Farmasi Industri. Edisi III. Jiliid II. Editor: Lachman, L Penerjemah:
Siti Suyatmi, Jakarta: UI-Press. Hal. 643-703.
BSN. (2006). Petunjuk Pengujian Organoleptik dan atau Sensori. Jilid I. Departemen kesehatan RI. Hal. 1,5-11.
Cartensen, J.T. (1977). Pharmaceutical of Solid Dosage Forms. New York: A Wiley Interscience Publication John Wiley and Son. Hal. 133-135
Dalimartha, S. (2000). Atlas Tumbuhan Obat Indonesia. Jilid 1. Jakarta: Trubus Agriwidya. Hal 130-132.
Depkes RI. (2012). Pewarna Makanan. http://depkes.go.id /index.php/ berita/ pressrelease//923html. Diakses pada tanggal: 15 Desember 2013.
Ditjen POM. (1979). Farmakope Indonesia. Edisi III. Departemen Kesehatan RI. Jakarta. Hal. 6-7.
Ditjen POM. (1995). Farmakope Indonesia. Jilid IV. Jakarta: Departemen Kesehatan RI. Hal. 1087.
Ditjen POM. (1995). Materia Medika Indonesia. Jilid V. Jakarta: Departemen Kesehatan RI. Hal. 321, 325, 333-337.
Ditjen POM. (2000). Parameter Standar Umum Ekstrak Tanaman. Cetakan Pertama. Departemen Kesehatan RI. Jakarta. Hal. 1,9-12.
Ditjen POM. (2010). Farmakope Herbal Indonesia. Jilid I. Jakarta: Departemen Kesehatan RI. Hal. 140-141.
Farnsworth, N.R. (1966). Biological and Phytochemical Screening of Plants.
Journal of Pharmaceutical Sciences. 55(3): 263.
Harbone, J.B. (1987). Metode Fitokimia, Penuntun Cara Moder Menganalisa
Tumbuhan. Terjemahan Kosasih Padmawinata. Edisi II. Bandung:
ITB Press. Hal. 147.
Heyne. K (1987). Tumbuhan Berguna Indonesia. Jilid III. Cetakan – I. Yayasan Sarana Wana Jaya. Jakarta. Hal. 1534.
Parrot, L.(1971). Pharmaceutical Technology. Amerika: Burges Publishing Company. United Stated of America. Hal. 82.
Saati, E.A. dan Hidayat, N. (2006). Membuat Pewarna Alami. Cetakan I. Trubus Agrisana. Hal 1-10.
Sentra Imformasi IPTEK. (2009). Senggani. Desember 2013.
Sharma, R., Rajput, M., Prakash, P., dan Sharma, S. (2011). Fast Disolving Delivery Sytem On review. International Journal of Pharmacy. 2(10): 21-29
Siregar, C.J.P., dan Wikarsa, S. (2010). Teknologi Farmasi Sediaan Tablet
Dasar-Dasar Praktis. Cetakan II. Penerbit Buku Kedokteran EGC.
Jakarta. Hal. 1, 2, 8, 416-418.
Soekarto, S. T. (1985). Penilaian Organoleptik untuk Industri Pangan dan Hasil Pertanian. Bhatara Aksara. Jakarta. Hal. 57.
Voigt, R. (1995). Buku Pelajaran Teknologi Farmasi. Cetakan II. Penerjemah: Soedani Noerono. Yogyakarta: UGM-Press. Hal. 159.
Lampiran 2 Gambar tumbuhan dan buah senduduk
Gambar: Tumbuhan senduduk
Lampiran 3 Mikroskopik simplisia
Keterangan
1. Endokarp 4. Serabut sklerenkrim 1
2
3 4 5
Lampiran 5 Gambar sediaan tablet
1. Formula 1 (2%)
2. Formula 2 (3%)
Lampiran 6 Perhitungan Penetapan Karakteristik Simplisia Perhitungan Penetapan Kadar Air Simplisia
% Kadar air = Volume air (ml)
Berat sampel (g) x 100%
1. Berat sampel : 5,007 g
Volume air : 0,3 ml
% Kadar air = 0,3 ml
5,007 g x 100% = 5,99%
2. Berat sampel : 5,014 g
Volume air : 0,3 ml
% Kadar air = 0,3 ml
5,014 g x 100% = 5,98%
3. Berat sampel : 5,017 g
Volume air : 0,4 ml
% Kadar air = 0,4 ml
5,017 g x 100% = 7,97%
% Kadar air rata-rata = 5,99% + 5,98% + 7,97%
3
Lampiran 6 (Lanjutan)
Lampiran 6 (Lanjutan)
Perhitungan Penetapan Kadar Sari yang Larut dalam Etanol
% Kadar sari larut dalam etanol = Berat Sari
% Kadar sari larut dalam etanol rata-rata= 20,97% + 20,64% + 20,33%
3
Lampiran 6 (Lanjutan)
Perhitungan Penetapan Kadar Abu Total
% Kadar abu total = Berat Abu
Berat Simplisi
x 100% 1. Berat simplisia : 2,006 g
Berat abu : 0,03 g
% Kadar abu total = 0,03
2,006x 100% = 1,49%
2. Berat simplisia : 2,010 g Berat abu : 0,032 g
% Kadar abu total = 0,032
2,010x 100% = 1,59%
3. Berat simplisia : 2,007 g Berat abu : 0,029 g
% Kadar abu total = 0,029
2,007 x 100% = 1,44%
% Kadar abu total rata-rata =
1,49% + 1,59% + 1,44%
3
Lampiran 6 (Lanjutan)
Perhitungan Penetapan Kadar Abu yang Tidak Larut dalam Asam
% Kadar abu tidak larut dalam asam = Berat Abu
Berat Simplisia
x 100% 1. Berat simplisia : 2,006 g
Berat abu : 0,008 g
% Kadar abu tidak larut dalam asam =0,008
2,006 x 100%
= 0,39%
2. Berat simplisia : 2,010 g Berat abu : 0,012 g
% Kadar abu tidak larut dalam asam = 0,012
2,010x 100%
= 0,59% 3. Berat simplisia : 2,007 g
Berat abu : 0,009 g
% Kadar abu tidak larut dalam asam = 0,009
2,007 x 100% = 0,45%
% Kadar abu tidak larut asam rata-rata = 0,39% + 0,59% + 0,45%
3
Lampiran 7 Pembuatan ekstrak buah senduduk
Dimasukkan ke dalam wadah
Ditambahkan 2000 ml pelarut etanol 96% yang mengandung asam asetat 1%
Dimaserasi selama 24 jam pada suhu ruangan, sambil sekali-kali diaduk selama 6 jam pertama Disaring
Ditambahkan 2000 ml pelarut etanol 96% yang mengandung asam asetat 1% Dimaserasi selama 24 jam pada suhu ruangan, sambil sekali-kali diaduk selama 6 jam pertama
Disaring
Ektrak dikumpulkan
Dirotari sampai pelarutnya habis (tidak ada lagi pelarut yang menguap)
Di freeze dryer selama kurang lebih 24 jam
200 g serbuk
Ekstrak Residu
Filtrat Residu
Lampiran 8 Pembuatan tablet parasetamol dengan zat warna buah senduduk Ditimbang lagi, hingga diperolah massa yang sesuai
Ditambahkan sedikit demi sedikit massa 2 ke massa 1, sambil digerus hingga diperoleh massa yang kompak Digranulasi dengan ayakan mesh 12.
Dikeringkan granulasi dalam lemari pengering pada suhu 40o-60o C
Diayak lagi ganulat kering dengan ayakan mesh 14 dan dicek kembali beratnya.
Ditambahkan Mg-stearat, talkum dan bahan pengembang luar