BAB I PENDAHULUAN
1.1 Latar Belakang
Sterilisasi adalah suatu usaha untuk membebaskan alat-alat atau bahan dari segala bentuk kontaminasi dari mikroba. Proses pembersihan alat dan medium dalam kegiatan praktikum atau penanganan sampel mikroba sangat membutuhkan sterilisasi. Apabila teknik sterilisasi tidak diterapkan maka hasil yang dicapai tidak maksimal dan menimbulkan berbagai kontaminasi baik dari alat maupun media tumbuh mikroba (Dwidjoseputro, 1994).
Desinfeksi merupakan suatu caramembunuh suatu mikroorganisme penyebab penyakit dengan bahan kimia, sehingga hal ini dapat mengurangi kemungkinan terjadi infeksi dengan jalan membunuh mikroorganisme patogen. Metode desinfeksi menggunakan bahan yang disebut dengan desinfektanuntuk membunuh mikroba pada jaringan atau benda mati dan antiseptik yang digunakan untuk membunuh mikroba pada jaringan hidup. Desinfektan tersebut
antaralainberupa alkohol, etilen oksida, klor dan formaldehid. Penggunaan dan dosis desinfektan ini bervariasi tergantung jenis mikrobia yang akan di bunuh.
Pemahaman prinsip dasar sterilisasi dan desinfeksi merupakan dasar dalam pekerjaan di laboratorium terutama di laboratorium mikrobiologi. Teknik baru mengenai sterilisasi secara terus menerus telah dikembangkan. Sterilisasi, mutlak diperlukan untuk inaktivasi total seluruh kehidupan mikroba terutama yang berkaitan dengan kemampuan reproduksi mikroba(Kusnadi dkk, 2003). Bahan atau peralatan yang digunakan dalam laboratorium mikrobiologi haruslah dalam keadaan steril guna mencegah mikroba yang tidak dibutuhkan tumbuh dan mempengaruhi hasil pengamatan.
Tidak hanya di laboratorium, sterilisasi dan desinfeksi juga penting
diterapkan di kehidupan sehari-hari, misalnya membersihkan tangan dengan hand sanitizer yang merupakan sterilisasi dengan bahan kimia, membersihkan luka dengan antiseptik untuk mencegah terjadinya infeksi, dan merebus botol susu bayi dengan air panas guna membunuh mikroba yang ada di dalam botol. Berdasarkan latar belakang masalah di atas, maka kami bemaksud membahas lebih lanjut tentang sterilisasi dan desinfeksi beserta macam-macamnya.
1.2 Rumusan Masalah
1. Bagaimanakah pengertian dari sterilisasi dan desinfeksi? 2. Bagaimanakah macam-macam dari sterilisasi?
3. Bagaimanakah macam-macam desinfeksi? 1.3 Tujuan
1. Memaparkan pengertian dari sterilisasi dan desinfeksi. 2. Memaparkan macam-macam dari sterilisasi.
3. Memaparkan macam-macam desinfeksi.
BAB II PEMBAHASAN
2.1 Pengertian Sterilisasi dan Desinfeksi A. Sterilisasi
dalam usaha mendapatkan keadaan steril, mikroorganisme dapat dimatikan setempat oleh panas, gas-gas formaldehide, etilenoksida atau betapriolakton oleh bermacam-macam latutan kimia ataupun oleh sinar gamma. Mikroorganisme juga dapat disingkirkan secara mekanik dengan sentrifugasi kecepatan tinggi atau dengan cara filtrasi (Irianto, 2006).
B. Desinfeksi
Desinfeksi berarti mematikan atau menyingkirkan organisme yang dapat menyebabkan infeksi dengan bahan kimia. Desinfeksi biasanya dilaksanakan dengan menggunakan zat-zat kimia seperti fenol, formaldehid, klor, iodium atau sublimat. Pada umumnya desinfeksi dimaksudkan untuk mematikan sel-sel vegetatif yang lebih sensitif tetapi bukan spora-spora yang tahan panas(Irianto, 2006).
2.2 Macam-Macam Sterilisasi
Sterilisasi merupakan suatu proses untuk mematikan semua organisme yang terdapat pada suatu benda. Proses sterilisasi dapat dibedakan menjadi 3 macam, yaitu penggunaan panas dengan pemijaran dan udara panas, penyaringan, dan penggunaan bahan kimia dengan menggunakan etilena oksida, asam perasetat, formaldehida dan glutaraldehida alkalin (Hadioetomo, 1985).
Sterilisasi secara fisik adalah sterilisasi dengan menggunakan saringan, sterilisasi secara kimia adalah sterilisasi menggunakan bahan kimia seperti alkohol dan lain-lain, dan sterilisasi secara mekanik adalah sterilisasi
menggunakan alat. Dalam sterilisasi fisik, apabila panas digunakan bersama-sama dengan uap air maka biasa disebut dengan sterilisasi panas kering atau sterilisasi kering. Di lain pihak sterilisasi kimiawi dapat dilakukan dengan cara
menggunakan gas atau radiasi. Pemilihan metode didasarkan pada sifat bahan yang akan disterilisasi (Sutedjo, 1996).
Pada prinsipnya sterilisasi dapat dilakukan dengan 3 cara yaitu secara mekanik, fisik dan kimia.
A. Sterilisasi Secara Mekanik
Sterilisasi secara mekanik (filtrasi) merupakan salah satu teknik sterilisasi dengan menggunakan suatu saringan yang berpori sangat kecil (0.22 mikron atau 0.45 mikron) dengan tujuan agar mikroba tertahan pada saringan tersebut. Proses ini ditujukan untuk sterilisasi bahan yang peka panas, misalnya larutan enzim dan antibiotik. Sterlisasi mekanik digunakan Jika terdapat beberapa bahan yang akibat
pemanasan tinggi atau tekanan tinggi akan mengalami perubahan atau penguraian, misalnya dengan saringan (Suriawira, 1983).
Dalam mikrobiologi, penyaringan secara mekanik paling banyak digunakan adalah dalam penggunaan filter misalnya filter berkefeld, filter chamberlan, dan filter seitz. Jenis filter yang dipakai tergantung pada tujuan penyaringan dan benda yang akan disaring. Penyaringan dapat dilakukan dengan mengalirkan gas atau cairan melalui suatu bahan penyaring yang memilki pori-pori cukup kecil untuk menahan mikroorganisme dengan ukuran tertentu. Saringan akan tercemar sedangkan cairan atau gas yang melaluinya akan steril. Alat saring tertentu juga mempergunakan bahan yang dapat mengabsorbsi mikroorganisme. Saringan yang umum dipakai tidak dapat menahan virus. Oleh karena itu, sehabis penyaringan medium masih harus dipanaskan dalam autoclave. Penyaringan dilakukan untuk mensterilkan substansi yang peka tehadap panas seperti serum, enzim, toksin kuman, ekstrak sel dan lain-lain.
a. Menyaring cairan
Hal ini dapat dilakukan dengan berbagai filter seperti:
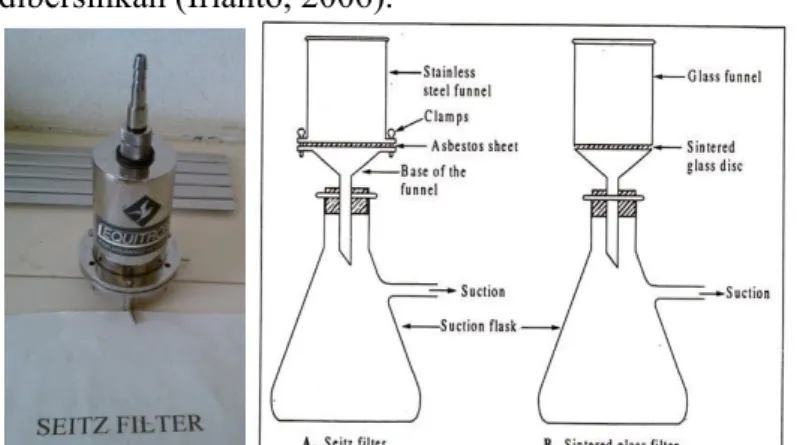
1. Seitz filter, yang menggunakan saringan asbestos atau serat-serat asbes sebagai alat penyaringannya, penyaring ini berbentuk keping bulat. Saringandari serat asbes ini lebih mudah dan lebih murah daripada saringan porselen. Saringan asbes dapat dibuang setelah dipakai, sedangkan saringan porselen terlalu mahal bila dibuang, tetapi terlalu sulit untuk dibersihkan (Irianto, 2006).
Sumber:
http://www.biologydiscussion.com/bacteria/sterilization/sterilization-of-bacteria-top-4-methods-microbiology/50088
2. Berkefeld filter, merupakan saringan berkefeld yang mempergunakan filter yang terbuat dari tanah diatomae dan saringan yang
menggunakan filter yang terbuat dari porselen yang tidak diglasir (Chamberland-pasteur filter). Filter ini seperti tabung kosong berbentuk lilin. Ukuran yang dimiliki oleh saringan berkefeld ini adalah sebagai berikut:
I. W (dense) digunakan untuk yang berpori halus II. N (normal) digunakan untuk yang berpori sedang III. V (course) untuk yang berpori kasar
3. Sedangkan filter Chamberland ukurannya dinyatakan sebagai L1 sampai L13. Dimana L1 untuk yang berpori paling halus dan L13 untuk yang berpori paling kasar (Irianto, 2006).
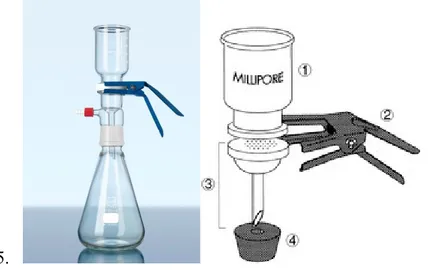
Gambar . Berkefeld filter dan Chamberland-pasteur filter Sumber: http://www.consciouswater.ca/gravity-water-filter/ 4. Sintered glass filter, Saringan ini terbuat dari serbuk kaca yang
berbentuk ceper. Ukurannya dinyatakan dengan EC (extra course), C (course), M (medium), (Fine), dan UF (ultra fine) (Irianto, 2006).
5.
Gambar . Sintered glass filter
Sumber: http://www.rivieraglass.co.in/laboratory-glassware.html Selain itu ada pula jenis filter yang serba guna, yaitu membran filteryang terbuat dari celulosa asetat. Membran fllter ini seperti kertas ceper yang memiliki diameter 50 mm dan tebal 0,1 mm. Diameter pori-porinya bermacam macam dari 0,1 µm lebih sampai kurang dari 0,005 µm. Membran filter ini berbeda dari saringan diatas, karena ke efektifanya sebagian besar karena sifatmengayak dari struktur yang berperforasi dan kehalusan dari pori-porinya. Lalu keuntungan khusus dari membran filter ini ialah bahwa semua mikroorganime yang berada dalam volum cairan yang besar seperti air susu, urine dan darah encer dapat terkumpul pada satu keping kecil filter dan mikroorganisme itu dapat di amati langsung (Irianto, 2006).
Gambar Sumber: membran
filterhttp://www.gelifesciences.com/webapp/wcs/stores/servlet/productById/en/G ELifeSciences/28415272
b. Menyaring udara
Untuk menjaga suatu alat yang sudah steril agar tidak tercemar oleh mikroba atau untuk menjaga agar suatu biakan kuman tidak tercemar oleh kuman yang lain, maka alat-alat tersebut harus ditutup dengan kapas, karena kapas mudah ditembus udara tetapi dapat menahan mikroorganisme. Harus dijaga agar kapas tidak menjadi basah, oleh karena kapas yang basah memungkinkan kuman menembus ke dalam. Untuk mencegah pencemaran oleh kuman-kuman udara pada waktu menuang pembenihan, dapat dipergunakan suatu alat yang disebut laminar flow bench dimana udara yang masuk ke dalamnya disaring terlebih dahulu dengansuatu saringan khusus. Saringan ini ada batas waktu pemakaiannya dan harus diganti dengan yang baru apabila sudah tidak berfungsi lagi.
Gambar laminar flow bench
Sumber: http://www.bmlabosis.com/Urunler/2063/Laminar-FLow-Calisma-Kabinleri
B. Sterilisasi Secara Fisik
Sterilisasi secara fisik merupakan sterilisasi menggunakan alat. Dalam sterilisasi fisik, apabila panas digunakan bersama-sama dengan uap air maka biasa disebut dengan sterilisasi panas basah atau sterilisasi basah dan apabila hanya menggunakan udara panas disebut sterilisasi panas kering atau sterilisasi kering. Pemilihan metode didasarkan pada sifat bahan yang akan disterilisasi (Sutedjo, 1996).
Sterilisasi yang paling umum dilakukan dapat berupa sterilisasi secara fisik (pemanasan, penggunaan sinar gelombang pendek yang dapat dilakukan selama senyawa kimia yang akan disterilkan tidak akan berubah atau terurai
akibat temperatur atau tekanan tinggi). Dengan udara panas, dipergunakan alat “bejana/ruang panas” (oven dengan temperatur 170oC sampai 180oC dan waktu yang digunakan adalah 2 jam yang umumnya untuk peralatan gelas) (Suriawiria, 2005).
Menurut Tim Dosen Mikrobiologi Universitas Tadulako(2011), sterilisasi dibedakan menjadi dua jenis yaitu:
1. Sterilisasi dengan cara fisik a) Pemanasan
Air dan uap adalah media panas yang baik. Dalam waktu relatif singkat, alat yang akan disterilkan akan mencapai suhu yang diinginkan. Udara adalah penyalur panas yang kurang baik. Oleh karena itu, untuk mecapai suhu yang diinginkan akan membutuhkan waktu yang cukup lama.
1) Pemanasan Kering
Cara ini untuk membunuh mikroba hanya memakai udara panas kering yang tinggi. Sterilisasi panas kering dibedakan atas :
a) Panas membara (flaming)
Dengan jalan menaruh benda yang akan di sterilkan dalam nyala api bunsen sampai merah membara. Alat yang disterilkan yaitu sengkelit, jarum, ujung pinset dan ujung gunting.
b)Pemijaran panas (glowing)
Api digunakan untuk mensterilisasi peralatan seperti jarum inokulasi, cawan petri, kaca objek, pinset, mulut tabung biakan, scalpel, dan kaca benda. Sesudah disterilkan peralatan tersebut harus didinginkan terlebih dahulu sebelum dipergunakan, khusus untuk jarum inokulasi dan pipet setelah dipijarkan atau dipanaskan di atas api, selanjutnya didinginkan dalam larutan alkhol 70% kemudian dibakar dengan melewatkan benda dalam api bunsen, namun tidak sampai menyala terbakar.kembali untuk
menghilangkan sisa alkohol, setelah itu dinginkan lagi di dalam larutan alkhol dan dibiarkan/diangin-anginkan dan tidak perlu dibakar lagi.
Alat yang digunakan adalah oven. Alat ini terbuat dari kotak logam, udara yang terddapat di dalamnya mendapat udara panas melalui panas dari nyala listrik. Alat yang disterilkan yaitu tabungreaksi, cawan petri, pipet, scalpel dari logam, gunting, botoldan alat-alat gelas lainnya. Pemanasan satu jam dengann temperatur 160oC dianggap cukup.Sterilisasi panas kering ini merupakan sterilisasi dengan udara panas.Prinsip kerja dari alat ini lebih sederhana yaitu pintu oven dibuka dan semua alat-alat yang akan disterilkan disusun rapi. Setelah itu pintu oven ditutup, suhu diseting pada angka 160oC-180oC selama 1-2 jam.
Keuntungan dari pemanasan kering adalah tidak adanya uap air yang membasahi bahan atau alat yang disterilkan.Sterilisasi panas kering biasa digunakan untuk alat-alat atau bahan-bahan dengan uap yang tidak dapat berpenetrasi secara mudah atau untuk peralatan yang terbuat dari kaca. Pada sterilisasi panas kering, pembunuhan mikroorganisme terjadi melalui mekanisme oksidasi sampai terjadi koagulasi protein sel (Lukas, 2006).
2) Pemanasan Basah
Pemanasan basah merupakan pemansan yang menggunakan air atau uap air. Uap air adalah media penyalur panas yang terbaik dan terkuat daya penetrasinya. Panas basah mematikan mikroba. Oleh karena
koagulasi dan denaturasi enzim dan protein protoplasma mikroba. Untuk mematikan spora diperlukan panas basah selama 15 menit pada suhu 121oC. Sterilisasi panas basah dapat dibedakan atas tiga golongan yaitu: a) Panas basah <100oC (Pasteurisasi)
Pasteurisasi yaitu pemanasan pada suhu 60oC selama 30 menit. Pasteurisasi tidak dapat membunuh spora atau dipanaskan pada suhu 71,6oC – 80oC selama 15 – 30 detik kemudian cepat – cepat didinginkan.
b) Panas basah pada suhu 100oC
Di sini menggunakan air mendidih (suhu 100oC) selama 10 menit. Untuk mematikan bentuk spora dilakukan pemansan 3 hari berturut – turut selama 15 – 45 menit sehingga spora yang tidak
mati pada pemanasan pertama akan beruah menjadi bentuk vegetatif pada hari kedua steleh inkubasi pada suhu 37oC begituu pula spora yang tidak mati pada hari kedua, akan berubah menjadi bentuk vegetatif pada hari ketiga.
c) Panas basah >100oC
Sterilisasi dengan cara ini hasilnya mutlak steril, sehingga biasa dipergunakan di rumah sakit dan laboratorium besar. Cara ini menggunakan tangki yang diisi dengan uap air yang disebut
autoclave. Alat yang disterilkan adalah alat dari kaca, kain kasa, media pembenihan, cairan injeksi, dan bahan makanan.
3) Pendinginan
Suhu rendah menyebabkan pertumbuhan dan perkembangbiakan mikroba terhenti. Cara ini dipakai untuk mengawetkan bahan makanan yang mudah
membusuk, misalnya daging, karena pada suhu rendah ini, bahan makanan itu tidak akan dirombaknya. Pada suhu -20oC (minus dua puluh derajat Celcius) (suhu lemari pendingin pada umumnya) mikroba tidak bisa merombak makanan sehingga tidak terjadi pembusukan. Beberapa bakteri mati pada suhu 0oC
misalnya Neisseria gonorrhoea, Treponema pallida (Indan Endjang, 2003: 41-42) Suhu rendah tidak membunuh mikroba, tetapi hanya memperlambat bahkan menghentikan proses metabolisme. Ketika mikroba dipindah ke suhu normal pertumbuhannya maka mikroba tersebut akan tumbuh dan berkembang. Suhu refrigerasi (4C) hanya mencegah pertumbuhan mikroba dan
memperpanjang umur makanan. Namun banyak bakteri yang masih bertahan hidup di suhu tersebut, sehingga dapat mengkontaminasi makanan yang disimpan di dalam lemari es. Pembekuan sampai suhu -20C dapat menghentikan
metabolisme mikroba, tetapi tidak merusak atau membunuh mikroba. Suhu rendah mampu menyimpan kultur mikroba pada suhu -196C dalam nitrogen cair mampu menyimpan mikroba sampai 10 tahun tanpa membunuhnya.
Metode sterilisasi dengan menggunakan radiasi dilakukan dengan menggunakan sinar UV ataupun dengan metode ionisasi. Sinar UV dengan panjang gelomabang 260 nm memiliki daya penetrasi yang rendah sehingga tidak mematikan mikroorganisme namun dapat mempenetrasi gelas, air, dan substansi lainnya. Sinar UV ini bereaksi dengan asam nukleat sel mikroorganisme dan menyebabkan ikatan antara molekul-molekul timin yang bersebelahan dan menyebabkan terbentuknya diimer timin. Dimer timin dapat menghalangi replikasi DNA normal dengan menutup jalan enzim replikasi. Penggunaan sterilisasi dengan sinar UV antara lain untuk sterilisasi kabinet dan ruangan. Endospora bakteri resisten terhadap sinar UV. Metode sterilisasi dengan ionisasi sebesar 2,5 Mrad dapat mempenetrasi jauh ke dalam objek. Penggunaan teknik ini, misalnya dengan radiasi gamma dari kobalt-60, lebih kuat daya tembusnya dibandingkan dengan cahaya UV dan tidak dilakukan dalam laboratorium. Metode sterilisasi ini ditujukan untuk merusak asam nukleat mikroorganisme dan digunakan untuk bahan-bahan yang tidak dapat disterilisasi menggunakan panas, contohnya bahan plastik sekali pakai (disposable plasticware), antibiotik, hormon, dan jarum suntik (syrnge) (Sylvia T. Pratiwi, 2008: 140-141)
a. Radiasi Ultraviolet
Mekanisme Kerusakan Oleh Radiasi Ultraviolet.
Cahaya ultraviolet meliputispektrum radiasi dari 15 – 390 nm. Efektivitas cahaya ultraviolet sebagai suatu bahan mutagenik dan mematikan berhubungan erat dengan panjang gelombangnya. Panjang gelombang bersifat bakterisida yang paling efektif ialah pada rentang 240 – 280 nm,dengan panjang optimum sekitar 260 nm, yang dilaporkan mengalami absorbs maksimum oleh DNA. Mekanisme efek mematikan sinar UV yang terbanyak pada bakteri, karena absorbsi
menyebabkan kerusakan DNA. Radiasi UV mengarah pada pembentukan ikatan kovalen antara residu pirimidin yang berdekatan satu sama lainpada rantai yang sama, menghasilkan formasi dimer pirimidin tipe-siklobutan. Dimer ini
merupakan bentuk penyimpangan DNA dan bergabung dengan pasangan basanormal. Hal tersebut mengakibatkan suatu hambatan sintesis DNA dan efek sekundernya menghambat pertumbuhan dan respirasi. Cahaya UV juga bersifat mutagenik. Efek mutagenik bergantung pada induksi oleh dimer
siklobutan dari respon SOS, yang secara serasi mengatur grup operon terrepresi secara negative. Efek lain dari radiasi UV, misalnya fotohidrasi sitosin dan pautan-silang rantai DNAkomplemen, tetapi UV dalam dosis yang sangat tinggi perlu diatur sebagaimekanisme terbesar untuk merusak sel.
Penggunaan Cahaya UV.
Radiasi UV dapat dihasilkan secara buatan dengan lampu asap merkuri. Unit energi radiasi diukur dalam mikrowatt per unit area per unitwaktu. Cahaya UV 15 watt menghantarkan radiasi 38µW/cm2 /s pada jarak 1 m. Radiasi UV sama efektifnya untuk bakteri gram-positif maupun gram-negatif. Untuk sebagian besar bakteri yang tidak membentuk spora, dosis yang mematikan bervariasi mulai dari 1800 µW/cm2 /s sampai 6500 µW/cm2 /s. Spora bakteri membutuhkan 10 kali dosis tersebut.Saat ini sudah ada lampu yang disebut lampu germisidal, yang memancarkan sinar ultraviolet dengan konsentrasi tinggi dengan daya germisidal paling efektif,yaitu terletak pada daerah 260 – 270 nm. Lampu germisidal banyak digunakan untuk mengurangi populasi mikroba di kamar-kamar bedah rumah sakit, di ruang aseptik untuk pengisian obat-obatan industri farmasi, pada tempat pengisian produk steril kedalam tabung kecil atau ampul dengan pipet dan di industri-industri pangan serta persusuan untuk membersihkan permukaan yang terkontaminasi.
Meskipun komponen radiasi UV secara tidak diragukan bersifat
bakterisida, tetapi radiasi UV tidak layak digolongkan sebagai bahan pensterilisasi karena ketidakjelasan dalam penggunaannya. Tidak seperti radiasi ionisasi, energi radiasi UV adalah rendah, dan daya tembusnya kecil. Radiasi UV tidak menembus benda padat, dan hanya sedikit menembus benda cair. Bahkan selapis kaca yang tipis dapat menahan sebagian besar sinar tersebut. Oleh karena itu, sinar UV tidak berpengaruh terhadap mikroorganisme yang terlindung dari pancaran langsung sinar tersebut (“incident beams”). Jadi hanya mikroorganisme yang ada di permukaan suatu benda yang secara langsung terkenai sinar ultraviolet, yang rentan terhadap pembasmian.
Komponen Radiasi Pengionisasi.
Radiasi pengionisasi dikelompokkan menjadi dua golongan sesuai dengan komponen fisiknya : (1) yang memiliki masa dan bermuatan atau tidak bermuatan, dan (2) hanya energi saja. Beberapa radiasi pengionisasi merupakan produk dari kerusakan radioaktif (sinar-α, -β, -γ ), dan yang lainnya dihasilkan pada suatu mesin sinar-x, melalui pengeboman partikel, atau reactor nuklir. Radiasi
pengionisasi yang memiliki nilai terbesar untuk keperluan sterilisasi ialah sinar-x, sinar-γ elektromagnetik, dan partikel sinar katoda (electron terakselerasi buatan). Radiasi tersebut memiliki sejumlah energi yang lebih besar daripada yang
dikandung dalam radiasi UV, sehingga kemampuan untuk menghasilkan efek mematikan juga lebih besar. Daya tembus radiasi pengionisasi mendukung efektivitasnya sebagai bahan sterilisasi. Sinar katoda, karena sifat partikelnya, memiliki energi dari dalam , dan akibatnya memiliki daya tembus terbesar, meskipun sinar-α dan sinar-γ memiliki daya tembus yang lebih besar.Karena sifat mekanisme dilibatkan, maka aktivitas optimum tidak pernah terjadi pada
permukaan bahan yang disinari. Dengan sinar-γ , aktivitas optimum terjadi hanya bagian dalam atau di bawah permukaan, dengan sinar katoda hal itu terjadi lebihdalam beberapa sentimeter
Efek Mematikan.
Sebagian besar bakteri yang tidak membentuk spora, relatif sensitif terhadap radiasi pengionisasi. Diantara bakteri tersebut, bakteri
gram-positif umumnya lebih resisten daripada bakteri Gram-negatif, spora sebagian besarmikroorganisme bersifat resisten-radiasi.Kematian mikroorganisme karena paparan radiasi pengionisasi biasanyabersifat eksponensial melalui periode sterilisasi, meskipun dalam beberapa kasus hal tersebut cenderung sigmoidal. Kemiringan kurva waktu-survivor ditentukan oleh intensitas penyinaran, tetapi hubungan dosis dengan persentase organisme yangdibunuh, selalu eksponensial. Menuju akhir proses, suatu efek bagian akhir menjadi mencolok, perlu ditegaskan bahwa dosis penuh secara yakin sudah diberikan.
Meskipun dosis sterilisasi bergantung pada tingkat kontaminasi awal, suatu dosis 2,5 Mrad radiasi pengionisasi (1 Mrad = 106 rad, 1 rad= absorbsi energi 100 ergs/gram udara) sudah diterima sebagai dosis sterilisasi.Dosis tersebut, cukup untuk membunuh sebagian besar mikroorganisme dan jugatersedia sebagai dosis yang aman untuk digunakan dalam praktek
Bidang Farmasi dan kedokteran, merupakan bidang utama yang
menggunakan radiasi pengionisasi untuk sterilisasi. Khususnya untuk sterilisasi benda atau bahan seperti alat bedah sekali-pakai, benang jahit terbuat dari usus hewan (“cat gut”), benang jahit nilon, dan alat-alat yang berhubungan dengan kedokteran.
5) Sterilisasi Dengan Vibrasi Sonik Dan Ultrasonik
Vibrasi suara pada frekuensi tinggi, dalam rentang ultrasonik dan dapat didengar (20-1000 kc), merupakan teknik yang sering digunakan untuk merusak sel mikroba. Generator gelombang suara yang secara luas digunakan untuk keperluan operasi, dalam rentang frekuensi 9-100 kc/s. Tidak ditemukan frekuensi khusus,tetapi secara umum dengan meningkatkan frekuensi gelombang
ultrasonik.Vibrasi ultrasonik juga dapat menyebabkan depolimerisasi
makromolekuldan pengelompokan-kembali intramolekuler. Pelepasan rantai-ganda oleh vibrasisonik dihasilkan untuk pemindahan DNA, dan integrasi kedalam genom inang dapat dihambat. Mikroorganisme memiliki sensitivitas yang berbeda terhadap vibrasi sonik dan ultrasonik. Sebagian besar batang Gram-negatif bersifat rentan, dan diantara sebagian besar yang resisten adalah
Staphylococcus, membutuhkan waktu paparan yang lama. Meskipun vibrasi sonik dapat mematikan populasi bakteri, tetapi ada juga yang bertahan hidup.
Akibatnya, perlakuan dengan vibrasi sonik tidak memiliki nilai praktis untuk sterilisasi dan disinfeksi.
Sehubungan dengan pengendalian mikroorganisme, yang terpenting ialah mekanisme kerja gelombang suara berfrekuensi tinggi pada pembersih
ultrasonik,yaitu unit-unit berisi cairan yang dilalui oleh gelombang suara tersebut. Gelombangsuara berfrekuensi tinggi menempuh perjalanannya melalui cairan tadi, makaterbentuklah sejumlah besar gelombang kecil yang setelah mencapai
ukuran tertentumenghilang dengan sangat cepat. Fenomena ini dinamakan kavitasi (“cavitation”),yaitu tenaga yang ditimbulkan akan menghilangkan debu atau partikel-partikel (termasuk mikroorganisme) dari permukaan benda yang ada dalam cairan tersebut. Pembersih ultrasonik lebih efisien untuk membersihkan bahan organik dari peralatan dibandingkan dengan penyikatan secara mekanis.
C. Sterilisasi Secara Kimia
Sterilisasi secara kimia merupakan suatu cara membunuh suatu
mikroorganisme penyebab penyakit dengan bahan kimia, sehingga hal ini dapat mengurangi kemungkinan terjadi infeksi dengan jalan membunuh
mikroorganisme patogen.Sterilisasi dengan menggunakan bahan kimia biasa disebut dengan desinfeksi.Sterilisasi secara kimia biasanya menggunakan senyawa desinfektan dan antispetik.Metode sterilisasi kimiayang menggunakan bahan desinfektan digunakan untuk membunuh mikroba pada benda mati, seperti alat-alat laboratorium dan bahan antiseptik yang digunakan untuk membunuh mikroba pada jaringan hidup, seperti jaringan tubuh. Penggunaan dan dosis desinfektandan antiseptik ini bervariasi tergantung jenis mikrobia yang akan di bunuh.Contoh kelompok-kelompok utama bahan antimikrobial, yaitu.
1. Fenol dan Persenyawaan Fenolat
Fenoldigunakan untuk pertama kalinya oleh Lister sekitar tahun 1860 – an di dalam pekerjaannya untuk mengembangkan teknik – teknik pembedahan aseptik, fenol telah lama menjadibahan standar pembanding bagi desinfektan lain untuk mengevaluasi aktivitas bakterisidanya.
2. Alkohol
Sterilisasi dengan bahan kimia biasanya digunakan alkohol 70%. Menurut Gupte (1990), etil alkohol sangan efektif pada kadar 70 % daripada 100 % dan ini tidak membunuh spora. Sterilisasi dengan alkohol dilakukan pada proses
pembuatan kultur stok dan teknik isolasi. Alkohol 70 % disemprotkan pada tangan praktikan dan alat-alat seperti makropipet dan mikropipet.Alkohol bila digunakan pada kulit kontaknya terlalu pendek untuk menimbulkan banyak efek germisida dan alkohol segera menguap karena sifatnya mudah menguap. Akan tetapi, alkohol dapat menyingkirkan minyak, partikel debu, dan bakteri. Menurut Gupte (1990), alkohol 70 % dapat menyebabkan denaturasi protein dan koagulasi.
5. Deterjen 6. Aldehide
Sterilisasi secara kimia dapat dilakukan dengan carapemaparan gas atau uap untuk membunuh mikroorganisme dan sporanya. Gas dengan cepat
berpenetrasi ke dalam porisehingga mikroorganisme yang terkristal sekalipun akan terbunuh.Menurut Lay dan Hastowo (1992), bahan yang menjadi rusak bila disterilkan pada suhu yang tinggi dapat disterilkan secara kimiawi dengan menggunakan gas.Bahan kimia yang sering digunakan untuk sterilisasi kimia ditunjukkan oleh Tabel 2.1.
Tabel 2.1 Bahan Kimia Untuk Sterilisasi
No .
Bahan Kimia Ciri-ciri
1. Alkohol Daya kerjanya adalah mengkoagulasi protein, cairan alkohol yang umum digunakan berkonsentrasi 70-80% karena konsentrasi yang lebih tinggi atau lebih rendah kurang efektif.
2. Khlor Gas khlor dengan air akan menghasilkan ion hipokloride yang akan mengkoagulasikan protein sehingga membran sel rusak dan terjadi inaktivasi enzim.
3. Yodium Daya kerjanyaadalah bereaksi dengan tyrosin yaitu suatu asam amino dalam emzim atau protein
mikroorganisme, antiseptik berbasis iodium tidak tepat bila digunakan pada sterilisasi alat medis atau gigi, karena dapat meninggalkan noda.
4. Formaldehida 8 % Konsentrasi 8% merupakan konsentrasi yang cukup ampuh untuk mematikan sebagian besar
mikroorganisme, daya kerjanya adalah berkaitan dengan amino dalam protein mikrobia, bahan ini bekerja secara lambat dan memerlukan tingkat kelembaban relatif sekitar 70%, formaldehide biasa dijual dalam bentuk polimer padat paraformaldehide dalam bentuk flakes atau tablet atau dalam bentuk
formalin.
5. Glutaraldehide Bahan ini bersifat non korosif dan bekerja lebih cepat daripada formaldehid, hanya diperlukan beberapa jam untuk membunuh bakteri, bahan ini aktif melawan bakteri vegetatif; spora; jamur; virus yang
mengandung lipid maupun yang tidak.
6. Gas etilen oksida Gas ini digunakan terutama untuk mensterilkan bahan yang dibuat dari plastik.
7. Natrium
diklorososianurat
Bahan ini berbentuk bubuk, berisi 60% klor, diterapkan pada tumpahan darah atau cairan yang bersifat memiliki bahaya bagi biologi lain selama 10 menit baru kemudian dilanjutkan dengan pembersihan yang lebih lanjut.
8. Kloramina Bahan ini berbentuk serbuk berisi 25% klor, dan hampir tidak berbau, dapat digunakan untuk membasmi kuman air pada minuman, hanya mengandung 1-2 mg/L klor.
9. Klor dioksida Bahan ini adalah sebuah germisida kuat dan bekerja secara cepat, bahan aktif ini didapat dengan cara mereaksikan asam klorida dengan natrium hipoklorit. 10. Senyawa fenolik Senyawa ini aktif melawan bakteri vegetatif dan virus
lipid, namun tidak aktif dalam melawan spora, senyawa ini biasanya berupa Triklosan dan
Klorosilenol yang biasa digunakan sebagai antiseptik. 11. Senyawa Amonium
Kuartener
Banyak digunakan sebagai campuran dan juga dikombinasikan dengan germisida lain, seperti alkohol.
12. Hidrogen peroksida Merupakan oksidan kuat dan germisida efektif yang berspektrum luas, bahan ini dinilai lebih aman bagi manusia dan lingkungan daripada klor.
(Sumber: Lay &Hastowo, 1992)
Salah satu contoh sederhana penerapan sterilisasi secara kimia yang sangat sering digunakan dalam kehidupan sehari-hari adalah penggunaan hand sanitizer.
Handsanitizer merupakan produk inovasi pembersih tangan tanpa air yang juga dikenal dengan pembersih tangan antiseptik. Produk hand sanitizer ini
mengandung antiseptik yang digunakan untuk membunuh kuman yang ada di tangan, yang terdiri dari alkohol dan triklosan. Jenis produk hand sanitizer inipun juga semakin beragam, baik komposisinya, zat pembawanya, serta telah
dipasarkan produk-produk baru yang digunakan secara meluas di masyarakat (Desiyanto & Sitti, 2013).
Mencuci tangan dengan hand sanitizer sangat dianjurkan karena mencuci tangan dengan air mengalir ataupun sabun saja tidak cukup. Saat mencucitangan dengan menggunakan air mengalir, hasilnya hanya sedikit sekali kuman yang hilang karena pada waktu mencuci tangan menggunakan air mengalir, kuman ikut terbawa oleh air yang mengalir meskipun tidak seefektif apabila ditambahkan dengan sabun atau pun dengan zat antiseptik lainnya.Saat mencuci tangan dengan sabun yang tidak mengandung antispetik tidak efektif dalam menghilangkan kuman dan hanya mampu mengangkat kotoran dan minyak saja pada kulit(Desiyanto & Sitti, 2013).
Hand sanitizer mengandung alkohol sebagai bahan utama pembersih tangan. Alkohol mempunyai efek bakterisida yang cepat terhadap bakteri vegetatif gram positif dan gram negatif, MRSA, M.tuberkulosis, beberapa jenis jamur, non-envelope virus. Alkohol bekerja pada bakteri dengan cara mendenaturasi protein dan menghancurkan membran sitoplasma bakteri. E.coli merupakan bakteri vegetatif gram negatif berbentuk kokobasil yang mempunyai peptidoglikan tipis pada dinding sel nya dan dua lapis posfolipid pada membran sitoplasmanya, sehingga alkohol bisa bekerja pada E.coli dengan mendenaturasi protein pada membran sitoplasmanya (Desiyanto & Sitti, 2013).
Pemilihanhand sanitizersebagai alternatif untuk mencuci tangan, perlu dipertimbangkan komposisinya yaitu alkohol, agar dalam pemakaiannya benar-benar efektif terhadap penurunan jumlah angka kuman pada tangan. Alkohol akan bekerja maksimal pada konsentrasi 60-80%. Konsentrasi terbaik alkohol sebagai antiseptik adalah 60-80%. Konsentrasi alkohol lebih tinggi mengurangi kemampuannya dalam
mendenaturasi protein karena denaturasi protein membutuhkan air sehingga pemilihan hand sanitizer terbaik adalah dengan kandungan alkohol sebanyak 60-80%(Desiyanto & Sitti, 2013).
2.3 Macam-Macam Desinfeksi.
Desinfeksi berarti mematikan atau menyingkirkan organisme (kecuali spora dan virus) yang dapat menyebabkan infeksi dengan bahan kimia. Desinfeksi
biasanya dilaksanakan dengan menggunakan zat-zat kimia seperti fenol, formaldehid, klor, iodium atau sublimat terhadap benda mati. Pada umumnya desinfeksi dimaksudkan untuk mematikan sel-sel vegetatif yang lebih sensitif tetapi bukan spora-spora yang tahan panas (Irianto, 2006).
Desinfektan
Desinfektan didefinisikan sebagai bahan atau zat kimia yang digunakan untuk mencegah terjadinya infeksi atau pencemaran jasad renik seperti bakteri dan virus, juga untuk membunuh atau menurunkan jumlah mikroorganisme atau kuman penyakit lainnya (bahan yang digunakan untuk desinfeksi). Bahan desinfektan dapat digunakan untuk proses desinfeksi tangan, lantai, ruangan, peralatan dan pakaian. Hasil proses desinfeksi dipengaruhi oleh beberapa faktor, di antaranya:
1. Beban organik (beban biologis) yang dijumpai pada benda. 1. Tipe dan tingkat kontaminasi mikroba.
2. Pembersihan atau dekontaminasi benda sebelumnya. 3. Konsentrasi desinfektan.
4. Struktur fisik benda.
5. Suhu dan pH dari proses desinfeksi.
Sebelum dilakukan desinfeksi, penting untuk membersihkan alat-alat tersebut dari sisa bahan yang berminyak karena dapat menghambat proses desinfeksi.
Desinfeksi dapat dilakukan melalui cara mencuci, mengoleskan,
merendam, dengan bahan desinfektan, dan menjemur, dengan tujuan mencegah terjadinya infeksi dan mengondisikan alat dalam keadaan siap pakai (Hidayat, A. Aziz Alimul, 2012).
Pemilihan desinfektan merupakan bagian penting dari peran tim pengendalian infeksi. Sehingga dalam pemilihan suatu antiseptik perlu diperhatikan absorpsi, kompatibilitas instrumen, keamanan dan aktivitas mikroba(Fraise, 1999) .
Antiseptik
hidup seperti pada permukaan kulit dan membran mukosa (Levinson, 2008), (Madigan, 2006). Pada dasarnya ada persamaan jenis bahan kimia yang digunakan sebagai antiseptik dan desinfektan. Tetapi tidak semua bahan desinfektan adalah bahan antiseptik karena adanya batasan dalam penggunaan antiseptik. Antiseptik tersebut harus memiliki sifat tidak merusak jaringan tubuh atau tidak bersifat keras. Terkadang penambahan bahan desinfektan juga dijadikan sebagai salah satu cara dalam proses sterilisasi, yaitu proses pembebasan kuman. Tetapi pada
kenyataannya tidak semua bahan desinfektan dapat berfungsi sebagai bahan dalam proses sterilisasi.
Antiseptik berbeda dengan antibiotik dan desinfektan, yaitu antibiotik digunakan untuk membunuh mikroorganisme di dalam tubuh, dan desinfektan digunakan untuk membunuh mikroorganisme pada benda mati (Madigan, 2006). Hal ini disebabkan antiseptik lebih aman diaplikasikan pada jaringan hidup, daripada desinfektan. Penggunaan desinfektan lebih ditujukan pada benda mati, contohnya wastafel atau meja. Akan tetapi, antiseptik yang kuat dan dapat mengiritasi jaringankemungkinan dapat dialihfungsikan menjadi desinfektan contohnyaadalah fenol yang dapat digunakan baik sebagai antiseptik maupun desinfektan.Banyak zat kimia yang digolongkan sebagai antiseptik. Berikut antiseptik yang umumnya digunakan:
1. Alkohol 60-90% (etil, atau isopropil, atau ”methylated spirit”). 2. Klorheksidin glukonat 2-4% (Hibiclens, Hibiscrub, Hibitane).
3. Klorheksidin glukomat dan setrimide, dalam berbagai konsetrasi (Savlon). 4. Yodium 3%, yodium dan produk alkohol berisi yodium atau tincture (yodium tinktur).
5. Iodofor 7,5-10% berbagai konsentrasi (Betadine atau Wescodyne). 6. Kloroksilenol 0,5-4% (para kloro metaksilenol atau PCMX) berbagai konsentrasi (Dettol).
Gambar .contoh beberapa macam antiseptik
Sumber: http://apotik.berkahanugrah.net/produk-2337-betadine-vaginal-douche-100ml.html
Tingkatan untuk proses desinfeksi
Proses Tingkat inaktivasi mikroba Cara
Desinfeksi Tingkat Tinggi
Menghancurkan semua mikro-organisme
kecuali spora bakteri yang jumlahnya banyak
-Dipanaskan dengan suhu 650C-770C dengan waktu 30 menit
-Dikukus
-Desinfeksi dengan bahan kimia glutaradehid, hidrogen peroxida, dan khlorin
Desinfeksi Tingkat Sedang Menghancurkan bakteri vegetatif, mycobacteria, kebanyakan jamur
namun tidak dapat
menghancurkan spora bakteri
-Desinfeksi dengan cairan, yaitu desinfektan rumah sakit dengan label
tentang aktivitas
tuberculocidal, dengan waktu 1 menit Desinfeksi Tingkat Rendah Menghancurkan bakteri vegetatif, beberapa jamur,
tapi tidak untuk mikobakteri atau spora bakteri
-Desinfeksi dengan cairan, yaitu desinfektan rumah sakit tanpa label
tentang aktivitas
tuberculocidal, dengan waktu 1 menit
Oleh karena itu pemilihan tiap jenis proses desinfeksi harus disesuaikan dengan tujuan yang akan dicapai dengan mempertimbangkan beberapa hal misalnya hasil proses desinfeksi, , efektifitas, serta pertimbangan lainnya.
BAB III PENUTUP
3.1 Kesimpulan
Berdasarkan rumusan masalah di atas, maka dapat di tarik kesimpulan sebagai berikut:
1 Pengertian dari sterilisasi adalah suatu usaha untuk membebaskan alat-alat atau bahan dari segala bentuk kontaminasi dari mikroba.
Sedangkan pengertian dari disinfeksi adalah suatu cara membunuh suatu mikroorganisme penyebab penyakit dengan bahan kimia.
2 Macam-macam sterilisasi berdasarkan caranya dapat dilakukan dengan 3 cara yaitu, sterilisasi secara mekanik, sterilisasi secara fisik, dan sterilisasi secara kimia.
3 Macam-macam desinfeksi ada 2 cara, yaitu desinfeksi dengan menggunakan senyawa desinfektan dan desinfeksi menggunakan senyawa antiseptik.
3.2 Saran
1. Mahasiswa mampu memahami lebih rinci mengenai sterilisasi dan desinfeksi beserta macam-macamnya.
2. Mahasiswa mampu menerapkan prinsip sterilisasi dan desinfeksi saat akan melakukan praktikum di laboratorium mikrobiologi, yaitu dengan
menyeterilkan alat-alat dan diri kita masing-masing agar media atau bahan yang diuji tidak terkontaminasi oleh mikroorganisme.
3. Sebelum melakukan sterilisasi dengan kimiawi perlu dikaji terlebih dahulu benda yang akan di sterilisasi. Setelah itu pilih bahan yang efektif sesuai dengan tujuan sterilisasi.
4. Pemilihanhand sanitizersebagai alternatif untuk mencuci tangan, perlu dipertimbangkan komposisinyaagar dalam pemakaiannya benar-benar efektif terhadap penurunan jumlah angka kuman pada tangan.
DAFTAR RUJUKAN
Desiyanto, A. F. & Sitti, N. J. 2013. Efektivitas Mencuci Tangan Menggunakan Cairan Pembersih Tangan Antiseptik (Hand Sanitizer) terhadap Jumlah Angka Kuman. Jurnal Kesehatan Masyarakat, 7(2): 55-112. Dwidjoseputro, S. 1994. Sterilisasi. Jakarta: Gramedia Pustaka Utama.
Entjang, Indan., 2003.Mikrobiologi Dan Parasitologi Untuk Akademi Perawat Dan Sekolah Tenaga Kesehatan yang Sederajat. PT. CITRA ADITIA BAKTI. Bandung.
Fraise. 1999. Choosing disinfectants. The Journal of Hospital Infection. Vol 43, hal 255-264.
Gupte, S. 1990. Mikrobiologi Dasar. Jakarta: Binarupa Aksara.
Hadioetomo, R. S. 1993. Mikrobiologi Dasar dalam Praktek : Teknik dan Prosedur Dasar Laboratorium. Jakarta: Gramedia Pustaka Utama. Hidayat, A. Aziz Alimul. 2012. Pengantar Kebutuhan Dasar Manusia: Aplikasi
Konsep dan Proses Keperawatan. Jakarta: Salemba Medika.
Irianto, Koes. 2006. Mikrobiologi Menguak Dunia Mikroorganisme. Bandung: Yrama Widia.
Kusnadi, Pristiwati, Ammi, S., Widi, P. & Diana, R. 2003. Mikrobiologi. Bandung: JICA.
Lay, B. W. dan Hastowo. 1982.Mikrobiologi. Jakarta: Rajawali Press.
Levinson W. 2008. Review of Medical Microbiology & Imunology, Tenth Edition. New York: The McGraw-Hill Companies, Inc.
Lukas, Stefanus. 2006. Formulasi Steril. Penerbit Andi: Yogyakarta.
Madigan MT, Martinko JM, Brock TD. 2006. Brock Biology of Microorgnisms. New Jersey: Pearson Prentice Hall.
Pratiwi, Sylvia T, Mikrobiologi Farmasi,(Jakarta: Erlangga, 2008) Rutala & Weber. 2013. Disinfection and sterilization: An overview.American
Journal of Infection Control. Vol 41. Hal S2-S5.
Suriawira, 1983. Pengantar Mikrobiologi Umum. Bandung: Angkasa
Suriawiria, Unus. 2005. Pengantar Mikrobiologi Umum. Angkasa: Bandung. Sutedjo, MM. 1996. Mikrobiologi Tanah. Rineka Cipta: Jakarta.
Tim Dosen Mikrobiologi. 2011. Penuntun Praktikum Mikrobiologi. Palu: FMIPA Universitas Tadulako.