EFEK HEPATOPROTEKTIF JANGKA PENDEK INFUSA DAUN Macaranga tanariusL.PADA TIKUS JANTAN GALUR WISTAR
TERINDUKSI PARASETAMOL
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Ilmu Farmasi
Oleh : Ari Widya Nugraha
NIM : 078114061
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
i
EFEK HEPATOPROTEKTIF JANGKA PENDEK INFUSA DAUN Macaranga tanariusL.PADA TIKUS JANTAN GALUR WISTAR
TERINDUKSI PARASETAMOL
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Ilmu Farmasi
Oleh : Ari Widya Nugraha
NIM : 078114061
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iv
”Iman membuka pintu kepada prestasi
yang paling tinggi”
vii
PRAKATA
Puji dan syukur penulis panjatkan ke hadirat Tuhan Yang Maha Esa atas
berkat dan rahmat-Nya, sehingga penulis dapat menyelesaikan skripsi dengan
judul “Efek Hepatoprotektif Jangka Pendek Infusa Daun M. tanarius pada
Tikus Jantan Galur Wistar Terinduksi Parasetamol” ini dengan baik. Skripsi
ini disusun untuk memenuhi salah satu syarat untuk memperoleh gelar Sarjana
Farmasi Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
Penyelesaian skripsi ini tentunya tidak lepas dari bantuan dari berbagai
pihak, baik secara langsung maupun secara tidak langsung. Oleh karena itu
penulis hendak mengucapkan terima kasih kepada :
1. Tuhan Yesus Kristus yang telah memberikan hikmat, kekuatan, tuntunan, dan
pertolongan kepada penulis sehingga skripsi ini dapat terselesaikan sesuai
dengan rencana-Nya.
2. Dekan Fakultas Farmasi Universitas Sanata Dharma.
3. Phebe Hendra, M.Si., Ph.D., Apt., selaku Dosen Pembimbing skripsi ini atas
segala kesabaran untuk selalu membimbing, memberi motivasi, dan memberi
masukan kepada penulis dalam menyusun skripsi ini.
4. Yosef Wijoyo, M.Si., Apt., selaku Dosen Penguji skripsi atas bantuan dan
masukkan kepada penulis demi kemajuan skripsi ini.
viii
6. Yohanes Dwiatmaka, M.Si., selaku Dosen Pembimbing Akademik penulis atas bantuan, masukkan, pendampingan dan dukungan kepada penulis demi
kemajuan skripsi ini.
7. Rini Dwiastuti, M.Si., Apt., selaku Kepala Penanggungjawab Laboratorium
Fakultas Farmasi yang telah memberi izin dalam penggunaan fasilitas
laboratorium Farmakologi-Toksikologi dan Farmakognosi-Fitokimia demi
terselesaikannya skripsi ini.
8. Mas Parjiman dan Mas Heru selaku laboran Laboratorium Farmakologi, Mas
Kayat dan Mas Ratijo selaku laboran Laboratorium Hayati, Mas Wagiran,
selaku laboran Farmakognosi-Fitokimia, serta mas Andri selaku laboran di
kebun obat, atas segala bantuan dan kerjasama selama di laboratorium.
9. Rekan-rekan penelitian tim macaranga, Ariyanti Prima Andini, Elisa Eka,
Dina Wulandari, Andreas Arry Mahendra, dan Aloysia Yossi Kurniawati atas
bantuan, kerjasama, perjuangan dan suka duka yang telah kita alami bersama
selama penelitian.
10. Teman-teman seperjuangan, Cosmaz Mora, Aloysius Bimo Tiar, Hendrika Toi
Doja, Agustina Nila, dan Maria Ratri Damarini atas persahabatan, suka duka
dan kebersamaan kita.
11. Teman-teman FKK A, FKK B, dan FST angkatan 2007 atas kebersamaan kita.
12. Teman-teman UKF Basket Farmasi atas dukungan dan kebersamaan selama
ini.
13. Pihak-Pihak lain yang turut membantu penulis namun tidak dapat disebutkan
ix
Penulis menyadari bahwa setiap manusia tidak ada yang sempurna. Oleh
karena itu, penulis mengharapkan adanya kritik, saran dan masukan demi
kemajuan di masa yang akan datang. Semoga tulisan ini dapat memiliki manfaat
sekecil apapun bagi perkembangan ilmu pengetahuan khususnya di bidang
kefarmasian, serta semua pihak, baik mahasiswa, lingkungan akademis, maupun
masyarakat.
Yogyakarta, 2 Januari 2010
x
DAFTAR ISI
HALAMAN JUDUL………... i
HALAMAN PERSETUJUAN PEMBIMBING………... ii
HALAMAN PENGESAHAN………... iii
HALAMAN PERSEMBAHAN………... iv
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH v PERNYATAAN KEASLIAN KARYA………... vi
PRAKATA...…... vii
DAFTAR ISI………... x
DAFTAR TABEL………... xiv
DAFTAR GAMBAR... xv
DAFTAR LAMPIRAN………... xvi
INTISARI………... xii
ABSTRACT………... xiii
BAB I. PENGANTAR………... 1
A. Latar Belakang………..………... 1
1. Permasalahan...………...………... 3
2. Keaslian penelitian………...……... 4
3. Manfaat penelitian………..…... 5
B. Tujuan Penelitian... 5
BAB II. PENELAHAAN PUSTAKA... 6
xi
B. Kerusakan Hati... 9
C. Hepatotoksin... 10
D. Parasetamol... 10
E. Metode Uji Hepatotoksisitas... 13
F.Macaranga tanariusL... 14
1. Sinonim………... 14
2. Nama daerah………... 14
3.Taksonomi dari daunMacaranga tanariusL. ...………... 15
4. Morfologi………... 15
5. Kandungan tanaman... 15
J. Landasan Teori... 18
K. Hipotesis ... 19
BAB III. METODE PENELITIAN... 20
A. Jenis dan Rancangan Penelitian... 20
B. Variabel Penelitian dan Definisi Operasional ... 20
1. Variabel penenlitian... 20
2. Definisi operasional... 21
C. Bahan Penelitian... 21
1. Bahan utama... 21
2. Bahan kimia... 21
D. Alat Penelitian……... 22
1. Alat pembuatan infusa daunM. tanarius... 22
xii
E. Tata Cara Penelitian ... 23
1. Determinasi daunM. tanarius... 23
2. Pengumpulan bahan uji... 23
3. Pembuatan serbuk daunM. tanarius... 23
4. Pembuatan infusa daunM. tanarius... 24
5. Pembuatan CMC-Na 1%... 24
6. Pembuatan suspensi parasetamol... 24
7. Uji pendahuluan... 25
8. Pengelompokan dan perlakuan hewan uji... 25
9. Pembuatan serum... 26
10. Pengukuran aktivitas serum ALT dan AST... 26
F. Tata Cara Analisis Hasil………...…... 27
BAB IV . HASIL DAN PEMBAHASAN ... 28
A. Hasil Determinasi Tanaman………... 28
B. Orientasi Waktu Pencuplikan Darah Hewan Uji... 28
C. Efek Hepatoprotektif Jangka Pendek Infusa DaunM. tanariusterhadap Ti-kus Jantan Terinduksi Parasetamol... 32
1. Kontrol negatif aquadest 5 g/kgBB………... 36
2. Kontrol parasetamol 2,5 g/kgBB………... .37
3. Kontrol perlakuan infusa daunM. tanarius5 g/kgBB... 38
4. Perlakuan infusa daunM. tanariusdosis 5 g/kgBB pada tikus jantan terinduksi parasetamol 2,5 g/kgBB………... 38
xiii
BAB V. KESIMPULAN DAN SARAN... 45
A. Kesimpulan... 45
B. Saran... 45
DAFTAR PUSTAKA... 46
LAMPIRAN... 49
xiv
DAFTAR TABEL
Tabel I. Aktivitas serum ALT dan Perbandingan Antar Waktu Pencuplikan Darah
pada Parasetamol Dosis 2,5 g/kgBB... 29
Tabel II. Aktivitas serum AST dan Perbandingan Antar Waktu Pencuplikan Darah
pada Parasetamol Dosis 2,5 g/kgBB... 30
Tabel III. Pengaruh perlakuan jangka pendek infusa daunM. tanarius5g/kg BB di
lihat dari aktivitas serum ALT pada berbagai variasi waktu terhadap hepa
toksisitas parasetamol... 33
Tabel IV. Pengaruh perlakuan jangka pendek infusa daunM. tanarius5g/kg BB di
lihat dari aktivitas serum AST pada berbagai variasi waktu terhadap hepa
xv
DAFTAR GAMBAR
Gambar 1. Struktur mikroskopik hati... ... 6
Gambar 2. Struktur parasetamol... 10
Gambar 3. Metabolisme parasetamol dan pembentukan metabolit NAPQI
serta mekanismenya pada terjadinya kematian sel
... 12
Gambar 4. Struktur senyawa dalam tanamanM. tanarius... 17
Gambar 5. Diagram batang aktivitas ALT tikus setelah induksi parasetamol 2,5
g/kg BB pada pencuplikan darah 24 jam, 48 jam, dan 72 jam... 30
Gambar 6. Diagram batang aktivitas AST tikus setelah induksi parasetamol 2,5
g/kg BB pada pencuplikan darah 24 jam, 48 jam, dan 72 jam... 31
Gambar 7. Diagram batang pengaruh praperlakuan IDM dosis 5 g/kg BB pada
aktivitas ALT tikus... 35
Gambar 8. Diagram batang pengaruh praperlakuan IDM dosis 5 g/kg BB pada
xvi
DAFTAR LAMPIRAN
Lampiran 1. Foto daunM. tanarius... 49
Lampiran 2. Foto infusa daunM. tanarius……... 49
Lampiran 3. Surat pengesahan determinasi tanamanM. tanarius... 50
Lampiran 4. Hasil AnalisisKolmogorov-SmirnovdilanjutkanAnova One-Way
data ALT pada orientasi waktu pengambilan cuplikan darah
sete-lah pemberian parasetamol dosis toksik (2,5 g/kgBB)... 51
Lampiran 5. Hasil AnalisisKolmogorov-SmirnovdilanjutkanAnova One-Way
data AST pada orientasi waktu pengambilan cuplikan darah
sete-lah pemberian parasetamol dosis toksik (2,5 g/kgBB)... 54
Lampiran 6. Hasil analisis statistik data ALT perlakuan infusa daumM. tanarius
(5 g/kgBB) pada tikus jantan terinduksi parasetamol dosis toksik
(2,5g/kgBB)... 57
Lampiran 7. Hasil analisis statistik data AST perlakuan infusa daumM. tanarius
(5 g/kgBB) pada tikus jantan terinduksi parasetamol dosis toksik
(2,5g/kgBB)... 77
Lampiran 8. Perhitungan Efek Hepatoprotektif Data ALT... 83
xvii
INTISARI
Telah dilakukan penelitian tentang efek hepatoprotektif jangka pendek infusa daun Macaranga tanarius L. pada tikus jantan terinduksi parasetamol.
Penelitian ini bertujuan untuk memperoleh informasi apakah pemberian jangka pendek infusa daun M. tanarius dapat memberikan efek hepatoprotektif, dan
seberapa lama waktu efektif yang diperlukan untuk berefek hepatoprotektif. Penelitian ini merupakan penelitian eksperimental murni dengan rancangan penelitian acak lengkap pola searah. Metode yang digunakan dalam penelitian ini adalah metode pengukuran aktivitas serum Alanin Aminotransferase (ALT) and serum Aspartat Aminotransferase (AST). Sebanyak 40 tikus jantan galur Wistar dibagi menjadi 8 kelompok, yaitu kelompok kontrol positif (parasetamol dosis 2,5 g/kg BB), kelompok kontrol negatif (hanya diberikan aquadest 5 g/kg BB), kelompok kontrol infusa daunM. tanariusdosis 5 g/kg BB,
dan 5 kelompok perlakuan yang diberi dosis infusa M. tanarius 5 g/kg BB berturut-turut selama ½, 1, 2, 4, dan 6 jam, kemudian diberi parasetamol. Pada 48 jam setelah pemberian parasetamol, diambil cuplikan darah melalui sinus orbitalis mata. Darah yang diambil ditetapkan aktivitas serum ALT dan AST-nya.
Praperlakuan jangka pendek infusa daun M. tanarius 5 g/kg BB mampu menghasilkan efek hepatoprotektif pada tikus jantan terinduksi parasetamol 2,5 g/kg BB dengan waktu ½, 1, 2, 4, dan 6 jam. Waktu paling efektif dalam menghasilkan efek hepatoprotektif yaitu pada waktu 1 jam.
xviii
ABSTRACT
An investigation of hepatoprotective effects of short-term leaves of
Macaranga tanarius L. aqueous extract paracetamol induced in male rats. This
study aimed to obtain information on whether the provision of short term leaves of M. tanarius infusa can provide hepatoprotective effects, and how many time
most effective to produce the hepatoprotective effects.
This research is a pure experimental design with randomized complete unidirectional pattern. The method used in this research is a method of measuring the activity of serum Alanine Aminotransferase (ALT) and serum Aspartate Aminotransferase (AST). A total of 40 male Wistar rats were divided into 8 groups: positive control (paracetamol dose of 2,5 g / kg BB), negative control group (given only distilled water 5 g / kg BB), control group leaves aqueous extractM. tanariusdose of 5 g / kg BB, and 5 treatment groups were given doses
of aqueous extract M. tanarius 5 g / kg BB consecutively for ½, 1, 2, 4, and 6 hours, then given paracetamol. At 48 hours after administration of paracetamol, blood samples were taken through the eye orbital sinus. Blood serum taken specified activity ALT and AST it.
Leaves short-term pre-treatment aqueous extract M. tanarius 5 g / kg BB is able to produce hepatoprotective effects in male rats induced paracetamol 2,5 g / kg BB with a time of ½, 1, 2, 4, and 6 hours. The most effective time in the hepatoprotective effect at the time of 1 hour.
1
BAB I
PENGANTAR
A. Latar Belakang
Hati berperan utama dalam metabolisme dari lemak, karbohidrat, dan protein serta dalam detoksifikasi. Aktivitas hati tersebut didukung dengan memiliki kapasitas cadangan yang besar pula serta hanya memerlukan 10%-20% fungsi jaringan untuk mempertahankan kerjanya (PriceandWilson, 1984). Adanya kapasitas cadangan hati, menyebabkan kerusakan hati tampak ketika hati telah dirusak lebih dari 80%. Kerusakan sel hati dapat dibagi menjadi dua, yaitu kerusakan sel hati akut dan kerusakan sel hati kronis. Kerusakan sel hati akut umumnya diakibatkan nekrosis sel hati yang dapat disebabkan oleh virus hepatitis, obat dan bahan kimia yang toksik. Kerusakan sel hati kronis biasanya diakibatkan oleh sirosis (ChandrasomaandTaylor, 1995).
Pada pengobatan penyakit hati dapat dilakukan antara lain dengan terapi suportif seperti diet, pengeluaran racun (akibat overdosis obat, parasetamol, atau alkohol) kemudian dilakukan terapi aktif. Penggunaan obat tradisional dari bahan tumbuhan baik di Barat maupun Cina membuktikan secara farmakologi dan klinis memberikan efek menguntungkan pada perbaikan hati (Williamson, David, dan Fred, 1996).
Saat ini penggunaan parasetamol dalam masyarakat sendiri sudah sangat luas. Pada umumnya parasetamol aman jika diberikan pada dosis terapetik, yaitu 1 – 4 gram per hari (Forrest, 2006). Dosis parasetamol yang dapat menyebabkan toksik pada manusia normal adalah 15 g (Madan, 1977). Penggunaan overdosis dapat menginduksi terjadinya kerusakan pada hati pada pasien akibat salah satu metabolismenya, yaitu NAPQI (N-asetil-p-benzoquinoneimine) yang sangat reaktif dan menimbulkan hepatotoksisitas (Forrest, 2006). Oleh sebab itu, parasetamol dapat digunakan sebagai salah satu senyawa model dalam penelitian, seperti pada penelitian James, Philip, dan Jack (2003) tentang analisis terhadap dosis hepatotoksik dari asetaminofen (parasetamol).
Indonesia sendiri pemanfaatan tanaman ini sangat sedikit, sehingga tanaman ini sangat menarik dieksplorasi lebih lanjut.
Phommart, Pakawadee, Nitirat, Somsak, dan Somyote (2005) melaporkan salah satu konstituen dari ekstrak n-heksan dan kloroform dari daun M. tanarius berupa flavonoid mempunyai aktivitas antioksidan terhadap DPPH dan nymphaeols B sebagai agen antiinflamasi pada uji siklooksigenase-2. Matsunami, dkk (2006) dan Matsunami, dkk (2009) melaporkan adanya senyawa glikosida, yaitumacarangioside A-C danmallophenolB yang diisolasi dari ekstrak metanolM. tanariusmenunjukkan aktivitas penangkapan radikal terhadap DPPH.
Dari uraian di atas, maka penelitian ini dilakukan untuk menguji efek hepatoprotektif dari daun M. tanarius ini secara jangka pendek. Penelitian efek hepatoprotektif M. tanarius jangka pendek ini dilakukan untuk membandingkan dengan penelitian efek hepatoprotektif jangka panjang (Mahendra, 2011) yang juga dilaksanakan secara bersama. Eksplorasi tanaman tersebut yang dimungkinkan memiliki manfaat di Indonesia, sangat bagus untuk dikembangkan dan dilakukan.
1. Permasalahan
Berdasarkan uraian-uraian di atas, maka dapat dirumuskan permasalahan sebagai berikut.
a. Apakah praperlakuan jangka pendek dapat memberi efek hepatoprotektif pada tikus jantan terinduksi parasetamol?
2. Keaslian penelitian
Sejauh pengamatan penulis, telah dilakukan penelitian oleh Phommart, dkk (2005) melaporkan kandungan senyawa baru, yaitu tanarifuranonol, tanariflavanon C, dan tanariflavanon D bersama dengan tujuh kandungan yang telah diketahui, yaitu
nymphaeol A, nymphaeol B, nymphaeol C, tanariflavanon B, blumenol A (vomifoliol), blumenol B (7,8 dihydrovomifoliol), danannuionone yang antara lain dapat digunakan sebagai antiinflamasi, antioksidan dan antitumor yang diperoleh dari ekstraksi menggunakan pelarutn-heksan dan kloroform dari daun M. tanarius. Matsunami, dkk (2006; 2009) melakukan penelitian dan diketahui bahwa kandungan glikosida, yaitu macarangioside A-C dan mallophenol B pada daun M.
tanarius yang diisolasi dari esktrak metanol mempunyai aktivitas penangkapan radikal terhadap DPPH.
Selain itu, oleh James, dkk (2003), pada penelitian ini dilakukan analisis terhadap dosis hepatotoksik dari asetaminofen (parasetamol) dengan subyek uji mencit. Pada saat yang bersamaan dengan penelitian ini, juga dilakukan penelitian efek analgesik ekstrak metanol-air daunM. tanarius(Andini, 2010) dan infusa daun
M. tanarius (Wulandari, 2010). Selain itu, juga dilakukan penelitian mengenai efek antiinflamasi ekstrak metanol-air daun M. tanarius (Kurniawati, 2010). Pada ketiga penelitian tersebut diduga kandungan glikosida yaitu macarangioside A-C dan
tanarius dengan tikus jantan terinduksi parasetamol belum pernah dilakukan sebelumnya.
3. Manfaat penelitian
a. Manfaat teoritis
Penelitian ini diharapkan dapat bermanfaat bagi pengembangan ilmu pengetahuan khususnya ilmu kefarmasian mengenai infusa daun M. tanarius yang memiliki efek hepatoprotektif jangka pendek.
b. Manfaat praktis
Penelitian ini diharapkan dapat memberikan informasi kepada masyarakat akan manfaat daunM. tanariusyang memiliki efek hepatoprotektif jangka pendek.
B. Tujuan Penelitian
1. Tujuan umum
Penelitian ini bertujuan untuk membuktikan adanya efek hepatoprotektif pada tikus jantan terinduksi parasetamol dengan praperlakuan jangka pendek dari infusa daunM. tanarius.
2. Tujuan khusus
6
BAB II
PENELAAHAN PUSTAKA
A. Anatomi dan Fisiologi Hati
Hati adalah kelenjar terbesar yang memiliki berat rata-rata 1500 g
atau 25% dari berat tubuh. Hati merupakan organ plastis lunak yang dicetak oleh
struktur sekitarnya. Permukaan superior adalah cembung dan terletak di bawah
kanan diafragma dan sebagian kubah-kubah kiri. Bagian bawah hati adalah
cekung dan merupakan atap dari ginjal kanan, lambung, pankreas, dan usus (Price
and Wilson, 1984).
Terdapat dua lobus utama yang menyusun hati yaitu lobus kanan dan
lobus kiri. Lobus kanan dibagi lagi menjadi segmen anterior dan posterior,
sedangkan lobus kiri dibagi menjadi segmen medial dan lateral oleh ligamentum
farsiforme. Ligamentum farsiforme ini berjalan dari hati ke diafragma dan dinding
depan abdomen (Price and Wilson, 1984).
Hepatosit (sel parenkim hati) merupakan sebagian besar dari organ hati.
Hepatosit bertanggung jawab terhadap peran sentral hati dalam metabolisme.
Sel-sel ini terletak di anatara sinusoid yang terisi darah dan saluran empedu seperti
tampak pada gambar 1. SelKupffer melapisi sinusoid hati dan merupakan bagian
penting dari sistem retikuloendotelial tubuh (Lu, 1995). Sel Kupffer ini memiliki
fungsi utama menelan bakteri dan benda asing lain dalam darah. Oleh sebab itu,
hati merupakan salah satu organ utama sebagai pertahanan terhadap invasi bakteri
dan agen toksik (Price and Wilson, 1984).
Selain cabang-cabang vena porta dan arteria hepatika yang melingkari
bagian perifer lobulus hati, juga terdapat saluran empedu seperti ditunjukkan pada
gambar 1. Saluran emepedu interlobular membentuk kapiler empedu yang sangat
kecil dinamakan kanalikuli, yang berjalan ditengah-tengah lempengan sel hati
(Price and Wilson, 1984).
Hati memiliki kapasitas fungsi cadangan. Pada hati normal 80% dari
bagian hati tersebut bekerja tanpa batas. Hati memiliki fungsi dalam sintesis,
ekskretori dan metabolisme. Fungsi pensintesis disini sebagai sumber plasma
albumin, plasma globulin, termasuk α1-antitripsin (α- antiprotease) dan banyak
protein sebagai koagulan. Fungsi menekskresi atau ekskretori, yaitu ekskresi
substansi-substansi dalam empedu. Komponen utama dalam empedu tersebut
adalah bilirubin. Selain itu kolesterol, urobilinogen, dan asam empedu juga
terdapat pada empedu (Chandrasoma and Taylor, 1995).
Hati berperan utama dalam metabolisme dari lemak, karbohidrat, dan
dari jaringan adiposa dan rangkaian medium atau pendek asam lemak yang
diabsorbsi oleh usus dibawa menuju hati. Trigliserid, kolesterol, dan fosfolipid
disintesis dalam hati dari asam lemak dan kompleksnya dengan protein aseptor
lipid spesifik untuk membentuk lipoprotein dengan densitas sangat rendah yang
masuk ke dalam plasma. Hati juga memetabolisme lipoprotein dengan densitas
intermediet dan rendah (Chandrasoma and Taylor, 1995).
Pada metabolisme karbohidrat, hati merupakan sumber utama glukosa
plasma. Setelah makan, glukosa berasal dari absorbsi oleh usus. Pada saat
berpuasa, glukosa dihasilkan dari glikogenolisis dan glukonogenesis dalam hati.
Hati merupakan tempat penyimpanan utama glikogen tubuh. Ketika terjadi
kekurangan glukosa, asam lemak dimetabolisme hati menjadi bentuk keton yang
berperan sebagai sumber energi alternatif dari banyak jaringan (Chandrasoma and
Taylor, 1995).
Selain itu, hati merupakan organ utama dalam katabolisme dan sintesis
urea. Urea akan disekresikan oleh hati ke dalam plasma, yang kemudian akan
diekskresi dalam ginjal. Pada detoksifikasi, hati berperan vital dalam detoksifikasi
komponen racun nitrogen yang dihasilkan dari usus selain itu banyak obat serta
bahan kimia lainnya (Chandrasoma and Taylor, 1995).
Aktivitas hati tersebut didukung dengan memiliki kapasitas cadangan
yang besar pula serta hanya memerlukan 10%-20% fungsi jaringan untuk
B. KerusakanHati
Adanya kapasitas cadangan hati, menyebabkan kerusakan hati tampak
ketika hati telah dirusak lebih dari 80%. Kerusakan sel hati dapat dibagi menjadi
dua yaitu kerusakan sel hati akut dan kerusakan sel hati kronis (Chandrasoma and
Taylor, 1995).
Kerusakan sel hati akut umumnya diakibatkan nekrosis sel hati yang luas
dan akut yang dapat disebabkan oleh virus hepatitis, obat dan bahan kimia yang
toksik. Kerusakan hati akut dapat digolongkan menjai jaundice (kuning),
hipoglikemia, kecenderungan untuk perdarahan yang disebabkan kegagalan
sintesis faktor pembeku darah dalam hati, gangguan elektrolit dan asam basa,
hepatik ensefalopati, sindrom hepatorenal, dan kenaikkan serum enzim yang
berhubungan dengan kasus nekrosis sel hati. Kerusakan sel hati akut memiliki
angka kematian yang tinggi (Chandrasoma and Taylor, 1995).
Kerusakan sel hati kronis biasanya diakibatkan oleh sirosis, yang
berkaitan dengan nekrosis sel hati, fibrosis, dan regenerasi nodular. Efek dari
kerusakan hati kronis, yaitu penurunan sintesis albumin, menyebabkan rendahnya
serum albumin, edema, dan ascites, penurunan protrombin dan faktor VII, IX, dan
X yang menimbulkan perdarahan. Hipertensi portal, hepatik ensefalopati, sindrom
hepatorenal, dan perubahan endokrin yang disebabkan kesalahan metabolisme
C. Hepatotoksin
Banyak obat dan senyawa kimia dapat menyebabkan kerusakan hati
dengan mekanisme yang bervariasi. Obat dan senyawa kimia yang menyebakan
kerusakan hati dapat dibagi menjadi 2, yaitu toksisitas yang dapat diprediksi
(tergantung dosis) dan toksisitas yang tidak dapat diprediksi (idiosinratik)
(Chandrasoma and Taylor, 1995).
Menurut Forrest, 2006 obat yang dapat mengakibatkan kerusakan pada
hati diklasifikasikan menjadi 2 tipe, yaitu tipe yang dapat diprediksi (tipe A) dan
tidak dapat diprediksi (tipe B). Reaksi hepatik yang dapat diprediksi akibat obat
(tipe A) bergantung kepada dosis obat dan bila diberikan dapat mempengaruhi
sebagian besar orang yang menelan obat tersebut dalam jumlah yang cukup dalam
menimbulkan efek toksik. Contoh dari obat tersebut seperti parasetamol, salisilat,
tetarsiklin, dan metotrexat.
Idiosinkratik atau reaksi hepatik tidak dapat diprediksi (tipe B) terjadi
dengan frekuensi rendah (1 : 1000). Tipe ini tidak bergantung pada osis dan
terjadi pada beberapa orang karena adanya reaksi imun atau hipersensitivitas.
Contoh obat pada tipe ini seperti klorpromazine, halotan, dan isoniazid (INH).
D. Parasetamol
Parasetamol atau N-asetil-p-aminofenol dengan struktur senyawa seperti
tampak pada gambar 2, memiliki rumus molekul C8H9 NO2 dan bobot molekul
151,16. Senyawa ini memiliki bentuk berupa serbuk hablur, putih, tidak berbau,
dan rasa sedikit pahit. Parasetamol dapat larut dalam air mendidih, natrium
hidroksida 1N, dan mudah larut dalam etanol (Anonim, 1995).
Obat ini merupakan analgesik dan antipiretik yang efektif, akan tetapi
tidak memiliki efek antiinflamasi seperti aspirin. Parasetamol berguna untuk nyeri
ringan sampai sedang seperti nyeri kepala, mialgia, nyeri pasca kelahiran, dan
keadaan lain. Dosis nyeri akut dan demam dapat dapat ditatalaksana dengan
325-500 mg 4 kali sehari dan untuk anak-anak dalam dosisnya sebanding yang lebih
kecil (Katzung, 1989).
Pada pemakaian dosis terapi, kadang-kadang timbul peningkatan ringan
dalam enzim hati tanpa ikterus, keadaan ini reversibel bila obat dihentikan.
Pemakaian 15 g parasetamol bisa menyebabkan kematian disebabkan
hepatotoksisitas yang parah dengan nekrosis lobulus sentral, kadang-kadang
disertai nekrosis tubulus ginjal akut (Katzung, 1989).
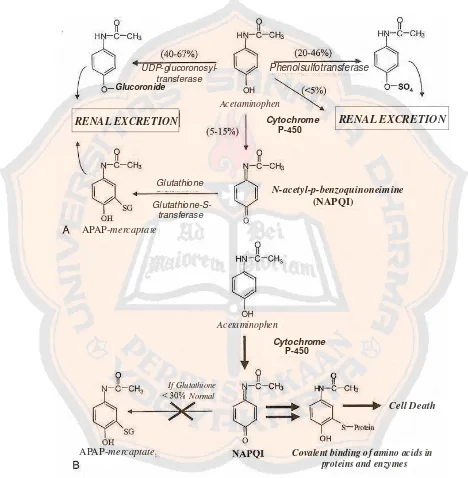
Pada gambar 3 digambarkan bahwa dosis terapetik parasetamol
dimetabolisme dengan konjugasi glukoronida dan komponen sulfat, kemudian
diekskresikan melalui urine. Pada proporsi kecil (5-15%) dioksidasi dengan enzim
oksidase menjadi bentuk yang reaktif, yaitu N-asetil-p-benzoquinoneimine
(NAPQI). Ketika terjadi overdosis, jalur konjugasi menjadi jenuh dan semakin
banyak parasetamol yang dioksidasi. Hal ini mengakibatkan cadangan glutation
metabolit NAPQI. Komponen tersebut akan mengikat secara langsung pada sel
hati, sehingga dapat menyebabkan nekrosis (Forrest, 2006).
UDP-glucoronosyl-transferase
RENAL EXCRETION RENAL EXCRETION
Phenolsulfotransferase
Covalent binding of amino acids in proteins and enzymes
Gambar 3.Metabolisme parasetamol dan pembentukan metabolit NAPQI serta
E. Metode Uji Hepatotoksisitas
Zimmerman (1978) mengemukakan beberapa parameter yang dapat
digunakan untuk mengevaluasi kerusakan hati antara lain : (1) uji enzim serum ;
(2) pemeriksaan asam amino dan protein; (3) perubahan penyusun kimia dalam
hati; (4) uji ekskretori hati; dan (5) analisis histologi.
1) Uji enzim serum
Pengukuran enzim serum (atau plasma) dilakukan untuk mendeteksi
ketoksikan pada hati yang kemudian didukung dengan analisis histologi. Apabila
terjadi kerusakan hati, enzim akan dilepaskan ke dalam darah dari sitosol dan
organela subsel, seperti mitokondria, lisosom, dan nukleus (Zimmerman, 1978).
Enzim-enzim transaminase adalah contoh yang paling utama kelompok enzim hati
yang level serumnya berubah selama gangguan hepatoseluler. Transaminase
terdiri atas alanin aminotransferase (ALT) dan aspartat aminotransaminase (AST).
Sebagian besar AST terdapat di hati dan otot rangka, serta tersebar ke seluruh
jaringan. Meskipun enzim ALT terdapat pula pada beberapa bagian jaringan,
konsentrasi terbesarnya pada semua spesies adalah di hati sehingga ALT
merupakan petunjuk yang lebih spesifik terhadap nekrosis hati daripada AST.
Pada keadaan nekrosis, sel hati akan dipecah sehingga enzim ALT yang terdapat
di dalam sel hati keluar dan masuk ke dalam aliran darah. Peningkatannya bisa
2) Pemeriksaan asam amino dan protein
Pemeriksaan asam amino dan protein penting dilakukan karena
metabolisme asam amino di hati membentuk ammonia dan ureum terjadi secara
lebih lambat dan meningkatkan kadar globulin (Zimmerman, 1978).
3) Perubahan penyusun kimia dalam hati
Perubahan penyusun kimia dalam hati menjelaskan mekanisme kerusakan
hati. Pengukuran jumlah lemak di dalam hati mempunyai hubungan yang dekat
dengan terjadinya steatosis (Zimmerman, 1978).
4) Uji ekskretori hati
Kemampuan hati untuk mensintesis urea, kolesterol, plasma protein, dan
mempertahankan kadar glukosa darah serta asam amino merupakan sebagian
contoh fungsi hati. Adanya ketidaknormalan dari beberapa fungsi hati tersebut
dapat menunjukkan terjadinya kerusakan hati. Perubahan kecepatan metabolisme
obat yang terjadi di hati dapat dijadikan parameter hepatotoksisitas (Zimmerman,
1978).
F. Macaranga tanariusL. 1. Sinonim
Ricinus tanarius L., Macaranga molliuscula, Macaranga tomentosa,
Mappa tanarius(Starr, Kim,andLloyd, 2003). 2. Nama daerah
Di Indonesia tanaman ini dikenal dengan nama tutup ancur (Jawa), mapu
3. Taksonomi dari daunMacaranga tanariusL.
Kingdom :Plantae
Sub-kingdom :Tracheobionta
Divisio :Spermatophyta
Sub-divisio :Magnoliophyta
Classis :Magnoliopsida
Sub-classis :Rosidae
Ordo :Euphorbiales
Familia :Euphorbiaceae
Genus :Macaranga
Spesies :Macaranga tanariusL. (Anonim, 2008).
4. Morfologi
M. tanarius pohon kecil sampai sedang, dengan dahan agak besar. Daun
berseling, agak membundar, dengan stipula besar yang luruh. Perbungaan
bermalai di ketiak, bunga ditutupi oleh daun gagang. Buah kapsul berkokus 2, ada
kelenjar kekuningan di luarnya. Biji membulat, menggelembur. Jenis ini juga
mengandung tanin yang cukup untuk menyamak jala dan kulit (Anonim, 2010).
5. Kandungan tanaman
Dilaporkan empat kandungan baru dari daun M. tanarius MÜLL.-ARG.
(Euphorbiaceae) megastigmate glukosida (Matsunami, dkk, 2009). Matsunami,
dkk (2006) dan Matsunami, dkk (2009) melaporkan adanya senyawa glikosida
yaitumacarangiosideA-C dan mallophenolB yang diisolasi dari ekstrak metanol
kimia dari tanin dalam daun M. tanarius MUELL., et ARG. (Euphorbiaceae)
melaporkan tujuh hydrolyzable tannin yang baru (22-28), bersama dengan dua
puluh satu tanin yang telah diketahui sebelumnya (Lin, Gen-ichiro dan Itsuo,
1990). Selain itu, juga ditemukan ditemukan tiga kandungan baru yaitu
tanarifuranonol, tanariflavanon C, dan tanariflavanon D bersama dengan tujuh
kandungan yang telah diketahui yaitu nimfaeol A, nimfaeol B, nimfaeol C,
tanariflavanon B, blumenol A (vomifoliol), blumenol B (7,8 dihidrovomifoliol,
dan annuionone). Salah satu konstituen dari ekstrak n-heksan dan kloroform dari
daun M. tanarius berupa flavonoid mempunyai aktivitas antioksidan terhadap
DPPH dan nymphaeols B sebagai agen antiinflamasi pada uji siklooksigenase-2.
Adanya kandungan macaranga sebagai senyawa antioksidan dariM. tanariusyang
berpeluang sebagai agen antiinflamasi, dapat mencegah terjadinya oksidasi
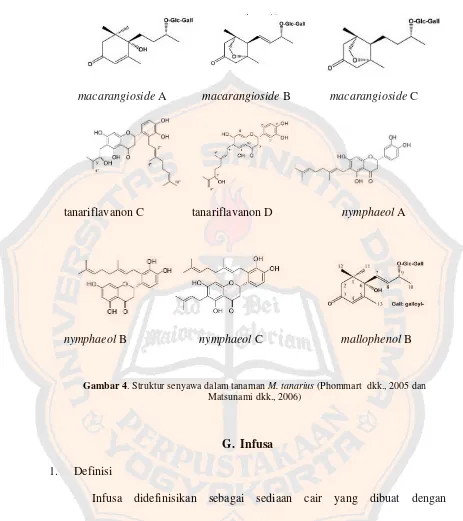
macarangiosideA macarangiosideB macarangiosideC
tanariflavanon C tanariflavanon D nymphaeolA
nymphaeolB nymphaeolC mallophenolB
Gambar 4. Struktur senyawa dalam tanamanM. tanarius(Phommart dkk., 2005 dan
Matsunami dkk., 2006)
G. Infusa
1. Definisi
Infusa didefinisikan sebagai sediaan cair yang dibuat dengan
mengekstraksi simplisia nabati dengan air pada suhu 90°C selama 15 menit
(Anonim, 1995).
2. Pembuatan
Infusa dapat dibuat dengan cara mencampur simplisia dengan derajat
selama 15 menit terhitung mulai suhu mencapai 90°C sambil berkali-kali diaduk.
(Anonim, 1995).
H. Landasan Teori
Kerusakan hati dapat menghasilkan nekrosis maupun sirosis pada sel-sel
hati. Pada kerusakan hati ini salah satunya dapat diketahui dari adanya
peningkatan aktivitas enzim tertentu yang dilepaskan ke dalam darah. Enzim
tersebut seperti alanin aminotransferase (ALT) dan aspartat aminotransaminase
(AST) yang menunjukkan adanya nekrosis pada sel hati. Peningkatan aktivitas
serum enzim tersebut dapat mencapai 10-100 kali dari normal (Zimmerman, 1978)
Parasetamol merupakan salah satu senyawa model hepatotoksik yang
dapat menginduksi terjadinya hepatotoksik, terutama bila dipakai pada dosis
berlebih yaitu 15 g pada individu normal. Hal ini disebabkan adanya pembentukan
metabolit NAPQI (N-asetil-p-benzoquinoeimine) melalui oksidasi yang sangat
reaktif dan dapat berikatan langsung dengan sel-sel hati (Forrest, 2006).
Matsunami, dkk (2006) melaporkan adanya senyawa glikosida, yaitu
macarangioside A-C dan mallophenol B yang diisolasi dari ekstrak metanol M. tanarius dan menunjukkan aktivitas penangkapan radikal terhadap DPPH.
Adanya senyawa glikosida yang memiliki aktivitas penangkapan radikal terhadap
DPPH, maka dilakukan pendekatan dalam penelitian ini.
Glikosida merupakan senyawa yang kurang larut dalam pelarut organik
dengan penggunaan air sebagai pelarut infusa, maka dapat diperoleh lebih banyak
senyawa yang memiliki aktivitas menangkap radikal bebas tersebut.
Adanya kandungan glikosida dalam M. tanarius sebagai senyawa
penangkap radikal bebas, dimungkinkan dapat menangkap radikal bebas seperti
NAPQI. Hal ini mencegah NAPQI merusak sel hati seperti terjadinya nekrosis sel.
Penangkapan radikal bebas oleh senyawa glikosida dalam M. tanarius seperti
macarangioside A-C dan mallophenol B dimungkinkan dilakukan dalam jangka panjang (selama 6 hari) ataupun jangka pendek (kurang dari 6 jam).
I. Hipotesis
Infusa daun M. tanarius memiliki efek hepatoprotektif jangka pendek
pada tikus jantan terinduksi parasetamol. Hal ini dapat diketahui dari adanya
20
BAB III
METODOLOGI PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini termasuk jenis penelitian eksperimental murni dimana dilakukan perlakuan terhadap sejumlah variabel penelitian. Rancangan penelitian ini termasuk rancangan acak lengkap pola searah.
B. Variabel Penelitian dan Definisi Operasional
1. Variabel penelitian
a. Variabel bebas
Lama pemberian infusa daunM. tanarius, yaitu variasi jam pemberian infusa daunM. tanariusdosis tertentu pada tikus jantan terinduksi parasetamol.
b. Variabel tergantung
Efek hepatoprotektif jangka pendek infusa daun M. tanarius. Terhadap sel hati tikus yang terinduksi parasetamol, dengan tolok ukur kuantitatif berdasarkan penurunan aktivitas serum ALT dan AST.
c. Variabel pengacau terkendali
Bahan daun M. tanarius yang dipanen dari Kebun Obat Fakultas Farmasi Sanata Dharma Yogyakarta pada 10 Agustus 2010, cara penyimpanan serbuk daunM. tanarius, rute pemberin infusa secara per oral.
d. Variabel pengacau tak terkendali Kondisi patologis hewan uji
2. Definisi operasional
a. Infusa daun M. tanarius , merupakan serbuk kering daun M. tanarius. yang direbus dengan air pada suhu 900selama 15 menit dengan konsentrasi 100% b. Efek hepatoprotektif infusa adalah kemampuan infusa daunM. tanarius. dosis
tertentu melindungi hati dari hepatotoksin
c. Jangka pendek, yaitu penelitian dilakukan dalam selang waktu ½ jam, 1 jam, 2 jam, 4 jam, dan 6 jam.
C. Bahan Penelitian
1. Bahan utama
a. Subyek uji yang digunakan dalam penelitian ini yaitu tikus jantan putih galur Wistar (berat badan ± 150 – 250 gram, umur : 2 – 3 bulan) diperoleh dari laboratorium Imono Fakultas Farmasi USD Yogyakarta.
2. Bahan kimia
a. Bahan hepatotoksin yang digunakan adalah parasetamol, yang diperoleh dari PT. Konimex Solo
b. Kontrol negatif berupa aquadest yang diperoleh dari Laboratorium Farmakologi-Toksikologi Fakultas Farmasi USD Yogyakarta.
c. Pelarut untuk infusa dengan aquadest yang diperoleh Laboratorium Farmakognosi-Fitokimia Fakultas Farmasi USD Yogyakarta.
d. Bahan untuk mengukur aktivitas serum ALT dan AST berupa reagen SGPT dan SGOT dyasis yang diperoleh dari Laboratorium Farmakologi-Toksikologi Fakultas Farmasi USD Yogyakarta.
e. Aquabidest yang dipergunakan dalam uji serum darah diperoleh dari PT. IKAPHARMINDO PUTRAMAS Jakarta-Indonesia.
D. Alat Penelitian
1. Alat pembuatan infusa daunM. tanarius
Seperangkat alat gelas, yaitu Bekker glass, gelas ukur, cawan porselen, batang pengaduk, penangas air dengan stirer, mesin penyerbuk, dan timbangan analitik.
2. Alat uji hepatoprotektif
user manual (E.merck, Darmsadt, Germany), stopwatch, vortex (Genie, Wilten, Holland), dan sentrifuse.
E. Tata Cara Penelitian
1. Determinasi daunM. tanarius
Determinasi daun M. tanarius dilakukan dengan mencocokkan ciri-ciri tanamanM. tanariuspada buku acuan determinasi (Koorders dan Valeton, 1918) dan disesuaikan dengan kunci determinasinya. Determinasi dilakukan oleh Bapak Ign. Y. Kristio Budiasmoro, M.Si dosen Program studi Pendidikan Biologi Fakultas JP MIPA USD Yogyakarta.
2. Pengumpulan bahan uji
Bahan uji yang digunakan adalah daun M. tanarius yang masih segar dan berwarna hijau, dipanen dari Kebun Obat Fakultas Farmasi USD Yogyakarta pada 10 Agustus 2010.
3. Pembuatan serbuk daunM. tanarius
Daun M. tanarius dicuci dengan air mengalir hingga bersih dan diangin-anginkan hingga kering. Pengoptimalan pengeringan dilakukan dengan oven pada suhu 500 C selama 24 jam. Daun yang telah kering diserbuk dengan alat penyerbuk. Setelah didapatkan serbuk kasar daun, kemudian dilakukan pengayakan dengan ayakan no. 50 untuk mendapatkan serbuk daunM. tanariusyang lebih halus.
4. Pembuatan infusa daunM. tanarius
dijaga tetap dalam suhu tersebut selama 15 menit. Waktu 15 menit dihitung ketika suhu pada campuran mencapai 90°C. Setelah 15 menit, campuran tersebut diambil dan diperas untuk mendapatkan 25,0 mL infusa daunM. tanarius.
5. Pembuatan CMC-Na 1%
Suspending agent CMC-Na 1% dibuat dengan mendispersikan 1,0 gram CMC-Na yang telah ditimbang seksama ke dalam air mendidih dengan volume 100,0 mL. Suspensi CMC-Na ini digunakan untuk membuat suspensi parasetamol.
6. Pembuatan suspensi parasetamol
Suspensi parasetamol dalam CMC-Na 1% dibuat dengan mensuspensikan 25,0 gram parasetamol yang telah ditimbang seksama ke dalam CMC-Na 1%. Banyaknya parasetamol yang disuspensikan pada CMC-Na 1% disesuaikan pada dosis yang akan diberikan.
7. Uji pendahuluan
a. Penetapan dosis hepatotoksik parasetamol
Penetapan dosis hepatotoksik ini dilakukan dengan melakukan studi literatur. Pada penelitian ini ditetapkan dosis hepatotoksik parasetamol yaitu 2,5 g/kg BB . (Yunita, Antonius, Erly, Imelda, dan Imono, 2006). Pemilihan dosis hepatotoksik ini karena dosis tersebut menyebabkan kerusakan sel-sel hati pada tikus jantan tetapi tidak menyebabkan kematian pada tikus jantan.
b. Penetapan waktu pencuplikan darah
pencuplikan darah tikus jantan dengan cara membagi tikus jantan dikelompokan dengan jumlah 5 ekor. Diambil darahnya pada jam ke 24, jam ke 48, dan jam ke 72. Serum darah diambil untuk diukur aktivitas serum ALT dan AST.
8. Pengelompokan dan perlakuan hewan uji
Hewan percobaan yang dibutuhkan sebanyak 40 ekor tikus jantan dibagi secara acak dalam 8 kelompok sama banyak. Kelompok I merupakan kontrol hepatotoksin parasetamol dengan dosis 2,5 g/kg BB secara per oral. Kelompok II merupakan kontrol negatif yaitu pemberian aquadest dosis 5 g/kg BB secara per oral. Kelompok III merupakan kontrol perlakuan yaitu pemberian infusaM. tanariusdosis 5 g/kg BB secara per oral. Kelompok IV-VIII diberikan infusa daunM. tanariusdosis 5 g/kg BB, kemudian secara berturut-turut pada ½, 1, 2, 4, dan 6 jam setelah perlakuan diberikan dosis hepatotoksik parasetamol 2,5 g/kg BB. Pada jam ke-48 setelah diberi parasetamol, semua kelompok diambil darahnya pada daerah sinus orbitalis mata untuk penetapan aktivitas serum ALT dan AST.
9. Pembuatan serum
Darah mencit diambil melalui sinus orbitalis mata dengan pipa kapiler dan ditampung dalam evendrof, kemudian disentrifugasi dengan kecepatan 3000 rpm selama 15 menit dan diambil supernatannya (serum).
10. Pengukuran aktivitas serum ALT dan AST
LDH (laktat dehidrogenase). Reagen II berisi 2-oksoglutarat dan NADH. Analisis dilakukan dengan reaksi sebagai beikut, serum atau plasma sebanyak 100µL dicampur dengan reagen I sebanyak 800 µL, setelah itu dicampurkan 200 µL reagen II, dan dibaca resapan setelah satu menit.
Pada analisis fotometri dengan serum AST dilakukan reaksi sebagai berikut, yaitu reagen I dan reagen II. Reagen I berisi TRIS (pH 7,65), L-Aspartat, LDH (laktat dehidrogenase), dan MDH (malat dehidrogenase). Reagen II berisi 2-oksoglutarat dan NADH. Analisis dilakukan dengan reaksi sebagai berikut, serum atau plasma sebanyak 100µL dicampur dengan reagen I sebanyak 800 µL. Setelah itu dicampurkan 200 µL reagen II, dan dibaca resapan setelah satu menit.
Aktivitas enzim dilihat pada panjang gelombang 340 nm, suhu 37o, dan faktor koreksi 1745. Aktivitas serum ALT dan AST dinyatakan dalam U/L. Pengukuran aktivitas serum ALT dan AST dilakukan di Laboratorium Farmakologi-Toksikologi Fakultas Farmasi USD Yogyakarta.
F. Tata Cara Analisis Hasil
Data aktivitas serum ALT dan AST dianalisis dengan metode Kolmogorov
28
BAB IV
HASIL DAN PEMBAHASAN
A. Hasil Determinasi Tanaman
Pada penelitian ini penulis melakukan determinasi terhadap tanaman yang akan digunakan, yaitu M. tanarius. Determinasi ini dilakukan untuk memastikan bahwa tanaman dan yang digunakan adalah benarM. tanarius. Determinasi tanaman dilakukan di Laboratorium Farmakognosi Fitokimia, Fakultas Farmasi Universitas Sanata Dharma Yogyakarta. Determinasi dilakukan hingga tingkat spesies dengan identifikasi bagian bunga, buah, batang, dan daun yang membuktikan bahwa benar tanaman tersebut merupakanM. tanarius.
B. Orientasi Waktu Pencuplikan Darah Hewan Uji
aktivitas serum ALT yang terdapat secara spesifik dalam organ hati. Aktivitas serum ALT terdapat pada hati, jantung, otot, serta jaringan lain. Adanya kombinasi kenaikkan serum ALT dan AST pada hewan uji menunjukkan terjadinya kerusakan hati, kombinasi kedua enzim ini lebih sensitif dibandingkan dengan enzim golongan hidrogenase lain.
Berikut merupakan hasil orientasi waktu pencuplikan darah hewan uji yang disajikan dalam bentuk tabel dan diagram batang :
Tabel I. Aktivitas serum ALT dan perbandingan antar waktu pencuplikan darah pada
parasetamol dosis 2,5 g/kg BB
Waktu Pencuplikan
(Jam)
Purata Aktivitas serum ALT+ SE
Perbedaan Terhadap
24 jam 48 jam 72 jam
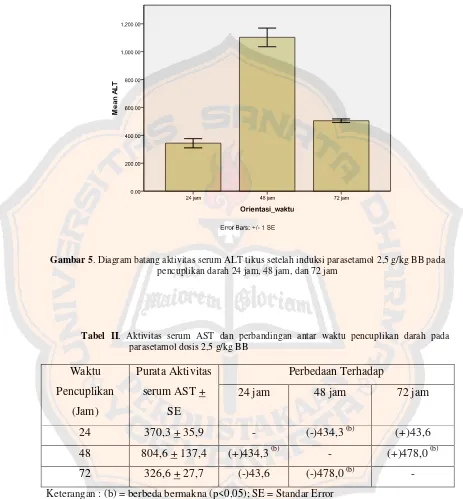
Gambar 5. Diagram batang aktivitas serum ALT tikus setelah induksi parasetamol 2,5 g/kg BB pada pencuplikan darah 24 jam, 48 jam, dan 72 jam
Tabel II. Aktivitas serum AST dan perbandingan antar waktu pencuplikan darah pada
parasetamol dosis 2,5 g/kg BB
Waktu Pencuplikan
(Jam)
Purata Aktivitas serum AST +
SE
Perbedaan Terhadap
24 jam 48 jam 72 jam
Gambar 6. Diagram batang aktivitas serum AST tikus setelah induksi parasetamol 2,5 g/kg BB pada pencuplikan darah 24 jam, 48 jam, dan 72 jam
Untuk data tabel II dan gambar 6 dari serum AST juga menunjukkan adanya peningkatan pada pencuplikan darah 48 jam dibandingkan dengan pencuplikan darah pada 24 jam dan 72 jam. Selain itu, dari kedua data serum ALT dan AST secara statistik menunjukkan perbedaan yang bermakna pada pencuplikan darah 48 jam (p<0,05) dibandingkan dengan pencuplikan darah 24 jam dan 72 jam. Oleh sebab itu, penulis memilih pencuplikan darah hewan uji pada 48 jam setelah induksi parasetamol dengan dosis 2,5 g/kg BB.
C. Efek Hepatoprotektif Jangka Pendek Infusa DaunM. tanariusTerhadap Tikus Jantan Terinduksi Parasetamol
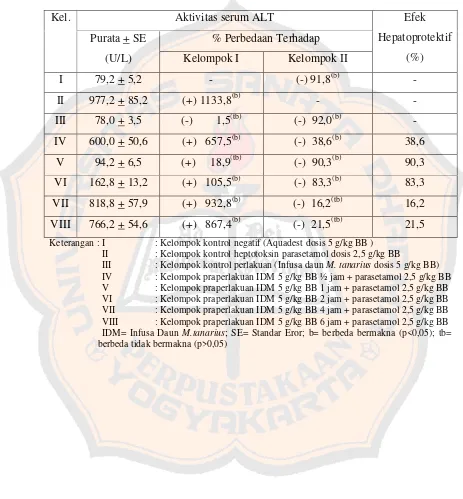
Tabel III. Pengaruh perlakuan jangka pendek infusa daunM. tanarius5 g/kg BB dlihat dari aktivitas serum ALT pada berbagai variasi waktu terhadap hepatoksisitas parasetamol
Kel. Aktivitas serum ALT Efek
Hepatoprotektif (%) Purata + SE
(U/L)
% Perbedaan Terhadap Kelompok I Kelompok II
I 79,2 + 5,2 - (-) 91,8(b)
-Keterangan : I : Kelompok kontrol negatif (Aquadest dosis 5 g/kg BB ) II : Kelompok kontrol heptotoksin parasetamol dosis 2,5 g/kg BB
Tabel IV. Pengaruh perlakuan jangka pendek infusa daunM. tanarius5 g/kg BB dilihat dari aktivitas serum AST pada berbagai variasi waktu terhadap hepatoksisitas parasetamol
Kel. Aktivitas serum AST Efek
Hepatoprotektif (%) Purata + SE (U/L) % Perbedaan Terhadap
Kelompok I Kelompok II
I 138,4 + 4,9 - (-) 79,4(b)
-Keterangan : I : Kelompok kontrol negatif (Aquadest dosis 5 g/kg BB ) II : Kelompok kontrol hepatotoksin parasetamol dosis 2,5 g/kg BB
Gambar 7. Diagram batang pengaruh praperlakuan IDM dosis 5 g/kg BB pada aktivitas serum ALT tikus
Gambar 8. Diagram batang pengaruh praperlakuan IDM dosis 5 g/kg BB pada aktivitas serum AST
1. Kontrol negatif (Aquadest 5 g/ kg BB)
Aktivitas serum ALT yang dihasilkan dari kelompok ini adalah 79,2 + 5,2 U/L (tersaji pada tabel III). Nilai serum ALT ini dijadikan patokan nilai normal serum ALT dalam penelitian ini selanjutnya. Sebagai data pendukung dilakukan pengukuran terhadap aktivitas dari serum AST yang menghasilkan data 138,4 + 4,9 U/L (tersaji pada tabel IV), data ini juga digunakan sebagai patokan nilai normal dari penelitian ini selanjutnya. Tujuan dari kontrol negatif ini adalah memastikan bahwa peningkatan aktivitas serum ALT dan AST pada tikus jantan adalah akibat pemberian hapatotoksin parasetamol, bukan akibat dari aquadest dan memastikan bahwa efek hepatoprotektif pada tikus jantan yang terinduksi parasetamol adalah akibat praperlakuan infusa daunM. tanarius.
2. Kontrol hepatotoksin (parasetamol 2,5 g/kg BB)
Kontrol hepatotoksin ini bertujuan untuk mengetahui pengaruh induksi parasetamol 2,5 g/kg BB terhadap sel hati tikus, selain itu juga digunakan sebagai patokan dalam menganalisa efek hepatoprotektif infusa daun M. tanarius. Aktivitas serum ALT kontrol hepatotoksin parasetamol 2,5 g/kg BB adalah sebesar 977,2 + 85,2 (tersaji pada tabel III), sedangkan untuk aktivitas serum AST dihasilkan data 673,2 + 110,3 (tersaji pada tabel IV).
Dibandingkan dengan aktivitas serum ALT kontrol negatif sebesar 79,2 + 5,2 U/L maka terlihat adanya kenaikan aktivitas serum ALT sekitar 12,3 kalinya, sedangkan persentase perbedaan 1133,8% dibandingkan dengan kontrol negatif. Kenaikan aktivitas serum ALT lebih dari 10 kali lipat ini dapat menunjukkan bahwa kondisi sel hati tikus telah mengalami kerusakan.
3. Kontrol perlakuan (Infusa DaunM. tanarius5 g/kg BB)
Kelompok ini dilakukan perlakuan dengan pemberian dosis 5 g/kg BB infusa daunM. tanariuspada tikus tanpa pemberian parasetamol. Aktivitas serum ALT yang dihasilkan adalah 78,0 + 3,5 U/L (pada tabel III). Bila dibandingkan dengan kontrol negatif menunjukkan perbedaan 1,5% dan secara statistik menunjukkan perbedaan tersebut tidak bermakna (p>0,05). Hal ini berarti infusa daun M. tanarius tidak menimbulkan efek yang berbeda dari kontrol negatif aquadest.
Pada aktivitas serum AST dari kelompok ini menurut hasil uji statistik (pada tabel IV) adalah 121,2 + 6,2 U/L. Perbandingan dengan kontrol negatif menunjukkan perbedaan 12,4% dan secara statistik perbedaan tersebut tidak bermakna (p>0,05). Hasil ini menunjukkan bahwa infusa M. tanarius juga tidak menaikkan aktivitas serum AST pada tikus jantan. Untuk itu dapat dikatakan bahwa infusa daun M.
tanariusini tidak memiliki efek yang berpengaruh pada sel hati tikus jantan.
4. Perlakuan infusa daun M. tanarius 5 g/kg BB pada tikus jantan terinduksi parasetamol 2,5 g/kg BB
Pada penelitian ini penulis membatasi waktu praperlakuan jangka pendek infusa daunM. tanariussebelum pemejanan parasetamol adalah ½ jam sampai 6 jam. Dari rentang waktu tersebut, ditentukan waktu sebagai praperlakuan infusa daunM.
tanariusyaitu ½, 1, 2, 4, dan 6 jam.
menunjukkan berbeda bermakna (p<0,05), sedangkan efek hepatoprotektif yang dihasilkan adalah 38,6%. Hal ini menujukkan efek hepatoprotektif yang dihasilkan belum terlalu besar, sehingga dosis infusa daunM. tanariuspada kelompok ini belum dapat melindungi sel hati dari kerusakan yang terjadi secara optimal.
Data aktivitas serum ALT tersebut didukung dengan pengukuran aktivitas serum AST yang secara statistik dihasilkan 661,2 + 45,9 U/L. Dibandingkan dengan kontrol hepatotoksin parasetamol menunjukkan berbeda tidak bermakna (p>0,05) dan memiliki efek hepatoprotektif 1,7%. Aktvitas serum AST belum menunjukkan penurunan dengan efek hepatoprotektif yang sangat kecil tersebut. Hal ini menguatkan data aktivitas serum AST dimana pada praperlakuan ½ jam tersebut belum dapat melindungi hati dari hepatotoksik parasetamol.
Kelompok praperlakuan 1 jam infusa daun M. tanarius 5g/kg BB (kelompok V) dari tabel III menunjukkan hasil aktivitas serum ALT 94,2 + 6,5 U/L. Pada praperlakuan ini aktivitas serum ALT mengalami penurunan 10,3 kali dibandingkan dengan kontrol hepatotoksin parasetamol dan memiliki persentase perbedaan dari kontrol hepatotoksin parasetamol 90,3%. Hasil ini menunjukkan perbedaan yang bermakna (p<0,05) dibandingkan dengan kontrol hepatotoksin parasetamol . Dari efek hepatoprotektif pada serum ALT kelompok ini memiliki efek paling tinggi, yaitu 90,3%.
menunjukkan perbedaan yang bermakna (p<0,05) dibandingkan dengan kontrol hepatotoksin parasetamol, selain itu pada efek hepatoprotektif memiliki persentase tertinggi yaitu 72,2%. Dari data yang dihasilkan tersebut dapat disimpulkan bahwa kelompok praperlakuan 1 jam infusa daun M. tanariusmampu melindungi hati dari kerusakan sel-sel hati akibat adanya hepatotoksin parasetamol pada tikus jantan.
Pada praperlakuan 2 jam infusa daun M. tanarius 5 g/kg BB (kelompok V) didapatkan hasil 162,8 + 13,2 U/L dengan persentase perbedaan dibandingkan dengan kontrol positif adalah 83,3%. Dari data tersebut terjadi penurunan aktivitas serum ALT 6 kali dan uji statistik menunjukkan hasil yang berbeda bermakna (p<0,05) dibandingkan dengan kontrol hepatotoksin parasetamol. Efek hepatoprotektif yang dihasilkan juga tergolong tinggi yaitu 83,3%. Akan tetapi, hasil ini lebih rendah dibandingkan dengan kelompok praperlakuan 1 jam.
Praperlakuan 4 jam infusa daun M. tanarius menunjukkan hasil aktivitas serum ALT 818,8 + 57,9 U/L dengan persentase perbedaan dibandingkan dengan kontrol hepatotoksin parasetamol adalah 16,2%. Secara statistik menunjukkan hasil yang berbeda tidak bermakna (p>0,05) dibandingkan kontrol hepatotoksin parasetamol. Untuk efek hepatoprotektif yang dihasilkan memiliki persentase terkecil diantara semua kelompok praperlakuan, yaitu 16,2%. Untuk aktivitas serum AST yang dihasilkan adalah 862,4 + 37,6 U/L lebih tinggi dibandingkan dengan kontrol hepatotoksin parasetamol. Persentase perbedaan dibandingkan kelompok kontrol hepatotoksin parasetamol adalah 28,1% dan secara statistik berbeda tidak bermakna (p>0,05). Pada efek hepatoprotektif yang dihasilkan adalah 28,1%. Dari data serum ALT didukung data serum AST tersebut menunjukkan kemampuan infusa dalam melindungi sel hati pada kelompok ini lebih kecil dan mengalami penurunan dibandingkan kelompok praperlakuan 1 dan 2 jam.
dibandingkan dengan kelompok kontrol hepatotoksin parasetamol. Efek hepatoprotektif pada aktivitas serum AST ini juga kecil dibandingkan kelompok 1 dan 2 jam, yaitu sebesar 20,6%. Dari hasil aktivitas serum ALT didukung data serum AST menunjukkan bahwa pada klompok praperlakuan 6 jam memiliki kemampuan yang rendah dalam melindungi sel-sel hati dari hepatotoksin parasetamol.
Adanya kandungan glikosida seperti macarangioside A-C dan mallophenol B pada M. tanarius dimungkinkan dapat menangkap radikal bebas atau metabolit aktif seperti NAPQI pada proses terjadinya toksisitas oleh parasetamol. Pada pendekatan struktur kimia senyawa glikosida tersebut memiliki gugus karbonil (C=O) dengan ikatan rangkap terkonjugasi, hal ini memungkinkan terjadinya penangkapan metabolit aktif NAPQI sehingga ikatan kovalen antara NAPQI dengan protein sel dapat diminimalkan.
D. Rangkuman Pembahasan
Hasil yang diperoleh dalam penelitian ini adalah praperlakuan jangka penek infusa daunM. tanarius 5 g/kg BB mampu menghasilkan efek hepatoprotektif pada waktu ½, 1, 2, 4, dan 6 jam secara berturut-turut untuk serum ALT adalah 38,6%; 90,3%; 83,3%; 16,2%; 21,5%. Sedangkan pada serum AST memiliki efek hepatoprotektif pada ½, 1, 2, 4, dan 6 jam secara berturut-turut sebesar 1,7%; 72,2%; 57,9%; 28,1%; 20,6%. Hasil ini sesuai dengan hipotesis yaitu infusa daun M.
Pada kelompok kontrol positif perlakuan M. tanarius menunjukkan hasil yang berbeda tidak bermakna dibandingkan dengan kontrol negatif aquadest. Hal ini menujukkan bahwa infusa daunM. tanarius tidak memiliki pengaruh terhadap sel-sel hati tikus jantan, sehingga kenaikkan serum ALT dan AST pada penilitian ini diakibatkan oleh induksi parasetamol pada tikus jantan.
Jangka waktu pemberian infusa M. tanarius yang paling baik sebagai hepatoprotektor adalah pada praperlakuan 1 jam dan 2 jam. Akan tetapi, pada uji statistik keduanya berbeda tidak bermakna dalam menurunkan aktivitas serum ALT dan AST. Pada penelitian ini dipilih pada waktu praperlakuan infusa daun M.
tanarius 1 jam sebagai waktu paling efektif. Hal ini dikarenakan waktu yang dibutuhkan lebih singkat, yaitu hanya 1 jam dalam memberikan efek hepatoprotektif pada tikus jantan.
ketiga adalah adanya penangkapan radikal bebas oleh senyawa yang terkandung dalamM. tanarius yaitu macarangioside A-C dan mallophenolB. Senyawa tersebut dapat menangkap radikal bebas NAPQI dan menjadikannya metabolit sekunder, sehingga dapat dibuang melalui ekskresi ginjal tubuh.
45
BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
Berdasarkan hasil data yang diperoleh dan analisis statistik yang telah dilakukan, maka dapat disimpulkan :
1. Praperlakuan jangka pendek infusa daun M. tanarius 5 g/kg BB mampu menghasilkan efek hepatoprotektif pada tikus jantan terinduksi parasetamol 2,5 g/kg BB dengan waktu ½, 1, 2, 4, dan 6 jam secara berturut-turut untuk GPT-serum adalah 38,6%; 90,3%; 83,3%; 16,2%; 21,5% dan GOT-GPT-serum pada ½, 1, 2, 4, dan 6 jam secara berturut-turut sebesar 1,7%; 72,2%; 57,9%; 28,1%; 20,6%. 2. Praperlakuan 1 jam infusa daunM. tanarius5 g/kg BB merupakan waktu paling
efektif untuk menghasilkan efek hepatoprotektif pada tikus jantan teriduksi parasetamol 2,5 g/kg BB.
B. Saran
Perlu dilakukan penelitian lebih lanjut mengenai :
1. Uji hepatoprotektif dengan infusa daun M. tanarius untuk induksi hepatotoksin yang lain seperti karbon tetraklorida atau galaktosamin.
2. Uji kandungan senyawa antioksidan yang spesifik pada tanaman M. tanarius dalam menimbulkan efek hepatoprotektif.
46
DAFTAR PUSTAKA
Andini, A.P., 2010, Efek Analgesik Ekstrak Metanol-Air DaunMacaranga tanarius L. Pada Mencit Betina Galur Swiss, Skripsi, Universitas Sanata Dharma, Yogyakarta
Anonim, 2008, Informasi Spesies- Mara Macaranga tanarius L. M.A. http://www.plantamor.com/index.php?plant=804, diakses tanggal 19 Maret 2010
Anonim, 2010, Prosea-Macarangatanarius,
http://www.proseanet.org/prohati4/browser.php?docsid=162, diakses tanggal 19 Maret 2010
Chandrasoma, P., & Taylor, C.R., 1995,Concise Pathology, 2ndedition, 620-623, 626, 641-642, FRC Path Prentice Hall International, USA
Direktorat Jendral Pengawasan Obat dan Makanan RI, 1995, Farmakope Indonesia, Edisi IV, 7, 649, Departemen Kesehatan Republik Inonesia, Jakarta
Forrest, E., 2006, Hepatic Disorders, in Anne, L., (Eds.),Adverse Drug Reaction, 2nd ed, 193, 201, 202, Pharmaceutical Press, London
Hastuti, T., 2008, Aktivitas enzim Transaminase dan Gambaran Histopatologi Tikus yang Diberikan Kelapa Kopyor Pasca Induksi Parasetamol,Laporan Penelitian, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institus Pertanian Bogor, Bogor
James, L.P., Philip, R.M., dan Jack, A.H., 2003, Acetaminophen-Induced Hepatotoxicity, Am. Soc. Pharm. Expe. Therap., 31, 1499-1506.
Katzung, B.G., 1989, Farmakologi Dasar dan Klinik, Edisi 3, 488-489, Penerbit Buku Kedokteran EGC, Jakarta
Kavalci C., Kavalci G., dan Sezenler E., 2009, Acetaminophen poisoning: Case Report, In. J. Tox., Volume 6 Number 2
Koorders, S.H dan Valeton Th., 1918, Atlas der Baumarten Von Java, Buch und Steindruckerei von Fa. P. W. M. TRAP, Leiden
Lenny, S., 2006, Isolasi dan Uji Bioaktifitas Kandungan kimia Utama Puding Merah dengan Metode Uji Brine Shrimp, Laporan Penelitian, 5, Departemen Kimia Fakultas MIPA USU, Medan
Lenny, S., 2006, Senyawa Flavonoida, Fenilpropanoida, dan Alkaloida, Laporan Penelitian,14-16, Departemen Kimia Fakultas MIPA USU, Medan
Lim, T.Y., Lim Y.Y., Yule C.M., 2008, Evaluation of antioxidant, antibacterial and anti-tyrosinase activities of four Macaranga species,Elsevier, Vol 114, 594 Lin, J.H., Gen-ichiro N., dan Itsuo N., 1990, Tannins and Related Compounds.
XCIV.1) Isolation and Characterization of Seven New Hydrolyzable Tannins from the Leaves of Macarangan tanarius (L.) MUELL., et ARG., Chem. Pharm. Bull.,38 (5) 1218-1223
Lu, F.C., 1995, Basic Toxicology : Fundamentals, Target Organs, and Assesment, diterjemahkan oleh Edi Nugroho, Edisi 2, 206-220, Penerbit Universitas Indonesia
Madan, L.P., 1977, Acetaminophen Toxicity,J. Clin. Pharm, 17, 557
Mahendra, A.A., 2011, Efek Hepatoprotektif Infusa Daun Macaranga tanarius L. Pada Tikus Jantan Terinduksi Parasetamol,Skripsi, Universitas Sanata Dharma, Yogyakarta
Matsunami K., Ichiko T., Takakazu S., Mitsunori A., Kazunari ., Hideaki O., dkk., 2006, Radical-Scavenging Activities of New Megastigmane Glucosides from Macaranga tanarius L. MÜLL.-ARG., Chem. Pharm. Bull., 54(10) 1403— 1407
Matsunami, K., Hideaki O., Kazunari K., Takakazu S., Masatoshi K., Kentaro Y., dkk., 2009, Absolute configuration of (+)-pinoresinol 4-O-[600-O-galloyl]-b-D-glucopyranoside, macarangiosides E, and F isolated from the leaves of Macaranga tanarius,Phytochemistry, 70 (2009) 1277–1285
Olson, K. R., 2006,Poisoning & Drug Overdose, Mc Graw Hill, San Fransisco. Phommart, S., Pakawadee S., Nitirat C., Somsak., dan Somyote S., 2005,
Constituents of the Leaves of Macaranga tanarius,J. Nat. Prod., 68, 927-930. Price, A.S and Wilson M.L., 1984, Patofisiologi : Konsep Klinik Proses-Proses
Robinson, T., 1991, The Organic Constituent of Higher Plants, diterjemahkan oleh Kosasih Padmawinata, Edisi ke-6, 191-193, ITB, Bandung
Starr, F., Kim, S., and Lloyd, L., 2003, Macaranga tanarius L., United States Geological Survey--Biological Resources Division Haleakala Field Station, Maui, Hawai'i
Widyaningrum, Y., 2004, efek Hepatoprotektif Kombinasi Jus Wortel (Daucus carota, L.) dan Apel Hijau ( Pyrus malus, L.) Pada Mencit Jantan Terinduksi Parasetamol,Skripsi, 24-25, Universitas Sanata Dharma, Yogyakarta
Williamson, E.M., David T.O., dan Fred J.E., 1996, Pharmacological Methods in Phytotherapy Research Volume 1: Selection, Preparation, and Pharmacological Evaluation of Plant Material, 47, John Wileys & Sons, Cichester, England World Health Organisation (WHO), 2008a, Hepatitis B,
http://www.who.int/mediacentre/fact-sheets/fs204/en/, diakses tanggal 23 desember 2010
World Health Organisation (WHO), 2008b, Hepatitis A, http://www.who.int/mediacentre/fact-sheets/fs328/en/, diakses tanggal 23 desember 2010
World Health Organisation (WHO), 2009, Cancer, http://www.who.int/mediacentre/fact-sheets/fs297/en/, diakses tanggal 23 desember 2010
Wulandari, D., 2010, Efek Analgesik Infusa Daun Macaranga tanarius L. Pada Mencit Betina Galur Swiss,Skripsi, Universitas Sanata Dharma, Yogyakarta Yunita, Antonius A., Erly S., Imelda W., dan Imono A. D., 2006, Efek
Hepatoprotektif Rebusan Herba Putri Malu (Mimosa pudica, L.) pada Tikus Terangsang Parasetamol, Laporan Penelitian, Laboratorium Farmakologi dan Toksikologi, Fakultas Farmasi, Universitas Sanata Dharma, Laboratorium Farmakologi dan Toksikologi, Fakultas Farmasi, Universitas Gadjah Mada Yogyakarta
LAMPIRAN
Lampiran 1. Daun M. tanarius
Lampiran 4. Hasil AnalisisKolmogorov-SmirnovdilanjutkanAnova One-Way data ALT pada orientasi waktu pengambilan cuplikan darah setelah pemberian parasetamol dosis toksik (2,5 g/kgBB)
Descriptive Statistics
N Mean Std. Deviation Minimum Maximum
ALT 9 650.3333 352.24033 304.00 1214.00
One-Sample Kolmogorov-Smirnov Test
ALT
N 9
Normal Parametersa,,b Mean 650.3333 Std. Deviation 352.24033
Most Extreme Differences Absolute .305
Positive .305
Negative -.163
Kolmogorov-Smirnov Z .914
Asymp. Sig. (2-tailed) .374
a. Test distribution is Normal.
Oneway
95% Confidence Interval for
Mean
Minimum Maximum Lower Bound Upper Bound
24 jam 3 343.6667 57.81292 33.37830 200.0514 487.2819 304.00 410.00
48 jam 3 1102.3333 115.14484 66.47890 816.2977 1388.3690 984.00 1214.00
72 jam 3 505.0000 22.06808 12.74101 450.1799 559.8201 482.00 526.00
Total 9 650.3333 352.24033 117.41344 379.5774 921.0892 304.00 1214.00
ANOVA
ALT
Sum of Squares df Mean Square F Sig.
Between Groups 958410.667 2 479205.333 84.132 .000
Within Groups 34175.333 6 5695.889
Total 992586.000 8
(I-J) Std. Error Sig.
95% Confidence Interval
Lower Bound Upper Bound
24 jam 48 jam -758.66667* 61.62191 .000 -956.3040 -561.0293 72 jam -161.33333 61.62191 .102 -358.9707 36.3040
48 jam 24 jam 758.66667* 61.62191 .000 561.0293 956.3040 72 jam 597.33333* 61.62191 .000 399.6960 794.9707 72 jam 24 jam 161.33333 61.62191 .102 -36.3040 358.9707
48 jam -597.33333* 61.62191 .000 -794.9707 -399.6960 *. The mean difference is significant at the 0.05 level.
ALT
Scheffea Orientasi
_waktu N
Subset for alpha = 0.05
1 2
24 jam 3 343.6667
72 jam 3 505.0000
48 jam 3 1102.3333
Sig. .102 1.000
Means for groups in homogeneous subsets are
displayed.
Lampiran 5. Hasil AnalisisKolmogorov-SmirnovdilanjutkanAnova One-Way data AST pada orientasi waktu pengambilan cuplikan darah setelah pemberian parasetamol dosis toksik (2,5 g/kgBB)
Descriptive Statistics
N Mean Std. Deviation Minimum Maximum
SGOT 9 500.5556 260.93922 273.00 1029.00
One-Sample Kolmogorov-Smirnov Test
SGOT
N 9
Normal Parametersa,,b Mean 500.5556 Std. Deviation 260.93922
Most Extreme Differences Absolute .255
Positive .255
Negative -.192
Kolmogorov-Smirnov Z .766
Asymp. Sig. (2-tailed) .600
a. Test distribution is Normal.
b. Calculated from data.
ANOVA
SGOT
Sum of Squares df Mean Square F Sig.
Between Groups 419036.222 2 209518.111 10.003 .012
Within Groups 125678.000 6 20946.333
Total 544714.222 8
24 jam 3 370.3333 62.22808 35.92740 215.7502 524.9164 330.00 442.00
48 jam 3 804.6667 238.01330 137.41705 213.4088 1395.9245 555.00 1029.00
72 jam 3 326.6667 48.12830 27.78689 207.1093 446.2240 273.00 366.00
Multiple Comparisons
(I-J) Std. Error Sig.
95% Confidence Interval
Lower Bound Upper Bound
24 jam 48 jam -434.33333* 118.17031 .029 -813.3360 -55.3306 72 jam 43.66667 118.17031 .935 -335.3360 422.6694
48 jam 24 jam 434.33333* 118.17031 .029 55.3306 813.3360 72 jam 478.00000* 118.17031 .019 98.9973 857.0027 72 jam 24 jam -43.66667 118.17031 .935 -422.6694 335.3360
48 jam -478.00000* 118.17031 .019 -857.0027 -98.9973 *. The mean difference is significant at the 0.05 level.
Homogeneous Subsets
Subset for alpha = 0.05
1 2
72 jam 3 326.6667
24 jam 3 370.3333
48 jam 3 804.6667
Sig. .935 1.000
Means for groups in homogeneous subsets are
displayed.
Lampiran 6. Hasil analisis statistik data ALT perlakuan infusa daum M. tanarius (5 g/kgBB) pada tikus jantan terinduksi parasetamol dosis toksik (2,5 g/kgBB)
One-Sample Kolmogorov-Smirnov Test
ALT
N 40
Normal Parametersa,,b Mean 447.0500 Std. Deviation 373.31206
Most Extreme Differences Absolute .254
Positive .254
Negative -.151
Kolmogorov-Smirnov Z 1.604
Asymp. Sig. (2-tailed) .012
a. Test distribution is Normal.
b. Calculated from data.
Kruskal-Wallis Test
Ranks
Kontrol_perlakuan N Mean Rank
ALT Kelompok kontrol aquadest 5 7.10
Kelompok kontrol parasetamol 5 35.60
Kelompok kontrol Macaranga 5 6.00
Kelompok 1/2 jam 5 24.40
Kelompok 1 jam 5 10.90
Kelompok 2 jam 5 18.00
Kelompok 4 jam 5 32.00
Kelompok 6 jam 5 30.00
Test Statisticsa,b
ALT
Chi-Square 34.907
df 7
Asymp. Sig. .000
a. Kruskal Wallis Test
b. Grouping Variable:
Kontrol_perlakuan
Mann-Whitney Test
Ranks
Kontrol_perlakuan N Mean Rank Sum of Ranks
ALT Kelompok kontrol aquadest 5 3.00 15.00
Kelompok kontrol parasetamol 5 8.00 40.00
Total 10
Test Statisticsb
ALT
Mann-Whitney U .000
Wilcoxon W 15.000
Z -2.611
Asymp. Sig. (2-tailed) .009
Exact Sig. [2*(1-tailed Sig.)] .008a a. Not corrected for ties.
Mann-Whitney Test
Ranks
Kontrol_perlakuan N Mean Rank Sum of Ranks
ALT Kelompok kontrol aquadest 5 5.90 29.50
Kelompok kontrol Macaranga 5 5.10 25.50
Total 10
Test Statisticsb
ALT
Mann-Whitney U 10.500
Wilcoxon W 25.500
Z -.419
Asymp. Sig. (2-tailed) .675
Exact Sig. [2*(1-tailed Sig.)] .690a a. Not corrected for ties.
b. Grouping Variable: Kontrol_perlakuan
Mann-Whitney Test
Ranks
Kontrol_perlakuan N Mean Rank Sum of Ranks
ALT Kelompok kontrol aquadest 5 3.00 15.00
Kelompok 1/2 jam 5 8.00 40.00
Test Statisticsb
ALT
Mann-Whitney U .000
Wilcoxon W 15.000
Z -2.611
Asymp. Sig. (2-tailed) .009
Exact Sig. [2*(1-tailed Sig.)] .008a a. Not corrected for ties.
b. Grouping Variable: Kontrol_perlakuan
Mann-Whitney Test
Ranks
Kontrol_perlakuan N Mean Rank Sum of Ranks
ALT Kelompok kontrol aquadest 5 4.20 21.00
Kelompok 1 jam 5 6.80 34.00
Total 10
Asymp. Sig. (2-tailed) .175
Exact Sig. [2*(1-tailed Sig.)] .222a a. Not corrected for ties.