OPTIMASI KONSENTRASI SOY LECITHIN DAN DURASI SONIKASI FORMULASI NANOPARTIKEL LIPID DENGAN ZAT AKTIF RESORCINOL MENGGUNAKAN PROBE SONICATOR: APLIKASI
METODE FACTORIAL DESIGN
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm.)
Program Studi Farmasi
Oleh :
Agustine Nita Wulandari NIM : 178114125
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
2021
ii
Persetujuan Pembimbing
OPTIMASI KONSENTRASI SOY LECITHIN DAN DURASI SONIKASI FORMULASI NANOPARTIKEL LIPID DENGAN ZAT AKTIF RESORCINOL MENGGUNAKAN PROBE SONICATOR :APLIKASI
METODE FACTORIAL DESIGN
Skripsi yang diajukan oleh Agustine Nita Wulandari
NIM : 178114125
Telah disetujui oleh
Pembimbing Utama
(Dr. apt. Rini Dwiastuti) Tanggal : 3 Juni 2021
iii
Pengesahan Skripsi Berjudul
OPTIMASI KONSENTRASI SOY LECITHIN DAN DURASI SONIKASI FORMULASI NANOPARTIKEL LIPID DENGAN ZAT AKTIF RESORCINOL MENGGUNAKAN PROBE SONICATOR :APLIKASI
METODE FACTORIAL DESIGN
Oleh :
Agustine Nita Wulandari NIM : 178114125
Dipertahankan di hadapan Panitia Penguji Skripsi Fakultas Farmasi
Universitas Sanata Dharma Pada tanggal : 18 Juni 2021
Mengetahui Fakultas Farmasi Universitas Sanata Dharma
Dekan
Dr. apt. Yustina Sri Hartanti
Panitia Penguji Tanda Tangan
1. apt. Wahyuning Setyani, M.Sc. ………
2. Dr. Jeffry Julianus, M.Si. ………
3. Dr. apt. Rini Dwiastuti ………
iv
PERNYATAAN KEASLIAN KARYA
Saya menyatakan dengan sesungguhnya bahwa skripsi yang saya tulis ini tidak memuat karya atau bagian karya orang lain, kecuali yang telah disebutkan dalam kutipan dan daftar pustaka, dengan mengikuti ketentuan sebagaimana layaknya karya ilmiah. Apabila di kemudian hari ditemukan indikasi plagiarisme pada naskah ini, maka penulis bersedia menanggung segala sanksi sesuai peraturan perundang-undangan yang berlaku.
Yogyakarta, 3 Juni 2021 Penulis,
Agustine Nita Wulandari
v
LEMBAR PERNYATAAN PERSETUJUAN
PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS
Yang bertanda tangan di bawah ini, saya mahasiswa Universitas Sanata Dharma :
Nama : Agustine Nita Wulandari
Nomor Mahasiswa : 178114125
Demi pengembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul :
Optimasi Konsentrasi Soy Lecithin dan Durasi Sonikasi Formulasi Nanopartikel Lipid dengan Zat Aktif Resorcinol Menggunakan Probe Sonicator: Aplikasi Metode Factorial Design.
Dengan demikian saya memberikan kepada Perpustakaan Universitas Sanata Dharma hak untuk menyimpan, me-ngalihkan dalam bentuk media lain, mengelolanya dalam bentuk pangkalan data, mendistribusikan secara terbatas, dan mempublikasikannya di Internet atau media lain untuk kepentingan akademis tanpa perlu meminta ijin dari saya maupun memberikan royalti kepada saya selama tetap mencantumkan nama saya sebagai penulis.
Atas kemajuan teknologi informasi, saya tidak berkeberatan jika nama, tanda tangan, gambar atau image yang ada di dalam karya ilmiah saya terindeks oleh mesin pencari (search engine), misalnya google.
Demikian pernyataan ini yang saya buat dengan sebenarnya.
Dibuat di Yogyakarta Pada tanggal : 21 Juli 2021
Yang menyatakan
(Agustine Nita Wulandari)
vi ABSTRAK
Resorcinol merupakan senyawa untuk pengobatan penyakit kulit secara topikal dengan sifat kepolaran yang tinggi sehingga kemampuan difusinya terhambat oleh penghalang lapisan lipid pada stratum corneum kulit. Menjerap senyawa resorcinol pada sistem nanopartikel lipid diharapkan dapat mengatasi permasalahan tersebut. Penelitian ini bertujuan untuk mengetahui formula optimum dengan ukuran partikel yang baik dan memperoleh nilai efisiensi penjerapan menggunakan metode Factorial Design.
Penelitian ini merupakan eksperimen kuasi dengan variabel bebas yaitu konsentrasi soy lecithin dan durasi sonikasi. Variabel tergantung yaitu ukuran partikel dan efisiensi penjerapan. Rancangan optimasi menggunakan FD software Minitab17. Analisis statistik menggunakan Analysis of Variance (ANOVA).
Dari uji parameter persamaan model secara serentak diperoleh nilai p- value = 0,000 untuk respon ukuran partikel yang menunjukkan bahwa variabel- variabel bebas telah mewakili model. Sedangkan dari uji parameter persamaan model untuk pengujian efisiensi penjerapan diperoleh nilai p-value = 0,110 yang menunjukkan model yang digunakan tidak valid. Area optimum hanya dapat ditentukan untuk respon ukuran partikel. Analisis response optimizer digunakan untuk menentukan prediksi formula yang optimal dimana formula 2 dengan konsentrasi soy lecithin 6,5% w/v dan 40 menit sonikasi terprediksi sebagai formula optimum. Waktu penyimpanan yang konsisten perlu diperhatikan sebelum pengujian dilakukan terkait dengan stabilitas sediaan uji.
Kata kunci : soy lecithin, durasi sonikasi, optimasi.
vii ABSTRACT
Resorcinol is a compound for the treatment of skin diseases topically with high polarity so that diffusion ability is hampered by the barrier of the lipid layer in the stratum corneum of the skin. Entrapment of resorcinol in lipid nanoparticle systems is expected to overcome these problems. This study aims to determine the optimum formula with a good particle size and to obtain the value of entrapment efficiency using the Factorial Design method.
This study is a quasi-experimental with independent variables, namely the concentration of soy lecithin and duration of sonication. The dependent variables are particle size and entrapment efficiency. Optimization using FD with software Minitab17. Statistical analysis using Analysis of Variance (ANOVA).
From the simultaneous test of the model equation parameters, the p-value
= 0.000 for the particle size response indicates that the independent variables represent the model. Meanwhile, from the model equation parameter test for testing the entrapment efficiency, the p-value = 0.110, which indicates the model used is not valid. The optimum area can only be determined for the particle size response.
Response optimizer analysis was used to determine the optimal formula prediction which formula 2 with soy lecithin concentration of 6.5% w/v and 40 minutes of sonication was predicted as the optimum formula. Consistency of storage time needs to be considered before testing is carried out regarding the stability of the test preparation.
Keywords : soy lecithin, sonication duration, optimization.
viii DAFTAR ISI
Halaman
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
LEMBAR PERNYATAAN KEASLIAN KARYA ... iv
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI... v
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... ix
DAFTAR GAMBAR ... x
DAFTAR LAMPIRAN ... xi
PENDAHULUAN ... 1
METODOLOGI PENELITIAN ... 4
Jenis dan Rancangan Penelitian ... 4
Alat dan Bahan Penelitian ... 4
Perancangan Desain Penelitian ... 5
Pembuatan Sediaan Nanopartikel Lipid ... 7
Pengujian Ukuran Partikel ... 8
Pengukuran Nilai Persen Efisiensi Penjerapan ... 9
Analisis Data Statistik ... 10
HASIL DAN PEMBAHASAN ... 12
Formulasi Sediaan Nanopartikel Lipid Resorcinol ... 12
Pengujian Ukuran Partikel Sediaan Nanopartikel Lipid ... 12
Pengujian Efisiensi Penjerapan ... 15
Respon Sifat Fisik Sediaan Berdasarkan Statistik ANOVA ... 17
Penentuan Area dan Komposisi Optimum ... 22
KESIMPULAN DAN SARAN ... 24
Kesimpulan ... 24
Saran ... 24
DAFTAR PUSTAKA ... 25
LAMPIRAN ... 29
BIOGRAFI PENULIS ... 54
ix
DAFTAR TABEL
Halaman
Tabel I. Faktor dan Level dalam Penelitian ... 5
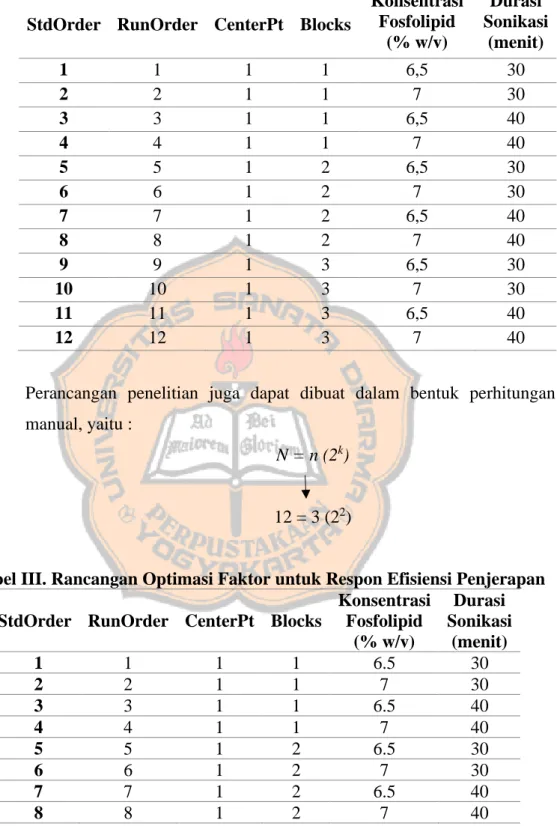
Tabel II.Rancangan Optimasi Faktor untuk Respon Ukuran Partikel ... 6
Tabel III. Rancangan Optimasi Faktor untuk Respon Efisiensi Penjerapan ... 6
Tabel IV. Formula Acuan Nanopartikel Lipid Resorcinol... 7
Tabel V. Formula Modifikasi Nanopartikel Lipid Resorcinol ... 8
Tabel VI. Hasil Ukuran Partikel dan Nilai IP Sediaan Nanopartikel Lipid ... 14
Tabel VII. Data Hasil Pengujian Efisiensi Penjerapan ... 17
Tabel VIII. Respon Ukuran Partikel pada Uji Statistik ANOVA ... 18
Tabel IX. Data Prediksi dan Aktual terhadap Respon Ukuran Partikel ... 18
Tabel X. Respon Efisiensi Penjerapan pada Uji Statistik ANOVA ... 21
x
DAFTAR GAMBAR
Halaman
Gambar 1. Uji Normalitas Residual untuk Respon Ukuran Partikel ... 19
Gambar 2. Grafik Uji Homokedastisitas untuk Respon Ukuran Partikel ... 19
Gambar 3. Grafik Uji Independensi Residual untuk Respon Ukuran Partikel ... 20
Gambar 4. Diagram Efek Pareto terhadap Ukuran Partikel ... 20
Gambar 5. Contour Plot Respon Ukuran Partikel terhadap Kedua Variabel ... 23
xi
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Pengujian Ukuran Partikel ... 29
Lampiran 2. Dokumentasi Hasil Formulasi Sediaan Nanopartikel Resorcinol ... 41
Lampiran 3. Pengujian Efisiensi Penjerapan ... 42
Lampiran 4. Data Optimasi Fase Gerak Metode Analisis HPLC ... 52
Lampiran 5. Data Perhitungan Persentase Efisiensi Penjerapan ... 53
1 PENDAHULUAN
Pengembangan sediaan obat dengan pembawa berbasis lipid telah meningkat dimana menggunakan banyak sistem partikulat lipid seperti liposom, transfersom, etosom, niosom, dan iskom (immunostaining coplexes) (Rajabi and Mousa, 2016). Nanopartikel lipid merupakan nanopartikel dengan komponen molekul lipid yang memiliki beberapa keunggulan seperti tingkat toksisitasnya yang rendah (Rajabi and Mousa, 2016), efisiensi pemuatan obat, dan potensinya dalam melepaskan obat (Attama et al., 2012). Nanopartikel lipid berkembang pesat karena memiliki potensi yang menguntungkan dalam sistem penghantaran obat, pengobatan klinis, dan pengembangan penelitian (Puri et al., 2009).
Banyak penelitian formulasi liposom yang menggunakan fosfolipid soy lecithin karena memiliki stabilitas yang baik terhadap variasi pH atau konsentrasi garam dalam formula (Machado et al., 2014). Soy lecithin itu sendiri mengandung asam lemak tak jenuh yang tinggi sehingga memiliki kompatibilitas dan penetrasi yang baik dalam tubuh (Kang et al., 2005) (cit., Putri et al., 2017).
Phosphatidylcholine merupakan fosfolipid utama dari pembentukan lesitin kedelai (Risselada and Marrink, 2009) (cit., Dwiastuti et al., 2016a). Fosfolipid fosfatidilkolin atau yang biasanya disebut "lesitin" memiliki sifat amphiphilic yang akan mempermudah terbentuknya bilayer konsentris (atau juga awalnya disebut
"bangosom" oleh A.D. Bangham) (Puri et al., 2009).
Penghantaran oleh soy lecithin ini dapat diterapkan pengaplikasiannya pada bahan aktif resorcinol. Penggunaan resorcinol dalam sediaan farmasi digunakan sebagai pengobatan pada kondisi kulit yang bermasalah secara topikal, seperti jerawat, dermatitis seboroik, eczema, psoriasis, dan kutil. Sediaan resorcinol juga bisa dalam bentuk sediaan anti-jerawat dengan konsentrasi maksimum 2% (World Health Organization, 2006). Dalam suatu pengujian obat, asam salisilat merupakan senyawa yang memiliki nilai sebanding dengan resorcinol dalam sifat keratolitiknya setelah resorcinol pertama kali diperkenalkan ke dalam penggunaan obat (Welsch, 2008) dengan mekanisme aksi mengurangi kohesi antar sel antara korneosit dengan melarutkan bahan semen antarsel dan mengurangi pH stratum corneum, sehingga meningkatkan hidrasi dan pelunakan (Jacobi et al., 2015) dan
mengelupas dengan tidak memiliki nilai absorbsi pada sistemik ketika digunakan secara topikal (Medscape, 2020). Resorcinol memiliki kelarutan sebesar 1 g dalam 0,9 mL (O’Neil, 2013) (HSDB, 2020a) yang merupakan senyawa polar dengan kelarutan air yang tinggi yang berdampak pada kemampuan difusinya pada kulit yang terhambat oleh penghalang fase lipid dengan viskositas tinggi atau lapisan hidrofobik (Azzahra dan Musfiroh, 2018) pada stratum corneum kulit (Welsch, 2008). Fosfolipid digunakan sebagai sistem penghantar obat (Azzahra dan Musfiroh, 2018) yang diharapkan dapat mengatasi permasalahan tersebut.
Pembuatan sistem nanopartikel lipid, yaitu liposom dengan soy lecithin, menggunakan metode kombinasi metode pemanasan (metode Mozafari) dengan sonikasi (Dwiastuti et al., 2016b). Dari metode sintesis tersebut, ukuran diameter partikel dapat dipengaruhi oleh suhu pencampuran (Putri et al., 2017) dan durasi proses sonikasi (Dua, et al., 2012). Suhu transisi soy lecithin dalam pembuatan sistem penghantar obat sangat perlu diperhatikan. Soy lecithin memiliki suhu transisi pada 50-60oC. Dispersi soy lecithin membentuk fase gel pada suhu kurang dari 50°C, sedangkan jika di atas suhu transisi, akan membentuk fase kristal cair.
Membran berubah dari fase gel menjadi fase kristal cair. Dalam pembuatan sistem liposom, setiap molekul dapat bergerak lebih bebas kemudian membentuk lapisan lipid menjadi liposom pada fase cair, sehingga tahap ini merupakan titik kritis saat formulasi (Putri et al., 2017). Pada penelitian ini akan dilakukan sintesis sediaan nanopartikel lipid pada suhu 60oC sesuai dengan literatur yang diacu (Dwiastuti et al., 2018, 2016b, 2016a).
Pada proses sonikasi, gelombang ultrasonik memiliki energi yang dapat memecah sistem dari ukuran besar menjadi lebih kecil. Ukuran partikel yang dihasilkan tidak boleh terlalu kecil terkait dengan jumlah obat yang dapat dijerap, sehingga perlu dioptimalkan lama waktu sonikasi (Shashi et al., 2012). Selain terkait jumlah obat yang dapat dijerap, ukuran partikel dengan ukuran ≤ 40 nm dapat mempengaruhi kinerja obat topikal karena terjadi penetrasi ke lapisan dermis melalui stratum corneum (Gautam et al., 2011). Dalam penelitian yang dilakukan Putri et al. (2017), dalam mensintesis nanopartikel lipid membutuhkan durasi sonikasi yang sesuai yaitu selama 30 menit dan 40 menit pada suhu pembuatan
60oC. Optimasi faktor konsentrasi fosfolipid dalam sediaan nanopartikel lipid juga menjadi hal yang penting karena berpengaruh pada ukuran nanopartikel yang dihasilkan (Narsaiah et al., 2013). Dalam penelitian (Dwiastuti et al., 2016a), diperoleh nilai ukuran partikel yang sesuai dalam range (50-100 nm) dan dengan nilai SD terendah dengan konsentrasi fosfolipid sebesar 68 mg/mL, dari hasil tersebut, peneliti akan mensintesis sediaan nanopartikel lipid dengan membuat dua level yang masuk dalam range konsentrasi fosfolipid standar tersebut.
Sintesis ini melibatkan fenomena penjerapan obat dalam sistem kompleks nanopartikel lipid dimana dapat mewakili jumlah zat aktif resorcinol yang terperangkap (Chang and Yeh, 2012) dan menjadi hal penting untuk menentukan kandungan obat dalam sistem kompleks tersebut menggunakan metode analisis yang sesuai (Jeschek et al., 2016). Penentuan kadar free drug dapat dilakukan dengan perhitungan persen efisiensi penjerapan dalam sediaan liposom (yang juga termasuk dalam sediaan nanopartikel lipid) yang dibantu dengan metode HPLC (Chimanuka, Gabriëls, Detaevernier, and Plaizier-Vercammen, 2002) (cit., Dwiastuti et al., 2018). Hal tersebut didukung juga oleh dua penelitian sebelumnya yang telah mengembangkan metode HPLC dalam kuantifikasi resorcinol dalam sediaan perawatan rambut (De et al., 2016, 2014).
Ketika optimisasi formula maupun proses formulasi, desain screening, misalnya full factorial dapat memungkinkan screening sejumlah besar faktor dalam jumlah eksperimen yang relatif kecil. Metode ini digunakan untuk mengidentifikasi faktor yang paling mempengaruhi sistem yang diterapkan dalam konteks proses pengoptimalan. Paling sering, faktor-faktor dievaluasi pada dua tingkat dalam desain ini. Desain faktorial dengan dua level untuk masing-masing faktor, biasa digunakan dalam proses desain skrining karena pertimbangan efisiensi dan ekonomis (Candioti et al., 2014).
Dalam penelitian ini, optimasi konsentrasi fosfolipid dan durasi sonikasi dalam formulasi sediaan nanopartikel lipid dari fosfolipid soy lecithin dengan menggunakan kombinasi metode pemanasan (suhu pembuatan 60oC) dan ultrasonikasi untuk menghasilkan sistem penghantar bahan aktif resorcinol dengan ukuran partikel yang baik menggunakan metode analisis desain faktorial.
4 METODOLOGI PENELITIAN
Jenis dan Rancangan Penelitian
Jenis penelitian termasuk jenis penelitian eksperimental kuasi, dimana tidak dilakukan randomisasi terhadap variabel bebas konsentrasi soy lecithin dalam formula dan durasi sonikasi, dengan menggunakan metode factorial design (FD) dan dua level untuk menentukan konsentrasi fosfolipid yaitu soy lecithin dan durasi sonikasi optimum pada formulasi sediaan nanopartikel lipid dengan bahan aktif resorcinol sehingga dapat memperoleh sediaan dengan ukuran partikel yang baik dan nilai efisiensi penjerapannya. Dalam penelitian ini, penentuan level untuk mencapai parameter ukuran partikel sebesar 50-100 nm dan memperoleh nilai efisiensi penjerapan sediaan berdasarkan pada hasil penelitian yang dilakukan oleh Dwiastuti et al., (2016a) yang memasuki range ukuran partikel yang mencapai 50- 100 nm.
Alat dan Bahan Penelitian
Alat-alat yang digunakan dalam penelitian ini adalah mortir dan stamper, Model 300VT probe sonicator, ultra-turrax, blender, hot plate, ultra-purified water (Thermo Scientific, Amerika), HPLC dengan UV detector (Shimadzu LC-2010C, Japan), gelas ukur 100 mL, gelas beaker 250 mL, pipet tetes, batang pengaduk, magnetic stirrer, thermometer, statif, neraca analitik (OHAUS (min 0.01), America), cawan porselen, sendok, micropipette (Socorex), particle size analyzer (PSA) dengan Dynamic Light Scattering (DLS) Universitas Islam Indonesia, VIVASPIN 500 3kDa, software Minitab17, Microtube, dan wadah penyimpanan (botol vial 100 mL).
Bahan-bahan yang digunakan dalam penelitian ini adalah Resorcinol (Pharmaceutical Grade) (Tokyo Chemical Industry), serbuk soy lecithin (Nacalai Pharmaceutical Grade), ethanol (Pro-Analysis Grade), aquabidest (Laboratorium Kimia Analisis Instrumen Universitas Sanata Dharma), fase gerak HPLC (Acetonitrile : Methanol (gradient grade for liquid chromatography, Merck, USA) : Aquabidest), dan aluminium foil.
Perancangan Desain Penelitian
a. Penentuan faktor dan level penelitian
Berdasarkan latar belakang permasalahan dalam penelitian ini, maka faktor yang akan diteliti adalah konsentrasi dari fosfolipid soy lecithin dan durasi sonikasi dalam proses sintesis sediaan nanopartikel lipid. Kedua faktor tersebut akan dibuat dua variasi level untuk menunjang proses optimasi, dimana penentuan level dipandu pada hasil pustaka acuan yang memiliki hasil sediaan yang memenuhi persyaratan (Dwiastuti et al., 2016a). Berikut faktor dan level penelitian yang telah ditentukan :
Tabel I. Faktor dan Level dalam Penelitian Faktor
Level Level Rendah
(-1)
Level Tinggi (+1) Konsentrasi soy lecithin 6,5 % w/v 7 % w/v
Durasi Sonikasi 30 menit 40 menit
b. Perancangan desain optimasi konsentrasi fosfolipid dan durasi sonikasi menggunakan aplikasi Minitab17
Merancang faktor konsentrasi fosfolipid dan durasi sonikasi pada Factorial Design menggunakan aplikasi Minitab17. Rancangan optimasi dapat dilihat pada Tabel II dan Tabel III.
Penelitian ini ditujukan untuk menguji pengaruh kedua faktor (konsentrasi fosfolipid dan durasi sonikasi) dengan variasi level sebanyak dua level. Kedua metode perancangan eksperimen tersebut menunjukkan bahwa jumlah eksperimen yang dilakukan sebanyak 12 kali running untuk variabel tergantung ukuran partikel dan 8 kali running untuk variabel tergantung persentase efisiensi penjerapan. Dalam percobaan ini, dilakukan replikasi sebanyak tiga kali (Putri et al., 2017) untuk uji ukuran partikel dengan pembagian menjadi tiga blok dan dua replikasi untuk uji efisiensi penjerapan dan dibuat pembagian menjadi dua blok dimana pembagian tersebut dilakukan di bawah kondisi yang relatif homogen bertujuan untuk meminimalkan bias dan variansi kesalahan karena faktor yang tidak terkendali.
Tabel II. Rancangan Optimasi Faktor untuk Respon Ukuran Partikel StdOrder RunOrder CenterPt Blocks
Konsentrasi Fosfolipid
(% w/v)
Durasi Sonikasi
(menit)
1 1 1 1 6,5 30
2 2 1 1 7 30
3 3 1 1 6,5 40
4 4 1 1 7 40
5 5 1 2 6,5 30
6 6 1 2 7 30
7 7 1 2 6,5 40
8 8 1 2 7 40
9 9 1 3 6,5 30
10 10 1 3 7 30
11 11 1 3 6,5 40
12 12 1 3 7 40
Perancangan penelitian juga dapat dibuat dalam bentuk perhitungan manual, yaitu :
N = n (2k)
12 = 3 (22)
Tabel III. Rancangan Optimasi Faktor untuk Respon Efisiensi Penjerapan StdOrder RunOrder CenterPt Blocks
Konsentrasi Fosfolipid
(% w/v)
Durasi Sonikasi
(menit)
1 1 1 1 6.5 30
2 2 1 1 7 30
3 3 1 1 6.5 40
4 4 1 1 7 40
5 5 1 2 6.5 30
6 6 1 2 7 30
7 7 1 2 6.5 40
8 8 1 2 7 40
Perancangan penelitian juga dapat dibuat dalam bentuk perhitungan manual, yaitu :
N = n (2k)
8 = 2 (22)
Keterangan : N : Total respon n : Jumlah replikasi 2 : Jumlah level k : Jumlah faktor
(Mee, 2009; Riswanto et al., 2019) Pembuatan Sediaan Nanopartikel Lipid
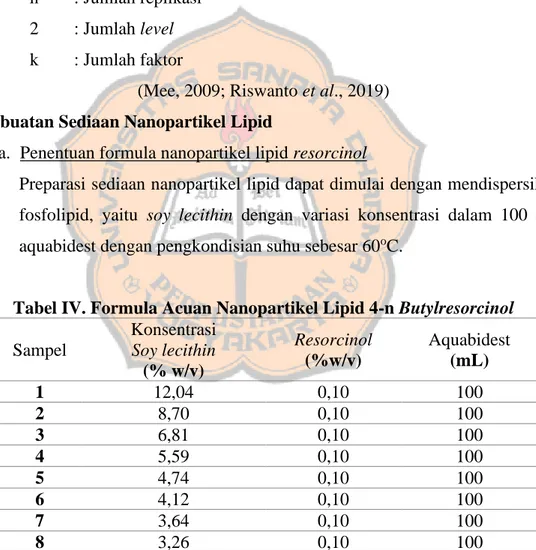
a. Penentuan formula nanopartikel lipid resorcinol
Preparasi sediaan nanopartikel lipid dapat dimulai dengan mendispersikan fosfolipid, yaitu soy lecithin dengan variasi konsentrasi dalam 100 mL aquabidest dengan pengkondisian suhu sebesar 60oC.
Tabel IV. Formula Acuan Nanopartikel Lipid 4-n Butylresorcinol Sampel
Konsentrasi Soy lecithin
(% w/v)
Resorcinol (%w/v)
Aquabidest (mL)
1 12,04 0,10 100
2 8,70 0,10 100
3 6,81 0,10 100
4 5,59 0,10 100
5 4,74 0,10 100
6 4,12 0,10 100
7 3,64 0,10 100
8 3,26 0,10 100
(Dwiastuti et al., 2016a)
Tabel V. Formula Modifikasi Nanopartikel Lipid Resorcinol
Formula Faktor Resorcinol
(%w/v)
Aquabidest (mL)
A B
F1 +1 -1
0,066 (penyesuaian
jumlah mol)
100
F2 -1 +1
F3 -1 -1
F4 +1 +1
Keterangan:
• Faktor A = konsentrasi soy lecithin, dan faktor B = durasi sonikasi
• Nilai level (-1, +1) dapat dilihat pada Tabel I b. Formulasi sediaan nanopartikel lipid resorcinol
Penimbangan bahan dilakukan secara seksama dari soy lecithin dan resorcinol menggunakan neraca analitik. Masing-masing 6,5 gram dan 7 gram soy lecithin didispersikan dalam 100 mL aquabidest di atas hot plate dengan bantuan magnetic stirrer dengan pengkondisian suhu pembuatan 60oC. Setelah mencapai suhu 60oC, campuran tersebut ditambahkan dengan larutan 0,066 %w/v resorcinol dan dihomogenkan menggunakan blender dengan kecepatan high (Christania et al., 2020) selama 60 sekon dan dilakukan kembali pengkondisian suhu 60oC di atas hot plate.
Homogenisasi campuran dilanjutkan menggunakan instrumen ultra-turrax selama 60 sekon dengan skala 4 (Christania et al., 2020). Hasil campuran tersebut dilanjutkan dengan sonikasi menggunakan probe sonicator selama variasi durasi sonikasi (30 menit dan 40 menit) dengan suhu pengkondisian 60oC. Adapun pengaturan probe sonicator pada suhu pembuatan 60oC adalah dengan amplitudo (power) konstan sebesar 40% (Emami et al., 2012) dengan pulse frequency sebesar 60% (Siddiqui et al., 2014).
Pengujian Ukuran Partikel
Pengujian ukuran partikel menggunakan Particle Size Analyzer (PSA) dengan Dynamic Light Scattering (DLS) di Universitas Islam Indonesia, Yogyakarta.
Sebanyak 0,5 µL hasil sintesis nanopartikel lipid dimasukkan ke dalam 25 mL labu ukur, lalu ditambahkan dengan aquabidest hingga tanda batas dan dihomogenkan.
Sebanyak 0,5 mL larutan nanopartikel lipid dituangkan ke dalam kuvet dan ukuran
partikel dapat diukur. Adapun hasil pengujian yang diharapkan adalah ukuran partikel sebesar 50-100 nm (Sułkowski et al., 2005).
Pengukuran Nilai Persen Efisiensi Penjerapan (%EE) a. Pemisahan free drug menggunakan Nanosep
Jumlah resorcinol yang terperangkap dalam sistem nanopartikel lipid dievaluasi dengan metode ultrafiltrasi menggunakan tabung filter Sartorius Vivaspin (Vivaspin, Goettingen, Jerman) dengan membran filter yang memiliki cut-off berat molekul 3 kDa. Dua ratus mikroliter sistem dispersi bermuatan resorcinol yang tidak diencerkan ditempatkan di ruang atas tabung dan disentrifugasi pada 12.000 rpm selama 45 menit (Minispin, Eppendorf, Hamburg, Jerman). Mengencerkan 100 µL filtrat menggunakan ethanol dalam labu ukur 5 mL, dan jumlah resorcinol yang tidak terperangkap diukur menggunakan kromatografi cair kinerja tinggi (HPLC) (Tofani et al., 2016). Bentuk resorcinol yang bebas dari sistem nanopartikel lipid dalam supernatan hasil sentrifugasi menunjukkan jumlah free drug atau yang tidak terjerap (Dwiastuti et al., 2016a). Penentuan supernatan yang merupakan bentuk free drug dari resorcinol berdasarkan pada nilai bobot molekulnya. Bobot molekul resorcinol sebesar 110,11 g/mol (National Center of Biotechnology Information, 2020c), dimana nilai tersebut lebih kecil dari bobot molekul soy lecithin dengan nilai 643,9 g/mol (National Center of Biotechnology Information, 2020d).
b. Penyiapan instrumen HPLC
1) Pembuatan Larutan Standar Resorcinol
Sepuluh miligram resorcinol ditimbang secara seksama, dimasukkan ke dalam 10 mL labu ukur dan dilarutkan dengan ethanol. Kalibrasi larutan standar dari resorcinol dibuat variasi konsentrasi, yaitu 10; 20; 30; 40;
50; 60; dan 70 ppm (Dwiastuti et al., 2018). Pembuatan larutan standar dengan variasi konsentrasi 2,4,6,8,10 ppm juga dilakukan untuk uji sensitivitas sistem HPLC.
2) Pengkondisian HPLC
Standar kalibrasi dari resorcinol dan larutan sampel dianalisis menggunakan Shimadzu LC2010 HPLC dengan UV detector. Kolom HPLC yang digunakan adalah Phenomenex® C18 column (250 x 4.6 mm, 5 μm). Fase gerak yang digunakan yaitu methanol-acetonitrile- redistilled water (Dwiastuti et al, 2021) yang telah dioptimasi dengan perbandingan 10:89:1 v/v. Besar flow rate dari fase gerak sebesar 0,8 mL/menit (Dwiastuti et al., 2018) dengan mode elusi gradien. Semua larutan uji diinjeksi ke dalam sistem HPLC dengan volume injeksi 10 μL dan dideteksi menggunakan UV detector pada lambda 279 nm (Dwiastuti et al., 2018).
3) Uji Kesesuaian Sistem
Kesesuaian sistem HPLC untuk proses analisis ditunjukkan dengan menginjeksikan 6 replikasi larutan standar dengan suatu konsentrasi sebelum dilakukan analisis sampel. Kriteria yang diterima adalah ketika nilai %RSD dari waktu retensi dan nilai luas area senyawa resorcinol muncul pada kromatogram setelah diinjeksikan dimana memiliki nilai tailing factor di bawah 2,0 (Dwiastuti et al., 2018).
4) Uji Estimasi Kuantitatif
Estimasi kuantitatif untuk resorsinol dilakukan dengan menggunakan metode multi-point calibration . Grafik kalibrasi senyawa dibuat dan diterapkan dalam penentuan kuantitatif untuk resorcinol (Dwiastuti et al., 2021).
c. Perhitungan % Efisiensi Penjerapan
Efisiensi penjerapan resorcinol dapat ditentukan dengan perhitungan :
% EE = 𝑗𝑢𝑚𝑙𝑎ℎ 𝑎𝑛𝑎𝑙𝑖𝑡 −𝑗𝑢𝑚𝑙𝑎ℎ 𝑎𝑛𝑎𝑙𝑖𝑡 𝑡𝑖𝑑𝑎𝑘 𝑡𝑒𝑟𝑒𝑛𝑘𝑎𝑝𝑠𝑢𝑙𝑎𝑠𝑖 (𝑓𝑟𝑒𝑒 𝑑𝑟𝑢𝑔)
𝑗𝑢𝑚𝑙𝑎ℎ 𝑎𝑛𝑎𝑙𝑖𝑡 (𝑡𝑜𝑡𝑎𝑙 𝑑𝑟𝑢𝑔) × 100%
Analisis Data Statistik
Metode analisis statistik yang digunakan yaitu uji two-way Analysis of Variance (ANOVA) dengan jenis rancangan Factorial Design menggunakan program
aplikasi Minitab17. Data yang dihasilkan dalam penelitian ini berupa data hasil pengujian ukuran partikel dan persentase efisiensi penjerapan sediaan nanopartikel lipid. Analisis data pada penelitian ini melihat data pergeseran dari tiap faktor variasi konsentrasi soy lecithin dan durasi sonikasi menggunakan Minitab17 sehingga didapatkan interaksi dari kedua faktor pada dua level untuk masing- masing respon melalui suatu persamaan. Rancangan ini dapat digunakan untuk melihat respon dan mengetahui apakah terdapat perbedaan bermakna antar formula mengunakan two-way ANOVA dengan tingkat kepercayaan 95%. Nilai p-value <
0,05 sehingga menunjukkan adanya perbedaan signifikan pada ukuran partikel dan persentase efisiensi penjerapan sediaan nanopartikel lipid resorcinol.
12 HASIL DAN PEMBAHASAN
Formulasi Sediaan Nanopartikel Lipid Resorcinol
Pembuatan nanopartikel lipid resorcinol menggunakan bahan utama fosfolipid soy lecithin sebagai bahan untuk membentuk sistem lipid bilayer agar bahan aktif resorcinol dapat terjerap dalam sistem tersebut. Penelitian ini menggunakan metode sonikasi dan pemanasan dalam pembuatan sediaan nanopartikel lipid dan berdasarkan pada penelitian yang telah dilakukan oleh Putri et al. (2017).
Pembuatan sistem nanopartikel lipid ini menggunakan suhu pemanasan sebesar 60°C dengan durasi sonikasi selama tiga puluh dan empat puluh menit. Peneliti menggunakan suhu tersebut dikarena pemanasan juga berpengaruh pada pembentukan sistem nanopartikel lipid, dimana soy lecithin memiliki suhu transisi pada suhu 50-60oC. Dispersi soy lecithin akan membentuk fase gel pada suhu kurang dari 50°C, sedangkan jika di atas suhu transisi, akan membentuk fase kristal cair. Membran berubah dari fase gel menjadi fase kristal cair. Dalam pembuatan sistem liposom, setiap molekul dapat bergerak lebih bebas kemudian membentuk lapisan lipid menjadi liposom pada fase cair, sehingga tahap ini merupakan titik kritis saat formulasi (Putri et al., 2017). Pada penelitian ini akan dilakukan sintesis sediaan nanopartikel lipid pada suhu 60oC sesuai dengan literatur yang diacu (Dwiastuti et al., 2018, 2016b, 2016a) dan telah dioptimasi melalui penelitian yang dilakukan oleh Putri et al. (2017) dan menghasilkan ukuran partikel ≤100nm.
Selama proses pembuatan sediaan nanopartikel lipid, peneliti mengkondisikan suhu pemanasan agar tetap pada 60°C ± 2°C menggunakan hot plate karena terjadi penurunan suhu pada saat proses pencampuran menggunakan blender dan ultra- turrax serta selama penggunaan probe sonicator. Penelitian ini menggunakan etanol dalam membantu melarutkan bahan aktif resorcinol karena senyawa resorcinol memiliki kelarutan yang baik pada pelarut ini (Haynes, 2017).
Pengujian Ukuran Partikel Sediaan Nanopartikel Lipid
Setelah pembuatan sediaan nanopartikel selesai, dilakukan pengujian untuk mengetahui ukuran partikel menggunakan instrumen PSA dan nilai presentase efisiensi penjerapan menggunakan instrument HPLC. Instrumen Particle Size Ana
13
-lyzer menggunakan prinsip Dynamic Light Scattering (DLS), dimana DLS mengukur ukuran hidrodinamik partikel dengan mekanisme menembakkan cahaya dari laser yang melewati suspensi koloid terdispersi dan menganalisis modulasi intensitas cahaya yang tersebar sebagai fungsi waktu (Lim et al., 2013). Gerak Brown dari partikel berkorelasi dengan diameter hidrodinamiknya. Pengukuran DLS menggunakan sudut hamburan 90 derajat menggunakan laser helium-neon sebagai sumber cahaya, yaitu posisi detektor pada sudut siku-siku 90 derajat terhadap cahaya datang (Griffiths et al., 2015). Gerak Brown dari masing-masing partikel diintrepretasikan menjadi ukuran partikel, yang dihitung dengan perangkat lunak menggunakan persamaan Stokes Einstein (Raval et al., 2018). Adapun data ukuran partikel dipaparkan dalam data Z-Average yang merupakan nilai rata-rata ukuran partikel pada intensitas cahaya yang dapat terukur menggunakan PSA. Nilai target ukuran partikel yang diinginkan adalah sebesar > 40nm yang merupakan ukuran partikel yang dapat bekerja secara lokal (Gautam et al., 2011) hingga diameter 100 nm yang merupakan ukuran nanopartikel lipid yang sering digunakan sebagai pembawa dalam sistem pengiriman obat karena mempunyai kemampuan distribusi yang baik (Sułkowski et al., 2005).
Pengujian sampel menggunakan PSA membantu dalam mengetahui nilai indeks polidispersitas sediaan uji. Nilai indeks polidispersitas (PDI) merupakan parameter yang menggambarkan penyebaran distribusi ukuran partikel dan nilainya dapat bervariasi dari 0 hingga 1, dimana partikel koloid dengan PDI kurang dari 0,1 menunjukkan partikel monodisperse dan nilai lebih dari 0,1 dapat menunjukkan distribusi ukuran partikel polidispersi (Raval et al., 2018). Nilai PDI merupakan nilai kuadrat dari deviasi standar dibagi dengan diameter partikel rata-rata. Nilai PDI antara 0,1 dan 0,25 menunjukkan rentang distribusi kecil dalam ukuran partikel, sedangkan nilai PDI> 0,5 menunjukkan dispersitas partikel yang lebih besar dalam kaitannya dengan ukuran (Cooper et al., 2014). Adapun nilai polidispersitas yang baik adalah <0,3 (Badran, 2014).
Gambar pada Lampiran 1 menunjukkan kurva distribusi ukuran partikel nanopartikel lipid yang memiliki hasil sebaran mendekati distribusi normal atau right-handed inclination. Kurva distribusi normal ditandai dengan bentuk kurva
yang menyerupai lonceng simetris. Kurva distribusi ukuran partikel untuk sebagian besar kelompok partikel adalah asimetris dan cenderung ke arah diameter yang lebih besar dengan diameter kecil yang menempati sebagian besar dari keseluruhan partikel (Xu and Zhou, 2014). Pembuatan nanopartikel lipid resorcinol menghasilkan ukuran partikel dan nilai IP sebesar :
Tabel VI. Hasil Ukuran Partikel dan Nilai PI Sediaan Nanopartikel Lipid Resorcinol
Formula Replikasi
Ukuran Partikel (nm)
Polydispersity Index
1
1 124,4 0,158
2 123,3 0,176
3 125,4 0,106
2
1 114,3 0,198
2 113,6 0,133
3 113,2 0,224
3
1 130,0 0,181
2 128,9 0,226
3 127,2 0,274
4
1 120,8 0,206
2 120,0 0,121
3 119,7 0,272
Dari data Tabel VI menunjukkan bahwa seluruh sampel belum masuk dalam range target ukuran partikel. Ukuran partikel dari masing-masing sampel uji memiliki ukuran melebihi 100 nm, namun masih dalam range target ukuran partikel yang baik bila diaplikasikan yaitu 50-150nm (Ko and Lee, 2010; Liang et al., 2004;
Sułkowski et al., 2005). Ukuran partikel yang dihasilkan belum mencapai 100nm dipengaruhi oleh mekanisme probe sonicator yang digunakan untuk formulasi sediaan uji. Probe sonicator memberikan energi tinggi ke suspensi lipid namun memiliki kecenderungan terjadinya overheating yang dapat mempengaruhi proses penjerapan sediaan uji (Mozafari, 2010). Probe sonicator memberikan daya yang diarahkan ke volume suspensi yang kecil dan memiliki gaya geser yang rendah sehingga tidak memastikan bahwa semua volume suspensi melewati bagian tip sonikator ini (Taylor, 2010), hal ini menyebabkan nanopartikel yang memiliki ukuran partikel yang baik hanya yang mengalami kontak langsung dengan tip
sonikator. Probe sonicator yang digunakan memiliki kecenderungan tidak mengalami kontak langsung dengan seluruh volume sediaan uji, sehingga diperlukan kombinasi dengan pengadukan kecepatan tinggi untuk memperoleh hasil yang optimal (Taylor, 2010). Meskipun memiliki nilai indeks polidispersitas yang sangat kecil, namun pembuatan sistem nanopartikel lipid ini akan memberikan hasil ukuran partikel yang lebih baik menggunakan instrumen bath sonicator, seperti hasil pada penelitian yang dilakukan Dwiastuti et al. (2018) dengan nilai ukuran partikel <100nm dengan nilai polidispersitas <0,3.
Pengujian dilakukan dalam masa penyimpanan kurang dari 30 hari setelah hari pembuatan sediaan, sehingga waktu penyimpanan tidak mempengaruhi besarnya ukuran partikel yang diperoleh. Berdasarkan penelitian yang telah divalidasi oleh Dwiastuti, et al (2018), sediaan dalam masa penyimpanan di bawah 30 hari, menghasilkan sediaan ukuran partikel di bawah 100 nm dengan peningkatan ukuran partikel ± 2nm setiap minggunya.
Berdasarkan data pada Tabel VI, nilai indeks polidispersitas menunjukkan sebaran ukuran partikel masuk dalam nilai distribusi yang baik, yaitu di bawah 0,3 (Badran, 2014). Nilai indeks polidispersitas yang rendah menunjukkan bahwa sistem dispersi tersebut memiliki sifat yang lebih stabil untuk jangka panjang.
Rentang indeks polidispersitas pada kisaran 0-0,5 menunjukkan ukuran partikel telah terdistribusi secara homogen(Gao et al., 2008).
Pengujian Efisiensi Penjerapan
Jumlah free drug dari resorcinol dalam sediaan dan persentase efisiensi penjerapan resorcinol telah ditentukan dalam penelitian ini. Metode HPLC dengan detektor spektrofotometer UV-Vis dengan panjang gelombang 279nm (Dwiastuti et al., 2021) yang telah dioptimasi digunakan untuk menentukan kandungan free drug resorcinol dalam sediaan uji. Adapun fase gerak yang digunakan dalam metode HPLC adalah metanol:acetonitril:redistilled water dengan perbandingan 10:89:1 v/v dan flow rate sebesar 0,8 mL/menit dengan mode elusi gradien. Hasil optimasi tersebut menunjukkan nilai uji kesesuaian sistem dengan nilai %RSD pada 6 kali replikasi injeksi larutan standar 40ppm sebesar kurang dari 2% dan peak yang
dihasilkan pada kromatogram memiliki nilai tailing factor kurang dari 2,0. Hasil pengujian estimasi kuantitatif juga menunjukkan nilai R2 sebesar 0,9995 dengan persamaan kalibrasi :
y = 16630x + 17911 (1)
Uji kesesuaian sistem berfungsi untuk mengkonfirmasi kinerja sistem HPLC terhadap pemisahan analit (Dwiastuti et al., 2021). Pemisahan analit resorcinol menggunakan metode HPLC muncul dengan retensi waktu sekitar 3,4 menit. Nilai persentase efisiensi penjerapan dihitung berdasarkan dari nilai area pada kromatogram yang muncul. Area yang muncul pada kromatogram larutan standar resorcinol yang telah dibuat, digunakan sebagai acuan dalam perhitungan efisiensi penjerapan. Konsentrasi standar yang telah dibuat adalah 44ppm, dan ditemukan luas area sebesar 658052,5 menggunakan metode analisis HPLC dengan pengaturan fase gerak yang telah dioptimasi. Filtrat hasil sentrifugasi sediaan uji menggunakan nanosep sebanyak 100µL akan diencerkan menggunakan ethanol dalam labu ukur 5mL.
Hasil persentase efisiensi penjerapan pada Tabel VII menghasilkan nilai rerata 68,75395434% untuk F1, F2 dengan nilai rerata sebesar 66,68580044%, F3 dengan nilai rerata sebesar 68,032100825%, dan F4 dengan nilai rerata sebesar 75,5801288%. Nilai persentase efisiensi penjerapan tersebut memiliki nilai yang lebih tinggi dari hasil penelitian yang dilakukan oleh Dwiastuti et al. (2018), menggunakan nanopartikel soy lecithin dengan senyawa aktif 4-nBR dengan metode pemanasan dan sonikasi yang menghasilkan nilai persentase efisiensi penjerapan sebesar 48.75 (± 37.28)% setelah penyimpanan sediaan selama 30 hari.
Tabel VII. Data Hasil Pengujian Efisiensi Penjerapan Replikasi Formula
Kandungan Free Drug Resorcinol (µg/mL)
Jumlah Penimbangan
Analit (mg)
Persentase Efisiensi Penjerapan (%)
1
F1 199,6257138 65 69,28835173
F2 220,4204072 65 66,08916813
F3 224,2550556 67 66,52909617
F4 183,2941901 66 72,22815302
2
F1 206,5728798 65 68,21955695
F2 212,6641871 65 67,28243275
F3 194,9753249 64 69,53510548
F4 134,8345307 64 78,93210458
Respon Sifat Fisik Sediaan Berdasarkan Statistik Analysis of Variance (ANOVA)
Respon sifat fisik yang dihasilkan dari kedua faktor yang digunakan yaitu kosentrasi soy lecithin dan durasi sonikasi dilakukan pengujian statistik menggunakan Analysis of Variance (ANOVA) software Minitab17. Uji statistik ANOVA akan menunjukkan nilai signifikansi (p-value) setiap faktor dan interaksinya berpengaruh atau tidak terhadap respon yang dihasilkan. Nilai p-value yang dianggap memberikan pengaruh atau berbeda bermakna apabila nilai p-value
< 0,05 (Afsah-Hejri et al., 2011).
a. Respon ukuran partikel
Pada penelitian ini dilakukan uji statistik ANOVA untuk melihat pengaruh kedua faktor terhadap respon ukuran partikel yang dihasilkan.
Faktor memiliki pengaruh terhadap respon apabila nilai p-value < 0,05. Nilai p-value model dilihat terlebih dahulu untuk melihat apakah model yang digunakan tersebut valid dan dapat digunakan persamaannya dalam menentukan efek kedua faktor terhadap respon ukuran partikel. Berikut persamaan FD untuk respon ukuran partikel:
y= 651,2 – 73,47 (konsentrasi soy lecithin) – 15,54 (durasi sonikasi) + 2,160 (konsentrasi soy lecithin*durasi sonikasi) (2)
Tabel VIII. Respon Ukuran Partikel pada Uji Statistik ANOVA Signifikansi
Model R2
0,000 98,67%
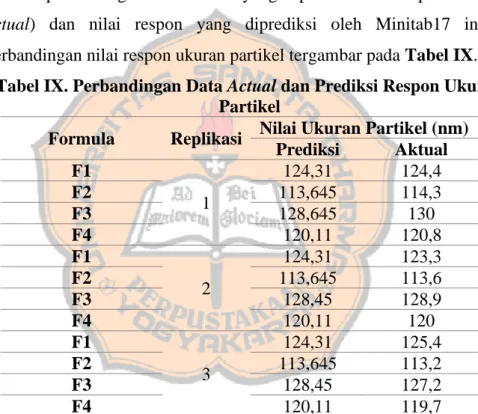
Nilai p-value dari model adalah 0,000 (<0,05) sehingga menunjukkan bahwa model yang digunakan telah valid. Model yang valid tersebut membuat persamaan regresi dari Minitab17 dapat digunakan untuk melihat perbandingan antara nilai yang diperoleh selama percobaan (data actual) dan nilai respon yang diprediksi oleh Minitab17 ini. Data perbandingan nilai respon ukuran partikel tergambar pada Tabel IX.
Tabel IX. Perbandingan Data Actual dan Prediksi Respon Ukuran Partikel
Formula Replikasi Nilai Ukuran Partikel (nm) Prediksi Aktual F1
1
124,31 124,4
F2 113,645 114,3
F3 128,645 130
F4 120,11 120,8
F1
2
124,31 123,3
F2 113,645 113,6
F3 128,45 128,9
F4 120,11 120
F1
3
124,31 125,4
F2 113,645 113,2
F3 128,45 127,2
F4 120,11 119,7
Dilakukan analisis persamaan model yaitu pengujian asumsi residual untuk mengansumsi apakah residual bersifat identik, independen, dan terdistribusi normal atau tidak. Pengujian asumsi normalitas residual berutujuan untuk mendeteksi apakah nilai residual berdistribusi normal atau tidak (Febrianto et al., 2018). Dari hasil yang ditampilkan pada Gambar 1, menunjukkan bahwa titik-titik residual yang diplot jatuh kira-kira hampir sepanjang garis lurus, sehingga residualnya normal atau setidaknya mendekati normal (Mathews, 2005).
Gambar 1. Uji Normalitas Residual untuk Respon Ukuran Partikel Pengujian asumsi residual identik dilakukan untuk memeriksa apakah varian residual dari model yang diperoleh sama penyebarannya (homokedastisitas) atau tidak. Dari plot yang dihasilkan pada Gambar 2, diperoleh bahwa residual tersebar secara acak dan tidak membentuk pola tertentu yang menunjukkan bahwa asumsi residual identik terpenuhi. Residu memiliki jumlah variasi yang hampir sama pada semua tingkat nilai yang dipasang (Matthew, P.G., 2005).
Gambar 2. Grafik Uji Homokedastisitas untuk Respon Ukuran Partikel Uji asumsi indipendensi residual dilakukan untuk mengetahui apakah antara faktor yang digunakan saling berhubungan atau tidak. Pada Gambar 3 terlihat bahwa tidak ada pola yang memungkinkan residual diprediksi dari pola yang mendahuluinya, sehingga error tampak independent (Matthew, P.G., 2005).
Gambar 3. Grafik Uji Independensi Residual untuk Respon Ukuran Partikel
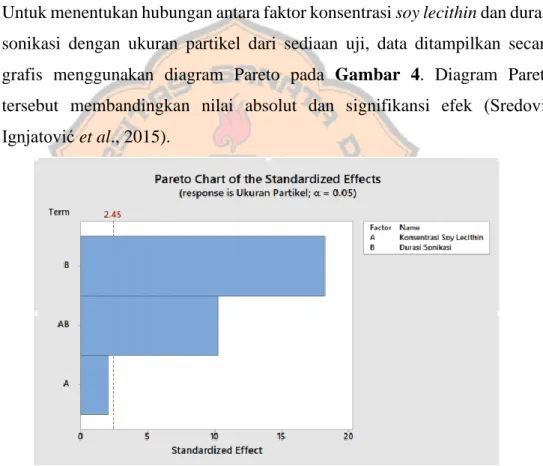
Untuk menentukan hubungan antara faktor konsentrasi soy lecithin dan durasi sonikasi dengan ukuran partikel dari sediaan uji, data ditampilkan secara grafis menggunakan diagram Pareto pada Gambar 4. Diagram Pareto tersebut membandingkan nilai absolut dan signifikansi efek (Sredović Ignjatović et al., 2015).
Gambar 4. Diagram Efek Pareto terhadap Ukuran Partikel
Dari gambar diagram tersebut, terdapat garis vertikal dengan nilai 2.45 yang merupakan baseline interval kepercayaan 95% (Sredović Ignjatović et al., 2015). Faktor yang paling signifikan secara statistik yang mempengaruhi ukuran partikel yang dihasilkan adalah durasi sonikasi dan interaksi durasi sonikasi dengan konsentrasi soy lecithin merupakan faktor lain yang masuk sebagai pengaruh signifikan secara statistik. Besaran relatif dari variabel proses ditentukan berdasarkan efek faktor dan nilai p-value yang
sesuai (Sredović Ignjatović et al., 2015). Durasi sonikasi yang tinggi terbukti dapat mereduksi diameter nanopartikel dengan amplitudo sonikator sebesar lebih dari 55% (Esmaeilzadeh-Gharedaghi et al., 2012). Hasil ini mengonfirmasi bahwa faktor durasi sonikasi memiliki pengaruh terhadap ukuran partikel sediaan uji yang dihasilkan.
Hasil analisis statistik menggunakan metode ANOVA Two-Way menunjukkan nilai R-square model yang diperoleh sudah baik yaitu sebesar 98,67%. Nilai R-square sudah memenuhi persyaratan bahwa variabel bebas berpengaruh kuat terhadap respon hanya jika nilai R2 ≥ 0,8 (Riswanto et al., 2020). Respon yang dihasilkan menunjukkan bahwa nilai p-value untuk konsentrasi soy lecithin sebesar 0,092 yang sesuai dengan data pada diagram Pareto pada Gambar 8, yang menunjukkan bahwa variabel konsentrasi soy lecithin tidak berpengaruh secara signifikan terhadap ukuran partikel yang dihasilkan.
b. Respon efisiensi penjerapan
Pada penelitian ini dilakukan uji statistik ANOVA untuk melihat pengaruh kedua faktor terhadap respon efisiensi penjerapan yang dihasilkan.
Faktor berpengaruh terhadap respon apabila nilai p-value < 0,05. Nilai p- value model dilihat terlebih dahulu untuk melihat apakah model tersebut valid dan dapat digunakan persamaannya dalam menentukan efek kedua faktor terhadap respon efisiensi penjerapan resorcinol. Berikut persamaan FD untuk respon efisiensi penjerapan:
y=381 – 47,6 (konsentrasi soy lecithin) – 10,76 (durasi sonikasi) + 1,634 (konsentrasi soy lecithin*durasi sonikasi) (3)
Tabel X. Respon Efisiensi Penjerapan pada Uji Statistik ANOVA Signifikansi
Model R2
0,110 86,83%
Nilai p-value dari model adalah 0,110 (>0,05) sehingga menunjukkan bahwa model tidak valid. Hal ini juga menunjukkan bahwa kedua faktor atau
rentang level tidak berpengaruh signifikan terhadap respon efisiensi penjerapan. Intepretasi nilai p-value kedua faktor dan interaksinya serta persamaan yang didapatkan tidak dapat ditindaklanjuti karena nilai p-value model sudah menunjukkan tidak berpengaruh signifikan (tidak valid). Hal ini menunjukkan bahwa pada rentang konsentrasi soy lecithin dan durasi sonikasi yang peneliti gunakan tidak berpengaruh terhadap respon efisiensi penjerapan. Jangka waktu penyimpanan sediaan uji yang sangat lama, yaitu lebih dari 30 hari penyimpanan yang membuat sediaan tidak stabil.
Ketidakstabilan sediaan uji didukung oleh faktor tidak adanya stabilizer yang ditambahkan pada sediaan uji. Penambahan stabilizer akan membentuk ikatan sambung silang dengan senyawa pembawa sehingga menjadikan partikel tetap stabil dan menghasilkan penjerapan partikel yang baik (Pawar et al., 2008).
Penentuan Area dan Komposisi Optimum
Model yang didapatkan pada respon ukuran partikel menunjukkan hasil p- value yang signifikan. Nilai p-value yang signifikan ini menyebabkan persamaan yang sudah didapatkan melalui uji statistik ANOVA dapat digunakan untuk memprediksi respon yang dihasilkan ketika diaplikasikan level pada kedua faktor untuk menghasilkan nilai respon yang optimal. Hal tersebut membuat contour plot yang dihasilkan juga dapat digunakan untuk menentukan area optimum dari optimasi faktor konsentrasi soy lecithin dan durasi sonikasi menggunakan metode desain faktorial.
Pengaturan optimasi dengan analisis response optimizer yaitu menggunakan mode target dengan nilai terendah 50nm, nilai target 100nm, dan nilai tertinggi sebesar 150nm. Hasil yang diperoleh dari pengaturan optimasi ini adalah F2 dengan konsentrasi soy lecithin sebesar 6.5% w/v dan durasi sonikasi selama 40 menit. Prediksi hasil pengujian ukuran partikel F2 dari ketiga replikasinya memperoleh nilai Z-Average terendah, yaitu sebesar 113.7nm. Hasil tersebut sesuai dengan hasil penelitian yang dilakukan oleh Esmaeilzadeh- Gharedaghi et al. (2012) yaitu peningkatan durasi sonikasi dalam konsentrasi fosfolipid yang rendah menyebabkan penurunan yang signifikan pada diameter
partikel nano. Hasil prediksi ini sesuai dengan analisis menggunakan contour plot seperti pada Gambar 5.
Dari Gambar 5 menunjukkan bahwa untuk dapat memperoleh ukuran partikel seminimal mungkin, yaitu area berwarna biru tua dengan nilai prediksi ukuran partikel <115nm yaitu dengan mengaplikasikan konsentrasi soy lecithin sebesar 6,5 %w/v dan durasi sonikasi selama 40 menit.
Gambar 5. Contour Plot Respon Ukuran Partikel terhadap Kedua Variabel Model untuk efisiensi penjerapan tidak menunjukkan adanya hasil p-value yang signifikan. Nilai p-value yang tidak signifikan ini menyebabkan persamaan yang sudah didapatkan melalui uji statistik ANOVA tidak dapat digunakan. Hal tersebut membuat contour plot yang dihasilkan juga tidak dapat digunakan untuk menentukan area optimum dari optimasi faktor konsentrasi soy lecithin dan durasi sonikasi menggunakan metode desain faktorial.
Pada analisis Minitab17, titik optimum pada model efisiensi penjerapan ditemukan. Titik optimum ditentukan melalui analisis response optimizer dengan menetapkan mode yang disesuaikan. Mode yang digunakan untuk respon efisiensi penjerapan adalah mode minimum dengan pengaturan nilai target sebesar 50% dan nilai tertinggi sebesar 100%. Mode minimum ini digunakan karena nilai efisiensi penjerapan yang diharapkan adalah lebih dari 50%. Titik optimum tersebut berada pada formula F2 dengan konsentrasi soy lecithin sebesar 6,5% w/v dan durasi sonikasi selama 40 menit. Pada formula F2 didapatkan respon nilai efisiensi penjerapan sebesar 66.6858%.
24 KESIMPULAN DAN SARAN
Kesimpulan
1. Konsentrasi soy lecithin dan durasi sonikasi yang dapat menghasilkan respon ukuran partikel yang optimal ditemukan pada formula 2 dengan konsentrasi soy lecithin sebesar 6,5%w/v dan durasi sonikasi selama 40 menit meskipun belum memasuki rentang nilai ukuran partikel yang diharapkan. Tidak ditemukan formula optimal untuk respon efisiensi penjerapan karena faktor waktu penyimpanan sediaan uji yang tidak terkontrol.
2. Ditemukan area optimum pada contour plot untuk respon ukuran partikel yaitu pada area berwarna biru tua yang menunjuk pada konsentrasi soy lecithin sebesar 6,5% w/v dan durasi sonikasi selama 40 menit. Tidak dapat ditentukan area optimum pada analisis contour plot untuk respon efisiensi penjerapan. Formula 2 dengan level konsentrasi fosfolipid soy lecithin sebesar 6,5% w/v dan durasi sonikasi selama 40 menit menghasilkan suatu sistem nanopartikel lipid yang terprediksi optimal pada analisis response optimizer.
3. Diperoleh nilai efisiensi penjerapan dengan nilai rerata 68,75395434% untuk F1, F2 dengan nilai rerata sebesar 66,68580044%, F3 dengan nilai rerata sebesar 68,032100825%, dan F4 dengan nilai rerata sebesar 75,5801288%.
Saran
1. Waktu pengujian sediaan nanopartikel lipid resorcinol sebaiknya dikendalikan dalam jangka waktu yang konsisten dihitung sejak formulasi selesai dilakukan.
2. Dapat dilakukan penambahan stabilizer pada proses formulasi untuk menjaga stabilitas sediaan dan dapat memperoleh nilai efisiensi penjerapan yang baik.
3. Perlu dilakukan validasi metode analisis pada hasil formulasi dengan konsentrasi soy lecithin 6,5% w/v dan durasi sonikasi 40 menit.
25
DAFTAR PUSTAKA
Afsah-Hejri, L., Jinap, S., Arzandeh, S., Mirhosseini, H., 2011. Optimization of HPLC Conditions for Quantitative Analysis of Aflatoxins in Contaminated Peanut. Food Control, 22(3–4), 381–388.
Attama, A.A., Momoh, M.A., Builders, P.F., 2012. Lipid Nanoparticulate Drug Delivery Systems: A Revolution in Dosage Form Design and Development in Recent Advance in Novel Drug Carrrier Systems, in:
Intech. p. 38.
Badran, M., 2014. Formulation and In Vitro Evaluation of Flufenamic Acid Loaded Deformable Liposomes for Improved Skin Delivery. Digest Journal of Nanomaterials and Biostructures, 9(1), 83–91.
CAMEO-Chemical, 2020. Resorcinol.
https://cameochemicals.noaa.gov/chemical/4409, diakses tanggal 15 Desember 2020.
Candioti, L.V., Zan, M.M. De, Cámara, M.S., Goicoechea, H.C., 2014.
Experimental Design and Multiple Response Optimization using The Desirability Function in Analytical Methods Development. Talanta, 124, 123–138.
Christania, F.S., Dwiastuti, R., Yuliani, S.H., 2020. Lipid and Silver Nanoparticles Gels Formulation of Tempeh Extract. Journal of Pharmaceutical Sciences and Community, 16(2), 56–62.
Cooper, D.L., Conder, C.M., Harirforoosh, S., 2014. Nanoparticles in Drug Delivery: Mechanism of Action, Formulation and Clinical Application towards Reduction in Drug-associated Nephrotoxicity. Expert Opinion on Drug Delivery, 11(10), 1661–1680.
Dwiastuti, R., Christin, D., Putri, A., Hariono, M., Octa, F.D., 2021. Multiple Response Optimization of an HPLC Method for Analyzing Resorcinol and 4- n -Butyl Resorcinol in Lipid Nanoparticles 21(2), 502–511.
Dwiastuti, R., Marchaban, Istyastono, E.P., Riswanto, F.D.O., 2018. Analytical Method Validation and Determination of Free Drug Content of 4-n- butylresorcinol in Complex Lipid Nanoparticles using RP-HPLC Method.
Indonesian Journal of Chemistry, 18(3), 496–502.
Dwiastuti, R., Noegrohati, S., Istyastono, E.P., Marchaban, 2016a. Formulation and Physical Properties Observations of Soy Lecithin Liposome Containing 4- n-butylresorcinol. AIP Conference Proceedings, 1755.
Dwiastuti, R., Noegrohati, S., Istyastono, E.P., Marchaban, 2016b. Metode Pemanasan dan Sonikasi Menghasilkan Nanoliposom dari Fosfolipid Lesitin Kedelai (Soy Lecithin). Jurnal Farmasi Sains dan Komunitas, 13(1), 23–27.
Emami, J., Rezazadeh, M., Varshosaz, J., Tabbakhian, M., Aslani, A., 2012.
Formulation of LDL Targeted Nanostructured Lipid Carriers Loaded with Paclitaxel: A Detailed Study of Preparation, Freeze Drying Condition, and In Vitro Cytotoxicity. Journal of Nanomaterials, 2012, 1–10.
Esmaeilzadeh-Gharedaghi, E., Faramarzi, M.A., Amini, M.A., Rouholamini
Najafabadi, A., Rezayat, S.M., Amani, A., 2012. Effects of Processing Parameters on Particle Size of Ultrasound Prepared Chitosan Nanoparticles: An Artificial Neural Networks Study. Pharmaceutical Development and Technology, 17(5), 638–647.
Febrianto, L.S., Dwidayati, N.K., Hendikawati, P., 2018. Perbandingan Metode Robust Least Median of Square (LMS) Dan Penduga S untuk Menangani Outlier pada Regresi Linier Berganda. Unnes Journal of Mathematics, 7(1), 83–95.
Gao, L., Zhang, D., Chen, M., 2008. Drug Nanocrystals for the Formulation of Poorly Soluble Drugs and Its Application as a Potential Drug Delivery System. Journal of Nanoparticle Research, 10(5), 845–862.
Gautam, A., Singh, D., Vijayaraghavan, R., 2011. Dermal Exposure of Nanoparticles: An Understanding. Journal of Cell and Tissue Research, 11(1), 2703–2708.
Griffiths, P.C., Cattoz, B., Ibrahim, M.S., Anuonye, J.C., 2015. Probing the Interaction of Nanoparticles with Mucin for Drug Delivery Applications Using Dynamic Light Scattering. European Journal of Pharmaceutics and Biopharmaceutics, 97(May), 218–222.
Haynes, W.M., 2017. CRC Handbook of Chemistry and Physics, 97th Editi. ed.
CRC Press LLC, Boca Raton.
Hibbert, D.B., 2012. Experimental Design in Chromatography: A Tutorial Review.
Journal of Chromatography B: Analytical Technologies in the Biomedical and Life Sciences, 910, 2–13.
Hazardous Substances Data Bank, 2020a. Resorcinol. Pubchem.
https://pubchem.ncbi.nlm.nih.gov/source/hsdb/722, diakses tanggal 15 Desember 2020.
Hazardous Substances Data Bank, 2020b. Resorcinol. Pubchem.
https://pubchem.ncbi.nlm.nih.gov/compound/Resorcinol#section=LogP, diakses tanggal 15 Desember 2020.
Jacobi, A., Mayer, A., Augustin, M., 2015. Keratolytics and Emollients and Their Role in the Therapy of Psoriasis: a Systematic Review. Dermatology and Therapy, 5(1), 1–18.
Kang, K.C., Lee, C. Il, Pyo, H.B., Jeong, N.H., 2005. Preparation and Characterization of Nano-Liposomes using Phosphatidylcholine. Journal of Industrial and Engineering Chemistry, 11(6), 847–851.
Ko, S., Lee, S.C., 2010. Effect of Nanoliposomes on The Stabilization of Incorporated Retinol. African Journal of Biotechnology, 9(37), 6158–
6161.
Koshiyama, K., Wada, S., 2016. Collapse of a Lipid-Coated Nanobubble and Subsequent Liposome Formation. Scientific Reports, 6(June), 1–8.
Liang, X., Mao, G., Ng, K.Y.S., 2004. Mechanical Properties and Stability Measurement of Cholesterol-Containing Liposome on Mica by Atomic Force Microscopy. Journal of Colloid and Interface Science, 278(1), 53–
62.
Lim, J., Yeap, S.P., Che, H.X., Low, S.C., 2013. Characterization of Magnetic Nanoparticle by Dynamic Light Scattering. Nanoscale Research Letters,
8(1), 1–14.
Machado, A.R., Assis, L.M. de, Machado, M.I.R., Souza-Soares, L.A. de, 2014.
Importance of Lecithin for Encapsulation Processes. African Journal of Food Science, 8(4), 176–183.
Martien, R., Adhyatmika, Irianto, I.D.K., Farida, V., Sari, D.P., 2012.
Perkembangan Teknologi Nanopartikel Sebagai Sistem Penghantaran Obat. Majalah Farmaseutik, 8(1), 133–144.
Mathews, P.G., 2005. Design of Experiments with MINITAB, The American Statistician.
Medscape, 2020. Resorcinol. https://reference.medscape.com/drug/compound-w- for-kids-salicylic-acid-topical-999359#10, diakses tanggal 15 Desember 2020.
Mee, R.W., 2009. Analysis of Full Factorial Experiments, in: A Comprehensive Guide to Factorial Two-Level Experimentation. Springer, p. 29.
Mozafari, M.R., 2010. Nanoliposomes : Preparation and Analysis, in: Methods in Molecular Biology. Humana Press, pp. 35–36.
National Center of Biotechnology Information, 2020a. Resorcinol. Pubchem.
https://pubchem.ncbi.nlm.nih.gov/compound/Resorcinol#section=Structu res, diakses tanggal 15 Desember 2020.
National Center of Biotechnology Information, 2020b. Resorcinol. Pubchem.
https://pubchem.ncbi.nlm.nih.gov/compound/Resorcinol#section=Solubil ity, diakses tanggal 15 Desember 2020.
National Center of Biotechnology Information, 2020c. Resorcinol. Pubchem.
https://pubchem.ncbi.nlm.nih.gov/compound/Resorcinol#section=Chemi cal-and-Physical-Properties, diakses tanggal 15 Desember 2020.
National Center of Biotechnology Information, 2020d. Lecithin from Soybean.
Pubchem. https://pubchem.ncbi.nlm.nih.gov/compound/Lecithin-from- Soybean#section=Computed-Properties, diakses tanggal 15 Desember 2020.
Puri, A., Loomis, K., Smith, B., Lee, J.H., Yavlovich, A., Heldman, E., Blumenthal, R., 2009. Lipid-based nanoparticles as pharmaceutical drug carriers: From concepts to clinic. Critical Reviews in Therapeutic Drug Carrier Systems, 26(6), 523–580.
Putri, D.C.A., Dwiastuti, R., Marchaban, Nugroho, A.K., 2017. Optimization of Mixing Temperature and Sonication Duration in Liposome Preparation.
Jurnal Farmasi Sains Dan Komunitas, 14(2), 79–85.
Rajabi, M., Mousa, S., 2016. Lipid Nanoparticles and Their Application in Nanomedicine. Current Pharmaceutical Biotechnology, 17(8), 662–672.
Raval, N., Maheshwari, R., Kalyane, D., Youngren-Ortiz, S.R., Chougule, M.B., Tekade, R.K., 2018. Importance of Physicochemical Characterization of Nanoparticles in Pharmaceutical Product Development, Basic Fundamentals of Drug Delivery. Elsevier Inc.
Risselada, H.J., Marrink, S.J., 2009. Curvature Effects on Lipid Packing and Dynamics in Liposomes Revealed by Coarse Grained Molecular Dynamics Simulations. Physical Chemistry Chemical Physics, 11, 2056–
2067.
Riswanto, F.D.O., Desra, A., Sari, R.M., Thomas, V., Rohman, A., Pramono, S., Martono, S., 2020. Employing an R Software Package RSM for Optimizing of Genistein, Daidzein, and Glycitein Separation and Its Application for Soy Milk Analysis by HPLC Method. Indonesian Journal of Chemistry, 20(5), 1184–1198.
Riswanto, F.D.O., Rohman, A., Pramono, S., Martono, S., 2019. Application of Response Surface Methodology as Mathematical and Statistical Tools in Natural Product Research. Journal of Applied Pharmaceutical Science, 9(10), 125–133.
Shah, R., Eldridge, D., Palombo, E., Harding, I., 2015. Lipid Nanoparticles:
Production, Characterization and Stability. Springer, New York.
Siddiqui, A., Alayoubi, A., El-Malah, Y., Nazzal, S., 2014. Modeling The Effect of Sonication Parameters on Size and Dispersion Temperature of Solid Lipid Nanoparticles (SLNs) by Response Surface Methodology (RSM).
Pharmaceutical Development and Technology, 19(3), 342–346.
Sredović Ignjatović, I.D., Onjia, A.E., Ignjatović, L.M., Todorović, Ž.N., Rajaković, L. V., 2015. Experimental Design Optimization of the Determination of Total Halogens in Coal by Combustion–Ion Chromatography. Analytical Letters, 48(16), 2597–2612.
Sułkowski, W.W., Pentak, D., Nowak, K., Sułkowska, A., 2005. The Influence of Temperature, Cholesterol Content and pH on Liposome Stability. Journal of Molecular Structure, 744–747, 737–747.
Taylor, A.C., 2010. Advances in Nanoparticle Reinforcement in Structural Adhesives, in: Advances in Structural Adhesive Bonding. Woodhead Publishing Limited, pp. 151–182.
Tofani, R.P., Sumirtapura, Y.C., Darijanto, S.T., 2016. Formulation, Characterisation, and In Vitro Skin Diffusion of Nanostructured Lipid Carriers for Deoxyarbutin Compared to a Nanoemulsion and Conventional Cream. Scientia Pharmaceutica, 84(4), 634–645.
Vitorino, C.S.P., 2013. Lipid Nanoparticles and Permeation Enhancement for Transdermal Drug Delivery. Universidade de Coimbra, Portugal.
Welsch, F., 2008. Routes and Modes of Administration of Resorcinol and Their Relationship to Potential Manifestations of Thyroid Gland Toxicity in Animals and Man. International Journal of Toxicology, 27(1), 59–63.
World Health Organization, 2006. Resorcinol, Concise International Chemical Assessment Document 71. WHO Press, Switzerland.
Xu, Z., Zhou, B., 2014. Fundamentals of Air Cleaning Technology and Its Application in Cleanrooms Chapter 1: Particle and Size Distribution, in:
Springer-Verlag Berlin Heidelberg. pp. 12–26.
1.
29 LAMPIRAN
Lampiran 1. Pengujian Ukuran Partikel Setelah Pembuatan Replikasi 1
Formula 1
Formula 2
Formula 3
Formula 4
Setelah Pembuatan Replikasi 2 Formula 1
Formula 2
Formula 3
Formula 4
Setelah Pembuatan Replikasi 3 Formula 1
Formula 2
Formula 3
Formula 4
Lampiran 2. Dokumentasi Hasil Formulasi Sediaan Nanopartikel Resorcinol
Formula Gambar Sediaan
F1
F2
F3
F4
Lampiran 3. Pengujian Efisiensi Penjerapan
Kromatogram Larutan Standar
Data Replikasi I Formula 1
Formula 2
Formula 3
Formula 4
Data Replikasi II Formula 1
Formula 2
Formula 3