i
SINTESIS DAN KARAKTERISASI
MEMBRAN POLISTIRENA TERFLUORINASI
UNTUK DIRECT METHANOL FUEL CELL
ADE NURBANI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2012
ABSTRAK
ADE NURBANI. Sintesis dan Karakterisasi Membran Polistirena Terfluorinasi
untuk Direct Methanol Fuel Cell. Dibimbing oleh SRI MULIJANI dan
MUHAMMAD KHOTIB.
Salah satu jenis sumber energi terbarukan adalah direct methanol fuel cell
(DMFC) yang menggunakan metanol sebagai bahan bakar. Komponen utama
dalam DMFC adalah membran penukar proton. Penelitian ini menggunakan
polistirena terfluorinasi (PSf) sebagai membran penukar proton melalui proses
fluorinasi. Membran PSf dibuat dengan konsentrasi PSf 5%, 10%, dan 15%.
Fluorinasi menyebabkan perubahan sifat fisik membran dengan munculnya pori
pada membran. Water uptake terbaik dimiliki oleh PSf 5%, yaitu 11.07 %.
Aktivasi membran menyebabkan konduktivitas proton yang dihasilkan meningkat
dari 0.52 × 10
-7S/cm menjadi 0.54 × 10
-7S/cm untuk polistirena (PS) dan 0.44 ×
10
-7S/cm menjadi 0.69× 10
-7S/cm untuk PSf. Uji kualitatif permeabilitas
metanol menunjukkan hasil yang baik dengan keringnya permukaan bawah
membran karena metanol tidak melewati membran. Dalam sistem DMFC
konduktivitas proton membran PSf lebih tinggi dibandingkan membran PS,
sedangkan ragam konduktivitas pada membran PSf disebabkan oleh adanya jarak
pada membran PSf.
ABSTRACT
ADE NURBANI. Synthesize and Characterization Fluorinated Polystyrene
Membrane for Direct Methanol Fuel Cell. Supervised by SRI MULIJANI and
MUHAMMAD KHOTIB.
One of common energy resources is direct methanol fuel cell (DMFC), which
use methanol as fuel. The important component in DMFC is proton exchange
membrane. The study used fluorinated polystyrene membrane (PSf) as proton
exchange membrane through fluorination process. PSf membrane was made with
PSf concentration of 5%, 10%, and 15 %. Fluorination has caused change of
membrane physical properties with presence of pores in the membranes. The best
water uptake was shown by PSf 5% that is 11.07%. Membrane activation
increased the proton conductivity from 0.52 × 10
-7S/cm to 0.54 × 10
-7S/cm for
polysryrene (PS) and 0.44 × 10
-7S/cm to 0.69× 10
-7S/cm for the PSf. Qualitative
test of methanol permeability showed good result with dry underneath the surface
of membrane because methanol did not pass through the membrane. In DMFC
system, proton conductivity of the PSf membrane is higher than that of PS
membrane, while variation of conductivity from PSf membranes is caused by gaps
at the PSf membranes.
SINTESIS DAN KARAKTERISASI
MEMBRAN POLISTIRENA TERFLORINASI
UNTUK DIRECT METHANOL FUEL CELL
ADE NURBANI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2012
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada Departemen Kimia
Judul : Sintesis dan Karakterisasi Membran Polistirena Terfluorinasi untuk
nnnnnnn
Direct Methanol Fuel Cell
Nama : Ade Nurbani
NIM : G44080067
Disetujui
Pembimbing I
Dr Sri Mulijani, MS
NIP 19630401 199103 2 001
Pembimbing II
Muhammad Khotib, S.Si, M.Si
NIP 19781018 200701 1 002
Diketahui
Ketua Departemen Kimia
Prof Dr Tun Tedja Irawadi, MS
NIP 19501227 197603 2 002
PRAKATA
Puji syukur penulis panjatkan kepada Allah SWT atas segala karunia-Nya
sehingga karya ilmiah ini berhasil diselesaikan. Tema penelitian yang dilakukan
sejak bulan Februari 2012 adalah sel bahan bakar, dengan judul Sintesis dan
Karakterisasi Membran Polistirena Terfluorinasi untuk Direct Methanol
Fuel Cell.
Terimakasih penulis ucapkan kepada Dr Sri Mulijani, MS dan Muhammad
Khotib S.Si, M.Si selaku pembimbing yang telah memberikan saran, kritik,
dorongan, ilmu, serta bimbingannya selama penelitian dan penulisan karya ilmiah.
Di samping itu, penghargaan penulis sampaikan kepada Bapak Jajang, Bapak
Hery dan Bapak Akhir dari Departemen Fisika IPB yang telah membantu selama
pengumpulan data. Penulis juga mengucapkan terimakasih kepada staf
Laboraorium Kimia, yaitu Pak Ismail, Pak Sawal, Pak Caca, Ibu Ai, Mas Eko, dan
Pak Wawan atas segala fasilitas dan kemudahan yang telah diberikan.
Ungkapan terimakasih tak terhingga kepada orang-orang tersayang Emih,
Bapak, Teteh Ifa, Aa Tito, dan Imam atas nasihat, semangat, dan doa-doa yang
telah diberikan. Penulis juga mengucapkan terimakasih kepada Mimi, Fiqoh, Kak
Tyas, Dwi, Fadli, Dumas, DJ, Ryna, Dinov, Nui, Tice, Sahabat Kimia Fisik,
Pochan & Zulfa atas doa, kebersamaan, diskusi, dan semangat yang berguna
dalam penyelesaian karya ilmiah ini. Semoga tulisan ini bermanfaat dan dapat
menambah ilmu pengetahuan bagi penulis dan pembaca umumnya.
Bogor, Juli 2012
RIWAYAT HIDUP
Penulis dilahirkan di Subang pada tanggal 14 April 1990 sebagai anak
ketiga dari pasangan Warno Sumarno dan Omih Rodiana. Tahun 2008 penulis
lulus dari SMU PGRI 1 Bekasi dan pada tahun yang sama masuk ke Departemen
Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian
Bogor melalui jalur Undangan Seleksi Masuk IPB. Penulis diterima di Program
Studi S1 Kimia, departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan
Alam, Institut Pertanian Bogor.
Kegiatan akademik yang dijalani Penulis selain perkuliahan adalah menjadi
asisten Praktikum Kimia Fisik untuk mahasiswa departemen Kimia dan Ilmu
Teknologi Pangan. Selama masa perkuliahan Penulis juga aktif di kegiatan
non-akademik, seperti menjadi staf Pengembangan Sumber Daya Mahasiswa pada
tahun 2009 dan bendahara umum pada tahun 2010 di Ikatan Mahasiswa Kimia
IPB (Imasika). Penulis juga melaksanakan praktik lapang di PT Pupuk Kujang
Cikampek pada tahun 2011. Selain itu, penulis aktif di kegiantan intrakampus,
seperti turut serta di Ikatan Himpunan Mahasiswa Kimia Indonesia (Ikahimki)
sebagai Staf Kaderisasi pada tahun 2010-2012.
DAFTAR
ISI
Halaman
DAFTAR GAMBAR ... viii
DAFTAR LAMPIRAN ... viii
PENDAHULUAN ... 1
BAHAN DAN METODE ... 1
Bahan dan alat ... 1
Tahapan penelitian ... 1
HASIL DAN PEMBAHASAN ... 2
Sintesis membran polistirena terfluorinasi ... 2
Analisis gugus fungsi dan morfologi membran ... 3
Water uptake dan permeabilitas metanol ... 4
Konduktivitas proton membran dan sistem DMFC ... 4
SIMPULAN ... 6
SARAN ... 6
DAFTAR PUSTAKA ... 6
DAFTAR GAMBAR
Halaman
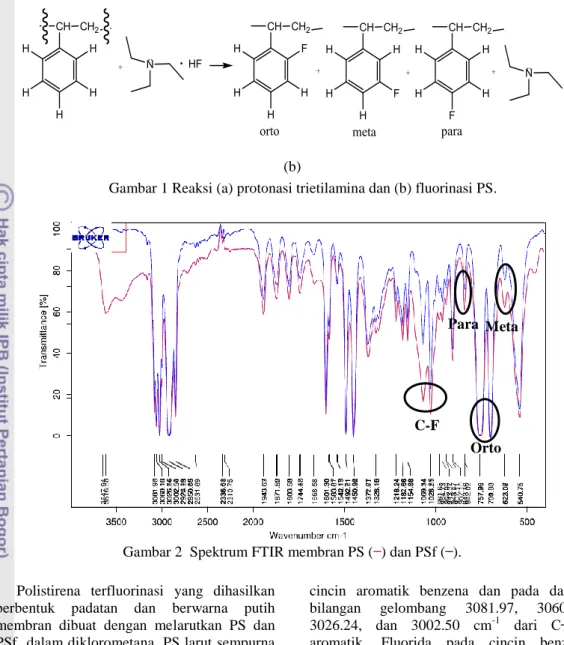
1 Reaksi (a) Protonasi trietilamina (b) Fluorinasi PS……….3
2 Spektrum FTIR membran PS (
) dan PSf (
) ... 3
3 Struktur permukaan atas perbessaran 5000x (a1) PS; (a2) PSf dan penampang
lintang membran perbesaran 1000x (b1) PS; (b2)PSf ... 4
4 Hubungan water uptake dengan konsentrasi membran ... 4
5 Hubungan konduktivitas membran PSf aktivasi dan nonaktivasi ... 4
6 Reaksi redoks sistem DMFC ... 5
7 Hubungan konduktivitas proton pada suhu kamar dan 60 °C ... 5
8 Hubungan antara konsentrasi, konduktivitas proton dan arus ... 5
DAFTAR LAMPIRAN
Halaman
1 Diagram alir penelitian ... 9
2 Data untuk bobot molekul polimer ... 10
3 Data water uptake ... 13
4 Konduktivitas proton membran ... 14
1
PENDAHULUAN
Penelitian sumber energi alternatif terus dilakukan, salah satunya adalah pengembangan sel bahan bakar (Hasan 2007). Sel bahan bakar berpotensi menggeser pilihan energi konvensional. Sel bahan bakar dinilai memiliki keuntungan, antara lain ramah lingkungan dengan tidak dihasilkannya polutan (Holland et al. 2007) dan tidak menimbulkan kebisingan (Hasan 2007), berbeda dengan bahan bakar fosil yang dinilai memiliki beberapa kerugian, seperti menghasilkan polutan berupa gas CO2, gas CO (Bae 2005), dan berasal dari sumber bahan bakar yang tidak dapat diperbarui.
Sel bahan bakar merupakan sistem elektrokimia yang mengubah energi kimia menjadi energi listrik. Salah satu jenis sel bahan bakar ini adalah direct metanol feul cell (DMFC). Komponen penyusun DMFC terdiri dari elektroda pada sisi katoda juga anoda dan membran penukar proton sebagai komponen utama dari DMFC. Membran penukar proton berfungsi sebagai sarana tranportasi proton dari anoda menuju katoda (Yohan et al. 2005).
Membran yang sering digunakan sebagai membran polimer elektrolit adalah Nafion® (Parra 2004), politetrafluoroetilena, dan polietereterketon (Wootthikanokkhan & Seeponkai 2006). Saat ini membran yang sering digunakan adalah Nafion® karena memiliki gugus sulfonat yang mampu menghantarkan proton dan ketahanan mekanik termal yang baik (Hendrana 2007). Namun membran Nafion® juga memiliki kekurangan, yaitu mahal dan memiliki permeabilitas metanol yang tinggi (Liu et al. 2010). Permeabilitas metanol yang tinggi dapat menyebabkan Nafion® tidak maksimal digunakan dalam DMFC. Selain itu menurut Neburchilov et al. (2007) Nafion® baik digunakan pada suhu kurang dari 80 °C. Oleh karena itu, saat ini banyak dikembangkan material baru yang diharapkan dapat menggantikan fungsi Nafion® dalam sel bahan bakar agar lebih baik dari segi kualitas dan harga.
Penelitian ini mengembangkan jenis membran elektrolit polimer baru berasal dari polistirena (PS). PS banyak terkandung dalam sterofoam yang sering digunakan untuk bungkus makanan dan alat penyangga elektronik. Sehingga sterofoam menjadi limbah di lingkungan karena sulit terdegradasi oleh alam (BPOM 2008). Oleh karena itu, menjadi daya tarik tersendiri untuk
mengembangkan membran polistirena sebagai membran penukar proton.
Pengubahan sifat-sifat ini dapat dilakukan dengan metode fluorinasi. Fluorinasi membran polistirena dilakukakan untuk menciptakan muatan negatif pada membran dengan masuknya gugus fluorida. Membran polistirena terfluorinasi (PSf) diharapkan bersifat ionik yang mampu menghantarkan listrik. Potensi inilah yang dikembangkan untuk melihat manfaat membran polistirena terfluorinasi sebagai DMFC yang menggunakan metanol sebagai bahan bakar.
BAHAN DAN METODE
Bahan dan AlatBahan yang digunakan meliputi limbah sterofoam, diklorometana, HF teknis, trietilamin. Alat yang digunakan meliputi SEM JEOL JSM 836 OLA, FTIR BRUCKER TENSOR 27, dan impedance analyzer.
Tahapan Penelitian
Diagram alir penelitian dapat dilihat pada Lampiran 1.
Pembuatan Trietilamina.xHF
Trietilamina.xHF dibuat dengan merekasikan trietilamina dengan HF langsung. Trietilamina sebanyak 10 mL ditambahkan HF teknis sebanyak 15 mL bertahap, kemudian diaduk hingga gas HF hilang.
Sintesis Polistirena terfluorinasi
Polistirena sebanyak 3 g dilarutkan dalam 60 mL kloroform. Larutan polistirena ditambahkan 24 g Et3N.xHF kemudian diaduk. Selanjutnya larutan PSf dipanaskan dalam radas refluks pada suhu 100 °C selama 4 jam, didinginkan pada suhu kamar. Setelah dingin larutan PSf dicuci menggunakan air bebas ion hingga pH 5 menggunakan corong pisah. Lapisan air dibuang, lalu lapisan bawah diuapkan menggunakan rotavapor. Selanjutnya larutan PSf dikering udarakan.
Pembuatan Membran PSf
Pembuatan membran PSf dilakukan menggunakan teknik inversi fasa. PSf dilarutkan dalam diklorometana hingga diperoleh konsentrasi PSf 5%, 10%, dan 15%. Kemudian larutan PSf dituangkan diatas pelat kaca yang telah diberi selotip pada keempat sisinya dengan ketebalan yang sama, lalu dicetak dengan cara mendorong larutan polimer tersebut sampai diperoleh lapisan tipis
2
(Baker 2006), selanjutnya pelepasan membran dilakukan dengan merendam plat kaca dalam air bebas ion.
Penentuan Bobot Molekul Polimer
PSf 0.1 0.3 g dilarutkan masing-masing dalam 10 mL kloroform, kemudian dimasukan dalam labu ukur 25 mL dan tera. Larutan PSf sebanyak 20 mL dimasukan kedalam viskometer Ostwald. Waktu alir dari masing-masing larutan PSf diukur sebanyak tiga kali ulangan. Blanko yang digunakan adalah kloroform tanpa PSf. Bobot molekul ditentukan menggunakan perhitungan sesuai dalam Lampiran 2.
Analisis Morfologi Memrban dan Gugus Fungsi
Permukaan membran dicirikan menggunakan SEM. Perbesaran yang dikenai pada membran adalah 1000× untuk melihat permukaan atas membran dan 5000× untuk melihat penampang lintang membran.
Analisis gugus fungsi yang terdapat dalam membran menggunakan spektrofotometer inframerah transformasi fourier (FTIR). Sehingga, diperoleh spektrum inframerah dari membran polistirena dan polistirena terfluorinasi.
Water Uptake
Membran polistirena dan polistirena terfluorinasi digunting sebesar 1 × 1 cm dari sisi yang berbeda, kemudian dipanaskan pada suhu 120 °C menggunakan oven selama 24 jam (Shin et al. 2005). Bobot kering diperoleh dari bobot membran setelah dipanaskan dalam oven. Membran kering masing-masing direndam dalam air deionisasi pada suhu kamar selama 48 jam (Liu et al. 2010). Bobot basah diperoleh dari bobot membran setelah perendaman. Penentuan kadar air dalam membran dihitung menggunakan rumus dibawah ini.
( ) [( )
]
Keterangan:
W : Water uptake (%)
Wwet : Bobot basah membran (gram) Wdry : Bobot kering membran (gram)
Permeabilitas Metanol
Permeabilitas metanol diuji secara kualitatif untuk melihat metanol yang lewat melalui membran. Kompartemen A diisi dengan metanol kemudian posisi sistem dibalik agar metanol berada diatas membran selama 30 menit, kemudian bagian bawah
membran dilap dengan tisu untuk melihat metanol yang terdifusi melalui membran.
Konduktivitas Proton
Elektrode karbon dari baterai dibersihkan dan dibuat pipih pada salah satu sisinya. Aktivasi elektrode dilakukan dengan merendam elektrode kedalam HCl 1N selama 1 hari, kemudian dilanjutkan perendaman dengan NaOH 1N selama 1 hari. Elektrode aktif dicuci dengan air deionisasi sebanyak 3 kali ulangan. Elektrode karbon aktif direndam dalam air deionisasi hingga akan digunakan.
Membran PSf diaktivasi dengan cara direbus dalam air deionisasi selama 1 jam. Selanjutnya membran direbus kembali dalam H2O2 selama 1 jam, dan dilanjutkan dalam H2SO4 selama 1 jam. Kemudian membran yang dibilas dengan air bebas ion 3 kali.
Membran yang telah dan belum diaktivasi diukur luasnya sesuai dengan luas elektrode, kemudian diukur ketebalannya. Konduktivitas proton dari membran diukur menggunakan alat impedance analyzer.
Uji Aplikasi Sistem DMFC
Sistem DMFC memiliki 2 sisi, yaitu sisi katode dan anode. Sisi anode berisi 100 mL metanol 3N, sedangkan sisi katode berisi 50 mL K3Fe(CN)6 dan 50 mL K2HPO4. Membran diletakan diantara kedua sisi anode dan katode, kemudian kedua sisi dihubungkan elektrode karbon yang telah diaktivasi. Konduktivitas proton ditentukan menggunakan impedance analyzer.
HASIL DAN PEMBAHASAN
Sintesis membran polistirena terfluorinasiPolistirena terfluorinasi diperoleh melalui reaksi polistirena dan garam fluorida. Garam fluorida terbuat dari reaksi trietilamina dengan asam fluorida (HF). Trietilamina digunakan untuk menurunkan reaktivitas F (TCI 2008), sehingga lebih aman digunakan. Garam trietilamina akan terprotonasi, kemudian fluorida yang bermuatan negatif akan menyerang benzuna atau dehidrobenzena pada posisi orto, meta, dan para (Gambar 1).
3
(b)
Gambar 1 Reaksi (a) protonasi trietilamina dan (b) fluorinasi PS.
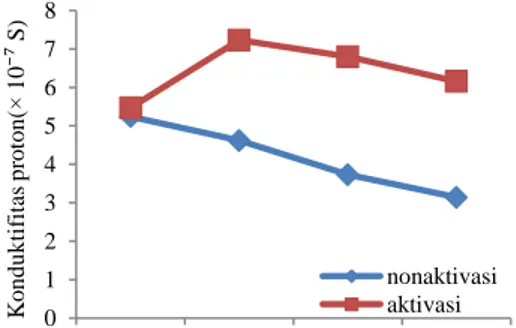
Gambar 2 Spektrum FTIR membran PS ( ) dan PSf ( ). Polistirena terfluorinasi yang dihasilkan
berbentuk padatan dan berwarna putih membran dibuat dengan melarutkan PS dan PSf dalam diklorometana. PS larut sempurna dalam diklorometana karena adanya kesamaan sifat nonpolar (Cowd 1991). Pembuatan membran menghasilkan variasi warna putih. Intensitas warna PSf 15% > PS > PSf 10% > PSf 5%. Perbedaan penambahan fluorida pada PS menyebabkan perbedaan intensitas warna.
Masuknya fluorida dapat merubah berat molekul polimer. Hal ini ditunjukan berat molekul PSf lebih besar dibandingkan PS, yaitu 239634.78 lebih besar dari pada 79777.77 (Lampiran 2). Hasil menunjukan bobot molekul PSf hampir tiga kali bobot molekul PS. Hal ini terjadi akibat PSf yang diperoleh belum murni.
Analisis Gugus Fungsi dan Morfologi Membran
Spektrum FTIR dari membran PS (Gambar 2) menunjukan adanya serapan pada daerah bilangan gelombang 1492.71 cm-1 dari
cincin aromatik benzena dan pada daerah bilangan gelombang 3081.97, 3060.16, 3026.24, dan 3002.50 cm-1 d i aromatik. Fluorida pada cincin benzena aromatik pada polistirena ditunjukan di daerah bilangan gelombang 1028.55 dan 1069.14 cm1. Kemungkinan masuknya fluorida pada cincin benzena aromatik ditunjukan pada daerah bilangan gelombang 757.93 dan 701.38 cm-1 untuk posisi orto, 623.07 cm-1 untuk posisi meta, dan 842.02 cm-1 untuk posisi para. Ketajaman pita menunjukan bahwa fluorida tersubtitusi pada posisi meta dan para. Sedangkan pada posisi orto sangat sedikit karena pita yang dihasilkan saling bertumpang tindih. Spektrum PSf menunjukan penambahan daerah bilangan gelombang pada 981.65 cm-1 yang berasal dari 1,3,5-benzena trisubtitusi.
Morfologi membran merupakan karakteristik membran dilihat dari pori. Struktur permukaan dan penampang lintang dapat dilihat secara mikroskopis dari foto yang dihasilkan oleh SEM. Hasil SEM
C-F Para
Orto Meta
4
memperlihatkan lapisan atas membran PS (Gambar 3a1) maupun PSf (Gambar 3a2) tidak berpori, sehingga diharapkan selektivitas membran tinggi, sehingga hanya proton yang dapat dilewatkan oleh membran bukan metanol atau hasil samping oksidasi metanol.
(a1) (a2)
(b1) (b2)
Gambar 3 Struktur permukaan atas membran perbesaran 5000x (a1) PS; (a2) PSf dan penampang lintang membran perbesaran 1000x (b1) PS; (b2) PSf.
Penampang lintang membran PS berbeda dengan PSf. Masuknya fluorida menyebabkan adanya pori pada lapisan tengah membran (Gambar 3b). Besar pori yang dihasilkan sebesar ±1.9 μm yang termasuk kedalam membran asimetrik (Mulder 1996). Pori pada lapisan tengah akan memengaruhi jarak atom atau molekul pada polimer (Hendrana et al. 2007). Jarak ini akan mengganggu aliran proton yang nantinya akan mempengaruhi nilai konduktivitas proton.
Water uptake dan Permeabilitas Metanol
Hubungan water uptake dengan konsentrasi membran ditunjukan oleh Gambar 4.
Gambar 4 Hubungan water uptake dengan konsentrasi membran.
Water uptake PSf lebih besar dibandingkan PS. Meningkatnya water uptake dalam membran PSf dapat terjadi karena adanya pori dalam membran (Li et al. 2010). Air yang
masuk akan mengisi pori yang ada dalam penampang lintang membran.
Water uptake membran PSf menunjukan semakin tinggi konsentrasi membran maka semakin rendah persentase water uptake. Semakin tinggi water uptake maka kandungan air dalam membran akan semakin besar (Lampiran 3). Hal ini akan mempengaruhi kinerja membran dalam aplikasi ke DMFC. Menurut Rikukawa (2000) semakin tinggi water uptake maka konduktivitas proton akan semakin tinggi karena semakin banyak molekul air dalam membran yang dapat menjadi media transfer proton. Namun, semakin tinggi water uptake juga akan meningkatkan permeabilitas metanol yang dapat menurunkan stabilitas membran.
Kebradaan air memengaruhi transport metanol dalam membran melalui ikatan hidrogen antara air dengan metanol. Namun, hasil menunjukan tidak ada metanol yang terlewatkan ketika uji kualitatif permeabilitas metanol yang ditunjukan dengan keringnya tisu pada permukaan bawah membran. Hal ini dikarenakan permukaan membran yang dihasilkan tidak berpori. Sehingga dapat dikatakan membran PSf memiliki water uptake dan permeabilitas metanol yang baik.
Konduktivitas Proton Membran dan Sistem DMFC
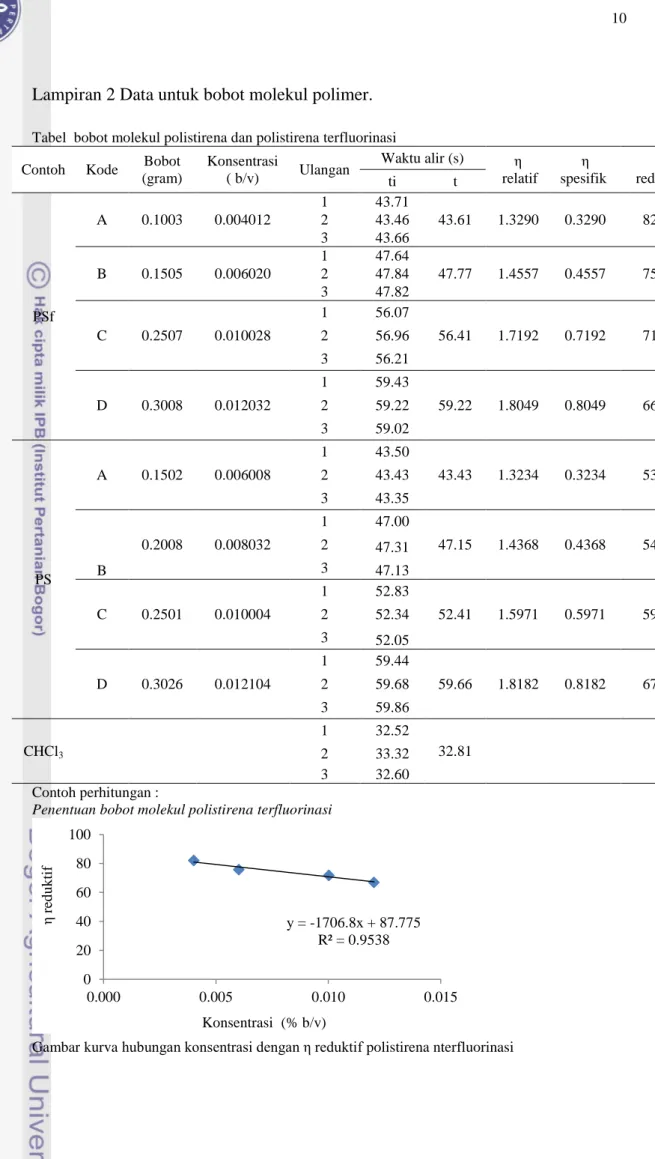
Konduktivitas proton membran menunjukan kemampuan proton dapat bergerak dari anode menuju katode. Hasil menunjukan konduktivitas membran yang diaktivasi lebih besar dibandingkan membran yang tidak diaktivasi (Gambar 5).
Gambar 5 Hubungan konduktivitas membran PSf aktivasi dan nonaktivasi.
Konduktivitas proton membran PS dan PSf yang diaktivasi berturut-turut adalah 5.47 × 10-7, 7.23× 10-7, 6.8× 10-7, dan 6.16× 10-7 S/cm. Nilai ini lebih besar dibandingkan membran PS dan PSf tidak diaktivasi, yaitu 5.24 ×10-7, 4.62 ×10-7, 3.73 ×10-7, dan 3.14 0 2 4 6 8 10 12 0 5 10 15 Wa te r u p ta ke ( %) Konsentrasi (%) 0 1 2 3 4 5 6 7 8 0 5 10 15 K o n d u k ti fi ta s p ro to n (× 10 ⁻⁷ S) Konsentrasi (%) nonaktivasi aktivasi Pori
5
×10-7 S/cm. Ini menunjukan bahwa membran yang mampu menghantarkan proton dengan baik adalah membran PSf 5%. Hal ini sesuai dengan hasil water uptake yang didapat, dimana membran PSf 5% memiliki nilai water uptake tertinggi, karena keberadaan air dapat membrantu transfer proton dalam membran.
Sistem DMFC menggunakan metanol sebagai bahan bakar pada sisi anode. Metanol lebih mudah teroksidasi dibandingkan air sebagai pelarutnya. Potensial reduksi metanol lebih kecil dibandingkan air, yaitu 0.76 V < 0.83 V. Potensial reduksi lebih kecil akan lebih mudah teroksidasi. Oksidasi metanol mengasilkan elektron, proton dan gas CO2 (Gambar 6). Elektron akan dihantarkan oleh elektrode dari anode menuju katode yang nantinya akan terukur arusnya. Proton yang dihasilkan akan dilewatkan oleh membran menuju katode. Anode : CH3OH +7H2OCO2 + 6H3O + + 6e -Katode : 6 Fe3+ +6 e- 6Fe2+ Redoks : CH3OH + 7H2O + 6 Fe3+ CO2 + 6Fe2+ +6H3O+
Gambar 6 Reaksi redoks sistem DMFC. Sistem DMFC dilakukan dalam dua kondisi suhu, yaitu suhu kamar dan suhu 60°C. Hasil menunjukan bahwa sistem DMFC pada suhu 60°C memiliki konduktivitas yang lebih besar dibandingkan dengan suhu kamar (Gambar 7). Hal ini disebabkan kenaikan suhu meningkatkan kinetika reaksi oksidasi metanol (Neburchilov et al. 2007).
Gambar 7 Hubungan konduktivitas proton pada suhu kamar dan 60°C.
Energi kinetik reaksi oksidasi metanol yang tinggi akan meningkatkan laju reaksi. Berbeda halnya dengan kondisi sistem pada suhu kamar yang menghasilkan nilai konduktivitas proton yang lebih rendah. Hal ini dapat diakibatkan reaksi oksidasi metanol pada suhu kamar berjalan lebih lambat dibandingkan pada suhu 60 °C. Sehingga,
menghasilkan konduktivitas proton lebih rendah.
Pada prinsipnya metanol tidak selalu teroksidasi sempurna membentuk CO2, tetapi dapat juga menjadi formaldehida. Oksidasi metanol menjadi formaldehida menghasilkan elektron dan proton yang lebih sedikit dibandingkan oksidasi sempurna menghasilkan CO2. Sehingga menurunkan nilai konduktivitas proton yang dihasilkan. Hal ini juga dapat dilihat dari tidak munculnya gelembung dalam sistem DMFC pada suhu, sedangkan pada suhu 60 °C muncul gelembung yang diduga CO2 -.
Konduktivitas proton sistem DMFC menggunakan membran PSf pada suhu 60°C di atas membran PS. Namun, konduktivitas proton yang dihasilkan tidak berbanding lurus dengan konsentrasi PSf. Nilai konduktivitas proton membran PSf 5% lebih tinggi dibandingkan membran PSf 10% dan 15% (Gambar 8). Hal ini dipengaruhi oleh nilai water uptake membran PSf 5% lebih tinggi dibandingkan dengan membaran lainnya.
Gambar 8 Hubungan antara konsentrasi, konduktivitas proton dan tegangan.
Water uptake akan mempengaruhi rigiditas membran. Membran yang kurang rigid akan sulit menghantarkan proton karena adanya jarak atau gap yang akan menyebabkan pergerakan proton cukup besar (Hendrana et al. 2007). Sehingga nilai konduktivitas proton yang terbaca menjadi kecil (Lampiran 4) walaupun gugus fluorida pada PSf lebih tinggi. Arus PSf 5% lebih tinggi dibandingkan membran lainnya, karena kemampuan sistem menghantarkan arus atau konduktans pada sistem dengan membran PSf 5% lebih besar.
0 0.001 0.002 0.003 0.004 T kamar T 60°C K o n d u k ti v it as p ro to n (S/ c m) Suhu sistem DMFC PS PSf 5% PSf10% PSf 15% 0 0.005 0.01 0.015 0.02 0.025 0.03 0 0.0005 0.001 0.0015 0.002 0.0025 0.003 0.0035 0.004 PS PSf 5% PSf 10% PSf 15% A ru s (m A ) Membran K o n d u k ti v it as P ro to n ( S /c m) konduktivitas Arus
6
SIMPULAN
Membran polistirena terfluorinasi dapat dibuat dengan mereaksikan garam fluorida dengan polistirena secara langsung yang ditunjukan dengan hasil FTIR. Hasil SEM menunjukan bahwa fluorida dalam polistirena membuat adanya pori pada penampang lintang membran. Uji permeabilitas metanol secara kualitatif menunjukan hasil yang baik, dengan keringya permukaan bawah membran. Konduktivitas proton membran PSf aktivasi lebih baik dibandingkan PSf nonaktivasi. Peningkatan suhu menghasilkan konduktivitas proton pada system lebih tinggi dibandingkan pada suhu kamar. Sistem dengan PSf 5% menghasilkan arus dan konduktivitas lebih tinggi dibandingkan membran lainnya.
SARAN
Perlu dilakukan analisis TGA untuk mengetahui ketahanan termal membran. Selain itu perlu dilakukan variasi suhu sistem DMFC untuk mengetahui sifat elektrokimia sitem sel bahan bakar dan penggunaan elektroda Pt untuk membantu oksidasi metanol. Selain itu, pengukuran permeabilitas metanol secara kuantitatif diperlukan untuk mengetahui keberadaan metanol secara pasti dalam sistem.
DAFTAR PUSTAKA
Bae B. 2005. Nafion®-graft-polystyrene sulfonic acid membranes for direct methanol fuel cells. Journal of Membrane Science 276: 51-58.
Baker RW. Membrane Technology in the Chemical Industry: Future Directions. Didalam: Nunes SP, Peinemann KV, editor. 2006. Membrane Technology in
the Chemical Industry. Ed rev.
Weinheim: Wiley-VCH. hlm 329-333. [BPOM] Badan Pengawas Obat dan
Makanan. 2008. Kemasan Polistirena Foam (Styrofoam). Jakarta: BPOM. Cowd MA. 1991. Kimia Polimer. Firman H,
penerjemah; Padmawinata K, editor. London: J Murray. Terjemahan dari: Polymer Chemistry.
Hasan A. 2007. Aplikasi sistem fuel cell sebagai energi ramah lingkungan di
sector ransportasi dan pembangkit. J. Tek. Ling. 8: 277-286.
Hendrana S. Pujiastutu S, Sudirman, Rahayu I, dan Rustam YH. 2007. Pengaruh suhu dan tekanan proses pembuatan terhadap konduktivitas ionic membran PEMFC berbasis polstirena tesulfonasi. Jurnal Sains Materi Indonesia 8: 187-191.
Holland BJ, Zhu JG, Jamet L. 2007. Fuel Cell Technology and Aplication [karya tulis]. Sydney: University of Technology, Faculty of Enginerring. Li YS, Zhao TS, Yang WW. Measurement of
water uptake and transport properties in anion exchange membrane. International Journal of Hydrogen Energy 35: 5656-5665.
Liu Q, Song L, Zhang Z, dan Liu X. 2010. Preparation and characterization of the PVDF-based composite membrane for direct methanaol fuel cell. Inernational Journal of Energy and Environment 1:643-656.
Mulder M. 1996. Basic Principles of
Membran Technology. Netherland:
Kluwer.
Parra et al. 2004. Synthesis, Testing, and Characterization of a Novel Nafion Membrane with Superior Performance in Photoassisted Immobilized Fenton Catalysis. J: American Chemical Societ 20: 5621 -5629.
Rikukawa M dan Sanui K. 2000. Proton-Conducting Polymer electrolyte membranes based on hydrocarbon polymer. Polymer Science 25: 1463-1502.
Shin JP, Chang BJ, Kim JH, Le SB, Suh DH. 2005. Sulfonated polystyrene/ PTFE composite membrane. Journal of membrane Science 251: 247-254. [TCI]Tokyo Chemical Indusry. 2008.
Fluorinatig Reagents & building blocks for fluorinated Biochemical Compounds.Tokyo: TCI UK Ltd.
7
Neburchilov V, Martin J, Wang, Zhang J. 2007. A review of polymer electrolyte membrane for direct methanol fuel cell. Journal of Power Science 169: 221-238.
Wootthikanokkhan J dan Seeponkai N. 2006. Methanol permeability and properties of DMFC membrane based on sulfonated PEEK/PVDF. Journal of Apllied Polymer Science 102:5941-5947.
Yohan, Nur RM, Hendrajaya L, Siradj ES. 2005. Sintesis bahan membran sel bahan bakar: kopolimerisasi stirena pada film ETFE dengan teknik iradiasi awal. Makara 9:72-77.
9
9
Lampiran 1 Diagram alir penelitian.
Pembuatan Et3N.xHF
Sintesis polistirena terfluorinasi
Pencirian membran FTIR SEM Uji Pengaruh Konduktifitas proton T kamar & T 60°C Permeabilitas metanol Water uptake Bobot molekul Kualitatif Kuantitatif Aktivasi elektrode Aktivasi membran
10
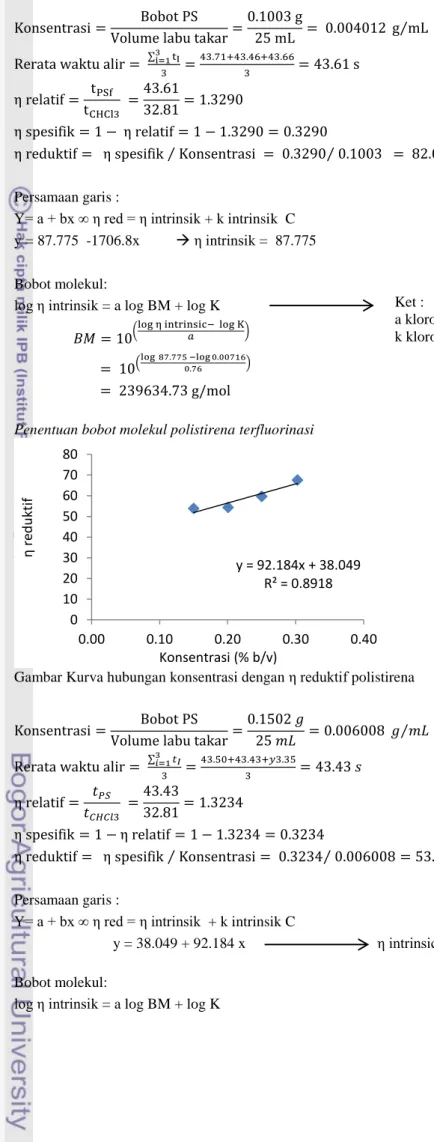
Lampiran 2 Data untuk bobot molekul polimer.
Tabel bobot molekul polistirena dan polistirena terfluorinasi Contoh Kode Bobot
(gram) Konsentrasi ( b/v) Ulangan Waktu alir (s) η relatif η spesifik η reduktif ti t PSf A 0.1003 0.004012 1 43.71 43.61 1.3290 0.3290 82.01 2 43.46 3 43.66 B 0.1505 0.006020 1 47.64 47.77 1.4557 0.4557 75.70 2 47.84 3 47.82 C 0.2507 0.010028 1 56.07 56.41 1.7192 0.7192 71.72 2 56.96 3 56.21 D 0.3008 0.012032 1 59.43 59.22 1.8049 0.8049 66.89 2 59.22 3 59.02 PS A 0.1502 0.006008 1 43.50 43.43 1.3234 0.3234 53.84 2 43.43 3 43.35 B 0.2008 0.008032 1 47.00 47.15 1.4368 0.4368 54.38 2 47.31 3 47.13 C 0.2501 0.010004 1 52.83 52.41 1.5971 0.5971 59.69 2 52.34 3 52.05 D 0.3026 0.012104 1 59.44 59.66 1.8182 0.8182 67.59 2 59.68 3 59.86 CHCl3 1 32.52 32.81 2 33.32 3 32.60 Contoh perhitungan :
Penentuan bobot molekul polistirena terfluorinasi
Gambar kurva hubung n konsent si deng n η eduktif polistirena nterfluorinasi y = -1706.8x + 87.775 R² = 0.9538 0 20 40 60 80 100 0.000 0.005 0.010 0.015 η red u k tif Konsentrasi (% b/v)
11 ⁄ ∑ ⁄ ⁄ Persamaan garis :
Y= + bx ∞ η ed = η int insik + k intrinsik C y = 87.775 -1706.8x η int insik = 87.775 Bobot molekul:
log η int insik = a log BM + log K ( ) ( )
Penentuan bobot molekul polistirena terfluorinasi
Gambar Kurva hubungan konsentrasi dengan η eduktif polistirena
⁄ ∑ ⁄ ⁄ Persamaan garis :
Y= + bx ∞ η ed = η int insik + k intrinsik C
y = 38.049 + 92.184 x η int insic = 38.049 Bobot molekul:
log η int insik = a log BM + log K
y = 92.184x + 38.049 R² = 0.8918 0 10 20 30 40 50 60 70 80 0.00 0.10 0.20 0.30 0.40 η re d u kt if Konsentrasi (% b/v) Ket : a kloroform = 0.76 k kloroform = 0.00716
12
( ) ( ) g/mol
13
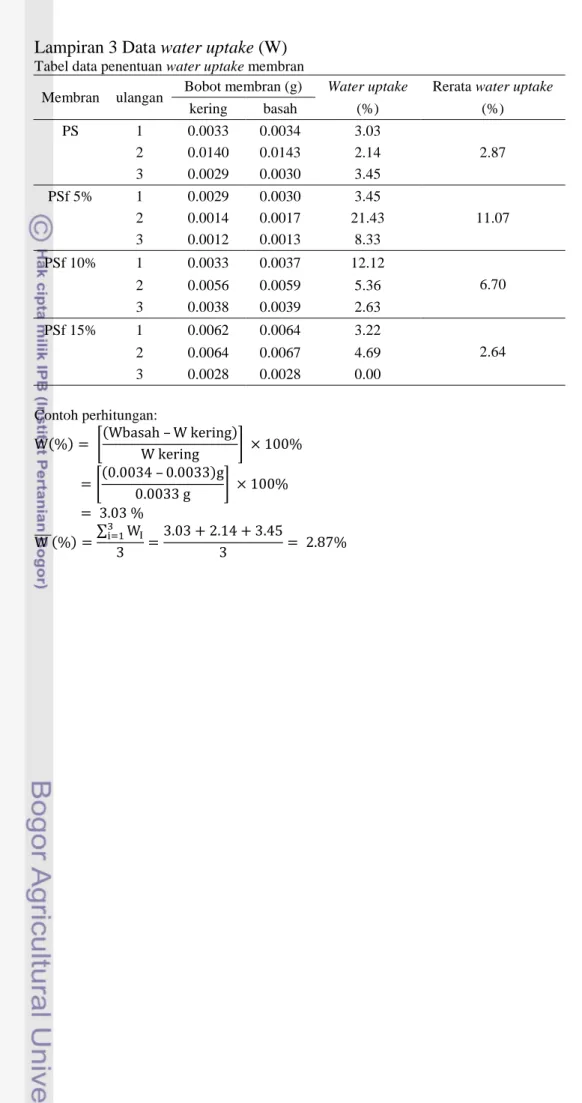
Lampiran 3 Data water uptake (W)
Tabel data penentuan water uptake membran
Membran ulangan Bobot membran (g) Water uptake Rerata water uptake
kering basah (%) (%) PS 1 0.0033 0.0034 3.03 2.87 2 0.0140 0.0143 2.14 3 0.0029 0.0030 3.45 PSf 5% 1 0.0029 0.0030 3.45 11.07 2 0.0014 0.0017 21.43 3 0.0012 0.0013 8.33 PSf 10% 1 0.0033 0.0037 12.12 6.70 2 0.0056 0.0059 5.36 3 0.0038 0.0039 2.63 PSf 15% 1 0.0062 0.0064 3.22 2.64 2 0.0064 0.0067 4.69 3 0.0028 0.0028 0.00 Contoh perhitungan: ( ) [( ) ] [( ) ] ̅̅̅̅( ) ∑
14
Lampiran 4 Konduktivitas proton membran
Tabel Penentuan konduktivitas proton membran
Perlakuan Konsentrasi G (μS) L/A (/cm) ( ×10-7 S/cm) nonaktivasi PS 627.13 0.00083 0.52 PSf 5% 553.63 0.44 PSf 10% 446.30 0.36 PSf 15% 376.16 0.30 aktivasi PS 654.49 0.00083 0.54 PSf 5% 865.88 0.69 PSf 10% 814.66 0.67 PSf 15% 793.60 0.63 Contoh perhitungan: ( ) ⁄
15
Lampiran 5 Uji Aplikasi Sistem DMFC
Keterangan : 1 : Termometer
2 : Elektroda karbon pada anode 3 : Elektroda karbon pada katode 4 : Impedance analyzer tipe LCR 5 : Hot plate
Gambar Pengujian membran untuk sistem DMFC. Tabel Penentuan konduktivitas proton sistem DMFC.
Konsentrasi PSf (%) Konduktivitas (μs) Jarak elektroda (cm) Konduktivitas proton (S/cm) 0 371.68 0.00058 5 448.06 7.50 0.00071 10 402.08 0.00063 15 427.46 0.00068 Contoh perhitungan: ( ) ( ⁄ ⁄ ) ( ( ) ⁄ (a) (b)
Gambar Sistem DMFC (a) suhu kamar (b) suhu 60 °C.
1 2 3 4 5