LAPORAN PRAKTIKUM KIMIA
KOROSI
KELOMPOK 3 : AULIA J. N. FAISHAL ANWAR S. FANNY AVIANUARI HARLINA j. RIKA IRNAWATI SIGIT ABDUL M.TAHUN AJARAN 2010/2011
SMAN 1 DEMAK
LAPORAN PRAKTIKUM
I.
TUJUAN
Dalam melaksanakan praktikum percobaan tentang korosi kita dapat membuktikan proses korosi dalam kehidupan sehari-hari, dan adapun tujuanya sebagai berikut :
1. Mengetahui bagaimana proses korosi berlangsung
2. Mengetahui factor-faktor penyebab korosi
3. Diharapkan mampu memahami bagaimana
pencegahan korosi
I. ALAT DAN BAHAN
ALAT : – Gelas Ukur – Pipet tetes – Gunting-cutter BAHAN : – Gelas kosong
– Air (tulis sumbernya : cth : air PAM, air sumur, air
hujan, dsb) – HCl
– Paku (masih bagus-belum berkarat) – Plastik kresek
– Karet – Selotip
I. LANGKAH KERJA
1. Siapkan alat dan bahan, pastikan bersih dan tidak ada
campuran bahan lain.
1. Gelas pertama :
Masukan paku ke dalam gelas aqua yang kosong
2. Gelas kedua :
Masukan paku dan air ke dalam gelas aqua dengan posisi paku terpelungkup, sehingga semua bagian terkena air
3. Gelas Ketiga :
Masukan paku dan air ke dalam gelas, namun posisi paku berdiri sehingga tidak semua bagian paku terkena air.
4. Gelas ke-empat :
Masukan paku dan HCl ke dalam gelas aqua dengan posisi paku terpelungkup, sehingga semua bagian terkena air. Agar paku tidak terjatuh ke dalam air, gunakan selotip dan tempelkan selotip + paku ke dinding gelas.
5. Gelas ke-Lima :
Masukan paku ke dalam gelas lalu tutup dengan plastic hingga tidak ada udara yang bisa masuk ke dalam gelas.
6. Gelas ke-enam :
Masukan paku dan air ke dalam gelas dengan posisi paku terpelungkup, sehingga semua bagian terkena air.
Lalu tutup dengan plastic hingga tidak ada udara yang bisa masuk ke dalam gelas.
7. Gelas Ke-tujuh :
Masukan paku dan air ke dalam gelas namun posisi paku berdiri sehingga tidak semua bagian paku terkena air. Agar paku tidak terjatuh ke dalam air, gunakan selotip dan tempelkan selotip + paku ke dinding gelas.
Lalu tutup dengan plastic hingga tidak ada udara yang bisa masuk ke dalam gelas.
8. Gelas Ke-8 :
Masukan paku dan HCl ke dalam gelas lalu tutup dengan plastic hingga tidak ada udara yang bisa masuk ke dalam gelas.
1. Catat perubahan pada paku tiap harinya…!!!
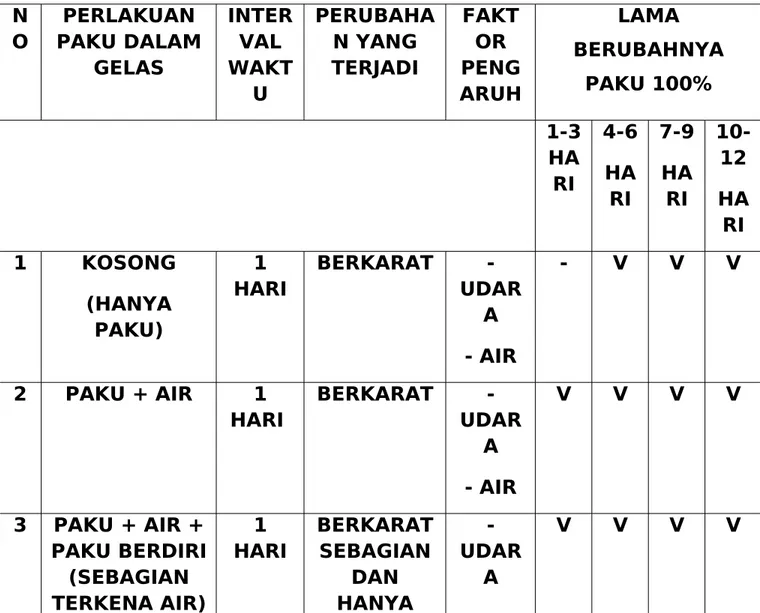
TABEL PENGAMATAN N O PERLAKUAN PAKU DALAM GELAS INTER VAL WAKT U PERUBAHA N YANG TERJADI FAKT OR PENG ARUH LAMA BERUBAHNYA PAKU 100% 1-3 HA RI 4-6 HA RI 7-9 HA RI 10-12 HA RI 1 KOSONG (HANYA PAKU) 1 HARI BERKARAT - UDAR A - AIR - V V V 2 PAKU + AIR 1 HARI BERKARAT - UDAR A - AIR V V V V 3 PAKU + AIR + PAKU BERDIRI (SEBAGIAN TERKENA AIR) 1 HARI BERKARAT SEBAGIAN DAN HANYA - UDAR A V V V V
YANG TERKENA AIR. - AIR 4 PAKU + HCL 1 HARI BERKARAT warna hitam, BERGELEM BUNG - UDAR A - - V v 5 PAKU (TERTUTUP RAPAT OLEH PLASTIK) 1 HARI TIDAK BERKARAT - - - -6 PAKU + AIR(TERTUTU P RAPAT OLEH PLASTIK) 1 HARI BERKARAT - AIR - - V V 7 AIR + PAKU BERDIRI (SEBAGIAN TERKENA AIR) + (TERTUTUP RAPAT OLEH PLASTIK) 1 HARI BERKARAT SEBAGIAN DAN HANYA YANG TERKENA AIR. - AIR - - V V 8 PAKU + HCl 1 HARI BERKARAT warna hitam, TIDAK ADA GELEMBUN G - - - V V I. PEMBAHASAN
Pada peristiwa korosi, logam mengalami oksidasi,
sedangkan oksigen (udara) mengalami reduksi. Karat
logam umumnya adalah berupa oksida atau karbonat.
Rumus kimia karat besi adalah Fe
2O
3.nH
2O, suatu zat
padat yang berwarna coklat-merah.
Pada korosi besi, bagian tertentu dari besi itu berlaku
sebagai anode, di mana besi mengalami oksidasi.
Fe(s) <--> Fe
2+(aq) + 2e
Elektron yang dibebaskan di anode mengalir ke bagian
lain dari besi itu yang bertindak sebagai katode, di mana
oksigen tereduksi.
O
2(g) + 4H
+(aq) + 4e <--> 2H
2O(l)
atau
O
2(g) + 2H
2O(l) + 4e <--> 4OH
-(aq)
Ion
besi(II)
yang
terbentuk
pada
anode
selanjutnya teroksidasi membentuk ion besi(III) yang
kemudian membentuk senyawa oksida terhidrasi, yaitu
karat besi. Mengenai bagian mana dari besi itu yang
bertindak sebagai anode dan bagian mana yang bertindak
sebagai katode, bergantung pada berbagai faktor,
misalnya zat pengotor, atau perbedaan rapatan logam
itu.Korosi dapat juga diartikan sebagai serangan yang
merusak logam karena logam bereaksi secara kimia atau
elektrokimia dengan lingkungan. Ada definisi lain yang
mengatakan bahwa korosi adalah kebalikan dari proses
ekstraksi logam dari bijih mineralnya. Contohnya, bijih
mineral logam besi di alam bebas ada dalam bentuk
senyawa besi
oksida
atau besi
sulfida
, setelah diekstraksi
dan diolah, akan dihasilkan besi yang digunakan untuk
pembuatan baja atau baja
paduan
. Selama pemakaian,
baja tersebut akan bereaksi dengan lingkungan yang
menyebabkan korosi (kembali menjadi senyawa besi
oksida).
Deret
Volta
akan membantu untuk dapat mengetahui
kemungkinan terjadinya korosi. Kecepatan korosi sangat
tergantung pada banyak factor.
II. KESIMPULAN :
Dari percobaan yang telah dilaksanakan, dapat ditarik suatu kesimpulan jika KOROSI terjadi karena adanya satu pengaruh lingkungan terhadap suatu benda, dan adanya beberapa factor yang menyebabkan korosi terjadi , adapun factor itu adalah :
1. Udara – O2 : Korosi terjadi lebih mudah jika suatu
logam berekasi dengan udara disekitarnya, jadi korosi akan lebih cepat terjadi jika oksigen bereaksi dengan mengoksidasi logam tertentu yang cukup reaktif, seperti besi (Fe).
2. Air – H2O : Korosi juga akan terjadi jika pereduksinya
adalah air (H2O) , sehingga jika lebih mudah suatu
logam cukup reaktif jika telah berinteraksi dengan air,
3. Jenis Pereduksi : tidak semua pereduksi mampu
menyebabkan korosi, contohnya HCl, dan larutan lainya dari asam halida.
4. Jenis Logam : Logam yang sangat reaktif dapat mencegah logam lain untuk bereduksi sehingga kejadian korosi dapat dicegah.
5. ada atau tidaknya lapisan oksida, karena lapisan
oksida dapat menghalangi beda potensial terhadap elektroda lainnya yang akan sangat berbeda bila masih bersih dari oksida.
I. PERTANYAAN
2. Samakah kecepatan terjaddinya karat pada setiap paku ?
Jika berbeda , urutkan paku berdasarkan kecepatan terjadinya karat
1. Faktor-faktor apa saja yang menyebabkan besi
berkarat?
2. Jika besi diganti dengan logam lain, misalnya aluminiuum, apa yang terjadi jelaskan…!! JAWAB :
1. GELAS YANG BERKARAT : GELAS 1, 2 , 3 , 4 ,6 , 7 ,8
HANYA SAJA WAKTU DAN WARNA KARAT BERBEDA 2. TIDAK SAMA, URUTAN PAKU BERDASARKAN
INTERVAL WAKTU CEPATNYA BERKARAT : 2>3>1>4>6>7>8>5
3. FAKTOR :
– Udara – O2 : Korosi terjadi lebih mudah jika suatu
logam berekasi - dengan udara disekitarnya, jadi korosi akan lebih cepat terjadi jika oksigen bereaksi dengan mengoksidasi logam tertentu yang cukup reaktif, seperti besi (Fe).
– Air – H2O : Korosi juga akan terjadi jika pereduksinya
adalah air (H2O) , sehingga jika lebih mudah suatu
logam cukup reaktif jika telah berinteraksi dengan air,
– Jenis Pereduksi : tidak semua pereduksi mampu
menyebabkan korosi, contohnya HCl, dan larutan lainya dari asam halida.
– Jenis Logam : Logam yang sangat reaktif dapat
mencegah logam lain untuk bereduksi sehingga kejadian korosi dapat dicegah.
– ada atau tidaknya lapisan oksida, karena lapisan
oksida dapat menghalangi beda potensial terhadap elektroda lainnya yang akan sangat berbeda bila masih bersih dari oksida.
1. Yang terjadi jika besi diganti aluminium, maka
jenis logam yang reaktif (mudahnya mendapatkan lapisan oksida) sehingga tidak akan beroksidasi walaupun terkena air dan tidak akan bereduksi terhadap pengaruh lingkungan.
CAPTURING PROVE :
PAKU + HCL – PAKU PADA GELAS 4
HANYA PAKU DITUTUP RAPAT DENGAN
PLASTIK
PAKU BERDIRI + AIR , SEBAGIAN PAKU
TERKENA AIR – PADA GELAS
PAKU + AIR
PAKU + AIR DITUTUP RAPAT DENGAN
PAKU + HCl DITUTUP PLASTIK
PAKU BERDIRI + AIR DITUTUP RAPAT DENGAN PLASTIK
I. PENUTUP
Terima kasih atas perhatianya , semoga laporan ini bermanfaat . Dan kami mohon maaf apabila ada kesalahan kata yang kurang berkenan. Dan jangan lupa terus pelajari mapel Biologi , karena ilmu ini sangat bermanfaat bagi kehidupan kita secara langsung maupun tidak langsung. Wassalamuallaikum Wr.Wb.