1
A. Latar Belakang
Di tengah banyaknya jenis obat modern di pasaran dan munculnya berbagai jenis obat modern yang baru, belakangan ini terdapat kecenderungan global untuk kembali ke alam (back to nature). Beberapa hal yang mendorong masyarakat untuk menggunakan obat bahan alam antara lain mahalnya harga obat sintetis tertentu dan banyaknya efek samping yang timbul (Pramono, S., 2002). Obat tradisional Indonesia merupakan warisan budaya bangsa sehingga perlu dilestarikan, diteliti dan dikembangkan. Penelitian obat tradisional Indonesia mencakup penelitian obat herbal baik tunggal maupun dalam bentuk ramuan. Jenis penelitian yang telah dilakukan selama ini meliputi penelitian budidaya tanaman obat, analisis kandungan kimia, toksisitas, farmakodinamik, formulasi, dan uji klinik (Dewoto, 2007).
(Artocarpus chempeden Spreng.) bagian bijinya digunakan untuk mengobati diare dan akarnya untuk meredakan demam pada malaria; (Jagtap & Bapat, 2010).
Nangka (Artocarpus heterophyllus Lam.) merupakan salah satu tanaman yang tersebar luas di berbagai daerah tropis, terutama di Asia Tenggara. Nangka adalah salah satu tanaman terbanyak yang terdapat di pekarangan rumah dan boleh jadi adalah tanaman yang paling tersebar luas dan paling bermanfaat dalam genus Artocarpus. Daging buah dan biji dapat dimakan, buah muda dibuat sayur. Kayu dipakai untuk bahan bangunan, getah digunakan sebagai perekat untuk menangkap burung, dan untuk makanan ternak, serta batang dan kulit kayu mengandung zat warna yang dapat digunakan untuk mewarnai makanan atau bahan pakaian. Bagian-bagian dari nangka termasuk kulit pohon, akar, daun, dan buah dikaitkan dengan khasiatnya untuk kesehatan (Elevitch & Manner, 2006).
Bagian-bagian dari tanaman A. heterophyllus biasa digunakan untuk menyembuhkan penyakit, antara lain: daun digunakan untuk mengaktifkan susu pada wanita dan hewan, antisifilis, menghilangkan ulcer dan luka, serta sebagai obat cacing; akar digunakan untuk meringankan diare dan demam, kayu mempunyai efek sedatif (Khan, Omoloso, & Kihara, 2003), buah muda sebagai astringen; buah matang sebagai demulsen, nutrisi, dan laksatif (Lim, T. K., 2012).
agent). Hal ini mendorong banyak peneliti untuk melakukan penelitian lebih lanjut terhadap kayu nangka.
Dalam analisis flavonoid, berbagai metode isolasi dari bahan alam dapat diaplikasikan dan pemanfaatannya tergantung pada bahan alam yang akan diekstraksi. Adanya karbohidrat dan atau senyawa lipofilik dapat mempengaruhi profil komposisi kualitatif dan kuantitatif flavonoid serta turunannya dari ekstrak yang diperoleh. Hal-hal di atas perlu dipertimbangkan dalam pemilihan metode untuk persiapan sampel dan ekstraksi, dalam banyak kasus diperlukan perlakuan tambahan dengan Solid-Phase Extraction (SPE) dari sampel yang diambil (Grotewold, 2006). Pemilihan metode ekstraksi dan pemilihan pelarut merupakan hal yang penting dalam pembuatan ekstrak untuk sediaan obat tradisional. Ketepatan penggunaan pelarut dapat mempengaruhi efek yang diharapkan karena zat aktif yang terlarut berkaitan dengan pelarut yang digunakan tersebut(Departemen Kesehatan Republik Indonesia, 1986).
Metode ekstraksi sederhana yang sering digunakan termasuk untuk penelitian diantaranya, maserasi, perkolasi, namun tidak menutup kemungkinan dilakukan secara infundasi. Pelarut yang dapat digunakan adalah etanol, air, dan campurannya (Departemen Kesehatan Republik Indonesia, 1986). Fraksinasi sering dilakukan pada ekstrak kental yang diperoleh dari proses ekstraksi. Fraksinasi dilakukan dengan tujuan untuk meningkatkan kadar zat yang diinginkan dalam ekstrak.
melakukan penelitian agar didapatkan data ilmiah mengenai metode ekstraksi yang menghasilkan kadar flavonoid total paling tinggi sehingga dapat dijadikan acuan dalam memilih metode ekstraksi untuk pelaku usaha obat tradisional yang menggunakan flavonoid dari kayu nangka.
B. Rumusan Masalah Permasalahan yang diajukan dalam penelitian ini adalah:
1. Apakah kadar flavonoid total ekstrak kental kayu nangka yang diperoleh melalui ekstraksi secara maserasi lebih tinggi dibandingkan kadar flavonoid total ekstrak kental kayu nangka yang diperoleh melalui ekstraksi secara infundasi?
2. Apakah fraksi etanol dari ekstrak dekokta kayu nangka memiliki kadar flavonoid total yang lebih tinggi daripada ekstrak kental hasil maserasi?
C. Tujuan Penelitian Penelitian ini bertujuan untuk mengetahui:
1. Metode yang menghasilkan kadar flavonoid lebih tinggi dari ekstrak kayu nangka antara metode maserasi dan infundasi.
2. Pengaruh fraksinasi menggunakan etanol terhadap kadar flavonoid ekstrak kayu nangka hasil infundasi.
D. Manfaat Penelitian
pemilihan metode ekstraksi yang digunakan bagi industri yang memproduksi obat tradsional dengan kayu nangka sebagai bahan utamanya.
E. Tinjauan Pustaka 1. Nangka (Artocarpus heterophyllus Lam.)
a. Taksonomi dan Nama Daerah Klasifikasi Ilmiah Kerajaan : Plantae Divisi : Tracheophyta Kelas : Magnoliopsida Ordo : Rosales Suku : Moraceae Genus : Artocarpus
Spesies : Artocarpus heterophyllus Lam.
( ITIS (Integrated taxonomic information system), 2015) b. Nama daerah
Aceh: Pana, Panah, Panaih, Panas; Sunda: Nangka; Jawa: Nongka; Bali: Nangka; Bima: Nangga, Nanga; Sumba: Nangka, Nanga; Sulawesi Utara: Nangga; Seram Barat: Nongga; Seram Timur: Tehele kaolin; Irian Jaya: Naknak, Krour; Halmahera Utara: Naka; Ternate Tidore : Naka
Gambar 1. Pohon nangka (Artocarpus heterophyllus Lam.) (Elevitch & Manner, 2006)
c. Morfologi
1) Ukuran dan bentuk: Nangka tumbuh sepanjang tahun, tinggi 8-25 m (26-82 kaki) dan diameter batang 30-80 cm (12-32 inci). Seluruh bagian pohon akan mengeluarkan getah putih ketika dilukai.
2) Bunga: Berumah satu, alat reproduksi jantan dan betina pada satu pohon. 3) Daun: Daun berwarna hijau tua, berseling, mengkilap, kasar, kaku, besar
(panjang sampai 16 cm), berbentuk elips sampai oval. Bentuk daun muda sangat lobe (menjorok).
Kulit buah berwarna hijau hingga kuning kemerahan. Daging buah tipis hingga tebal. Setelah matang, daging buah berwarna kuning merah, lunak, manis dan aroma spesifik. Pohon nangka berakar tunggang dengan akar samping yang kuat dan dalam (Sunarjono 2010).
5) Biji: Berwarna cokelat terang sampai cokelat; bulat; panjang 2-3 cm dengan diameter 1,15 cm; serta dilapisi membran berwarna keputihan.
6) Perakaran nangka memiliki akar tunggang yang kuat (Elevitch & Manner, 2006).
7) Kayu: Sifat-sifat kayu nangka yaitu agak berat, agak keras atau keras, agak padat atau padat, serat agak kasar atau kasar, warna kuning sitrun mengkilat, warna akhirnya menjadi cokelat; kayu sukar dibelah, tetapi mudah dikerjakan, mudah diserut, dibubut, dan digilapkan (Heyne, K., 1987). d. Sinonim
Artocarpus integrifolia var. heterophylla (Lam.) Pers., Artocarpus brasiliensis Gomez, Artocarpus heterophylla Lam., Artocarpus integrifolia auct., Artocarpus integrifolia sensu Trimen non. L. f., Artocarpus integrifolia var. glabra Stokes, Artocarpus jaca Lam., Artocarpus maxima Blanco, Artocarpus philippinensis Lam., Polyphema jaca Lour., Saccus cauliflorum Gaertn., Tsjaka-maram Rheede (Lim, T. K., 2012).
e. Kegunaan
Di Jawa, kayu nangka banyak digunakan untuk membuat tiang bangunan, kentongan, dan lesung. Kayu tersebut baik sekali untuk membangun rumah dan membuat mebel (Heyne, K., 1987).
f. Kandungan Kimia
Wong dkk. (1992) menemukan bahwa buah nangka mengandung 45 senyawa volatil dan 32 diantaranya belum pernah dilaporkan. Proporsi besar dari ester (31,9%) dalam senyawa-senyawa volatil tersebut berperan penting terhadap rasa buah nangka. Selain itu, buah nangka merupakan sumber provitamin A karotenoid, meskipun tidak sebaik papaya (Lim, T. K., 2012). Bijinya kaya protein, kandungan proteinnya lebih tinggi daripada protein hewani seperti daging dan ikan laut (Ajayi, 2008).
Zat ekstraktif pada kayu nangka didominasi oleh senyawa semi polar yang terlarut dalam etil asetat seperti alkaloid, aglikon, terpenoid, flavonoid, dan glikosida (Amilya, 2014). Kayu nangka mengandung beberapa zat warna flavon (Dave dan Venkataraman, 1956; Dave dkk., 1960, 1961; Rao dkk., 1973) dan flavonoid yang memiliki aktivitas pemutih kulit (Arung dkk., 2006).
tirosinase jamur dan produksi melanin pada sel melanoma B16. Artokarpin, kudraflavon C, 6-prenilapigenin, kuwanon C, norartokarpin, dan albanin A yang diisolasi dari kayu nangka dapat menghambat biosintesis melanin pada sel melanoma B16 dengan sedikit bahkan tanpa sitotoksisitas (Arung dkk., 2006).
2. Ekstraksi
Proses penyarian tumbuhan pada dasarnya dibedakan menjadi dua fase, yaitu fase pencucian dan fase ekstraksi. Fase pencucian merupakan fase pertama dalam penyarian karena sebagian bahan aktif akan berpindah ke dalam bahan pelarut. Semakin halus serbuk simplisia maka akan semakin optimal pula jalannya proses pencucian ini. Pada fase ekstraksi terjadi peristiwa pendesakan bahan pelarut untuk melarutkan komponen dalam sel yang tidak terluka. Mengalirnya bahan pelarut ke dalam ruang sel akan mengakibatkan pembengkakan protoplasma, dan terlarutnya bahan kandungan sel sesuai dengan kelarutannya (Voigt, R., 1994).
Prinsip ekstraksi adalah pelarutan/pengikatan zat aktif berdasarkan sifat kelarutannya dalam suatu pelarut (like dissolved like). Jenis dan mutu pelarut yang digunakan sangat menentukan keberhasilan proses ekstraksi. Pelarut yang digunakan harus dapat melarutkan zat yang diinginkan, mempunyai titik didih yang rendah, murah, dan tidak toksik (Ketaren, S., 1986).
pemilihan pelarut dan cara ekstraksi yang tepat (Departemen Kesehatan Republik Indonesia, 2000).
Cara penyarian yang sering dilakukan ada 4, yaitu infundasi, maserasi, perkolasi, dan sokletasi. Metode ekstraksi yang paling sederhana dan banyak dilakukan oleh masyarakat adalah infundasi dan maserasi.
a. Infundasi merupakan proses penyarian yang umum digunakan untuk menyari zat aktif yang larut dalam air. Penyarian dengan cara ini akan menghasilkan sari yang tidak stabil dan mudah tercemar oleh kuman dan kapang, sehingga sari yang diperoleh dengan cara infundasi tidak boleh disimpan lebih dari 24 jam.
Infusa adalah sediaan cair yang dibuat dengan menyari simplisia dengan air pada suhu 90ᴼC selama 15 menit. Dekokta adalah sediaan cair yang dibuat dengan menyari simplisia dengan air pada suhu 90ᴼC selama 30 menit (Departemen Kesehatan Republik Indonesia, 1986).
b. Maserasi merupakan cara ekstraksi yang dilakukan dengan merendam serbuk simplisia dalam cairan penyari. Keuntungan cara ini adalah cara pengerjaan dan peralatannya sederhana, meskipun demikian ada juga kerugiannya, yaitu waktu pengerjaannya relatif lebih lama dan penyariannya kurang sempurna (Departemen Kesehatan Republik Indonesia, 1986).
yang dikatalisis oleh cahaya dan juga untuk menghindari terjadinya perubahan warna (Voigt, R., 1994).
Alat yang dibutuhkan untuk melakukan maserasi adalah bejana dan pengaduk. Bejana digunakan sebagai wadah dalam proses perendaman simplisia oleh cairan penyari. Untuk simplisia yang mengandung senyawa-senyawa yang memiliki gugus ortodihidroksi atau hidroksikarbonil harus menggunakan baja yang tahan karat atau bahan logam lain yang dilapisi email. Hal ini bertujuan untuk mencegah terbentuknya kompleks antara logam berat dengan senyawa-senyawa yang memiliki gugus ortodihidroksi atau hidroksikarbonil. Pengaduk digunakan untuk mengaduk rendaman simplisia agar gradien konsentrasi tetap terjaga. Pengadukan dapat dilakukan secara manual atau dengan menggunakan pengaduk mekanik (Departemen Kesehatan Republik Indonesia, 1986).
3. Fraksinasi
Fraksinasi adalah suatu proses yang bertujuan untuk menghilangkan senyawa yang tidak dikehendaki tanpa berpengaruh pada senyawa yang dikehendaki, sehingga diperoleh ekstrak yang lebih murni yang mengandung senyawa yang dikehendaki. Pemilihan pelarut didasarkan pada senyawa yang dikehendaki (Departemen Kesehatan Republik Indonesia, 2000).
4. Flavonoid
a. Kerangka dasar dan pengertian flavonoid
yang dihubungkan oleh 3 atom karbon yang dapat atau tidak dapat membentuk cincin ketiga. Flavonoid terdapat dalam semua tumbuhan hijau sehingga dapat ditemukan pada setiap ekstrak tumbuhan (Markham, K.R., 1988). Golongan flavonoid dapat digambarkan sebagai deretan senyawa C6-C3-C6. Artinya,
kerangka karbonnya terdiri atas dua gugus C6 (cincin benzen tersubstitusi)
disambungkan oleh rantai alifatik tiga-karbon :
Gambar 2. Kerangka Flavonoid (Robinson, T., 1995)
Golongan terbesar flavonoid berciri mempunyai cincin piran yang menghubungkan rantai tiga-karbon dengan salah satu dari cincin benzena. Sistem penomoran untuk turunan flavonoid diberikan di bawah:
Gambar 3. Sistem penomoran turunan flavonoid (Robinson, T., 1995)
Diantara flavonoid khas yang mempunyai kerangka seperti di atas berbagai jenis dibedakan berdasarkan tahanan oksidasi dan keragaman lain pada rantai C3.
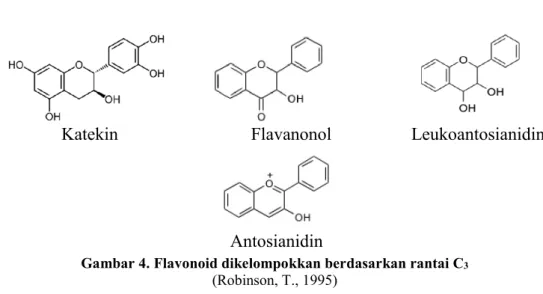
Katekin Flavanonol Leukoantosianidin
Antosianidin
Gambar 4. Flavonoid dikelompokkan berdasarkan rantai C3
(Robinson, T., 1995)
Auron dan khalkon juga tersusun atas kerangka karbon C6-C3-C6
sehingga termasuk senyawa flavonoid dan dimasukkan ke dalam golongan flavonoid minor (Grotewold, 2006).
Flavonoid terdistribusi luas pada makanan dan minuman yang berasal dari tanaman seperti buah-buahan, sayuran, teh, kakao, dan anggur. Diketahui bahwa kuersetin adalah komponen yang paling banyak ditemukan pada makanan dari berbagai flavonoid yang tergolong sebagai flavonol dan flavon (Grotewold, 2006).
Gambar 5. Struktur kimia kuersetin (Andersen & Markham, 2006)
LDL (Low Density Lipoprotein) sehingga menghambat agregasi platelet secara in vitro (Hertog dkk., 1997).
b. Flavonoid pada kayu nangka
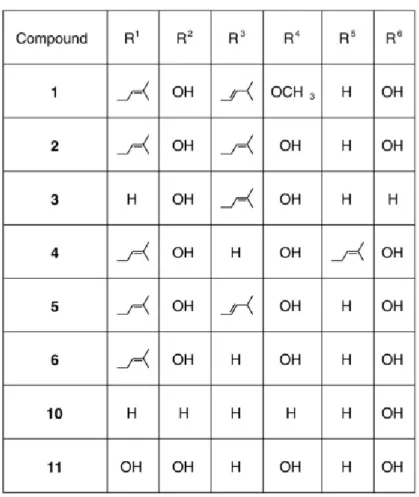
Beberapa zat warna flavon telah diisolasi dari kayu nangka, yaitu morin (11), dihidromorin, sinomakurin, artokarpin, isotokarpin, sikloartokarpin, artokarpesin, oksidihidroartokarpesin, artokarpetin, norartokarpetin, sikloartinon, artokarpenon (Dave dan Venkataraman, 1956; Dave dkk., 1960, 1961; Rao dkk., 1973).
Gambar 6. Struktur senyawa 1-11 (Arung dkk., 2010)
c. Penyarian dan pemisahan flavonoid
Menurut Harborne (1996), idealnya untuk analisis fitokimia harus digunakan jaringan tumbuhan yang segar. Beberapa menit setelah dikumpulkan, bahan tumbuhan tersebut harus dimasukkan ke dalam alkohol mendidih. Bila bahan tidak tersedia, maka jaringan yang diambil segar harus disimpan kering di dalam kantung plastik, dan biasanya akan tetap dalam keadaan baik untuk dianalisis setelah beberapa hari dalam perjalanan.
benar-benar kering, tumbuhan dapat disimpan sampai digunakan untuk analisis. Cara demikian telah dilakukan dengan berhasil pada analisis flavonoid, alkaloid, kuinon, dan terpenoid terhadap herbarium yang telah disimpan bertahun-tahun (Harborne, J. B., 1996).
Macam ekstraksi yang tepat bergantung pada tekstur dan kandungan air bahan tumbuhan yang diekstraksi dan pada jenis senyawa yang diisolasi (Harborne, J. B., 1996). Flavonoid mudah mengalami peruraian karena panas, kerja enzim, adanya air, dan pH. Oleh karena itu, beberapa usaha perlu dilakukan untuk menghindari perubahan molekul flavonoid pada proses isolasi. Diantaranya adalah segera memanasi bagian tanaman yang masih segar pada 50
0C. Pemanasan dimaksudkan untuk mencegah aktivitas enzim, tetapi panas yang
digunakan tidak terlalu tinggi.
5. Kromatografi
Kromatografi adalah metode pemisahan komponen-komponen dalam campuran berdasarkan perbedaan kecepatan migrasi komponen-komponen tersebut, yang dibawa oleh fase gerak, untuk melintasi fase diam (Skoog dkk., 2014).
atau dengan cara elusi dua dimensi; dan ketepatan penentuan kadar lebih baik karena komponen yang ditentukan adalah bercak yang tidak bergerak (Gandjar, I.G. & Rohman A., 2007).
a. Fase diam
Fase diam yang digunakan pada KLT merupakan penjerap berukuran kecil dengan diameter partikel antara 10-30 µm. Semakin kecil ukuran rata-rata partikel fase diam dan semakin sempit kisaran ukuran fase diam, maka semakin baik kinerja KLT dalam hal efisiensinya dan resolusinya.
Penjerap yang paling sering digunakan adalah silika dan serbuk selulosa, sementara mekanisme sorpsi yang utama pada KLT adalah partisi dan adsorbsi. Lapisan tipis yang digunakan sebagai penjerap juga dapat dibuat dari silika yang telah dimodifikasi, resin penukar ion, gel eksklusi, dan siklodestrin yang digunakan untuk pemisahan kiral (Gandjar, I.G. & Rohman A., 2007).
1) Silika
Silika gel atau silika adalah penjerap yang paling sering digunakan untuk analisis fitokimia secara kromatografi lapis tipis, misalnya untuk determinasi komponen racun seperti asam aristolokik pada pengobatan tradisional Cina.
silanol (Si-OH). Fase gerak pada silika gel biasanya lebih nonpolar dibandingkan silika gel yang bersifat polar, fase ini disebut fase normal (normal phase). (Waksmundzka-Hajnos dkk., 2008).
Silika paling berguna untuk memisahkan aglikon yang kurang polar, misalnya isoflavon, flavonon, metil flavon, dan flavonol (Markham, K.R., 1988).
2) Selulosa
Selulosa terdiri atas rantai panjang polimerisasi beta-glokopiranosa yang terhubung pada posisi 1-4. Mekanisme pemisahannya adalah partisi fase normal (normal phase) dengan menyerap air sebagai fase diam. Pemisahan fitokimia yang dapat dilakukan dengan menggunakan selulosa adalah untuk senyawa asam hidrosinamat ester, flavonol, glikosida, antosianin, aglikon flavon dan flavonon, saponin triterpenoid, dan glukosida iridoid (Waksmundzka-Hajnos dkk., 2008).
Selulosa ideal untuk memisahkan glikosida yang satu dari glikosida yang lain, memisahkan glikosida dari aglikon, dan untuk memisahkan aglikon yang kurang polar. Selulosa sering digunakan untuk identifikasi flavonoid secara umum (Markham, K.R., 1988).
b. Fase gerak
komponen senyawa yang dipisahkan. Fase gerak harus mudah dihilangkan dari fase diam atau penjerap dan harus sesuai dengan metode deteksinya.
Umumnya, jika fase diam yang digunakan polar maka fase gerak yang digunakan sebaiknya nonpolar atau sedikit polar, sistem ini dinamakan sistem fase normal atau normal-phase (NP). Sebaliknya, bila fase diam bersifat nonpolar dan fase gerak polar, maka sistem ini disebut sistem fase terbalik atau reversed-phase (RP) (Waksmundzka-Hajnos dkk., 2008).
Flavon dan flavonol termetilasi atau teretilasi memerlukan fase gerak yang bersifat nonpolar seperti, kloroform-metanol (15:1). Aglikon flavonoid seperti apigenin dan kuersetin dapat memakai fase gerak kloroform-metanol (96:4) atau fase gerak lain yang sifat kepolarannya sama (Andersen & Markham, 2006).
c. Deteksi
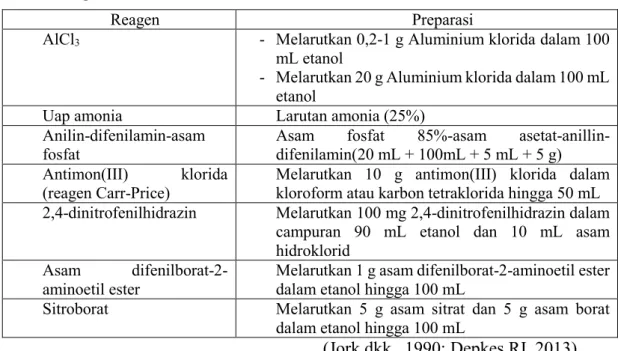
Tabel I. Reagen untuk deteksi flavonoid
Reagen Preparasi
AlCl3 - Melarutkan 0,2-1 g Aluminium klorida dalam 100
mL etanol
- Melarutkan 20 g Aluminium klorida dalam 100 mL etanol
Uap amonia Larutan amonia (25%)
Anilin-difenilamin-asam fosfat
Asam fosfat 85%-asam asetat-anillin-difenilamin(20 mL + 100mL + 5 mL + 5 g) Antimon(III) klorida
(reagen Carr-Price)
Melarutkan 10 g antimon(III) klorida dalam kloroform atau karbon tetraklorida hingga 50 mL 2,4-dinitrofenilhidrazin Melarutkan 100 mg 2,4-dinitrofenilhidrazin dalam
campuran 90 mL etanol dan 10 mL asam hidroklorid
Asam difenilborat-2-aminoetil ester
Melarutkan 1 g asam difenilborat-2-aminoetil ester dalam etanol hingga 100 mL
Sitroborat Melarutkan 5 g asam sitrat dan 5 g asam borat dalam etanol hingga 100 mL
(Jork dkk., 1990; Depkes RI, 2013) Beberapa flavonoid akan menunjukkan warna sebagai berikut ketika diamati di bawah sinar UV 366 nm:
1) Kuersetin, mirisetin, dan bentuk 3- dan 7-O-glikosidanya: jingga-kuning. 2) Kaempferol, isorhamnetin, dan bentuk 3- dan 7-O-glikosidanya:
kuning-hijau.
3) Luteolin dan bentuk 7-O-glikosidanya: jingga.
4) Apigenin dan bentuk 7-O-glikosidanya: kuning-hijau.
(Andersen & Markham, 2006)
6. Spektrofotometri
Pengukuran kuantitatif secara spektrofotometri ditetapkan dengan persamaan Lambert Beer sebagai berikut: A = abc
Absorptivitas (a) merupakan suatu konstante yang tidak tergantung pada konsentrasi (c), tebal kuvet (b), dan intensitas radiasi yang mengenai larutan sampel. Absorptivitas tergantung pada suhu, pelarut, struktur molekul, dan panjang gelombang radiasi. Satuan a ditentukan oleh satuan-satuan b dan c. Jika satuan c dalam molar (M) maka absorptivitas disebut dengan absorptivitas molar dan disimbolkan dengan dengan satuan M-1cm-1 atau Liter.mol-1cm-1. Jika c dinyatakan dengan persen berat/volume (g/100 mL) maka absorptivitas dapat ditulis dengan % dan juga seringkali ditulis dengan % . Nilai % merupakan absorbansi suatu senyawa yang diukur pada konsentrasi 1% b/v (1 g/100 mL) dan dengan kuvet yang mempunyai ketebalan 1 cm pada panjang gelombang dan pelarut tertentu.
NMR (Nuclear Magnetic Resonance) atau MS (Mass Spectrophotometry) (Andersen & Markham, 2006).
F. Landasan Teori
Prinsip ekstraksi adalah pelarutan/pengikatan zat aktif berdasarkan sifat kelarutannya dalam suatu pelarut (like dissolved like). Salah satu kriteria pelarut yang akan digunakan yaitu harus dapat melarutkan zat yang diinginkan (Ketaren, S., 1986). Ekstraksi dengan metode infundasi menggunakan pelarut akuades (polar), sedangkan ekstraksi dengan metode maserasi menggunakan pelarut etanol (semi-polar).
Kandungan kayu nangka yang dapat diekstraksi didominasi oleh senyawa semi polar yang terlarut dalam etil asetat seperti alkaloid, aglikon, terpenoid, flavonoid, dan glikosida (Amilya, 2014). Beberapa flavonoid yang telah berhasil diisolasi dari kayu nangka adalah artokarpanon, artokarpin, kudraflavon C, 6-prenilapigenin, kuwanon C, norartokarpin, dan albanin A (Arung dkk., 2006). Berdasarkan strukturnya, flavonoid pada kayu nangka lebih banyak yang berupa aglikon sehingga akan lebih larut dalam etanol 96% yang bersifat semipolar.
G. Hipotesis
Hipotesis yang diajukan dalam penelitian ini adalah:
1. Ekstrak kental hasil maserasi kayu nangka memiliki kadar flavonoid total lebih tinggi dibandingkan ekstrak kental hasil infundasi kayu nangka. 2. Fraksi etanol dari ekstrak kental hasil infundasi kayu nangka memiliki kadar