Oleh :
SUKRON NI’AM O 121 14 016
PROGRAM STUDI PETERNAKAN
JURUSAN PETERNAKAN
FAKULTAS PETERNAKAN DAN PERIKANAN
UNIVERSITAS TADULAKO
LAPORAN LENGKAP PRAKTIKUM BIOKIMIA
Di susun Sebagai Salah SatuSyarat Dalam Menyelesaikan Mata Kuliah
Biokimia
Oleh :
SUKRON NI’AM O 121 14 016
PROGRAM STUDI PETERNAKAN
JURUSAN PETERNAKAN
FAKULTAS PETERNAKAN DAN PERIKANAN
UNIVERSITAS TADULAKO
HALAMAN PENGESAHAN
Judul : Laporan Lengkap Praktikum Bahan Makanan Ternak
Nama : Sukron Ni’am
Stambuk : O 121 14 016
Kelompok : II ( Dua )
Program Studi : Peternakan
Fakultas : Peternakan dan Perikanan
Universitas : Tadulako
Palu, Desember 2015
Penyusun
Menyetujui,
Koordinator Asisten Praktikum Asisten Praktikum
Ibrahim Hamzah Ibrahim Hamzah O 121 12 036 O 121 12 036
Mengetahui,
Dosen Koordinator Mata Kuliah Mikrobiologi
UCAPAN TERIMA KASIH
Puji skukur penulis panjatkan kehadirat Allah SWT atas limpah rahmat
serta karunia-Nya kepada penulis untuk menyelasikan laporan praktikum
mengenai “Uji karbohidrat, Protein, Lipid dan Enzim’’ yang dapat terlaksana
dengan baik. Tak lupa penyusun mengucapkan banyak terima kasih kepada semua
pihak yang telah banyak berperan penting dalam membantu penyusunan laporan
ini. Khususnya kepada Prof. Dr. Ir. Hj. Asriani Hasanuddin, MS selaku dosen
pembimbing mata kuliah biokimia yang banyak memberikan semangat dan
masukan baik dalam teori maupun pelaksanaannya, dan terima kasih juga kepada
kakak asisten dosen yang telah memberikan bimbingan dan arahan selama
kegiatan praktik hingga sampai saat penyusunan laporan ini.
Dalam penyusunan laporan lengkap ini penulis menyadari bahwa masih
sangat jauh dari kesempurnaan dan masih banyak kekurangan, oleh karana itu
penulis mengharapkan kritik dan saran yang bersifat membangaun sehingga dapat
dijadikan pedoman agar memperbaiki penyusunan laporan selnjutnya. Dan
semoga laporan ini dapat bermanfaat bagi kita semua terutama kepada penulis
sendiri, baik sekarang maupun di masa yang akan datang.
Palu, November 2015
DAFTAR TABEL
Nomor Halaman
1. Alat dan Bahan Pada Uji Karbohidrat... 10
2. Alat dan Bahan Pada Uji Asam Amino dan Protein... 11
3. Alat dan Bahan Pada Uji Lipid... 11
4. Alat dan Bahan Pada Uji Enzim... 12
5. Pengamatan Percobaan B Karbohidrat... 12
DAFTAR GAMBAR
Nomor Halaman
I. PENDAHULUAN
1.1 Latar Belakang
Biokimia merupakan ilmu yang mempelajari struktur dan fungsi komponen
selular, seperti protein, karbohidrat, lipid, asam nukleat, dan biomolekul lainnya. Saat ini biokimia lebih terfokus secara khusus pada kimia reaksi
termediasi enzim dan sifat-sifat protein. Secara biokimia karbohidrat adalah
polihidroksil-aldehida atau polihidroksil-keton, atau senyawa yang menghasilkan
senyawa-senyawa ini bila dihidrolisis. Karbohidrat mengandung gugus fungsi
karbonil (sebagai aldehida atau keton) dan banyak gugus hidroksil. Pada awalnya,
istilah karbohidrat digunakan untuk golongan senyawa yang mempunyai rumus
(CH2O)n, yaitu senyawa-senyawa yang n atom karbonnya tampak terhidrasi oleh
molekul air. Namun demikian, terdapat pula karbohidrat yang tidak memiliki
rumus demikian dan ada pula yang mengandung nitrogen, fosforus, atau sulfur.
Karbohidrat menyediakan kebutuhan dasar yang diperlukan tubuh makhluk hidup.
Monosakarida, khususnya glukosa, merupakan nutrien utama sel. Misalnya, pada
vertebrata, glukosa mengalir dalam aliran darah sehingga tersedia bagi seluruh sel
tubuh.
Sel-sel tubuh tersebut menyerap glukosa dan mengambil tenaga yang
tersimpan di dalam molekul tersebut pada proses respirasi selular untuk
menjalankan sel-sel tubuh. Selain itu, kerangka karbon monosakarida juga
berfungsi sebagai bahan baku untuk sintesis jenis molekul organik kecil lainnya,
karbohidrat memiliki nilai energi 4 Kalori. Dalam menu makanan orang Asia
Tenggara termasuk Indonesia, umumnya kandungan karbohidrat cukup tinggi,
yaitu antara 70–80%. Bahan makanan sumber karbohidrat ini misalnya
padi-padian atau serealia (gandum dan beras), umbi-umbian (kentang, singkong, ubi
jalar), dan gula.
1.2 Tujuan
Tujuan dari praktikum biokimia pembuatan ekstra amilum, uji karbohidrat,
asam amino dan protein, uji biuret, dan penentuan angka penyabunan, penentuan
FFA,pengeruh konsentrasi enzim, dan pengaruh suhu adalah supaya mahasiswa
mengetahui dan memahami bagaimana cara yang baik dan melakukan percobaan
karbohidrat, protein, lipid, dan enzim agar manghasilkan hasil percobaan yang
benar dalam melakukan penelitian tersebut.
1.3 Kegunaan
Menentukan ekstrak pati dari umbi-umbian atau kentang untuk melihat
perubahan pada kentang setelah di panaskan dengan mengunakan uji kuantitatif
dan kwalitatif karbohidrat yang telah di peroleh, pada protein untuk menentukan
uji kualitatif dalam asam amino dan protein sedangkan lipid dan enzim yaitu
menentukan asam lemak bebas dan angka penyabunan serta dalam enzim
II. TINJAUAN PUSTAKA
2.1 Karbohidrat
Karbohidrat atau hidrat arang atau zat pati, berasal dari bahan baku nabati.
Kadar karbohidrat dalam pakan ikan, dapat berkisar antara 10 –50%.
Kemampuan ikan untuk memanfaatkan karbohidrat ini tergantung pada
kemampuannya untuk menghasilkan enzim pemecah karbohidrat (amilase).
Ikan karnivora biasanya membutuhkan karbohidrat sekitar 12%, sedangkan
untuk omnivora kadar karbohidratnya dapat mencapai50% (Teguh, 2009).
Karbohidrat adalah senyawa organik yang mengandung atom Karbon,
Hidrogen dan Oksigen, dan pada umumnya unsur Hidrogen clan oksigen
dalam komposisi menghasilkan H2O. Di dalam tubuh karbohidrat dapat
dibentuk dari beberapa asam amino dan sebagian dari gliserol lemak. Akan
tetapi sebagian besar karbohidrat diperoleh dari bahan makanan yang
dikonsumsi sehari-hari, terutama sumber bahan makan yang berasal dari
tumbuh-tumbuhan. Sumber karbohidrat nabati dalam glikogen bentuk glikogen,
hanya dijumpai pada otot dan hati dan karbohidrat dalam bentuk laktosa hanya
dijumpai di dalam susu. Pada tumbuh-tumbuhan, karbohidrat di bentuk dari
basil reaksi CO2 dan H2O melalui proses foto sintese di dalam sel-sel
tumbuh-tumbuhan yang mengandung hijau daun (klorofil). Matahari
merupakan sumber dari seluruh kehidupan, tanpa matahari tanda-tanda dari
Karbohidrat merupakan sumber karbon untuk organisme hidup.
serealia maupun dalam batang tanaman. Selain dari sumber nabati, karbohidrat
juga berasal dari pangan hewani yang terbentuk dalam jumlah yang kecil melalui
proses biosintesa glikogen dan sintesa secara kimiawi. Karbohidrat dapat
dioksida menjadi energi, misalnya glukosa dalam sel jaringan manusia dan
hewan. Dalam tubuh, karbohidrat mengalami perubahan atau metabolisme yang
menghasilkan antara lain glukosa yang terdapat dalam darah. Sedangkan
karbohidrat yang disintesa dalam hati berupa glikogen digunakan oleh sel-sel
pada jaringan otot sebagai sumber energy (Pujianto, 2008).
2.2 Protein
Protein adalah senyawa organik kompleks berbobot molekul tinggi yang
merupakan polimer dari monomer-monomer asam amino yang dihubungkan
satu sama lain dengan ikatan peptida. Molekul protein mengandung karbon,
hidrogen, oksigen, nitrogen dan kadang kala sulfur serta fosfor. Protein
berperan penting dalam struktur dan fungsi semua sel makhluk hidup dan virus.
berperan dalam fungsi struktural atau mekanis, seperti misalnya protein yang
membentuk batang dan sendi sitoskeleton (Desrizal, 2011).
Tidak semua protein adalah enzim. Keratin protein struktural pada rambut
hewan dan hormon insulinmerupakan contoh protein bukan enzim. Setiap
polipeptida dari suatu protein juga memiliki monomer yang tersusun
dalam tatanan linear tertentu (struktur primer protein) tetapi monomernya adalah
kedua puluh asam amino tersebut. Dengan demikian, asam nukleat dan protein
berisi informasi yang ditulis dalam dua bahasa kimia yang berbeda (Campbell,
2002).
Denaturasi protein adalah kondisi di mana struktur sekunder, tersier
maupun kuartener dari suatu protein mengalami modifikasi tanpa ada pemecahan
ikatan peptida. Denaturasi dapat berupa rusaknya struktur tiga matra dari suatu
protein. Denaturasi protein ada dua macam, yaitu pengembangan rantai peptide
(terjadi pada polipeptida) dan pemecahan protein menjadi unit yang lebih kecil
tanpa disertai pengembangan molekul (terjadi pada ikatan sekunder)
(Anugrah, 2011).
Selain sifat-sifat yang umum, kebanyakan protein alam masih mempunyai
satu atau lebih sifat khusus. Sifat khusus tersebut mempunyai daya
angkut oksigen, mempunyai daya sebagai alat pengangkut lipida; mempunyai
kelarutan tertentu dalam garam encer atau asam encer; dan mempunyai
aktivitas sebagai enzim. Protein tersebut yang dipengaruhi oleh pemanasan,
sinar ultraviolet, gelombang ultrasonik dan pengocokan yang kuat atau
sendiri dapat diartikan sebagai suatu proses perubahan konfigurasi tiga dimensi
molekul protein tanpa menyebabkan kerusakan ikatan peptida (Sumardjo, 2006).
2.3 Lipid
Lipid didefinisikan sebagai senyawa yang tak larut dalam air yang
diektraksi dari makhluk hidup dengan menggunakan pelarut yang kurang
polar atau pelarut non polar. Istilah lipid mencangkup golongan
senyawa-senyawa yang memiliki keanekragaman struktur, dan tidak ada skema
penggolongan lipid yang bisa diterima diseluruh dunia. Ciri khas yang
umum dijumpai disemua lipid adalah kamdungan hidrokarbonnya diturunkan
dari polimerasi asetat yang diikuti dengan reduksi rantai segera setelah rantai
itu terbentuk (Kuchel dkk, 2002).
Lipid sangat penting di dalam tubuh, baik untuk struktur maupun fungsi
tubuh. Simpanan lemak memberikan cadangan energi, menyekat dan
memberi beberapa perlindungan. Lipid lain merupakan konstituen penting
membran sel (fosfolipid), merupakan prekursor untuk hormon steroid, bekerja
sebagai molekul pengatur (misalnya leukotrin, protoglandin, tromboksan
dan transpor lemak seluruh tubuh (lipoprotein), serta lemak pelarut
vitamin berfungsi dalam pembekuan darah, fungsi penglihatan dan antioksidan
(Brooker, 2005).
Lipid merupakan bentuk energi tubuh yang paling pekat. Sel-sel otak
hanya menggunakan glukosa tetapi jaringan tubuh lainnya seperti otot jantung
lebih memilih lipid sebagai sumber energi. Asam lemak akan mengalami oksidasi
krebs, tidak perlu melalui jalur glikolisis. Reaksi ini disebut sebagai reaksi
oksidasi-beta karena yang dioksidasi adalah atom karbon kedua (James,
dkk., 2008).
Lipid terkonjugasiterbentuk dari pengikatan gugus fosfat atau gula ke
molekul lemak. Fosfolid dan Glikolipid ini merupakan konstituen intgral struktur
dinding sel. Sterol juga berfungsi sebagai building block. Struktural di sel
dan membran serta sebagai konstituen hormon dan metabolit lain. Karena tidak
larut dalam air, lipid memerlukan mekanisme pengangkutan khusus agar
bersirkulasi dalam darah. Asam lemak bebas hanya terdapat dalam jumlah
kecil di dalam darah dan umumnya berikatan secara longgar dengan
albumin. Komponen-komponen lipid utama yang dijumpai dalam plasma
adalah trigliserida, koleterol, dan fosfolipid. Ketiganya terdapat dan diangkut
dalam darah sebagai lipoprotein, suatu kompleks makromolekul yang sangat
besar dari lipid dan protein khusus (apolipoprotein) yang membantu
pengemasan, kelarutan, dan metabolisme lemak (Sacher dan Ricard, 2005).
Oksidasi asam lemak tidak jenuh akan menghasilkan peroksida dan
selanjutnya akan terbentuk aldehida. Inilah yang menyebabkan terjadinya bau dan
rasa yang tidak enak atau tengik. Kelembaban udara, cahaya, suhu tinggi dan
adanya bakteri perusak adalah faktor-faktor yang menyebabkan terjadinya
ketengikan. Gliserol yang diperoleh dari hasil penyabunan lemak atau minyak
adalah suatu zat cair yang tidak berwarna dan mempunyai rasa yang
2.4 Enzim
Enzim adalah suatu kelompok protein yang menjalankan dan mengatur
perubahan-perubahan kimia dalam sistem biologi. Zat ini dihasilkan oleh
organ-organ hewan dan tanaman, yang secara katalik menjalankan berbagai
reaksi, seperti pemecahan hidrolisis, oksidasi, reduksi, isomerisasi, adisi, transfer
radikal dan kadang-kadang pemutusan rantai karbon. Kebanyakan enzim yang
terdapat di dalam alat-alat atau organ-organ organisme hidup berupa larutan
koloidal dalam cairan tubuh, seperti air ludah, darah, cairan lambung dan
cairan pankreas (Sumardjo, 2006).
Kekhususan suatu enzim berhubungan dengan adanya kesesuaian antara
bentuk tempat aktifnya dengan bentuk substratnya. Namun demikian, tempat
aktif itu bukanlah suatu tempat penerima yang kaku bagi substrat tersebut.
Ketika substrat memasuki tempat aktif, maka enzim akan terinduksi untuk
mengubah bentuknya sedikit sehingga tempat aktif akan lebih pas mengelilingi
substrat itu (Campbell, 2002).
Pada suhu yang lebih tinggi, kecepatan molekul substrat meningkat,
sehingga pada saat bertumbukan dengan enzim, energi molekul substrat
berkurang. Hal ini memudahkan terikatnya molekul substrat pada sisi aktif
enzim. Aktifitas enzim meningkat dengan meningkatnya suhu sampai pada titik
tertentu (Aryulina, dkk., 2006).
Enzim sebagai katalisator, suatu enzim berikatan dengan substrat rekasi
dan mengubah substrat menjadi prodak. Substrat berikatan dengan
dengan residu asam amino enzim. Geometri ruang yang diperlukan untuk semua
interaksi antara substrat dan enzim menyebabkan setiap enzim selektif bagi
substratnya, dan memastikan bahwa yang dihasilkan hanyalah prodak spesifik
(Marks, dkk., 2000).
Enzim memiliki kemampuan katalis yang sangat efisien dan kuat
meskipun dalam konsentrasi yang rendah. Enzim adalah protein spesifik
yang dapat dimanfaatkan kembali karena enzim akan selalu muncul kembali
dalam keadaan utuh setelah substrat diubah menjadi produk. Untuk mempercepat
reaksi-reaksi dapat dilakukan dengan menaikkan suhu, namun hal tersebut tidak
sesuai sebagai sumber energi pengaktif bagi organisme (Setiowati dan Furqonita,
III. METODE PRAKTIKUM
3.1 Waktu dan Tempat
3.1.1 Praktikum Karbohidrat dan Protein
Praktikum Biokimia Pengujian Karbohidrat dan Protein dilaksanakan pada
hari Jum’at, 16 Oktober 2015 pukul. 13.00 WITA bertempat di Laboratorium
Perikanan, Fakultas Peternakan dan Perikanan, Universitas Tadulako, Palu.
3.1.2 Pratikum Lipid dan Enzim
Praktikum Biokimia Pengujian Karbohidrat dan Protein dilaksanakan pada
hari Sabtu, 23 oktober 2015 pikul. 13.00 WITA bertempat di Laboratorium
Perikanan, Fakultas Peternakan dan Perikanan, Universitas Tadulako, Palu.
3.2 Alat dan Bahan 3.2.1 Karbohidrat
1. Isolasi Amilum Dari Kentang
Tabel 1. Alat Dan Bahan Isolasi Amilum Dari Kentang
Alat Bahan
Pisau + blender Kentang 500 gr
Kain saringan Gelas piala 500 ml
Gelas ukur 250 ml Etanol 95 %
3.3 Prosedur Kerja
300 gr kentang dikupas dan dicuci lalu dipotong – potong, kemudian
dihomogenisasi dengan 200 ml air dalam belender dalam 1 menit. Bubur kentang
yang diperoleh disaring dengan mengunakan kain saringan didapatkan cairan
berwarna keruh yang di tampung dala gelas piala 500 ml, residu yang tersisa kain
di buang.
Setelah diperoleh semua cairan dikocok dan campuran diberikan
mengendap beberapa waktu sehingga akan terjadi diendapan amilum. Larutan
bagian atas didekantasi dan endapan ditambakan lagi 200 ml air, aduk secara
sempurna dan setelah itu dibiarkan seperti diatas dan larutan bagian atas dibuang,
pekerjaan terahir adalah menambakan laruran etanol 95 % kedalam endapan
sebanyak 100 ml lalu didekantasi lagi setelah itu disaring endapan dengan corong
lalu dikeringkan dengan cara penyebaran pada suhu kamar. Setelah itu ditimbang
beratnya.
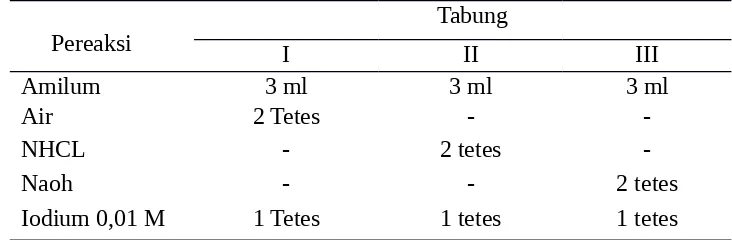
2. Uji Iodida Pada Amilum
Tabel 2 alat dan bahan Uji Iodida Pada Amilum
Alat Bahan
Tabung Reaksi Larutan Amilum 1%
A) Cara Kerja
Iodium 0,01 M 1 Tetes 1 tetes 1 tetes
Campuran yang berwarna dipanaskan, catat adanya perubahan warna, dinginkan dan catat lagi terjadinya perubahan warna.
3.2.2 Protein
Masukan kedalam masing-masing tabung reaksi tambakan larutan protein
dan asam amino sebanyak 3 ml. Setelah itu ditambahkan 1 ml NaOH campurkan
dengan baik, selanjutnya masukan setetes CuSO4 kocok amati perubahan ya ng
terjadi .jika timbul warna tambahkan lagi setetes atau lebih CuSO4 dan amati
perubahan yang terjadi.
Alat Bahan
Pendingin tegak Minyak kelapa
Erlemeyer 250 ml Minyak bimoli
Buret NaOH 1 M
Timbangan Indikator Pp
Pipetetessumbat gabus / karet HCL 1 M
C) Prosedur kerja
1. Penentuan Angka Penyabunan
a. Timbang 2,5 ml minyak dengan teliti kedalam erlemeyer 250 ml,
tambahkan 25 ml NaOH. Setelah itu tutup dengan pendingin balik,
didihkan dengan hati-hati selam 15 menit.
b. Setelah itu dinginkan dan tambahkan dengan beberapa tetes indikator pp
dan titrasi dengan HCL untuk mengetahui kelebihan NaOH.
c. Lakukan hal yang sama terhadap larutan blanko (NaOH) dan titrasi dengan
HCL 1 M .
d. Hitung angka penyabunan dengan rumus Sbb.
Angka penyabunan = 28,05x(Titrasi Blanko- Sample) Berat Sampel
2. Penentuan Asam Lemak Bebas
a. Timbang sample sebanyak 10 gr kedalam elenmeyer, kemudian tambahkan alcohol panas sebanyak 25 ml. selanjutnya tambahkan idikator pp
sebanyak 4 tetes.
b. Titrasi dengan NaOH 0,1 M sampai larutan tampak berubah menjadi merah muda dan tidak tidak hilang selama 30 detik.
Catatan : Untuk minyak Bimoli adalah oleat dengan BM = 256 dan
minyak kelapa asam larut dengan BM = 200.
3.2.4 Enzim
Tabel 5. Alat Dan Bahan Percobaan Enzim
Alat Bahan
1. Siapkan 3 buah tabung reaksi, tambahkan masing-masing 2 ml larutan
amilum 1% kedalam setiap tabung masukan 5 tetes larutan iodium.
2. Setelah itu masukan ekstrak enzim sebanyak 2 ml,3 ml dan 4 ml, pada
masing-masing tabung reaksi. Catat berapa lama waktu yang
diperlukan sehinga larutan tidak berwarna biru lagi.
B. Pengaruh Suhu Terhadap Aktivitas Enzim Cara kerja:
1. Siapkan 3 buah tabung reaksi, tambahkan masing-masing 2 ml larutan
2. Tabung reaksi kemudian disiapkan dalam berbagai suhu yaitu suhu
kamar 45o C dan 50o C.
3. Setelah 5 menit tambahkan larutan enzim, selanjutnya catat waktu
perubahan warna larutan dari amilum.
IV. HASIL DAN PEMBAHASAN
4.1.1 Percobaan I : Karbohidrat Pengamatan Percobaan A
1. Berat kentang (sampel) = 297gr
2. Kentang setelah diblender akan terjadi Hancur menjadi bubur kentang
berwarna coklat mudah keruh.
3. Amilum dalam suspensi alkohol bewarna Putih keruh setelah kering
bewarna putih susu.
4. Berat amilum setelah kering = 2,57 gr.
5. % kadar amilum dalam kentang = 20 %
Pengamatan Percobaan B
Perubahan Tabung
I II III
Warna sebelum ditambahkan iodium Bening Bening Bening Warna setelah ditambhakan iodium Bening Biru Bening
Warna setelah pemanasan Bening Bening Bening
Warna setelah didinginkan Bening Biru Bening
4.1.2 Percobaan II : Uji Asam Amino Dan Protein Pengamatan Percobaan A
Larutan sampel NaOH 2,5 M CuSO40,01 M CuSO40,01 M berlebihan
Larutan Protein 2 ml 1 tetes 8 Tetes
Cystein 3 ml 3 tetes 3 tetes
4.1.3 Percobaan III : Lipid Pengamatan Percobaan A
Volume HCl pada titrasi blanko = 2 4,8 ml
Perubahan yang diamati pada waktu titrasi adalah dari warna merah muda ke
warna bening
Nilai angka penyabunan : MB = 12. MK 17,1
Pengamatan Percobaan B
Volume NaOH pada titrasi 1 = 5 ml
Volume NaOH pada titrasi 2 = ...ml
Volume rata-rata = ,,,ml
Perubahan yang diamati pada waktu titrasi adalah dari warna bening Ke warna
merah muda
Nilai % FFA = MB = 0,020736 x MK = 0,0064
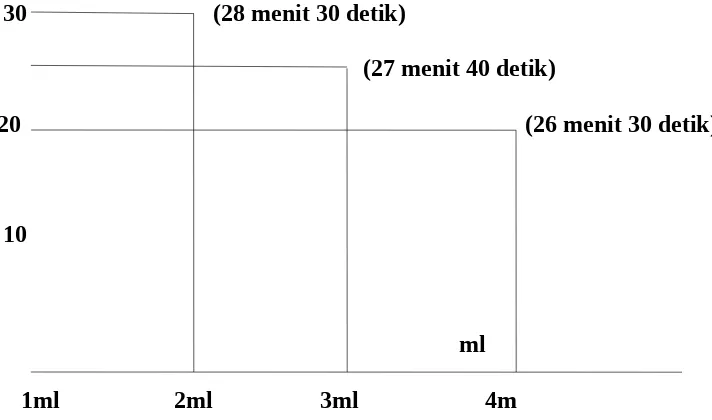
4.1.4 Percobaan IV : Enzim Pengamatan Percobaan A
1. Waktu yang diperlukan terjadinya perubahan warna tabung 1 = 1710 detik.
2. Waktu yang diperlukan terjadinya perubahan warna tabung 2 = 1652 detik.
3. Waktu yang diperlukan terjadinya perubahan warna tabung 3 = 1600 detik.
4. Perubahan warna disebabkan oleh apa adanya tambahan ekstrak touge kedalam masing-masing tabung reaksi.
5. Perubahan warna dari biru perak ke putih.
30 (28 menit 30 detik)
(27 menit 40 detik)
20 (26 menit 30 detik)
10
ml 1ml 2ml 3ml 4m
Pengamatan Percobaan B
1. Waktu yang diperlukan terjadinya perubahan warna tabung 1 = (suhu 450= 46 detik dan suhu 50 0 = 26 detik ).
2. Waktu yang diperlukan terjadinya perubahan warna tabung 2 = ( suhu 450 = 39 detik dan suhu 50 0 = 25 detik ).
3. Waktu yang diperlukan terjadinya perubahan warna tabung 3 = ( suhu 450 = 134 detik dan suhu 500 = 33 detik ).
4. Kenapa suhu dapat mempengaruhi aktivitas enzim kerna enzim sangat peka dan terpengaruh pada suhu.
Gambar 2. Grafik Pngaruh Suhu Terhadap Aktivitas Enzim (menit)
35
Waktu 30
20
15 ( oc)
10 20 30 40 50
Suhu
4.2 Pembahasan 4.2.1 Karbohidrat
Pengamatan Percobaan A
Pada saat dblender, struktur kentang akan hancur dan akan tersisa patinya,
menurut Girindra, (1986) pati merupakan gula cadangan yang terdapat dalam
tumbuhan, atau buah-buahan. Pati terdiri atas amilosa dan amilopektin.
Kandungan pati akan terlepas dari ampas kentang pada saat dilakukan
penyaringan dengan kain saring, selanjutnya pada saat didiamkan beberapa menit
pati akan mengendap pada dasar air. Selanjutnya pati akan diberi alcohol sehingga
warnanya menjadi putih keruh, penambahan alcohol akan mempercepat proses
pengeringan, sehingga larutan amilum yang disuspensi dengan alcohol akan
menyebapkan air mudah menguap dan tersisa bubuk amilum yang berwarna putih
Pengamatan Percobaan B
Pada tabung satu penambahan amilum, air dan iodium akan menyebapkan
perubahan warna dari bening menjadi biru pekat, sedangkan pada tabung dua
penamban amilum dan HCL serta Iodium akan menyebapkan perubahan warna
penambahan HCL sebanyak tiga tetes, HCL mnyebapkan kerja iodium terhambat
selai itu tidak adanya penambahan air menyebapkan iodium lambat bereaksi
sehingga warnanya menjadi biru keunguan. Sedangkan tabung tiga penambahan
amilum, NaOH dan iodium, Iodim tidak bereaksi pada amilum karena adanya
penambahan larutan NaOH. Amilum akan memberikan warna biru dengan adanya
penambahan iodium, penambahan iodium akan dapat masuk dan menduduki
posisi dalam gelung helical yang terbentuk jika amilosa berada pada air (Girindra,
1986)
Pemanasan dengan suhu tinggi akan menyebapkan larutan tidak berubah
warna, perubahan warna hanya terjadi pada pemanasan dengan suhu tinggi karena
air akan menguap dan reaksi iodium terhambat sehingga warna menjadi bening
sedangkan pada saat ddidinginkan kembali warna larutan kembali menjadi biru.
4.2.2 Asam Amino dan Protein
Pada tepung ikan penambahan NaOH 2,3 m pada tepung ikan sebanyak
satu tetes, CuSO4 0,01 m sebanyak satu tetes dan CuSO4 0,01 m berlebih tidak
menyebapkan perubahan warna pada sampel tepung ikan, artinya pada sampel
tepung ikan tidak mengandung protein.
Pada putih telur penambahan NaOH 2,3 m pada tepung ikan sebanyak
satu tetes, CuSO4 0,01 m sebanyak satu tetes dan CuSO4 0,01 m berlebih dapat
menyebapkan perubahan warna sampel putih telur manjadi berwarna ungu pada
saat ditambahkan CuSO4 0,01 m berlebih, hal ini menandakan bahwa putih telur
mengandung protein.
berlebih tidak menyebapkan perubahan warna yang signifikan pada sampel asam
amino Cystein. Uji biuret merupakan salah satu cara untuk mengidentifikasi
adanya protein, dalam larutan basa biuret memberikan warna violet dengan
CuSO4 karena akan terbentuk kompleks Cu2+ dengan gugus CO dan gugus NH
dari rantai peptida dalam suasana basa
4.2.3 Lipid
Percobaan A
Adanya perbedaan volume titrasi blanko dengan volume titrasi sampel
disebapkan adanya kandungan lemak pada larutan sampel, sehingga menyebapkan
pada saat dititrasi dengan menggunakan HCL akan menimbulkan warna
Berdasarkan hasil pengamatan pada pengaruh suhu terhadap aktifitas
enzim, dihasilkan perbedaan penampakan hasil reaksi. Dimana terjadi
perubahan warna dan struktur enzim pada penambahan masing masing 2 ml
terjadinya perubahan warna pada tabung 1 yaitu 46 detik pada suhu 450 C dan 26
detik pada suhu 500 C, Sedangkan pada tabung 2 yaitu 39 detik ada suhu 450 C dan
25 detik ada suhu 50 0 C Dan pada tabung 3 membutuhkan waktu 134 detik ada
suhu 450 C dan 33 detik ada suhu 500 C. Hal ini disebabkan oleh pekanya enzim
terhada perubahan suhu.
V. PENUTUP
5.1 Kesimpulan
Berdasarkan praktikum yang telah dilakukan dapat di peroleh
kesimpulan :
1. Pada pengujian karbohidrat dengan larutan etanol, dalam tabung I dan II
tidak dapat bereaksi karena tidak menghasilkan warna kuning, Sedangkan
2. Pada percobaan protein di dapatkan warna ungu, hal ini di sebabkan
penambahan CuSO4 sehingga terbentuk kompleks antar Cu2+ dengan gugus
amino dari protein. Makin kuat intensitas warna ungu yang di hasilkan ini
menunjukkan makn panjang ikatan peptidanya.
3. Pada pengujian lemak untuk penyabunan lemak atau minyak harus di
panaskan dengan larutan alkali.
4. Pada penyabunan enzim di dapatkan bahwa konsentrasi dan suhu
memegang peranan penting bagi aktifitas enzim.
5.2 Saran
Saran yang dapat diajukan pada praktikum kali ini adalah sebaiknya dalam
setiap hasil reaksi dijelaskan dengan hubungan sebab-akibat, sehingga
praktikan dapat memahami hasil praktikum.
DAFTAR PUSTAKA
Abercrombie,M. dan M.Thain.1993.Kamus Lengkap Biologi. Jakarta: Erlangga.
Anugrah. 2011. Denaturasi Protein. Vol. 3 (1) : 17-18
Aryulina, Diah., Choirul Muslim, Syalfinaf Manaf, Endang W. Winarni. 2006.
Biologi. Erlangga. Jakarta.
Azis, Pradhana. 2007. Enzim dan Faktor-Faktor Yang Mempengaruhi Laju Kerja Enzim. FIK Biochemical Experiment Class. Jakarta.
Brooker, Chris. 2005. Ensiklopedia Keperawatan. Buku Kedokteran EGC. Jakarta
Desrizal. 2011. Fungsi Protein Bagi Tubuh. Vol. 7 (1) : 19-20. Desrizal. 2011. Fungsi Protein BagiTu buh. Vol. 9 (1) : 14-16.
Hutagalung, Haloman. 2004. Karbohidrat. Ilmu Gizi, Fakultas Kedokteran Universitas Sumatera Utara. Sumatera.
Irawan, M. Anwari. 2007. Karbohidrat. Sport Science Brief. 1 (03) : 2-5. James, Joyce. Colin Baker, dan Helen Swain. 2008. Prinsip-Prinsip Sains Untuk Keperawatan. Erlangga. Jakarta Suryani. 2008. Penentuan Lipid. FMIPA UI. Jakarta
Koesnandar. 2001. Biokonversi. Jurnalmikrobiologiindonnesia. Vol. 6 (1) : 15-18
Kuchel, Philip, dan Ralston B. Gregory. 2002. Biokimia. Erlangga. Jakarta.
Marks, Dawn B., Allan D. Marks, Collen M. Smith. 2000. Biokimia. Penerbit Buku Kedokteran. Jakarta.
Mutiara, Indah. 2008. Enzim. Fakultas Kedokteran Universitas Sumatera Utara. Sumatera.
Petrucci, Winarno, 1995.penelitian pratikum lipid saponifikas.jakarta : erlangga
Pujianto, Agus. 2008. Kimia Makanan. Pendidikan Tata Boha. Universitas Sumatera. Sumatera.
Rachman, Riyan Syah., Tampico P., Viona M., Tri Nanda., Ervansyah. 2012.
Enzim Kinetik dan Inhibitor. Universitas Brawijaya. Malang.
Sacher, A. Ronald., dan Richard A. 2005. Tinjauan Klinis Hasil Pemeriksaan Laboratorium. Buku Kedokteran EGC. Jakarta.
Samsuri, Istamar dkk. 2004. Biologi SMA kelas XI. Erlangga : Malang
Sari., M. 2011. SkripsiIdentifikasi Protein Menggunakan Fourier Transform Infrared (FTIR). Fakultasteknik. Universitas Indonesia. Depok
Setiowati, Tetty., dan Deswaty Furqonita. 2007. Biologi Interaktif. Azka Press. Jakarta.
Sumardjo, Damin. 2006. Pengantar Kimia : Buku Panduan Kuliah Mahasiswa
Sunarya, Yayan. (2003). Kimia Dasar 2 Bandung:Alkemi Grafisindo Press
Teguh. 2009. Kebutuhan Nutrisi Pakan Ikan Dan Udang. Vol. 6 (1) : 21-22.
RIWAYAT PENULIS
Penulis bernama lengkap SUKRON NI’AM
lahir di Desa Rio Mukti. Pada tanggal 23
Februari 1996. Penulis adalah putra kedua dari
tiga bersaudara dari pasangan AHMAD FATONI
dan MASRIAH. Pada tahun 2002 penulis memulai pendidikan di SD Impres 5 Rio Pakava,
Desa Rio Mukti, kecamatan Rio Pakava,
Kabupaten Donggala.
Pada tahun 2008 penulis melanjutkan pendidikannya ke SMPI
Langensari dan lulus pada tahun 2009 kemudian melanjutkan pendidikan ke MA
AN-NUR Panca Mukti dan lulus pada tahun 2014. Pada tahun 2014 penulis
melanjutkan study ke jenjang yang lebih tinggi yaitu Universitas Tadulako melalui
jalur SBMPTN dan diterima sebagai mahasiswa baru di Universitas Tadulako,
Fakultas Peternakan Dan Perikanan , Jurusan Peternakan. Dan saat ini penulis