OPTIMASI METODE KROMATOGRAFI CAIR KINERJA TINGGI
(KCKT) UNTUK PENETAPAN KADAR ANTIOKSIDAN
TERSIER BUTIL HIDROKUINON (TBHQ)
DALAMMINYAK GORENG SETELAH
PENGGORENGANBERULANG
TESIS
JABANGUN LUMBANBATU127006009/ KIM
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
OPTIMASI METODE KROMATOGRAFI CAIR KINERJA TINGGI
(KCKT) UNTUK PENETAPAN KADAR ANTIOKSIDAN
TERSIER BUTIL HIDROKUINON (TBHQ)
DALAM MINYAK GORENG SETELAH
PENGGORENGAN BERULANG
TESIS
Diajuka n Sebagai Salah Satu Syarat Untuk Memperoleh Gelar Master Sains Dalam Program Studi Ilmu K imia Pada Fakultas Matematika Dan Ilmu Pengetahuan Alam
Universitas Sumatera Utara
Oleh
JABANGUN LUMBANBATU127006009/ KIM
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
Telah diuji pada
Tanggal : 22Juli 2014
PANITIA PENGUJI TESIS
KETUA : Prof.D r. Harlem Marpaung
PERSETUJUAN
Judul Tesis : OPTIMASI METODE KROMATOGRAFI CAIR KINERJA TINGGI (KCKT) UNTUK PENETAPAN KADAR AN TIOKSIDAN TERSIER BUTIL HIDROKUIN ON (TBHQ)DALAM MINYAK
GORENG SETELAH PENGGOR ENGANBERULANG
Nama Mahasiswa : JABANGUN LUMBANBATU Nomor Pokok : 127006009
Prog ram Studi : MAGISTER (S2) ILMU KIMIA
Menye tujui Komisi Pembimbing
Prof.D r.Harlem Marpaung Dr.M . Pandapotan Nas ution, M PS,Apt
Ketua Anggota
Ketua Program Studi Dekan
Prof. Basuki Wirjosentono, MS, Ph.D Dr. Sutarman, M.Sc
PERN YATAAN ORISINALITAS
OPTIMASI METODE KROMATOGRAFI CAIR KINERJA TINGGI (KCKT) UNTUK PEN ETAPAN KADAR ANTIOKSID ANTERSIER BUTIL
HIDROKUIN ON (TBHQ)DALAM MINYAK GORENG SETELAH PENGGORENGAN BERULANG
TESIS
Dengan ini saya menyatakan bahwa tesis ini adalah hasil karya saya sendiri kecuali kutipan dan ringkasan yang tiap satunya telah dijelaskan sumbernya dengan jelas.
Medan, J uli 2014 Penulis
OPTIMASI METODE KROMATOGRAFI CAIR KINERJA TINGGI (KCKT) UNTUK PENETAPAN KADAR ANTIOKSIDAN TERSIER BUTIL
HIDROKUINON (TBHQ) DALAM MINYAK GORENG SETELAH PENGGORENGAN BERULANG
ABSTRAK
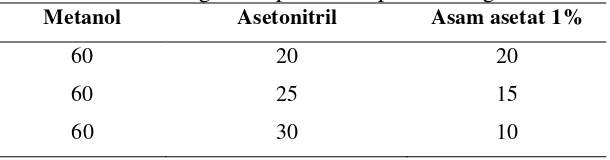
Kromatografi cair kinerja tinggi (KCKT) dengan metode elusi gradien untuk penentuan kadar antioksidan sintetik tertier butil hidrokuinon (TBHQ) dalam minyak goreng setelah penggorengan berulang telah dipelajari. Sistem kromatografi menggunakan fasa gerak campuran metanol : asetonitril : asam asetat 1% (60:30:10), (60:25:15), (60:20:20) dengan laju alir 0,5 mL/menit, 1 mL/menit dan 1,5 mL/menit. Kondisi optimum diperoleh pada fasa gerak campuran metanol : asetonitril : asam asetat 1% (60:20:20) dengan laju alir 0,5 mL/menit. Metode ini memiliki presisi dan akurasi yang baik dengan nilai koefisien korelasi sebesar 0,998, persen perolehan kembali sebesar 98,8-101,1%, limit deteksi (LOD) sebesar 7.8 mg/L, keseksamaan
intra-day sebesar 0,66% dan inter-day sebesar 0,26-0,53%. Hasil analisis kadar antioksidan TBHQ di dalam dalam minyak goreng diperoleh sebesar 169,07 mg/kg. Sedangkan kadar antioksidan TBHQ setelah penggorengan pertama, kedua dan ketiga yaitu 116,23 mg/kg, 101,71 mg/kg dan 88,89 mg/kg. Nilai ini menunjukkan bahwa jumlah antioksidan TBHQ yang ditambahkan ke dalam minyak goreng masih berada di bawah batas maksimum menurut PERMENKES No.1168/MenKes/Per/X/1999.
OPTIMIZATION OF HIGH PERFORMANCE LIQUID CHROMATOGRAPHY (HPLC) METHOD FOR DETERMINATION OF TERTIARY BUTYL
HYDROQUINONE (TBHQ) ANTIOXIDANT LEVEL IN COOKING OIL AFTER REPEATED FRYING
ABSTRACT
High performance liquid chromatography (HPLC) with gradient elution method for the determination of tertiary butyl hydroquinone a synthetic antioxidant (TBHQ) in cooking oil after frying repeatedly been studied. Chromatography system using a mobile phase mixture of methanol : acetonitrile : 1% acetic acid were (60:30:10), (60:25:15), (60:20:20) with a flow rate 0,5 mL/min, 1 mL/min and 1,5 mL/min. The optimum conditions obtained at the mobile phase a mixture of methanol : acetonitrile : 1% acetic acid (60:20:20) with a flow rate 0,5 mL/min. This method has a good precision and accuracy with a correlation coefficient 0,998, percent recoveries of 98,8 to 101,1%, the limit of detection (LOD) 7,8 mg/L, the intra-day precision 0,66% and inter-intra-day 0,26 to 0,53%. The results of the analysis in the levels of antioxidants TBHQ in edible oils obtained at 169,07 mg/kg. While the levels of antioxidant TBHQ after frying the first, second and third are 116,23 mg/kg, 101,71 mg/kg and 88,89 mg/kg. This value indicates that the amount of the antioxidant TBHQ were added to the cooking oil is still below the maximum limit according PERMENKES No.1168/Menkes/Per/X/1999.
KATA PENGANTAR
Puji syukur kehadirat Tuhan Yang Maha Esa yang telah melimpahkan rahmat dan
hidayah-Nya sehingga penulis dapat menyelesaikan penelitian dan penulisan tesis
dengan judul “Optimasi Metode Kromatografi Cair Kinerja Tinggi (KCKT) Untuk
Penetapan Kadar Antioksidan Tersier Butil Hidrokuinon (TBHQ)Dalam
MinyakGoreng Setelah Penggorengan Berulang” yang merupakan salah satu syarat
untukmemperolehgelarMagister IlmuKimia pada Fakultas Matematika Dan Ilmu
Pengetahuan Alam Universitas SumateraUtara.
Selama menyelesaiakan penelitian dan penulisan tesis ini penulistelah banyak
mendapatkan bantuandan dorongan dari berbagai pihak, baik moril maupun
materil. Untuk itu penulis ingin menghaturkan penghargaan dan terima kasih yang tak
terhingga kepada Bapak Prof. Dr. dr. Syahril Pasaribu, DMT&H, M.Sc, (CTM),
Sp.A(K) dan Dr. Sutarman, M.Sc selaku Rektor Universitas Sumatera Utara dan
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Sumatera
Utara atas kesempatan dan fasilitas yang diberikan kepada penulis dalam
menyelesaikan pendidikan di Pascasarjana Ilmu Kimia.Bapak Prof. Basuki
Wirjosentono, MS, Ph.D dan Dr. Hamonangan Nainggolan, M.Sc selaku Ketua
Program Studi dan Sekretaris Pascasarjana Ilmu Kimia atas kesempatan yang
diberikan kepada penulis untuk menjadi mahasiswa di Pascasarjana Ilmu Kimia.
Penulis menyampaikan terima kasih kepada Bapak Prof. Dr. Harlem
Marpaung selaku dosen pembimbing I dan Bapak Dr. M. Pandapotan Nasution MPS,
Apt selaku dosen pembimbing II yang telah banyak memberikan bimbingan,arahan,
masukan, saran dan dorongan dengan penuh kesabaran yang tulus dan ikhlas bagi
penulis dalam melakukan penelitian dan penyelesaian tesis ini. Terima kasih penulis
sampaikan kepada Bapak Prof. Basuki Wirjosentono, MS, Ph.D, Bapak Prof. Dr.
dosen penguji yang telah banyak memberikan saran dan masukan bagi penulis dalam
penyelesaian tesis sehingga menjadi semakin baik.
Penulis menyampaikan terima kasih kepada Bapak Drs.W.Purba dan Bapak
Parlidungan Purba SH, MM selaku Ketua dan Pembina Yayasan Sari Mutiara,Ibu
Dr.Ivan Elisabeth Purba M.Kes selaku Rektor Universitas Sari Mutiara Indonesia,
Medan yang telah banyak memberikan kesempatan,fasilitas,dorongan, bimbingan
danarahan kepada penulis untuk dapat mengikuti perkuliahan di Program Studi
Magister Ilmu Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas
Sumatera Utara,Medan.Bapak Dr.Hamonangan Nainggolan M.Sc dan Bapak Ridwan,
M.Si selaku Kepala dan Operator Laboratorium TerpaduFakultas Matematika dan
Ilmu Pengetahuan Alam Universitas Sumatera Utara yang telah banyak memberikan
bantuan, arahan dan saran guna kelancaran dalam penelitian.
Terimakasih untuk Istriku tersayang Rolensa Hutapea, S.Si danAnakku yang
kubanggakan Yosua Torang Nanda Lumbanbatu SE.Ak yang selalu mendoakan dan
berkorban baik moril maupun materil kepada penulis selama menjalani
pendidikan,penelitian dan penyelesaian tesis ini.
Kiranya Tuhan Yang Maha Esa memberikan balasan yang berlipat ganda atas
kebaikan dan bantuan yang telah diberikan kepada penulis.
Akhirnya penulis menyadari bahwa tesis ini masih jauh dari kesempurnaan
oleh karena itu, penulis mengharapankan kritik dan saran yang bersifat membangun
dari semua pihak,semoga tulisan ini dapat menjadi sumbangan yang berarti bagi Ilmu
Pengetahuan Khususnya bagi bidang Ilmu Kimia.
Medan, Juli 2014
Penulis,
DAFTAR RIWAYAT HIDUP
DATA PRIBADI
Nama Lengkap : Jabangun Lumbanbatu
Tempat dan Tanggal Lahir : Dolok Sanggul, 27 Desember 1955 Alamat : Jl. Gaperta Komp. Tosiro No. E-2 Medan
Email/ Hp
Nama Ayah : J. Lumbanbatu (Alm) Nama Ibu : B. Banjarnahor (Alm)
DATA PENDIDIKAN
- Lulus SD Negeri 1122, Bdr. Khalipah, Sergai pada tahun 1968 - Lulus SMP Katholik, T. Tinggi pada tahun 1971
- Lulus SPA (Sekolah Pengatur Analis) DepKes RI pada tahun 1975
- Lulus PAKA (Program Ahli Kimia) Universitas Sumatera Utara, Medan pada tahun 1984
- Lulus Sarjana Biologi (Lingkungan) Universitas Medan Area, Medan pada tahun 1999
DATA PEKERJAAN
- Staff Balai Laboratorium Kesehatan, UPT Dinas Kesehatan Provinsi Sumatera Utara (1977-1999)
- Kepala Seksi Toksikologi dan Kimia Lingkungan Balai Laboratorium Kesehatan, UPT Dinas Kesehatan Provinsi Sumatera Utara(1999-2012)
- Dosen Tetap Universitas Sari Mutiara Indonesia, Medan (2012-Sekarang)
KURSUS, PELATIHAN DAN SEMINAR
- Pelatihan dalam dan luar negeri selama menjadi Staff Balai Laboratorium Kesehatan, UPT Dinas Kesehatan Provinsi Sumatera Utara
DAFTAR ISI
Halaman
ABSTRAK i
ABSTRACT ii
KATA PENGANTAR iii
RIWAYAT HIDUP v
DAFTAR ISI vi
DAFTAR TABEL ix
DAFTAR GAMBAR x
DAFTAR LAMPIRAN xi
BAB 1. PENDAHULUAN
1.1.Latar Belakang 1
1.2. Perumusan Masalah 3
1.3. Tujuan Penelitian 3
1.4. Manfaat Penelitian 4
1.5. Pembatasan Penelitian 4
BAB 2.TINJAUAN PUSTAKA
2.1. Minyak Goreng 6
2.1.1. Sifat fisik minyak 7
2.1.2. Sifat kimia minyak 8
2.1.3. Minyak goreng berulang kali 9
2.1.4. Bahaya minyak goreng berulang bagi kesehatan 10
2.2.Antioksidan 11
2.2.1. Manfaat antioksidan 12
2.2.2. Mekanisme kerja antioksidan 13
2.2.3. Tersier butyl hidrokuinon 14
2.3.Metode analisis antioksidan 14
2.4.Kromatografi Cair Kinerja Tinggi 15
2.4.1. Pemisahan dalam KCKT 16
2.4.2. Parameter penting pada KCKT 18
2.4.2.1. Waktu retensi (tR
2.4.2.2. Faktor Kapasitas (k’) 19
) 18
2.4.2.3.Selektivitas (α) 20
2.4.2.4. Efisiensi Kolom (N) 21
2.4.2.5. Resolusi (Rs) 22
2.4.2.6. Faktor ikutan (Tf) dan faktor asimetri (As
2.4.3. Instrumen KCKT 24
) 22
2.4.3.2. Pompa 25
2.4.3.3. Injector 25
2.4.3.4. Kolom 26
2.4.3.5. Detektor 26
2.4.3.6. Perekam atau rekorder 27
2.5. Validasi Metode 27
2.5.1. Linearitas 27
2.5.2. Akurasi (kecermatan) 28
2.5.3. Presisi (keseksamaan) 28
2.5.4. Batas deteksi dan batas kuantitasi (LOD dan LOQ) 28
2.5.5Selektifitas (spesifisitas) 29
2.5.6. Rentangan (kisaran) 29
2.5.7. Kekuatan (ketahanan) 30
2.5.8. Kekasaran (Ketangguhan) 30
BAB 3. METODOLOGI PENELITIAN
3.1. Alat 31
3.2. Bahan 31
3.3. Prosedur Penelitian 31
3.3.1. Preparasi sampel 31
3.3.2. Penyiapan larutan standar TBHQ 32
3.3.3. Optimasi sistem KCKT 32
3.3.4. Validasi metode KCKT 32
3.3.4.1. Ujilinieritas 32
3.3.4.2. Uji akurasi 33
3.3.4.3. Ujipresisi 33
3.3.4.4. Penentuan limit deteksi 34
3.3.4.5. Penetapan kadar TBHQ 34
3.4. Bagan Penelitian 36
3.4.1. Preparasi sampelminyak goreng 36
3.4.2. Optimasi sistem KCKT 37
3.4.3. Penetapan kadar TBHQ dalam minyak goreng 38
BAB 4. HASIL DAN PEMBAHASAN
4.1. Optimasi sistem KCKT 39
4.2. Validasi metode KCKT 43
4.2.1. Ujilinieritas 43
4.2.2. Ujiakurasi 44
4.2.3. Uji presisi 45
4.2.4. Penentuan limit deteksi (LOD) 47
BAB 5. KESIMPULAN DAN SARAN
5.1. Kesimpulan 51
5.2. Saran 51
DAFTAR PUSTAKA 52
DAFTAR TABEL
Nomor Judul Halaman
Tabel 2.1 Standar mutu minyak goreng 7
Tabel 3.1 Perbandingan komposisi campuran fasa gerak 32
Tabe l 4.1 Data waktu retensi dan luas area tersier butil hidrokuinon (TBHQ)konsentrasi 50 ppm menggunakan komposisi fasa gerak (60:20:20); (60:25:15); (60:30:10) dengan laju alir 0,5; 1,0; 1,5
mL/menit 39
Tabel 4.2 Hasil analisis persen perolehan kembali
antioksidanTBHQ dalam minyak 44
Tabel 4.3 Hasil analisis kadar antioks idan TBHQ pada uji
intra-day 45
Tabel 4.4 Hasil analisis kadar antioks idan TBHQ pada uji
intra-day (hari ke-1) 46
Tabel 4.5 Hasil analisis kadar antioksidan TBHQ pada uji
intra-day (hari ke-2) 46
Tabel 4.6 Hasil analisis kadar antioksidan TBHQ pada uji
intra-day(hari ke-3) 47
Tabel 4.7 Hasil analisis limit deteksi (LOD) metode KCKT 48
DAFTAR GAMBAR
Nomor Judul Halaman
Gambar 2.1 Strukt ur TBHQ 14
Gambar 2.2 Ilustrasi proses pemisahan yang terjadi didalam kolom
kromatografi cair kinerja tinggi 17
Gambar 2.3 Kromatogram puncak tunggal yang diperoleh dari
analisis KCKT 18
Gambar 2.4 Kromatogram dua puncak yang diperoleh dari analisis
KCKT 19
Gambar 2.5 Kromatogram hasil analisis kromatografi cair kinerja
tinggi engan berbagai selektifitas dan efisiensi 21
Gambar 2.6 Bentuk p uncak k romatogram 23
Gambar 2.7 Pengukuran derajat asimetris puncak 24
Gambar 2.8 Instrumen dasar KCKT 25
Gambar 4.1 Kromatogram hasil penyuntikan larutan standar TBHQ 50 ppm dengan laju alir 0,5 mL/menit menggunakan komposisi fasa gerakmetanol : asetonitril : asam asetat 1% (a) 60:20:20; (b) 60:25:15
dan (c) 60:30:10 41
Gambar 4.2 Kromatogram hasil penyuntikan larutan standar TBHQ 50 ppm dengan laju alir 1,0 mL/menit menggunakan komposisi fasa gerakmetanol : asetonitril : asam asetat 1% (a) 60:20:20; (b) 60:25:15
dan (c) 60:30:10 41
Gambar 4.3 Kromatogram hasil penyuntikan larutan standar TBHQ 50 ppm dengan laju alir 1,5 mL/menit menggunakan komposisi fasa gerakmetanol : asetonitril : asam asetat 1% (a) 60:20:20; (b) 60:25:15
dan (c) 60:30:10 42
Gambar 4.4 Kurva kalibrasi antioksidan TBHQ 44
DAFTAR LAMPIRAN
Nomor Judul Halaman
Lampiran A1 Kromatogram hasil penyuntikan larutan standar TBHQ 50 ppm yang dianalisa secara KCKT menggunakan kolom C18 (3,9x150 mm); detektor UV (280 nm); suhu kolom 30oC; fasa gerak campuran metanol : asetonitril : asam
asetat 1% (60:30:10) dan laju alir 0,5 mL/menit 58
Lampiran A2 Kromatogram hasil penyuntikan larutan standar TBHQ 50 ppm yang dianalisa secara KCKT menggunakan kolom C18 (3,9x150 mm); detektor UV (280 nm); suhu kolom 30oC; fasa gerak campuran metanol : asetonitril : asam
asetat 1% (60:30:10) dan laju alir 1 mL/menit 59
Lampiran A3 Kromatogram hasil penyuntikan larutan standar TBHQ50 ppm yang dianalisa secara KCKT menggunakan kolom C18 (3,9x150 mm); detektor UV (280 nm); suhu kolom 30oC; fasa gerak campuran metanol : asetonitril : asam
asetat 1% (60:30:10) dan laju alir 1,5 mL/menit 60
Lampiran A4 Kromatogram hasil penyuntikan larutan standar TBHQ 50 ppm yang dianalisa secara KCKT menggunakan kolom C18 (3,9x150 mm); detektor UV (280 nm); suhu kolom 30oC; fasa gerak campuran metanol : asetonitril : asam
asetat 1% (60:25:15) dan laju alir 0,5 mL/menit 61
Lampiran A5 Kromatogram hasil penyuntikan larutan standar TBHQ 50 ppm yang dianalisa secara KCKT menggunakan kolom C18 (3,9x150 mm); detektor UV (280 nm); suhu kolom 30oC; fasa gerak campuran metanol : asetonitril : asam
Lampiran A6 Kromatogram hasil penyuntikan larutan standar TBHQ 50 ppm yang dianalisa secara KCKT menggunakan kolom C18 (3,9x150 mm); detektor UV (280 nm); suhu kolom 30o
63 C; fasa gerak campuran metanol :
asetonitril : asam asetat 1% (60:25:15) dan laju alir 1,5 mL/menit
Lampiran A7 Kromatogram hasil penyuntikan larutan standar TBHQ 50 ppm yang dianalisa secara KCKT menggunakan kolom C18 (3,9x150 mm); detektor UV (280 nm); suhu kolom 30o
64 C; fasa gerak campuran metanol :
asetonitril : asam asetat 1% (60:20:20) dan laju alir 0,5 mL/menit
Lampiran A8 Kromatogram hasil penyuntikan larutan standar TBHQ 50 ppm yang dianalisa secara KCKT menggunakan kolom C18 (3,9x150 mm); detektor UV (280 nm); suhu kolom 30o
65 C; fasa gerak campuran metanol :
asetonitril : asam asetat 1% (60:20:20) dan laju alir 1 mL/menit
Lampiran A9 Kromatogram hasil penyuntikan larutan standar TBHQ 50 ppm yang dianalisa secara KCKT menggunakan kolom C18 (3,9x150 mm); detektor UV (280 nm); suhu kolom 30o
66 C; fasa gerak campuran metanol :
asetonitril : asam asetat 1% (60:20:20) dan laju alir 1,5 mL/menit
Lampiran B1 Kromatogram hasil penyuntikan larutan standar TBHQ 10 ppm yang dianalisa secara KCKT menggunakan kolom C18 (3,9x150 mm); detektor UV (280 nm); suhu kolom 30o
67 C; fasa gerak campuran metanol :
Lampiran B2 Kromatogram hasil penyuntikan larutan standar TBHQ 25 ppm yang dianalisa secara KCKT menggunakan kolom C18 (3,9x150 mm); detektor UV (280 nm); suhu kolom 30o
67 C; fasa gerak campuran metanol :
asetonitril : asam asetat 1% (60:20:20) dengan laju alir 0,5 mL/menit
Lampiran B3 Kromatogram hasil penyuntikan larutan standar TBHQ 50 ppm yang dianalisa secara KCKT menggunakan kolom C18 (3,9x150 mm); detektor UV (280 nm); suhu kolom 30oC; fasa gerak campuran metanol : asetonitril : asam asetat 1% (60:20:20) dengan laju alir 0,5 mL/menit
68 Lampiran B4 Kromatogram hasil penyuntikan larutan
standar TBHQ 100 ppm yang dianalisa secara KCKT menggunakan kolom C18 (3,9x150 mm); detektor UV (280 nm); suhu kolom 30oC; fasa gerak campuran metanol : asetonitril : asam asetat 1% (60:20:20) dengan laju alir0,5 mL/menit
68 Lampiran B5 Kromatogram hasil penyuntikan larutan
standar TBHQ 150 ppm yang dianalisa secara KCKT menggunakan kolom C18 (3,9x150 mm); detektor UV (280 nm); suhu kolom 30oC; fasa gerak campuran metanol : asetonitril : asam asetat 1% (60:20:20) dengan laju alir 0,5 mL/menit
69 Lampiran B6 Kromatogram hasil penyuntikan larutan
standar TBHQ 200 ppm yang dianalisa secara KCKT menggunakan kolom C18 (3,9x150 mm); detektor UV (280 nm); suhu kolom 30oC; fasa gerak campuran metanol : asetonitril : asam asetat 1% (60:20:20) dengan laju alir 0,5 mL/menit
69
Lampiran B7 Kromatogram hasil penyuntikan larutan standar TBHQ 250 ppm yang dianalisa secara KCKT menggunakan kolom C18 (3,9x150 mm); detektor UV (280 nm); suhu kolom 30oC; fasa gerak campuran metanol : asetonitril : asam asetat 1% (60:20:20) dengan laju alir 0,5 mL/menit
70
Lampiran C1 Kromatogram antioksidan TBHQ dalam minyak goreng (sampel A) dengan fasa gerak campuran metanol : asetonitril : asam asetat 1% (60:20:20)dan laju alir 0,5 mL/menit
71 Lampiran C2 Kromatogram antioksidan TBHQ di dalam
minyak goreng setelah penggorengan pertama (sampel B) dengan fasa gerak campuran metanol : asetonitril : asam asetat 1% (60:20:20) dan laju alir 0,5 mL/menit
72 Lampiran C3 Kromatogram antioksidan TBHQ di dalam
minyak goreng setelah penggorengan kedua (sampel C) dengan fasa gerak campuran metanol : asetonitril : asam asetat 1% (60:20:20) dan laju alir 0,5 mL/menit
73 Lampiran C4 Kromatogram antioksidan TBHQ di dalam
minyak goreng setelah penggorengan ketiga (sampel D) dengan fasa gerak campuran metanol : asetonitril : asam asetat 1% (60:20:20) dan laju alir 0,5 mL/menit
74 Lampiran D1 Kromatogram hasil persen perolehan kembali
pada penambahan antioksidan TBHQ 50 ppm yang dianalisa secara KCKT menggunakan kolom C18 (3,9x150 mm); detektor UV (280 nm); suhu kolom 30o
75 C; fasa gerak campuran
metanol : asetonitril : asam asetat 1% (60:20:20) dengan laju alir 0,5 mL/menit
Lampiran D2 Kromatogram hasil persen perolehan kembali pada penambahan antioksidan TBHQ 100 ppm yang dianalisa secara KCKT menggunakan kolom C18 (3,9x150 mm); detektor UV (280 nm); suhu kolom 30o
76 C; fasa
gerak campuran metanol : asetonitril : asam asetat 1% (60:20:20) dengan laju alir 0,5 mL/menit
Lampiran D3 Kromatogram hasil persen perolehan kembali pada penambahan antioksidan TBHQ 150 ppm yang dianalisa secara KCKT menggunakan kolom C18 (3,9x150 mm); detektor UV (280 nm); suhu kolom 30o
77 C; fasa
gerak campuran metanol : asetonitril : asam asetat 1% (60:20:20) dengan laju alir 0,5 mL/menit
Lampiran D4 Kromatogram hasil persen perolehan kembali pada penambahan antioksidan TBHQ 200 ppm yang dianalisa secara KCKT menggunakan kolom C18 (3,9x150 mm); detektor UV (280 nm); suhu kolom 30oC; fasa gerak campuran metanol : asetonitril : asam asetat 1% (60:20:20) dengan laju alir 0,5
mL/menit 78
Lampiran E1 Sertifikat antioksidan Tersier Butil
Hidrokuinon(TBHQ) 79
Lampiran F1 AntioksidanTersier Butil Hidrokuinon
(TBHQ) 80
Lampiran F2 Proses persiapan sampel minyak goreng
sebelum dan setelah penggorengan berulang 80
Lampiran F3 Sampel minyak goreng sebelum dan setelah
penggorengan berulang kali 80
Lampiran F4 Sentrifuge (Thermo biofuge primo R) 81
Lampiran F5 Rotary Evaporator Vacum
(BUCHIR210/R215) 81
Lampiran F6 Proses ekstaksi sampel menggunakan
pengocok vortex mixer (fisher scientific) 81
Lampiran F7 Analisis sampel menggunakanHPLC Waters
510 Pump 82
Lampiran G1 Kurva kalibrasi TBHQ 83
Lampiran G2 Contoh perhitungan kadar antioksidan TBHQ 83
Lampiran G3 Contoh perhitungan persen perolehan kembali 84
Lampiran G4 Contoh perhitungan presisi (keseksamaan)
intra-daydan inter-day 84
Lampiran G5 Contoh perhitungan limit deteksi (LOD) 85
OPTIMASI METODE KROMATOGRAFI CAIR KINERJA TINGGI (KCKT) UNTUK PENETAPAN KADAR ANTIOKSIDAN TERSIER BUTIL
HIDROKUINON (TBHQ) DALAM MINYAK GORENG SETELAH PENGGORENGAN BERULANG
ABSTRAK
Kromatografi cair kinerja tinggi (KCKT) dengan metode elusi gradien untuk penentuan kadar antioksidan sintetik tertier butil hidrokuinon (TBHQ) dalam minyak goreng setelah penggorengan berulang telah dipelajari. Sistem kromatografi menggunakan fasa gerak campuran metanol : asetonitril : asam asetat 1% (60:30:10), (60:25:15), (60:20:20) dengan laju alir 0,5 mL/menit, 1 mL/menit dan 1,5 mL/menit. Kondisi optimum diperoleh pada fasa gerak campuran metanol : asetonitril : asam asetat 1% (60:20:20) dengan laju alir 0,5 mL/menit. Metode ini memiliki presisi dan akurasi yang baik dengan nilai koefisien korelasi sebesar 0,998, persen perolehan kembali sebesar 98,8-101,1%, limit deteksi (LOD) sebesar 7.8 mg/L, keseksamaan
intra-day sebesar 0,66% dan inter-day sebesar 0,26-0,53%. Hasil analisis kadar antioksidan TBHQ di dalam dalam minyak goreng diperoleh sebesar 169,07 mg/kg. Sedangkan kadar antioksidan TBHQ setelah penggorengan pertama, kedua dan ketiga yaitu 116,23 mg/kg, 101,71 mg/kg dan 88,89 mg/kg. Nilai ini menunjukkan bahwa jumlah antioksidan TBHQ yang ditambahkan ke dalam minyak goreng masih berada di bawah batas maksimum menurut PERMENKES No.1168/MenKes/Per/X/1999.
OPTIMIZATION OF HIGH PERFORMANCE LIQUID CHROMATOGRAPHY (HPLC) METHOD FOR DETERMINATION OF TERTIARY BUTYL
HYDROQUINONE (TBHQ) ANTIOXIDANT LEVEL IN COOKING OIL AFTER REPEATED FRYING
ABSTRACT
High performance liquid chromatography (HPLC) with gradient elution method for the determination of tertiary butyl hydroquinone a synthetic antioxidant (TBHQ) in cooking oil after frying repeatedly been studied. Chromatography system using a mobile phase mixture of methanol : acetonitrile : 1% acetic acid were (60:30:10), (60:25:15), (60:20:20) with a flow rate 0,5 mL/min, 1 mL/min and 1,5 mL/min. The optimum conditions obtained at the mobile phase a mixture of methanol : acetonitrile : 1% acetic acid (60:20:20) with a flow rate 0,5 mL/min. This method has a good precision and accuracy with a correlation coefficient 0,998, percent recoveries of 98,8 to 101,1%, the limit of detection (LOD) 7,8 mg/L, the intra-day precision 0,66% and inter-intra-day 0,26 to 0,53%. The results of the analysis in the levels of antioxidants TBHQ in edible oils obtained at 169,07 mg/kg. While the levels of antioxidant TBHQ after frying the first, second and third are 116,23 mg/kg, 101,71 mg/kg and 88,89 mg/kg. This value indicates that the amount of the antioxidant TBHQ were added to the cooking oil is still below the maximum limit according PERMENKES No.1168/Menkes/Per/X/1999.
BAB 1
PENDAHULUAN
1.1Latar Belakang
Minyak goreng merupakan salah satu kebutuhan pokok manusia yang berfungsi
sebagai media dalam pengolahan bahan pangan. Selain dapat memperbaiki struktur
fisik dari bahan pangan yang digoreng, minyak goreng dapat menambah nilai gizi dan
nilai kalori serta memberikan citarasa yang khas dari bahan pangan.Oleh karena itu,
penggorengan dengan minyak goreng lebih banyak dipilih sebagai cara dalam
pengolahan makanan.
Dalam penggunaannya, minyak goreng sering dipakai untuk menggoreng
secara berulang-ulang. Penggunaan minyak goreng secara berulang-ulang akan
menyebabkan kerusakan pada minyak goreng.Ketaren (1986) mengungkapkan bahwa
minyak yang dipanaskan berulang-ulang pada suhu tinggi dan dalam waktu yang
cukup lama maka, akan menghasilkan senyawa polimer yang berbentuk padat dalam
minyak.Selain itu, adanya pemanasan berulang-ulang menyebabkan oksidasi asam
lemak tak jenuh yang kemudian membentuk gugus peroksida dan monomer siklik.
Hal ini dapat menimbulkan dampak negatif bagi yang mengkonsumsinya, yaitu
menyebabkan berbagai gejala keracunan (Ketaren, 1986). Beberapa penelitijuga
melaporkan bahwa konsumsi minyak goreng pemakaian berulang dapat menimbulkan
kerusakan karbohidrat, protein, peroksidasi lemak, kerusakan membran sel hingga
kerusakan DNA (Reynertson, 2007; Dorffman dkk, 2009).
Perlindungan terhadap kerusakan termal dan oksidatif minyak dapat dilakukan
dengan menambahkan antioksidan sintetik,salah satunya yaitu tersier butil
hidrokuinon (TBHQ)(Sanhuezadkk,2000; Aluyor dan Ori-Jesu, 2008; Pimpa dkk,
2009; Ryu, 2009; Hossain dkk, 2013; Banu dan Prasad, 2013). Meskipun antioksidan
memiliki peran penting dalam menjagakualitas minyak,penggunaan antioksidan
E
Berdasarkan Peraturan Menteri Kesehatan No.1168/MenKes/Per/X/1999 tentang
Bahan Tambahan Makanan, kadar antioksidan TBHQ yang diperbolehkan dalam
makanan yaitu 200 mg/kg. Sedangkan menurut WHO (1999) nilai Acceptable Daily
Intake (ADI) dari antioksidan TBHQ yaitu 0-0,2 mg/kg berat badan.
fektivitas antioksidan bervariasi tergantung pada makanan, kondisi
pengolahan dan penyimpanan. Antioksidan TBHQ menjadi kurang efektif dalam
memberikan perlindungan terhadap minyak akibat terdekomposisi dan hilang melalui
penguapan selama penggorengan (Hammama dan Nawar, 1991; Tyagi dan
Vasishtha,1996; Allam dan Mohamed, 2002; Marmesat dkk, 2010; Reda, 2011).Oleh
karena itu, pemantauan kadar antioksidan dalam minyak setelah penggorengan
Kromatografi cair kinerja tinggi (KCKT) merupakan metode yang sering
digunakan dalam analisis antioksidan sintetik karena sifatnya yang fleksibel dan
memiliki presisi dan sensitivitas yang baik (Karovicova dan Simko, 2000). Penetapan
kadar antioksidan TBHQ dalam minyak goreng menggunakan metode KCKT telah
banyak dilaporkan (Chaerianisa, 2012; Xiu-Qin dkk, 2009; Saad dkk, 2011; Xijin dan
Zhicai, 2011). Akhir-akhir ini, beberapa peneliti juga telah melakukan pengembangan
metode KCKT dengan cara optimasi untuk meningkatkan kinerja dari kromatografi.
Menurut Kromidas (2006) optimasi yang paling sederhana dan sering dilakukan yaitu
terhadap perbandingan fasa gerak dan laju alir. penting untuk dilakukan.
Tanuwijaya(2007)melaporkan bahwa kadar antioksidan TBHQ, BHA dan BHT
dalam mie instan yang ditetapkandengan metode KCKT pada optimasifasa gerak
metanol: asetonitril : asam asetat 1% (60 : 20 : 20),(60 : 25 : 15) dan (60 : 30 : 10)
denganlaju alir 1 mL/menit yaitusebesar 1,37-1,44 µg/gram mie instan. Selain itu, nilai
perolehan kembaliantioksidan TBHQ yaitu sebesar 93,8-98,3%, BHA sebesar
87,2-98,3% dan BHT sebesar 76,2-92,3% dengan batas deteksi masing-masing sebesar0,99
Berdasarkan uraian diatas, maka penulis tertarik untuk melakukan optimasi
metode KCKT untuk penetapan kadar antioksidan TBHQ dalam minyak goreng
setelah penggorengan berulang. Mengingat, kajian tentang penetapan kadar
antioksidan TBHQ dalam minyak setelah penggorengan berulang belum dilakukan.
Syarat pemilihan utama setelah memilih metode HPLC yang sesuai adalah
menentukan sistem pelarut untuk analisa. Kriteria pemilihan melibatkan waktu
analisa, efisiensi keseluruhan dan resolusi. Selain itu, percepatan aliran fasa gerak
akan memainkan peranan dalam parameter ini. Oleh karena itu, pada penelitian ini
akan dilakukan optimasi fasa gerak metanol : asetonitril : asam asetat 1%dengan
variasi perbandingan (60:20:20), (60:25:15) dan (60:30 :10) dengan laju alir yang berbeda
yaitu 0,5 mL/menit, 1mL/menit dan 1,5 mL/menit. Kondisi optimum yang diperoleh
selanjutnya digunakan untuk penetapan kadar antioksidan TBHQ dalam minyak
setelah penggorengan berulang. Untuk uji validasi metode KCKT, dilakukan uji
linieritas, uji akurasi (kecermatan) dengan parameter persen perolehan kembali
(80-120%), uji presisi (keseksamaan) dengan parameter simpangan baku relatif (RSD ≤
2%) dan limit deteksi (LOD).
1.2 Perumusan Masalah
1. Bagaimana metode KCKT dapat digunakan untuk penetapan kadar
antioksidan dalam minyak goreng sebelum dan setelah penggorengan
berulang.
2. Apakah optimasi metode KCKT pada penetapan kadar antioksidan TBHQ
dalam minyak goreng sebelum dan setelah penggorengan berulang memenuhi
persyaratan uji validasi.
3. Apakah kadar antioksidan TBHQ dalam minyak goreng sebelum dan setelah
penggorengan berulang memenuhi persyaratan Peraturan Menteri Kesehatan
1.3 Tujuan Penelitian
1. Menentukan kondisi optimum untuk analisis kadar antioksidan TBHQ dalam
minyakgoreng sebelum dan setelah penggorengan berulang
2. Melakukan validasi metode analisis KCKT pada penetapan kadar antioksidan
TBHQ dalam minyak gorengsebelum dan setelah penggorengan berulang.
3. Mengevaluasi kadar antioksidan TBHQ dalam minyak goreng sebelum dan
setelah penggorengan berulang dengan Keputusan Menteri Kesehatan
No.1168 /MenKes/Per/X/1999 tentang Bahan Tambahan Makanan.
1.4 Manfaat Penelitian
Penelitian ini bermanfaat dalam mengembangkan metode alternatif untuk
menciptakan kondisi kromatografi yang optimum pada penetapan kadar antioksidan
TBHQ dalam minyak goreng. Penelitian ini juga diharapkan dapat memberikan
informasi kepada masyarakat sebagai konsumen mengenai kadar antioksidan dalam
produk minyak goreng komeril sebelum dan setelah penggorengan berulang.
Sehingga, masyarakat dapat lebih berhati-hati dalam memilih produk pangan yang
aman untuk dikonsumsi.
1.5 Pembatasan Penelitian :
Penelitian dilaksanakan mengunakan dua variable, yaitu:
1. Variabel bebas:
- Perbandingan komposisi fase gerak
Metanol : Acetonitril : Asam asetat 1%
60 : 20 : 20
60 : 25 : 15
60 : 30 : 10
- Laju alir fase gerak : 0,5 mL/menit, 1 mL/menit dan 1,5 mL/menit
2. Variabel tetap:
- Detektor UV (280 nm)
- Tekanan ≤ 200 bar
- Suhu oven kolom 30o
- Uji validasi metode KCKT yaitu:linieritas, akurasi (kecermatan), presisi
BAB 2
TINJAUAN PUSTAKA
2.1 Minyak Goreng
Minyak goreng merupakan minyak yang telah mengalami proses pemurnian yang
meliputi degumming, netralisasi, pemucatan dan deodorisasi (Sugiati, 2007).
Sedangkan menurut SNI (2013) minyak goreng adalah bahan pangan dengan
komposisi utama trigliserida yang berasal dari bahan nabati dengan atau tanpa
perubahan kimiawi termasuk hidrogenasi, pendinginan dan telah melalui proses
rafinasi atau pemurnian yang digunakan untuk menggoreng. Minyak goreng
berfungsi sebagai penghantar panas, penambah rasa gurih dan penambah nilai kalori
bahan pangan (Ketaren, 1986).
Di Indonesia minyak pangan yang banyak digunakan adalah minyak nabati.
Secara umum, di pasaran ditawarkan dua macam minyak goreng yaitu minyak goreng
yang berasal dari tumbuhan (minyak nabati) dan minyak goreng yang berasal dari
hewan yang terkenal tallow(minyak atau lemak berasal dari sapi) dan lard(minyak
atau lemak berasal dari babi). Minyak goreng nabati contohnya minyak sawit, minyak
kelapa, minyak jagung, minyak kedelai, minyak zaitun dan lain-lain.
Mutu minyak goreng ditentukan oleh titik asapnya, yaitu suhu pemanasan
minyak sampai terbentuk akreolein yang tidak diinginkan dan dapat menimbulkan
rasa gatal pada tenggorokan hidrasi gliserol akan membentuk aldehida tidak jenuh
atau akrelein tersebut. Makin tinggi titik asap, makin baik mutu minyak goreng itu.
Titik asap suatu minyak goreng tergantung dari kadar gliserol bebas. Lemak yang
telah digunakan untuk menggoreng titik asapnya akan turun, karena telah terjadi
hidrolisis molekul lemak. Oleh karena itu untuk menekan terjadinya hidrolisis,
pemanasan lemak atau minyak sebaiknya dilakukan pada suhu yang tidak terlalu
tinggi dari seharusnya (Winarno, 2004).Standar mutu minyak goreng menurut
Tabel 2.1.Standar mutu minyak goreng
Kriteria uji Satuan Syarat
Keadaan bau, warna dan rasa - Normal
Air % b/b Maks 0.30
Asam lemak bebas
(dihitung sebagai asam laurat)
% b/b Maks 0,30
Bahan Makanan Tambahan Sesuai SNI.022-M dan Permenkes
No.722/Menkses/Per/IX/88
Catatan *dalam kemasan kaleng
Sumber: Standar Nasional Indonesia 01-3741-2002
2.1.1Sifat fisik minyak
Minyak memiliki beberapa sifat fisik yang dapat membedakan minyak dengan lemak
atau senyawa lainnya, diantaranya:
- Warna, terdiri dari 2 golongan, golongan pertama yaitu zat warna alamiah,
golongan ini secara alamiah terdapat dalam bahan yang mengandung minyak dan
ikut terekstrak bersama minyak pada proses ekstrasi. Zat warna tersebut antara lain
α dan β karoten (berwarna kuning), xantofil (berwarna kuning kecoklatan), klorofil (berwarna kehijauan) dan antosianin (berwarna kemerahan).Golongan kedua yaitu
zat warna dari hasil degradasi zat warna alamiah, yaitu warna gelap disebabkan
oleh bahan untuk membuat minyak yang telah busuk atau rusak, warna kuning
umumnya terjadi pada minyak tidak jenuh.
- Kelarutan, minyak tidak larut dalam air kecuali minyak jarak (castor oil), dan
minyak sedikit larut dalam alkohol, etil eter, karbon disulfida dan pelarut halogen.
- Titik didih (boiling point) akan semakin meningkat dengan bertambah panjangnya
rantai karbon asam lemak tersebut.
2.1.2 Sifat kimia minyak
Dalam minyak, terdapat beberapa proses kimia yang dapat terjadi akibat adanya
interaksi antara struktur kimia yang dimiliki oleh minyak dan lingkungannya yaitu:
- Hidrolisa, dalam reaksi hidrolisa minyak akan diubah menjadi asam lemak bebas
dan gliserol. Reaksi hidrolisa yang dapat menyebabkan kerusakan minyak atau
lemak terjadi karena terdapatnya sejumlah air dalam minyak tersebut.
- Oksidasi, proses oksidasi berlangsung bila terjadi kontak antara sejumlah oksigen
dengan minyak. Terjadinya reaksi oksidasi akan mengakibatkan bau tengik pada
minyak dan lemak.Menurut Smith (1991) mekanisme oksidasi pada umumnya
terdiri dari tiga tahap utama, yaitu inisiasi, propagasi dan terminasi. Pada tahap
inisiasi terjadi pembentukan radikal bebas lemak (R•), yaitu suatu senyawa yang
bersifat tidak stabil dan sangat reaktif akibat dari hilangnya satu atom hidrogen
(persamaan 1). Tahap ini berlangsung lambat dan terjadi karena adanya cahaya
atau logam. Pada tahap propagasi, radikal lemak akan bereaksi dengan oksigen
membentuk radikal peroksida (ROO•). Radikal peroksida selanjutnya akan
menyerang molekul lemak lain (RH) menghasilkan hidroperoksida (ROOH) dan
radikal lemak baru (persamaan 2 dan 3). Tahap ini merupakan reaksi rantai yang
berlangsung sangat cepat. Hidroperoksida yang terbentuk bersifat tidak stabil dan
akan terdegradasi menjadi senyawa-senyawa seperti aldehida, keton dan asam
yang menyebabkan bau serta rasa tengik. Reaksi oksidasi akan berakhir pada tahap
terminasi, yaitu melalui reaksi antar radikal bebas (persamaan 4).
Propagasi : R• + O2 → ROO• (2)
Faktor-faktor yang dapat memicu terjadinya oksidasi antara lain panas, cahaya,
logam, suasana basa, derajat ketidakjenuhan, pigmen dan oksigen
- Hidrogenasi, proses hidrogenasi bertujuan untuk menumbuhkan ikatan rangkap
dari rantai karbon asam lemak pada minyak.
- Esterifikasi, proses esterifikasi bertujuan untuk mengubah asam-asam lemak dari
trigliserida dalam bentuk ester. Dengan menggunakan prinsip reaksi ini
hidrokarbon rantai pendek dalam asam lemak yang menyebabkan bau tidak enak
dapat ditukar dengan rantai panjang yangbersifat tidak menguap.
2.1.3Minyak goreng berulang kali
Minyak goreng berulang kali adalah minyak limbah yang bisa berasal dari jenis-jenis
minyak goreng seperti halnya minyak jagung, minyak sayur, minyak samin dan
sebagainya.Minyak ini merupakan minyak bekas pemakaian kebutuhan rumah
tanggaumumnya,dapat di gunakan kembali untuk keperluaran kuliner. Akan tetapi
bila ditinjau dari komposisi kimianya,minyak goreng berulangkali mengandung
senyawa-senyawa yang bersifat karsinogenik yang terbentuk selama proses
penggorengan (Raharjo, 2009).
Penggunaan yang lama dan berkali-kalidapat menyebabkan ikatan rangkap
pada minyak teroksidasi sehingga membentuk gugusperoksida dan monomer
siklik.Awal dari kerusakan minyak goreng adalahterbentuknya akrolein pada minyak
goreng. Akrolein ini menyebabkanrasagatal pada tenggorokan pada saat
Minyak goreng berulang kali atau yang disebut minyak jelantah telah
mengalami penguraian molekul-molekul, sehingga titik asapnya turun drastis dan
biladisimpan dapat menyebabkan minyak menjadi berbautengik. Bau tengik dapat
terjadi karena penyimpanan yang salah dalam jangka waktu tertentu menyebabkan
pecahnya ikatan trigliserida menjadi gliserol dan FFA (free fatty acid) atau asam
lemak jenuh (Ketaren, 2005).Semakin sering digunakan tingkat kerusakan minyak
akan semakin tinggi. Penggunaan minyak berkali-kali akan meningkatkan perubahan
warna menjadi coklat sampai kehitam-hitaman pada minyak tersebut.
2.1.4 Bahaya minyak goreng berulangkali bagi kesehatan
Pemakaian minyak goreng berulang sampai dua kali masih dapat ditoleransi, namun
jika lebih dari dua kali, terlebih jika warnanya sudah berubah menjadi
kehitam-hitaman, maka minyak tersebut sudah tidak baik dan harus dihindarkan (Ketaren,
2005). Penggunaan minyak goreng secara berulang dapatmembahayakan kesehatan
tubuh. Hal tersebut dikarenakan pada saat pemanasan akan terjadi proses degradasi,
oksidasi dan dehidrasi dari minyak goreng. Proses tersebut dapat membentuk radikal
bebas dan senyawa toksik yang bersifat racun,sehingga membahayakan tubuh
(Pangkahila, 2011).
Minyak goreng berulang, khususnya yang dihasilkan dari proses deep
fryingmerupakan radikal bebas dari luar tubuh (eksogen) yang dapat memicu
terjadinya stres oksidatif di dalam tubuh dan menimbulkan kerusakan karbohidrat,
protein, peroksidasi lipid, kerusakan membran sel hingga kerusakan DNA
(Deoxyribo- Nucleic Acid) (Reynertson, 2007; Dorffman dkk, 2009; Arief, 2009).
Stres oksidatif yang berlangsung terus menerus dapat mempercepat penuaan dan
menyebabkan timbulnya penyakit degeneratif, inflamasi, aterosklerosis dan kanker).
Hasil kajian dari Badan Pengawasan Obat dan Makanan (Badan POM)
menemukan bahwa penggunaan minyak goreng berulang berdampak pada kesehatan.
Pemanasan minyak goreng berkali - kali (lebih dari dua kali) pada suhu tinggi akan
Density Lipoproteins (LDL), trigliserida, dan insulin, serta menurunkan High Density
Lipoproteins(HDL) di dalam darah (Dhaka dkk, 2011; Wahab dkk, 2011).
Beberapa studi pada tikus juga menunjukkan bahwa pemberian diet
tinggilemak trans menyebabkan terjadinya resistensi insulin, peningkatan berat
badan, lemak abdominal, lemak subkutaneus, dan terutama akumulasi trigliserida
pada organ hati karena terjadi penurunan oksidasi lipid dan peningkatan sintesis asam
lemak bebas. Hal ini dapat memicu terjadinya obesitas, sindrom metabolik, steatosis
hepatik, dan lipotoksisitas (toksisitas sel akibat akumulasi abnormal lemak)
(Kavanagh dkk, 2007; Dorfman dkk, 2009).
Percobaan yang dilakukan Machado dkk (2010) dengan menggunakan tikus
percobaan yang diberi diet asam lemak trans, PUFA dan SFAditemukan bahwa asam
lemak trans mendorong perubahan yang mirip dengan sindrom metabolik pada
manusia. Asupan asam lemak trans menginduksi akumulasi lemak di hati yang
kemudian memicu terjadinya NASH. Selain itu, Siagian dkk (2002) menyimpulkan
bahwa pemberian per oral minyak kelapa bekas gorengan yang dipanaskan
berulangkali terhadap mencit galur Swiss dapat menimbulkan kongesti hati,
perlemakan dan nekrosis hati.
2.2 Antioksidan
Antioksidan adalah senyawa yang ditambahkan dalam jumlah kecil ke dalam
senyawa senyawa yang bersifat tidak jenuh, terutama lemak dan minyak untuk
memperlambat proses oksidasi. Suatu senyawa untuk dapat digunakan sebagai
antioksidan harus mempunyai sifat dapat membentuk radikal bebas dengan cepat
(menyumbangkan atom hidrogen lebih cepat daripada molekul lemak) dan dapat
terkonsentrasi pada permukaan atau lapisan lemak (bersifat lipofilik).Selain itu, untuk
antioksidan dalam makanan harus tahan pada kondisi pengolahan makanan (Cahyadi,
2006).
tentang perkembangan senyawa berkhasiat antioksidan telah banyak dikembangkan
baik senyawa alam maupun senyawa sintetis. Berdasarkan asalnya, antioksidan dapat
dibagi menjadi antioksidan alami dan sintetik (Ketaren, 1986). Antioksidan alami
antara lain: tokoferol, asam askorbat, flavonoid dan β-karoten.Sedangkan antioksidan sintetik yaitu BHA (Butil Hidroksi Anisol), BHT (Butil Hidroksi Toluen), PG (Propil
Galat) dan TBHQ (Tersier Butil Hidrokuinon).Penggunaan kombinasi beberapa jenis
antioksidan memberikan perlindungan yang lebih baik terhadap oksidasi jika
dibandingkan dengan penggunaan satu jenis antioksidan saja (Cahyadi, 2006).
2.2.1. Manfaat antioksidan
Berkaitan dengan fungsinya, senyawa antioksidan di klasifikasikan dalam lima tipe
antioksidan, yaitu:
1. Primary antioxidants, yaitu senyawa-senyawa fenol yang mampu memutus
rantai reaksi pembentukan radikal bebas asam lemak. Senyawa antioksidan
yang termasuk kelompok ini, misalnya BHA, BHT, PG, TBHQ dan tokoferol.
2. Oxygen scavengers,yaitu senyawa-senyawa yang berperan sebagai pengikat
oksigen sehingga tidak mendukung reaksi oksidasi. Dalam hal ini, senyawa
tersebut akan mengadakan reaksi dengan oksigen yang berada dalam sistem
sehingga jumlah oksigen akan berkurang. Contoh dari senyawa-senyawa
kelompok ini adalah vitamin C (asam askorbat), askorbilpalminat, asam
eritorbat dan sulfit.
3. Secondary antioxidants,yaitu senyawa-senyawa yang mempunyai kemampuan
untuk berdekomposisi hidroperoksida menjadi prodak akhir yang stabil. Tipe
antioksidan ini pada umumnya digunakan untuk menstabilkan poliolefin resin.
Contohnya asam tiodipropionat dan dilauriltiopropionat.
4. Antioxidative EnzimeI,yaitu enzim yang berperan mencegah terbentuknya
radikal bebas. Contohnya glukose oksidase, superoksidase dismutase(SOD),
5. Chelators sequestrants,yaitu senyawa-senyawa yang mampu mengikat logam
seperti besidan tembaga yang mampu mengkatalis reaksi oksidasi lemak.
Senyawa yang termasuk didalamnya adalah asam sitrat, asam amino,
ethylenediaminetetra acetid acid (EDTA) dan fosfolipid.
2.2.2 Mekanisme kerja antioksidan
Menurut Stuckey (1972) penghambatan oksidasi lipida oleh antioksidan melalui lebih
dari satu mekanisme tergantung pada kondisi reaksi dan sistem makanan. Salah satu
mekanisme kerja antioksidan adalah dengan menyediakan hidrogen untuk bereaksi
dengan radikal bebas dan memutuskan reaksi berantai oksidasi sebelum terbentuk
produk akhir penyebab ketengikan, contohnya antioksidan golongan fenolat (AH2
dan AH). Radikal bebas fenolat yang terbentuk stabil (berenergi rendah) karena
adanya hibridisasi resonansi (Smith,1991).
Antioksidan sebaiknya ditambahkan ke lipida seawal mungkin untuk
menghasilkan efek maksimum. Menurut Coppen (1983), antioksidan hanya akan
benar-benar efektif bila ditambahkan seawal mungkin selama periode induksi, yaitu
suasana periode awal oksidasi lipida terjadi dimana oksidasi masih berjalan secara
lambat dengan kecepatan seragam.
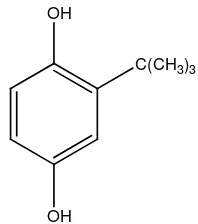
2.2.3Tersier butil hidrokuinon
minyak-minyakan yang berasal dari tanaman (minyak nabati). Bila TBHQ
direkomendasikan dengan BHA yang memiliki kemampuan antioksidan yang baik
pada pemanggangan akan memberikan kegunaan yang lebih luas (Sherwin, 1990).
OH
C(CH3)3
OH
Gambar 2.1Struktur TBHQ
TBHQ dikenal berbentuk bubuk putih sampai coklat terang, mempunyai
kelarutan cukup pada lemak dan minyak, tidak membentuk kompleks warna dengan
Fe dan Cu tetapi dapat berubah pink dengan adanya basa. TBHQ memiliki rumus
molekul (CH3)3CC6H3(OH)2 dan memiliki nama lain seperti
tert-butyl-1,4-benzenediol atau 2-tert-butylhydroquinone. Sedangkan sifat fisik yang dimilikinya
antara lain memiliki berat molekul = 166.22, titik didih (760 mmHg) = 300oC, titik
leleh = 126.5-128.6oC dan intensitas baunya sangat rendah (Buck,1991).
2.3 Metode Analisis Antioksidan
Berbagai metode analisis telah banyak dilaporkan untuk penentuan antioksidan dan
pengawet dalam makanan, kosmetik maupun obat-obatan. Saat ini,kromatografi cair
kinerja tinggi (KCKT)adalah metodeyang paling banyak digunakan untuk
analisisantioksidan sintetik karena sifatnya yang fleksibel, presisi, sensitivitasyang
memadai, mudah dilakukan dan lebih efisien(Karovicova danSimko, 2000; Razali
dkk, 1997; Wang dkk, 2013).Meskipunmetode analisislain sepertikromatografi lapis
elektroforesis kapiler(Boyce danSpickett,
Xijin dan Zhicai (2011), mengungkapkan
1999) dan kromatografi
gas-spektrofotometer masa(GC-MS) (Guo dkk, 2007) juga telah dilaporkan.
tingginya presisi dan sensitivitas
yang dimiliki oleh KCKT(persen perolehan kembali diatas 90%) menyebabkan
metode inimenjaditeknikutamauntuk analisisantioksidan sintetikpadadaging, sup,
saus, makanan hewan, minyak kelapa sawit,keripik kentangdan jagung, keju,sereal,
minumandanhati.Pernyataan ini juga didukung oleh
Menurut Snyder dan Kirkland (1979) KCKT memiliki banyak kelebihan jika
dibandingkan dengan metode lainnya, yaitu:
Cabuk dan Kokturk (2013) bahwa
KCKT merupakan metode yang sederhana dan efisien dalam penetapan kadar
antioksidan sintetik dalam minuman. Pada kondisi optimum, persen perolehan
kembali diperoleh sebesar 53-98%, linieritas yang baik dengan koefisien kolerasi
sebesar 0,9975-0,9997, standar deviasi sebesar 1,0-5,2% dan limit deteksi sebesar
0,85-2,73 μg/mL.
- mampu memisahkan molekul-molekul dari suatu campuran
- mudah melaksanakannya
- kecepatan analisis dan kepekaan yang tinggi
- dapat dihindari terjadinya dekomposisi/ kerusakan bahan yang dianalisis
- resolusi yang baik
- dapat digunakan bermacam-macam detektor
- kolom dapat digunakan kembali
- mudah melakukan perolehan kembali sampel (sample recovery)
2.4 Kromatografi Cair Kinerja Tinggi
Kromatografi cair kinerja tinggi (KCKT) dikembangkan pada akhir tahun 1960 dan
1970. KCKT merupakan sistem pemisahan dengan kecepatan dan efisiensi yang
tinggi karena didukung oleh kemajuan dalam teknologi kolom, sistem pompa tekanan
berbagai analit secara kualitatif maupun kuantitatif, baik dalam komponen tunggal
ataupun campuran.
Pada KCKT, fase diam berupa kolom modern dengan partikel yang sangat
kecil (ditempatkan dalam kolom tertutup), sedangkan fasa gerak berupa cairan yang
dialirkan ke kolom menggunakan bantuan pompa dan terdapat detektor yang sensitif
(McMaster, 2007).Berdasarkan mekanisme pemisahannya, kromatografi dapat
diklasifikasikan berdasarkan adsorpsi, partisi, pertukaran ion dan berdasarkan
eksklusi ukuran. Pada partisi dibedakan lagi menjadi kromatografi fasa normal dan
fasa terbalik (Moffat, 2005).
Saat ini, KCKT sudah sangat luas digunakan sebagai teknik pemisahan baik
untuk analisis sampel dan pemurnian dalam variasi sampel baik dalam bidang
farmasi, bioteknologi, lingkungan, polimer dan industri makanan (Settle, 1997).
Kegunaan umum KCKT adalah untuk pemisahan sejumlah senyawa organik,
anorganik maupun biologis, analisis ketidakmurnian (impurities) dan analisis
senyawa-senyawa yang tidak mudah menguap. KCKT sering digunakan untuk
menetapkan kadar senyawa-senyawa tertentu seperti asam-asam amino, asam-asam
nukleat dan protein dalam cairan fisiologis, menentukan kadar senyawa-senyawa
aktif obat dan lainnya (Gandjar dan Rohman, 2007).
2.4.1 Pemisahan dalam KCKT
Pemisahan analit dalam kolom kromatografi terjadi didasarkan pada aliran fase gerak
yang membawa campuran analit melalui fase diam dan perbedaan interaksi analit
dengan permukaan fase diam menyebabkan terjadinya perbedaan waktu perpindahan
setiap komponen senyawa dalam campuran (Kazakevich dan LoBrutto,2007).
Komponen senyawa yang terpisah dalam sistim KCKT akan dibawa oleh fase
gerak menuju detektor dan sinyal yang terekam oleh detektor disebut sebagai
puncak,sedangkan keseluruhan puncak yang direkam oleh detektor selama proses
detektor selama analisis mempunyai dua informasi yaitu informasi kualitatif dan
informasi kuantitatif (Meyer, 2004).
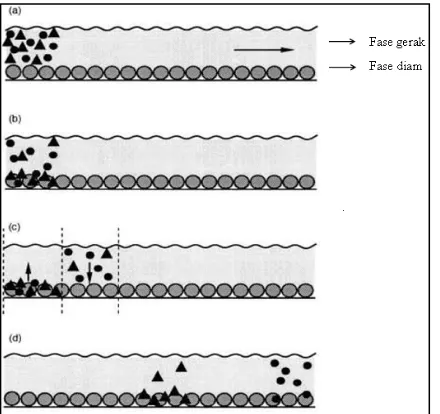
Sebagai contoh dapat digambarkan campuran dua senyawa yang berbeda
dimasukkan kedalam sistim kromatografi (partikel • dan ▲) (Gambar 2.2a) dan pada
saat fase gerak mengalir maka partikel ▲akan cenderung tinggal menetap difase
diam dan partikel • akan terbawa didalam fase gerak (Gambar 2.2b). Masuknya fase
gerak yang berkelanjutan dalam kolom akan menimbulkan kesetimbangan baru,
molekul sampel dalam fasa gerak diadsorpsi sebagian oleh permukaan fasa diam
berdasarkan koefisien distribusinya, sedangkan molekul yang sebelumnya diadsorpsi
akan muncul kembali di fasa gerak (Gambar 2.2c ). Setelah proses ini terjadi berulang
kali, kedua komponen akan terpisah. Komponen • yang lebih suka dengan fasa gerak
akan berpindah lebih cepat dari pada komponen ▲ yang cenderung menetap di fase
diam, sehingga komponen • akan muncul terlebih dahulu dalam kromatogram, yang
kemudian diikuti oleh komponen ▲(Gambar 2.2d) (Mayer, 2004).
2.4.2 Parameter penting pada KCKT
2.4.2.1 Waktu retensi (tR
Waktu retensi atau retention time (t
)
R
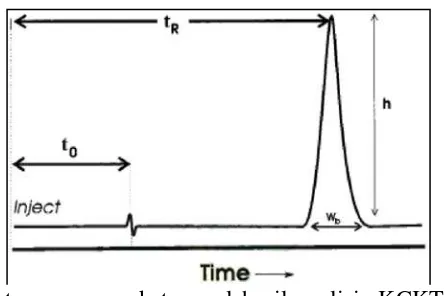
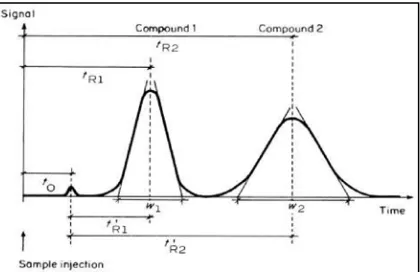
Sebuah puncak memiliki tinggi puncak (h) dan lebar puncak (W
) didefenisikan sebagai waktu yang diperlukan
untuk membawa keluar suatu komponen dari dalam kolom kromatografi. Waktu
retensi biasanya digunakan untuk menentukan kuat lemahnya interaksi analit di
dalam kolom kromatografi. Waktu retensi suatu zat selalu konstan pada kondisi
kromatografi yang sama. Suatu puncak kromatografi dapat diidentifikasi dengan
membandingkan waktu retensinya terhadap baku (Meyer, 2004).
b). Lebar
puncak yang diukur biasanya merupakan lebar pada 5% tinggi puncak (W0,05). Tinggi
dan luas puncak berkaitan secara proporsional atas kadar ataupun jumlah analit
tertentu yang terdapat dalam sampel (memiliki informasi kuantitatif). Namun
demikian, luas puncak lebih umum digunakan dalam proses analisis karena lebih
akurat dan lebih cermat daripada perhitungan menggunakan tinggi puncak (Ornaf dan
Dong, 2005). Kromatogram dari KCKT dapat dilihat pada Gambar 2.3.
Gambar 2.4Kromatogram dua puncak hasil analisis KCKT (Meyer, 2004)
Pada Gambar 2.4 dapat dilihat bahwa, w adalah lebar puncak dan to disebut
waktu hampa (void time/dead time), yaitu waktu tambat pelarut yang tidak tertahan
atau waktu yang dibutuhkan oleh fase gerak untuk melewati kolom (Meyer, 2004).
Waktu retensi dipengaruhi oleh laju alir (μ) dan panjang kolom (L). Jika laju alir
lambat atau kolom panjang, maka tR
µ= �
�� (9)
akan semakin besar dan sebaliknya. Waktu
retensi dipengaruhi oleh laju alir (μ) dapat dihitung dengan menggunakan rumus:
2.4.2.2 Faktor Kapasitas (k’)
Menurut Ornaf dan Dong tahun 2005, Faktor kapasitas (k’) merupakan suatu ukuran
derajat tambatan dari analit yang tidak dipengaruhi laju alir dan panjang kolom.
Faktor kapasitas dihitung dengan membagi waktu tambat bersih (tR) dengan waktu
hampa (t0) seperti yang dapat dilihat pada rumus berikut ini:
�′ =�′�
�0 =
�� − �0
�0 (10)
Faktor kapasitas juga disebut sebagai faktor tambat (k) dalam beberapa
dengan ukuran kolom yang berbeda namun memiliki fase diam dan fase gerak yang
sama, maka faktor kapasitas dari analit pada kedua sistem kromatografi cair kinerja
tinggi tersebut secara teoritis adalah sama (Kazakevich dan LoBrutto, 2007).
Faktor kapasitas yang disukai berada diantara nilai 1 hingga 10. Jika nilai
faktor kapasitas terlalu kecil menunjukkan bahwa analit terlalu cepat melewati kolom
sehingga tidak terjadi interaksi antara analit dengan fase diam dan oleh karena itu,
tidak akan muncul didalam kromatogram. Sebaliknya jika faktor kapasitas terlalu
besar maka akan mengindikasikan waktu analisis yang panjang (Meyer, 2004). Nilai
faktor kapasitas dari analit yang lebih kecil dari 1 dan juga lebih besar dari 20 akan
menjadi masalah dalam analisis menggunakan kromatografi cair kinerja tinggi (Ornaf
dan Dong, 2005).
2.4.2.3 Selektivitas (α)
Menurut Kazakevich dan LoBrutto tahun 2007, Selektifitas (α) adalah kemampuan sistem kromatografi untuk membedakan analit yang berbeda. Selektifitas ditentukan
sebagai rasio perbandingan faktor kapasitas (k’) dari analit yang berbeda:
� =�2
�1 =
��2− �0
��1− �0 (11)
Nilai selektifitas yang didapatkan dalam sistem kromatografi cair kinerja
tinggi harus lebih besar dari 1. Seletivitas juga dikenal sebagai faktor pemisahan atau
tambatan relatif (Ornaf dan Dong, 2005).
Proses pemisahan antara dua komponen dalam kromatografi cair kinerja
tinggi hanya dimungkinkan bila kedua komponen memiliki kecepatan yang berbeda
dalam melewati kolom (Ornaf dan Dong, 2005). Kemampuan sistem kromatografi
dalam memisahkan atau membedakan analit yang berbeda dikenal sebagai
selektivitas. Selektivitas umumnya bergantung kepada sifat analit tersebut dan
seperti metanol dan asetonitril juga diketahui dapat mempengaruhi sifat selektivitas
(Kazakevich dan LoBrutto, 2007).
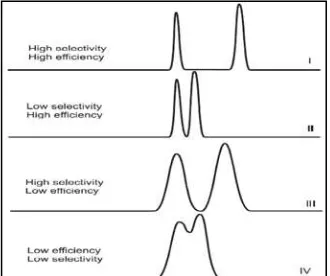
Gambar 2.5Kromatogram hasil analisis kromatografi cair kinerja tinggi dengan berbagai selektifitas dan efisiensi (Kazakevich dan LoBrutto, 2007)
2.4.2.4 Efisiensi Kolom (N)
Ukuran kuantitatif dari efisiensi kolom disebut sebagai nilai lempeng (plate number)
atau N (Ornaf dan Dong, 2005). Menurut Kazakevich dan LoBrutto tahun 2007,
Efisiensi adalah ukuran tingkat penyebaran puncak dalam kolom. Efisiensi kolom
ditunjukkan dari jumlah lempeng teoritikal atau theoretical plates (N), yang dapat
dihitung dengan rumus:
�= 16 ���
��
2
(12)
Menurut Snyder dan Kirkland tahun 1979, kolom yang efisien adalah kolom
yang mampu menghasilkan pita sempit dan memisahkan dengan baik setiap analit
dalam campuran (sampel). Nilai lempeng akan semakin tinggi jika ukuran kolom
semakin panjang, hal ini berarti proses pemisahan yang terjadi semakin baik.
Hubungan yang proporsional antara nilai lempeng pengan panjang kolom disebut
sebagai tinggi setara dengan lempeng teoritikal (Height Equivalent of a Theoritical
�= �
� (13)
Tujuan utama dari analisis kromatografi cair kinerja tinggi secara praktik
adalah untuk mendapatkan nilai lempeng teoritis yang maksimum, tinggi setara setara
dengan lempeng teoritikal yang minimum dan efisiensi kolom yang tertinggi (Snyder
dan Kirkland, 1979).
2.4.2.5Resolusi (Rs)
Menurut Ornaf dan Dong tahun 2005, resolusi (Rs) merupakan derajat pemisahan
dari dua puncak analit yang berdekatan. Resolusi dapat didefinisikan sebagai
perbedaan waktu tambat antara dua puncak dibagi dengan rata-rata lebar kedua
puncak. Oleh karena itu resolusi dapat dihitung dengan menggunakan rumus sebagai
berikut ini:
Pemisahan yang terpisah dengan sempurna telah dapat terlihat bila resolusi
setara dengan 1. Akan tetapi, pada analisis kuantitatif, resolusi yang ditunjukkanharus
lebih besar dari 1,5. Sementara itu, bila kedua puncak yang berdekatan memiliki
perbedaan ukuran yang signifikan, maka diperlukan nilai resolusi yang lebih besar
(Meyer, 2004).
2.4.2.6Faktor ikutan (Tf) dan faktor asimetri (As
Idealnya, puncak kromatogram akan memperlihatkan bentuk Gaussian dengan derajat
simetris yang sempurna (Ornaf dan Dong, 2005). Namun kenyataannya, puncak yang
simetris secara sempurna jarang dijumpai (bentuk Gaussian seperti yang ditunjukkan
pada Gambar 2.6). Jika diperhatikan secara cermat, maka hampir setiap puncak dalam
kromatografi memperlihatkan tailing (Dolan, 2003). Pada Gambar 2.7, ditunjukkan
tiga jenis bentuk puncak.
Gambar 2.6Bentuk puncak kromatogram (Meyer, 2004).
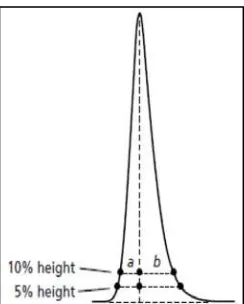
Pengukuran derajat asimetris puncak dapat dihitung dengan 2 cara, yakni:
faktor ikutan atau tailing factor (Tf) dan faktor asimetris. Faktor ikutan atau tailing
factor (Tf) seperti yang diterangkan dalam Farmakope Amerika Serikat edisi ketiga
puluh (United States Pharmacopoeia 30th Edition (USP XXX)) tahun 2007 dihitung
dengan menggunakan lebar puncak pada ketinggian 5% (W0,05) rumusnya dituliskan
sebagai berikut:
�� =�+�
2 � (15)
Dengan nilai a dan b merupakan setengah lebar puncak pada ketinggian 5% seperti
Gambar 2.7Pengukuran derajat asimetris puncak (Dolan, 2003).
Sedangkan faktor asimetri (As) dapat dihitung dengan rumus sebagai berikut:
�� = �� (16)
Akan tetapi, nilai a dan b dalam perhitungan faktor asimetri merupakan
setengah lebar puncak pada ketinggian 10% seperti yang ditunjukkan di Gambar 2.7.
Jika nilai a sama dengan b, maka faktor tailing dan asimetri bernilai 1. Kondisi ini
menunjukkan bentuk puncak yang simetris sempurna (Dolan, 2003). Bila puncak
berbentuk tailing, maka kedua faktor ini akan bernilai lebih besar dari 1 dan
sebaliknya bila puncak berbentuk fronting, maka faktor tailing dan asimetri akan
bernilai lebih kecil dari 1 (Hinshaw, 2004).
2.4.3 Instrumen KCKT
Pada dasarnya peralatan pokok yang harus ada di dalam suatu sistem KCKT adalah
sebagai berikut, wadah fasa gerak, pompa, injektor, kolom, detektor dan rekorder
Gambar 2.8Instrumen dasar KCKT (McMaster, 2007).
2.4.3.1 Wadah fase gerak
Sesuai dengan namanya, fungsi dari wadah fasa gerak adalah untuk menampung fase
gerak yang akan dialirkan ke dalam kolom dengan bantuan pompa. Wadah fasa gerak
biasanya terbuat dari gelas dengan volume yang bervariasi bergantung dari jumlah/
volume fasa gerak yang dibutuhkan.
2.4.3.2 Pompa
Pompa di dalam sistem KCKT berfungsi untuk mendorong fase gerak masuk
kedalam kolom. Tekanan pompa yang diperlukan harus cukup tinggi karena kolom
KCKT berisi partikel-partikel yang sangat kecil. Pompa yang cocok digunakan untuk
KCKT adalah pompa yang mempunyai syarat sebagaimana syarat wadah pelarut
yakni harus inert terhadap fase gerak. Bahan yang umum dipakai untuk pompa adalah
gelas, baja tahan karat, teflon, dan batu nilam. Pompa yang dgunakan sebaiknya
mampu memberikan tekanan sampai 5000 psi dan mampu mengalirkan fase gerak
dengan kecepatan alir 3 mL/menit (Rohman, 2009).
2.4.3.3Injektor
Ada 3 jenis injektor, yaitu syringe injector, loop valve dan automatic injector
(Dong, 2005).Katup putaran (loop valve) umumnya digunakan untuk menginjeksi
volume lebih besar daripada 10 μl dan sekarang digunakan dengan cara otomatis. Bila
katup difungsikan, maka cuplikan di dalam putaran akan bergerak ke dalam kolom
(Dong, 2005). Sedangkan automatic injector atau disebut juga autosampler memiliki
prinsip yang mirip, hanya saja sistem penyuntikannya bekerja secara otomatis
(Meyer, 2004).
2.4.3.4Kolom
Kolom merupakan jantung atau bagian yang terpenting dari suatu instrumen KCKT
karena didalam kolom terjadi pemisahaan komponen-komponen cuplikan. Oleh
karena itu, berhasil atau tidaknya suatu analisis atau pemisahaan
komponen-komponen sangat tergantung pada kolom yang digunakan. Pemisahan dapat terjadi
karena fase diam yang terdapat di dalam kolom dapat mengadakan interaksi dengan
berbagai kompoen dengan kekuatan yang berbeda satu sama lain, sehingga
masing-masing komponen akan keluar dari kolom dengan waktu retensi (tR
Kolom umumnya terbuat dari baja anti karat dengan tingkat 316 (316 grade
stainless steel) dan dikemas dengan fase diam tertentu. Ukuran panjang kolom untuk
tujuan analitik berkisar antara 10 cm hingga 25 cm dan diameter dalam berkisar 3
mm hingga 9 mm (Brown dan DeAntonis, 1997). Sedangkan untuk tujuan preparatif
panjang berkisar antara 30 cm atau lebih dan diameter dalam berkisar 10 mm hingga
25,4 mm (Meyer, 2004).
) yang juga
berbeda.
2.4.3.5 Detektor
Karakteristik detektor yang baik adalah sensitif, batas deteksi rendah, respon yang
linier, mampu mendeteksi solut secara universal, tidak destruktif, mudah
dioperasikan, memiliki volume pendeteksian (dead volume) yang kecil dan tidak
Sewell, 1977). Beberapa detektor yang paling sering digunakan dalam KCKT adalah
detektor spektrofotometri ultraviolet/visible, photodiode-array (PDA), fluoresensi,
spektrometri massa, indeks bias dan elektrokimia (Rohman dan Gandjar, 2007).
2.4.3.6 Perekam atau rekorder
Alat pengumpul data seperti komputer, integrator dan rekorder dihubungkan ke
detektor. Alat ini akan menangkap sinyal elektronik dari detektordan memplotkannya
kedalam kromatogram sehingga dapat dievaluasi oleh analis (Brown dan DeAntonis,
1997).
2.5 Validasi Metode
Validasi metode analisis ialah suatu tindakan penilaian terhadap parameter tertentu,
berdasarkan percobaan laboratorium, untuk membuktikan bahwa parameter tersebut
memenuhi persyaratan untuk digunakannya. Tujuan utama validasi adalah untuk
menjamin bahwa metode analisis yang digunakan mampu memberikan hasik yang
cermat dan handal sehingga dapat dipercaya (Harnita, 2004).
Beberapa parameter analisis yang harus dipertimbangkan dalam validasi
metode analisis diuraikan dan didefinisikan sesuai dengan cara penentuannya.
Parameter yang digunakan ialah batas deteksi dan kuantitasi, presisi, akurasi, dan
linearitas. Selain itu digunakan pula parameter keterulangan (repeatability) dan
ketangguhan (rudgedness).
2.5.1 Linieritas
Linieritas menggambarkan hubungan antara respon detektor dengan konsentrasi
analit yang diketahui. Linieritas dapat diperoleh dengan mengukur beberapa
konsentrasi standar yang berbeda antara 50-150% dari kadar analit dalam sampel
kemudian data diproses menggunakan regresi linier sehingga diperoleh slope,
2.5.2Akurasi (kecermatan)
Akurasi merupakan ukuran yang menunjukkan kedekatan nilai hasil analisis dengan
kadar analit yang sebenarnya. Akurasi dinyatakan sebagai persen perolehan kembali
(recovery) analit yang ditambahkan (Harnita, 2004).Akurasi dapat ditentukan dengan
2 (dua) metode yaitu:
1. Metode simulasi (Spike-placebo recovery) analit murni ditambahkan kedalam
campuran/ sampel, kemudian campuran/ sampel ini dianalisis dan jumlah
analit hasil analisis dibandingkan dengan jumlah analit teoritis yang
diharapkan
2. Metode penambahan standar (Sandard Addition Method) adalah perlakuan
pemasukan langsung analit yang telah diketahui konsentrasinya kedalam
sediaan campuran/ sampel farmasi otentik ( Ermer, 2005; Harmita, 2004 )
2.5.3 Presisi (keseksamaan)
Presisi ialah ukuran yang menunjukkan derajat kesesuaian antarhasil uji individual,
diukur melalui penyebaran hasil individual dari rata-rata jika prosedur diterapkan
secara berulang pada sampel-sampel yang diambil dari campuran yang homogen.
Menurut CDER (1994), presisi dibagi menjadi tiga, yaitu keterulangan
(repeatability), ketertiruan (reproducibility), dan presisi antara (intermediate
precision). Keterulangan ialah presisi metode jika dilakukan berulang kali oleh analis
yang sama pada kondisi sama dan dalam interval waktu yang pendek. Ketertiruan
ialah presisi metode jika dilakukan berulang kali oleh analis yang berbeda pada
kondisi berbeda. Presisi antara merupakan ukuran ketertiruan pada kondisi operasi
normal antara laboratorium dan antaranalis.
2.5.4 Batas deteksi dan batas kuantitasi (LOD dan LOQ)
Batas deteksi adalah konsentrasi analit terendah yang terdapat dalam sampel yang
masih mampu dideteksi. Sedangkan batas kuantitasi adalah konsentrasi analit