INTISARI
p-Phenylenediamine (PPD) merupakan senyawa pewarna yang terkandung dalam pewarna rambut oksidatif. Kadar PPD yang diperbolehkan maksimum sebesar 6% (60 mg/g sampel) karena dapat mengiritasi kulit. Meskipun demikian, banyak pewarna rambut yang tidak mencantumkan kadar PPD pada kemasannya. Penelitian ini bertujuan untuk menentukan pH dan polaritas sistem kromatografi cair kinerja tinggi (KCKT) yang sesuai untuk penetapan kadar PPD serta mendapatkan sistem KCKT dan metode penetapan kadar PPD yang dapat memberikan hasil yang valid.
Instrumen KCKT yang digunakan terdiri dari detektor UV pada λ 254 nm dan sistem elusi isokratik dengan jenis kolom, fase gerak, laju alir, dan suhu oven yang diubah hingga didapatkan pemisahan PPD yang optimal. Parameter optimasi yang diacu adalah nilai resolusi (Rs), tailing factor (TF), jumlah lempeng (N), tinggi lempeng (HETP), dan waktu retensi (tR). Uji kesesuaian sistem KCKT yang telah dioptimasi untuk penetapan kadar PPD mengacu pada parameter presisi (keterulangan dan presisi antara), linearitas, dan sensitivitas.
Hasil penelitian menunjukkan bahwa sistem KCKT yang optimal untuk pengukuran PPD adalah kolom C18 dengan fase gerak asetonitril:air = 10:90 + amonia 10% hingga pH 8, pada suhu lingkungan, dan laju alir 0,5 mL/menit. Sistem KCKT optimal tersebut memenuhi parameter validitas setelah dilakukan uji kesesuaian sistem, sehingga disimpulkan dapat digunakan sebagai metode penetapan kadar PPD.
ABSTRACT
p-Phenylenediamine (PPD) is the colorant contained in oxidative hair dyes with allowed maximum concentration of 6% (60 mg/g sample) because it is irritative to skin. Despite of that, majority of hair dyes don’t provide information about the amount of PPD on its packaging. The aims of this study are to determine the pH and polarity of high performance liquid chromatography (HPLC) system appropriate for determination of PPD and to obtain the HPLC condition and method which can give valid results.
The HPLC instrument equipped with UV detector at 254 nm and isocratic elution while using variation of column, mobile phase, flow rate, and oven temperature to acquire optimum separation of PPD. The parameters are resolution (Rs), tailing factor (TF), plate number (N), plate height (HETP), and retention time (tR). System suitability test was performed on optimum HPLC condition with the parameters of precision (repeatability and intermediate precision), linearity, and sensitivity.
The results show the optimum HPLC condition for PPD determination are C18 column; acetonitrile:water = 10:90 adjusted to pH of 8 with a 10% ammonia solution, as the mobile phase; ambient temperature; and 0,5 mL/min of flow rate. The HPLC system mentioned will be able to give reliable results as it passed all parameters on system suitability test hence, can be used as a technique to determine PPD.
ii
OPTIMASI PENETAPAN KADAR P-PHENYLENEDIAMINE (PPD) DAN UJI KESESUAIAN SISTEM KROMATOGRAFI CAIR KINERJA
TINGGI (KCKT)
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh:
Verni Emelia
NIM : 118114033
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iv
I’m so glad to be born,
I’m so lucky to be the daughter of my loving mom and dad,
I’m so excited to grow among my sisters and brother,
I’m so joyous to be a part of society,
I’m so contented to be a companion of my friends,
I’m so delighted to be considered a rival or even an enemy,
I’m so thankful to be able to learn precious lessons from people who come and go,
I’m so grateful as a student of my teachers,
I’m so pleased that I have studied at my alma mater,
I’m so honored to live in my lovely hometown and country,
I’m so happy to be who I am today.
This work is dedicated to all of the above mentioned parties,
for who I am today was magnificently sculptured by them yesterday,
vii PRAKATA
Puji syukur penulis panjatkan kepada Tuhan Yang Maha Esa atas kasih
karunia-Nya, sehingga penulis dapat menyelesaikan skripsi dengan judul
“Optimasi Penetapan Kadar p-Phenylenediamine (PPD) dan Uji Kesesuaian Sistem Kromatografi Cair Kinerja Tinggi (KCKT)” ini dengan baik. Skripsi ini disusun untuk memenuhi persyaratan memperoleh gelar Sarjana Strata Satu
Program Studi Farmasi Fakultas Farmasi Universitas Sanata Dharma.
Penulis mendapat banyak dukungan dari berbagai pihak baik secara moril
maupun materiil selama proses penyusunan skripsi ini, maka dalam kesempatan
ini, penulis ingin mengucapkan terima kasih yang tulus kepada:
1. Prof. Dr. Sri Noegrohati, Apt., selaku dosen pembimbing, atas segala
bimbingan, masukan, penghiburan, dan motivasi kepada penulis
2. Bapak Sanjayadi, M.Si., selaku ‘pembimbing tanpa tanda jasa’, atas segala
bimbingan, masukan, penghiburan, cerita, suka duka, dan motivasi kepada
penulis
3. Ibu Aris Widayati, M.Si., Ph.D., Apt., selaku dekan Fakultas Farmasi
Universitas Sanata Dharma
4. Bapak Jeffry Julianus, M.Si., selaku dosen penguji skripsi atas motivasi,
bantuan, kritik, dan masukkan kepada penulis selama penyusunan skripsi
5. Bapak F. Dika Octa Riswanto, M.Sc. selaku dosen penguji skripsi atas
bantuan, kritik, dan masukkan kepada penulis selama penyusunan skripsi
6. Kementrian Pendidikan Nasional Republik Indonesia atas Program Beasiswa
viii
7. Ibu Dr. Sri Hartati Yuliani, Apt., selaku kepala laboratorium yang telah
memberikan izin untuk penggunaan laboratorium di lingkungan Fakultas
Farmasi
8. Pak Bimo, Pak Bima, Pak Parlan, Pak Kun, Pak Mus, selaku laboran di
lingkungan laboratorium Fakultas Farmasi yang turut memberikan bantuan
selama penggunaan laboratorium untuk penelitian skripsi ini
9. Segenap dosen dan karyawan yang telah memberikan segala pengajaran dan
ilmu kepada penulis selama masa studi di Fakultas Farmasi
10. Orang tua penulis atas motivasi, doa, pengertian, serta cinta yang tak
terhingga diberikan kepada penulis
11. Tim PPDers, Rita, Canly, Shiro, selaku sahabat, partners in crime, serta
teman seperjuangan skripsi, atas segala masukan, motivasi, suka duka,
keceriaan, kegilaan, ejekan, cerita, keluh kesah, dan cinta yang dibagikan dan
diberikan kepada penulis
12. Sahabat yang jauh di mata dekat di hati, Vero dan Margaret, atas motivasi,
doa, kebersamaan, suka duka, cinta, serta cerita yang diberikan dan dilalui
bersama penulis sejak dulu hingga sekarang
13. Sahabat yang dekat di mata apalagi di hati, Ester, Sisca, Ingrid, Uci, Greta,
dan Evi, atas motivasi, cerita, suka duka, dinamika, serta makanan yang
dibagikan kepada penulis
14. Tim golongan umur dewasa, Henra, Tia, Dea, atas canda tawa, motivasi,
cerita faktual maupun fiktif, serta ilmu pendewasaan diri yang telah dibagikan
ix
15. Tim analisis, Eva, Yolana, Me Li, Miko, Kiki, Devi, Lika, Yolanda, Adit,
selaku teman-teman seperjuangan skripsi bidang analisis di bawah bimbingan
Bu Nunuk dan Pak Sanjaya
16. Teman-teman angkatan 2011 Prodi S1 Fakultas Farmasi Sanata Dharma yang
menjalani masa studi bersama-sama dengan penulis dan berperan dalam
pembentukan pribadi penulis yang lebih baik
17. Seluruh pihak yang tidak dapat disebutkan satu per satu, atas bantuan secara
langsung maupun tidak langsung yang diberikan kepada penulis dalam
penelitian dan penulisan skripsi ini.
Penulis menyadari bahwa skripsi ini masih memiliki banyak kekurangan,
sehingga segala bentuk masukan, kritik, dan saran yang membangun sangat
diharapkan. Terlepas dari segala ketidaksempurnaan, penulis berharap skripsi ini
dapat memberikan manfaat terhadap kemajuan ilmu pengetahuan dan teknologi di
lingkungan masyarakat dan negara Republik Indonesia
.
Yogyakarta, 5 Juni 2015
xi
C. Kromatografi……….
D. Kromatografi Cair Kinerja Tinggi (KCKT)………..
E. Optimasi……….
F. Pengaruh Laju Alir Terhadap Efisiensi Pemisahan………...
G. Uji Kesesuaian Sistem………...
2. Optimasi jenis fase diam, fase gerak, suhu oven, dan laju alir KCKT..
xii
A. Pembuatan seri larutan baku PPD……….
B. Optimasi Jenis Fase Diam, Fase Gerak, Suhu Oven, dan Laju Alir
KCKT………
1. Optimasi polaritas fase diam dalam analisis PPD dengan KCKT…….
2. Optimasi pH dan polaritas fase gerak dalam analisis PPD dengan
KCKT………
3. Optimasi laju alir fase gerak dalam analisis PPD dengan KCKT…….
4. Optimasi suhu oven dalam analisis PPD dengan KCKT………...
5. Hasil optimasi sistem KCKT untuk analisis PPD……….
ixiii
DAFTAR TABEL
Tabel I. Kolom dengan berbagai fase diam yang dipakai dalam
penelitian ini………
Tabel II. Kondisi sistem KCKT yang diubah-ubah dalam optimasi……..
Tabel III. Batas % CV parameter presisi (keterulangan) yang dapat
diterima menurut standar AOAC………
Tabel IV. Batas nilai r yang harus dilampaui dan hubungannya dengan
banyaknya penetapan kadar (n)………..
Tabel V. Deret eluotropik dan nilai UV cut-off pelarut KCKT………….
Tabel VI. Viskositas kombinasi fase gerak metanol:air (baris atas) dan
asetonitril:air (baris bawah) pada suhu tertentu (B = komposisi
organik)………...
Tabel VII. Nilai TF, Rs, N, HETP, dan tR puncak baku PPD setiap
kondisi sistem KCKT dengan fase diam C18……….
Tabel VIII. Nilai TF, Rs, N, HETP, dan tR puncak baku PPD setiap
kondisi sistem KCKT dengan fase diam C8………..………….
Tabel IX. Nilai TF, Rs, N, HETP, dan tR puncak baku PPD setiap
kondisi sistem KCKT dengan fase diam C2………...
Tabel X. Nilai TF, Rs, N, HETP, dan tR puncak baku PPD setiap
kondisi sistem KCKT dengan fase diam diol………..
xiv
Tabel XII. Nilai TF, Rs, N, dan HETP puncak baku PPD terbaik pada
setiap fase diam………...
Tabel XIII. Persen CV nilai tR dan AUC baku PPD……….
Tabel XIV. Data persamaan regresi linier baku PPD……… 59
60
ixv
DAFTAR GAMBAR
Gambar 1. Proses oksidasi molekul PPD (I) menjadi p-benzoquinone
diimine (III), p-benzoquinone monoimine (V), benzoquinone
(VI), dan Bandrowski’s base (II)………..
Gambar 2. Skema instrumentasi KCKT……….
Gambar 3. Hubungan tR, t0, dan k……….
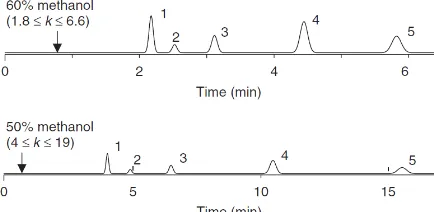
Gambar 4. Pengaruh komposisi fase gerak terhadap k………...
Gambar 5. Nilai Rs dan hubungannya dengan pemisahan terhadap
puncak lain………
Gambar 6. Perhitungan nilai Rs puncak kromatogram………...
Gambar 7. Bentuk puncak yang mungkin muncul dalam pemisahan
dengan KCKT………...
Gambar 8. Perhitungan nilai TF suatu puncak kromatogram……….
Gambar 9. Nilai TF dan hubungannya dengan bentuk puncak dan
pemisahan dengan puncak lain……….
Gambar 10. Perhitungan nilai N suatu puncak kromatogram………...
Gambar 11. Difusi Eddy pada kolom KCKT………...
Gambar 12. Difusi longitudinal pada kolom KCKT……….
Gambar 13. Ilustrasi transfer massa pada kolom KCKT………..
Gambar 14. Pengaruh laju alir terhadap efisiensi pemisahan………...
Gambar 15. Pengaruh komposisi asetonitril, metanol, dan tetrahidrofuran
xvi
Gambar 16. Segitiga selektivitas fase gerak KCKT……….
Gambar 17. Distribusi bentuk molekul PPD dalam berbagai pH………….
Gambar 18. Susunan molekul fase diam C18………...
Gambar 19. Kromatogram dengan kolom C18……….
Gambar 20. Molekul fase diam C8………...
Gambar 21. Kromatogram baku PPD dengan fase diam C8………
Gambar 22. Molekul fase diam C2………...
Gambar 23. Kromatogram baku PPD dengan C2……….
Gambar 24. Molekul fase diam diol……….
Gambar 25. Kromatogram baku PPD dengan kolom diol………...………
Gambar 26. Kromatogram dengan fase diam poliol silika………...
Gambar 27. Plot kumulatif AUC terhadap jumlah baku PPD (ng)………..
Gambar 28. Perbedaan profil linieritas antara kisaran massa baku PPD
ixvii
DAFTAR LAMPIRAN
Lampiran 1. Certificate of Analysis (CoA) Baku PPD I...………
Lampiran 2. Certificate of Analysis (CoA) Baku PPD II...………...
Lampiran 3. Perhitungan student’s t-test slope persamaan garis kisaran
massa baku PPD 20-80 ng dan 80-200 ng………
Lampiran 4. Perhitungan LOD……...………...
Lampiran 5. Contoh perhitungan polaritas fase gerak………...
Lampiran 6. Perhitungan ANOVA satu arah untuk slope kurva baku...…... 71
71
72
72
73
ixviii
INTISARIp-Phenylenediamine (PPD) merupakan senyawa pewarna yang terkandung dalam pewarna rambut oksidatif. Kadar PPD yang diperbolehkan maksimum sebesar 6% (60 mg/g sampel) karena dapat mengiritasi kulit. Meskipun demikian, banyak pewarna rambut yang tidak mencantumkan kadar PPD pada kemasannya. Penelitian ini bertujuan untuk menentukan pH dan polaritas sistem kromatografi cair kinerja tinggi (KCKT) yang sesuai untuk penetapan kadar PPD serta mendapatkan sistem KCKT dan metode penetapan kadar PPD yang dapat memberikan hasil yang valid.
Instrumen KCKT yang digunakan terdiri dari detektor UV pada λ 254 nm dan sistem elusi isokratik dengan jenis kolom, fase gerak, laju alir, dan suhu oven yang diubah hingga didapatkan pemisahan PPD yang optimal. Parameter optimasi yang diacu adalah nilai resolusi (Rs), tailing factor (TF), jumlah lempeng (N), tinggi lempeng (HETP), dan waktu retensi (tR). Uji kesesuaian sistem KCKT yang telah dioptimasi untuk penetapan kadar PPD mengacu pada parameter presisi (keterulangan dan presisi antara), linearitas, dan sensitivitas.
Hasil penelitian menunjukkan bahwa sistem KCKT yang optimal untuk pengukuran PPD adalah kolom C18 dengan fase gerak asetonitril:air = 10:90 + amonia 10% hingga pH 8, pada suhu lingkungan, dan laju alir 0,5 mL/menit. Sistem KCKT optimal tersebut memenuhi parameter validitas setelah dilakukan uji kesesuaian sistem, sehingga disimpulkan dapat digunakan sebagai metode penetapan kadar PPD.
xix ABSTRACT
p-Phenylenediamine (PPD) is the colorant contained in oxidative hair dyes with allowed maximum concentration of 6% (60 mg/g sample) because it is irritative to skin. Despite of that, majority of hair dyes don’t provide information about the amount of PPD on its packaging. The aims of this study are to determine the pH and polarity of high performance liquid chromatography (HPLC) system appropriate for determination of PPD and to obtain the HPLC condition and method which can give valid results.
The HPLC instrument equipped with UV detector at 254 nm and isocratic elution while using variation of column, mobile phase, flow rate, and oven temperature to acquire optimum separation of PPD. The parameters are resolution (Rs), tailing factor (TF), plate number (N), plate height (HETP), and retention time (tR). System suitability test was performed on optimum HPLC condition with the parameters of precision (repeatability and intermediate precision), linearity, and sensitivity.
The results show the optimum HPLC condition for PPD determination are C18 column; acetonitrile:water = 10:90 adjusted to pH of 8 with a 10% ammonia solution, as the mobile phase; ambient temperature; and 0,5 mL/min of flow rate. The HPLC system mentioned will be able to give reliable results as it passed all parameters on system suitability test hence, can be used as a technique to determine PPD.
1 BAB I PENGANTAR
A. Latar Belakang
Seiring dengan meningkatnya perhatian masyarakat terhadap penampilan
fisiknya, berbagai produk perawatan tubuh dan kosmetik tersedia luas di pasaran,
salah satunya adalah pewarna rambut. Pewarna rambut termasuk produk kosmetik
yang dipakai oleh sebagian besar penduduk di dunia, baik pria maupun wanita,
untuk mendapatkan warna rambut yang menambah percaya diri penggunanya,
misalnya untuk menyamarkan uban ataupun untuk mengikuti perkembangan tren.
Pada tahun 2001, dilaporkan bahwa pasar global untuk pewarna rambut
menghasilkan tujuh miliar dolar Amerika Serikat per tahun dan diperkirakan akan
meningkat 8-10% per tahun hingga lima tahun yang akan datang. Hal ini membuat
pasar pewarna rambut menjadi pasar dengan pertumbuhan paling pesat di industri
produk perawatan rambut (The Economist Newspaper, 2001).
Pewarna rambut adalah sediaan kosmetik yang digunakan dalam tata rias
rambut untuk mewarnai rambut atau untuk mengembalikan warna rambut asalnya
(Dirjen POM, 1985). p-Phenylenediamine (PPD) merupakan salah satu komposisi
utama pewarna rambut jenis oksidasi yang berperan sebagai pemberi warna.
Mayoritas produk pewarna rambut mengandung PPD, terutama yang membuat
warna rambut menjadi hitam. Namun, penggunaan produk pewarna rambut yang
mengandung PPD pada individu yang sensitif akan menyebabkan timbulnya
masalah kulit seperti dermatitis dan alergi (Pardede, Nababan, dan Mahadi, 2008).
tahun akibat penggunaan pewarna rambut merek ternama yang mengandung PPD.
Reaksi alergi tersebut berujung pada kematian setelah korban mengalami koma
selama 1 tahun (Brooke, 2015).
Kandungan PPD tidak hanya terdapat dalam pewarna rambut biasa,
namun juga dalam pewarna rambut henna. Pewarna rambut henna mengandung
tumbuhan henna (Lawsonia inermis L.) yang telah digunakan sejak lama untuk
mewarnai rambut. Banyak produk pewarna rambut henna yang diklaim alami,
lebih aman dari pewarna rambut sintetis, dan hanya mengandung henna ternyata
juga mengandung PPD. Pewarna rambut henna yang mengandung PPD biasanya
disebut ‘black henna’. Adanya PPD dapat memberikan warna yang lebih tahan
lama dan lebih hitam dibandingkan produk pewarna rambut henna yang tidak
mengandung PPD karena henna hanya dapat memberi warna jingga kecoklatan
atau merah kecoklatan (U.S. Food and Drug Administration, 2015). Penggunaan
PPD dalam produk pewarna rambut henna akan lebih berisiko, sebab banyak
konsumen yang tidak mengetahui adanya kandungan PPD dan percaya bahwa
pewarna rambut henna tersebut sepenuhnya aman dan alami.
Berdasarkan peraturan Kepala Badan Pengawas Obat dan Makanan
Republik Indonesia (BPOM RI) nomor HK.00.05.42.1018 tentang bahan
kosmetik (2008), kadar maksimum PPD yang diperbolehkan dalam pewarna
rambut adalah sebesar 6%. Namun, seringkali pada produk pewarna rambut tidak
dicantumkan mengenai banyaknya kandungan PPD, sehingga penelitian mengenai
penetapan kadar PPD secara kuantitatif dalam produk pewarna rambut perlu
Metode kromatografi cair kinerja tinggi (KCKT) merupakan metode
analisis yang digunakan untuk analisis dan pemisahan hampir semua jenis
campuran senyawa kimia, dapat dilakukan oleh banyak laboratorium karena
peralatan dan instrumennya tersedia luas di pasaran, serta memiliki presisi
pengukuran yang sangat baik (Snyder, Kirkland, and Dolan, 2010). Penentuan
kadar PPD lebih baik menggunakan suatu metode pemisahan seperti KCKT
karena sifat PPD yang mudah mengalami oksidasi menjadi berbagai senyawa lain
(Corbett, 1972). Pemisahan PPD akan sangat bergantung pada nilai pH dan
polaritas sistem KCKT karena PPD merupakan senyawa basa lemah yang
memiliki dua nilai pKa, yaitu 6,46 dan 3,04 (ChemAxon, 2014), sehingga dalam
lingkungan pH yang berbeda, distribusi bentuk molekul PPD dan polaritasnya
akan berbeda pula. Kualitas pemisahan PPD menggunakan teknik KCKT dapat
ditingkatkan pula dengan mengatur sistem KCKT pada suhu oven kolom dan laju
alir yang optimal (Snyder et al., 2010).
Penelitian tentang optimasi penetapan kadar PPD melalui pengaturan pH
dan polaritas sistem KCKT dan uji kesesuaian sistem KCKT ini adalah tahap
pertama dalam rangkaian penelitian mengenai PPD dalam sampel pewarna rambut
oksidatif. Hasil penelitian ini akan digunakan untuk tahap penelitian selanjutnya
yang mencakup optimasi penetapan kadar PPD dan uji kesesuaian sistem KCKT,
validasi metode analisis PPD dalam formulasi pewarna rambut oksidatif,
penentuan kinetika penetrasi PPD dalam pewarna rambut oksidatif pada kulit
1. Permasalahan
Berdasarkan latar belakang, maka timbul permasalahan sebagai berikut:
a. Bagaimanakah jenis fase diam, fase gerak, suhu oven kolom, dan laju alir
yang optimal agar didapatkan pH dan polaritas sistem KCKT yang sesuai
pada penetapan kadar PPD, sehingga dapat menghasilkan pemisahan yang
baik?
b. Apakah sistem KCKT yang telah diatur pada pH dan polaritas hasil optimasi
telah dapat memberikan hasil analisis yang valid setelah dilakukan uji
kesesuaian sistem?
2. Keaslian penelitian
Sejauh penelusuran peneliti, penelitian tentang PPD pernah dilakukan
secara KCKT pasangan ion fase terbalik, kolom C16 dengan gugus aktif amida,
fase gerak asetonitril:dapar fosfat pH 6 dengan sistem elusi gradien, pengukuran
pada suhu kamar (25±1 ºC), serta detektor photodiode-array (PDA) (Rastogi,
Worsøe, and Jensen, 2001); menggunakan kolom C18 dan fase gerak
asetonitril:dapar asetat 10 mM (sistem elusi gradien), serta detektor PDA (Fu,
2010); dengan kolom C8 dan fase gerak metanol:asam asetat 0,05 M yang
ditambah larutan amonia 10% hingga pH 5,9 yang dipompa dengan sistem elusi
gradien, pengukuran pada suhu oven 48 ºC, serta detektor UV (Vincent, Bordin,
and Rodríguez, 2002); menggunakan kolom C18 dan fase gerak metanol:asam
asetat 0,05 M = 5:95 yang ditambahan larutan amonia 10% hingga pH 5,9 dengan
sistem elusi isokratik, pengukuran pada suhu 30 ºC, serta detektor indeks bias
Penelitian terhadap pengaturan pH dan polaritas sistem KCKT melalui
optimasi jenis fase diam, fase gerak, suhu oven kolom, dan laju alir fase gerak,
serta uji kesesuaian sistem KCKT untuk penetapan kadar PPD belum pernah
dilakukan sebelumnya.
3. Manfaat penelitian
a. Manfaat metodologis. Penelitian ini diharapkan dapat menjadi
alternatif metode penetapan kadar PPD atau aplikasinya dengan teknik KCKT.
b. Manfaat praktis. Penelitian ini diharapkan dapat memberikan
informasi terkait pemilihan sistem KCKT yang sesuai serta memenuhi parameter
optimasi dan validasi atau aplikasinya dalam penetapan kadar PPD dengan teknik
KCKT.
B. Tujuan Penelitian
1. Menentukan sistem kromatografi yang sesuai digunakan dalam determinasi
PPD dengan cara mengatur pH dan polaritas sistem KCKT.
2. Mendapatkan hasil pengukuran PPD yang valid menggunakan metode
6 BAB II
PENELAAHAN PUSTAKA
A. Pewarna Rambut
Pewarna rambut adalah sediaan kosmetik yang digunakan dalam tata rias
rambut untuk mewarnai rambut atau untuk mengembalikan warna rambut asalnya
(Dirjen POM, 1985). Berdasarkan durasi daya lekatnya, pewarna rambut
diklasifikasikan menjadi tiga macam, yaitu pewarna rambut temporer,
semi-permanen dan semi-permanen (Azis dan Muktiningsih, 1999).
p-Phenylenediamine (PPD) atau p-diaminobenzene adalah penyusun
utama pewarna rambut permanen yang juga dikenal sebagai pewarna rambut
oksidatif, (Helmenstine, 2003). Daya oksidatif pewarna rambut ini juga dapat
merusak rambut dan menyebabkan dermatitis kontak (Acton, 2013).
B. p-Phenylenediamine (PPD)
p-Phenylenediamine (PPD) adalah suatu amin aromatik yang digunakan
dalam hampir setiap cat rambut di pasaran. p-Phenylenediamine adalah senyawa
yang tidak berwarna, menjadi berwarna pada saat teroksidasi, dan pada keadaan
teroksidasi sebagian menyebabkan alergi bagi individu yang sensitif. Paparan
terhadap PPD meski dalam konsentrasi rendah selanjutnya dapat menimbulkan
reaksi hipersensitivitas tipe lambat yang bermanifestasi sebagai dermatitis kontak
alergi (Pardede dkk., 2008).
Bobot molekul PPD adalah 108,14 g/mol, berwujud serbuk kristal
berwarna putih hingga sedikit merah, dan dapat menjadi lebih gelap karena
bagian air dingin, larut dalam alkohol, kloroform, eter. Kelarutan PPD pada suhu
22 °C dalam air sebesar < 10% (b/v), dalam etanol sebesar < 10% (b/v), dan
dalam DMSO sebesar > 20% (b/v) (United States Department of Labor, diakses
tanggal 18 April 2014). Pada suhu 25 °C, kelarutan PPD dalam air adalah 4 g/100
mL. Log Pow PPD sebesar –0,25 (National Center for Biotechnology
Information, diakses tanggal 4 Juni 2015); titik leleh pada suhu 139-141 °C
(Merck index: 145-147 °C), tekanan uap < 1 mmHg pada suhu 21 °C (produk
teknis), titik didih pada suhu 267 °C, dan panjang gelombang maksimum sebesar
281,9 nm (Scientific Committee on Consumer Safety, 2012).
Senyawa ini memiliki nilai pKa 1 = 6,46 dan pKa 2 = 3,04 (ChemAxon,
2014), sehingga struktur molekulnya sangat bergantung pada nilai pH. Bila
terpapar oksigen, PPD sangat mudah mengalami autoksidasi menjadi produk
oksidasi seperti Bandrowski’s base, benzoquinone, p-benzoquinone monoimine
dan p-benzoquinone diimine (Gambar 1) (Corbett, 1972).
Gambar 1. Proses oksidasi molekul PPD (I) menjadi p-benzoquinone diimine (III), p-benzoquinone monoimine (V), benzoquinone (VI), dan Bandrowski’s base (II)(Corbett, 1972)
Berdasarkan peraturan Kepala BPOM RI nomor HK.00.05.42.1018
tentang bahan kosmetik (2008), kadar maksimum PPD yang diperbolehkan dalam
C. Kromatografi
Kromatografi adalah metode pemisahan yang didasarkan pada perbedaan
kecepatan migrasi analit ketika suatu komponen sampel dilewatkan pada fase
diam menggunakan fase gerak. Fase diam terdiri dari partikel-partikel padat atau
semipadat atau cair yang dikemas dalam suatu tabung yang kemudian disebut
kolom. Fase gerak dipompa ke dalam kolom pada kecepatan tertentu. Fase gerak
dapat berupa gas, zat cair atau fluida superkritis (Hansen, Pedersen-Bjergaard, and
Rasmussen, 2012).
Berdasarkan mekanisme pemisahannya, kromatografi dibedakan menjadi
kromatografi adsorbsi, kromatografi partisi, kromatografi pasangan ion,
kromatografi penukar ion, kromatografi eksklusi ukuran, dan kromatografi
afinitas. Berdasarkan alat yang digunakan, kromatografi dapat dibagi atas
kromatografi kertas, kromatografi lapis tipis, yang keduanya sering disebut
dengan kromatografi planar, kromatografi gas dan kromatografi cair kinerja tinggi
(KCKT) (Gandjar dan Rohman, 2007).
D. Kromatografi Cair Kinerja Tinggi (KCKT)
Kromatografi cair kinerja tinggi atau KCKT atau biasa juga disebut
dengan HPLC (high performance liquid chromatography) merupakan teknik
kromatografi yang paling banyak digunakan dalam analisis farmasetika. Fase
gerak yang digunakan adalah zat cair, sehingga metode ini disebut sebagai
kromatografi cair. Analisis menggunakan KCKT dapat memberikan hasil yang
akurat dan presisi untuk analisis senyawa secara kuantitatif, walaupun dalam
Teknik KCKT dilakukan dengan menginjeksikan sampel ke dalam kolom,
sementara fase gerak dipompa terus-menerus melalui kolom ke detektor, analit
akan terpisah di dalam kolom menurut kekuatan interaksinya dengan fase diam
dan fase gerak. Semakin lemah interaksi analit dengan fase diam, semakin cepat
analit tersebut keluar kolom. Analit yang keluar kolom akan dideteksi oleh
detektor, lalu sinyal yang terdeteksi akan diplot terhadap waktu oleh komputer
dan disebut kromatogram (Snyder et al., 2010).
Instrumentasi KCKT terdiri dari wadah fase gerak, pompa bertekanan
tinggi (mencapai 4000 psi) dan mampu memompa fase gerak dengan kecepatan
hingga 10 mL/menit, injektor (biasanya dengan volume injeksi 20 L), kolom
yang berisi berbagai macam fase diam, detektor (biasanya digunakan
spektrofotometer UV/visibel), sistem komputasi pengolah data kromatogram,
serta injektor sampel otomatis atau oven kolom untuk instrumen yang lebih rumit
(Watson, 2012). Instrumentasi KCKT secara skematik dapat dilihat pada Gambar
2.
E. Optimasi
Optimasi metode dapat dilakukan secara manual dengan melibatkan
variasi satu variabel percobaan dalam satu waktu, sedangkan variabel yang lain
dibuat tetap, lalu respon yang terjadi dicatat. Variabel-variabel tersebut dapat
berupa laju alir, komposisi fase diam dan atau fase gerak, suhu, λ deteksi, dan pH.
Selama tahap optimasi, nilai resolusi, bentuk puncak, jumlah lempeng, kapasitas
kolom, waktu retensi, batas deteksi, batas kuantifikasi, dan parameter kualitas
pemisahan dan pengukuran lain harus dimaksimalkan hingga didapatkan nilai
yang paling baik dan memenuhi syarat (Gandjar dan Rohman, 2007).
Pada pemisahan analit menggunakan metode KCKT, dikenal istilah
waktu retensi dan faktor retensi/faktor kapasitas. Waktu retensi (tR) adalah ukuran
waktu yang dihitung saat cuplikan diinjeksikan hingga suatu komponen campuran
keluar kolom (Hendayana, 2006). Waktu retensi pelarut (zat yang tidak teretensi)
disebut dead-time (waktu mati) dan disimbolkan sebagai tm atau t0. Faktor retensi
(k) atau faktor kapasitas (k’) merupakan banyaknya solut pada fase diam dibagi
dengan banyaknya solut pada fase gerak. Nilai k merupakan nilai yang penting
bagi peneliti dalam proses interpretasi dan peningkatan kualitas pemisahan. Nilai
k tidak perlu dihitung karena dalam suatu pengembangan metode analisis ataupun
analisis rutin, nilai k cukup diperkirakan berdasarkan rumus berikut (Snyder et al.,
2010):
= (1)
Ilustrasi proses pemisahan analit X, Y, dan Z menggunakan KCKT dapat
dan k. Semakin besar tR, makin besar pula nilai k. Nilai k yang dikehendaki
adalah nilai k yang tidak terlalu kecil (k < 1), tetapi juga tidak terlalu besar, yaitu
k ≤ 10 sebab pada nilai tersebut, puncak yang dihasilkan biasanya lebih tinggi,
lebih sempit, dan tR yang lebih singkat. Nilai k < 1 dapat menghasilkan puncak
dengan resolusi yang buruk karena kemungkinan terjadinya penumpukan dengan
puncak lain. Maka dari itu, nilai k yang biasanya disarankan adalah 1 ≤ k ≤ 10
atau untuk resolusi yang lebih baik nilai k sebaiknya 2 ≤ k ≤ 10 (Snyder et al.,
2010).
Gambar 3. Hubungan tR, t0, dan k (Snyder et al., 2010)
Nilai k sebagian besar dipengaruhi oleh kekuatan elusi fase gerak,
sehingga perbedaan komposisi komponen fase gerak dapat menghasilkan nilai k
yang berbeda pula (Snyder et al., 2010). Semakin kuat komposisi fase gerak
tersebut, semakin kecil nilai k yang dihasilkan. Pengaruh komposisi fase gerak
terhadap nilai k pada pemisahan menggunakan kolom C18 dapat dilihat pada
gambar berikut.
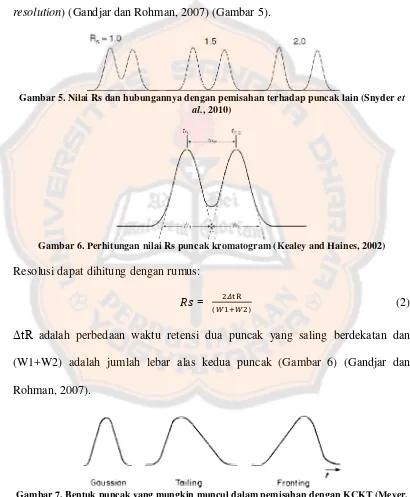
Resolusi (Rs) adalah perbedaan antara waktu retensi dua puncak yang
saling berdekatan dibagi dengan rata-rata lebar puncak. Nilai Rs harus mendekati
atau ≥ 1,5 agar memberikan puncak yang terpisah dengan baik (baseline
resolution) (Gandjar dan Rohman, 2007) (Gambar 5).
Gambar 5. Nilai Rs dan hubungannya dengan pemisahan terhadap puncak lain (Snyder et al., 2010)
Gambar 6. Perhitungan nilai Rs puncak kromatogram (Kealey and Haines, 2002)
Resolusi dapat dihitung dengan rumus:
=
( ) (2)
ΔtR adalah perbedaan waktu retensi dua puncak yang saling berdekatan dan
(W1+W2) adalah jumlah lebar alas kedua puncak (Gambar 6) (Gandjar dan
Rohman, 2007).
Gambar 7. Bentuk puncak yang mungkin muncul dalam pemisahan dengan KCKT (Meyer, 2004)
Tailing factor (TF) adalah ukuran yang menyatakan bentuk puncak.
(Gaussian). Nilai TF > 1 menunjukkan puncak mengalami pengekoran (tailing)
dan nilai TF < 1 berarti puncak mengalami fronting (Gambar 7). Nilai TF yang
diperbolehkan adalah < 2. Bila nilai TF ≥ 2 maka, harus dilakukan optimasi
sistem KCKT hingga dihasilkan puncak TF < 2 karena akan berpengaruh pada
pemisahan (Gambar 9) (Snyder et al., 2010). TF dapat dihitung dengan rumus:
= , (3)
Gambar 8. Perhitungan nilai TF suatu puncak kromatogram (Hansen et al., 2012) Simbol d adalah setengah lebar puncak sebelah kiri dan W0,05 adalah lebar alas
puncak. Nilai keduanya diukur pada 5% tinggi puncak dari alas puncak (Hansen et
al., 2012) (Gambar 8).
Gambar 9. Nilai TF dan hubungannya dengan bentuk puncak dan pemisahan dengan puncak lain (Snyder et al., 2010)
Plate number (N) atau jumlah lempeng dan height equivalent to a
kromatografi. Semakin besar nilai N, semakin efisien suatu pemisahan sebaliknya,
semakin kecil nilai HETP, semakin efisien suatu pemisahan karena didasarkan
pada teori plat yang menyatakan bahwa sepanjang kolom terjadi proses
kesetimbangan ekstraksi sebanyak N kali dan HETP merupakan tinggi setiap plat
(Hendayana, 2006).
Nilai N berbanding terbalik terhadap efisiensi kolom (HETP). Semakin
besar nilai N, maka semakin kecil nilai HETP yang berarti bahwa kolom
memberikan efisiensi yang baik pula (Gandjar dan Rohman, 2007). Nilai N dan
HETP dapat dihitung dengan rumus:
= 5,54 (
/
) (4)
= (5)
tR adalah waktu retensi, Wh/2 adalah lebar setengah puncak (Gambar 10), L adalah
panjang kolom dalam cm (sentimeter).
Gambar 10. Perhitungan nilai N suatu puncak kromatogram (Kealey and Haines, 2002)
F. Pengaruh Laju Alir Terhadap Efisiensi Pemisahan
Pada pemisahan menggunakan sistem KCKT, seringkali puncak yang
efisien. Fenomena ini disebut band broadening (pelebaran puncak) dan
dipengaruhi oleh kondisi sistem KCKT, yaitu laju alir. Pengaruh ini dapat
dijelaskan melalui persamaan van Deemter (6). Simbol H menunjukkan HETP, A,
B, dan C berturut-turut menunjukkan besarnya difusi Eddy, difusi longitudinal,
dan transfer massa, serta u menunjukkan besarnya laju alir (Snyder et al., 2010).
(6)
Difusi Eddy menjelaskan bahwa terdapat molekul analit yang mencapai
ujung kolom lebih cepat sementara yang lain lebih lambat karena melalui jalur
yang berbeda (Gambar 11). Fenomena ini menyebabkan terjadinya pelebaran
puncak karena perbedaan waktu molekul mencapai detektor. Hal ini terjadi karena
distribusi ukuran partikel fase diam yang tidak merata, sehingga tidak terpengaruh
oleh laju alir (Hendayana, 2006).
Gambar 11. Difusi Eddy pada kolom KCKT (Meyer, 2004)
Difusi longitudinal merupakan kecenderungan molekul-molekul analit
untuk berdifusi ke daerah di dalam kolom yang tidak ditempati oleh molekul lain
(dari konsentrasi yang lebih tinggi ke konsentrasi yang lebih rendah). Semakin
lama analit berada dalam kolom, semakin besar pula kecenderungan untuk
berdifusi yang menyebabkan melebarnya puncak kromatogram. Hal ini terjadi
sebab molekul yang berdifusi searah dengan aliran fase gerak akan tiba lebih
berbeda (Gambar 12). Peningkatan laju alir akan menurunkan kemungkinan
terjadinya difusi longitudinal (Hendayana, 2006).
Gambar 12. Difusi longitudinal pada kolom KCKT (Hendayana, 2006)
Sebagian molekul analit berada dalam fase gerak dan sebagian lagi
berada dalam fase diam ketika diinjeksikan ke dalam kolom. Bila fase gerak yang
membawa sebagian molekul analit mengalir dengan terlalu cepat, sementara
sebagian molekul yang masih tertinggal pada fase diam tidak dapat meninggalkan
kolom dengan kecepatan yang sama, maka akan terjadi pelebaran puncak akibat
molekul analit yang tiba di ujung kolom secara tidak bersamaan (Gambar 13)
(Hendayana, 2006).
Gambar 13. Ilustrasi transfer massa pada kolom KCKT (Hendayana, 2006)
Pengaruh laju alir terhadap efisiensi pemisahan dapat dilihat pada grafik
berikut (Gambar 14). Pada grafik tersebut, dapat disimpulkan bahwa untuk
mencapai efisiensi yang optimum (HETP paling kecil), bukan berarti laju alir
harus diatur paling kecil ataupun paling besar, namun harus diatur sedemikian
Gambar 14. Pengaruh laju alir terhadap efisiensi pemisahan (Hansen et al., 2012)
G. Uji Kesesuaian Sistem
Uji kesesuaian sistem (UKS) adalah suatu proses untuk memastikan
bahwa instrumen dan prosedur analisis yang digunakan pada pengujian tertentu
beroperasi dengan benar, sehingga memberikan hasil yang dapat dipercaya. Uji
kesesuaian sistem biasanya dilakukan sebelum proses analisis sampel dilakukan.
Parameter untuk UKS dapat berbeda-beda tergantung keperluan analisis (Snyder
et al., 2010).
Parameter UKS dalam penelitian ini mengacu pada kriteria validitas
analisis menggunakan KCKT, yaitu presisi, linearitas, dan batas deteksi (LOD).
Parameter presisi yang digunakan adalah keterulangan (repeatability) dan presisi
antara (intermediate precision/ruggedness). Keterulangan menunjukkan
kedekatan antarhasil pengukuran yang didapatkan dari metode pengukuran yang
sama, laboratorium yang sama, serta dilakukan oleh operator dan instrumen yang
sama dalam jangka waktu pengukuran yang singkat. Presisi antara menunjukkan
variasi pengukuran dalam laboratorium yang sama yang diperoleh dari metode
pengukuran yang sama, sampel yang identik, serta dilakukan oleh operator dan
hari) (United States Pharmacopeia, 2006). Presisi (keterulangan) dinyatakan
dengan koefisien variansi/coefficient of variation (CV) yang dapat dihitung
dengan rumus:
CV = 100 x SD / (7)
Simbol SD adalah standar deviasi dan X adalah nilai rata-rata data (Gandjar dan
Rohman, 2007).
Linearitas adalah kemampuan (dalam rentang tertentu) untuk
mendapatkan hasil penelitian yang proporsional terhadap konsentrasi analit dalam
sampel. Semakin mendekati -1 atau 1 nilai koefisien korelasi (r), semakin baik
dan linear kurva bakunya (Gandjar dan Rohman, 2007).
Limit of detection/batas deteksi (LOD) adalah konsentrasi yang
menghasilkan sinyal instrumen yang berbeda signifikan dari sinyal blanko (Miller
and Miller, 2010). Sensitivitas dapat ditentukan dari LOD dan slope. LOD dapat
dihitung dari regresi linier y = (b ± Sb) x + (a ± Sa) dengan rumus:
LOD = 3 (Sa/b) (8)
Simbol b adalah slope atau kemiringan kurva baku, Sb merupakan standar deviasi
slope, a adalah intersep, dan Sa merupakan standar deviasi intersep (Gonzales and
Herrador, 2007). Nilai slope diperoleh dari nilai b pada persamaan regresi linier y
= bx + a. Slope menunjukkan respon alat.
H. Metode Analisis Baku
Sejauh penelusuran pustaka penulis, belum terdapat metode analisis baku
PPD dalam pewarna rambut menggunakan instrumen KCKT. Metode analisis
dalam penelitian tertentu, sehingga merupakan suatu pengembangan metode
seperti yang dilakukan oleh Rastogi et al. (2001). Terdapat metode analisis baku
PPD dalam pewarna rambut pada AOAC (Association of Official Analytical
Chemists) (1984) yang menggunakan metode gravimetri. European Commission
pada tahun 1999 mengeluarkan metode analisis baku PPD dalam pewarna rambut
menggunakan metode TLC (Thin Layer Chromatography).
I. Landasan Teori
p-Phenylenediamine (PPD) merupakan salah satu komposisi utama
dalam pewarna rambut permanen jenis oksidatif. Pada penggunaan jangka pendek
maupun jangka panjang, PPD dapat menimbulkan efek buruk pada kesehatan
seperti dermatitis, mata iritasi dan berair, serta asma pada manusia. Menurut
peraturan yang berlaku, kadar PPD yang diperbolehkan dalam suatu sediaan
pewarna rambut maksimal sebesar 6%. Namun, pada kenyataannya, banyak
sediaan pewarna rambut yang tidak mencantumkan kadar PPD dalam produknya,
sehingga keamanan produk tersebut tidak dapat dipastikan.
Sifat PPD yang mudah mengalami oksidasi saat terpapar oksigen
dianalisis menggunakan instrumen KCKT dalam penelitian ini untuk memisahkan
PPD dengan produk oksidasinya. Metode analisis baku yang tersedia adalah
gravimetri dan TLC, namun kedua metode tersebut belum cukup baik untuk
memisahkan PPD dan tidak memiliki sistem pendeteksi sebaik instrumen KCKT
mengingat hasil dari penelitian ini akan digunakan dalam kajian keamanan dan
Oleh sebab itu, metode baku tersebut tidak digunakan dan dilakukan
pengembangan metode penetapan kadar menggunakan teknik KCKT.
Analisis PPD yang struktur molekulnya ditentukan oleh nilai pKa sangat
tergantung pada pH dan polaritas sistem KCKT, sehingga perlu dilakukan proses
optimasi khususnya pada jenis fase diam dan fase gerak. Optimasi suhu oven
kolom dan laju alir fase gerak juga dilakukan agar didapatkan kualitas pemisahan
yang baik, kemudian sistem KCKT yang telah optimal diuji kesesuaian sistemnya
sebelum digunakan untuk penetapan kadar PPD. Parameter pemisahan dengan
KCKT yang menunjukkan hasil optimum yaitu resolusi ≥ 1,5 pada kromatogram,
TF < 2, N > 2000, HETP kecil dan waktu retensi yang tidak lama (< 10 menit).
Parameter uji kesesuaian sistem dengan KCKT ditentukan dari linearitas
(koefisien korelasi/r), presisi keterulangan (koefisien variansi/CV) dan presisi
antara (signifikansi slope), serta sensitivitas (slope dan batas deteksi/LOD).
J. Hipotesis
1. Bila struktur molekul PPD ditentukan oleh pKa, maka pemilihan sistem
KCKT untuk penetapan kadar PPD harus diatur pH dan polaritasnya.
2. Metode penetapan kadar PPD menggunakan sistem KCKT yang telah
21 BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Jenis penelitian ini adalah eksperimental karena terdapat perlakuan
terhadap subjek uji dengan rancangan penelitian deskriptif.
B. Variabel Penelitian dan Definisi Operasional 1. Variabel
a. Variabel bebas. Variabel bebas dalam penelitian ini adalah konsentrasi
larutan baku PPD, jenis fase diam, komposisi fase gerak, suhu oven, dan laju alir
yang digunakan.
b. Variabel tergantung. Variabel tergantung dalam penelitian ini adalah
resolusi (Rs), tailing factor (TF), jumlah lempeng (N), nilai HETP, waktu retensi
(tR), limit of detection (LOD), slope, koefisien korelasi (r), dan koefisien variansi
(CV).
c. Variabel pengacau terkendali. Variabel pengacau terkendali dalam
penelitian ini adalah kemurnian pelarut yang digunakan. Hal tersebut dapat diatasi
dengan mengunakan pelarut pro analysis (p.a.)yang memiliki kemurnian tinggi.
d. Variabel pengacau tak terkendali. Variabel pengacau tak terkendali
dalam penelitian ini adalah kemungkinan oksidasi baku PPD.
2. Definisi operasional
a. Sistem KCKT yang dipergunakan adalah seperangkat alat KCKT yang
(communication bus module), dan komputer yang dilengkapi dengan
aplikasi penyaji data kromatogram.
b. Optimasi adalah proses penentuan sistem KCKT paling baik (optimal) yang
dilakukan dengan cara mengubah jenis fase diam, suhu oven kolom,
komposisi fase gerak yaitu jenis, pH, dan perbandingan volume fase gerak,
serta laju alirfase gerak.
c. Sistem KCKT optimal adalah kondisi KCKT yang mampu menghasilkan
puncak baku PPD yang baik dan dapat dilihat dari penentuan nilai resolusi
(Rs), tailing factor (TF), jumlah lempeng (N), nilai HETP, dan waktu retensi
(tR).
d. Resolusi (Rs) adalah ukuran pemisahan puncak baku PPD dengan puncak
komponen lain seperti natrium metabisulfit yang terletak paling dekat
dengan puncak PPD. Tailing factor adalah nilai yang mendefinisikan bentuk
puncak baku PPD yang dihasilkan. N dan HETP adalah ukuran efisiensi
pemisahan sistem KCKT terhadap baku PPD.
e. Penentuan nilai Rs, TF, N, HETP, dan tR adalah untuk puncak-puncak baku
PPD yang terlihat mencapai baseline resolution dari kromatogram.
f. Uji kesesuaian sistem KCKT adalah proses pemastian sistem KCKT yang
digunakan telah sesuai untuk digunakan dalam penetapan kadar baku PPD
dengan hasil yang dapat dipercaya yang dapat dilihat dari penentuan presisi
(keterulangan dan presisi antara) yang dilihat dari koefisien variansi (CV),
sensitivitas yang dilihat dari limit of detection (LOD) dan slope, serta
C. Bahan Penelitian
Bahan yang digunakan dalam penelitian ini adalah baku PPD 99,6%
(Nacalai Tesque, Inc.) dan 100,0% (Sigma Aldrich); metanol, asetonitril, natrium
metabisulfit, larutan amonia 10%, asam asetat, asam formiat dengan kualitas pro
analysis (E. Merck); Na2HPO4, KH2PO4, dan akuades.
D. Alat Penelitian
Alat yang digunakan dalam penelitian ini adalah neraca analitik (OHAUS
Pioneer tm PA214; maks. 60/120 g; min. 0,001 g; d = 0,01/0,1 mg),
ultrasonifikator (Branson 3510), kertas saring (Whatman; d = 47 mm; 0,45 μm),
syringe, mikropipet (Transferpette), milipore filter (Minisart; d = 30 mm; 0,45
µ m), pH meter (Hanna), indikator pH universal (E.Merck), tabung mikrosentrifus
1,5 mL (Eppendorf), seperangkat alat-alat gelas (Pyrex), instrumen KCKT yang
meliputi pompa (Waters, Model 510) dengan sistem elusi isokratik, injektor
(Rheodyne 7125; Loop 20L), oven kolom (Waters Millipore 1122) dan detektor
spektrofotometer ultraviolet (Waters Associates, Model 441; λ = 254 nm),
seperangkat komputer dengan CBM-102 (Shimadzu) dan perangkat lunak
(Shimadzu Labsolutions: GCsolution versi 2.30.00SU4), perangkat lunak Powerfit
v.6.05, serta kolom kromatografi seperti yang ditunjukkan pada Tabel I.
Tabel I. Kolom dengan berbagai fase diam yang dipakai dalam penelitian ini
Fase diam Merek Dimensi
Diol Chrompack Lichrosorb 250 x 4,6 10-100
E. Tata Cara Penelitian 1. Pembuatan seri larutan baku PPD
a. Pembuatan larutan natrium metabisulfit 0,01 M. Sejumlah lebih
kurang 1,9 g natrium metabisulfit ditimbang seksama lalu dilarutkan dalam
akuades yang telah disaring dengan kertas Whatman hingga 1 L.
b. Pembuatan larutan stok PPD 2 mg/mL dan larutan intermediet PPD 40 g/mL. Larutan stok PPD 2 mg/mL dibuat dengan menimbang seksama lebih
kurang 100 mg baku PPD lalu dilarutkan dengan larutan natrium metabisulfit 0,01
M dan diencerkanhingga batas dalam labu takar 50 mL. Larutan intermediet PPD
40 g/mL dibuat dari larutan stok 2 mg/mL.
c. Pembuatan seri larutan baku PPD. Seri larutan baku dibuat dari larutan intermediet dengan konsentrasi 40 g/mL sebanyak tujuh seri konsentrasi
yaitu 1, 2, 3, 4, 6, 8, dan 10 g/mL.
2. Optimasi jenis fase diam, fase gerak, suhu oven, dan laju alir KCKT Masing-masing seri larutan baku PPD dengan konsentrasi 1, 2, 3, 4, 6, 8,
dan 10 g/mL diinjeksikan ke dalam KCKT dengan volume 20 µL. Optimasi
pemisahan sistem KCKT dilakukan pada setiap kolom yang tertera pada Tabel I
dengan mengubah kondisi suhu oven kolom, komposisi dan laju alir fase gerak
seperti yang ditunjukkan pada Tabel II. Nilai TF, Rs, N, HETP, dan tR ditetapkan
dari data kromatogram yang dihasilkan untuk masing-masing perlakuan/optimasi.
Contoh penyiapan fase gerak asetonitril:air = 10:90 pH 8 adalah dengan
mencampur air (akuades) sebanyak 90 mL yang telah ditambah larutan amonia
disaring menggunakan kertas saring Whatman dengan dibantu pompa vakum lalu
di-degassing dengan ultrasonifikator selama 20 menit.
Tabel II. Kondisi sistem KCKT yang diubah-ubah dalam optimasi
Komposisi fase gerak
Suhu oven (ºC) Suhu lingkungan (32-33) 34
36 40 45 48
Pengubahan pH fase gerak dilakukan dengan menambahkan dapar fosfat
0,15 M, amonia 10%, asam asetat 0,05 M atau asam formiat. Dapar fosfat 0,15 M
dibuat dengan menimbang seksama lebih kurang 57,731 g Na2HPO4 dan 35,3833
g KH2PO4 lalu dilarutkan dalam akuades hingga 1 L.
3. Uji kesesuaian sistem KCKT
Uji kesesuaian sistem KCKT dilakukan dengan tujuan untuk mengetahui
kelayakan sistem KCKT untuk digunakan dalam penentuan kadar baku PPD
berdasarkan tiga parameter, yaitu presisi (keterulangan dan presisi antara),
a. Presisi (keterulangan) sistem KCKT. Nilai CV digunakan untuk
menentukan keterulangan sistem KCKT yang telah optimal. Parameter
keterulangan ditetapkan dengan cara menginjeksikan larutan baku PPD dengan
konsentrasi 1, 3, 4, 6, dan 10 g/mL dengan volume 20 µL ke dalam sistem
KCKT sebanyak 5 kali. Respon alat berupa luas puncak PPD masing-masing
konsentrasi larutan baku yang diperoleh dapat dihitung nilai rata-rata, (standar
deviasi) SD, dan CV.
c. Presisi antara (intermediet) sistem KCKT. Parameter presisi antara
ditetapkan dengan cara menginjeksikan larutan baku PPD dengan konsentrasi 1, 2,
3, 4, 6, 8, dan 10 g/mL dengan volume 20 µL ke dalam sistem KCKT. Linieritas
hubungan antara jumlah PPD yang diinjeksikan dengan respon alat diplotkan
dalam bentuk kurva baku dan dihitung parameter statistik, yaitu intersep (a), slope
(b), dan koefisien korelasi (r). Metode pengukuran yang sama dilakukan pada 3
hari yang berbeda. Nilai slope dari ketiga persamaan kurva baku tersebut dihitung
signifikansinya menggunakan perhitungan statistik.
b. Linieritas hubungan konsentrasi baku PPD dengan respon sistem
KCKT. Koefisien korelasi (r) digunakan untuk menentukan linieritas hubungan
konsentrasi baku PPD dengan respon sistem KCKT yang telah optimal. Parameter
linieritas ditetapkan dengan cara menginjeksikan larutan baku PPD dengan
konsentrasi 1, 2, 3, 4, 6, 8, dan 10 g/mL dengan volume 20 µL ke dalam sistem
KCKT. Linieritas hubungan antara jumlah PPD yang diinjeksikan dengan respon
alat diplotkan dalam bentuk kurva baku dan dihitung parameter statistik, yaitu
c. Sensitivitas sistem KCKT. Nilai LOD dan slope digunakan untuk
menentukan sensitivitas sistem KCKT yang telah optimal. Parameter sensitivitas
ditetapkan dengan cara menginjeksikan larutan baku PPD dengan konsentrasi 1, 2,
3, 4, 6, 8, dan 10 g/mL dengan volume 20 µL ke dalam sistem KCKT. Persamaan
kurva baku dari hasil injeksi tersebut dapat ditentukan dan dapat dihitung nilai
LOD dan slope.
F. Analisis Hasil 1. Analisis hasil optimasi KCKT
Analisis hasil optimasi KCKT dilakukan sesuai dengan persamaan (2)
hingga (5). Berikut ini ditentukan syarat-syarat nilai Rs, TF, N, HETP, tR yang
harus dicapai agar sistem KCKT dinyatakan optimal untuk penentuan kadar PPD.
a. Daya pisah (resolusi). Nilai Rs harus ≥ 1,5 karena akan memberikan
pemisahan puncak yang baik (Gandjar dan Rohman, 2007).
b. Bentuk puncak. Nilai TF yang dikehendaki adalah ≤ 2 karena tidak
mengganggu atau berpengaruh terhadap pemisahan, sedangkan nilai TF > 2 dapat
berpotensi mengganggu dan memberikan efek terhadap pemisahan secara rutin
(Snyder et al., 2010).
c. Jumlah lempeng (N) dan HETP. Nilai N (jumlah lempeng) yang
direkomendasikan secara umum adalah > 2000 dengan HETP menyesuaikan
panjang kolom dan nilai N (Snyder et al., 2010).
d. Waktu retensi (tR). Waktu retensi yang diharapkan dalam penelitian
2. Analisis hasil UKS KCKT
Analisis hasil UKS KCKT dilakukan sesuai dengan persamaan (7) dan
(8). Berikut ini ditentukan syarat-syarat nilai CV, r, LOD, dan slope yang harus
dicapai agar sistem KCKT dinyatakan sesuai untuk penentuan kadar PPD.
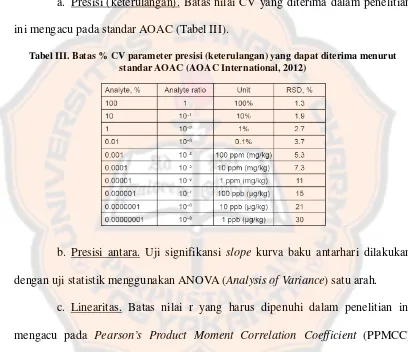
a. Presisi (keterulangan). Batas nilai CV yang diterima dalam penelitian
ini mengacu pada standar AOAC (Tabel III).
Tabel III. Batas % CV parameter presisi (keterulangan) yang dapat diterima menurut standar AOAC (AOAC International, 2012)
b. Presisi antara. Uji signifikansi slope kurva baku antarhari dilakukan
dengan uji statistik menggunakan ANOVA (Analysis of Variance) satu arah.
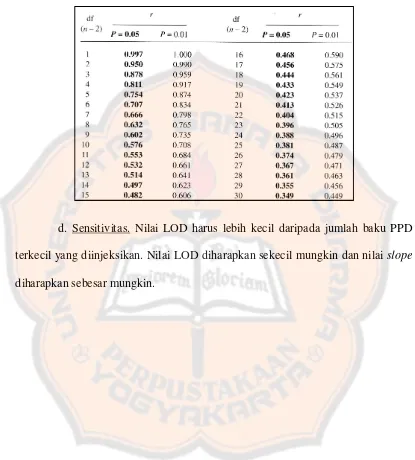
c. Linearitas. Batas nilai r yang harus dipenuhi dalam penelitian ini
mengacu pada Pearson’s Product Moment Correlation Coefficient (PPMCC)
(Tabel IV). Batas nilai r yang harus dipenuhi dilihat dari derajat kebebasan (df)
yaitu banyaknya pengukuran (n) – 2. Nilai r yang dicetak tebal menunjukkan nilai
r pada tingkat kepercayaan (1 – P) 95%, sedangkan nilai r yang tidak dicetak tebal
Tabel IV. Batas nilai r yang harus dilampaui dan hubungannya dengan banyaknya pengukuran (n) (Wheater and Cook, 2000)
d. Sensitivitas. Nilai LOD harus lebih kecil daripada jumlah baku PPD
terkecil yang diinjeksikan. Nilai LOD diharapkan sekecil mungkin dan nilai slope
diharapkan sebesar mungkin.
30 BAB IV
HASIL DAN PEMBAHASAN
Penetapan kadar PPD menggunakan instrumen KCKT karena peneliti
ingin memisahkan PPD dari produk oksidasinya. Instrumen KCKT harus dalam
kondisi yang optimal bila akan digunakan untuk penetapan kadar suatu analit.
Sistem KCKT yang beroperasi dalam keadaan tidak optimal akan memberikan
hasil analisis yang kurang baik, benar, dan efisien. Proses optimasi dalam
penelitian ini bertujuan untuk mendapatkan pH fase gerak serta polaritas fase
diam dan fase gerak sistem KCKT yang optimal agar dapat digunakan dalam
penetapan kadar PPD. Optimasi tersebut dapat dilakukan dengan mengubah jenis
fase diam dan fase gerak, laju alir serta suhu oven kolom hingga didapatkan
puncak PPD yang memenuhi parameter optimasi yang telah ditentukan.
A. Pembuatan Seri Larutan Baku PPD
Tujuan pembuatan seri larutan baku adalah untuk mengetahui hubungan
antara respon instrumen dengan konsentrasi baku PPD (analit) memenuhi kriteria
linieritas atau tidak, sehingga jika memenuhi dapat digunakan untuk menetapkan
kadar PPD dalam sampel pewarna rambut oksidatif atau sampel lain yang
mengandung PPD. Baku yang digunakan dalam penelitian ini merupakan baku
PPD dengan kemurnian 99,6% dan 100,0% berdasarkan Certificate of Analysis
(CoA) pada Lampiran 1 dan 2. Baku dengan kemurnian 99,6% diganti dengan
kemurnian 100,0% karena dalam proses optimasi yang dilakukan, sulit didapatkan
hasil pemisahan yang baik, sehingga peneliti mengganti baku yang digunakan
diperkirakan terjadi karena kemurnian baku yang kurang tinggi menyebabkan
banyak pengotor yang mengganggu pemisahan dan mengakibatkan proses
oksidasi baku PPD menjadi lebih cepat. Penanganan baku yang tidak tepat pada
awal penelitian juga mempercepat proses oksidasi baku PPD tersebut. Oleh sebab
itu, pada penggunaan baku 100,0%, peneliti berusaha menangani baku sebaik
mungkin dengan memisahkan sebagian kecil baku pada wadah yang berbeda dan
wadah baku diberi nitrogen setelah dibuka lalu ditutup rapat, kemudian disimpan
dalam lemari pendingin.
Pelarut baku PPD yang digunakan adalah natrium metabisulfit. Natrium
metabisulfit merupakan suatu serbuk kristal yang dapat larut dalam air, bersifat
sebagai reduktor, berfungsi sebagai antimikroba, antifungi, dan pengawet
makanan (Bareh, Shouk, and Kassem, 2011). Oleh karena itu, penggunaan
natrium metabisulfit dalam penelitian ini adalah sebagai antioksidan yang dapat
mencegah baku PPD mengalami oksidasi selama pemisahan dengan KCKT.
Penggunaan antioksidan sebagai pelarut PPD disebabkan oleh sifat PPD yang
mudah mengalami autooksidasi bila terpapar oksigen (Corbett, 1972).
B. Optimasi Jenis Fase Diam, Fase Gerak, Suhu Oven, dan Laju Alir KCKT
Variabel-variabel bebas yang dioptimasi dalam analisis ini sangat
berperan penting untuk penentuan kualitas pemisahan PPD. Oleh sebab itu,
optimasi sistem KCKT dengan mengubah variabel bebas tersebut diharapkan
1. Optimasi polaritas fase diam dalam analisis PPD dengan KCKT
Fase diam merupakan faktor yang sangat berperan penting dalam
optimasi karena menentukan retensi dan selektivitas. Retensi adalah tertahannya
analit pada fase diam dan selektivitas adalah kemampuan suatu metode untuk
mendeteksi analit yang diinginkan walaupun terdapat komponen lain dalam
sampel yang sama (Snyder, et al., 2010).
Fase diam yang digunakan dalam optimasi sistem KCKT dalam
penelitian ini ada lima macam, yaitu C18, C8, C2, diol, dan poliol silika.
Penggunaan fase diam C18, C8, dan C2 dengan fase gerak yang lebih polar akan
menghasilkan sistem KCKT fase terbalik dan sebaliknya, penggunaan fase diam
diol dan poliol silika dengan fase gerak yang lebih nonpolar akan menghasilkan
sistem KCKT fase normal.
2. Optimasi pH dan polaritas fase gerak dalam analisis PPD dengan KCKT Fase gerak pada penelitian ini terdiri dari komposisi metanol atau
asetonitril dan air atau air yang diberi dapar fosfat, serta asetonitril dan air yang
diberi amonia 10% atau asam asetat 0,05 M atau asam formiat. Optimasi fase
gerak dilakukan dengan menambah, mengurangi, atau mengubah komponen fase
gerak. Sistem elusi yang digunakan dalam penelitian ini adalah sistem isokratik
yaitu, komposisi fase gerak sama selama pengukuran berlangsung.
Metanol dan asetonitril digunakan sebagai kombinasi dengan air karena
pada pemisahan dengan fase normal (fase diam lebih polar daripada fase gerak),
kekuatan elusi meningkat seiring dengan meningkatnya polaritas fase gerak dan
daripada fase gerak), kekuatan elusi menurun dengan meningkatnya polaritas fase
gerak (Kealey and Haines, 2002) (Gambar 15). Polaritas (P’) air yang tinggi
(Tabel V) membuatnya menjadi eluen paling kuat pada KCKT fase normal karena
air berinteraksi dengan gugus polar fase diam, sehingga analit sulit berinteraksi
dengan fase diam dan akan terelusi lebih cepat, sebaliknya, air merupakan eluen
yang lemah pada KCKT fase terbalik karena sulit membasahi fase diam yang
nonpolar. Hal ini juga membuat fase gerak yang mengandung semakin banyak air
akan mempunyai waktu retensi yang semakin lama pada KCKT fase terbalik.
Kekuatan elusi pelarut pada fase diam polar dapat dilihat pula dari nilai εº (Tabel
V). Semakin tinggi εº, semakin kuat pelarut tersebut (Meyer, 2004). Oleh sebab
itu, kekuatan elusi fase gerak mempengaruhi pula nilai k. Semakin kuat suatu
komposisi fase gerak, semakin kecil nilai k puncak analit yang dihasilkan (Snyder
et al., 2010). Kombinasi metanol atau asetonitril dengan air berguna untuk
mengatur pemisahan analit yang lebih baik dibandingkan bila fase gerak hanya
terdiri dari air.
Gambar 15. Pengaruh komposisi asetonitril, metanol, dan tetrahidrofuran dalam air terhadap kekuatan elusinya pada KCKT fase terbalik (Meyer, 2004)
Gambar 16. Segitiga selektivitas fase gerak KCKT (Snyder et al., 2010)
Walaupun dengan mengubah perbandingan komponen fase gerak dapat
mengubah indeks polaritas (Lampiran 4) dan mempengaruhi kekuatan elusi dan
nilai k, tetapi perubahan tersebut tidak selektif, sehingga bila terdapat puncak
yang sangat menumpuk, bisa saja puncak tersebut terus menumpuk meskipun
polaritas fase gerak telah diubah secara signifikan. Pada kasus ini, akan lebih baik
mengubah selektivitas pelarut agar terjadi pemisahan yang baik. Terdapat dua cara
yang biasanya dilakukan, yang pertama yaitu mengubah jenis pelarut pada fase
gerak. Segitiga selektivitas fase gerak dapat menjadi panduan untuk memilih
pelarut tersebut (Harvey, 2000).
Pada Gambar 16, dapat dilihat segitiga selektivitas fase gerak KCKT
yang dibuat berdasarkan nilai dipolaritas (π*), keasaman (α), dan kebasaan (β)
masing-masing pelarut (Tabel V). Dipolaritas adalah ukuran kemampuan pelarut
berinteraksi dengan analit dengan kekuatan dipol dan polarisasi. Keasaman adalah
ukuran kemampuan pelarut untuk bertindak sebagai pendonor ikatan hidrogen
pelarut untuk bertindak sebagai akseptor ikatan hidrogen terhadap analit asam
(pendonor). Segitiga selektivitas tersebut menggambarkan bahwa pemilihan
kombinasi pelarut fase gerak lebih tepat bila dipilih pelarut yang tidak berada
pada area yang berdekatan supaya diperoleh selektivitas yang diinginkan (Meyer,
2004). Oleh sebab itu, dipilih pelarut asetonitril (ACN) yang merupakan pelarut
yang bersifat dipolar, serta metanol dan air yang bersifat sebagai pendonor H
untuk digunakan dalam pemisahan PPD untuk memodifikasi selektifitas fase
gerak agar pemisahan dapat berjalan dengan baik. Asetonitril yang bersifat dipolar
karena memiliki dipol positif pada atom C dari gugus nitril dapat berinteraksi
secara dipolar dengan PPD yang memiliki dipol negatif pada atom N. Metanol dan
air yang bersifat sebagai pendonor H dapat berinteraksi dengan PPD yang bersifat
basa (akseptor H).
Gambar 17. Distribusi bentuk molekul PPD dalam berbagai pH (ChemAxon, 2014)
Cara kedua untuk mengubah selektivitas fase gerak adalah dengan
mengubah pH. Analit yang bersifat asam lemah atau basa lemah akan berubah
Senyawa PPD merupakan analit yang dapat terionisasi pada pH tertentu (Gambar
17), sehingga pada pemisahannya menggunakan KCKT diperlukan dapar dalam
fase gerak agar dapat mempertahankan pH dan menghasilkan retensi yang
reprodusibel selama pemisahan (Snyder et al., 2010).
Tujuan pengubahan pH fase gerak adalah untuk mengamati pengaruh pH
pada pemisahan PPD menggunakan polaritas kolom tertentu. Pengaturan pH juga
penting pada pemisahan PPD menggunakan KCKT karena kecepatan
pembentukan produk oksidasi PPD (Bandrowski’s base) dipengaruhi pula oleh
peningkatan pH. Kecepatan oksidasi PPD meningkat pada pH > 8,5 (Corbett,
1972). Pada beberapa kombinasi komposisi fase gerak ditambahkan pula asam
asetat 0,05 M dan asam formiat dengan tujuan untuk mengatur pH fase gerak pada
suasana asam (± pH 5); dapar fosfat pH 7 pada suasana netral (± pH 7); amonia
10% pada suasana basa (± pH 8).
Nilai UV cut-off adalah panjang gelombang UV pelarut yang akan
memberikan serapan lebih dari 1,0 satuan absorbansi dalam kuvet 1 cm sehingga
dianjurkan untuk tidak menggunakan pelarut yang memiliki nilai UV cut-off
bertepatan atau mendekati panjang gelombang deteksi analit (Gandjar dan
Rohman, 2007). Air, metanol, dan asetonitril berturut-turut memiliki nilai UV
cut-off 170 nm, 205 nm, dan 190 nm (Tabel V) sehingga tidak mengganggu
pembacaan analit karena penelitian ini menggunakan detektor spektrofotometer
UV pada panjang gelombang cukup jauh dari nilai UV cut-off pelarut yaitu, 254
Viskositas fase gerak dapat mempengaruhi tekanan dan efisiensi kolom.
Semakin tinggi viskositas, semakin tinggi pula tekanan pada kolom, sebaliknya
semakin kecil nilai N. Maka dari itu, viskositas yang baik untuk fase gerak adalah
viskositas yang sekecil mungkin. Viskositas air, metanol, dan asetonitril
berturut-turut sebesar 0,89; 0,54; dan 0,34 cP. Kombinasi ketiga senyawa tersebut dapat
mempengaruhi viskositasnya. Tabel VI menyajikan data viskositas kombinasi fase
gerak antara metanol dan air serta asetonitril dan air dalam satuan cP pada
berbagai suhu.
Tabel VI. Viskositas kombinasi fase gerak metanol:air (baris atas) dan asetonitril:air (baris bawah) pada suhu tertentu (B = komposisi organik) (Snyder et al., 2010)
Partikel-partikel pengotor dalam fase gerak harus dihilangkan karena
dapat mengganggu proses analisis dan pembacaan analit karena partikel tersebut
dapat menyumbat pori-pori kolom. Oleh karena itu, fase gerak harus disaring
menggunakan kertas Whatman terlebih dahulu sebelum digunakan. Keberadaan
gas dalam fase gerak juga dapat mengganggu pembacaan analit (Gandjar dan
Rohman, 2007). Fase gerak di-degassing (dihilangkan gasnya) dengan