LAMPIRAN
Lampiran 1. Proses pengeringan getah kemenyan (Styrax spp.)
Lampiran 2. Pengujian kadar air
a) Sampel sebelum dioven b) Sampel setelah dioven
Lampiran 3. Pengujian kadar abu
Lampiran 4. Pengujian kadar kotoran
Lampiran 5. Pengujian titik lunak
Lampiran 6. Pengujian kadar asam sinamat
b) Sampel uji dalam larutan air dan MgSO4
c) Penyaringan larutan
e) Hasil Penguapan Kloroform
f) Contoh Uji dalam Larutan Etanol Netral
Lampiran 7. Ekstrak kental pengujian skrining fitokimia
a) Pemisahan filtrat dan residu ekstrak etanol
DAFTAR PUSTAKA
Akiyama, H., Fujii, K., Yamasaki, O., Oono, T., and Iwatsuki, K. Antibacterial Action Of Several Tennis Agains Staphylococcus aureus. Journal Of Antimicrobial Chemoterapy. Vol.48:487-91.
Arbi, J. 2010. Karakterisasi Simplisia dan Skrining Fitokimia Serta Uji Aktivitas Antimikroba Ekstrak Etanol Daun dan Getah Kemenyan (Styrax benzoin Dryland.) Terhadap Beberapa Mikroba. Skripsi. Universitas Sumatera Utara. Medan.
Atmoko, T. dan Ma’ruf, A. 2009. Uji Toksisitas dan Skrining Fitokimia Ekstrak Tumbuhan Sumber Pakan dan Orangutan Terhadap Larva Artemia Salina L. Jurnal Penelitian dan Konservasi Alam. Vol 6:37-45.
Azizah, B. dan Salamah, N. 2013. Standarisasi Parameter Non Spesifik dan Perbandingan Kadar Kurkumin Ekstrak Etanol dan Ekstrak Terpurifikasi Rimpang Kunyit. Jurnal Ilmiah Kefarmasian. Vol No.1 No.3, 2013:21-30. BPS. 2011. Tapanuli Utara Dalam Angka 2011. Badan Pusat Statistik Kabupaten
Tapanuli Utara.
Botanical Dermatology Database. 2004. Styracaceae (Styrax family). Botanical Dermatology Databas Brahmana, H.R., Bangun, N. dan Ginting, M. 1981. Penentuan Kadar Asam
Sinamat dari Kemenyan Tapanuli (Styrax Sumaterana J.J Sm). Penelitian FMIPA USU.
Darusman, D. 2001. Resiliensi kehutanan Masyarakat di Indonesia. Debut Press. Yogyakarta.
Dede. 1998. Pengelolaan Hutan Rakyat Kemenyan (Styrax spp.) dan kontribusinya Terhadap Pendapatan Rumah Tangga. Kehutanan Masyarakat; Beragam Pola Partisipasi Masyarakat Dalam Pengelolaan Hutan; Kerjasama IPB dan The Ford Foundation. CV. Dewi Sri Jaya. Bogor.
Departemen Kehutanan dan Perkebunan. 1999. Budidaya Tanamana Kemenyan. Jakarta.
Ditjen POM. 1979. Farmakope Indonesia. Edisi Ketiga. Departemen Kesehatan RI. Jakarta. Hal 29-31.
Ditjen POM. 1995. Materia Medika Indonesia, Jilid VI. Departemen Kesehatan RI. Jakarta. Hal 321-326, 333-337.
Farnsworth, N.R. 1996. Biological and Phytochemical Screening of Plants. Journal of Pharmaceutical Sciences. Vol 55(3):263.
Harbone, JB. 1987. Metode Fitokimia. Padmawinata K, Soediro I, Penerjemah. Bandung : ITB. Terjemahan dari: Phytochemical Methods oleh Kosasih Padmawinata dan Iwang Soediro. Penerbit ITB. Bandung. Hal 47-245. Harjadi, W. 1986. Ilmu Kimia Analitik Dasar. Jakarta. PT Gramedia Pustaka
Umum.
Hughes, I. 2002. The Resins of the BP and BPC.
Hutapea, J.R. 1994. Inventaris Tanaman Obat Indonesia. Edisi Ketiga. Jakarta. Departemen Kesehatan RI. Hal 279.
Pasaribu, J.R., dan Sipayung, W. 1999. Budidaya Kemenyan (Styrax spp.) Pedoman Teknis Konifera. Vol 2:1. Badan Penelitian dan Pengembangan Kehutanan dan Perkebunan. Balai Penelitian Kehutanan Pematang Siantar. Jayusman. 2014. Mengenal Pohon Kemenyan (Styrax spp.) Jenis dengan
Spektrum Pemanfaatan Luas yang Belum Dioptimakan. IPB Press. Bogor. Khan, M.L. 2001. Loban (Styrax Benxoine). Known as an incense, Loban has
mutipli benefits even as an medicine 22 februari 2015.
Kiswandono, A.A. 2008. Pengaruh Proses Maserasi dan Refluks Pada Daun dan Biji Kelor (Moringa Oleifera, lamk) Terhadap Identifikasi dan Rendemen Senyawa Bioaktif yang Dihasilkan. Hasil Penelitian. Universitas Tri Karya Medan.
Lenny, S. 2006. Senyawa Flavonoida, Fenilpropanoida dan Alkaloida. Karya Ilmiah FMIPA. Universitas Sumatera Utara.
Lumingkewas, M., Manarisip, J., Indriaty, F., Walangitan, A., Mandei, J., dan Suryanto, E. 2014.Aktivitas Antifotooksidan dan Komposisi Fenolik dari Daun Cengkeh (Eugenia aromatic L.) .Chem. Prog Vol.7 No.2, November 2014.
Markham, K.R. 1998. Cara Mengidentifikasi Flavonoid. ITB Press. Bandung. Nurachman, Z. 2002. Artoindonesianin untuk Antitumor
Diakses 20 Oktober 2015.
Pinyopusarerk. 1994. Styrax tonkineenses. Taxonomy, ecology, silviculture and Uses. The Australian Centre For Internasional Agriculture Research (Aciar). Technical Report No.31. Canberra.
Prat DE, BJF. Hudson. 1990. dalam Kiswandono (2008). Pengaruh Proses Maserasi dan Refluks Pada Daun dan Biji Kelor (Moringa Oleifera, lamk) Terhadap Identifikasi dan Rendemen Senyawa Bioaktif yang Dihasilkan. Hasil Penelitian. Universitas Tri Karya Medan.
Purbaya, M., Sari, T.I., Saputri, C.A., dan Fajriaty, M.T. 2011. Pengaruh Beberapa Jenis Bahan Penggumpal Lateks dan Hubungannya dengan Susut Bobot, Kadar Karet Kering dan Plastisitas. Prosiding Seminar nasional AvoER ke-3. ISBN: 979-587-395-4.
Redha, A. 2014. Flavonoid: Struktur, Sifat Antioksidatif dan Peranannya dalam Sistem Biologis. Vol.9 No.2 Sep.2010:196-202.
Robinson, T. 1995. Kandungan Organik Tumbuhan Tingkat Tinggi. ITB Press. Bandung.
Rodiani, T. dan Suprijadi. 2013. Analisis Titrimetri dan Gravimetri. Kementerian Pendidikan Nasional. Pusat Pengembangan dan Pemberdayaan Pendidik dan Tenaga Kependidikan Pertanian Cianjur.
Romansyah, Y. 2011. Kandungan Senyawa Bioaktif Antioksidan Karang Lunak Sarcophyton sp. Alami dan Transplantasi di Perairan Pulau Pramuka, Kepulauan Seribu. Skripsi. Fakultas Perikanan dan Ilmu Kelautan IPB. Rudyanto, M. 2008. Synthesis of Some Cinnamic Acid Derivatives : Effect of
Groups Attached on Aromatic Ring to the Reactivity of Benzaldehyde. Indo.J.Chem.,2008, 8(2), 226-230.
Rusdi. 1998. Tumbuhan sebagai Sumber Bahan Obat. Pusat Penelitian Universitas Andalas. Padang.
Santosa, G. 2010.Pemanenan Hasil Hutan Bukan Kayu : Penyadapan Getah Pinus. Institut Pertanian Bogor. Bogor.
Sasmuko, S.A. 1999. Karakteristik Kemenyan Sumatera Utara dan Laos. Prosiding Expose Hasil Penelitian Balai Penelitian Kehutanan Pematang Siantar, 30 Maret 1999 di Medan. Hlm 57-67. Balai Penelitian Kehutanan, Pematang Siantar.
Sasmuko, S.A. 2003. Potensi Pengembangan Kemenyan sebagai Komoditi Hasil Hutan Bukan Kayu Spesifik Andalan Sumatera Utara. Makalah Seminar Nasional Himpinan Alumni-IPB HAPKA Fakultas Kehutanan IPB Wilayah Regional Sumatera. Medan.
Sitinjak, H. 2012. Analisis Sifat Fisika-Kimia Kemenyan (Styrax Sumaterana J.J. SM) Asal Pengururan. Skripsi. Fakultas Kehutanan USU.
Sirait, M. 2007. Penentuan Fitokimia dalam Farmasi. ITB. Bandung. Standar Nasional Indonesia. Kemenyan (SNI 7940:2013).
Stahl, E. 1985. Analisis Obat secara Kromatografi dan Mikroskopik. ITB Press. Bandung.
Suradikusuma, E. 1989. Kimia Tumbuhan Depdikbud. Dirjen Pendidikan Tinggi. Pau. Ilmu Hayat IPB. Bogor.
Thomson, R.H. 1993. The Chemistri Of Natural Producst. 2 Edition,chapman and hall ltd.glasgow,UK.
Van Steenis. 1953. dalam Jayusman (2014). Mengenal Pohon Kemenyan (Styrax spp.) Jenis dengan Spektrum Pemanfaatan Luas yang Belum Dioptimakan. IPB Press. Bogor.
Waluyo, T.K., Hastoeti, P., dan Prihatiningsih, T. 2006. Karakteristik dan Sifat Fisika-Kimia Berbagai Kualitas Kemenyan Di Sumatera Utara. Jurnal Penelitian Hasil Hutan 24 (1) : 47-61. Pusat Penelitian dan Pengembangan Hasil Hutan. Bogor.
Wibowo, C. 2012. Analisis Sebaran Iklim Klasifikasi Schmidt-Ferguson Menggunakan Sistem Informasi Geografis di Kabupaten Bantaeng Sulawesi-Selatan. Skripsi. Teknologi Pangan Universitas Hasanuddin.
Widiarto, S. 2009. Volumetri/Titrimetr Oktober 2015.
METODE PENELITIAN
Waktu dan Tempat Penelitian
Penelitian ini dilakukan pada bulan Mei sampai September 2015. Penelitian ini dilaksanakan di Laboratorium Kimia Organik Fakultas Matematika dan Ilmu Pegetahuan Alam, Universitas Sumatera Utara. Tempat pengambilan sampel dilakukan di kawasan Hutan Batang Toru Blok Barat, Kecamatan Adiankoting, Kabupaten Tapanuli Utara, Provinsi Sumatera Utara.
Bahan dan Alat Penelitian
Bahan yang digunakan pada penelitian ini adalah getah kemenyan (Styrax spp.) yang terdiri dari tiga jenis yaitu kemenyan Toba (Styrax paralleloneurum PERK), kemenyan Durame (Styrax benzoine Dryland), dan
kemenyan Bulu (Styrax benzoine var hiliferum). Bahan kimia yang digunakan adalah bahan-bahan kimia berkualitas pro analisis antara lain akuades, amonia, asam klorida, asam sulfat, aseton, dietil eter, etanol, ferri klorida, indikator fenoltalein, kalium hidroksida, kloroform, magnesium sulfat, metanol, natrium bikarbonat, natrium hidroksida, pereaksi (dragendorff, liebermann-burchad, mayer, dan wagner).
24
panci, pipet tetes, spatula, tanur, termometer, timbangan digital, lampu spiritus, buret, dan tiang statif.
Prosedur Penelitian
Pengambilan sampel
Pengambilan sampel dilakukan secara acak tanpa membandingkan kualitasnya. Sampel yang digunakan dalam penelitian ini adalah getah kemenyan (Styrax spp.) yang diperoleh dari kawasan sekitar Hutan Batang Toru Blok Barat, Kecamatan Adiankoting, Kabupaten Tapanuli Utara, Provinsi Sumatera Utara.
Persiapan bahan baku
Pada tahapan ini sampel getah kemenyan (Styrax spp.) dikering-anginkan dengan cara disebar di atas karton. Sampel dikeringkan di areal yang teduh dan tidak terkena sinar matahari hingga kering dan rapuh. Setelah kering sampel dihaluskan dengan cara ditumbuk sampai menjadi serbuk.
Pembuatan larutan
1. Pereaksi Mayer
Sebanyak 1,4 gr raksa (II) klorida dilarutkan dalam air suling hingga 60 ml, pada wadah lain ditimbang sebanyak 5 gr kalium iodida lalu dilarutkan dalam 10 ml air suling, kedua larutan dicampurkan dan ditambahkan air suling hingga diperoleh larutan 100 ml (Ditjen POM, 1995)
2. Pereaksi Drangendorf
didiamkan sampai memisah sempurna. Larutan yang jernih diambil dan diencerkan dengan air suling hingga volume larutan 100 ml (Ditjen POM, 1995). 3. Pereaksi Wagner
Sebanyak 10 ml akuades dipipet kemudian 2,5 gr iodin dan 2 gr kalium iodida lalu dilarutkan dan diencerkan dengan akuades menjadi 200 ml dalam labu takar (Romansyah, 2011).
4. Pereaksi Liebermann-Burchard
Sebanyak 0,6 gr bismut subnitrat dalam 2 ml HCl pekat dan 10 ml akuades. Di wadah lain sebanyak 6 gr kalium iodida dilarutkan dalam 10 ml akuades. Kedua larutan tersebut dicampur dengan 7 ml HCl pekat dan 15 ml akuades (Harborne, 1987).
5. Larutan NaOH 0,1 N
Sebanyak 4 gr natrium hidroksida dilarutkan dalam 100 ml air suling (Ditjen POM, 1979).
6. Larutan H2SO4 2 N
Sebanyak 5,4 ml larutan asam sulfat pekat ditambahkan air suling sampai 100 ml (Ditjen POM, 1995).
7. Larutan Etanol Netral
Sejumlah etanol (95%) Pekat ditambahkan 0,5 ml larutan fenolftalein pekat dan natrium hidroksida 0,02 atau 0,1 N secukupnya hingga larutan berwarna merah jambu. Etanol netral pekat harus dibuat baru (Ditjen POM, 1979).
8. Larutan Indikator Fenolftalein
26
9. Larutan KOH-Etanol 0,5 N
Sebanyak 7 gr dan dilarutkan dengan etanol dalam labu takar 250 ml sampai garis batas dan distandarisasi dengan menggunakan larutan H2C2O4 0,1 N
dan indikator fenolftalein.
Pengujian visual
1. Warna
Mutu didasarkan pada penampilan warna sebagaimana dilihat pada tabel 4 :
Tabel 4. Klasifikasi getah kemenyan dengan parameter warna
Parameter Kelas Mutu
A B C
Warna Putih Bersih Putih kecoklatan
(50% putih 50% coklat)
Coklat keputihan (25% putih 75% coklat)
2. Kadar Air
Pengujian kadar air dilakukan dengan cara melihat butiran tidak lengket satu sama lain dan jika dipegang tidak lengket di tangan, serta rapuh apabila dipatahkan dengan tangan.
Pengujian laboratorium
1. Kadar air
Contoh uji kemenyan ditimbang 2 gram dimasukkan ke dalam cawan porselin yang telah diketahui bobot kosongnya. Kemudian cawan tersebut dipanaskan di dalam oven pada suhu 105 ᵒC selama 3 jam. Setelah itu didinginkan di dalam desikator dan ditimbang untuk mengetahui bobot keringnya, pemanasan contoh uji diulang sampai diperoleh bobot yang kosntan. Kadar air dihitung dengan rumus :
Kadar air = B – C
Keterangan :
A = Bobot cawan kosong (gram)
B = Bobot cawan + sampel sebelum pengeringan (gram) C = Bobot cawan + sampel setelah pengeringan (gram) 2. Kadar abu
Contoh uji kemenyan ditimbang 3 gram dimasukkan ke cawan porselin yang sudah diketahui beratnya. Selanjutnya dimasukkan ke tanur dengan suhu + 625 ᵒC sampai menjadi abu. Cawan didinginkan dan ditimbang sampai berat tetap. Kadar abu dihitung dengan rumus :
Kadar abu = W1 – W
W2 – W x 100% Keterangan :
W = Bobot cawan kosong (gram) W1 = Bobot cawan + abu (gram) W2 = Bobot cawan + kemenyan (gram) 3. Kadar kotoran
Contoh uji kemenyan ditimbang 2 gram dimasukkan ke dalam erlenmeyer 100 ml dan dilarutkan dengan 25 ml aseton. Larutan disaring dengan kertas saring. Residu kemenyan yang tertinggal dicuci dengan aseton dan dikeringkan pada suhu (105 + 3) ᵒC selama 6 jam hingga bobot tetap. Kadar kotoran dihitung dengan rumus :
Kadarkotoran = W2 – W1
W x 100% Keterangan :
28
W1 = Bobot kertas saring (gram)
W2 = Bobot kertas saring ditambah bahan tak larut aseton (gram) 4. Titik lunak
Contoh uji kemenyan ditimbang 0,02 gram dimasukkan ke dalam pipa kapiler yang terlebih dahulu salah satu ujungnya ditutup. Kemudian pipa kapiler dan termometer di letakkan dalam alat melting point. Lalu diamati dan dicatat suhu (ᵒC) yang tertera pada termometer saat contoh uji mulai meleleh sampai contoh uji meleleh secara keseluruhan.
5. Kadar asam sinamat
dinetralkan kemudian didinginkan. Indikator fenolftalein ditambahkan dan dititrasi dengan NaOH 0,1 N. Kemudian dihitung titer NaOH yang habis terpakai. Kadar asam sinamat dihitung dengan rumus :
Kadar asam sinamat = V x N x 148,2
W x 100%
Keterangan :
V = Volume NaOH yang habis terpakai (ml) N = Normalitas larutan NaOH (mg/ml) 148,2 = Bobot molekul asam sinamat W = Bobot contoh uji (mg)
Skrining Fitokimia
Contoh uji kemenyan ditimbang 25 gram dan direndam dalam etanol 100
ml selama 24 jam. Larutan tersebut disaring, kemudian residu hasil penyaringan dibuang. Sementara etanol pada filtrat hasil penyaringan diuapkan sampai terbentuk ekstrak kental yang akan digunakan sebagai contoh uji untuk menentukan jenis metabolit sekunder. Skrining fitokimia meliputi pemeriksaan senyawa golongan alkaloida, flavonoid, senyawa fenolik, saponin, tanin, dan triterpenoid/steroid sebagai berikut :
1. Alkaloid
Sebanyak 0,3 gram contoh uji dilarutkan dalam 10 ml kloroform-amonia lalu disaring. Fitrat hasil penyaringan ditambahkan beberapa tetes H2SO4 2M,
30
jingga dengan pereaksi dragendorff, dan endapan coklat dengan pereaksi wagner, maka sampel tersebut positif mengandung alkaloid (Suradikusuma et al., 1998). 2. Flavonoid dan Senyawa Fenolik
Sebanyak 0,5 gram contoh uji ditambahkan metanol 30% sampai terendam kemudian dipanaskan. Filtratnya ditambahkan NaOH 10% dan H2SO4. Warna
merah yang terbentuk karena penambahan NaOH 10% menunjukkan terdapatnya senyawa fenolik hidrokuinon, sedangkan warna merah yang terbentuk akibat penambahan H2SO4 pekat menunjukkan terdapatnya senyawa flavonoid
(Harbone, 1987). 3. Saponin
Sebanyak 0,5 gram contoh uji di dalam gelas piala ditambahkan 50 ml air panas dan dididihkan selama 5 menit, kemudian disaring. Setelah itu larutan akan diuji saponin dan tanin. Filtrat hasil penyaringan sebanyak 10 ml diambil dan dimasukkan ke dalam tabung reaksi tertutup selama 10 menit, terbentuknya busa yang stabil menandakan adanya saponin (Kiswandono, 2008).
4. Tanin
Sebanyak 10 ml filtrat yang dihasilkan pada pengujian saponin, ditambahkan FeCl3 1%. Identifikasi tanin yang positif ditandai dengan adanya
warna biru tua atau hijau kehitaman (Kiswandono, 2008). 5. Triterpenoid/steroid
asam asetat anhidrida dan 1 tetes H2SO4 pekat). Adanya warna merah atau ungu
32
HASIL DAN PEMBAHASAN
Persiapan Bahan Baku
Pengeringan bahan baku dilakukan dengan cara pengeringan secara alami yaitu dengan dikeringanginkan di udara terbuka sampai getah kemenyan kering dan getas. Pengeringan bertujuan untuk mengurangi kandungan air disamping mencegah pertumbuhan mikroorganisme dalam bahan baku yang disebabkan karena kandungan air yang tinggi pada sampel jika tidak dikeringkan (Kiswandono, 2008).
Getah kemenyan yang sudah kering dibuat menjadi serbuk dengan dihaluskan menggunakan alu dan mortal. Tujuan dari dihaluskannya getah kemenyan adalah untuk memperluas permukaan bahan baku sehingga pada tahap ekstraksi, interaksi antara pelarut pengekstrak dengan sampel yang diekstraksi menjadi lebih efektif dan pelarut pengekstrak akan lebih mudah mengambil zat-zat yang terkandung dalam getah.
Gambar 6. Serbuk getah kemenyan (a) Toba (b) Durame (c) Bulu
Pengujian Visual
Warna dan kadar air
air dilakukan dengan melihat antara butiran getah kemenyan tidak lengket satu sama lain. Hasil pengamatan warna dan kadar air pada getah kemenyan Toba, Durame, dan Bulu sebagaimana dilihat pada tabel 5.
Tabel 5. Pengamatan visual getah parameter warna dan kadar air
Jenis Getah Kemenyan Warna Kadar Air
Kemenyan Toba
(Styrax paralleloneurum PERK)
Putih kekuningan Rapuh/antara butiran tidak lengket
Kemenyan Durame (Styrax benzoine Dryland)
Putih kuning kecoklatan
Rapuh/antara butiran tidak lengket
Kemenyan Bulu
(Styrax benzoine var hiliferum)
Coklat kehitaman Rapuh/antara butiran tidak lengket
Gambar 7. Pengamatan visual getah kemenyan (a) Toba (b) Durame (c) Bulu
Berdasarkan pengamatan pada warna yang dilakukan diperoleh data pada Tabel diatas. Getah kemenyan Toba pada pengamatan berwarna putih kekuningan, kemenyan Durame berwarna putih kuning kecoklatan, sedangkan pada kemenyan Bulu berwarna coklat kehitaman. Pada semua getah kemenyan belum memenuhi persyaratan visual SNI 7940:2013. Hal ini kemungkinan dipengaruhi oleh adanya kotoran yang menempel pada kemenyan pada saat penyadapan yang belum dibersihkan. Kotoran tersebut dapat berupa pasir, serpihan kulit batang dan lain-lain.
34
apabila dipatahkan dengan tangan hal tersebut dipengaruhi proses pengeringan getah kemenyan. Pada proses pengeringan yang dilakukan getah kemenyan dihamparkan diatas karton dengan tumpukan yang tidak terlalu tinggi. Kemudian getah kemenyan dibuat diruangan yang dapat dimasuki oleh udara. Getah kemenyan tidak dapat dikeringkan dengan sinar matahari dikarenakan getah kemenyan akan kembali menjadi lembek dan meleleh kembali. Pengeringan dilakukan sampai getah kemenyan benar-benar kering dan getas. Pada penelitian ini lama pengeringan getah kemenyan berkisar + dua bulan. Pada pengujian kadar air telah memenuhi persyaratan visual getah kemenyan SNI 7940:2013.
Pengujian Laboratorium
Kadar air
Hasil pengujian kadar air yang diperoleh disajikan pada gambar berikut.
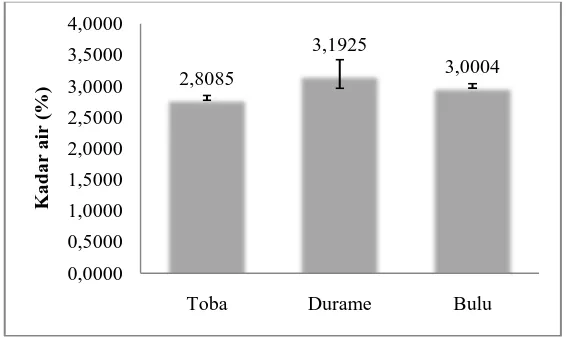
Gambar 8. Pengujian kadar air
Berdasarkan data pengujian kadar air yang dilakukan hasil yang didapatkan pada setiap jenis kemenyan berbeda-beda. Rata-rata persen kadar air tertinggi pada getah kemenyan Durame yaitu 3,1925% sedangkan persen kadar air terendah pada getah kemenyan Toba yaitu 2,8085%. Penurunan bobot sampel yang cepat menunjukkan mudahnya air keluar dari getah kemenyan sehingga
perhitungan persen kadar air yang diperoleh juga relatif rendah. Demikian juga sebaliknya penurunan bobot sampel yang lambat menunjukkan sulitnya air keluar dari kemenyan, sehingga persen kadar air yang diperoleh relatif tinggi.
Penetapan kadar air dilakukan untuk memberikan batasan minimal kandungan air yang masih ditolerir di dalam getah maupun ekstrak. Penentuan kadar air berguna untuk menduga keawetan atau ketahanan sampel dalam penyimpanan serta untuk mengoreksi rendemen yang dihasilkan. Kadar air sampel bahan alam biasanya harus lebih rendah dari 10% agar bakteri atau jamur tidak tumbuh sehingga sampel dapat disimpan dalam waktu yang lama (winarmo, 1997). Pengujian kadar air pada getah kemenyan yang dilakukan telah memenuhi syarat SNI 7940:2013 dengan kadar air maksimun 5%.
Pengujian kadar air ditetapkan dengan cara gravimetri, yaitu diperoleh dengan cara menghitung bobot bahan sebelum dan sesudah dikeringkan pada temperatur di atas titik didih air. Sehingga diharapkan semua air akan menguap pada suhu tersebut dan pada periode waktu tertentu (Harjadi, 1986).
Kadar abu
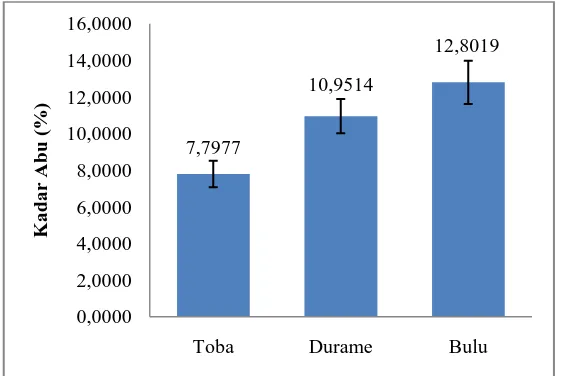
Hasil pengujian kadar yang diperoleh disajikan pada gambar berikut.
36
Berdasarkan pengujian kadar abu yang dilakukan pada setiap jenis kemenyan rata-rata persen kadar abu tertinggi terdapat pada getah kemenyan Bulu yaitu 12,8018% sedangkan persen kadar abu terendah terdapat pada getah Toba yaitu 7,7977%. Kandungan getah kemenyan tentu berbeda-beda persentasenya untuk setiap jenis. Pada proses pemanasan untuk mendapatkan kadar abu, kandungan getah kemenyan yang ada mengalami penguapan sehingga menyisakan bahan-bahan atau materi yang tidak menguap. Hal ini sesuai dengan pernyataan Azizah (2013) yang menyatakan bahwa penetapan kadar abu dilakukan dengan pengabuan di dalam tanur bersuhu + 625 ᵒC. Sampel yang berada dalam tanur mengalami pemanasan pada temperatur dimana senyawa organik dan turunannya terdestruksi dan menguap sehingga yang tertinggal hanya unsur mineral dan anorganik. Selain itu penetapan kadar abu juga dimaksudkan untuk mengontrol jumlah pencemar benda-benda organik seperti tanah, pasir yang seringkali terikut dalam sampel.
7940:2013 yang mensyaratkan persen kadar abu untuk mutu A dan B < 1 dan mutu C berkisar antara > 1- < 2.
Kadar kotoran
Hasil pengujian kadar kotoran yang diperoleh disajikan pada gambar berikut.
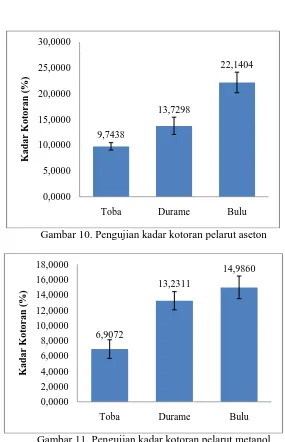
Gambar 10. Pengujian kadar kotoran pelarut aseton
Gambar 11. Pengujian kadar kotoran pelarut metanol
Berdasarkan pengujian kadar kotoran yang dilakukan dengan menggunakan pelarut aseton dapat dilihat bahwa rata-rata persen kadar kotoran tertinggi terdapat pada getah kemenyan Bulu yaitu 22,1402% sedangkan persen kadar kotoran terendah pada kemenyan Toba yaitu 9,7438%. Berdasarkan
38
pengujian kadar kotoran yang dilakukan dengan pelarut metanol dapat dilihat bahwa rata-rata persen kadar kotoran tertinggi terdapat pada getah kemenyan Bulu yaitu 14,9860% sedangkan persen kadar kotoran terendah pada kemenyan Toba yaitu 6,9072 %. Pada pengujian kadar kotoran pelarut yang digunakan ada dua yaitu pelarut aseton dan metanol. Penggunaan dua pelarut ini dimaksudkan sebagai perbandingan.
Pada data yang dihasilkan dapat dilihat bahwa pengujian kadar kotoran dengan pelarut metanol lebih baik. Getah kemenyan lebih larut dalam pelarut metanol hal ini terlihat dari persen kadar kotoran yang relatif lebih rendah. Sedangkan dengan menggunakan pelarut aseton persen kadar kotoran yang dihasilkan relatif lebih tinggi. Pada pengujian ini dapat dilihat bawah jenis pelarut yang digunakan berpengaruh terhadap persen kadar kotoran yang dihasilkan. Hal ini kemungkinan disebabkan karena senyawa yang terdapat dalam getah kemenyan ini lebih banyak yang bersifat polar dibandingkan bersifat semipolar. Metanol merupakan salah satu pelarut yang bersifat polar, sedangkan aseton adalah pelarut yang bersifat semipolar (Lumingkewas et al, 2014).
kotorannya, karena semakin kecil ukurannya maka semakin sulit dilakukan pemisahan kemenyan dengan kotoran-kotoran yang ada. Persen kadar kotoran yang dihasilkan belum memenuhi SNI 7940:2013 yang mensyaratkan persen kadar kotoran untuk mutu A dan B < 1 dan mutu C berkisar antara > 1 - < 5.
Titik lunak
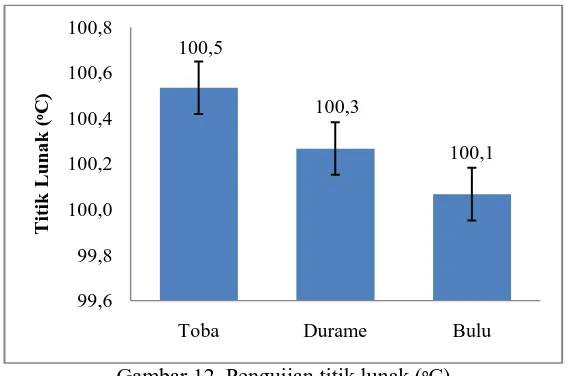
Hasil pengujian titik lunak yang diperoleh disajikan pada gambar berikut.
Gambar 12. Pengujian titik lunak (ᵒC)
Berdasarkan pengujian yang dilakukan diperoleh data titik lunak getah kemenyan dimana rata-rata derajat titik lunak tertinggi terdapat pada getah kemenyan Toba yaitu 100,5 ᵒC sedangkan rata-rata derajat titik lunak terendah pada getah kemenyan Bulu yaitu 100,1 ᵒC. Getah kemenyan pada pengujian kadar air, kadar abu, dan kadar kotoran memiliki hubungan terbalik dengan pengujian titik lunak yaitu semakin tinggi kadar air, kadar abu, dan kadar kotoran getah maka semakin rendah titik lunak yang diperoleh. Demikian juga sebaliknya semakin rendah kadar air, kadar abu, dan kadar kotoran getah maka semakin tinggi titik lunak yang diperoleh. Hal ini sesuai dengan pernyataan Sitinjak (2012) yang menyatakan bahwa pengujian titik lunak berhubungan dengan tingkat kemurnian getah kemenyan.
40
Penentuan derajat titik lunak dilakukan dengan metode pipa kapiler yaitu dengan termometer dan pipa kapiler dimasukkan ke dalam alat melting point. Kemudian dicatat suhu saat sampel mulai meleleh dan saat sampel meleleh secara keseluruhan. Titik lunak ditunjukan dengan perubahan bentuk getah kemenyan dari zat padat menjadi cair (meleleh). Perubahan wujud getah kemenyan terjadi pada suhu yang berbeda-beda pada setiap jenisnya. Titik lunak atau titik leleh adalah temperatur dimana zat padat berubah wujud menjadi zat cair pada tekanan 1 atm atau suhu ketika fase padat dan cair sama-sama berada dalam keadaan kesetimbangan (Sitinjak, 2012). Derajat titik lunak yang dihasilkan telah memenuhi SNI 7940:2013 yang mensyaratkan derjat titik lunak untuk mutu A > 92, mutu B > 88 dan mutu C > 80.
Kadar asam sinamat
Hasil pengujian kadar asam sinamat yang diperoleh disajikan pada gambar berikut.
Gambar 13. Pengujian kadar asam sinamat
Berdasarkan gambar 13 Persen kadar asam sinamat tertinggi pada getah kemenyan Toba sebesar 40,1515% dan persen kadar asam sinamat terendah pada
getah kemenyan Bulu yaitu 15,3561%. Kadar asam sinamat menunjukkan tingkat kemurnian suatu kemenyan (Sitinjak, 2012). Pada setiap jenis kemenyan persen kadar asam sinamat yang diperoleh bervariasi. Hal ini dikarenakan setiap jenis kemenyan memiliki tingkat kemurnian yang berbeda-beda. Kemurnian dari getah kemenyan dapat dipengaruhi oleh faktor pengotor seperti kulit batang, pasir, tanah yang melekat pada getah. Kemurnian getah kemenyan semakin rendah karena semakin sulit memilah antara getah dan kotoran (Waluyo et al, 2006).
Menurut Hughes (2002) kadar asam sinamat yang terdapat pada getah kemenyan bebas minimal 11%. Kadar asam sinamat hasil pengujian pada getah kemenyan semuanya jauh di atas 11% sehingga hasil penelitian ini memenuhi persyaratan minimal kadar asam sinamat yang terkandung dalam getah. Hal ini menunjukkan bahwa pengujian yang dilakukan telah berhasil dengan baik.
Menurut Khan (2001) bahan getah kemenyan mengandung asam sinamat, asam benzoat, stirol, vanilin, stiracin, koniferilbenzoat, koniferilsinamat, resin benzoeresinol, dan suma resinotannol. Menurut Brahmana et al (1981) Asam sinamat merupakan faktor yang sangat penting dalam penentuan mutu dan harga getah kemenyan. Senyawa asam sinamat ini memberikan bau yang spesifik pada getah kemenyan (Lubis et al, 1984).
42
dihasilkan telah memenuhi SNI 7940:2013 yang mensyaratkan persen kadar asam sinamat untuk mutu A > 30, mutu B berkisar antara 21-29, dan mutu C < 20.
Skrining Fitokimia
Hasil pengujian fitokimia pada sampel getah kemenyan sebagaimana dilihat pada tabel 6.
Tabel 6. Hasil uji skrining fitokimia
Uji Fitokimia Jenis Kemenyan
Toba Durame Bulu
Skrining merupakan langkah awal dari pemeriksaan tumbuhan untuk
membuktikan ada tidaknya senyawa kimia tertentu dalam tumbuhan. Pengujian fitokimia dilakukan sebagai skrining awal untuk mengetahui kandungan metabolit
sekunder pada getah kemenyan. Pengujian yang dilakukan yaitu uji alkaloid, flavonoid dan senyawa fenolik, saponin, tanin, dan triterpenoid/steroid.
Gambar 14. Pengujian alkaloid (a) Toba (b) Durame (c) Bulu
Pada pengujian alkaloid penambahan pereaksi Mayer akan menyebabkan terbentuknya endapan berwarna putih yang menunjukkan hasil yang positif mengandung senyawa alkaloid proses yang sama juga dilakukan pada penambahan reaksi Dragendorff, dan Wagner. Pada pereaksi Dragendorff akan terbentuk endapan berwarna merah jingga sedangkan untuk pereaksi Wagner akan terbentuk endapan berwarna coklat. Menurut Sangi et al (2012) pereaksi Mayer mengandung merkuri klorida dan kalium iodida. Pereaksi Drangendorff mengandung kalium iodida dan bismuth subnitrat dalam asam asestat glasial. Hampir semua alkaloid yang ditemukan dialam mempunyai keaktifan biologis tertentu, ada yang sangat beracun tetapi ada pula yang sangat berguna dalam pengobatan. Jenis dan konsetrasi alkaloid dapat menjadi sangat beracun, salah satu jenis alkaloid yang sangat beracun yaitu nikotin. Alkaloid memiliki kegunaan di bidang medis antara lain sebagai analgetika dan narkotika, mengubah kerja jantung, penurunan tekanan darah, obat asma, sebagai antimalaria, stimulan uterus dan anestesi lokal (Sirait, 2007).
44
endapan pada seluruh sampel baik getah kemenyan Toba, Durame, dan Bulu. Hal ini menunjukkan bahwa pada sampel getah kemenyan Toba, Durame, dan Bulu hanya mengandung alkaloid dalam jumlah yang sangat sedikit.
Gambar 15. Pengujian flavonoid dan fenolik (a) Toba (b) Durame (c) Bulu
Prat dan Hudson (1990 dalam Kiswandono, 2008:30) menyebutkan bahwa kandungan flavonoid dan senyawa fenolik yang ditemukan pada tanaman dapat beraktivitas sebagai antioksidan dan penghambat pertumbuhan tumor. Hal ini juga sesuai dengan pernyataan Redha (2010) yang menyatakan bahwa flavonoid sebagai salah satu kelompok senyawa fenolik yang banyak terdapat dalam jaringan tanaman dapat berperan sebagai antioksidan. Pada sampel yang mengandung flavonoid penambahan H2SO4 pekat akan menyebabkan terbentuk
warna merah dan pada sampel yang mengandung senyawa fenolik penambahan NaOH 10% akan menyebabkan tebentuk warna merah. Pada gambar 15 dapat dilihat terbentuk warna merah pekat pada pengujian flavonoid yang menandakan bahwa sampel getah kemenyan positif mengandung flavonoid dan pada pengujian senyawa fenolik tidak terbentuk warna merah yang menandakan sampel tidak mengandung senyawa fenolik.
digunakan sebagai antioksidan karena komponen bioaktif ini merupakan fenol terbesar. Senyawa-senyawa fenolat yang terkandung dalam tumbuhan mampu menangkap radikal-radikal peroksida.
Gambar 16. Pengujian saponin dan tanin (a) Toba (b) Durame (c) Bulu
Saponin adalah senyawa aktif permukaan yang kuat yang menimbulkan busa jika dikocok dalam air menurut Robinson (1995) saponin memiliki kemampuan sebagai pembersih dan antiseptik yang berfungsi membunuh atau mencegah pertumbuhan mikroorganisme. Indikator positif dari uji saponin adalah terbentuknya busa yang tetap stabil setelah sampel dimasukkan ke dalam tabung reaksi tertutup selama 10 menit. Pada gambar 15 dapat dilihat pada sampel terbentuk busa yang stabil, dengan demikian getah kemenyan positif mengandung saponin.
Tanin merupakan senyawa aktif metabolit sekunder yang diketahui mempunyai beberapa khasiat yaitu sebagai astrigen, anti diare, anti bakteri dan antioksidan (Desmiaty et al, 2008). Identifikasi tanin yang positif ditandai dengan adanya warna biru tua atau hijau kehitaman. Indikasi terhadap senyawa tanin dilakukan melalui penambahan FeCl3. Senyawa tanin adalah senyawa yang
bersifat polar karena adanya gugus OH, ketika ditambahkan FeCl3 10% akan
46
adanya senyawa tanin (Robinson, 1995). Menurut Sangi et al (2008) tanin terhidrolisis akan menunjukkan warna biru kehitaman sedangkan tanin terkondensasi akan menunjukkan warna hijau kehitaman ketika penambahan FeCl3. Pada gambar 16 dapat dilihat bahwa getah kemenyan Toba, Durame, dan
Bulu mengandung tanin yang ditandai dengan terbentuknya warna biru atau hijau kehitaman.
Gambar 17. Pengujian triterpenoid/steroid (a) Toba (b) Durame (c) Bulu
yang menandakan sampel tidak mengandung steroid. Golongan-golongan senyawa triterpenoid diketahui memiliki aktivitas fissiologis tertentu seperti antijamur, antibakteri, antivirus, kerusakan hati, gangguan menstruasi, dan dapat mengatasi penyakit diabetes (Asih et al, 2010). Dengan demikian hasil skrining fitokimia yang dilakukan dapat dilihat bahwa getah kemenyan positif mengandung
alkaloid, flavonoid, saponin, tanin dan triterpenoid/steroid dan negatif mengandung senyawa fenolik dan steroid.
Penentuan Kualitas Getah Kemenyan
Menurut SNI 7940:2013 perbedaan sifat fisika-kimia getah kemenyan mempengaruhi penentuan kualitas atau mutunya. Sifat fisika dari setiap kualitas getah kemenyan ditunjukkan dengan perbedaan pada warna sedangkan sifat kimianya ditunjukkan dengan perbedaan pada kadar air, kadar abu, kadar kotoran, titik lunak, dan kadar asam sinamat. Berdasarkan klasifikasi dan persyaratan khusus getah kemenyan yang ditetapkan SNI 7940 : 2013 dapat diketahui kualitas atau mutu dari tiga jenis getah kemenyan (Styrax spp.) seperti pada tabel 7.
Tabel 7. Penentuan kualitas getah kemenyan
No. Parameter/Kualits Jenis Getah Kemenyan
Toba Durame Bulu
1. Warna Putih kekuningan Putih kuning
kecokelatan
48
Asam sinamat merupakan faktor yang sangat penting dalam penentuan kualitas atau mutu getah kemenyan. Hal ini sesuai dengan pernyataan Waluyo et al (2006) yang menyatakan bahawa asam sinamat merupakan komponen utama
getah kemenyan, maka kadar asam sinamat menjadi unsur utama untuk pengelompokan kualitas getah dan diikuti sifat-sifat lainnya seperti kadar kotoran, kadar abu, dan titik leleh.
Pada kualifikasi SNI 7940:2013 pengujian kadar air tidak termasuk dalam parameter penentunan kualitas getah kemenyan. Penetapan kadar air dilakukan untuk memberikan batasan minimal kandungan air yang masih ditolerir di dalam getah maupun ekstrak. Penentuan kadar air berguna untuk menduga keawetan atau ketahanan sampel dalam penyimpanan serta untuk mengoreksi rendemen yang dihasilkan. Pengujian kadar air pada getah kemenyan yang dilakukan telah memenuhi syarat standarisasi dengan kadar maksimum 5% (SNI 7940:2013).
Pada tabel 7 dapat dilihat perbedaan sifat fisika-kimia getah kemenyan Toba, Durame, dan Bulu. Pada pengujian warna, kadar kotoran, kadar abu ketiga jenis kemenyan tidak memenuhi standar yang ditetapkan sedangkan pada pengujian titik lunak dan kadar asam sinamat memenuhi standar yang ditetapkan. Salah satu penyebab perbedaan kualitas pada ketiga jenis getah kemenyan yaitu cara pengambilan sampel yang dilakukan secara acak. Sehingga pada sampel ditemukan warna, bentuk, dan ukuran yang bervariasi yang mempengaruhi sifat fisika-kimia getah kemenyan.
yang menyatakan bahwa faktor-faktor yang mempengaruhi produktivitas getah yaitu : kualitas tempat tumbuh, umur, kerapatan pohon, jumlah koakan tiap pohon, arah sadap terhadap matahari, jangka waktu pelukaan, sifat individu pohon dan keterampilan penyadap serta pemberian stimulansia.
Faktor lingkungan yang mempengaruhi kualitas getah dapat juga disebabkan saat proses pemanenan getah setelah terlebih dahulu pohon ditakik, diguris, dan disugi. Pohon yang diguris kemudian ditinggal selama 3–4 bulan, selanjutnya pada luka bekas takikan akan keluar getah dari pohon menurut Purbaya et al (2011) getah yang keluar dari pohon akan segera tercemar oleh jasad renik yang berasal dari udara luar atau dari peralatan yang digunakan. Jasad renik ini akan mempengaruhi kualitas getah yang diperoleh.
50
KESIMPULAN DAN SARAN
Kesimpulan
1. Berdasarkan penelitian yang dilakukan terdapat perbedaan sifat fisika-kimia ketiga jenis getah kemenyan yang berdampak terhadap penentuan kualitas getah kemenyan.
2. Hasil pengujian titik lunak dan kadar asam sinamat pada getah kemenyan (Styrax spp.) Tapanuli Utara sudah masuk dalam kualifikasi SNI 7940:2013. 3. Pada skrining fitokimia yang dilakukan getah kemenyan mengandung jenis
metabolit sekunder alkaloid, flavonoid, saponin, tanin, dan triterpenoid/steroid.
Saran
Kepada penelitian selanjutnya disarankan untuk melakukan perlakuan
TINJAUAN PUSTAKA
Taksonomi Kemenyan
Taksonomi pohon kemenyan menurut Jayusman (2014) sebagai berikut : Kingdom : Plantae
Subkingdom : Tracheobionta Superdivisio : Spermatophyta Divisio : Magnoliophyta Kelas : Magnoliopsida Subkelas : Dilleniidae Ordo : Ebenales Famili : Styracaceae
Gambar 1. Pohon kemenyan (Styrax spp.)
6
DRYLAND), Bulu (Styrax benzoine var. hiliferum), dan Siam (Styrax tonkinennsis).
Umumnya masyarakat di Tapanuli dan Dairi, Provinsi Sumatera Utara hanya membudidayakan jenis Toba dan Durame secara luas sedangkan jenis Bulu kurang banyak dibudidayakan. Jenis kemenyan Siam hingga saat ini belum banyak dikembangkan di Indonesia, namun telah dirintis penguasaan budidayanya oleh Balai Penelitian kehutanan Sumatera.
Morfologi Pohon Kemenyan
Morfologi pohon Kemenyan menurut Jayusman (2014) sebagai berikut :
Pohon
Kemenyan termasuk pohon besar, tinggi dapat mencapai (20-40) m dan diameter batang mencapai (60-100) cm. Batang lurus dengan percabangan sedikit. Kulit beralur tidak terlalu dalam (3-7) mm dengan warna kulit merah anggur.
Daun
Kemenyan berdaun tunggal dan tersusun secara spiral. Daun berbentuk oval bulat, bulat memanjang (ellips) dengan dasar daun bulat dengan ujung runcing. Sebelah atas daun berwarna hijau dan sebelah bawah berwarna kekuning-kuningan dengan pinggiran daun rata. Panjang daun mencapai (4-15) cm, lebar daun (5-7,5) cm, tangkai daun (5-13) cm, helai daun mempunyai nervi (7-13) pasang. Warna daun jenis Toba lebih gelap kecoklatan dan lebih tebal dibandingkan jenis Durame dan Bulu.
Bunga
mahkota bunga masing-masing lima buah. Kemenyan berbunga secara teratur satu kali setiap tahun. Waktu berbunga pohon kemenyan pada bulan November sampai Januari.
Buah dan biji
Buah kemenyan berbentuk bulat gepeng dan lonjong berukuran (2,5-3) cm. Biji berukuran (15-19) mm, dengan warna coklat keputihan. Biji kemenyan terdapat di dalam buah dengan kulit buah berukuran (1,75-3,1) mm. Biji kemenyan Toba berwarna coklat tua dan lebih gelap dibandingkan jenis Durame dan Bulu.
Syarat Tumbuh Kemenyan
Tanaman ini umumnya tumbuh secara alami di Sumatera Utara, beberapa syarat tumbuh kemenyan menurut Departemen Kehutanan dan Perkebunan (1999) sebagai berikut :
Tanah
Tanaman kemenyan tidak memerlukan persyaratan yang istimewa terhadap jenis tanah, dapat tumbuh pada tanah bertekstur berat sampai ringan dan tanah yang kurang subur sampai yang subur lebih baik. Jenis tanaman ini tidak tahan terhadap genangan, sehingga untuk pertumbuhan memerlukan tanah yang mempunyai porositas tinggi, di samping itu yang perlu diperhatikan tingkat keasaman tanah (pH tanah). Berdasarkan kenyataan di lapangan tanaman kemenyan tumbuh baik pada tingkat pH tanah antara 4 -7.
Iklim
8
mm/tahun, suhu bulanan (17-29) ᵒC dan kelembaban rata-rata 85,04% dengan iklim basah Schmidt dan Ferguson tipe A dan B. Menurut Wibowo (2012) tipe iklim A adalah daerah sangat basah dengan ciri vegetasi hutan hujan tropika (0 < Q < 14,3) dan tipe iklim B adalah daerah basah dengan ciri vegetasi hutan hujan tropika (14,3 < Q < 33,3). Keadaan iklim sangat besar pengaruhnya terhadap pertumbuhan tanaman kemenyan.
Topografi
Secara alamiah tanaman kemenyan yang banyak terdapat di Sumatera Utara tumbuh mulai dari dataran rendah sampai ketinggian 1500 meter di atas permukaan laut (mdpl), tetapi rata-rata tumbuh pada ketinggian antara (100-700) mdpl. Jenis tanaman ini tumbuh pada keadaan lapangan dari mulai datar sampai berbukit/bergelombang.
Jenis-Jenis Kemenyan
Menurut Jayusman (2014) jenis-jenis kemenyan ada empat yaitu sebagai berikut :
Kemenyan Toba (Styrax paralleloneurum PERK)
Kemenyan Durame (Styrax benzoine DRYLAND)
Kemenyan Durame merupakan jenis kedua yang paling banyak dibudidayakan di daerah Tapanuli. Jenis ini tumbuh dan menyebar pada ketinggian mulai dari > 60 mdpl di daerah Sumatera Selatan dan Tapanuli Selatan, sedangkan di sentra produksi kemenyan Tapanuli Utara banyak ditemukan pada ketinggian > 600 mdpl. Umumnya kemenyan Durame dibudidayakan secara campuran dengan jenis Toba dan Bulu. Penampilan daun jenis Durame terkesan lebih terang warnanya dibandingkan jenis Toba. Getah yang dihasilkan memiliki aroma balsamat agak tajam, warna putih-kuning kecokelatan dengan ukuran butiran getah panjang (3-5) cm dan lebar (1-1,5) cm.
Kemenyan Bulu (Styrax benzoine var hiliferum)
Kemenyan Bulu merupakan jenis yang kurang banyak dikenal, hal ini disebabkan oleh jumlah populasinya yang relatif sedikit. Jenis ini secara alam banyak ditemukan di hutan alam Sibatuloteng-Simalungun dan cukup banyak dibudidayakan di daerah Pahae dan Sarulla, Kabupaten Tapanuli Utara. Namun di salah satu daerah Dolok Sanggul, jenis ini jarang atau sulit ditemukan. Getah yang dihasilkan memiliki aroma balsamat kurang tajam, warna putih-kuning kecokelatan dengan ukuran butiran getah panjang (3-5) cm dan lebar (1-1,5) cm.
Kemenyan Siam (Styrax tonkineensis Pierre)
10
lembut atau aroma vanila, besar butiran getah memiliki panjang (2,5-3,5) cm dan lebar (1,5-1,9) cm.
Penyadapan dan Penakikan Getah Kemenyan
Kegiatan penyadapan secara umum terdiri dari kegiatan menakik, membersihkan, dan mensugi. Kegiatan menakik merupakan kegiatan pertama yang dilakukan dalam pengelolaan hutan kemenyan. Kegiatan menakik meliputi kegiatan membersihkan semak-semak yang berdekatan dengan pohon kemenyan, kemudian dilanjutkan dengan membersihkan pohon kemenyan dengan cara mengguris (mengikis) bagian kulit pohon tersebut. Kegiatan ini dilakukan untuk membersihkan lumut yang menempel pada kulit pohon sehingga getah yang dihasilkan tidak kotor (Dede, 1998).
Potensi dan Penyebaran Kemenyan
Pohon kemenyan menyebar pada berbagai negara meliputi Malaysia, Thailand, Indonesia, dan Laos. Indonesia memiliki daerah sebaran pohon kemenyan di Pulau Sumatera, Pulau Jawa bagian Barat dan Kalimantan Barat. Sumatera memiliki sebaran terluas, terutama daerah Tapanuli dan Dairi. Diperkirakan hampir 67% dari luas kebun kemenyan yang ada di Indonesia terdapat di daerah Tapanuli Utara.
Gambar 2. Peta sebaran kemenyan di Tapanuli Utara Sumber : BPS Tapanuli Utara
12
Tanaman kemenyan merupakan tanaman terluas yang diusahakan oleh masyarakat di Kabupaten Tapanuli Utara, yaitu pada tahun 2011 seluas 16.181,50 ha. Tanaman kemenyan tersebar di seluruh kecamatan Tapanuli Utara, sebagaimana dilihat pada tabel 1.
Tabel 1. Luas dan produksi kemenyan di kabupaten Tapanuli Utara
No. Kecamatan
10 Pangaribuan 5.086,50 4.821,50 1.031,61 213,96
11 Garoga 522,00 346,50 127,49 367,94
Sumber : Kabupaten Tapanuli Utara Dalam Angka, 2012.
Kualitas Getah Kemenyan
Menurut Sasmuko (1999) kualitas kemenyan yang diperdagangkan di Sumatera belum memiliki suatu standar umum yang berlaku, baik dalam transaksi pedagang dan eksportir. Perbedaan standar tersebut menurut petani, pedagang, dan pengolah, antara lain:
Petani
Pedagang dan pengolah
Pengolah merupakan industri yang mengolah getah kemenyan dari kemenyan mentah menjadi kemenyan tampangan. Kemenyan yang dibeli pedagang berupa sam-sam (campuran), mata kasar dan mata halus (kualitas I dan II), tahir (kualitas III), dan jurur (kualitas IV). Getah disortir dengan memakai ayakan, sehingga dapat diatur sesuai dengan mutu yang diinginkan, dapat dilihat pada tabel 2.
Tabel 2. Kualitas getah kemenyan menurut pedagang dan pengolah
No. Mutu Keterangan
1. Kualitas I Kemenyan mata kasar atau sidungkapi adalah bongkahan kemenyan berwarna putih sampai putih kekuning-kuningan dengan rata-rata diameter > 2 cm.
2. Kualitas II Kemenyan mata halus adalah kemenyan berwarna putih sampai putih kekuning-kuningan berdiameter 1 - 2 cm.
3. Kualitas III Kemenyan tahir adalah jenis kemenyan yang bercampur dengan kulit atau kotoran lainnya, berwarna cokelat dan terkadang berbintik-bintik putih atau kuning serta besarnya lebih dari ukuran kemenyan mata halus. 4. Kualitas IV Kemenyan jurur adalah kemenyan yang biasa dicampur atau disamakan
dengan kemenyan tahir. Warnanya merah dan lebih kecil dari mata halus.
5. Kualitas V Kemenyan barbar adalah kulit kemenyan yang dikumpulkan sedikit demi sedikit saat pembersihan.
6. Kualitas VI Kemenyan abu adalah sisa-sisa yang berasal dari semua kualitas getah kemenyan. Bentuk dan warnanya seperti abu kasar.
Sumber : Sasmuko, 1999
Perdagangan getah kemenyan di dalam negeri telah mengenal penggolongan kualitas baik lokal maupun standar kualitas kemenyan nasional. Standar Nasional Indonesia (SNI) kemenyan disusun karena diperlukan persyaratan mutu getah kemenyan dalam rangka mengikuti perkembangan pasar yang cukup tinggi dan teknologi pangan. Berdasarkan SNI 7940:2013 getah kemenyan dapat dilihat pada tabel 3.
Tabel 3. Klasifikasi dan persyaratan khusus pada getah kemenyan
Parameter Satuan Kelas Mutu
A B C
Warna - Putih Bersih Putih kecoklatan
(50% putih 50% coklat)
14
Kadar abu % < 1 < 1 >1 - < 5
Kadar kotoran % < 1 < 1 >1 - < 2
Titik lunak 0C > 92 > 88 > 80
Kadar asam sinamat % > 30 21 - 29 < 20
Sumber: Standar Nasional Indonesia (SNI) No.7940-2013
Kandungan Kimia Kemenyan
Daun kemenyan mengandung saponin, flavonoid dan polifenol (Hutapea, 1994). Getah kemenyan mengandung asam sinamat, asam benzoat, esternya (seperti koniferilbenzoat, koniferilsinamat dan asam sinamilsinamat), triterpenoid/steroid (berupa turunannya yaitu asam siaresinolik dan asam sumaresinolik) (Stahl, 1985).
Manfaat Getah Kemenyan
Menurut Jayusman (2014) secara tradisional getah kemenyan digunakan sebagai dupa pada upacara religi. Getah kemenyan juga digunakan pada industri pembuatan rokok dengan mencampurkan tembakau rokok dan getah kemenyan. Khan (2001) menyebutkan bahwa getah kemenyan mengandung asam sinamat (C6H5CH-CHOOH). Kandungan asam sinamat pada getah kemenyan berperan
penting sebagai bahan penolong pada pembuatan berbagai bahan kimia. Seiring perkembangan zaman asam sinamat digunakan pada berbagai industri kimia. Menurut Jayusman (2014) penggunaan asam sinamat sebagai berikut :
Pembuatan obat-obatan (farmasi)
Asam sinamat pada bidang farmasi digunakan sebagai antiseptic, expectorant (pelega pernafasan), obat katarak mata, dan pada pembuatan
Pembuatan parfum dan kosmetik
Asam sinamat pada pembuatan parfum dimanfaatkan sebagai fix active yang berfungsi menahan aroma pada parfum agar tahan lama. Negara Perancis telah menghasilkan parfum dengan paten bernama “Lait Virginal”. Pada pembuatan kosmetik asam sinamat dimanfaatkan sebagai sun screening agent yaitu sebagai pelindung kulit terhadap sinar matahari dan juga karena memiliki sifat astrigent, sehingga dapat mengeluarkan kotoran-kotoran yang terdapat pada kulit (wajah).
Pengawetan makanan dan minuman
Asam sinamat pada pengawet makanan dan minuman digunakan sebagai food additive yaitu bahan tambahan untuk makanan dan minuman terutama
pengawetan. Menurut Botanical Dermatology Database (2004) bahwa jumlah asam sinamat yang dibutuhkan untuk setiap kilogram/liter makanan atau minuman untuk pengawetan sebanyak 1,25 mg.
Asam Sinamat
Asam sinamat adalah senyawa bahan alam dengan rumus kimia C6H5CHCHCOOH atau C9H8O2, berwujud kristal putih, sedikit larut dalam air,
dan mempunyai titik leleh 133°C serta titik didih 300°C. Asam sinamat terdapat dalam berbagai tanaman, misalnya mesoyi (Messoia aromatica Becc) dan kemenyan (Styrax spp.). Senyawa ini memiliki berbagai aktivitas biologis, antara lain antibakteri, anestetik, antiinflamasi, antispasmodik, antimutagenik, fungisida, herbisida serta penghambat enzim tirosinase (Rudyanto et al., 2008).
16
senyawa fenol utama yang berasal dari jalur shikimat. Biosintesa senyawa fenilpropanoida yang berasal dari jalur shikimat pertama kali ditemukan dalam mikroorganisme seperti bakteri, kapang dan ragi, sedangkan asam shikimat pertama kali ditemukan pada tahun 1885 dari tumbuhan lllicium religiosum dan kemudian ditemukan dalam banyak tumbuhan.
O
OH
(a) (b)
Gambar 3. Kerangka dasar (a) fenilpropanoida, (b) asam sinamat
Pokok-pokok reaksi biosintesa dari jalur shikimat dimulai dengan pembentukan asam shikimat dimulai dengan kondensasi aldol antara suatu tetrosa yaitu eritrosa dan asam fosfoenolpiruvat. Pada kondensasi ini, gugus metilen -CH2- dari asam fosfoenolpiruvat berlaku sebagai nukleofil dan beradisi dengan
gugus karbonil C=O dari eritrosa menghasilkan suatu gula yang terdiri dari 7 atom karbon. Selanjutnya reaksi yang analog (intramolekuler) menghasilkan asam 5-dehidrokuinat yang mempunyai lingkar sikloheksana yang kemudian diubah menjadi asam shikimat.
O
Asam p-kumarat Asam kafeat
O
Gambar 4. Berbagai turunan asam sinamat
Titrasi atau Volumetri
18
yang dianalisis dan larutan standar tersebut berlangsung secara kuantitatif. Analisa titrimetri merupakan satu bagian kimia analisis. Perhitungannya berdasarkan hubungan stoikiometri dari reaksi-reaksi kimia dimana a molekul analit A, bereaksi dengan t molekul reagensia T. Reagensia T disebut titran, ditambahkan sedikit demi sedikit dari dalam buret.
aA + tT Produk
Larutan dalam buret bisa berupa larutan standar yang konsentrasinya diketahui dengan cara standarisasi ataupun larutan dari zat yang akan ditentukan konsentrasinya. Penambahan titran diteruskan sampai jumlah T secara kimia setara atau ekuivalen, maka keadaan tersebut dikatakan telah mencapai titik ekuivalensi dari titrasi itu. Untuk mengetahui kapan penambahan titran itu harus dihentikan, digunakan zat indikator yang dapat menunjukkan terjadinya kelebihan titran dengan perubahan warna. Perubahan warna ini bisa tepat atau tidak tepat
pada titik ekuivalensi. Titik dalam titrasi pada saat indikator berubah warna disebut titik akhir titrasi.
Gambar 5. Proses titrasi
- Reaksi harus berjalan sesuai dengan suatu persamaan reaksi tertentu, tidak boleh ada reaksi sampingan.
- Harus ada perubahan yang terlihat pada saat titik ekuivalen tercapai, baik secara kimia maupun fisika.
- Harus ada indikator yang cocok untuk menentukan titik akhir titrasi, jika reaksi tidak menunjukkan perubahan kimia dan fisika.
- Reaksi harus berlangsung cepat, sehingga titrasi dapat dilakukan dalam beberapa menit (widiarto, 2009).
Skrining Fitokimia
Skrining fitokimia adalah pemeriksaan kimia secara kualitatif terhadap
senyawa-senyawa aktif biologis yang terdapat dalam simplisia dan ekstrak tumbuhan. Senyawa - senyawa tersebut adalah senyawa organik, oleh karena itu skrining terutama ditujukan untuk golongan senyawa organik seperti alkaloida, flavonoid, triterpenoid/steroid, tanin, dan sapotanin. Skrining merupakan langkah awal dari pemeriksaan tumbuhan tersebut untuk membuktikan ada tidaknya senyawa kimia tertentu dalam tumbuhan tersebut yang dapat dikaitkan dengan aktivitas biologinya (Farnsworth, 1996). Uraian beberapa metabolit sekunder tersebut adalah sebagai berikut:
Alkaloid
Alkaloid merupakan golongan zat tumbuhan sekunder yang terbesar. Alkaloid mencakup senyawa bersifat basa yang mengandung satu atau lebih atom nitrogen, biasanya dalam gabungan, sebagai bagian dari sistem siklik. Alkaloid sering bersifat racun bagi manusia dan banyak yang mempunyai kegiatan fisiologi
20
(Harbone, 1987). Pada umumnya alkaloid merupakan senyawa padat berbentuk kristal atau amorf, tidak berwarna dan mempunyai rasa pahit. Dalam bentuk bebas alkaloid merupakan basa lemah yang sukar larut dalam air tetapi mudah larut dalam pelarut organik (Rusdi, 1998).
Flavonoid
Flavonoid merupakan senyawa polar yang umumnya mudah larut dalam pelarut polar seperti etanol, metanol, butanol, aseton, dan lain-lain (Markham, 1988). Nurachman (2002) menambahkan bahwa senyawa-senyawa flavonoid umumnya bersifat antioksidan dan banyak yang telah digunakan sebagai salah satu komponen bahan baku obat-obatan.
Saponin
Saponin berasal dari bahasa Latin yaitu “sapo” yang berarti sabun dan sifatnya menyerupai sabun. Saponin merupakan senyawa aktif permukaan yang kuat yang menimbulkan busa jika dikocok dalam air dan pada konsetrasi yang rendah sering menyebabkan hemolisis sel darah merah. Beberapa saponin bekerja sebagai antimikroba dan saponin tertentu menjadi penting karena dapat diperoleh dari beberapa tumbuhan dengan hasil yang baik dan digunakan sebagai bahan baku untuk sintesis hormon steroid yang digunakan dalam bidang kesehatan (Robinson, 1995).
Tanin
pembentukan iaktan senyawa kompleks tanin terhadap ion logam yang dapat menambah daya toksisitas tanin itu sendiri (Akiyama et al., 2001).
Triterpenoid/steroid
1
PENDAHULUAN
Latar Belakang
Hutan di Indonesia memiliki kekayaan sumber daya alam yang tinggi. Selain kayu dari hutan yang dapat dihasilkan, berbagai jenis hasil hutan juga bisa digunakan sebagai bahan baku industri. Masyarakat sekitar hutan memanfaatkan hasil hutan bukan kayu sebagai sumber mata pencaharian. Beberapa hasil hutan bukan kayu yang biasa dikenal masyarakat antara lain seperti rotan, bambu, nipah, getah, damar, minyak atsiri, madu, dan lain-lain.
Salah satu hasil hutan bukan kayu berupa getah adalah kemenyan (Styrax spp.). Kemenyan diperoleh dengan cara disadap dari pohon kemenyan. Tanaman ini selain tumbuh di Indonesia juga tumbuh di beberapa negara lain, diantaranya Malaysia, Thailand, Laos dan Vietnam. Tanaman kemenyan di Indonesia banyak ditemukan di Sumatera Utara, Kalimantan Barat, dan Jawa bagian Barat (Jayusman, 1999).
Sumatera utara dikenal sebagai daerah penghasil kemenyan terbesar di Indonesia. Daerah-daerah penghasil kemenyan berada di kabupaten Tapanuli Utara, Dairi, Toba Samosir dan Tapanuli Tengah. Kabupaten Tapanuli Utara merupakan sentra produksi kemenyan Sumatera Utara yang mempunyai luas tanaman + 16.322,3 Ha dengan rata-rata produksi 3.626,48 ton/tahun (Kabupaten Tapanuli Utara Dalam Angka, 2012).
dan United State of America. Sekitar 67% dari hasil ekspor kemenyan tersebut berasal dari Tapanuli Utara dan sisanya berasal dari daerah lain di Indonesia yang juga menghasilkan getah kemenyan.
Getah kemenyan merupakan komoditi cukup penting dan perlu mendapat perhatian lebih besar karena merupakan komoditi khas Sumatera Utara dan telah memberikan kontribusi ekonomis bagi masyarakat khususnya petani di Kabupaten Tapanuli Utara. Menurut Sasmuko (1999) produksi getah kemenyan cenderung menurun dan produktifitasnya rendah. Hal ini disebabkan karena pengelolaannya masih dilakukan secara tradisional.
Menurut Waluyo et al (2006) pada umumnya getah kemenyan diperdagangkan dalam bentuk kepingan/bongkahan yang tidak merata besarnya, sedangkan kualitas maupun tingkat harga ditentukan secara visual seperti besar kecilnya kepingan, warna, bau, kebersihan dan kerapuhan. Pembagian kualitas kemenyan yang dilakukan hanya berdasarkan penampilan fisik.
Berdasarkan uraian tersebut, maka dilakukan penelitian secara kuantitatif dengan uji laboratorium mengenai sifat fisika-kimia getah kemenyan (Styrax spp.), sehingga penentuan kualitas getah kemenyan (Styrax spp.) dapat dilakukan berdasarkan sifat fisika-kimianya.
Rumusan Masalah
3
Sifat fisika dari setiap kualitas kemenyan ditunjukkan dengan perbedaan pada warna sedangkan sifat kimianya ditunjukkan dengan perbedaan pada kadar air, kadar abu, kadar kotoran, titik lunak, dan kadar asam sinamat yang dikandung oleh kemenyan.
Perbedaan sifat fisika-kimia tersebut tentu saja mempengaruhi penentuan kualitas kemenyan itu sendiri. Sehingga nantinya dalam pemasaran kemenyan ini, akan terjadi perbedaan nilai/harga jual dari masing-masing kualitas kemenyan. Berdasarkan hal tersebut penelitian mengenai sifat fisika-kimia kemenyan perlu dilakukan supaya pengelompokan kualitas kemenyan dapat dilakukan secara kuantitatif. Kemenyan juga diketahui memiliki senyawa bioaktif, maka perlu juga dilakukan penentuan jenis metabolit sekunder pada kemenyan sehingga dapat memberikan informasi kepada masyarakat apabila kemenyan tersebut digunakan sebagai obat.
Tujuan Penelitian
Tujuan penelitian ini adalah untuk :
1. Mengetahui sifat fisika-kimia getah kemenyan (Styrax spp.) Tapanuli Utara. 2. Mengetahui penentuan kualitas atau kelas mutu berdasarkan sifat fisika-kimia
getah kemenyan (Styrax spp.) Tapanuli Utara.
3. Mengetahui senyawa metabolit sekunder yang terdapat pada kemenyan (Styrax spp.) Tapanuli Utara.
Manfaat Penelitian
i
ABSTRACT
North Tapanuli a benzoin gums production centers in Indonesia. Benzoin gums trafficked consists of a kind of benzoin gum Toba (Styrax paralleloneurum Perk), benzoin gum Durame (Styrax benzoine dryland), and benzoin gum Bulu (Styrax benzoine var hiliferum). The purpose of this study was intended to determine differences in physical-chemical properties of various types of benzoine gums on the market, which is expected later grouping quality benzoin gums can be considered quantitatively based on the physico-chemical properties. Physical-chemical properties of benzoin gums tested is color, moisture content, impurity content, ash content, softening point, and cinnamic acid levels. The results showed the water content testing, softening point, and cinnamic acid levels qualify as SNI 7940: 2013 while on testing colors, impurity content, and ash content not included in the qualification SNI 7940: 2013. In the phytochemical screening test positive benzoine gums containing the type of secondary metabolites, alkaloids, flavonoids, saponins, tannins, and triterpenoids/steroids.
ABSTRAK
Tapanuli Utara merupakan sentra produksi getah kemenyan di Indonesia. Getah kemenyan yang di perdagangkan terdiri dari jenis kemenyan Toba (Styrax paralleloneurum PERK), kemenyan Durame (Styrax benzoine Dryland), dan kemenyan Bulu (Styrax benzoine var hiliferum). Tujuan penelitian ini dimaksudkan untuk mengetahui perbedaan sifat fisika-kimia berbagai jenis getah kemenyan yang ada di pasaran, sehingga diharapkan nantinya pengelompokan kualitas getah kemenyan dapat dipertimbangkan secara kuantitatif berdasarkan sifat fisika-kimianya. Sifat fisika-kimia getah kemenyan yang diuji adalah warna, kadar air, kadar kotoran, kadar abu, titik lunak, dan kadar asam sinamat. Hasil penelitian menunjukkan pada pengujian kadar air, titik lunak, dan kadar asam sinamat masuk dalam kualifikasi SNI 7940:2013 sedangkan pada pengujian warna, kadar kotoran, dan kadar abu tidak masuk dalam kualifikasi SNI 7940:2013. Pada pengujian skrining fitokimia getah kemenyan positif mengandung jenis metabolit sekunder alkaloid, flavonoid, saponin, tanin, dan triterpenoid/steroid.
STUDI SIFAT FISIKA-KIMIA GETAH KEMENYAN
(Styrax spp.) DARI TAPANULI UTARA
SKRIPSI
Oleh :
Agnes Farida Lumbantobing 121201029
Teknologi Hasil Hutan
PROGRAM STUDI KEHUTANAN
FAKULTAS KEHUTANAN
UNIVERSITAS SUMATERA UTARA
ABSTRACT
North Tapanuli a benzoin gums production centers in Indonesia. Benzoin gums trafficked consists of a kind of benzoin gum Toba (Styrax paralleloneurum Perk), benzoin gum Durame (Styrax benzoine dryland), and benzoin gum Bulu (Styrax benzoine var hiliferum). The purpose of this study was intended to determine differences in physical-chemical properties of various types of benzoine gums on the market, which is expected later grouping quality benzoin gums can be considered quantitatively based on the physico-chemical properties. Physical-chemical properties of benzoin gums tested is color, moisture content, impurity content, ash content, softening point, and cinnamic acid levels. The results showed the water content testing, softening point, and cinnamic acid levels qualify as SNI 7940: 2013 while on testing colors, impurity content, and ash content not included in the qualification SNI 7940: 2013. In the phytochemical screening test positive benzoine gums containing the type of secondary metabolites, alkaloids, flavonoids, saponins, tannins, and triterpenoids/steroids.
ii
ABSTRAK
Tapanuli Utara merupakan sentra produksi getah kemenyan di Indonesia. Getah kemenyan yang di perdagangkan terdiri dari jenis kemenyan Toba (Styrax paralleloneurum PERK), kemenyan Durame (Styrax benzoine Dryland), dan kemenyan Bulu (Styrax benzoine var hiliferum). Tujuan penelitian ini dimaksudkan untuk mengetahui perbedaan sifat fisika-kimia berbagai jenis getah kemenyan yang ada di pasaran, sehingga diharapkan nantinya pengelompokan kualitas getah kemenyan dapat dipertimbangkan secara kuantitatif berdasarkan sifat fisika-kimianya. Sifat fisika-kimia getah kemenyan yang diuji adalah warna, kadar air, kadar kotoran, kadar abu, titik lunak, dan kadar asam sinamat. Hasil penelitian menunjukkan pada pengujian kadar air, titik lunak, dan kadar asam sinamat masuk dalam kualifikasi SNI 7940:2013 sedangkan pada pengujian warna, kadar kotoran, dan kadar abu tidak masuk dalam kualifikasi SNI 7940:2013. Pada pengujian skrining fitokimia getah kemenyan positif mengandung jenis metabolit sekunder alkaloid, flavonoid, saponin, tanin, dan triterpenoid/steroid.
RIWAYAT HIDUP
Penulis dilahirkan di Tarutung pada tanggal 01 Februari 1994 dari Bapak Robert Lumbantobing dan Ibu Ruslan Manalu. Penulis merupakan anak ketiga dari empat bersaudara. Pada tahun 2006 penulis lulus dari sekolah tingkat dasar SD Negeri 173524, pada tahun 2009 penulis telah menyelesaikan sekolah tingkat pertama SMP Swasta Budhi Dharma Balige, tahun 2012 penulis lulus dari sekolah tingka menengah SMA Negeri 01 Balige, dan pada tahun yang sama lulus seleksi masuk Universitas Sumatera Utara melalui jalur Seleksi Nasional Masuk Perguruan Tinggi Negeri (SNMPTN) di Program Studi Kehutanan Departemen Kehutanan.
Selama mengikuti masa perkuliahan penulis mengikuti Praktik Pengenalan Ekosistem Hutan (P2EH) di Pulau Sembilan Kabupaten Langkat Provinsi Sumatera Utara dan Praktik Kerja Lapangan di Perum Perhutani Divisi Regional Jawa Tengah KPH Pekalongan Timur. Selain itu penulis juga merupakan Asisten Laboratorium Hasil Hutan Non Kayu (2014), Pemanenan Hasil Hutan (2014), Hidrologi (2015) dan Dasar Pengelolaan Kayu Solid (2015). Penulis melakukan penelitian dengan judul “Studi Sifat Fisika-Kimia Kemenyan (Styrax spp.) dari Tapanuli Utara. Penulis melakukan penelitian di Laboratorium Kimia Organik Fakultas Matematika dan Ilmu Alam. Selama melakukan penelitian penulis
iv
KATA PENGANTAR
Puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Esa, atas segala rahmat dan karunia-Nya sehingga penulis dapat menyelesaikan skripsi yang berjudul “Studi Sifat Fisika-Kimia Kemenyan (Styrax spp.) dari Tapanuli Utara”.
Dalam pelaksanaan penelitian sampai penyelesaian skripsi penulis banyak mendapat bantuan, dukungan, dan motivasi dari berbagai pihak. Pada kesempatan ini penulis menghanturkan pernyataan terima kasih sebesar-besarnya kepada: 1. Bapak Dr. Apri Heri Iswanto., S.Hut., M.Si dan Bapak Dr. Agung Abadi
Kiswandono., S.Si., M.Si selaku ketua dan anggota komisi pembimbing yang telah membimbing dan memberi masukan berharga kepada penulis sampai pada ujian akhir.
2. Ibu Siti Latifah., S.Hut., M.Si., Ph.D selaku ketua program studi.
3. Kedua orangtua Bapak Robert Lumbantobing dan Ibu Ruslan Manalu, serta kakak Grace Lumbantobing, Rika Lumbantobing, dan adik Cynthia Lumbantobing yang memberikan kasih sayang dan perhatian yang sangat besar untuk keberhasilan penulis.
4. Asisten Laboratorium Kimia Organik Fakultas Matematika dan Ilmu Pengetahuan Alam yang membantu penulis di laboratorium selama penelitian.
Akhir kata penulis berharap semoga skripsi ini dapat bermanfaat bagi siapa saja yang membaca dalam pengembangan ilmu pengetahuan di Indonesia.
Medan, April 2016
vi
Kemenyan Toba (Styrax paralleloneurum PERK) ... 8
Kemenyan Durame (Styrax benzoine DRYLAND) ... 9
Kemenyan Bulu (Styrax benzoine var hiliferum) ... 9
Kemenyan Siam (Styrax tonkineensis Pierre) ... 9
Penyadapan dan Penakikan Getah Kemenyan ... 10
Potensi dan Penyebaran Kemenyan ... 11
Kualitas Getah Kemenyan... 12
Petani ... 12
Pedagang dan pengolah ... 13
Kandungan Kimia Kemenyan ... 14
Manfaat Kemenyan ... 14
Pembuatan obat-obatan (farmasi) ... 14
Pembuatan parfum dan kosmetik ... 15
Pengawetan makanan dan minuman ... 15
Asam Sinamat ... 15
Hal.
Triterpenoid/steroid ... 21
METODOLOGI PENELITIAN Waktu dan Tempat ... 23
Bahan dan Alat Penelitian ... 23
Prosedur Penelitian... 24
Pengambilan sampel ... 24
Pengujian laboratorium ... 26
1. Kadar air... 26
5. Triterpenoid/steroid... 30
HASIL DAN PEMBAHASAN Persiapan Bahan Baku... 32
Pengujian Visual ... 32
Warna dan kadar air ... 32
Pengujian Laboratorium ... 34
Kadar air ... 34
Penentuan Kualitas Getah Kemenyan ... 47
KESIMPULAN DAN SARAN Kesimpulan ... 50
viii DAFTAR PUSTAKA
DAFTAR TABEL
No. Hal.
1. Luas dan produksi kemenyan di kabupaten Tapanuli Utara ... 5
2. Kualitas getah kemenyan menurut perdagangan dan pengolah ... 11
3. Klasifikasi dan persyaratan khusus getah kemenyan ... 16
4. Klasifikasi getah kemenyan dengan parameter warna ... 26
5. Pengamatan visual getah parameter warna dan kadar air ... 33
6. Hasil skrining fitokimia ... 42
x
DAFTAR GAMBAR
No. Hal.
1. Pohon kemenyan (Styrax spp.) ... 5
2. Peta Sebaran kemenyan di Tapanuli Utara... 11
3. Kerangka dasar ... 16
4. Berbagai turunan asam sinamat ... 17
5. Proses titrasi ... 18
6. Serbuk getah kemenyan ... 32
7. Pengamatan visual getah kemenyan ... 33
8. Pengujian kadar air ... 34
9. Pengujian kadar abu ... 35
10. Pengujian kadar kotoran pelarut aseton ... 37
11. Pengujian kadar kotoran pelarut metanol ... 37
12. Pengujian titik lunak ... 39
13. Pengujian kadar asam sinamt ... 40
14. Pengujian alkaloid ... 43
15. Pengujian flavonoid dan senyawa fenolik ... 44
16. Pengujian saponin dan tanin ... 45