PENGARUH WAKTU TERHADAP KADAR VITAMIN C
YANG TERDAPAT PADA SARI MARKISA(Passiflora edulis
Sims.) SECARA VOLUMETRI DENGAN 2,6-DIKLOROFENOL
INDOFENOL
SKRIPSI
OLEH:
MERNA R SIPAHUTAR
NIM 101524013
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
2013
ii
PENGARUH WAKTU TERHADAP KADAR VITAMIN C
YANG TERDAPAT PADA SARI MARKISA(Passiflora edulis
Sims.) SECARA VOLUMETRI DENGAN 2,6-DIKLOROFENOL
INDOFENOL
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh
gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
MERNA R SIPAHUTAR
NIM 101524013
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
2013
iii
LEMBAR PENGESAHAN
PENGARUH WAKTU TERHADAP KADAR VITAMIN C
YANG TERDAPAT PADA SARI MARKISA (Passiflora edulis
Sims.) SECARA VOLUMETRI DENGAN 2,6-DIKLOROFENOL
INDOFENOL
OLEH: MERNA R SIPAHUTAR
NIM 101524013 Dipertahankan di Hadapan Panitia Penguji Skripsi
Fakultas Farmasi Universitas Sumatera Utara Pada tanggal: 23 Maret 2013
Diketahui Oleh: Pembimbing I
Dra. Siti Nurbaya, M.Si., Apt.
NIP 195008261974122001 Panitia Penguji,
Drs. Chairul Azhar Dalimunthe, M.Sc.,Apt NIP 194907061980021001
Pembimbing II
Dr. Muchlisyam, M.Si., Apt. NIP 195006221980021001
Dra. Siti Nurbaya, M.Si., Apt.
NIP 195008261974122001
Dra. Salbiah, M.Si., Apt. NIP 194810031987012001
Dra. Tuty Roida Pardede, M.Si., Apt. NIP 195401101980032001
Medan, Mei 2013 Fakultas Farmasi
Universitas Sumatera Utara Dekan,
Prof. Dr. Sumadio Hadisahputra, Apt. NIP 195311281983031002
iv
KATA PENGANTAR
Segala Puji syukur penulis ucapkan kepada Tuhan Yang Maha Esa atas
segala berkat rahmat dan karuniaNya, sehingga penulis dapat menyelesaikan
penelitian dan penyusunan skripsi ini.
Skripsi ini disusun untuk melengkapi salah satu syarat mencapai gelar
Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara, Medan
dengan judul: “Pengaruh Waktu Terhadap Kadar Vitamin C yang Terdapat
pada Sari Markisa (Passiflora edulis Sims) Secara Volumetri dengan 2,6-Diklorofenol Indofenol”.
Pada kesempatan ini dengan segala kerendahan hati penulis mengucapkan
terima kasih kepada: Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan,
Fakultas Farmasi Universitas Sumatera Utara yang telah memberikan fasilitas
kepada penulis sehingga dapat menyelesaikan pendidikan, Ibu Dra. Siti Nurbaya,
M.Si., Apt., dan Bapak Dr. Muchlisyam, M.Si., Apt., selaku dosen pembimbing
saya yang telah memberikan waktu dan petunjuk serta saran-saran selama
penelitian hingga selesainya skripsi ini, Ibu Sri Yuliasmi, S.Farm., M.Si., Apt.,
selaku penasihat akademik yang telah memberikan bimbingan kepada penulis
selama masa perkuliahan, Ibu Dra. Salbiah, M.Si., Apt., Ibu Dra. Tuty Roida
Pardede, M.Si., Apt., dan Bapak Drs. Chairul Azhar Dalimunthe, M.Sc., Apt.,
selaku dosen penguji saya yang memberikan saran dan arahan demi perbaikan
skripsi ini.
Terima kasih yang tulus penulis ucapkan kepada Ayahanda
Darjon Sipahutar dan Ibunda Henrika Rospita Pane yang telah memberikan cinta
v
dan kasih sayang yang tidak ternilai dengan apapun, doa yang tulus serta
pengorbanan baik materi maupun non-materi, adik ku tercinta (Winda, Heldro,
dan Manlintang), opung ku, dan seluruh keluarga yang memberi semangat serta
doa kepada penulis, teman-teman seperjuangan Ekstensi angkatan 2010 terima
kasih untuk perhatian, semangat, doa, dan kebersamaannya selama ini serta
seluruh pihak yang telah ikut membantu penulis namun tidak tercantum namanya.
Spesial untuk sahabat saya Juni Arnita, Elida, Fitri, Dewi Cytra, Iin, Indra yang
memberikan saya semangat dan dukungan dalam penulisan skripsi ini.
Penulis menyadari sepenuhnya bahwa dalam penulisan skripsi ini masih
jauh dari kesempurnaan, oleh karena itu dengan segala kerendahan hati, penulis
menerima kritik dan saran demi kesempurnaan skripsi ini.
Akhirnya, penulis berharap semoga skripsi ini dapat memberi manfaat
bagi kita semua.
Medan, Mei 2013
Penulis,
(Merna Romsani Sipahutar)
vi
PENGARUH WAKTU TERHADAP KADAR VITAMIN C YANG TERDAPAT PADA SARI MARKISA (Passiflora edulis Sims.) SECARA VOLUMETRI DENGAN 2,6-DIKLOROFENOL INDOFENOL
ABSTRAK
Buah Markisa merupakan salah satu buah yang banyak dikonsumsi oleh masyarakat. Buah ini memiliki aroma yang khas dan merupakan salah satu sumber vitamin C yang dapat meningkatkan daya tahan tubuh, sebagai anti oksidan, mencegah sariawan, dan gusi berdarah. Selain dapat dikonsumsi langsung, markisa juga dapat dibuat jus, sari buah atau ditambahkan pada minuman-minuman buah lainnya.
Buah markisa yang digunakan dalam penelitian ini adalah markisa ungu
(Passiflora edulis Sims) yang diperoleh dari Pasar Tradisional Padang Bulan,
Medan kilometer 4,5 yang berasal dari Desa Ajinembah, Kecamatan Merek, Kabupaten Tanah Karo. Penetapan kadar vitamin C dilakukan secara volumetri dengan 2,6-diklorofenol indofenol karena larutan ini selektif terhadap Vitamin C. Hasil penelitian menunjukkan bahwa kadar Vitamin C sari markisa segar (25,83 mg/100 g), didiamkan selama 1 jam (25,23 mg/100 g), 4 jam (23,64 mg/100 g), dan 8 jam (20,73 mg/100 g). Secara statistik dengan uji Duncan dan Anova menggunakan SPSS 17 diketahui adanya perbedaan kadar Vitamin C pada interval waktu tertentu yaitu pada sari segar, dibiarkan 1 jam, dibiarkan 4 jam, dan dibiarkan 8 jam. Pada uji validasi metode diperoleh persen recovery sebesar 95,86% dan RSD sebesar 0,22%.
Kata Kunci: Penetapan Kadar, Vitamin C, sari markisa, waktu, 2,6-Diklorofenol Indofenol.
vii
THE EFFECT OF TIME VITAMIN C
IN PASSION FRUIT ESSENCE (Passiflora edulis Sims.) BY VOLUMETRIC WITH 2,6-DICHLOROFENOL INDOFENOL
ABSTRACT
Passion fruit is one of fruit that is usually consumed by many people. Passion fruit has a distinctive aroma and one of the source of vitamin C that can increase endurance, as an anti-oxidant, prevent thrush, and prevent bleeding gums. Beside it can be consumed dirrectly, Passion fruit can be blend as juice, essence or be mixed with the other fruit beverages.
Passion fruit which is used in this study is the purple passion fruit (Passiflora edulis Sims) that is got from Traditional market Padang Bulan, Medan kilometri 4.5 originating from Ajinembah Village, Merek District, Tanah Karo Regency. The Assay of vitamin C conducted by volumetric method with 2,6-diklorofenol indofenol because this solution selective to vitamin C.
The result showed that the vitamin C content of fresh passion fruit essence (25.83 mg/100 g), allowed one hour (25.23 mg/100 g), 4 hours (23.64 mg/100 g), and 8 hours (20.73 mg/100 g). Statistically with Duncan and Anova, using SPSS 17 the difference in the levels of vitamin C at specific time intervals, namely the fresh juice, allowed 1 hour, 4 hours left, and left 8 hours. In the test method validation obtained percent recovery was 95.86 % and RSD is 0.22%.
Key words: Determination Levels, Vitamin C, passion fruit essence, time, 2.6-Diklorofenol Indofenol.
viii DAFTAR ISI
Halaman
JUDUL ... i
PENGESAHAN SKRIPSI ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xi
DAFTAR GAMBAR ... xii
DAFTAR LAMPIRAN ... xiii
BAB I PENDAHULUAN ... 1
1.1Latar Belakang ... 1
1.2Perumusan Masalah ... 3
1.3Hipotesis ... 3
1.4Tujuan Penelitian ... 4
1.5Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Markisa ... 5
2.2 Uraian Tumbuhan ... 5
2.3 Vitamin C ... 7
2.4 Fungsi Vitamin C ... 9
2.5 Metode Penetapan Kadar Vitamin C ... 10
ix
2.6 Analisis Kembali Vitamin C yang Ditambahkan pada Sampel
(Analisis Recovery) ... 13
2.7 Analisis Data Secara Statistik ... 14
2.7.1 Penolakan Hasil Pengamatan ... 14
BAB III METODE PENELITIAN ... 15
3.1 Waktu dan Tempat Penelitian ... 15
3.2 Identifikasi Tumbuhan ... 15
3.3 Bahan dan Alat ... 15
3.3.1 Alat-alat ... 15
3.3.2 Bahan-bahan ... 15
3.4 Rancangan Penelitian ... 16
3.4.1 Sampel ... 16
3.4.1.1 Pengambilan Sampel ... 16
3.5 Prosedur Penelitian ... 16
3.5.1 Pembuatan Pereaksi ... 16
3.5.2 Perhitungan Kesetaraan Pentiter 2,6-Diklorofenol Indofenol ... 17
3.5.3 Penyiapan Larutan Sampel ... 18
3.5.4 Penetapan Kadar Vitamin C dari Larutan Sampel ... 18
3.5.5 Penetapan Kadar Baku Vitamin C dengan Metode 2,6 Diklorofenol Indofenol ... 19
3.5.6 Uji Perolehan Kembali (Recovery) ... 19
3.5.7 Analisis Data Secara Statistik ... 20
3.5.7.1 Penolakan Hasil Pengamatan ... 20
3.5.7.2 Uji Ketelitian (Presisi) Metode Analisis ... 22
3.5.7.3 Pengujian Beda Nilai Rata-rata ... 22
x
BAB IV HASIL DAN PEMBAHASAN ... 23
4.1 Identifikasi Tumbuhan ... 23
4.2 Penetapan Kadar Baku Vitamin C dan Sari Markisa dengan Variasi Waktu ... 23
4.3 Uji Perolehan Kembali ... 27
BAB V KESIMPULAN DAN SARAN ... 29
5.1 Kesimpulan ... 29
5.2 Saran ... 29
DAFTAR PUSTAKA ... 30
LAMPIRAN ... 32
xi
DAFTAR TABEL
Halaman Tabel 1. Nilai Qkritis Pada Taraf Kepercayaan ... 21
Tabel 2. Hasil Penetapan Kadar Baku Vitamin C dan Sari Markisa
Dengan Variasi Waktu ... 24
Tabel 3. Persen Penurunan Baku Vitamin C dan Sari Markisa pada
Variasi Waktu ... 24
Tabel 4. Uji F Kadar Vitamin C dari Sari Markisa pada
Variasi Waktu ... 25
Tabel 5. Analisis Himpunan Homogen Kadar Vitamin C dari
Sari Markisa pada Variasi Waktu ……… 25
Tabel 6. Hasil Uji Perolehan Kembali dari Sari Markisa .……….… 27
xii
DAFTAR GAMBAR
Halaman
Gambar 1. Rumus Bangun Vitamin C ... 7
Gambar 2. Reaksi Perubahan Vitamin C ... 8
Gambar 3. Reaksi antara Vitamin C dan Iodin ... 11
Gambar 4. Reaksi Asam Askorbat dengan 2,6-Diklorofenol Indofenol ... 12
Gambar 5. Diagram Batang Kadar Baku Vitamin C dan Sari Markisa dengan Variasi Waktu ... 25
Gambar 6. Gambar Buah Markisa Ungu ... …... 34
Gambar 7. Gambar Bagian Isi Buah Markisa Ungu ………. 34
Gambar 8. Gambar Sari Markisa ……… 35
Gambar 9. Gambar Supernatan Sari Markisa ……….. 35
Gambar 10. Gambar Mikro Buret dan Larutan 2,6-diklorofenol indofenol .. 35
xiii
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Sertifikat Identifikasi Tumbuhan ... 32
Lampiran 2. Sertifikat Bahan Baku Pembanding ... 33
Lampiran 3. Sampel yang Digunakan ... 34
Lampiran 4. Flowsheet ... 36
Lampiran 5. Data Perhitungan Kesetaraan Larutan 2,6-Diklorofenol Indofenol ... 38
Lampiran 6. Perhitungan Kadar Vitamin C dari Sampel yang Dianalisis ... 41
Lampiran 7. Data Hasil Penetapan Kadar Vitamin C pada Sari Markisa ... 42
Lampiran 8. Data Hasil Penetapan Kadar Baku Vitamin C ... 43
Lampiran 9. Perhitungan Statistik Kadar Vitamin C dari Sampel yang Dianalisis pada Sari Markisa ... 44
Lampiran 10. Perhitungan Statistik Kadar Baku Vitamin C ... 48
Lampiran 11. Hasil Analisis Statistik ... 52
Lampiran 12. Contoh Perhitungan Analisis Perolehan Kembali (Recovery) ... 53
Lampiran 13. Data Analisis Perolehan Kembali (Recovery) Vitamin C dari Sari Markisa ... 54
Lampiran 14. Perhitungan Koefisien Variasi (% RSD) dari Sari Markisa Untuk Recovery ... 55
Lampiran 15. Tabel Distribusi F ... 56
Lampiran 16. Tabel Distribusi t ... 57
vi
PENGARUH WAKTU TERHADAP KADAR VITAMIN C YANG TERDAPAT PADA SARI MARKISA (Passiflora edulis Sims.) SECARA VOLUMETRI DENGAN 2,6-DIKLOROFENOL INDOFENOL
ABSTRAK
Buah Markisa merupakan salah satu buah yang banyak dikonsumsi oleh masyarakat. Buah ini memiliki aroma yang khas dan merupakan salah satu sumber vitamin C yang dapat meningkatkan daya tahan tubuh, sebagai anti oksidan, mencegah sariawan, dan gusi berdarah. Selain dapat dikonsumsi langsung, markisa juga dapat dibuat jus, sari buah atau ditambahkan pada minuman-minuman buah lainnya.
Buah markisa yang digunakan dalam penelitian ini adalah markisa ungu
(Passiflora edulis Sims) yang diperoleh dari Pasar Tradisional Padang Bulan,
Medan kilometer 4,5 yang berasal dari Desa Ajinembah, Kecamatan Merek, Kabupaten Tanah Karo. Penetapan kadar vitamin C dilakukan secara volumetri dengan 2,6-diklorofenol indofenol karena larutan ini selektif terhadap Vitamin C. Hasil penelitian menunjukkan bahwa kadar Vitamin C sari markisa segar (25,83 mg/100 g), didiamkan selama 1 jam (25,23 mg/100 g), 4 jam (23,64 mg/100 g), dan 8 jam (20,73 mg/100 g). Secara statistik dengan uji Duncan dan Anova menggunakan SPSS 17 diketahui adanya perbedaan kadar Vitamin C pada interval waktu tertentu yaitu pada sari segar, dibiarkan 1 jam, dibiarkan 4 jam, dan dibiarkan 8 jam. Pada uji validasi metode diperoleh persen recovery sebesar 95,86% dan RSD sebesar 0,22%.
Kata Kunci: Penetapan Kadar, Vitamin C, sari markisa, waktu, 2,6-Diklorofenol Indofenol.
vii
THE EFFECT OF TIME VITAMIN C
IN PASSION FRUIT ESSENCE (Passiflora edulis Sims.) BY VOLUMETRIC WITH 2,6-DICHLOROFENOL INDOFENOL
ABSTRACT
Passion fruit is one of fruit that is usually consumed by many people. Passion fruit has a distinctive aroma and one of the source of vitamin C that can increase endurance, as an anti-oxidant, prevent thrush, and prevent bleeding gums. Beside it can be consumed dirrectly, Passion fruit can be blend as juice, essence or be mixed with the other fruit beverages.
Passion fruit which is used in this study is the purple passion fruit (Passiflora edulis Sims) that is got from Traditional market Padang Bulan, Medan kilometri 4.5 originating from Ajinembah Village, Merek District, Tanah Karo Regency. The Assay of vitamin C conducted by volumetric method with 2,6-diklorofenol indofenol because this solution selective to vitamin C.
The result showed that the vitamin C content of fresh passion fruit essence (25.83 mg/100 g), allowed one hour (25.23 mg/100 g), 4 hours (23.64 mg/100 g), and 8 hours (20.73 mg/100 g). Statistically with Duncan and Anova, using SPSS 17 the difference in the levels of vitamin C at specific time intervals, namely the fresh juice, allowed 1 hour, 4 hours left, and left 8 hours. In the test method validation obtained percent recovery was 95.86 % and RSD is 0.22%.
Key words: Determination Levels, Vitamin C, passion fruit essence, time, 2.6-Diklorofenol Indofenol.
xiv BAB I PENDAHULUAN 1.1Latar Belakang
Markisa (Passiflora edulis Sims.) merupakan salah satu buah yang
memiliki kandungan vitamin C, mempunyai rasa asam. Markisa banyak
dibudidayakan di daerah tropis, termasuk di Indonesia. Manfaat markisa bagi
kesehatan manusia, menjadikannya memiliki nilai yang tinggi dan kesegaran rasa
markisa menjadi buah yang digemari masyarakat selain dikonsumsi langsung
markisa juga dapat dibuat jus, sari buah atau sering ditambahkan pada
minuman-minuman buah lainya untuk menambah rasa dan aroma yang khas (Ahmad, 1999).
Sari buah adalah cairan yang dihasilkan dari pemerasan atau penghancuran
buah segar yang telah masak. Pada prinsipnya dikenal dua macam sari buah,
yaitu: sari buah encer (dapat langsung diminum), yaitu cairan buah yang
diperoleh dari pengepresan isi buah, dilanjutkan dengan penambahan air dan gula
pasir. Sari buah pekat/sirup, yaitu cairan yang dihasilkan dari pengepresan daging
buah dan dilanjutkan dengan proses pemekatan, baik dengan cara pendidihan
maupun dengan penguapan hampa udara. Sirup ini tidak dapat langsung diminum,
tetapi harus diencerkan dulu dengan air (Badan Litbang Pertanian, 1989).
Markisa mempunyai nama lain yaitu, maracujá (Portugis), maracuyá
(Spanyol), passion fruit (Inggris), markisa (Indonesia) yang termasuk dalam
family Passifloraceae. Diperkirakan ada 500 spesies Passiflora dalam family
Passifloraceae, diantaranya markisa ungu (Passiflora edulis Sims.), dan markisa
kuning (Passiflora flavicarpa Deg.). Markisa ungu (Passiflora edulis Sims.) buah
muda berwarna hijau, sedangkan buah tua berwarna ungu tua, kulit buah keras.
1
xv
Markisa kuning (Passiflora flavicarpa Deg.) buah muda berwarna hijau,
sedangkan buah tua berwarna kuning muda, kulit buah tebal dan keras
(Anonima, 2003).
Markisa ungu merupakan buah yang kaya akan kandungan vitamin A,
vitamin C, vitamin B kompleks, fosfor, kalsium, kalium, karbohidrat, besi, air,
lemak, protein. Kandungan vitamin C yang terdapat pada buah dapat
meningkatkan daya tahan tubuh, merangsang pertumbuhan sel muda pada kulit
wajah, membantu metabolisme tubuh, sebagai anti oksidan, mencegah sariawan,
dan gusi berdarah (Anonimb, 2008).
Vitamin adalah senyawa-senyawa organik yang dibutuhkan untuk
meningkatkan daya tahan tubuh manusia yang secara alami tidak mampu untuk
mensintesis senyawa-senyawa tersebut tetapi sangat penting untuk pengaturan
metabolisme tubuh. Vitamin C dapat ditemukan pada buah-buahan juga
sayur-sayuran, kadarnya sangat dipengaruhi oleh pengolahan dan pendiaman dimana
vitamin ini mudah larut dalam air dan mudah rusak oleh oksidasi, panas,
pendiaman dan alkali. Penurunan kadar vitamin C akibat oksidasi dan udara dapat
dicegah dengan mengupayakan pengerjaannya secepat mungkin karena sifat dari
vitamin tersebut (Budiyanto, 2004).
Vitamin C dapat ditentukan kadarnya dengan beberapa metode seperti
titrasi iodimetri (Andarwulan dan Koswara, 1992), titrasi 2,6-diklorofenol
indofenol (Andarwulan dan Koswara, 1992; Horwitz, 2002), dan secara
spektrofotometri ultraviolet (Andarwulan dan Koswara, 1992).
Kebiasaan sebagian masyarakat yang sering meminum sari markisa yang
telah didiamkan beberapa jam menyebabkan peneliti tertarik untuk menetapkan
2
xvi
kadar vitamin C yang terdapat pada sari markisa segar, didiamkan selama 1 jam, 4
jam, dan 8 jam. Pada penelitian ini digunakan metode volumetri dengan
2,6-diklorofenol indofenol dimana terjadi reaksi reduksi 2,6-2,6-diklorofenol indofenol
dengan vitamin C.
Vitamin C akan mereduksi 2,6-diklorofenol indofenol maka kelebihan
larutan 2,6-diklorofenol indofenol sedikit saja akan terlihat dengan terjadinya
pewarnaan, dan juga merupakan cara yang paling selektif digunakan untuk
menentukan kadar vitamin C dalam bahan pangan (Andarwulan dan Koswara,
1992).
1.2Perumusan Masalah
a. Berapakah kadar vitamin C yang terdapat pada sari markisa ungu
(Passiflora edulis Sims.) segar dan sesudah didiamkan selama 1 jam, 4
jam, dan 8 jam.
b. Ada perbedaan kadar vitamin C yang terdapat pada sari markisa ungu
(Passiflora edulis Sims.) segar dan sesudah didiamkan selama 1 jam, 4
jam, dan 8 jam.
1.3 Hipotesis
a. Terdapat kadar vitamin C yang tinggi pada sari markisa ungu (Passiflora
edulis Sims.) segar dan kadar vitamin C berkurang sesudah didiamkan
selama 1 jam, 4 jam, dan 8 jam.
b. Terjadi penurunan kadar vitamin C pada sari markisa ungu (Passiflora
edulis Sims.) setelah didiamkan selama 1 jam, 4 jam, dan 8 jam.
3
xvii 1.4 Tujuan Penelitian
a. Untuk menetapkan kadar vitamin C pada sari markisa ungu (Passiflora
edulis Sims.) segar dan yang didiamkan selama 1 jam, 4 jam, dan 8 jam.
b. Untuk mengetahui penurunan kadar vitamin C pada sari markisa ungu
(Passiflora edulis Sims.) segar dan yang didiamkan selama 1 jam, 4 jam,
dan 8 jam.
1.5Manfaat Penelitian
Manfaat penelitian ini dapat dijadikan sebagai sumber informasi mengenai
kadar vitamin C pada sari markisa ungu (Passiflora edulis Sims.) segar dan yang
didiamkan selama 1 jam, 4 jam, dan 8 jam.
4
xviii BAB II
TINJAUAN PUSTAKA
2.1 Markisa
Markisa tergolong ke dalam tanaman genus Passiflora. Di Indonesia
terdapat dua jenis markisa, yaitu markisa ungu (Passiflora edulis Sims.) yang
tumbuh di dataran tinggi, dan markisa kuning (Passiflora flavicarva Deg.) yang
tumbuh di dataran rendah, taksonomi tanaman markisa ungu sebagai berikut:
Divisi : Spermatophyta
Subdivisi : Angiospermae
Kelas : Dicotyledoneae
Subkelas : Dialypetalae
Ordo : Violales
Famili : Passifloraceae
Genus : Passiflora
Spesies : Passiflora edulis Sims.
Kandungan gizi dalam buah markisa ungu (Passiflora edulis Sims.) setiap
100 gram bagian yang dapat dimakan, antara lain: protein 2,2-2,5 gram,
karbohidrat 15-20 gram, lemak 0,75-1,5 gram, vitamin C 20-30 mg, vitamin A
500 i.u, vitamin B kompleks 1,8 mg, kalium 348 mg, kalsium 10 mg, fosfor 12,50
mg, besi 0,20 mg, air 79 gram (Ahmad, 1999).
2.2 Uraian Tumbuhan
Di Indonesia markisa banyak ditanam di dataran tinggi Malino (Sulawesi
selatan) dan Brastagi (Sumatera utara). Tanaman markisa berupa semak menjalar.
Pada umumnya batang passifloraceae dapat memanjang hingga lebih dari 5 meter
5
xix
dan mengayu. Letak daunnya berselang-seling. Bunganya sempurna berkelopak 5
helai, tajuk bunganya 5 helai. Berbenang sari 5 batang, berputik 3, bakal buahnya
beruang 1, berbiji banyak yang melekat pada 3 bingkai pada dinding buah bagian
dalam. Bijinya dibungkus oleh selaput yang berisikan cairan (sari buah) yang
rasanya manis, asam manis, hingga asam (Anonima, 2003).
Batang semu, persegi, lunak, halus, pangkalnya membulat dan permukaan
licin, pertulangan daun menyirip. Tangkai bersegi panjang 2-6 cm. Bunga tunggal,
bulat, berkelamin 2, terletak diketiak daun, tangkai bergerigi, panjang 3-4 cm, dan
berwarna hijau. Benang sari bertangkai, bentuk tabung, panjang kurang lebih 6 cm
dan berwarna kuning. Mahkota bunga berbentuk lonjong permukaan beralur, dan
berwarna ungu. Buah berbentuk lonjong, panjang kurang lebih 20 cm, diameter
kurang lebih 15 cm, dan berwarna hijau keputihan. Biji berbentuk bulat pipih,
panjang kurang lebih 0,3 cm, dan berwarna putih. Akar tunggang berwarna putih
kotor (Anonimb, 2008).
Tanaman markisa tumbuh di daerah-daerah yang mempunyai ketinggian
antara 800-1.500 m dpl dengan curah hujan minimal 1.200 mm per tahun, suhu
lingkungan antara 20-30oC, tidak banyak angin. Tanaman markisa menghendaki
banyak air dengan curah hujan 1500-2000 mm per tahun dan sinar matahari
langsung (Anonimb, 2008).
Kondisi tanah yang dikehendaki banyak mengandung bahan organik
(subur) dan pH 5,5-6,5. Lokasi tempat bertanam sebaiknya terbuka, walaupun
tanaman tahan naungan. Tanaman tidak tahan terhadap kondisi lahan yang
tergenang air. Pada umumnya lokasi yang sesuai untuk tanaman markisa adalah
dataran tinggi, sehingga kondisi lahannya banyak yang berlereng. Sebaiknya
6
xx
kemiringan lahan tidak lebih dari 15%, jika lebih harus dibuat terasing untuk
memudahkan pemeliharaan tanaman (Anonima, 2003).
2.3. Vitamin C
Vitamin adalah senyawa organik yang diperlukan oleh tubuh dalam jumlah
sedikit, tetapi penting untuk melakukan fungsi metabolik di dalam tubuh. Vitamin
tidak dapat disintesa oleh tubuh kecuali vitamin K, maka vitamin harus ada dalam
makanan yang dikonsumsi (Andarwulan dan Koswara, 1989).
Vitamin C atau asam askorbat mempunyai berat molekul 176,13 dengan
rumus molekul C6H8O6. Vitamin C dalam bentuk murni merupakan kristal putih,
tidak berwarna, tidak berbau dan mencair pada suhu 190-192oC. Senyawa ini
bersifat reduktor kuat dan mempunyai rasa asam. Vitamin C sangat mudah larut
dalam air (1 gram dapat larut sempurna dalam 3 ml air), sedikit larut dalam
alkohol (1 gram larut dalam 50 ml alkohol absolut atau 100 ml gliserin) dan tidak
larut dalam benzen, eter, klorofom, minyak dan sejenisnya. Vitamin C tidak stabil
dalam bentuk larutan, terutma jika terdapat udara, logam-logam seperti Cu, Fe,
dan cahaya (Ditjen POM, 1995).
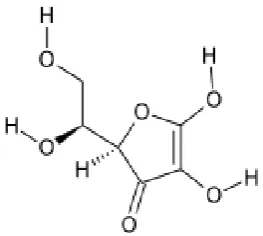
L-asam askorbat
Gambar 1. Rumus Bangun Vitamin C
7
xxi
Vitamin C (L-asam askorbat) bersifat sangat sensitif terhadap
pengaruh-pengaruh luar yang menyebabkan kerusakan seperti suhu, oksigen, enzim, kadar
air, dan katalisator logam. L-asam askorbat sangat mudah teroksidasi menjadi
asam dehidroaskorbat yang masih mempunyai keaktifan sebagai vitamin C. Asam
dehidroaskorbat secara kimia sangat labil dan dapat mengalami perubahan lebih
lanjut menjadi asam diketogulonat yang tidak memiliki keaktifan vitamin C lagi
(Andarwulan dan Koswara, 1989).
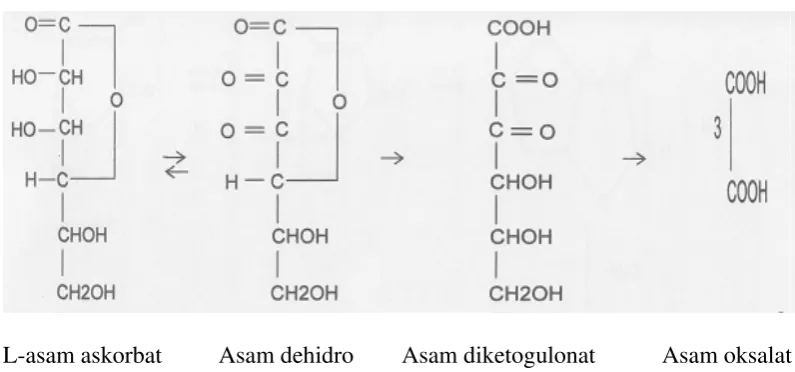
L-asam askorbat Asam dehidro Asam diketogulonat Asam oksalat
askorbat
Gambar 2. Reaksi Perubahan Vitamin C (Silalahi, 1985).
Sumber vitamin C adalah sayuran berwarna hijau, buah-buahan (perlu
diketahui, bahwa rasa asam pada buah tidak selalu sejalan dengan kadar vitamin C
dalam buah tersebut, karena rasa asam disebabkan oleh asam-asam lain yang
terdapat dalam buah bersama dengan vitamin C) (Poedjiadi, 1994).
Vitamin C dapat ditemukan di alam hampir pada semua tumbuhan
terutama sayuran dan buah-buahan, terutama buah-buahan segar. Oleh karena itu
sering disebut Fresh Food Vitamin. Jumlah vitamin C yang terkandung dalam
8
xxii
tanaman tergantung pada varietas dari tanaman, pengolahan, suhu, masa
pemanenan dan tempat tumbuh (Budiyanto, 2004).
Vitamin dapat dibedakan menjadi dua golongan yaitu vitamin yang dapat
larut dalam air dan vitamin yang dapat larut dalam lemak. Jenis vitamin yang
dapat larut dalam air adalah vitamin B kompleks dan vitamin C. Vitamin yang
dapat larut dalam lemak adalah vitamin A, D, E, dan K, serta provitamin A yaitu
betakaroten. Bahan makanan yang kaya akan vitamin adalah sayur-sayuran dan
buah-buahan (Sediaoetama, 2008).
2.4 Fungsi Vitamin C
Salah satu fungsi vitamin C didalam tubuh bersangkutan dengan sifat
alamiahnya sebagai anti oksidan yang berperan serta di dalam banyak proses
metabolisme yang berlangsung di dalam jaringan tubuh, antioksidan adalah
senyawa yang mempunyai struktur molekul yang dapat memberikan elektronnya
dengan cuma-cuma kepada molekul radikal bebas tanpa terganggu sama sekali
dan dapat memutus reaksi berantai dari radikal bebas (Sediaoetama, 2008;
Kumalaningsih, 2006).
Vitamin C dapat terserap sangat cepat dari alat pencernaan masuk ke
dalam saluran darah dan dibagikan keseluruh jaringan tubuh. Pada umumnya
tubuh menahan vitamin ini sangat sedikit. Kelebihan vitamin tersebut dibuang
melalui air kemih, jika seseorang mengkonsumsi vitamin ini dalam jumlah besar
(megadose), sebagian besar akan dibuang keluar, terutama bila orang tersebut
biasa mengkonsumsi makanan yang bergizi tinggi (Winarno, 1984).
Kebutuhan harian vitamin C bagi orang dewasa adalah sekitar 60 mg,
untuk wanita hamil 95 mg, anak-anak 45 mg, dan bayi 35 mg, namun karena
9
xxiii
banyaknya polusi di lingkungan antara lain oleh adanya asap-asap kendaraan
bermotor dan asap rokok maka penggunaan vitamin ini perlu ditingkatkan hingga
dua kali lipatnya yaitu 120 mg (Silalahi, 2006).
Kekurangan asupan vitamin C dapat menyebabkan penyakit sariawan atau
skorbut. Bila terjadi pada anak (6-12 bulan), gejala-gejala penyakit skorbut ialah
terjadinya pelembekan jaringan kolagen, infeksi, dan demam. Pada anak yang
giginya telah keluar, gusi membengkak, empuk dan terjadi pendarahan. Pada
orang dewasa skorbut terjadi setelah beberapa bulan menderita kekurangan
vitamin C dalam makanannya. Gejalanya ialah pembengkakan dan perdarahan
pada gusi, luka lambat sembuh sehingga mudah berdarah dan mengalami infeksi
berulang. Akibat yang parah dari keadaan ini ialah gigi menjadi goyah dan dapat
lepas (Winarno, 1984).
2.5 Metode Penetapan Kadar Vitamin C Metode penentuan kadar vitamin C yaitu:
a. Metode titrasi iodimetri
Iodium mengoksidasi senyawa-senyawa yang mempunyai potensial
reduksi yang lebih kecil dengan potesial reduksi iodum +0,535 volt, dalam hal ini
vitamin C mempunyai potensial reduksi (+0,116 volt) sehingga dapat dilakukan
titrasi langsung dengan iodium (Andarwulan dan Koswara, 1992; Rohman, 2007).
Titik akhir titrasi pada iodimetri ini dilakukan dengan menggunakan
indikator amilum yang akan memberikan warna biru kehitaman pada saat
tercapainya titik akhir titrasi (Gandjar dan Rohman, 2007).
Menurut Andarwulan dan Koswara (1989), metode iodimetri tidak efektif
untuk mengukur kandungan vitamin C dalam bahan pangan, karena adanya
10
xxiv
komponen lain selain vitamin C yang juga bersifat pereduksi. Senyawa-senyawa
tersebut mempunyai titik akhir yang sama dengan wasrna titik akhir titrasi vitamin
C dengan iodin.
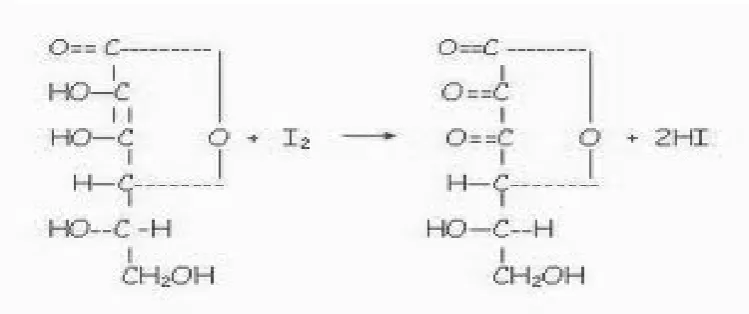
L-asam askorbat Asam dehidroaskorbat
Gambar 3. Reaksi antara vitamin C dan Iodin b. Metode titrasi 2,6-diklorofenol indofenol
Larutan 2,6-diklorofenol indofenol dalam suasana netral atau basa akan
berwarna biru sedangkan dalam suasana asam akan berwarna merah muda.
Apabila 2,6-diklorofenol indofenol direduksi oleh asam askorbat maka akan
menjadi tidak berwarna, dan bila semua asam askorbat sudah mereduksi
2,6-diklorofenol indofenol maka kelebihan larutan 2,6-2,6-diklorofenol indofenol sedikit
saja sudah akan terlihat terjadinya warna merah muda (Sudarmadji dkk, 1989).
Titrasi vitamin C harus dilakukan dengan cepat untuk menghindari
terjadinya oksidasi misalnya pada saat penyiapan sampel. Oksidasi ini dapat
dicegah dengan menggunakan asam metafosfat, asam asetat, asam trikloroasetat,
dan asam oksalat. Penggunaan asam-asam di atas juga berguna untuk mengurangi
oksidasi vitamin C oleh enzim-enzim oksidasi yang terdapat dalam jaringan
xxv
tanaman. Selain itu, larutan asam metafosfat-asetat juga berguna untuk pangan
yang mengandung protein karena asam metafosfat dapat memisahkan vitamin C
yang terikat dengan protein. Suasana larutan yang asam akan memberikan hasil
yang lebih akurat dibandingkan dalam suasana netral atau basa. (Andarwulan dan
Koswara, 1989).
Metode ini pada saat sekarang merupakan cara yang paling banyak
digunakan untuk menentukan kadar vitamin C dalam bahan pangan. Metode ini
lebih baik dibandingkan metode iodimetri karena zat pereduksi lain tidak
mengganggu penetapan kadar vitamin C. Reaksinya berjalan kuantitatif dan
praktis spesifik untuk larutan asam askorbat pada pH 1-3,5. Untuk perhitungan
maka perlu dilakukan standarisasi larutan 2,6-diklorofenol indofenol dengan
vitamin C standar (Sudarmadji dkk, 1989).
+
2,6-diklorofenol indofenol L-Asam Askorbat
Asam Dehidro askorbat 2,6-diklorofenol aminofenol
Gambar 4. Reaksi Asam Askorbat dengan 2,6-Diklorofenol Indofenol HO
Cl
N
OH Cl H
+
HO
Cl
N
O Cl
12
xxvi c. Metode Spektrofotometri Ultraviolet
Metode ini berdasarkan kemampuan vitamin C yang terlarut dalam air
untuk menyerap sinar ultraviolet, dengan panjang gelombang maksimum pada
265 nm dan A11 = 556a . Oleh karena vitamin C dalam larutan mudah sekali
mengalami kerusakan, maka pengukuran dengan cara ini harus dilakukan secepat
mungkin. Untuk memperbaiki hasil pengukuran, sebaiknya ditambahkan senyawa
pereduksi yang lebih kuat daripada vitamin C. Hasil terbaik diperoleh dengan
menambahkan larutan KCN (sebagai stabilisator) ke dalam larutan vitamin
(Andarwulan dan Koswara, 1989; Moffat dkk, 2005).
2.6 Analisis Kembali Vitamin C yang Ditambahkan pada Sampel (Analisis
Recovery)
Akurasi adalah ukuran yang menunjukkan kedekatan hasil analisis dengan
kadar analit yang sebenarnya. Akurasi dinyatakan sebagai persen perolehan
kembali (% recovery) analit yang ditambahkan (Harmita, 2004).
Kecermatan (Recovery) ditentukan dengan dua cara yaitu metode simulasi
(Spiked – placebo recovery) dan metode penambahan baku (Standard addition
method). Dalam metode simulasi, sejumlah analit bahan murni ditambahkan ke
dalam campuran bahan pembawa sediaan farmasi (plasebo) lalu campuran
tersebut dianalisis dan hasilnya dibandingkan dengan kadar analit yang
ditambahkan (kadar analit sebenarnya). Dalam metode penambahan baku
dilakukan dengan menambahkan sejumlah analit dengan konsentrasi tertentu pada
sampel yang diperiksa, lalu dianalisis dengan metode tersebut. Persen perolehan
kembali ditentukan dengan menentukan berapa persen analit yang ditambahkan
tadi dapat ditemukan (Harmita, 2004).
13
xxvii Rumus perhitungan persen Recovery:
% Recovery =
B – A
X 100 % C
Keterangan:
A = Kadar vitamin C sebelum penambahan baku vitamin C
B = Kadar vitamin C setelah penambahan baku vitamin C
C = Kadar vitamin C baku yang ditambahkan
2.7 Analisis Data Secara Statistik 2.7.1 Penolakan Hasil Pengamatan
Di antara hasil yang diperoleh dari satu seri penetapan kadar terhadap satu
macam sampel, ada kalanya terdapat hasil yang sangat menyimpang bila
dibandingkan dengan yang lain tanpa diketahui kesalahannya secara pasti
sehingga timbul kecenderungan untuk menolak hasil yang sangat menyimpang
(Gandjar dan Rohman, 2007).
Untuk memastikan hasil yang sangat menyimpang ditolak atau diterima,
perlu dilakukan analisis data secara statistika. Pada taraf kepercayaan 95% (α =
0,05), hasil analisis ditolak jika Qhitung > Qtabel (Gandjar dan Rohman, 2007).
14
xxviii BAB III
METODE PENELITIAN
Penelitian ini merupakan penelitian deskriptif. Penelitian ini bertujuan
untuk mengetahui kadar vitamin C dari sari markisa secara volumetri dengan
2,6-diklorofenol indofenol.
3.1 Waktu dan Tempat Penelitian
Penelitian dilakukan di laboratorium Kimia Farmasi Kualitatif Fakultas
Farmasi Universitas Sumatera Utara, pada bulan Agustus 2012 – Oktober 2012.
3.2 Identifikasi Tumbuhan
Identifikasi tumbuhan dilakukan oleh Herbarium Medanense (MEDA)
Universitas Sumatera Utara. Hasil identifikasi tumbuhan dapat dilihat pada
Lampiran 1, halaman 33.
3.3 Bahan dan Alat 3.3.1 Alat-alat
Alat-alat yang digunakan dalam penelitian ini adalah mikroburet 5 ml,
neraca analitik (Bueco Germany), pisau (Stenless), blender (Miyako), kertas
saring, statif dan klem, eksikator, oven (Memmert), pipet volum, botol timbang,
dan alat-alat gelas laboratorium.
3.3.2 Bahan-bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah berkualitas
proanalisis dari E.Merck jika tidak dinyatakan lain yaitu 2,6-diklorofenol
indofenol, asam metafosfat, asam asetat glasial 96 %, asam askorbat baku
15
xxix
(Jiangsu nutraceutical. CO.,I..TD), natrium bikarbonat 0,084 % (b/v), aquades
(Rudang).
3.4 Rancangan Penelitian 3.4.1 Sampel
3.4.1.1 Pengambilan Sampel
Metode pengambilan sampel yang digunakan adalah sampling purposif
yaitu sampel dipilih dengan pertimbangan sesuai dengan tujuan (purpose)
penelitian. Pengambilan sampel secara purposif, tanpa membandingkannya
dengan tumbuhan yang sama pada daerah lain.
Karakteristik buah markisa yang digunakan dalam penelitian ini adalah
kulit buah berwarna ungu (Passiflora edulis Sims.) yang diperoleh dari Pasar
Tradisional Padang Bulan, Medan, kilometer 4,5 yang berasal dari Desa
Ajinembah, Kecamatan Merek, Kabupaten Tanah Karo. Sampel diambil 2 kg,
disimpan dan diuji sesuai dengan prosedur penelitian. Gambar dapat dilihat pada
Lampiran 3, halaman 35.
3.5 Prosedur Penelitian 3.5.1 Pembuatan Pereaksi
Pembuatan pereaksi berdasarkan Farmakope Indonesia Edisi IV:
1. Larutan 2,6-diklorofenol indofenol 0,0008 N
Ditimbang seksama 62,5 mg natrium 2,6-diklorofenol indofenol yang telah
disimpan dalam eksikator, tambahkan 62,5 ml larutan NaHCO3 0,084% (b/v),
kocok kuat, setelah larut tambahkan aquades hingga 250 ml. Saring ke dalam
botol bersumbat kaca berwarna coklat.
16
xxx 2. Larutan asam metafosfat-asetat
Dilarutkan 15 g asam metafosfat dalam 40 ml asam asetat glasial dan
encerkan dengan air secukupnya hingga 500 ml. Simpan di tempat dingin, hanya
boleh digunakan dalam 2 hari.
3. Larutan NaHCO3 0,084 % (b/v)
Dilarutkan 84 mg NaHCO3 dalam 100 ml air.
3.5.2 Perhitungan Kesetaraan Pentiter 2,6-diklorofenol Indofenol
Ditimbang seksama 50 mg asam askorbat baku, pindahkan ke dalam labu
tentukur 100 ml, kemudian dilarutkan dengan larutan asam metafosfat-asetat,
dicukupkan sampai garis tanda. Dipipet 1 ml, dimasukkan ke dalam erlenmeyer
dan ditambahkan larutan asam metafosfat-asetat 6 ml. Titrasi segera dengan
larutan 2,6-diklorofenol indofenol hingga warna merah muda mantap tidak kurang
dari 5 detik. Lakukan titrasi blanko menggunakan 7 ml asam metafosfat-asetat dan
dititrasi dengan larutan 2,6-diklorofenol indofenol hingga warna merah muda
mantap. Kadar larutan baku 2,6-diklorofenol indofenol dinyatakan dengan
kesetaraan dalam mg asam askorbat (Horwitz, 2002).
Perhitungan kesetaraan dilakukan dengan rumus:
Kesetaraan (mg) =
Keterangan :
Va = Volume aliquot (ml)
W = Berat vitamin C (mg)
Vt = Volume titrasi (ml)
Vb = Volume blanko (ml)
Vc = Volume labu tentukur (ml)
17
xxxi
Contoh perhitungan dan hasil perhitungan dapat dilihat pada Lampiran 5,
halaman 39.
3.5.3 Penyiapan Larutan Sampel
Markisa dicuci dengan menggunakan air bersih, dilap dengan kain bersih,
dan ditimbang 2 kg buah markisa. Kemudian markisa dibelah menjadi dua bagian
dikeluarkan isinya dari kulitnya. Ditimbang isi markisa 500 gram dan diblender,
disaring, kemudian ditimbang 30 gram lalu dimasukkan ke dalam labu tentukur
100 ml, ditambahkan aquades sampai garis tanda, dihomogenkan, kemudian
disaring ke dalam erlenmeyer, filtrat pertama dibuang ± 20 ml, dan didiamkan
selama 1 jam, 4 jam dan, 8 jam.
3.5.4 Penetapan Kadar Vitamin C dari Larutan Sampel
Dipipet 10 ml filtrat, dimasukkan ke dalam erlenmeyer. Ditambahkan 5 ml
asam metafosfat-asetat. Dititrasi sari yang segar dengan larutan 2,6 diklorofenol
indofenol sampai terbentuk warna merah jambu sebagai titik akhir titrasi. Sesudah
didiamkan selama 1 jam, 4 jam dan 8 jam dipipet 10 ml filtrat, dimasukkan ke
dalam erlenmeyer. Ditambahkan 5 ml asam metafosfat-asetat. Dititrasi dengan
larutan 2,6 diklorofenol indofenol sampai terbentuk warna merah jambu sebagai
titik akhir titrasi dan dilakukan 6 kali pengulangan. Dilakukan penetapan blanko
(Horwitz, 2002).
Kadar Vitamin C (mg/g) =
Keterangan:
Vt = Volume titrasi (ml) Vb = Volume blanko (ml) VI = Volume labu tentukur (ml) Vp = Volume pemipetan (ml) Bs = Berat sampel (g)
18
xxxii
Contoh perhitungan dapat dilihat pada Lampiran 6, halaman 42.
3.5.5 Penetapan Kadar Baku Vitamin C dengan Metode 2,6 Diklorofenol Indofenol
Ditimbang 100 mg baku vitamin C, dimasukkan dalam labu tentukur
100 ml, ditambahkan aquades sampai garis tanda, dilarutkan. Dipipet 1 ml
dimasukkan ke dalam erlenmeyer. Ditambahkan 5 ml asam metafosfat-asetat.
Dititrasi dengan larutan 2,6 diklorofenol indofenol sampai terbentuk warna merah
jambu sebagai titik akhir titrasi. Sesudah didiamkan selama 1 jam, 4 jam dan 8
jam dipipet 1 ml filtrat, dimasukkan ke dalam erlenmeyer. Ditambahkan 5 ml
asam metafosfat-asetat. Dititrasi dengan larutan 2,6 diklorofenol indofenol sampai
terbentuk warna merah jambu sebagai titik akhir titrasi dan dilakukan 6 kali
pengulangan. Dilakukan penetapan blanko (Horwitz, 2002).
Kadar Vitamin C (mg/g) =
Keterangan:
Vt = Volume titrasi (ml)
Vb = Volume blanko (ml)
VI = Volume labu tentukur (ml)
Vp = Volume pemipetan (ml)
Bs = Berat sampel (g)
3.5.6 Uji Perolehan Kembali (Recovery)
Akurasi adalah ukuran yang menunjukkan kedekatan hasil analisis dengan
kadar analit yang sebenarnya. Akurasi dinyatakan sebagai persen perolehan
kembali (% recovery) analit yang ditambahkan (Harmita, 2004).
Metode adisi dapat dilakukan dengan menambahkan sejumlah analit
dengan konsentrasi tertentu pada sampel yang diperiksa, lalu dianalisis dengan
19
xxxiii
motode tersebut. Persen perolehan kembali ditentukan dengan menentukan berapa
persen analit yang ditambahkan tadi dapat ditemukan (Harmita, 2004).
Prosedur uji perolehan kembali (recovery) dengan metode adisi dilakukan
sebagai berikut: dikerjakan dengan prosedur yang sama seperti penetapan kadar
vitamin C dalam sampel dengan penambahan vitamin C baku yaitu 2,5 mg dengan
cara sebanyak 25 mg vitamin C baku dimasukkan ke dalam labu tentukur 100 ml
dan ditambahkan asam metafosfat-asetat sampai garis tanda (konsentrasi 0,25
mg/100 ml), lalu di pipet sebanyak 10 ml yang ditambahkan pada sampel yang
ditimbang seksama dan dilakukan enam kali pengulangan.
Menurut Harmita (2004), rumus perhitungan persen recovery adalah:
% Recovery = X 100%
Keterangan:
A = Kadar vitamin C sebelum penambahan baku vitamin
B = Kadar vitamin C setelah penambahan baku vitamin C
C = Kadar vitamin C baku yang ditambahkan
Data hasil analisis perolehan kembali (persen recovery) dapat dilihat pada
lampiran 13, halaman 56.
3.5.7 Analisis Data Secara Statistik 3.5.7.1 Penolakan Hasil Pengamatan
Di antara hasil yang diperoleh dari satu seri penetapan kadar terhadap satu
macam sampel, ada kalanya terdapat hasil yang sangat menyimpang bila
dibandingkan dengan yang lain tanpa diketahui kesalahannya secara pasti
sehingga timbul kecenderungan untuk menolak hasil yang sangat menyimpang
(Gandjar dan Rohman, 2007).
20
xxxiv
Untuk memastikan hasil yang sangat menyimpang ditolak atau diterima,
perlu dilakukan analisis data secara statistika. Pada taraf kepercayaan 95% (α =
0,05), hasil analisis ditolak jika Qhitung > Qtabel (Rohman dan Gandjar, 2007).
Untuk menghitung nilai Q digunakan rumus:
Hasil pengujian atau nilai Q yang diperoleh ditinjau terhadap daftar harga
Q pada Tabel 2.1, apabila Qhitung > Qkritis maka data tersebut ditolak.
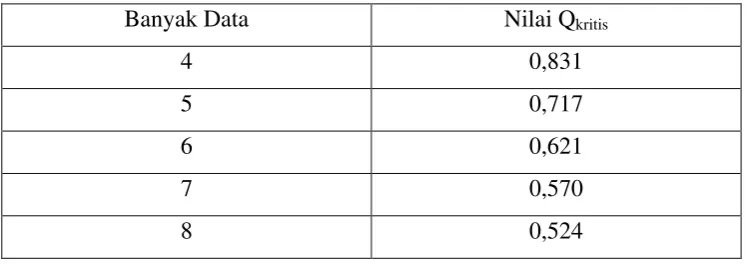
Tabel 1. Nilai Qkritis pada Taraf Kepercayaan 95%
Banyak Data Nilai Qkritis
4 0,831
5 0,717
6 0,621
7 0,570
8 0,524
Menurut Wibisono (2005), untuk menentukan kadar vitamin C di dalam
sampel dengan taraf kepercayaan 95%, α = 0.05, dk = n-1, dapat digunakan
rumus:
μ = X ± t (½α, dk) SD/√n
Keterangan
µ = Interval kepercayaan
X = Kadar rata-rata sampel
t = Harga t tabel sesuai dengan dk = n-1
α = Tingkat kepercayaan SD = Standar deviasi
n = Jumlah perlakuan
21
xxxv
Contoh perhitungan statistik kadar vitamin C dari sampel yang dianalisis
dapat dilihat pada Lampiran 9, halaman 45.
3.5.7.2 Uji Ketelitian (Presisi) Metode Analisis
Uji presisi (ketelitian) adalah ukuran yang menunjukkan derajat
kesesuaian antara hasil uji individual yang diterapkan secara berulang pada
sampel. Ketelitian diukur sebagai simpangan baku relatif (Relative Standard
Deviation) atau koefisien variasi (Harmita, 2004).
Rumus perhitungan persen RSD:
% RSD = ×
X SD
100%
Keterangan:
SD = standar deviasi
X= kadar rata-rata sampel
Data hasil perhitungan koefisien variasi (%RSD) dapat dilihat pada
Lampiran 14, halaman 57.
3.5.7.3 Pengujian Beda Nilai Rata-rata
Untuk mengetahui apakah kadar vitamin C berbeda pada tiap sampel,
maka dilakukan uji beda rata-rata kadar sampel yang diuji dengan uji F
menggunakan SPSS 17. Data berbeda secara signifikan jika F hitung > F tabel dan
data tidak berbeda secara signifikan jika F hitung < F tabel. Jika data yang diperoleh
berbeda secara signifikan, maka dilanjutkan dengan uji himpunan homogen
dengan cara analisis Duncan.
22
xxxvi BAB IV
HASIL DAN PEMBAHASAN 4.1 Identifikasi Tumbuhan
Hasil identifikasi tumbuhan yang dilakukan oleh Herbarium Medanense
(MEDA) Universitas Sumatera Utara adalah markisa ungu (Passiflora edulis
Sims.) Termasuk suku passifloraceae (Hasil identifikasi tumbuhan dapat dilihat
pada Lampiran 1, halaman 33).
4.2 Penetapan Kadar Baku Vitamin C dan Sari Markisa dengan Variasi Waktu
Hasil penetapan kadar vitamin C dari sari markisa segar dan baku vitamin
C pertama kali dilarutkan dan sesudah didiamkan selama 1 jam, 4 jam dan 8 jam,
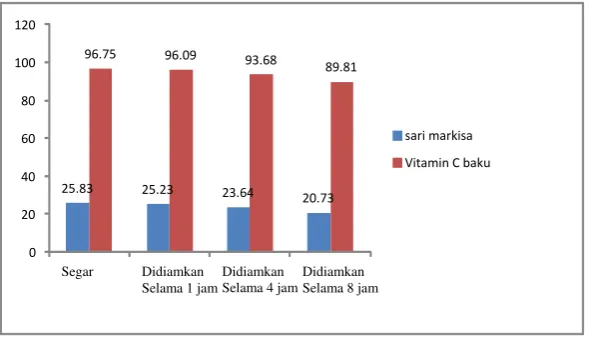
dapat dilihat pada Gambar 5 di bawah ini.
Gambar 5. Diagram Batang Kadar Baku Vitamin C dan Sari Markisa dengan Variasi Waktu.
Penetapan kadar vitamin C dilakukan secara volumetri dengan
2,6-diklorofenol indofenol. Data hasil penetapan kadar vitamin C dari sari markisa
segar dan baku vitamin C terlebih dahulu dilarutkan dan dibiarkan selama 1 jam,
4 jam, dan 8 jam dapat dilihat pada Tabel 2.
xxxvii
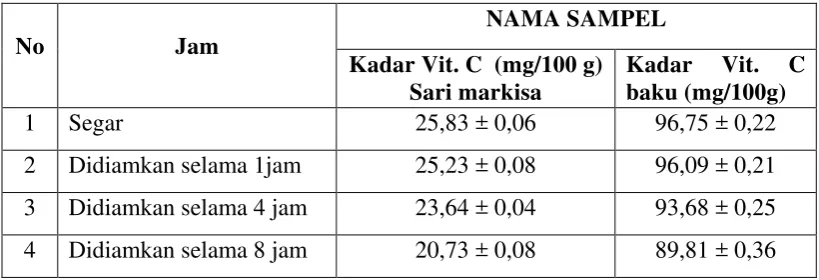
Tabel 2. Hasil Penetapan Kadar Baku Vitamin C dan Sari Markisa dengan Variasi Waktu.
No Jam
NAMA SAMPEL Kadar Vit. C (mg/100 g)
Sari markisa
Kadar Vit. C baku (mg/100g)
1 Segar 25,83 ± 0,06 96,75 ± 0,22
2 Didiamkan selama 1jam 25,23 ± 0,08 96,09 ± 0,21
3 Didiamkan selama 4 jam 23,64 ± 0,04 93,68 ± 0,25
4 Didiamkan selama 8 jam 20,73 ± 0,08 89,81 ± 0,36
Hasil analisis kemudian dilanjutkan dengan pengujian beda nilai kadar
rata-rata vitamin C sari markisa antar waktu, yaitu uji F dengan taraf kepercayaan
95% untuk mengetahui apakah variasi antar waktu sama atau berbeda
menggunakan Statistical Product And Service Solution (SPSS) dapat dilihat pada
Tabel 4.
Pada tabel di atas dapat kita lihat penurunan kadar baku vitamin C dan sari
markisa pada variasi waktu tertentu, dimana kadar baku vitamin C dan sari
markisa memiliki nilai penurunan yang berbeda pada tiap variasi waktu tertentu.
Persen penurunan dapat dilihat pada Tabel 3.
Tabel 3. Persen Penurunan Baku Vitamin C dan Sari Markisa pada Variasi Waktu
No Jam
NAMA SAMPEL
Kadar Vit. C (%) Kadar Vit. C baku (%)
1 Segar 0 0
2 Didiamkan selama 1jam 0,6 0,66
3 Didiamkan selama 4 jam 1,59 2,41
4 Didiamkan selama 8 jam 2,91 3,87
24
xxxviii
Tabel 4. Uji F Kadar Vitamin C dari Sari Markisa dengan Variasi Waktu.
Jumlah
Kuadrat Df
Rata-Rata
Kuadrat F Sig.
Antar Kelompok 93.509 3 31.170 7.1993 .000
Dalam Kelompok .087 20 .004
Total 93.595 23
Pada Tabel 4 di atas, diperoleh Fhitung sebesar 7.1993 dan Ftabel sebesar 3,10
dimana Fhitung > Ftabel. Hal ini menunjukkan bahwa kadar vitamin C sari markisa
segar yang didiamkan selama 1 jam, 4 jam, dan 8 jam, berbeda secara statistik.
Karena terdapat perbedaan yang signifikan, maka dilanjutkan uji himpunan
homogen dengan analisis Duncan.
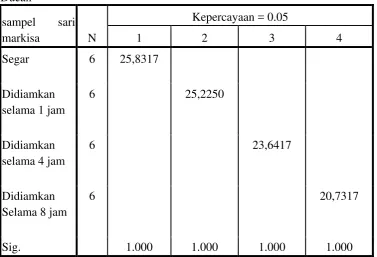
Tabel 5. Analisis Himpunan Homogen Kadar Vitamin C dari Sari Markisa dengan Variasi Waktu.
Ducan
sampel sari
markisa N
Kepercayaan = 0.05
1 2 3 4
Segar 6 25,8317
Didiamkan selama 1 jam
6 25,2250
Didiamkan selama 4 jam
6 23,6417
Didiamkan Selama 8 jam
6 20,7317
Sig. 1.000 1.000 1.000 1.000
Berdasarkan Tabel 5 di atas dapat dilihat bahwa ke empat perlakuan
menurut uji Duncan tidak berada dalam satu himpunan homogen, masing-masing
pada himpunan yang berbeda, artinya bahwa kadar vitamin C pada buah markisa
25
xxxix
yang dilakukan pendiaman dengan waktu yang berbeda pada sari markisa
memberikan hasil yang berbeda, dimana pada buah segar diperoleh kadar vitamin
C 25,83 mg/100 g, pada pendiman 1 jam, 4 jam, dan 8 jam diperoleh kadar
berturut-turut sebesar 25,23 mg/100 g, 23,64 mg/100 g, dan 20,73 mg/100 g ini
membuktikan bahwa lama pendiaman mempengaruhi kadar vitamin C pada sari
markisa.
Berdasarkan hasil penelitian di atas dapat diketahui bahwa kadar vitamin
C berkurang dari sari segar dan setelah pendiaman selama 1 jam, 4 jam dan 8 jam.
Hal ini karena vitamin C mudah larut dalam air, dan mudah rusak oleh oksidasi,
panas, pendiaman dan alkali. Karena itu agar vitamin C tidak banyak hilang,
sebaiknya pada proses pemotongan, penggilingan (blender) dan pendiaman dalam
waktu yang lama harus dihindari. Dalam “processed food”, kehilangan vitamin C
banyak terjadi diakibatkan oleh degradasi kimiawi (Andarwulan dan Koswara,
1989).
Menurut Winarno (1984), menyatakan bahwa dalam pembuatan sari
markisa biasanya terdapat sedikit kerusakan karetenoid pada proses pemanasan
yang lama, dan pendiaman beberapa jam, adanya kerusakan karetenoid perlu
diperhatikan karena karetenoid mudah teroksidasi. Timbulnya kerusakan pada
struktur tersebut dapat menyebabkan perubahan warna yang tidak stabil, misalnya
dari warna kuning berubah pucat dan menjadi putih kekuningan.
Proses pembuatan dan lamanya pembutan dapat mempengaruhi kadar
vitamin C dalam bahan pangan seperti buah-buahan. Pada penetapan kadar
vitamin C dari sari markisa, penyiapan larutan sampel melewati beberapa tahap
pengolahan seperti pemotongan dan penggilingan (blender) dan penimbangan
26 26
xl
yang memakan waktu lebih kurang 20 menit sehingga dapat mengalami
penurunan kadar vitamin C dari sari markisa.
Semua bahan pangan yang diolah akan mengalami derajat kehilangan
vitamin tertentu (tergantung cara pengolahannya). Pada umumnya, diinginkan
suatu pembuatan pangan yang dapat meminimumkan kehilangan zat gizi dan
menghasilkan sediaan yang aman dikonsumsi (Andarwulan dan Koswara, 1989).
4.3 Uji Perolehan Kembali
Hasil uji perolehan kembali (Recovery) vitamin C dari sari markisa dapat
dilihat pada Tabel 6.
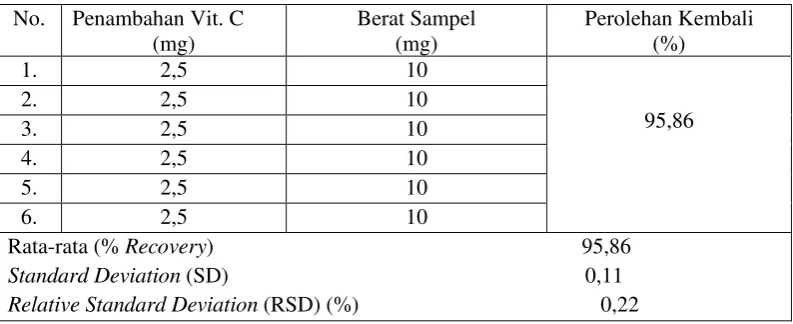
Tabel 6. Hasil Uji Perolehan Kembali dari Sari Markisa.
No. Penambahan Vit. C
(mg)
Berat Sampel (mg)
Perolehan Kembali (%)
1. 2,5 10
95,86
2. 2,5 10
3. 2,5 10
4. 2,5 10
5. 2,5 10
6. 2,5 10
Rata-rata (% Recovery) 95,86 Standard Deviation (SD) 0,11 Relative Standard Deviation (RSD) (%) 0,22
Pada Tabel 6 di atas, diperoleh persen recovery rata-rata adalah 95,86 %
dan persen RSD rata-rata adalah 0,22 % (Contoh perhitungan dan hasil
perhitungan dapat dilihat pada Lampiran 12, halaman 52). Kisaran rata-rata hasil
uji perolehan kembali yang diizinkan untuk kadar analit 0,01%-0,1% dalam
sampel yang diperiksa adalah 90%-107%, sedangkan persen RSD yang diizinkan
adalah tidak lebih dari 2% (Harmita, 2004). Dari hasil yang diperoleh tersebut
maka dapat disimpulkan bahwa akurasi dan presisi metode analisis yang
dilakukan cukup tinggi.
27
xli BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Hasil penetapan kadar vitamin C sari markisa secara volumetri dengan
2,6-diklorofenol indofenol diperoleh kadar vitamin C dari sari markisa segar
25,83 ± 0,06 mg/100 g, pada pendiaman 1 jam, 4 jam, dan 8 jam diperoleh kadar
berturut-turut 25,23 ± 0,08 mg/100 g, 23,64 ± 0,04 mg/100 g dan, 20,73 ± 0,08
mg/100 g.
Hasil kadar baku vitamin C setelah dilarutkan diperoleh 96,75 ± 0,22
mg/100 g, pada pendiaman 1 jam, 4 jam, dan 8 jam diperoleh kadar berturut-turut
96,09 ± 0,21 mg/100 g, 93,68 ± 0,25 mg/100 g, 89,81 ± 0,36 mg/100 g. Dari hasil
di atas dapat kita lihat bahwa pada penetapan kadar baku vitamin C dan sari
markisa pada pendiaman 1 jam kadar vitamin C tidak mengalami penurunan yang
signifikan sedangkan pada pendiaman 4 jam dan 8 jam kadar vitamin C
mengalami penurunan yang signifikan.
5.2 Saran
Disarankan kepada masyarakat sebaiknya jangan membiarkan sari markisa
didiamkan lama karena akan mengalami penurunan kadar vitamin C pada sari
markisa tersebut.
28
xlii
DAFTAR PUSTAKA
Ahmad
.
(1999). Nilai Kandungan Gizi Markisa. Diakses tanggal 21 juli 2012.Andarwulan, N., dan Koswara, S. (1989). Kimia Vitamin. Jakarta: Rajawali Press. Hal. 32-35, 44, 235.
Anonima. (2003). Markisa. Diakses tanggal 21 agustus net. id/ind/warintek/pengolahan pangan idx.php.markisa.
Anonimb. (2008). Tanaman Markisa. Diakses tanggal 10 juni 2012. Phytochemicals info/plants/passion-fruit.php.
Badan Litbang Pertanian. (1989), Pembuatan Sirup Buah. Pusat Penelitian dan Pengembangan Hortikultura. Jakarta. Hal. 2.
Budiyanto, A.K. (2004). Dasar-Dasar Ilmu Gizi. Edisi III. Malang: UMM-Press. Hal. 52.
Ditjen POM. (1995). Farmakope Indonesia. Edisi IV. Jakarta: Departemen Kesehatan RI. Hal. 1133, 1216.
Gandjar, I. G., dan Rohman, A. (2007). Kimia Farmasi Analisis. Yogyakarta: Pustaka Pelajar. Hal. 19, 22.
Harmita, (2004). Petunjuk Pelaksanaan Validasi Metode dan Cara Perhitungannya. Majalah Ilmu Kefarmasian 1(3): 118-119, 121-123.
Horwitz, W. (2002). Official Methods of Analysis of Association of Official
Analytical Chemist International. Edisi XVII. Maryland: AOAC
International Suite 500. Hal. 16-17.
Kumalaningsih, S. (2006). Antioksidan Alami. Surabaya: Trubus Angrisarana. Hal. 35.
Moffat, A. C., Osselton, M. D., dan Widdop, B. (2005). Clark’s Analysis of Drug and Poisons. Edisi III. London: Pharmaceutical Press. Hal. 112.
Poedjiadi, A. (1994). Dasar–Dasar Biokimia. Jakarta: Penerbit Universitas Indonesia. Hal. 393.
Sediaoetama, D. (2008). Ilmu Gizi. Jilid I. Jakarta: Penerbit Dian Rakyat. Hal. 19,22.
Silalahi, J. (2006). Makanan Fungsional. Yogyakarta: Penerbit Kanisius. Hal. 52-53.
29
xliii
Silalahi, J. (1985). Some Aspect of Vitamin C Retention in Potato Crisps. Thesis.
School of Food Science and Technology. Wales: The University of New
South Wales. Hal. 5.
Sudarmadji, S., Haryono, B., dan Suhardi. (1989). Analisa Bahan Makanan dan Pertanian. Yogyakarta: Liberty. Hal. 165-166.
Winarno, F.G. (1984). Kimia Pangan dan Gizi. Jakarta: PT. Gramedia Pustaka Utama. Hal. 119, 132-133.
30
xliv Lampiran 1. Sertifikat Identifikasi Tumbuhan
Lampiran 2. Sertifikat Bahan Baku lamPembanding Pabrik
31
xlv
Lampiran 2. Sertifikat Bahan Baku Pembanding
32
xlvi Lampiran 3. Sampel yang Digunakan
Gambar 6. Gambar Buah Markisa Ungu
Gambar 7. Gambar Bagian Isi Buah Markisa Ungu
33
xlvii
Gambar 8. Gambar sari Markisa
Gambar 9. Gambar Supernatan sari Markisa
Gambar 10. Gambar Mikro Buret dan Larutan 2,6-diklorofenol indofenol
34
xlviii Lampiran 4. Flowsheet
A. Sari Markisa
Dicuci dengan air mengalir
Dilap dengan kain bersih kemudian dibelah dan keluarkan isinya
Diblender kemudian saring
B. Kadar Vitamin C dari Sari Markisa
Ditimbang 30 g
Dimasukkan dalam labu tentukur 100 ml
Ditambahkan akuades sampai garis tanda.
Dihomogenkan dan disaring
Didiamkan 1 jam, 4 jam, dan 8 jam
Di pipet 10 ml dan dimasukkan kedalam Erlenmeyer
Ditambahkan 5 ml asam metafosfat asetat
Di titrasi dengan larutan 2,6- diklorofenol indofenol sampai terbentuk warna merah jambu. Buah Markisa
Larutan sampel
Sari
Titik Akhir Ttitrasi Sari
35
xlix C. Baku Vitamin C
Dimasukkan ke dalam labu tentukur 100 ml
Ditambahkan akuades sampai garis tanda
Dihomogenkan
Didiamkan 1 jam, 4 jam dan 8 jam.
Dipipet 1 ml dan dimasukkan ke
dalam Erlenmeyer
Ditambahkan 5 ml asam metafosfat asetat
Di titrasi dengan larutan 2,6- diklorofenol indofenol sampai terbentuk warna merah jambu
100 mg vit.C baku
Larutan vit.C baku
Titik Akhir Ttitrasi
36
l
Lampiran 5. Data Perhitrungan Kesetaraan Larutan 2,6-Diklorofenol Indofenol
Diklorofenol Indofenol (ml) Blanko (ml)
Kesetaraan larutan 2,6-diklorofenol indofenol dapat dihitung dengan rumus:
Kesetaraan =
Contoh perhitungan kesetaraan:
a) Berat vitamin C = 50,3 mg
Volume larutan vitamin C yang dititrasi = 1 ml
Rata rata volume titrasi = 2,63 ml
Volume larutan vitamin C yang dititrasi = 1 ml
li c) Berat vitamin C = 50,6 mg
Volume larutan vitamin C yang dititrasi = 1 ml
Rata rata volume titrasi = 3,12 ml
1 ml x 50,6 mg x
100 90 , 99
K3 = = 0,1631 mg vitamin C / ml 100 ml x (3,12 ml – 0,02 ml)
Harga rata-rata dan deviasi
K1 + K2 0,1925 + 0,1713
Kr1 = = = 0,1819 mg vitamin C / ml
2 2
K2 – Kr1
d1 = x 100% Kr1
0,1713 – 0,1819
= x 100% = 5,8 %
0,1819
K1 + K3 0,1925 + 0,1631
Kr2 = = = 0,1778 mg vitamin C/ ml
2 2
K1 – Kr2
d2 = x 100%
Kr2
0,1925 – 0,1778
= x 100% = 8,3 %
0,1778
K2 + K3 0,1713 + 0,1631
Kr3 = = = 0,1672 mg vitamin C / ml
2 2
38
lii K2 – Kr3
d3 = x 100%
Kr3
0,1713 – 0,1672
= x 100% = 2,5 %
0,1672
Kesetaraan vitamin C dengan harga rata rata d terkecil adalah d3 = 2,5 %,
maka kesetaraan vitamin C yang didapat untuk 1 ml 2,6-diklorofenol indofenol
setara dengan 0,1672 mg vitamin C.
39
liii
Lampiran 6. Perhitungan Kadar Vitamin C dari Sampel yang Dianalisis (Vt – Vb) x Kesetaraan x Vl
Kadar vitamin C (mg/g sampel) =
Vp x Bs
Keterangan:
Vt = volume titrasi (ml)
Vb = volume blanko (ml)
Vl = volume labu (ml)
Vp = volume larutan sampel yang dititrasi (ml)
Bs = berat sampel (g)
Contoh Penetapan kadar vitamin C pada sari Markisa
Volume titran = 4,67 ml
Kesetaraan = 0,1672 mg vitamin C
Volume labu tentukur = 100 ml
Berat sampel = 30,0000 g
Volume blanko = 0,02 ml
(4,67 ml – 0,02 ml) x 0,1672 mg/ml x 100 ml
Kadar vitamin C (mg/g bahan) =
10 ml x 30,0000 g
= 0,2592 mg/g
= 25,92 mg vitamin C/100 g sampel
40
liv
Lampiran 7. Data Hasil Penetapan Kadar Vitamin C pada Sari Markisa 7.1. Sari Markisa segar
NO Berat Sampel Volume Titran Kadar Kadar Rata-rata
(g) (ml) (mg/100g) (mg/100g)
7.2. Didiamkan selama 1 jam
7.3. Didiamkan selama 4 jam
NO Berat Sampel Volume Titran Kadar Kadar Rata-rata
(g) (ml) (mg/100g) (mg/100g)
7.4. Didiamkan selama 8 jam
NO Berat Sampel Volume Titran Kadar Kadar Rata-rata
(g) (ml) (mg/100g) (mg/100g)
NO Berat Sampel VolumeTitran Kadar Kadar Rata-rata
lv
Lampiran 8. Data Hasil Penetapan Kadar Baku Vitamin C 8.1. Baku vitamin C setelah dilarutkan
No. Berat Sampel
8.2. Didiamkan selama 1 jam No. Berat Sampel
8.3. Didiamkan selama 4 jam No. Berat Sampel
lvi
Lampiran 9. Perhitungan statistik kadar vitamin C dari sampel yang dianalisis pada sari Markisa.
9.1. Sari Markisa segar No. Kadar (mg/100 g)
Dari 6 data yang diperoleh, data ke-4 adalah data yang paling menyimpang maka
dilakukan uji Q.
Qhitung = Nilai yang dicurigai – Nilai yang terdekat
Nilai Qhitung tidak melebihi nilai Q0,95 yaitu 0,621 sehingga semua data diterima.
SD =
Rata-rata kadar vitamin C sari Markisa segar pada taraf kepercayaan 95% yaitu:
lvii 9.2. Didiamkan selama 1 jam
No. Kadar (mg/100 g)
Dari 6 data yang diperoleh, data ke-6 adalah data yang paling menyimpang maka
dilakukan uji Q.
Qhitung = Nilai yang dicurigai – Nilai yang terdekat
Nilai Qhitung tidak melebihi nilai Q0,95 yaitu 0,621 sehingga semua data diterima.
SD =
Rata-rata kadar vitamin C pada sari Markisa yang didiamkan selama 1 jam pada
taraf kepercayaan 95% yaitu:
lviii 9.3. Didiamkan selama 4 jam
No. Kadar (mg/100 g)
Dari 6 data yang diperoleh, data ke-4 adalah data yang paling menyimpang maka
dilakukan uji Q.
Qhitung = Nilai yang dicurigai – Nilai yang terdekat
Nilai Qhitung tidak melebihi nilai Q0,95 yaitu 0,621 sehingga semua data diterima.
SD =
Rata-rata kadar vitamin C pada sari Markisa yang didiamkan selama 4 jam pada
taraf kepercayaan 95% yaitu:
lix 9.4. Didiamkan selama 8 jam
No. Kadar (mg/100 g)
Dari 6 data yang diperoleh, data ke-6 adalah data yang paling menyimpang maka
dilakukan uji Q.
Qhitung = Nilai yang dicurigai – Nilai yang terdekat
Nilai Qhitung tidak melebihi nilai Q0,95 yaitu 0,621 sehingga semua data diterima.
SD =
Rata-rata kadar vitamin C sari Markisa yang didiamkan selama 8 jam pada taraf
kepercayaan 95% yaitu:
lx
Lampiran 10. Perhitungan statistik kadar vitamin C baku 10.1 Baku vitamin C setelah dilarutkan
No. Kadar (mg/100 g)
Dari 6 data yang diperoleh, data ke-2 adalah data yang paling menyimpang maka
dilakukan uji Q.
Qhitung = Nilai yang dicurigai – Nilai yang terdekat
Nilai Qhitung tidak melebihi nilai Q0,95 yaitu 0,621 sehingga semua data diterima.
SD =
Rata-rata kadar baku vitamin C setelah dilarutkan pada taraf kepercayaan 95%
lxi 10.2. Didiamkan selama 1 jam
No. Kadar (mg/100 g)
Dari 6 data yang diperoleh, data ke-3 adalah data yang paling menyimpang maka
dilakukan uji Q.
Qhitung = Nilai yang dicurigai – Nilai yang terdekat
Nilai Qhitung tidak melebihi nilai Q0,95 yaitu 0,621 sehingga semua data diterima.
SD =
Rata-rata kadar baku vitamin C yang didiamkan selama 1 jam pada taraf
kepercayaan 95% yaitu:
lxii 10.3. Didiamkan selama 4 jam
No. Kadar (mg/100 g)
Dari 6 data yang diperoleh, data ke-3 adalah data yang paling menyimpang maka
dilakukan uji Q.
Qhitung = Nilai yang dicurigai – Nilai yang terdekat
Nilai Qhitung tidak melebihi nilai Q0,95 yaitu 0,621 sehingga semua data diterima.
SD =
Rata-rata kadar baku vitamin C yang didiamkan selama 4 jam pada taraf
kepercayaan 95% yaitu:
lxiii 10.4. Didiamkan selama 8 jam
No. Kadar (mg/100 g)
Dari 6 data yang diperoleh, data ke-3 adalah data yang paling menyimpang maka
dilakukan uji Q.
Qhitung = Nilai yang dicurigai – Nilai yang terdekat
Nilai Qhitung tidak melebihi nilai Q0,95 yaitu 0,621 sehingga semua data diterima.
SD =
Rata-rata kadar baku vitamin C yang didiamkan selama 8 jam pada taraf
kepercayaan 95% yaitu:
lxiv Lampiran 11. Hasil Analisis Statistik
1.Uji F sari Markisa
Jumlah
Kuadrat Df
Rata-Rata
Kuadrat F Sig.
Antar Kelompok 93.509 3 31.170 7.1993 .000
Dalam Kelompok .087 20 .004
Total 93.595 23
2. Analisis Beda Nilai Rata-Rata Kadar Vitamin C dari Sari Markisa dengan Variasi Waktu.
sampel sari
markisa N
Kepercayaan = 0.05
1 2 3 4
Segar 6 25.8317
Didiamkan selama 1 jam
6 25.2250
Didiamkan selama 4 jam
6 23.6417
Didiamkan selama 8 jam
6 20.7317
Sig. 1.000 1.000 1.000 1.000
3. Uji F Baku Vitamin C
Jumlah
Kuadrat Df
Rata-Rata
Kuadrat F Sig.
Antar Kelompok 177.195 3 59.065 912.835 .000
Dalam Kelompok 1.294 20 .065
Total 178.489 23
51
lxv
4. Analisis Beda Nilai Rata-Rata Kadar Baku vitamin C dengan Variasi Waktu.
Baku vitamin
C N
Kepercayaan = 0.05
1 2 3 4
Setelah dilarutkan
6 96.7533
Didiamkan selama 1 jam
6 96.0850
Didiamkan selama 4 jam
6 93.6783
Didiamkan selama 8 jam
6 89.8133
Sig. 1.000 1.000 1.000 1.000
52