II. METODE PENELITIAN
2.1 Prosedur PenelitianPenelitian ini terdiri atas beberapa tahapan, dimulai dengan pemeliharaan udang vaname ke stadia uji, persiapan wadah dan media, pembuatan pakan meniran, persiapan patogen IMNV, perlakuan udang uji kemudian dilanjutkan pengamatan serta analisis data. Skema metode penelitian lebih rinci dapat dilihat pada Lampiran 1.
2.1.1 Pemeliharaan Udang Vaname (Litopenaeus vannamei)
Udang vaname penelitian ini diperoleh dari PT. Komindo Trading Utama (KTU), Anyer, Banten berukuran PL 10 SPF (spesific pathogen free). Sebelum digunakan untuk perlakuan, udang dipelihara terlebih dahulu selama 35 hari sehingga bobot rata-rata menjadi sebesar 1,37 gram. Akuarium yang digunakan untuk pemeliharaan sebelum perlakuan berukuran 60x50x50 cm berjumlah 4 buah. Sebelumnya akuarium dicuci dan didesinfeksi menggunakan detergen kemudian dikeringkan. Air laut yang digunakan berasal dari Ancol dengan salinitas 29,30 ppt. Air ditampung dalam tandon berukuran 2000 liter dan didesinfeksi dengan kaporit 30 ppm lalu diaerasi kuat selama 3 hari. Selama pemeliharaan, udang diberi pakan lima kali sehari sesuai dengan Feeding Rate (FR), yaitu pada pukul 06.00, 10.00, 12.00, 16.00, dan 22.00 WIB. Untuk menjaga kualitas air wadah pemeliharaan, setiap hari sekali dilakukan penyifonan air sebanyak 30% hingga 50%.
2.1.2 Persiapan Wadah dan Media
Wadah yang digunakan untuk perlakuan penelitian adalah akuarium dengan dimensi 60x30x30 cm berjumlah 24 buah. Sebelumnya akuarium dicuci dan didesinfeksi menggunakan kaporit 100 ppm kemudian dikeringkan. Akuarium diisi oleh air tawar dan didiamkan selama 24 jam. Selain itu, dilakukan pula pemasangan instalasi aerasi pada setiap akuarium. Setelah 24 jam, air dibuang dan dibilas dengan air bersih agar sisa-sisa kaporit yang menempel pada dinding akuarium terbuang. Kemudian akuarium diisi air laut dari tandon berukuran 100 liter. Masing-masing akuarium diisi air sebanyak 40 liter. Selain itu disiapkan
rata-rata 10 cm. Satu shelter dibuat dari 3 pipa paralon yang direkatkan dengan lem paralon. Shelter yang sudah kering didesinfeksi terlebih dahulu sebelum digunakan.
2.1.3 Pembuatan Pakan Mengandung Meniran
Meniran (Phyllantus niruri) untuk penelitian ini diperoleh dari Balitro, Cimanggu, Bogor. Tepung meniran dibuat dari bagian daun yang sebelumnya dicuci kemudian dikeringkan lalu dihaluskan dengan blender. Daun meniran yang sudah diblender disaring untuk mendapatkan ukuran yang lebih kecil. Sebelumnya campuran tepung meniran dengan putih telur sebanyak 2,5% dari jumlah pakan. Setelah itu, pakan komersil dimasukkan lalu diaduk dengan campuran meniran dan putih telur. Pakan yang sudah tercampur rata kemudian dikeringanginkan. Pakan yang mengandung meniran ini disimpan di dalam kotak plastik dan disimpan pada suhu ruang. Proses pembuatan pakan meniran dapat dilihat pada Lampiran 2.
2.1.4 Sumber Patogen IMNV
Sumber patogen IMNV berasal dari udang yang terinfeksi IMNV diperoleh dari tambak Pinang Gading, Bakauheni, Lampung. Sebelum diberikan ke udang uji patogen IMNV diganaskan (virulensi) dan diperbanyak pada udang yang lain. Perlakuan virulensi dan perbanyakan udang dilakukan pada akuarium berdimensi 30x30x50 cm berjumlah 3 buah. Infeksi virulensi dan perbanyakan IMNV dilakukan melalui oral, yaitu dengan memberikan pakan berupa daging udang yang sudah terinfeksi IMNV kepada udang lain. Untuk perlakuan pada udang uji-pun sama. Saat akan digunakan, udang dibersihkan dari karapas, kepala, dan ekor, sehingga diperoleh daging udang secara utuh, kemudian diblender dan ditimbang sesuai FR udang. Selanjutnya dapat diberikan pada udang uji.
2.1.5 Perlakuan Udang Uji
Penelitian ini terdiri dari lima perlakuan dengan tiga ulangan ditambah satu ulangan untuk histopatologi, perlakuan dosis meniran adalah sebagai berikut : Perlakuan A: Udang tidak diberi pakan meniran dan tidak diinfeksi IMNV
Perlakuan B: Udang tidak diberi pakan meniran dan diinfeksi IMNV (kontrol positif)
Perlakuan C: Udang diberi pakan meniran 10 mg/kg pakan dan diinfeksi IMNV Perlakuan D: Udang diberi pakan meniran 20 mg/kg pakan dan diinfeksi IMNV Perlakuan E: Udang diberi pakan meniran 30 mg/kg pakan dan diinfeksi IMNV
Sebelum diberi perlakuan udang diaklimatisasikan terlebih dahulu selama seminggu. Setiap akuarium ditebar udang masing-masing 10 ekor untuk pengamatan mortalitas dan pengamatan histopatologi 20 ekor/akuarium. Udang uji sebelum perlakuan ditimbang bobotnya menggunakan timbangan digital pada awal dan setiap minggunya untuk disampling. Kualitas air dipertahankan sesuai dengan kehidupan udang dan dilakukan pergantian air 30-50% dari volume total sebelum pemberian pakan.
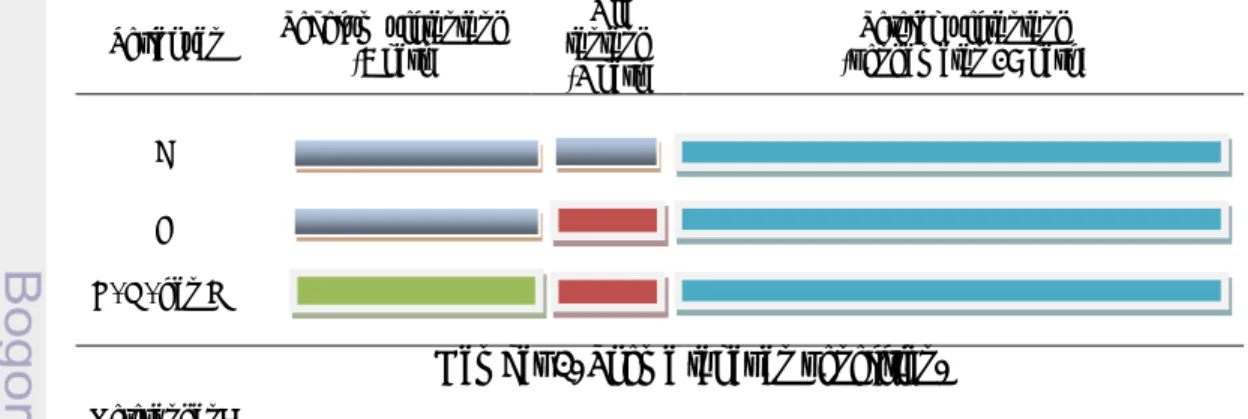
Udang uji kecuali perlakuan kontrol diberi pakan meniran sehari dengan feeding time lima kali sehari selama 7 hari sesuai dengan dosis yang ditentukan. Pemberian pakan meniran sesuai FR udang. Kemudian selama 3 hari, udang uji diberi pakan daging udang terinfeksi IMNV. Selama masa penginfeksian tidak dilakukan pergantian air. Hari ke-10 hingga hari ke-38 udang uji diberi pakan komersil dan dilakukan pengamatan untuk semua perlakuan pascainfeksi. Gambar 1 merupakan skema tahapan penelitian yang dilakukan.
Perlakuan Sebelum uji tantang(7 hari) tantangUji (3 hari)
Setelah uji tantang (pengamatan 29 hari ) A
B C, D, dan E
Gambar 1. Skema tahapan penelitian.
Keterangan:
= Tidak ada perlakuan infeksi IMNV dan ekstrak meniran = Pemeliharaan setelah uji tantang
= Infeksi IMNV
= Pemberian pakan meniran 10 mg/kg (perlakuan C), 20 mg/kg (perlakuan D), 30 mg/kg (perlakuan E)
32 h
3 h 32 h
2.2 Parameter yang Diamati 2.2.1 Tingkat Kelangsungan Hidup
Penghitungan jumlah udang yang masih hidup dilakukan pada akhir penelitian. Kelangsungan hidup udang uji dihitung dengan menggunakan persamaan sebagai berikut (Effendi 2004):
Keterangan:
SR = tingkat kelangsungan hidup (survival rate) (%) Nt = jumlah udang akhir (ekor)
No = jumlah udang awal (ekor) 2.2.2 Laju Pertumbuhan Spesifik
Bobot udang ditimbang di awal dan akhir pengamatan dengan menggunakan timbangan ketelitian 0,01. Laju pertumbuhan spesifik dapat diketahui dengan menggunakan rumus menurut Effendi (2004) :
Keterangan :
= laju pertumbuhan spesifik (%) Wt = bobot rata-rata ikan pada waktu t (g) Wo = bobot rata-rata ikan pada waktu awal (g) t = waktu pemeliharaan (hari)
2.2.3 Gejala Klinis
Keberadaan IMNV pada udang uji dengan melihat gejala klinis. Gejala klinis merupakan gejala yang timbul dari udang yang terinfeksi. Pengamatan dilakukan setiap hari secara obyektif dengan cara mengamati perubahan yang terjadi pada tubuh udang. Gejala klinis yang diamati ialah terbentuknya otot berwarna putih pada bagian ruas tubuh udang. Pengamatan gejala klinis dilakukan dengan pemberian scoring pada udang yang menunjukkan gejala otot putih, yaitu – (tidak ada gejala klinis), + (adanya otot putih pada ruas ke-5 sampai ke-6), ++
(adanya otot putih pada ruas ke-3 sampai ke-6), dan +++ (adanya otot putih pada seluruh ruas tubuh).
2.2.4 Respons Nafsu Makan
Pengamatan respon makan dilakukan setelah infeksi selama 29 hari. Pengamatan respon terhadap pemberian pakan menurut Evan (2009) dapat dilihat dari sisa pakan yang dimakan dan diklasifikasikan sebagai berikut :
Sangat responsif (++++) = tidak ada sisa pakan
Responsif (+++) = sisa pakan sebanyak 0 % - 10% Responsif sedang (++) = sisa pakan sebanyak 10% - 50% Kurang responsif (+) = sisa pakan sebanyak 50% - 80% Tidak responsif (-) = sisa pakan 80% - 100%
2.2.5 Kualitas Air
Pengukuran kualitas air dilakukan pada awal dan akhir penelitian yang terdiri dari mengecekan suhu, salinitas, pH, DO (Dissolved oxygen), dan TAN (Total Ammonia Nitrogen).
2.2.6 Analisis Histopatologi
Untuk melihat perubahan yang ditimbulkan akibat virus IMNV pada udang dilakukan pengamatan histopatologi. Pemeriksaan histologi adalah salah satu cara untuk mendeteksi adanya komponen patogen yang bersifat infektif melalui pengamatan secara mikro anatomi. Histologi adalah cabang ilmu biologi yang mempelajari tentang jaringan. Patologi adalah kajian tentang panyakit atau adaptasi terhadap perubahan-perubahan lingkungan eksternal dan internal (Spector dan Spector 1993). Jaringan udang yang dianalisis histopatologi ialah bagian hepatopankreas dan jaringan otot. Pengambilan sampel untuk analisa histopatologi dilakukan sebelum uji tantang dan sesudah uji tantang dengan IMNV. Proses pembuatan preparat histopatologi pada Lampiran 3.
2.2.7 Analisis Data
Data yang diperoleh dianalisis dengan menggunakan Microsoft Excel 2010 untuk membuat grafik dan diagram batang. Uji beda nyata dilakukan menggunakan analisis SPSS 16.0.