Praktikum KI2051 Kimia Organik
Percobaan 09
REAKSI SIKLO ADISI
DIELS-ALDER DAN RETRO DIELS-ALDER
&
Percobaan 10
KONDENSASI SENYAWA KARBONIL: Sintesis Dibenzalaseton
L A P O R A Noleh
Nama : Hasna Nisrina Firdausi
NIM : 13014038
Kelompok : III
Shift : Rabu siang
Tanggal Percobaan : 23 Maret 2016 Tanggal Pengumpulan : 30 Maret 2016
Asisten : Handani Andri (10513047)
LABORATORIUM KIMIA ORGANIK PROGRAM STUDI KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT TEKNOLOGI BANDUNG
Percobaan 9 Reaksi Siklo Adisi Diels-Alder dan Retro Diels-Alder
A. Tujuan Percobaan
1. Menentukan rendemen senyawa hasil reaksi Diels-Alder dan retro Diels-Alder 2. Menentukan titik leleh kristal hasil reaksi Diels-Alder dan retro Diels-Alder B. Prinsip Percobaan
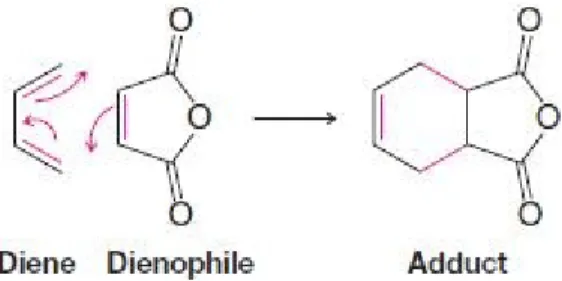
Secara umum, reaksi Diels-Alder adalah reaksi antara diena terkonjugasi (sistem 4π-elektron) dan senyawa yang mengandung ikatan rangkap dua (sistem 2π-4π-elektron) yang disebut dienofil (menyukai diena). Produk reaksi Diels-Alder disebut adduct. Dalam reaksi ini, dua ikatan baru dihasilkan dengan mengorbankan dua ikatan π dari diena dan dienofil. Adduct yang dihasilkan memiliki cincin dengan ikatan rangkap. Karena ikatan
biasanya lebih kuat daripada ikatan π, pembentukkan adduct akan lebih dominan namun kebanyakan reaksi Diels-Alder adalah reaksi bolak-balik. Pada umumnya, dienofil bereaksi dengan diena terkonjugasi melalui adisi 1,4 membentuk cincin. Proses ini disebut [4+2] sikloadisi, yang dinamai berdasarkan nomor atom dari masing-masing reaktan yang berikatan dengan cincin. Posisi manapun di kedua sisi diena atau dienofil dapat mengalami substitusi. Contoh reaksi Diels-Alder adalah sebagai berikut:
Gambar 1. Reaksi Diels-Alder secara umum Sumber: Organic Chemistry, Solomon.
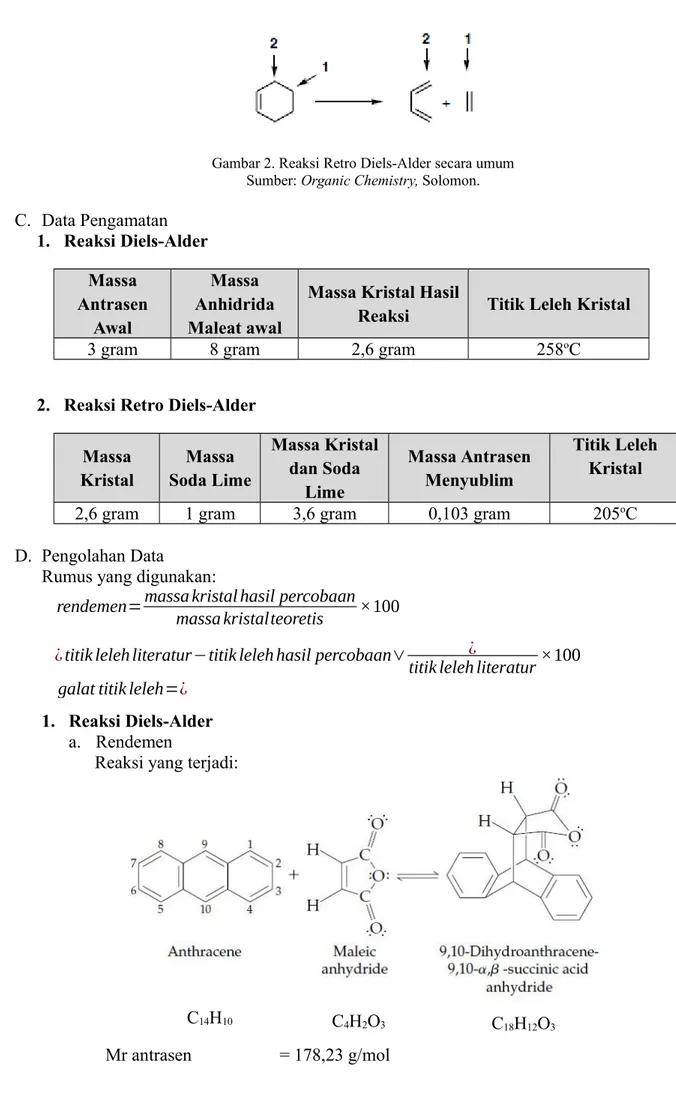
Reaksi retro Diels-Alder biasanya membutuhkan temperatur tinggi untuk melewati energi aktivasi dari cycloreversion. Dalam sintesis organik, reaksi retro Diels-Alder digunakan untuk melapisi fraksi diena atau untuk melindungi ikatan rangkap. Reaksi ini akan terjadi semakin cepat ketika ada suatu anion oksida yang menempati posisi 1 dan 2 pada cincin segienam. Cincin ini harus mengalami cycloreverse pada salah satu ujung dari diena awal atau pada satu karbon sp2 dari dienofil.
Gambar 2. Reaksi Retro Diels-Alder secara umum Sumber: Organic Chemistry, Solomon.
C. Data Pengamatan 1. Reaksi Diels-Alder Massa Antrasen Awal Massa Anhidrida Maleat awal
Massa Kristal Hasil
Reaksi Titik Leleh Kristal
3 gram 8 gram 2,6 gram 258oC
2. Reaksi Retro Diels-Alder
Massa Kristal Massa Soda Lime Massa Kristal dan Soda Lime Massa Antrasen Menyublim Titik Leleh Kristal
2,6 gram 1 gram 3,6 gram 0,103 gram 205oC
D. Pengolahan Data
Rumus yang digunakan:
rendemen=massa kristal hasil percobaan
massa kristalteoretis ×100
¿titik leleh literatur−titik leleh hasil percobaan∨ ¿
titik leleh literatur×100 galat titik leleh=¿
1. Reaksi Diels-Alder a. Rendemen
Reaksi yang terjadi:
Mr antrasen = 178,23 g/mol
C18H12O3
C4H2O3
Mr anhidrida maleat = 98,06 g/mol Mr C18H12O3 (adduct) = 276,29 g/mol
Mol antrasen awal = 3/178,23 = 0,0168 mol Mol anhidrida maleat = 8/98,06 = 0,0816 mol Antrasen adalah pereaksi pembatas.
Reaksi C14H10 C4H2O3 C18H12O3
Mula-mula 0,0168 mol 0,0816 mol
-Bereaksi -0,0168 mol -0,0168 mol +0,0168 mol
Setimbang - 0,0648 mol 0,0168 mol
Massa kristal C18H12O3 secara teoretis = 0,0168 x 276,29 = 4,642 gram
rendemen= 2,60
4,642× 100 =56,01 b. Galat titik leleh
Titik leleh C18H12O3 berdasarkan literatur adalah 263oC sehingga galat titik leleh
sebesar:
¿263−258∨ ¿
263×100 =1,90
galat titik leleh=¿
% kemurnian = (100-1,90)% = 98,1%
2. Reaksi Retro Diels-Alder a. Rendemen
Reaksi yang terjadi:
Massa C18H12O3 awal = 2,6 gram
Mol C18H12O3 awal = 2,6/276,29 = 9,4 x 10-3 mol
Reaksi C18H12O3 C14H10 + C4H2O3
Mula-mula 9,4 x 10-3 mol -
-Bereaksi -9,4 x 10-3 mol +9,4 x 10-3 mol +9,4 x 10-3 mol
C4H2O3
C14H10
Setimbang - 9,4 x 10-3 mol 9,4 x 10-3 mol
Massa antrasen secara teoretis = 9,4 x 10-3 x 178,23 = 1,675 gram
rendemen=0,103
1,675× 100 =6,15 b. Galat titik leleh
Titik leleh C4H10 berdasarkan literatur adalah 218oC sehingga galat titik leleh
sebesar:
¿218−205∨ ¿
218×100 =5,96
galat titik leleh=¿
% kemurnian = (100-5,96)% = 94,04% E. Pembahasan
Dalam reaksi Diels-Alder, anhidrida maleat bertindak sebagai dienofil sedangkan antrasen bertindak sebagai diena. Anhidrida maleat adalah dienofil yang baik karena memiliki dua gugus yang kuat menarik elektron dari ikatan rangkapnya. Pada percobaan reaksi Diels-Alder, toluena kering digunakan sebagai pelarut. Antrasen dan anhidrida maleat lebih mudah larut dalam toluena kering daripada produknya yaitu 9,10-dihidroantrasen-9,10-α,β-anhidrida suksinat. Hal ini menyebabkan produk akan mengkristal saat didinginkan sedangkan reaktan yang kemungkinan masih bersisa tidak akan ikut mengkristal. Refluks dilakukan dengan tujuan meningkatkan temperatur karena reaksi antara antrasen dan anhidrida maleat membutuhkan temperatur yang tinggi. Selain itu, refluks juga bertujuan untuk memperbesar laju reaksi. Soda lime yang digunakan dalam percobaan reaksi retro Diels-Alder berfungsi untuk memberikan suasana basa karena reaksi hanya dapat terjadi dalam suasana basa.
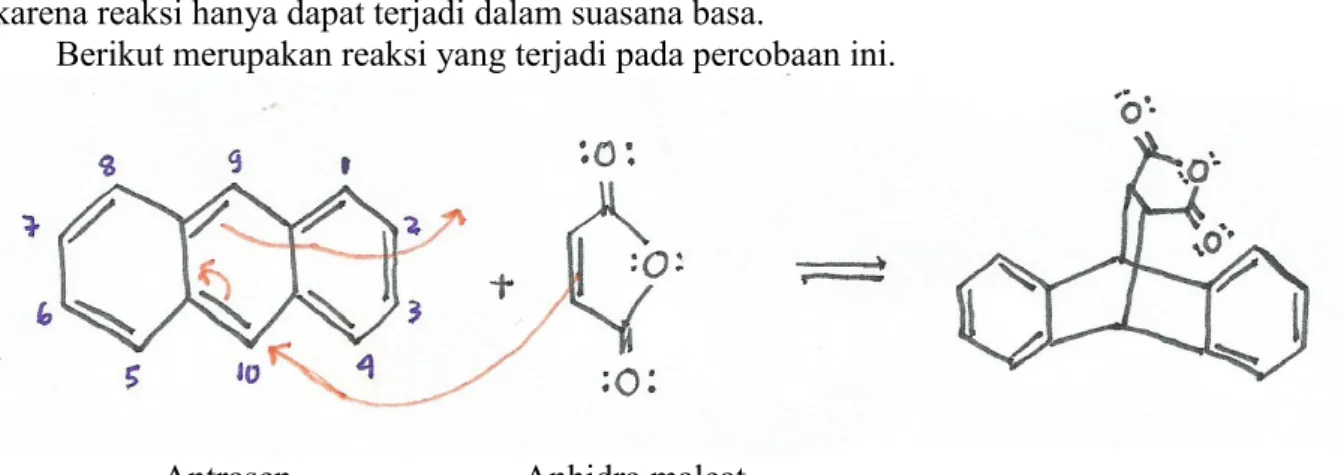
Berikut merupakan reaksi yang terjadi pada percobaan ini.
Antrasen Anhidra maleat
Gambar 3. Reaksi Diels-Alder Antrasen dan Anhidra maleat Sumber: Dokumen pribadi
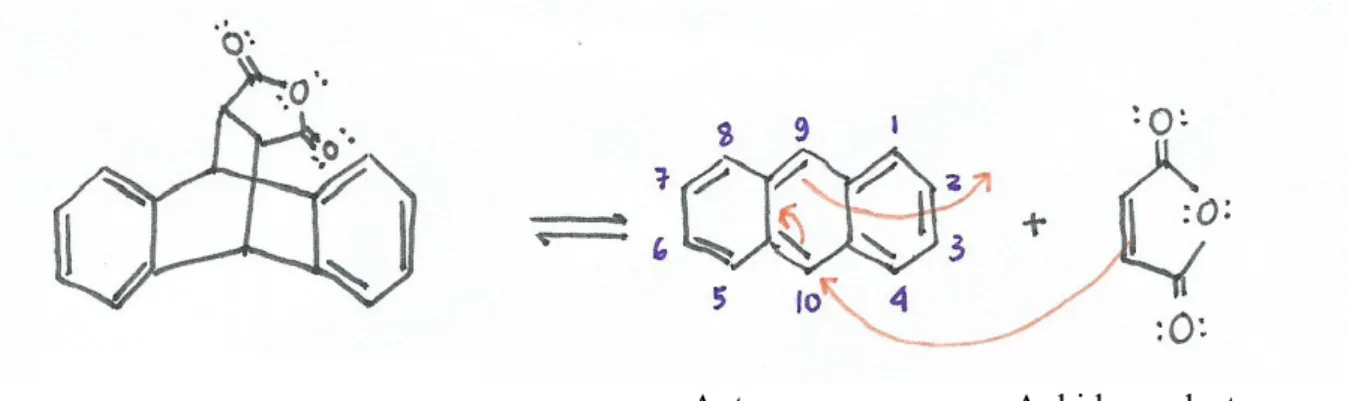
Antrasen Anhidra maleat
Gambar 4. Reaksi Retro Diels-Alder 9,10-dihidroantrasen-9,10-α,β-anhidrida suksinat. (Panah mekanisme pada antrasen dan anhidra maleat menyatakan bahwa reaksi dapat berlangsung
sebaliknya menjadi reaksi Diels-Alder) Sumber: Dokumen pribadi
Berdasarkan hasil perhitungan, diperoleh galat titik leleh yang cukup besar, yakni 5,96% (Asumsi galat dikatakan kecil apabila kurang dari 1%). Adanya galat ini menunjukkan bahwa kristal adduct yang diperoleh tidak murni. Anhidrida maleat yang kemungkinan tersisa dalam produk memiliki titik leleh lebih rendah daripada 9,10-dihidroantrasen-9,10-α,β-asam suksinat anhidrida sehingga titik leleh produk yang terukur menjadi lebih rendah daripada titik leleh 9,10-dihidroantrasen-9,10-α,β-asam suksinat anhidrida yang seharusnya.
F. Kesimpulan
1. Rendemen senyawa hasil reaksi Diels-Alder sebesar 56,01%, sedangkan hasil retro Diels-Alder sebesar 6,15%.
2. Titik leleh senyawa hasil:
a. Diels-Alder Tl= 258oC dengan galat sebesar 1,90%
Dengan demikian, % kemurnian = 98,1%
b. Retro Diels-Alder Tl = 205oC dengan galat sebesar 5,96%
Dengan demikian, % kemurnian = 94,04%
G. Daftar Pustaka
Fringuelli, Francesco & Taticchi, Aldo. 2002. The Diels-Alder Reaction: Selected
Practical Methods. New York: John Wiley & Sons. Halaman 15-18.
Solomon & Frykle. 2004. Organic Chemistry (8th ed.). Singapore: John Wiley & Sons. Halaman 608-609.
Wade, L. D. 1998. The Diels-Alder Reaction of Anthracene with Maleic Anhydride. Palmyra: H.A. Neidig. Halaman 155-157.
Percobaan 10 KONDENSASI SENYAWA KARBONIL: Sintesis Dibenzalaseton
A. Tujuan Percobaan
1. Menentukan rendemen kristal hasil sintesis.
2. Menentukan nilai Rf produk hasil sintesis dengan uji KLT. 3. Menentukan titik leleh produk hasil sintesis.
B. Prinsip Percobaan
Reaksi aldol (kondensasi aldol) adalah satu dari reaksi-reaksi dasar dalam kimia organik. Reaksi kondensasi adalah reaksi yang melibatkan penggabungan dua molekul bersamaan dengan putusnya molekul kecil yang stabil seperti air dan alkohol. Reaksi aldol dapat dimanfaatkan untuk mengkondensasi berbagai kombinasi dari aldehid dan keton.
Salah satu dari variasi reaksi kondensasi aldol adalah sintesis dibenzalaseton. Kondisi dari reaksi kondensasi aldol cenderung mengarah ke pembentukan produk yaitu dibenzalaseton. Dibenzalaseton tidak larut dalam larutan etanol dan dapat membentuk senyawa antara benzalaseton yang larut dengan baik dalam etanol. Kondensasi aldol melibatkan pembentukan enolat dengan menghilangkan proton asam dari karbon ke gugus karbonil pada aldehid atau keton diikuti dengan adisi nukleofilik dari enolat ini ke gugus karbonil pada aldehid atau keton. Reaksi kondensasi aldol biasanya dibantu dengan katalis basa dan melalui beberapa tahapan reaksi mekanistik. Tahap pertama diawali dengan pembentukkan enolat dengan bantuan katalis basa. Selanjutnya terjadi penyerangan dari nukleofil ke anion dari karbon pada gugus karbonil. Kemudian, terjadi protonasi pada anion yang dihasilkan membentuk produk aldol awal yaitu senyawa β-hidroksi karbonil. Tahap akhir adalah dehidrasi produk awal oleh enolatnya dengan bantuan katalis hidroksida. Semua tahapan dalam reaksi ini adalah reaksi bolak balik dan setimbang. Ketika senyawa β-hidroksi karbonil direaksikan dengan suatu basa, reaksi reverse aldol atau retro aldol akan terjadi.
C. Data Pengamatan Massa Produk Sebelum Rekristalisasi Warna Endapan Titik Leleh Sebelum Rekristalisasi Sesudah Rekristalisas i 0,5 gram kuning 125oC 100oC
UV Sebelum Rekristalisasi (A) Sesudah Rekristalisasi (B) Etil asetat/n-heksana (2:8) 2,67 cm 2,70 cm D. Pengolahan Data 1. Rendemen
Reaksi yang terjadi :
C6H5CHO CH3COCH3 C6H5CHCHCOCHCHC6H5
Volume benzaldehid mula-mula = 1 mL Volume aseton mula-mula = 0,37 mL
benzaldehid = 1,04 g/cm3 aseton = 0,791 g/cm3 Mr benzaldehid = 106,121 g/mol Mr aseton = 58,08 g/mol Mr dibenzalaseton = 234,3 g/mol B A
Massabenzaldehid mula−mula= ρ× V =1,04 × 1=1,04 gram
Massa asetonmula−mula= ρ× V =0,791 ×0,37=0,293 gram
Mol benzaldehid mula−mula=massabenzaldehid Mr benzaldehid =
1,04
106,121=9,8 ×10
−3
mol
Mol asetonmula−mula=massa aseton Mr aseton =
0,293
58,08=5,045 ×10
−3
mol
Pereaksi pembatas adalah benzaldehid.
Reaksi 2C6H5CHO + CH3COCH3 C6H5CHCHCOCHCHC6H5
Mula-mula 9,8 x 10-3 mol 5,045 x 10-3 mol
-Bereaksi -9,8 x 10-3 mol -4,9 x 10-3 mol +4,9 x 10-3 mol
Setimbang - 1,45 x 10-4 mol 4,9 x 10-3 mol
Massa kristal dibenzalaseton secarateoretis=(4,9× 10−3
)
×234,3=1,148 gramrendemen=massa kristal hasil percobaan massa kristalteoretis ×100
¿ 0,5 gram
1,148 gram×100 =43,55 2. Galat Titik Leleh
Berdasarkan literatur, titik leleh dibenzalaseton adalah 112oC sehingga galat titik
leleh adalah sebagai berikut. a. Sebelum Rekristalisasi
¿112−125∨ ¿
112×100 =11,61
galat titik leleh=¿
% kemurnian = (100-11,61)% = 88,39%
¿112−100∨ ¿
112×100 =10,71
galat titik leleh=¿
% kemurnian = (100-10,71)% = 89,29% 3. Retardation Factor (Rf)
Jarak tempuh pelarut atau eluen = 4,00 cm
Rf noda yang teramati dapat dihitung sebagai berikut.
a. Sebelum Rekristalisasi
Rf= jarak tempuh noda
jarak tempuh eluen=
2,67 cm
4,00 cm=0,6675 b. Sesudah Rekristalisasi
Rf= jarak tempuh noda
jarak tempuh eluen=
2,70 cm
4,00 cm=0 , 6750
E. Pembahasan
Natrium hidroksida yang digunakan pada percobaan ini berfungsi untuk menyumbangkan ion hidroksida yang akan menjadi katalis basa dalam reaksi pembentukan enolat. Elektron bebas yang dimiliki atom O pada OH- akan menyerang
atom H dari gugus metil pada aseton membentuk H2O. Produk yang terbentuk disebut
enolat. Enolat akan bereaksi dengan benzaldehid kemudian terjadi protonasi menghasilkan produk aldol awal yaitu senyawa β-hidroksi karbonil. Senyawa ini akan mengalami dehidrasi sehingga terbentuk dibenzalaseton. Etanol dalam percobaan ini bertindak sebagai pelarut. Aseton, benzaldehid, dan dibenzalaseton dapat larut dalam etanol panas. Ketika etanol dingin, aseton dan benzaldehid masih dapat larut namun dibenzalaseton sukar larut sehingga dibenzalaseton akan mengkristal ketika campuran didinginkan.
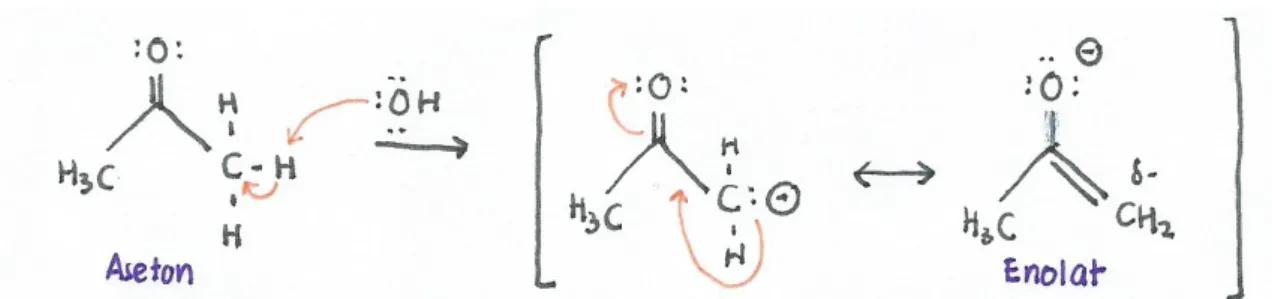
Berikut merupakan reaksi yang terjadi pada percobaan ini. (1)
Sumber: Dokumen pribadi
(2)
Gambar 6. Reaksi Aldol (2) – Sintesis dibenzalaseton Sumber: Dokumen pribadi
Jika dilihat dari struktur dibenzalaseton, senyawa ini bersifat non-polar karena bentuknya yang simetris. Eluen etil asetat/n-heksana (2:8) memiliki sifat non-polar yang
lebih dominan sehingga dibenzalaseton akan terbawa naik paling jauh ketika dilakukan kromatografi lapis tipis. Berdasarkan literatur, nilai Rf dibenzalaseton ketika
menggunakan eluen etil asetat/n-heksana (2:8) adalah berkisar 0,5. Nilai Rf yang
diperoleh dari percobaan adalah 0,6675 (sebelum rekristalisasi) dan 0,675 (setelah rekristalisasi). Hal ini menunjukkan bahwa kristal dibenzalaseton yang diperoleh tidak murni.
Berdasarkan literatur, titik leleh dibenzalaseton adalah 112oC. Dari hasil percobaan,
didapat titik leleh dibenzalaseton adalah 125oC (sebelum rekristalisasi) dan 100oC
(setelah rekristalisasi sehingga galat titik leleh yang diperoleh adalah 11,61% (sebelum rekristalisasi) dan 10,71% (setelah rekristalisai). Seperti sebelumnya, galat yang dapat diabaikan apabila kurang dari 1%. Dengan demikian, galat yang jauh di atas 1% ini menunjukkan bahwa masih ada pengotor dalam produk yang didapat sehingga titik leleh yang didapat tidak sesuai dengan literatur.
F. Kesimpulan
1. Persentase rendemen yang didapat yakni sebesar 43,55%. 2. Nilai Rf produk hasil percobaan didapat sebagai berikut.
a. Sebelum rekristalisasi, Rf = 0,6675 b. Setelah rekristalisasi, Rf = 0,6750
3. Titik leleh produk yang didapat beserta galat nya sebagai berikut.
a. Sebelum rekristalisasi, Tl = 125oC dengan galat sebesar 11,61%
Dengan demikian, % kemurnian = 88,39%
b. Setelah rekristalisasi, Tl = 100oC dengan galat sebesar 10,71%
Dengan demikian, % kemurnian = 89,29% G. Daftar Pustaka
Mayo, Dana W., et al. 2011. Microscale Organic Laboratory with Multistep and
Multiscale Syntheses (5th ed.). Hoboken: John Wiley & Sons. Halaman 309-311.
Verma, N. K., et al. 2012. Comprehensive Practical Chemistry. New Delhi: Laxmi Publications. Halaman 72.
Williamson, Kenneth L. & Masters, Katherine M. 2011. Macroscale and Microscale