BAB III
METODOLOGI PENELITIAN
3.1 LOKASI DAN WAKTU PENELITIAN
Penelitian ini dilakukan di Laboratorium Penelitian, Fakultas Teknik, Departemen Teknik Kimia, Universitas Sumatera Utara, Laboratorium Kimia Fisika Fakultas Matematika dan Ilmu Pengetahuan Alam, Departemen Kimia, Universitas Sumatera Utara dan Laboratorium Penelitian, Fakultas Farmasi, Universitas Sumatera Utara. Penelitian ini dilakukan kurang lebih selama 6 bulan.
3.2 ALAT DAN BAHAN 3.2.1 Alat
A.Alat Pembuatan Selulosa Nanokristal
Adapun alat yang digunakan untuk pembuatan selulosa nanokristal adalah sebagai berikut:
1. Hot plate 2. Sentrifugator 3. Ultrasonic bath 4. Membran dialisis
B.Alat Pembuatan Biokomposit
Adapun alat yang digunakan untuk pembuatan biokomposit adalah sebagai berikut:
1. Cetakan biokomposit 2. Hot plate
3.2.2 Bahan
A.Bahan yang digunakan dalam Pembuatan Selulosa Nanokristal Adapun bahan yang digunakan dalam pembuatan selulosa nanokristal antara lain berasal dari pengrajin kulit Kulit Rotan dan Toko Kimia Rudang Jaya, Medan:
1. Kulit Rotan. 2. Aquadest (H2O). 3. Asam Nitrat (HNO3).
4. Natrium Hidroksida (NaOH). 5. Natrium Hipoklorit (NaOCl). 6. Hidrogen Peroksida (H2O2). 7. Natrium Nitrit (NaNO2). 8. Natrium Sulfit (Na2SO3). 9. Asam Sulfat (H2SO4).
B.Bahan yang digunakan dalam Pembuatan Biokomposit
Adapun bahan yang digunakan dalam pembuatan biokomposit antara lain berasal dari Toko Kimia Rudang Jaya, Medan:
1. Pati Sagu. 2. Air.
3. Selulosa nanokristal. 4. Gliserol (C3H8O3). 5. Aquadest (H2O). 6. Asam Asetat (C6H8O7).
3.3 PROSEDUR PENELITIAN
3.3.1 Prosedur Pembuatan Selulosa Nanokristal Prosedur pembuatan selulosa nanokristal meliputi: A. Prosedur Preparasi Serat Kulit Rotan
3. Digunting hingga diperoleh ukuran kulit rotan yang lebih kecil. 4. Diblender dan diayak hingga ukuran 50 mesh.
B. Prosedur Ekstraksi α-Selulosa dari Kulit Rotan
Adapun prosedur ekstraksi α-selulosa dari kulit rotan adalah sebagai berikut [32]:
1. 75 gram serat dimasukkan ke dalam beaker glass, kemudian ditambah 1 L campuran HNO3 3,5% dan 10 mg NaNO2, dipanaskan diatas hotplate pada suhu 90 oC selama 2 jam.
2. Disaring dan ampas dicuci hingga filtrat netral.
3. 750 ml larutan yang megandung NaOH 2% dan Na2SO3 2% pada dimasak di atas hot plate suhu 50 oC selama 1 jam.
4. Disaring dan ampas dicuci hingga filtrat netral.
5. Dilakukan pemutihan dengan 250 ml larutan NaOCl 1,75% dengan panasan menggunakan hot plate pada temperatur mendidih selama 30 menit.
6. Disaring dan ampas dicuci hingga filtrat netral.
7. Dilakukan pemurnian α-selulosa dari sampel dengan 500 ml larutan NaOH 17,5% dengan pemanasan menggunakan hot plate pada suhu 80 oC selama 30 menit.
8. Disaring dan ampas dicuci hingga filtrat netral.
9. Dilakukan pemutihan dengan H2O2 10 % dengan pemanasan menggunakan hot plate pada suhu 60 oC dalam oven selama 1 jam. 10. Disaring dan ampas dicuci hingga filtrat netral.
C. Prosedur Isolasi Selulosa Nanokristal dari α–Selulosa
Adapun prosedur isolasi selulosa nanokristal dari α –selulosa adalah sebagai berikut [32]:
1. Sebanyak 1 gram α-Selulosa dilarutkan dalam 25 ml H2SO4 45% pada suhu 45 oC selama 45 menit.
4. Suspensi disentrifugasi dengan kecepatan 10000 rpm selama 25 menit hingga pH netral.
5. Diultrasonifikasi selama 10 menit.
6. Dimasukkan ke dalam membran dialisis dan rendam dalam 100 ml aquadest, diamkan selama 4 hari sambil distrirer.
7. Aquadest diuapkan pada suhu 70 oC untuk mendapatkan nanokristal selulosa.
3.4PROSEDUR PEMBUATAN BIOKOMPOSIT
3.4.1 Prosedur Pembuatan Biokomposit dari Pati Sagu
Adapun prosedur pembuatan biokomposit adalah sebagai berikut [4,43]:
1. Sejumlah massa pati dan NCC yang diinginkan ditimbang dengan perbandingan pengisi 1%, 2%, 3% dan 4% sebanyak 10 gram dari total berat kering pati-NCC.
2. Selulosa nanokristal dimasukkan ke dalam beaker glass dan ditambahkan aquadest sebanyak 100 ml.
3. Kemudian laurutan NCC dan aquadest didispersikan dengan menggunakan stirrer dengan kecepatan 1000 rpm selama 15 menit. 4. Setelah 15 menit ditambahkan pati sebanyak 10 gram kedalam
larutan NCC dan aquadest yang telah terdispersi.
5. Hot plate dipanaskan dan diatur temperatur yang akan digunakan. 6. Ditambahkan gliserol 30% dan asam asetat 10%, 20%, 30%, 40%
pada larutan pati-NCC, lalu diaduk sampai homogen. 7. Setelah homogen, hot plate dan stirrer dimatikan.
8. Beaker glass berisi larutan dikeluarkan dari hot plate, kemudian didinginkan sebelum dicetak.
9. Larutan dituangkan sebanyak 50 ml ke dalam cetakan, kemudian dikeringkan dalam oven pada T = 60 oC selama 24 jam.
11.Kemudian biokomposit dilepas dari cetakannya. Biokomposit siap untuk dianalisis.
3.5 FLOWCHART PERCOBAAN
3.5.1 Flowchart Pembuatan Selulosa Nanokristal A. Flowchart Preparasi Serat Kulit Rotan
Adapun Flowchart Preparasi Serat Kulit Rotan dapat dilihat pada Gambar 3.1 dibawah ini [32]:
Gambar 3.1 Flowchart Preparasi Serat Kulit Rotan Mulai
Kulit rotan dicuci dengan air
Dijemur di bawah sinar matahari hingga kering
Digunting hingga ukuran lebih kecil
Selesai
B. Flowchart Ekstraksi α-Selulosa dari Serat Kulit Rotan
Adapun Flowchart Ekstraksi α-Selulosa dari Serat Kulit Rotan dapat dilihat pada Gambar 3.2 dibawah ini [32]:
Mulai
Disaring dan serat dicuci hingga filtrat netral
75 gram serat dimasukkan kedalam beaker glass, kemudian ditambah 1 l campuran HNO3 3,5% dan 10 mg NaNO2, dipanaskan diatas hotplate pada suhu 90 oC selama 2 jam
Dimasak dengan 750 ml larutan yang megandung NaOH 2% dan Na2SO3 2% pada suhu 50 oC selama 1 jam
Dilakukan pemutihan dengan 250 ml larutan NaOCl 1,75% dan air (1:1) pada temperatur mendidih selama 0,5 jam
Serat disaring dan dicuci hingga filtrat netral
A
Disaring dan serat dicuci hingga filtrat netral
Dilakukan pemurnian alfa selulosa dari sampel dengan 500 ml larutan NaOH 17,5% pada suhu 80 oC selama 0,5 jam
Gambar 3.2 Flowchart Ekstraksi α-Selulosa dari Kulit Rotan
C. Flowchart Isolasi Selulosa Nanokristal dari α–Selulosa
Adapun Flowchart Isolasi Selulosa nanokristal dari α –Selulosa dapat dilihat pada Gambar 3.3 dibawah ini [32]:
Disimpan dalam desikator
Serat dicuci dan disaring sampai filrat netral
Selesai A
Dilakukan pemutihan dengan H2O2 10 % pada suhu 60 oC dalam oven selama 1 jam
Dibiarkan satu malam hingga terbentuk suspensi dan disentrifugasi dengan kecepatan 10000 rpm selama 25 menit hingga pH netral
Sebanyak 1 gram alfa selulosa dilarutkan ke dalam 25 ml H2SO4 45% pada suhu 45 oC selama 45 menit
Didinginkan dan ditambahkan 25 ml aquadest
Diultrasonifikasi selama 10 menit dan dimasukkan ke dalam membran dialisis
Direndam dalam 100 ml aquabidest, diamkan selama 4 hari sambil distrirer menit hingga pH netral
Gambar 3.3 Flowchart Isolasi Selulosa nanokristal dari α-Selulosa
3.5.2Flowchart Pembuatan Biokomposit
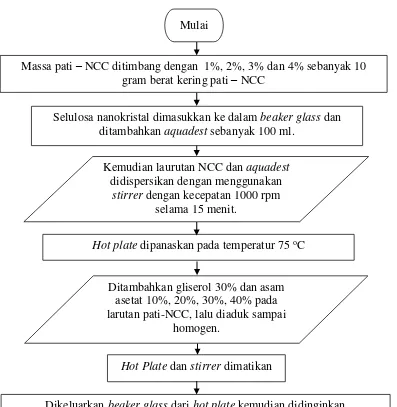
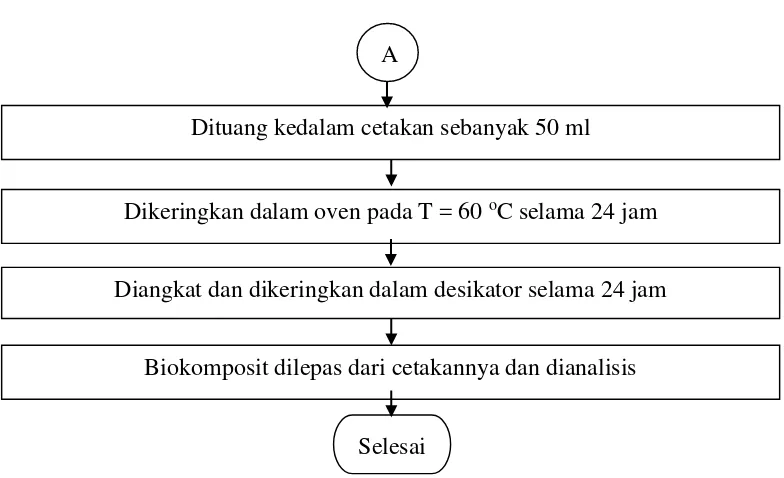
Adapun Flowchart Pembuatan Biokomposit dapat dilihat pada Gambar 3.4 dibawah ini [4,43]:
Aquabidest diuapkan pada suhu 70 oC dan didapat nanokristal selulosa
Selesai A
Hot Plate dan stirrer dimatikan Mulai
Selulosa nanokristal dimasukkan ke dalam beaker glass dan ditambahkan aquadest sebanyak 100 ml.
Hot plate dipanaskan pada temperatur 75 oC
Dikeluarkan beaker glass dari hot plate kemudian didinginkan Kemudian laurutan NCC dan aquadest
didispersikan dengan menggunakan stirrer dengan kecepatan 1000 rpm
selama 15 menit.
Massa pati – NCC ditimbang dengan 1%, 2%, 3% dan 4% sebanyak 10 gram berat kering pati – NCC
Ditambahkan gliserol 30% dan asam asetat 10%, 20%, 30%, 40% pada larutan pati-NCC, lalu diaduk sampai
Gambar 3.4 Flowchart Pembuatan Biokomposit Dari Pati Sagu
3.6 ANALISIS BIOKOMPOSIT DAN SELULOSA NANOKRISTAL 3.6.1 Analisis TEM (Transmission Electron Microscopy)
Sampel yang akan dianalisis dengan TEM (Transmission Electron Microscopy) yaitu berupa:
1. Selulosa nanokristal (NCC)
Tujuan dilakukan analisis ini adalah untuk menentukan ukuran partikel dan melihat morfologi selulosa nanokristal [38]. Analisis TEM (Transmission Electron Microscope) dilakukan di Laboratorium Terpadu, Universitas Gajah Mada, Yogyakarta.
3.6.2 Analisis SEM (Scanning Electron Microscopy)
Sampel yang akan dianalisis dengan SEM (Scanning Electron Microscopy) yaitu berupa:
1. Selulosa nanokristal.
2. Biokomposit dengan penambahan pengisi NCC.
Tujuan dilakukan analisis ini adalah untuk melihat morfologi selulosa nanokristal, morfologi penyebaran dengan penambahan pengisi NCC dan plasticizer gliserol dalam matriks pati sagu [38]. Analisis SEM (Scanning Electron Microscope)
Selesai
Dituang kedalam cetakan sebanyak 50 ml
Dikeringkan dalam oven pada T = 60 oC selama 24 jam
Diangkat dan dikeringkan dalam desikator selama 24 jam
dilakukan di Laboratorium Fisika, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Negeri Medan.
3.6.3 Analisis XRD (X-Ray Diffraction)
Sampel yang akan dianalisis dengan XRD (X-Ray Diffracion) yaitu pengisi selulosa nanokristal. Tujuan dilakukan analisis ini adalah untuk mengukur kristalinitas selulosa nanokristal yang dihasilkan. Analisis XRD (X-Ray Diffraction) dilakukan di Laboratorium Fisika, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Negeri Medan. Rumus perhitungan indeks kristalinitas dari sampel adalah sebagai berikut [51]:
CrI= [I002I-IAM
002 ] x100 (3.1) Keterangan:
Crl = Derajat relatif kristalinitas
I002 = Intensitas maksimum dari difraksi pola 0 0 2
IAM = Intensitas dari difraksi dalam unit yang sama pada 12-18o
3.6.4 Analisis FTIR (Fourier Transform Infra-Red)
Sampel yang akan dianalisis dengan FTIR (Fourier Transform Infra-Red) yaitu berupa:
1. Selulosa nanokristal.
2. Biokomposit dengan penambahan pengisi NCC.
Tujuan dilakukan analisis ini adalah untuk melihat apakah ada atau tidak terbentuknya gugus baru dalam produk biokomposit dengan pengisi NCC dan plasticizer gliserol [39]. Analisis FTIR (Fourier Transform Infra-Red) dilakukan di Laboratorium Penelitian Fakultas Farmasi Universitas Sumatera Utara, Medan.
3.6.5 Uji Densitas Dengan Standar ASTM D792-91, 1991
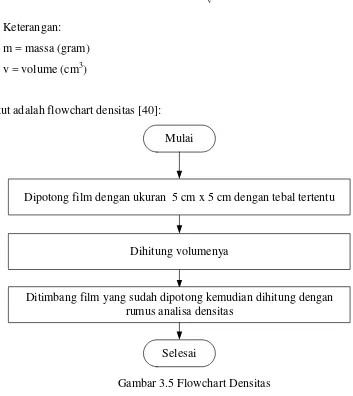
Adapun prosedur analisis densitas adalah sebagai berikut [40]:
1. Film dipotong dengan ukuran 5 cm x 5 cm dan tebal tertentu, kemudian dihitung volumenya.
Rapat massa (densitas) dari film dapat ditentukan dengan rumus [67]:
densitas (ρ)
=
mv (3.2) Keterangan:m = massa (gram) v = volume (cm3)
Berikut adalah flowchart densitas [40]: Mulai
Dipotong film dengan ukuran 5 cm x 5 cm dengan tebal tertentu
Dihitung volumenya
Ditimbang film yang sudah dipotong kemudian dihitung dengan rumus analisa densitas
Selesai
Gambar 3.5 Flowchart Densitas
3.6.6 Uji Kekuatan Tarik (Tensile Strength) Dengan Standar ASTM D 638 Kekuatan tarik adalah salah satu sifat dasar dari bahan produk biokomposit yang terpenting dan sering digunakan untuk karakteristik suatu bahan produk biokomposit. Kekuatan tarik suatu bahan didefenisikan sebagai besarnya beban maksimum (F maks) yang digunakan untuk memutuskan spesimennya bahan dibagi dengan luas penampang awal (Ao).
kemudian dijepit kuat dengan penjepit yang ada dialat. Mesin dihidupkan dan spesimen akan tertarik ke atas spesimen diamati sampai putus, dicatat tegangan maksimum dan regangannya [41]. Adapun rumusnya adalah sebagai berikut :
Fmaks = Gaya tarik yang diberikan kepada penampang spesimen (N) Ao = Luas penampang mula-mula spesimen sebelum diberikan
pembebanan (m2)
3.6.7 Prosedur Analisis Sifat Pemanjangan pada Saat Putus (Elongation at Break )
Elongasi adalah peningkatan panjang material saat diuji dengan beban tarik, dinyatakan dalam satuan panjang, biasanya inci atau millimeter. Persen elongasi adalah pemanjangan benda uji yang dinyatakan sebagai persen dari panjangnya. Percent elongation at break adalah persen pemanjangan pada saat putusnya benda uji Pengukuran dilakukan dengan cara yang sama dengan kekuatan tarik yaitu dilakukan berdasarkan ASTM D882 dengan ketentuan model Universal Testing Machine (UTM) [41]. Adapun rumusnya adalah sebagai berikut:
Elongasi(%) = ∆l
l0 × 100% (3.4) Keterangan :
∆l = Perubahan panjang (cm) l0 = Panjang awal (cm)
3.6.8 Uji Penyerapan Air Dengan Standar ASTM D570-98, 2005
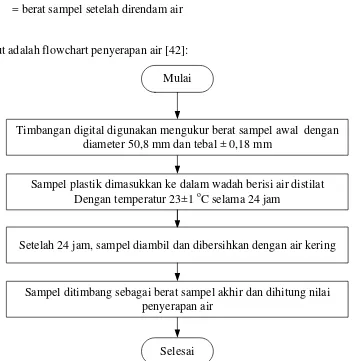
Adapun prosedur analisis penyerapan air adalah sebagai berikut [42]:
1. Dipotong biokomposit dengan diameter 50,8 mm dan tebal ± 0,18 mm dan ditimbang berat sampel.
Setelah 24 jam, sampel diambil dan dibersihkan dengan menggunakan kain kering. Rumus perhitungan penyerapan air dari sampel adalah sebagai berikut [67]:
Penyerapan Air (%) = W-Wo
Wo x 100 % (3.5) Keterangan:
Wo = berat sampel kering
W = berat sampel setelah direndam air
Berikut adalah flowchart penyerapan air [42]: Mulai
Timbangan digital digunakan mengukur berat sampel awal dengan diameter 50,8 mm dan tebal ± 0,18 mm
Sampel plastik dimasukkan ke dalam wadah berisi air distilat
Dengan temperatur 23±1 oC selama 24 jam
Setelah 24 jam, sampel diambil dan dibersihkan dengan air kering
Selesai
Sampel ditimbang sebagai berat sampel akhir dan dihitung nilai penyerapan air
BAB IV
HASIL DAN PEMBAHASAN
4.1 ANALISIS SELULOSA NANOKRISTAL (NCC)
4.1.1 Analisis Transmission Electron Microscope (TEM) Selulosa Nanokristal (NCC)
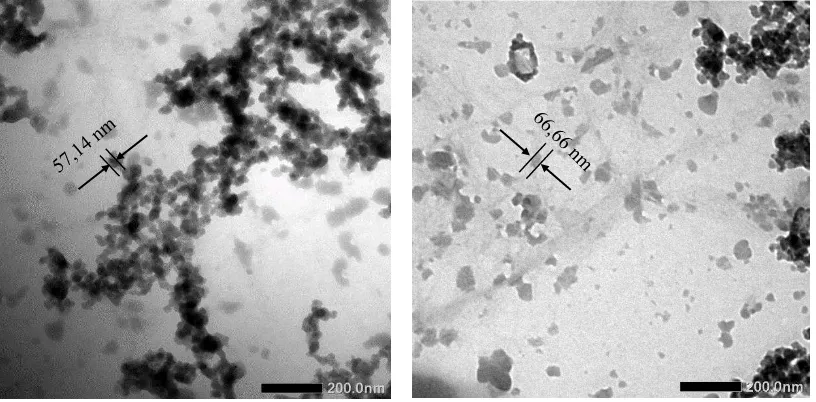
Transmission Electron Microscopy (TEM) merupakan teknik analisis yang digunakan untuk mengetahui morfologi serta ukuran partikel dari suatu molekul. Pada penelitian ini, analisis TEM digunakan untuk mengamati dan mengukur diameter dari selulosa nanokristal (NCC) yang diisolasi dari kulit rotan. Hasil karakterisasi Transmission Electron Microscope (TEM) dari selulosa nanokristal (NCC) kulit rotan yang diperoleh dengan metode hidrolisis asam sulfat dan proses ultrasonikasi dapat dilihat pada Gambar 4.1 berikut:
Gambar 4.1 Analisis Karakterisasi Transmission Electron Microscope (TEM) dari Selulosa Nanokristal (NCC) Kulit Rotan
Gambar di atas menunjukkan selulosa nanokristal (NCC) yang dihasilkan berbentuk bulat, saling bertumpuk satu sama lain dengan ukuran rata-rata 10 – 100 nanometer.
[44]. Oleh karena itu, beberapa proses diperlukan dalam penghilangan hemiselulosa dan lignin untuk memperoleh selulosa nanokristal (NCC).
Delignifikasi merupakan tahap pertama yang dilakukan untuk menghilangkan kandungan lignin dan hemiselulosa yang terdapat pada selulosa dengan menambahkan bahan alkali seperti natrium hidroksida (NaOH) 2% [58]. Pada penelitian ini dilakukan proses pemutihan sebanyak dua tahap. Natrium hipoklorit (NaOCl) 1,75% digunakan pada tahap pemutihan pertama. Selulosa yang dihasilkan pada tahap ini berwarna kuning pucat. Hal ini mengindikasikan bahwa lignin dan hemiselulosa masih terdapat di didalam sampel selulosa.
Setelah pemutihan pertama selesai, selulosa dilanjutkan ke proses alkalisasi menggunakan larutan natrium hidroksida (NaOH) 17,5%. Proses ini bertujuan untuk menghilangkan lignin dan hemiselulosa yang masih terperangkap di dalam selulosa sehingga dihasilkan produk berupa alfa selulosa. Alfa selulosa merupakan selulosa yang memiliki kandungan hemiselulosa dan lignin yang rendah [28].
Selanjutnya dilakukan tahap pemutihan yang kedua menggunakan larutan hidrogen peroksida (H2O2) 10%. Pada tahap ini dihasilkan selulosa berwarna putih yang mengindikasikan pengurangan kandungan lignin yang terdapat pada sampel alfa selulosa sudah berkurang dan siap untuk dilanjutkan dengan proses hidrolisis.
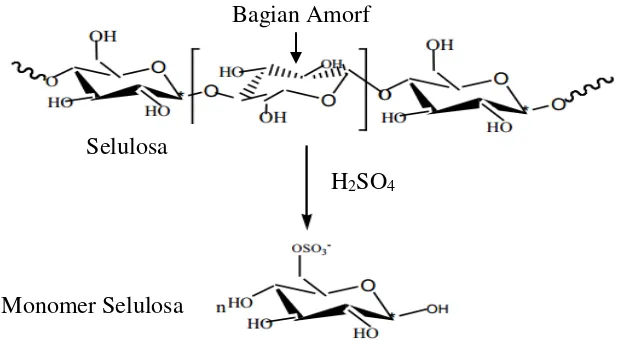
Proses selanjutnya adalah proses hidrolisis menggunakan asam sulfat (H2SO4) 45% yang digunakan untuk menghidrolisis bagian amorf pada serat selulosa sehingga serat terdegradasi menjadi pendek dan menghidrolisis hemiselulosa menjadi xilosa dan gula lain [45]. Reaksi hidrolisis selulosa dengan metode asam sulfat (H2SO4) dapat dilihat pada Gambar 4.2 berikut:
Gambar 4.2 Reaksi Hidrolisis Selulosa dengan Asam Sulfat (H2SO4) Selulosa
Monomer Selulosa
Proses sentrifugasi dilakukan setelah proses hidrolisis selesai. Pada proses sentrifugasi dilakukan penambahan air untuk mencuci sampel selulosa yang bertujuan untuk menetralkan dan mengendapkan selulosa setelah perlakuan hidrolisis. Proses ini berlangsung selama 25 menit dengan kecepatan putaran 10.000 rpm. Setelah proses sentrifugasi selesai, dilakukan proses ultrasonikasi yang bertujuan untuk memperkecil ukuran dan penghilangan kotoran yang masih menempel pada serat selulosa [51]. Tahap terakhir yang dilakukan adalah tahap pemisahan menggunakan membran dialisis yang bertujuan untuk mendapatkan bagian kristal selulosa.
Penghilangan lignin dan hemiselulosa dapat memudahkan proses isolasi nanoserat selulosa. Penghilangan bahan non-selulosa, seperti lignin, diharapkan dapat meningkatkan adhesi antara serat selulosa dan matriks film yang bersifat hidrofilik, seperti pati [46].
Ukuran nanoserat selulosa biasanya dipengaruhi oleh perlakuan isolasi atau ekstraksi nanoserat selulosa yang dilakukan. Serat yang masih mengandung lignin dan hemiselulosa menunjukkan ukuran yang lebih besar, dibandingkan nanoserat selulosa murni. Hemiselulosa juga dapat mencegah terjadinya agregasi nanoserat selulosa [47]. Fragmen kristal nanoserat selulosa dalam kondisi kering cenderung membentuk agregat. Agregat terjadi akibat pembentukan ikatan hidrogen karena adanya gugus hidrogen dan energi permukaan nanoserat selulosa yang tinggi [48].
Semakin kecil ukuran selulosa yang digunakan sebagai partikel pengisi, maka peningkatan kontak permukaan akan semakin besar dan juga daya interaksi/adhesi antara kedua bahan akan semakin besar pula sehingga sifat-sifat mekanik akan semakin bagus [49].
4.1.2 Analisis X-Ray Diffraction (XRD) Selulosa Nanokristal (NCC)
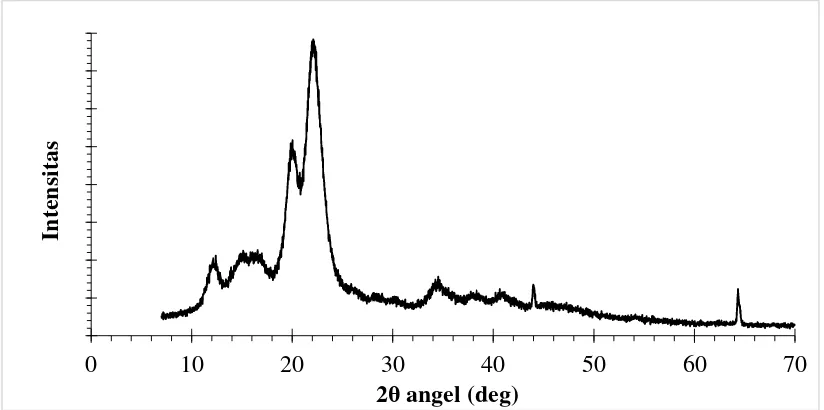
Karakterisasi X-Ray Diffraction (XRD) digunakan untuk menganalisis kristalinitas dari selulosa nanokristal (NCC) kulit rotan yang diperoleh dengan metode hidrolisis asam sulfat dan proses ultrasonikasi. Hasil dari pengujian kristalinitas menggunakan XRD ditunjukan oleh Gambar 4.2 di bawah ini.
Gambar 4.3 Hasil Spektrum XRD Selulosa nanokristal (NCC) dari Kulit Rotan
Dari gambar di atas, dapat diketahui puncak serapan dari spektrum yang dihasilkan oleh sampel selulosa nanokristal adalah pada 2θ = 12o,20o dan 22o. Pada puncak serapan pada 2θ = 12o dan20o menunjukkan struktur selulosa I, sedangkan puncak serapan pada 2θ = 22o mengindikasikan bagian kristal dari selulosa. Dari puncak serapan tersebut dapat ditentukan indeks kristalinitas dari selulosa nanokristal. Penentuan indeks kristalinitas dari bahan selulosa dapat dihitung melalui metode Segal, dengan persamaan di bawah ini [51]:
(4.1)
Persamaan 4.1 digunakan untuk menghitung indeks kristalinitas (crystallinity index), dimana I002 merupakan intensitas maksimum dari difraksi pola 002 yang merupakan representasi dari kedua zona yaitu zona kristal dan zona amorf sedangkan IAM merupakan intensitas dari difraksi dalam unit yang sama pada 2θ=18o yang merupakan representasi dari zona amorf [51, 52].
Dari hasil perhitungan menggunakan Persamaan 4.1 (perhitungan dapat dilihat pada Lampiran B) diperoleh indeks kristalinitas dari selulosa nanokristal (NCC) kulit rotan yaitu sebesar 84,46%, diindikasikan oleh puncak serapan yang tajam (sharp peak) dari spektrum yang dihasilkan pada sampel NCC.
Kristalinitas yang tinggi menunjukkan bahwa susunan rantai polimer dalam bahan tersusun secara teratur atau bagian kristalinnya lebih sempurna [53]. Peningkatan kristalinitas ini disebabkan oleh penurunan komposisi serat yang bersifat amorf akibat perlakuan kimiawi. Perlakuan kimiawi diarahkan untuk menghilangkan hemiselulosa, lignin, pektin, yang merupakan komponen serat yang berkontribusi terhadap bagian amorf serat [54]. Bagian amorf lebih mudah terhidrolisis dibandingkan dengan bagian kristalin, sehingga perlakuan hidrolisis menyebabkan serat menjadi lebih kristalin [55]. Hidrolisis asam pada selulosa diharapkan dapat melarutkan zona amorf pada kondisi yang digunakan dalam penelitian ini. Dimana, ion hidronium akan menembus ke dalam daerah amorf dari selulosa, mengakibatkan pemecahan hidrolitik ikatan glikosida dan pelepasan kristal tunggal [56].
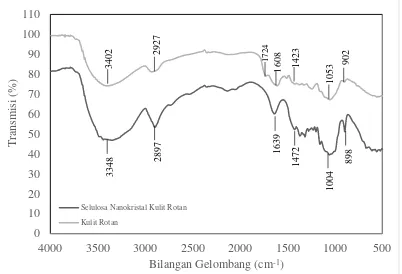
4.1.3 Analisis Fourier Transform InfraRed (FTIR) Selulosa Nanokristal (NCC) Karakterisasi Fourier Transform Infra Red (FTIR) selulosa nanokristal (NCC) kulit rotan yang diperoleh dengan metode hidrolisis asam sulfat dan proses ultrasonikasi dilakukan untuk mengidentifikasi gugus fungsi yang ada pada pengisi selulosa nanokristal (NCC) dan dibandingkan dengan kulit rotan sebagai bahan baku selulosa nanokristal (NCC). Karakterisasi FTIR dan daerah absorbansi gugus fungsi dari bahan pengisi selulosa nanokristal (NCC) dan kulit rotan dapat dilihat pada Gambar 4.4 dan Tabel 4.1 di bawah ini:
Gambar 4.4 Karakterisasi FT-IR Kulit Rotan dan Selulosa Nanokristal (NCC) Tabel 4.1 Daerah Absorbansi Gugus Fungsi dari Kulit Rotan dan Selulosa
Nanokristal Kulit Rotan
Gugus O-H Stretching 3300-3500 3402 3348
Gambar di atas menunjukkan karakteristik FTIR yang menunjukkan beberapa puncak serapan (peak) kunci yang dapat mengindikasikan suatu gugus sebagai ciri khusus dari sebuah senyawa. Pada hasil uji FTIR dengan sampel kulit rotan puncak serapan yang diperoleh banyak memiliki kesamaan, dikarenakan selulosa nanokristal (NCC) yang diperoleh merupakan hasil perlakuan kimia terhadap kulit rotan sehingga gugus-gugus yang mengindikasikan keberadaan selulosa terdapat pada puncak serapan dengan bilangan gelombang yang hampir sama.
Pada sampel kulit rotan yang digunakan terdapat beberapa puncak serapan yang muncul yaitu 3402, 2927, 1724, 1608, 1423, 1053 dan 902 cm-1. Sedangkan pada sampel selulosa nanokristal (NCC) puncak serapan yang muncul yaitu 3348, 2897, 2133, 1639, 1472, 1004 dan 898 cm-1. Puncak serapan besar pada bilangan gelombang 3402 cm-1 yang terdapat pada sampel kulit rotan dan 3348 cm-1 yang terdapat pada sampel selulosa nanokristal (NCC) mengindikasikan keberadaan dari gugus O-H (3300-3500 cm-1 merujuk pada O-H stretching) [58,51]. Semakin tajamnya puncak serapan gugus O-H ini disebabkan dari gugus asam dan alkohol yang terdapat pada serat selulosa nanokristal (NCC) [59].
Puncak serapan pada bilangan gelombang 2927 cm-1 dan 2897 cm-1 yang terdapat pada sampel kulit rotan dan sampel selulosa nanokristal (NCC) dari kulit rotan mengindikasikan keberadaan dari gugus C-H pada alkana (mendekati 2900 cm-1 merujuk pada C-H stretching). Gugus C-H stretching ini berasal dari gugus metil yang terdapat pada rantai selulosa. Semakin tajamnya puncak serapan gugus C-H stretching ini dipengaruhi oleh transformasi yang berkaitan dengan perubahan ikatan inter dan intramolekul selulosa [60].
Puncak serapan pada bilangan gelombang 1608 cm-1 dan 1639 cm-1 yang terdapat pada sampel kulit rotan dan sampel selulosa nanokristal (NCC) menyatakan keberadaan gugus fungsi O-H bending (1600-1640 cm-1 merujuk pada O-H bending). Semakin tajamnya puncak serapan gugus O-H bending yang terdapat pada selulosa nanokristal (NCC) disebabkan penjerapan (adsorpsi) oleh air, dimana terjadi interaksi yang kuat antara air yang teradsorpsi dengan gugus hidrofilik O-H yang terdapat pada selulosa nanokristal (NCC) [51, 62]. Gugus fungsi O-H bending ini merupakan gugus khas yang hanya dimiliki oleh selulosa dan tidak dimiliki oleh komponen penyusun selulosa lainnya seperti hemiselulosa dan lignin. Dapat dilihat pada Gambar 4.4 puncak serapan terhadap gugus O-H bending ini lebih menonjol pada sampel selulosa nanokristal (NCC) dibandingkan dengan kulit rotan.
Puncak serapan pada bilangan gelombang 1423 cm-1 dan 1472 cm-1 yang terdapat pada sampel kulit rotan dan sampel selulosa nanokristal (NCC) menyatakan keberadaan gugus fungsi C-H assymetric (mendekati 1400 cm-1 merujuk pada C-H assymetric)dimana gugus ini mewakili sifat kristal dari selulosa. Semakin tajamnya puncak serapan gugus C-H assymetric yang terdapat pada selulosa nanokristal (NCC) dapat disimpulkan bahwa puncak ini lebih disebabkan oleh selulosa dibandingkan oleh lignin [63] [51].
Puncak serapan pada bilangan gelombang 1053 cm-1 dan 1004 cm-1 yang terdapat pada sampel kulit rotan dan selulosa nanokristal (NCC) dianggap berasal dari getaran gugus cincin pyronose pada unit selulosa (1035-1170 cm-1 merujuk pada cincin pyronose) dimana puncak serapan ini menandakan pengayaan serat selulosa. Semakin tajamnya puncak serapan gugus C-O yang terdapat pada selulosa nanokristal (NCC) semakin mengindikasikan terdapatnya cincin pyronese yang merupakan gugus khas yang hanya dimiliki oleh unit selulosa dan tidak dimiliki oleh komponen lignin dan hemiselulosa [62].
kelompok fungsional sulfat yang menstabilkan suspensi selulosa nanokristal (NCC). Puncak ini terlihat setelah proses hidrolisis asam berlangsung [65].
4.2 ANALISIS BIOKOMPOSIT
4.2.1 Analisis Scanning Electron Microscope (SEM)
Hasil analisis Scanning Electron Microscopy (SEM) dari pati sagu, bioplastik dan biokomposit ditunjukkan pada Gambar 4.5.
(a) (b)
(c) (d)
Gambar 4.5 Analisis Morfologi Permukaan (a) Pati Sagu (b) Bioplastik (c) Biokomposit Dengan Penambahan Pengisi Selulosa Nanokristal (NCC) 1% dan
Asam Asetat 10% dan (d) Biokomposit Dengan Penambahan Pengisi Selulosa Nanokristal (NCC) 3% dan Asam Asetat 30%
ukuran granula pati. Pati sagu memiliki kandungan amilosa dan amilopektin sebesar 28% dan 72%. Amilosa merupakan struktur amorf sedangkan amilopektin merupakan struktur kristal yang dimiliki oleh pati. Kandungan amilopektin yang tinggi mengindikasikan pati sagu memiliki sifat kristal yang tinggi sehingga menyebabkan granula pati yang terbentuk saling terpisah satu sama lain [25,90].
Pada Gambar 4.5 (b) dapat dilihat morfologi bioplastik dengan penambahan gliserol. Penambahan gliserol sebagai plasticizer menyebabkan penurunan daya tarik inter dan intra molekul pati dan membentuk ikatan hidrogen yang lebih stabil antara plasticizer dan pati sehingga granula pati saling menyatu satu sama lain [91].
Pada hasil analisa SEM biokomposit pati sagu dengan penambahan 1% selulosa nanokristal (NCC) dan 10% asam asetat Gambar 4.5 (c) menunjukkan permukaan matriks yang tidak halus dan rata. Hal ini disebabkan interaksi yang buruk antara pati dan pengisi, dimana pengisi yang ada masih belum cukup untuk memenuhi seluruh ruang matriks dari pati sagu. Sedangkan pada Gambar 4.5 (d) yang merupakan biokomposit dengan penambahan 3% selulosa nanokristal (NCC) dan 30% asam asetat, terlihat permukaan matriks yang lebih halus dan juga terlihat bahwa selulosa nanokristal (NCC) telah terdisribusi secara seragam pada matriks pati sagu yang menunjukkan telah terjadinya interaksi yang baik. Distribusi selulosa nanokristal (NCC) yang seragam dikarenakan pengisi yang ada telah cukup untuk memenuhi ruang-ruang matriks, sehingga meningkatkan interaksi ikatan hidrogen antara selulosa dan pati [63].
4.2.2 Analisis Fourier Transform InfraRed (FTIR) Bioplastik Dan Biokomposit Dengan Pengisi Selulosa Nanokristal (NCC) Dan Co-Plasticizer Asam Asetat
Karakterisasi Fourier Transform Infra Red (FT-IR) pada bioplastik dan biokomposit dengan penambahan asam asetat dan NCC dilakukan untuk mengidentifikasi gugus fungsi yang ada pada masing-masing sampel. Dari analisa gugus fungsi menggunakan FT-IR diperoleh hasil spektrum dalam bentuk grafik yang dapat dilihat pada Gambar 4.6 berikut ini.
Gambar 4.6 Karakterisasi FT-IR Bioplastik dan Biokomposit dengan Asam Asetat dan NCC
Tabel 4.2 Daerah Absorbansi Gugus Fungsi dari Bioplastik dan Biokomposit dengan Asam Asetat dan NCC
Jenis Ikatan Bioplastik (cm-1)
Biokomposit dengan Asam
Asetat dan NCC (cm-1)
Gugus O-H Stretching 3537 3541
Gugus C-O-H 1122 1122
Biokomposit dengan Asam Asetat dan NCC
3537
Dari gambar di atas dapat diketahui bahwa spektrum bioplastik dan biokomposit dengan penambahan asam asetat dan selulosa nanokristal (NCC) tidak menunjukkan perbedaan yang mencolok, hal ini dikarenakan struktur yang hamper mirip antara struktur pati dengan struktur selulosa.
Puncak serapan pada bilangan gelombang 3537 cm-1 dan 3541 cm-1 yang terdapat pada bioplastik dan biokomposit dengan penambahan asam asetat dan selulosa nanokristal (NCC) mengindikasikan keberadaan dari gugus O-H. Peningkatan panjang gelombang atau puncak serapan yang menjadi sedikit lebih tajam pada ikatan O-H disebabkan karena interaksi dari hidrogen ketika komponen pati dan selulosa nanokristal dicampurkan pada proses pembuatan biokomposit, dimana ikatan hidrogen terdiri dari ikatan antara rantai amilosa dengan amilosa, amilosa dengan amilopektin dan amilosa dengan selulosa nanokristal dan amilopektin [67]. Selain gliserol, penggunaan asam asetat sebagai bahan pendamping plasticizer (co-plasticizer) akan membantu pendistribusian butiran pati dan pengisi. Pendistribusian ini dilakukan oleh asam asetat dengan cara merusak struktur pati. Struktur pati yang rusak nantinya akan diserap oleh gliserol, sehingga membuka jalan bagi asam asetat untuk meningkatkan interaksi antara pati dan pengisi [66].
Puncak serapan pada bilangan gelombang 929 cm-1 dan 1122 cm-1 yang terdapat pada biokomposit tanpa penambahan asam asetat dan selulosa nanokristal (NCC) mengindikasikan kehadiran rantai percabangan amilopektin yaitu gugus α-1,6 glikosidik dan rantai linier heliks amilum yang mempunyai gugus α-1,4 glikosidik. Kehadiran asam asetat menyebabkan putusnya rantai percabangan amilopektin yaitu gugus α-1,6 glikosidik (929 cm-1) pada biokomposit dengan penambahan asam asetat dan selulosa nanokristal (NCC) sehingga menyisakan rantai linier heliks amilum yang mempunyai gugus α-1,4 glikosidik (1122 cm-1) [37].
4.2.3 Pengaruh Penambahan Selulosa Nanokristal (NCC) dan Asam Asetat Terhadap Densitas Biokomposit
Gambar 4.7 berikut ini menunjukkan pengaruh penambahan selulosa nanokristal (NCC) dan asam asetat terhadap densitas biokomposit.
Gambar 4.7 Pengaruh Penambahan Selulosa Nanokristal (NCC) dan Asam Asetat Terhadap Densitas Biokomposit
Dari gambar di atas terlihat bahwa penambahan selulosa nanokristal (NCC) dan asam asetat terhadap densitas biokomposit diperoleh nilai densitas tertinggi adalah sebesar 0,26 gram/cm3 yang diperoleh pada penambahan selulosa nanokristal (NCC) 3% dengan penambahan asam asetat 30%. Sedangkan nilai densitas terendah diperoleh pada penambahan selulosa nanokristal (NCC) 1% dengan penambahan asam asetat 10% dengan nilai densitas sebesar 0,08 gram/cm3.
nilai densitas biokomposit mengalami penurunan karena sebaran selulosa nanokristal (NCC) yang tidak merata dan membentuk penggumpalan (agregat) sehingga mengurangi keefektifan penguatannya dalam kerapatan struktur biokomposit [43,71]. Densitas optimum biokomposit ini juga didukung oleh hasil Scanning Electron Microscope (SEM) yang sebelumnya disajikan pada gambar 4.5 dimana hasil Scanning Electron Microscope (SEM) menunjukkan bahwa biokomposit yang dihasilkan memiliki kerapatan yang baik, dan komponen-komponen penyusun biokomposit tersebut terlihat tercampur dengan cukup baik dan merata. Hal ini mendukung kualitas biokomposit yang dihasilkan memiliki kerapatan atau densitas yang cukup tinggi.
Dari Gambar 4.7 tersebut juga dapat dilihat semakin bertambahnya penambahan asam asetat hingga 30% mengakibatkan meningkatnya densitas biokomposit. Pada penambahan asam asetat 30% biokomposit memiliki nilai densitas yang tinggi karena asam asetat dapat merusak struktur pati. Struktur pati yang rusak nantinya akan diserap oleh gliserol, sehingga membuka jalan bagi asam asetat untuk meningkatkan interaksi antara pati dan pengisi yang kemudian akan meningkatkan kerapatan dari biokomposit yang dihasilkan [66,68]. Pada penambahan asam asetat 40% nilai densitas biokomposit mengalami penurunan karena asam asetat akan melonggarkan ikatan antar molekul dalam biokomposit sehingga mengurangi kekakuan struktur biokomposit, sekaligus juga diduga dapat mengurangi rapat massa biokomposit [72]. Ilustrasi ikatan hidrogen yang terbentuk antara asam asetat dan selulosa nanokritsal dapat dilihat pada gambar di bawah ini [69]:
Gambar 4.8 Iustrasi Pembentukan Ikatan Hidrogen Antara Asam Asetat dan Selulosa Nanokristal
Selulosa
Selulosa Asam Asetat
4.2.4 Pengaruh Penambahan Selulosa Nanokristal (NCC) dan Asam Asetat Terhadap Sifat Kekuatan Tarik (Tensile Strength) Biokomposit
Gambar 4.9 berikut ini menunjukkan pengaruh penambahan selulosa nanokristal (NCC) dan asam asetat terhadap sifat kekuatan tarik (tensile strength) biokomposit.
Gambar 4.9 Pengaruh Penambahan Selulosa Nanokristal (NCC) dan Asam Asetat Terhadap Sifat Kekuatan Tarik (Tensile Strength) Biokomposit
Dari gambar di atas terlihat bahwa penambahan selulosa nanokristal (NCC) dan asam asetat terhadap sifat kekuatan tarik biokomposit diperoleh nilai kekuatan tarik tertinggi adalah sebesar 2,84 MPa yang diperoleh pada penambahan selulosa nanokristal (NCC) 3% dengan penambahan asam asetat 30%. Sedangkan nilai kekuatan tarik terendah diperoleh pada penambahan selulosa nanokristal (NCC) 1% dengan penambahan asam asetat 10% dengan nilai kekuatan tarik sebesar 0,19 MPa.
bahwa selulosa nanokristal (NCC) yang digunakan bersifat compatible sebagai pengisi (filler) pada biokomposit berbahan dasar pati. Sifat compatible ini dikarenakan kemiripan kimia antar selulosa dan juga pati yang mengakibatkan terjadinya interaksi yang baik [78,79]. Hal ini juga didukung oleh hasil analisis Scanning Electron Microscope (SEM) pada Gambar 4.5 yang terdapat pada penambahan selulosa nanokristal (NCC) 3% dengan penambahan asam asetat 30% yang menunjukkan bahwa selulosa nanokristal (NCC) telah terdisribusi / terdispersi secara seragam pada matriks pati sagu sehingga menunjukkan telah terjadinya ikatan antarmuka yang baik. Nilai kekuatan tarik juga dipengaruhi oleh kerapatan massa suatu bahan, dimana semakin rapat suatu bahan, maka nilai dari kekuatan tarik akan semakin meningkat. Hal ini sesuai dengan penelitian Bilbao-Sainz, et.al (2016) yang menyatakan bahwa kerapatan suatu bahan akan meningkatkan sifat fisik dan mekaniknya. Penelitian ini menghasilkan sifat fisik berupa densitas yang meningkat dan nilai kekuatan mekanik berupa kekuatan tarik yang meningkat seiring dengan menigkatnya kerapatan masssa yang disebabkan penambahan selulosa nanokristal (NCC).
Namun, terdapat penurunan nilai kekuatan tarik pada penambahan selulosa nanokristal (NCC) 4%. Penurunan nilai kekuatan tarik ini seperti dilaporkan oleh Cho, et.al (2006) dan Roohani, et.al (2008) disebabkan karena selulosa nanokristal (NCC) membentuk penggumpalan (agregat) dalam matriks film. Tegangan (stress) yang disebabkan oleh penggumpalan (agregat) dalam matriks yang tidak dapat terdistribusi secara seragam, sehingga memunculkan perpindahan tegangan (stress) yang kurang seragam [74,75]. Siagian (2016) juga melaporkan bahwa massa pengisi selulosa yang tinggi akan memperlambat interaksi antar molekul bioplastik pati dan menyebabkan perkembangan struktur bioplastik menjadi heterogen dan hasil yang diskontinuitas. Ketidakhomogenan selulosa dengan larutan pati memicu pembentukan agregat [76].
Sifat kuat tarik juga akan menurun apabila distribusi pengisi (filler) berupa selulosa nanokristal (NCC) tidak merata dan pencampuran bahan yang tidak rata maupun tidak padu antara matriks dan pengisi (filler) [43,71].
memperbaiki sifat mekanik dari film pati. Dari hasil penelitian ini diperoleh peningkatan nilai kekuatan tarik seiring dengan penambahan asam asetat hingga 30%. Namun, pada penambahan asam asetat 40%, nilai kekuatan tarik menjadi menurun. Apabila percabangan amilopektin telah habis, maka asam asetat justru akan memutus rantai linier pada amilosa sehingga membentuk rantai amilum yang lebih pendek [37]. Hal inilah yang menyebabkan nilai kekuatan tarik menjadi menurun. Struktur amilosa dan amilopektin yang terdapat pada pati dapat dilihat pada gambar di bawah ini [80]:
Gambar 4.10 Struktur Amilosa dan Amilopektin yang Terdapat pada Pati
Selain dapat merusak rantai molekul pati yang bercabang menjadi struktur yang lebih linier, penambahan asam asetat sebagai bahan pendamping plasticizer (co-plasticizer) akan membantu pendistribusian butiran pati dan pengisi. Pendistribusian ini dilakukan oleh asam asetat dengan cara merusak struktur pati. Struktur pati yang rusak nantinya akan diserap oleh gliserol, sehingga membuka jalan bagi asam asetat untuk meningkatkan interaksi antara pati dan pengisi sehingga meningkatkan kekuatan tarik biokomposit yang dihasilkan seperti yang ditunjukkan pada Gambar 4.8 [66,69]. Peningkatan ikatan hidrogen didalam biokomposit dibuktikan oleh hasil analisis FTIR dimana tedapat puncak serapan pada bilangan gelombang 3537 cm-1 dan 3541 cm-1 yang terdapat pada bioplastik dan biokomposit dengan penambahan asam asetat dan selulosa nanokristal (NCC) yang mengindikasikan keberadaan dari gugus O-H. Interaksi hidrogen menyebabkan peningkatan puncak serapan ketika komponen pati dan selulosa nanokristal dicampurkan pada proses pembuatan biokomposit, dimana ikatan hidrogen terdiri dari ikatan antara rantai amilosa dengan amilosa, amilosa dengan amilopektin dan amilosa dengan selulosa nanokristal dan amilopektin [67].
4.2.5 Pengaruh Penambahan Selulosa Nanokristal (NCC) dan Asam Asetat Terhadap Pemanjangan Saat Putus (Elongation At Break) Biokomposit
Gambar 4.11 berikut ini menunjukkan pengaruh penambahan selulosa nanokristal (NCC) dan asam asetat terhadap pemanjangan saat putus (elongation at break) biokomposit.
Gambar 4.11 Pengaruh Penambahan Selulosa Nanokristal (NCC) dan Asam Asetat Terhadap Sifat Pemanjangan Saat Putus (Elongation at Break)
Biokomposit
Dari gambar di atas terlihat bahwa penambahan selulosa nanokristal (NCC) dan asam asetat terhadap sifat pemanjangan saat putus (elongation at break) biokomposit diperoleh nilai pemanjangan saat putus (elongation at break) tertinggi adalah sebesar 12,47% yang diperoleh pada penambahan selulosa nanokristal (NCC) 1% dengan penambahan asam asetat 20%. Sedangkan nilai pemanjangan saat putus (elongation at break) terendah diperoleh pada penambahan selulosa nanokristal (NCC) 3% dengan penambahan asam asetat 30% dengan nilai pemanjangan saat putus (elongation at break) sebesar 2,70%.
selulosa nanokristal (NCC) dapat meningkatkan sifat kuat tarik pada biokomposit yang dihasilkan, namun disatu sisi dapat menurunkan sifat pemanjangan saat putus (elongation at break) pada biokomposit yang dihasilkan [81]. Namun, terdapat peningkatan sifat pemanjangan saat putus (elongation at Break) pada penambahan selulosa nanokristal (NCC) 4%. Peningkatan sifat pemanjangan saat putus (elongation at break) ini seperti dilaporkan oleh Melissa, et.al (2014) disebabkan ketidakhomogenan selulosa dengan larutan pati yang memicu pembentukan penggumpalan (agregat) yang dapat menurunkan sifat kekuatan tarik (tensile strength) sehingga meningkatkan sifat pemanjangan saat putus (elongation at break) [63].
Interaksi antara selulosa nanokristal (NCC) dan pati mengakibatkan gerakan rantai polimer menjadi lebih terbatas yang menyebabkan kemampuan pemanjangan putus (elongation at break) pada biokomposit yang dihasilkan menjadi berkurang [78,82]. Hal ini berdasarkan penelitian Kaushik, et. al (2010) yang menunjukkan bahwa penambahan serat akan menurunkan persentase pemanjangan putus (elongation at break) pada biokomposit [83]. Pengaruh serat juga dapat menurunkan sifat pemanjangan saat putus (elongation at break), karena serat dapat mengurangi sifat higroskopis pada biokomposit. Air dalam matriks film biasanya berperan sebagai pemplastis. Interaksi antara rantai pati dan serat selulosa dapat mencegah terjadinya interaksi antara rantai pati dan air, sehingga mengurangi sifat higroskopis film berbahan dasar pati [81].
4.2.6 Pengaruh Penambahan Selulosa Nanokristal (NCC) dan Asam Asetat Terhadap Penyerapan Air (Water Uptake) Biokomposit
Gambar di bawah ini menunjukkan pengaruh penambahan selulosa nanokristal (NCC) pada penambahan 10% asam asetat terhadap sifat penyerapan air biokomposit.
Gambar 4.12 Pengaruh Waktu Terhadap Sifat Penyerapan Air Pada Asam Asetat 10%
Dari Gambar 4.12 dapat dilihat bahwa penambahan selulosa nanokristal (NCC) pada asam asetat 10% diperoleh waktu konstan sifat penyerapan air yaitu pada menit ke 140 dengan sifat penyerapan air yang diperoleh berada di antara 15,38% dan 9,37%. Semakin meningkatnya penambahan selulosa nanokristal (NCC) maka sifat penyerapan air (water uptake) biokomposit yang diperoleh akan semakin menurun. Hal ini seperti dilaporkan oleh Zainuddin, et.al (2013) dimana penambahan pengisi (filler) berupa selulosa nanokristal (NCC) dapat menurunkan penyerapan air, hal ini dikarenakan selulosa nanokristal (NCC) membentuk suatu ikatan kuat yang dapat mencegah pembengkakan pati dan juga penyerapan air (water uptake) [84]. Sedangkan pada penambahan selulosa nanokristal (NCC) 4% sifat penyerapan air (water uptake) biokomposit mengalami peningkatan karena selulosa nanokristal (NCC) yang semakin bertumpuk dan masih terdapatnya zona amorf pada selulosa nanokristal (NCC)
sehingga memudahkan air untuk berdifusi ke dalam biokomposit sehingga meningkatkan sifat penyerapan air (water uptake) [85,86].
Selain pengaruh penambahan selulosa nanokristal, penambahan asam asetat sebagai co-plasticizer juga mempengaruhi sifat penyerapan air biokomposit. Gambar berikut ini menunjukkan pengaruh penambahan asam asetat pada penambahan 1% selulosa nanokristal (NCC) terhadap sifat penyerapan air biokomposit.
Gambar 4.13 Pengaruh Waktu Terhadap Sifat Penyerapan Air Pada Selulosa Nanokristal (NCC) 1%
Dari Gambar 4.13 tersebut juga dapat dilihat bahwa setelah menit ke 140, penambahan asam asetat pada selulosa nanokristal (NCC) 1% diperoleh waktu konstan sifat penyerapan air, dengan sifat penyerapan air yang diperoleh berada di antara 27,58% dan 16,66%. Semakin bertambahnya asam asetat hingga 30% mengakibatkan meningkatnya penyerapan air biokomposit. Peningkatan persentase daya serap air ini disebabkan oleh peningkatan konsentrasi pemplastis, hal ini diduga menyebabkan ikatan yang terjadi antara pemlastis dan polimer menjadi rapuh ketika terkena air. Plasticizer larut dalam air, sehingga semakin tinggi konsentrasi plasticizer yang ditambahkan, maka semakin tinggi daya serap air pada biokomposit [87].
Gambar berikut ini menunjukkan pengaruh penambahan selulosa nanokristal (NCC) dan asam asetat pada kondisi konstan, yaitu pada saat menit ke 140.
Gambar 4.14 Pengaruh Penambahan Selulosa Nanokristal (NCC) dan Asam Asetat Terhadap Sifat Penyerapan Air Biokomposit
Dari gambar 4.14 terlihat bahwa penambahan selulosa nanokristal (NCC) dan asam asetat terhadap sifat penyerapan air (water uptake) biokomposit diperoleh nilai penyerapan air (water uptake) tertinggi adalah sebesar 27,58% yang diperoleh pada penambahan selulosa nanokristal (NCC) 1% dengan penambahan asam asetat 30%. Sedangkan nilai penyerapan air (water uptake) terendah diperoleh pada penambahan selulosa nanokristal (NCC) 3% dengan penambahan asam asetat 10% dengan nilai penyerapan air (water uptake) sebesar 9,37%.
BAB V
KESIMPULAN DAN SARAN
5.1 KESIMPULAN
Adapun kesimpulan yang dapat diambil pada penelitian ini adalah sebagai berikut:
1. Hasil analisis Transmission Electron Microscopy (TEM) dan X-Ray Diffraction (XRD) selulosa nanokristal (NCC) yang dihasilkan memiliki bentuk bulat dengan ukuran rata-rata 10–100 nm dan indeks kristalinitas sebesar 84,46%. Proses hidrolisis menggunakan asam sulfat dan ultrasonikasi menghasilkan selulosa nanokristal (NCC) yang terbebas dari lignin dan hemiselulosa, hal ini dibuktikan dengan analisa Fourier Ttransform Infrared (FTIR) yang menghasilkan puncak-puncak serapan yang lebih tajam dan memperlihatkan gugus-gugus khas dari selulosa.
2. Penambahan selulosa nanokristal (NCC) dan asam asetat mampu meningkatkan nilai dari kekuatan fisik dan mekanik biokomposit. Nilai optimum dari uji fisik dan mekanik bikomposit adalah dengan penambahan 3% selulosa nanokristal (NCC) dan 30% asam asetat. Dimana nilai dari uji densitas dan kekuatan tarik (tensile strength) adalah 0,26 gram/cm3 dan 2,84 MPa. Nilai terbaik dari pemanjangan saat putus (elongation at break) adalah 12,47% yang diperoleh pada penambahan 1% selulosa nanokristal (NCC) dan 20% asam asetat. Sedangkan dari uji penyerapan air (water uptake) yang terbaik adalah dengan penambahan selulosa nanokristal (NCC) 3% dan 10% asam asetat, dengan nilai 9,37%.
bioplastik. Hal ini menunjukkan bahwa selulosa nanokristal (NCC) dan asam asetat telah berhasil berikatan dengan gugus pati.
5.2 SARAN
Adapun saran yang dapat diberikan untuk kesempurnaan penelitian ini adalah: 1. Perlunya dilakukan perbandingan pengaruh kekristalan selulosa yang digunakan
sebagai pengisi dari sumber-sumber selulosa yang lain.
![Gambar 3.1 dibawah ini [32]:](https://thumb-ap.123doks.com/thumbv2/123dok/3751693.1487533/5.595.158.479.266.517/gambar-dibawah-ini.webp)