SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Ilmu Farmasi
Oleh: Grace Litad NIM : 068114020
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
ii SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Ilmu Farmasi
Oleh: Grace Litad NIM : 068114020
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
v
Kupersembahkan karya sederhana ini bagi :
Tuhanku Yesus Kristus, Juruselamat dan kekuatanku
Papaku Imat Sakai dan Mamaku Mariana Langidau
Kakakku Rima Yunlita dan Christine Linda, adikku Pissa
vii
berjudul Karakterisasi Ekstrak Etanolik Daun Jati Belanda (Guazuma ulmifolia Lamk.)
Skripsi ini ditulis sebagai salah satu syarat untuk mencapai gelar kesarjanaan pada Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
Terwujudnya penulisan skripsi ini tidak terlepas dari dukungan, bimbingan dan kerja sama dari berbagai pihak. Penulis menyampaikan terima kasih kepada:
1. Ibu Erna Tri Wulandari M.Si., Apt. selaku Dosen Pembimbing, yang telah memberikan bimbingan dan pengarahan yang sangat berguna demi terselesaikannya skripsi ini.
2. Bapak Yohanes Dwiatmaka M.Si., selaku Dosen Penguji yang telah memberikan kritik dan saran kepada penulis.
3. Bapak Dr. C. J. Soegihardjo, Apt. selaku Dosen Penguji yang telah memberikan kritik dan saran kepada penulis.
4. Seluruh staf Laboratorium Farmakognosi Fitokimia, Laboratorium Kimia, Kebun Tanaman Obat Universitas Sanata Dharma Yogyakarta: Mas Wagiran, Mas Sigit, Mas Parlan, Mas Kunto, Mas Bimo dan Mas Andre yang telah menemani dan membantu selama penelitian.
viii diberikan kepada penulis.
7. Teman-teman kost DIFA atas kebersamaan, tanggung jawab dan toleransi selama hidup berdampingan.
8. Teman-teman Fakultas Farmasi Angkatan 2006 kelas A dan kelas Farmasi Klinis Komunitas A (FKK A) atas kenangan indah, kebersamaan, keceriaan yang telah dialami selama masa perkuliahan dan praktikum. Penulis menyadari sepenuhnya bahwa dalam penelitian dan penyusunan skripsi ini banyak memiliki kekurangan. Oleh karena itu, penulis mengharapkan kritik dan saran yang membangun dari segenap pembaca demi penyempurnaan skripsi ini. Akhirnya, penulis berharap semoga skripsi ini dapat menambah pengetahuan dan wawasan bagi pihak yang membutuhkan.
x
Penelitian ini bertujuan untuk mengetahui karakter dari ekstrak etanolik daun jati belanda sebagai bahan baku dalam jamu pelangsing sehingga diperoleh produk yang mempunyai standar kualitas yang seragam dan terulang, serta kontinuitas kualitas produk dari segi SQE (Safety, Quality, Efficacy) dapat terjaga.
Penelitian ini merupakan jenis penelitian non eksperimental, berupa karakterisasi ekstrak yang mengikuti Parameter Standar Umum Ekstrak Tumbuhan Obat yang ditetapkan oleh Badan Pengawas Obat dan Makanan Republik Indonesia. Parameter yang diuji meliputi organoleptik ekstrak, identitas ekstrak, penetapan kadar air, kadar abu total, kadar abu larut air, kadar abu tidak larut asam, kadar sari larut air, kadar sari larut etanol, dan uji kandungan kimia senyawa identitas ekstrak friedelin-3β-ol secara kualitatif dan kuantitatif.
Hasil penelitian dianalisis secara deskriptif dan deskriptif komparatif diperoleh organoleptis ekstrak berbentuk kental, berwarna coklat tua kehitaman, tidak berbau, dan rasa agak kelat, kadar air 17,67 % b/b, kadar abu total 1,77 % b/b, kadar abu larut air 4,47 % b/b, kadar abu tidak larut asam 1,37 % b/b, kadar sari larut air 25,83 % b/b, kadar sari larut etanol 39,71 % b/b, dan rata-rata kadar senyawa identitas friedelin-3β-ol dalam sampel ekstrak etanolik daun jati belanda adalah (0,027 ± 1,15 x 10-3) % b/v.
xi
find out the character of bastard cedar’s leaves ethanolic extract as one of the basic materials of slimming medicinal herbs, so it is able to get the product that has the same and continual quality standard from the safety, quality, and efficacy side.
This is a non experimental research, namely characterization the extract that refers to Parameter Standar Umum Ekstrak Tumbuhan Obat by Badan Pengawas Obat dan Makanan Republik Indonesia. The general standard parameter includes extract’s organoleptic, extract’s identity, the determination of water content, ashes content, water soluble ashes content, acid dissoluble ashes content, water soluble material content, ethanol soluble material content, the test of qualitity and quantitiy of the extract’s identity chemical content, especially friedelin-3β-ol.
The results were analyzed descriptively and comparatively. As results, the organoleptic extract was thick, dark brown, smelless, and sourish, the water content score was 17,67 % w/w, the total ashes content was 1,77 % w/w, water soluble ashes content score was 4,47 % w/w, acid dissoluble ashes content score was 1,37 % w/w, water soluble material content score was 25,83 % w/w, ethanol soluble material content score was 39,71 % w/w, and the average score of the extract’s identity chemical content friedelin-3β-ol in bastard cedar’s leaves ethanolic extract sample was (0,027 ± 1,15 x 10-3) % w/v.
Key words : Guazuma ulmifolia Lamk., the characterization, bastard cedar’s leaves ethanolic extract, friedelin-3β-ol
p-tuenesulfon
xii
xiii
2. Deskripsi ………..
3. Nama daerah ………
4. Kandungan kimia ………. B. Ekstrak …… ………... 1. Definisi ekstrak .………... 2. Pengelompokan ekstrak ………... 3. Metode ekstraksi ………..
4. Penguapan ………
5. Ekstrak kental daun jati belanda (Extractum Guazumae
ulmfoliae Folii Spissum ) ……….
C. Standarisasi ………
1. Pembakuan simplisia ……… 2. Pembakuan ekstrak ……….. 3. Pembakuan sediaan obat tradisional ……… D. Kromatografi Lapis Tipis ………... E. Densitometri ………... F. Keterangan Empiris ………... BAB III. METODE PENELITIAN………..…………..
A. Jenis dan Rancangan Penelitian……….. 1. Jenis penelitian ……….
xiv
D. Bahan ……….
E. Jalannya Penelitian……….. 1. Determinasi tanaman ……….... 2. Pengumpulan bahan ………. 3. Pembuatan serbuk daun ………... 4. Pembuatan ekstrak kental daun jati belanda ……….... 5. Uji organoleptik ekstrak ………... 6. Identitas ekstrak ………... 7. Penetapan kadar air ……….. 8. Penetapan kadar abu total ……… 9. Penetapan kadar abu larut air ………... 10.Penetapan kadar abu tidak larut asam ……….. 11.Penetapan kadar sari larut air ………... 12.Penetapan kadar sari larut etanol ……….. 13.Uji kandungan senyawa identitas secara kuallitatif dan
kuantitatif ………. F. Analisis Hasil ………... BAB IV. HASIL DAN PEMBAHASAN………... A. Determinasi Tanaman ……… B. Pengumpulan Bahan ……….
xv
F. Identitas Ekstrak ………... G. Penetapan Kadar Air ………... H. Penetapan Kadar Abu Total ………... I. Penetapan Kadar Abu Larut Air ………. J. Penetapan Kadar Abu Tidak Larut Asam ……….. K. Penetapan Kadar Sari Larut Air ………. L. Penetapan Kadar Sari Larut Etanol ……… M. Uji Kandungan Senyawa Identitas Ekstrak Etanolik Daun Jati
xvi Tabel II.
Tabel III.
Data pembuatan kurva baku friedelin-3β-ol ……… Kadar senyawa identitas friedelin-3β-ol dalam sampel ekstrak etanolik daun jati belanda ………
52
xvii Kromatogram larutan standar friedelin-3β-ol dan sampel ekstrak etanolik daun jati belanda pada deteksi lampu UV λ 254 nm ………... Kromatogram larutan standar friedelin-3β-ol dan sampel ekstrak etanolik daun jati belanda pada deteksi lampu UV λ 365 nm ……… Kromatogram larutan standar friedelin-3β-ol dan sampel
ekstrak etanolik daun jati belanda setelah disemprot pereaksi antimon (III) klorida pada deteksi sinar tampak … Kromatogram larutan standar friedelin-3β-ol dan sampel
xviii
Data Pengentalan Ekstrak Cair ………... Data Identitas dan Organoleptik Ekstrak ……… Perhitungan Penetapan Kadar Air ………... Perhitungan Penetapan Kadar Abu Total ……… Perhitungan Penetapan Kadar Abu Larut Air ... Perhitungan Penetapan Kadar Abu Tidak Larut Asam ... Perhitungan Penetapan Kadar Sari Larut Air ………. Perhitungan Penetapan Kadar Sari Larut Etanol ………… Uji Kandungan Kimia Senyawa Identitas Secara Kualitatif dan Kuantitatif ……… Foto Bahan dan Alat Penelitian ………..
1
Obat tradisional atau yang biasa disebut jamu telah diakui keberadaanya sejak dulu baik di Indonesia maupun negara-negara lainnya dan sampai sekarang tetap dimanfaatkan, bahkan cenderung meningkat. Di Indonesia tumbuhan obat digunakan untuk meningkatkan kesehatan (promotif), memulihkan kesehatan (rehabilitatif), pencegahan penyakit (preventif) dan penyembuhan (kuratif). Namun eksistensinya belum dapat disetarakan dengan pelayanan pengobatan modern dengan menggunakan obat kimia, karena memang belum seluruhnya teruji keamanan dan manfaatnya. Selama ini kebanyakan manfaat dan pengembangannya hanya dari data empiris dan dari pengalaman yang diwariskan dari generasi ke generasi. Dalam era globalisasi, pengembangan teknologi dan bentuk pemanfaatan tumbuhan obat di Indonesia dalam pelayanan kesehatan saat ini sudah mengenal konsep ekstrak (Anonim, 2005 b).
Pada industri obat tradisional standarisasi bahan baku perlu dilakukan, baik yang berupa simplisia maupun yang berbentuk ekstrak atau sediaan galenik (Anonim, 2005 b). Hal ini dikarenakan mutu produk obat tradisional tergantung dari bahan awal, proses produksi, pengawasan mutu, bangunan, peralatan, dan personalia yang menangani (Anonim, 2005 a). Standarisasi bertujuan untuk menjaga kontinuitas dari produk obat tradisional yang dihasilkan, sehingga kontinuitas khasiat obat tersebut juga akan terjaga. Pada proses standarisasi dilakukan pengukuran parameter untuk mendapatkan mutu yang seragam dan terulang. Parameter yang diukur meliputi parameter non spesifik, parameter spesifik, dan uji kandungan kimia ekstrak. Parameter non spesifik meliputi susut pengeringan dan bobot jenis, kadar air, kadar abu, sisa pelarut, residu pestisida, cemaran logam berat, cemaran mikroba. Parameter spesifik meliputi identitas ekstrak, organoleptik eksrak, dan senyawa yang terlarut dalam pelarut tertentu. Uji kandungan kimia ekstrak meliputi pola kromatogram, kadar total golongan kandungan kimia dan kadar kandungan kimia tertentu (Sinambela, 2002).
Beberapa penelitian telah dilakukan terhadap daun jati belanda. Pramono, Nurwati dan Sugiyanto (2000) menyimpulkan bahwa lendir daun jati belanda peroral dapat menghambat perkembangan berat badan tikus dibanding air suling sebagai kontrol. Selain itu Monika dan Farida (2000) menyimpulkan bahwa ekstrak etanol daun jati belanda peroral dapat menurunkan kadar kolesterol total darah kelinci. Joshita (2000) menyatakan seduhan dan rebusan daun jati belanda berpengaruh meningkatkan aktivitas enzim lipase secara in vitro.
Ekstrak daun jati belanda merupakan salah satu bahan baku penyusun jamu pelangsing tubuh. Oleh karena itu, perlu dilakukan karakterisasi ekstrak daun jati belanda sebagai pedoman kualitas produk yang diproduksi. Karakterisasi ini bertujuan untuk mendapatkan karakter bahan baku obat dan menjaga kontinuitas SQE (Safety, Quality, Efficacy) produk dengan kualitas yang baik, di mana keamanan (safety) terkait dengan tingkat cemaran, mutu (quality) terkait dengan kandungan kimia, dan kemanjuran (efficacy) terkait dengan efek dari bahan baku penyusun produk tersebut (Anonim, 2005 b). Penentuan nilai ini dilakukan dengan mengacu pada parameter standar umum ekstrak tumbuhan obat (Anonim, 2000).
1. Perumusan masalah
Berdasarkan latar belakang di atas, maka timbul permasalahan : “Bagaimanakah karakter ekstrak etanolik daun jati belanda?”
2. Keaslian penelitian
Sejauh penelusuran pustaka yang dilakukan penulis, penelitian mengenai karakterisasi ekstrak etanolik daun jati belanda belum pernah dilakukan. Penelitian sebelumnya yang telah dilakukan untuk mengetahui kandungan kimia dalam jati belanda dan membuktikan khasiat daun jati belanda adalah :
a. Pengaruh Daun Jati Belanda terhadap Berat Badan dan Gambaran Hematologik Darah Tikus Betina Serta Identifikasi Komponen Lendirnya oleh Nurwati (1984).
b. Pengaruh Jamu Galian Singset dan Daun Jati Belanda terhadap Hepar Tikus Serta Skrinning Fitokimia Daun Jati Belanda oleh Yeniwati (1984).
c. Ekstraksi dan Identifikasi secara Kromatografi Lapis Tipis (KLT) dan Spektrofotometer UV Senyawa Alkaloid Tumbuhan Jati Belanda (Guazuma ulmifolia Lamk.) oleh Wulandari (1996).
d. Pengaruh Lendir Daun Jati Belanda (Guazuma ulmifolia Lamk.) oleh Pramono, Nurwati dan Sugiyanto (2000).
e. Pengaruh Ekstrak Daun Jati Belanda (Guazuma ulmifolia Lamk.) terhadap Penurunan Kadar Kolesterol Kelinci oleh Farida dan Monica (2000).
g. Aktivitas Lipase Pankreas Rattus Norvegicus Akibat Pemberian Ekstrak Etanol Daun Jati Belanda (Guazuma ulmifolia Lamk.) oleh Rahardjo (2005). h. Pengaruh Pemberian Infusa Daun Jati Belanda (Guazuma ulmifolia Lamk.)
terhadap Kadar Trigliserida dalam Plasma Tikus Putih Jantan Galur Wistar oleh Wijayanti (2007).
3. Manfaat penelitian a. Manfaat teoritis
Penelitian ini diharapkan dapat memberikan manfaat bagi perkembangan ilmu pengetahuan terutama yang berkaitan dengan obat tradisional mengenai karakter ekstrak etanolik daun jati belanda.
b. Manfaat praktis
Penelitian ini diharapkan dapat memberi informasi pada masyarakat mengenai kesesuaian karakter ekstrak etanolik daun jati belanda dengan parameter standar ekstrak yang telah ditetapkan sehingga dapat digunakan sebagai salah satu komponen penyusun dalam jamu pelangsing.
B. Tujuan Penelitian
6 BAB II
TINJAUAN PUSTAKA
A. Jati Belanda 1. Keterangan botani
Guazuma ulmifolia Lamk. merupakan anggota suku Sterculiaceae. Di Indonesia tanaman ini dikenal dengan nama jati belanda (Anonim, 1978).
2. Deskripsi
cokelat muda, dan berdiameter 2 mm. Akarnya tunggang dan berwarna putih kecoklatan (Sulaksana dan Jayusman, 2005).
3. Nama daerah
Tanaman jati belanda dalam berbagai bahasa adalah : Jawa : Jati Londo
Sumatera : Jati Belanda
Melayu : Jati Blanda (Syamsuhidayat dan Hutapea, 1991)
4. Kandungan kimia
Zat utama yang terkandung dalam seluruh bagian tanaman jati belanda adalah tanin dan lendir atau muscilago (Suharmiati dan Maryani, 2003).
Batang tanaman jati belanda kaya akan kandungan tanin dan proantosianidin. Kandungan kimia utama yang pernah ditemukan dalam berbagai bagian tanaman jati belanda adalah alkaloid, kafeina, caryophyllene, katekin, epikatekin, farnesol, friedelin, kaurenoic acid, precocene I, prosianidin B-2, prosianidin B-5, prosianidin C-1, sitosterol, terpen (Anonim, 2004 b).
Karena adanya kandungan tanin, tanaman jati belanda memiliki rasa agak kelat. Di samping itu, karena kandungan kimia lainnya seperti kafeina dan sterol, tanaman jati belanda memiliki bau aromatik yang lemah (Suharmiati dan Maryani, 2003).
B. Ekstrak 1. Definisi ekstrak
yang sesuai, kemudian semua atau hampir semua pelarut diuapkan dan massa atau serbuk yang tersisa diperlakukan sedemikian sehingga memenuhi standar baku yang telah ditetapkan (Anonim, 2000).
2. Pengelompokan ekstrak
Pengelompokan ekstrak berdasarkan sifatnya, yaitu :
a.Ekstrak encer (extractum tenue). Sediaan ekstrak encer ini memiliki konsistensi madu dan mudah dituang.
b.Ekstrak kental (extractum spissum). Sediaan ekstrak kental ini memiliki konsistensi liat dalam keadaan dingin dan tidak dapat dituang. Kandungan airnya berjumlah sampai 30 %.
c.Ekstrak kering (extractum siccum). Sediaan ekstrak kering ini memiliki konsistensi kering dan mudah digosokkan dengan kandungan lembab tidak lebih dari 5 %.
d.Ekstrak cair (extractum fluidum). Pada ekstrak cair memiliki konsistensi cair dan mudah dituang (Voight, 1994).
3. Metode ekstraksi
Penyarian (ekstraksi) merupakan kegiatan penarikan zat yang dapat larut dari bahan yang tidak dapat larut dengan pelarut cair. Menurut acuan Sediaan Galenik (1986), secara umum penyarian dapat dibedakan menjadi infundasi, maserasi, perkolasi, dan penyarian berkesinambungan.
a. Infundasi
merupakan sediaan cair yang dibuat dengan menyari simplisia dengan air pada suhu 90°C selama 15 menit. Cara ini sangat sederhana dan sering digunakan oleh perusahaan obat tradisional. Alat yang digunakan adalah panci dan penangas air.
b. Maserasi
Maserasi digunakan untuk penyarian simplisia yang mengandung zat aktif yang mudah larut dalam cairan penyari. Cairan penyari yang digunakan dapat berupa air, etanol, air-etanol atau pelarut lain. Maserasi dilakukan dengan cara merendam serbuk simplisia atau bahan dalam cairan penyari. Cairan penyari akan menembus dinding sel dan masuk ke dalam rongga sel yang mengandung zat aktif, zat aktif akan larut dan karena adanya perbedaan konsentrasi antara larutan zat aktif di dalam sel dengan di luar sel, maka larutan yang terpekat didesak ke luar.
c. Perkolasi
Prinsip perkolasi adalah serbuk simplisia ditempatkan pada bejana silinder, yang bagian bawahnya diberi sekat berpori. Cairan penyari dialirkan dari atas ke bawah melalui serbuk tersebut, cairan penyari akan melarutkan zat aktif sel-sel yang dilalui sampai mencapai keadaan jenuh.
d. Penyarian berkesinambungan
Proses ini dengan cara penggabungan antara proses penyarian yang dilanjutkan dengan proses penguapan (Anonim,1986).
4. Penguapan
ini dapat dilakukan melalui penguapan dengan menggunakan alat Vacuum Rotary Evaporator. Cara kerjanya yaitu perputaran labu dalam sebuah pemanas pada temperatur dan kecepatan putar tertentu, akan menguapkan cairan yang terkandung dalam ekstrak. Pembesaran permukaan penguapan menyebabkan penguapan berlangsung dalam waktu lebih singkat. Pengaturan dalamnya pencelupan ke dalam penangas air, suhu penangas, hampa udara dan suhu pendingin membuat kondisi optimal dapat terpenuhi sehingga proses pengentalan ekstrak dapat berlangsung cepat (Voigt, 1994).
5. Ekstrak kental daun jati belanda (Extractum Guazumae ulmifoliae Folii Spissum )
Menurut Monografi Ekstrak Tumbuhan Obat Indonesia (2004) yang ditetapkan oleh Badan Pengawas Obat dan Makanan Republik Indonesia, ekstrak kental daun jati belanda adalah ekstrak yang dibuat dari daun tumbuhan Guazuma ulmifolia Lamk., suku Sterculiaceae, mengandung flavonoid tidak kurang dari 3,2 %. Pemerian ekstrak ini meliputi bentuk kental, warna coklat tua, tidak berbau dan rasa agak kelat. Kandungan kimia yang dimiliki adalah tanin, flavonoid,
HO
H
H
H H
friedelin-3β-ol
Gambar 1. Struktur kimia friedelin-3β-ol
Ekstrak kental jati belanda memiliki kadar air tidak lebih dari 18,1%, kadar abu total tidak lebih dari 4%, kadar abu tidak larut asam tidak lebih dari 1,5%. Residu pestisida fosfor organik dan klor organik tidak lebih dari 5μg/kg,
cemaran logam berat Pb tidak lebih dari 10 mg/kg, Cd tidak lebih dari 0,3 mg/kg, dan As tidak lebih dari 10 μg/kg. Cemaran aflatoksin tidak lebih dari 20 μg/kg.
Cemaran mikroba meliputi angka lempeng total tidak lebih dari 10 kol/g, angka kapang/khamir tidak lebih dari 10 kol/g, dan bakteri patogen negatif (Anonim, 2004 a).
C. Standarisasi
Standarisasi dapat terbagi dalam tiga langkah, yakni sebagai berikut. 1. Pembakuan simplisia
Pembakuan simplisia sebagai bahan baku obat tradisional merupakan titik awal yang penting bagi pembakuan obat tradisional secara keseluruhan karena obat tradisional yang bermutu hanya akan dapat diperoleh bila simplisia yang menjadi bahan bakunya juga bermutu. Untuk mendapatkan obat tradisional yang baik dan terulangkan dalam bentuk, keamanan dan manfaat diperlukan juga keterulangan dari mutu simplisia. Oleh karena mutu tanaman sumber simplisia umumnya sangat bervariasi, maka untuk menetapkan bermutu tidaknya simplisia yang digunakan diperlukan standar mutu sebagai pegangan. Agar simplisia yang digunakan mempunyai mutu standar, industri obat tradisional disarankan dan didorong untuk melakukan budidaya dan mengembangkan sendiri tanaman sumber simplisia spesifikasi masing-masing industri dengan mutu standar yang relatif homogen (Anonim, 2000).
2. Pembakuan ekstrak
Selain simplisia, saat ini banyak industri obat tradisional yang menggunakan ekstrak dari simplisia secara langsung, yang dipakai sebagai bahan baku obat tradisonal yang akan digunakan dalam upaya pelayanan kesehatan. Pembakuan ekstrak sebagai bahan baku obat tradisional juga penting dilakukan untuk menghasilkan produk obat tradisional yang bermutu (Anonim, 2000).
dilakukan antara lain: a. Parameter kadar air
Tujuan dilakukan penetapan parameter kadar air adalah memberikan batasan minimal atau rentang besarnya kandungan air dalam bahan. Prinsipnya adalah pengukuran kandungan air yang berada di dalam bahan yang dapat dilakukan dengan cara yang sesuai dengan kondisi ekstrak yaitu cara titrasi, destilasi atau gravimetri. Nilai maksimal atau rentang kadar air yang diperbolehkan terkait secara langsung dengan kemurnian dan kontaminasi pada bahan baku atau ekstrak (Anonim, 2000).
b. Parameter kadar abu
Tujuan dilakukan penetapan parameter kadar abu adalah memberikan gambaran kandungan mineral internal dan eksternal yang berasal dari proses awal sampai terbentuknya ekstrak. Prinsip pengerjaannya adalah bahan dipanaskan pada temperatur dimana senyawa organik dan turunannya terdestruksi dan menguap sehingga tinggal unsur mineral anorganik. Nilai maksimal atau rentang kadar abu yang diperbolehkan terkait secara langsung dengan kemurnian dan kontaminasi pada bahan baku atau ekstrak (Anonim, 2000).
c. Parameter identitas ekstrak
yang digunakan, nama Indonesia tumbuhan dan senyawa identitas yang terkandung didalamnya (Anonim, 2000).
d.Parameter organoleptik ekstrak
Tujuan dilakukan uji organoleptik adalah untuk pengenalan awal yang sederhana dan seobjektif mungkin sehingga tidak terjadi kesalahan dalam pemilihan ekstrak yang digunakan sebagai bahan dasar pembuatan obat tradisional. Prinsip uji organoleptik ekstrak menggunakan pancaindera untuk mendeskripsikan bentuk, warna, bau, rasa dari ekstrak tersebut (Anonim, 2000).
e. Uji kandungan kimia tertentu dalam ekstrak
Tujuan dilakukan uji kandungan kimia tertentu dalam ekstrak adalah memberikan data kadar kandungan kimia tertentu sebagai senyawa identitas atau senyawa yang diduga bertanggung jawab pada efek farmakologi. Prosedur pengerjaan uji kandungan kimia identitas ini spesifik untuk masing-masing ekstrak yang distandarisasi (Anonim, 2000).
3. Pembakuan sediaan obat tradisional
pelayanan kesehatan formal, maka perlu dilakukan pembakuan sediaan obat tradisional agar terjamin mutu dan keamanannya (Anonim,2000).
D. Kromatografi Lapis Tipis
Kromatografi adalah prosedur pemisahan senyawa campuran berdasarkan perbedaan kecepatan migrasi, karena adanya perbedaan koefisien distribusi masing-masing senyawa di antara dua fase yang saling bersinggungan dan tidak saling campur, yang disebut sebagai fase gerak (mobile phase) yang berupa zat cair atau zat gas, dan fase diam (stationary phase) yang berupa zat cair atau zat padat (Noegrohati, 1994).
spektrofotometri, pada kromatografi lapis tipis dua dimensi, lempeng yang telah dielusi diputar 90o dan dielusi lagi, umumnya menggunakan bejana lain yang berisi pelarut lain (Anonim, 1995).
Faktor – faktor yang mempengaruhi gerakan bercak pada KLT atau mempengaruhi harga Rf adalah sebagai berikut.
1. Bahan penyerap, sifat dan aktivitasnya
Penyerap yang berbeda memberikan hasil pemisahan yang berbeda walaupun fase gerak dan bahan yang dipisahkan sama. Harga Rf dipengaruhi oleh aktivitas dari bahan penyerap karena dapat mempengaruhi daya adsorpsi. Aktivitas dapat dicapai dengan pemanasan dengan tujuan untuk menghilangkan molekul-molekul air.
2. Tebal dan kerataan dalam lapisan
Ketidakrataan lapisan menyebabkan aliran fase gerak tidak sama, yang menyebabkan harga Rf tidak sama. Tebal baku yang biasa digunakan adalah 0,25 mm.
3. Kemurnian fase gerak
Fase gerak tunggal akan memberikan pemisahan kurang baik. Jika digunakan fase gerak yang berupa campuran maka perbandingan yang digunakan harus diperhatikan.
4. Kejenuhan bejana kromatografi
5. Suhu
Pemisahan sebaiknya dilakukan pada suhu yang tetap, dimaksudkan untuk mencegah perubahan komposisi fase gerak atau kejenuhan bejana.
6. Jumlah cuplikan yang dianalisis
Jumlah cuplikan yang dianalisis jika terlalu banyak maka kecenderungan terjadi penyebaran. Penyebaran bercak atau terjadinya ekor sehingga akan memperbesar kesalahan harga Rf.
7. Kesetimbangan
Faktor kesetimbangan ini terlihat lebih nyata pada kromatografi lapis tipis dibanding kromatografi kolom, sehingga sangat perlu untuk KLT diusahakan di ruangan di dalam bejana jenuh dengan uap pelarut. Ketidakseimbangan di dalam bejana akan terlihat dari permukaan fase gerak yang terbentuk cekung atau fase gerak lebih cepat pada bagian tepi dibanding bagian tengah.
8. Struktur dan sifat kimia senyawa yang dipisahkan
Sifat kimia seperti mudah larut, teakanan uap dan kepolaran dapat mempengaruhi harga Rf dari suatu senyawa dibanding senyawa lainnya (Gandjar, 1991).
E. Densitometri
pencucian (Gritter, 1985).
Teknik pengukuran dapat didasarkan atas pengukuran intensitas sinar yang diserap (absorbansi), intensitas sinar yang dipantulkan (reflaktansi) atau intensitas sinar yang difluoresensikan (fluoresensi). Teknik pengukuran berdasarkan refleksi di mana sinar datang sebagian diserap dan sebagian lagi dipantulkan (Mintarsih, 1990).
Pada beberapa alat TLC scanner, sudah dilengkapi alat pemroses data atau mikro komputer, sehingga tinggi puncak dapat langsung dicatat sebagai data sekaligus dengan kromatogramnya dan dapat pula dicatat langsung sebagai kadarnya, melalui teknik pemrogaman tertentu (Mintarsih, 1990).
F. Keterangan Empiris
20 BAB III
METODOLOGI PENELITIAN A. Jenis dan Rancangan Penelitian 1. Jenis penelitian
Penelitian ini merupakan jenis penelitian non eksperimental, karena tidak diberikan perlakuan terhadap subjek uji.
2. Rancangan penelitian
Penelitian dilakukan melalui beberapa tahap sebagai berikut. a. Determinasi tanaman
b. Pengumpulan bahan (daun jati belanda) c. Pembuatan serbuk daun
d. Pembuatan ekstrak kental e. Uji organoleptik ekstrak f. Identitas ekstrak
g. Penetapan kadar air h. Penetapan kadar abu total i. Penetapan kadar abu larut air
j. Penetapan kadar abu tidak larut asam k. Penetapan kadar sari larut air
l. Penetapan kadar sari larut etanol
B. Definisi Operasional
1.Karakterisasi ekstrak adalah pengukuran kondisi ekstrak etanolik daun jati belanda mengikuti Parameter Standar Umum Ekstrak Tumbuhan Obat yang ditetapkan oleh Badan Pengawas Obat dan Makanan meliputi organoleptik ekstrak, identitas ekstrak, kadar air, kadar abu total, kadar abu larut air, kadar abu tidak larut asam, kadar sari larut air, kadar sari larut etanol, dan uji kandungan kimia senyawa identitas ekstrak secara kualitatif dan kuantitatif.
2.Ekstrak kental etanolik daun jati belanda adalah ekstrak yang diperoleh melalui proses maserasi serbuk daun jati belanda dengan etanol 95 % selama 3 x 24 jam, kemudian dilakukan penguapan dengan penguap vakum dilanjutkan dengan menggunakan oven hingga diperoleh ekstrak kental.
3.Senyawa identitas ekstrak adalah senyawa tertentu yang menjadi petunjuk spesifik terhadap ekstrak tersebut, dalam penelitian ini senyawa friedelin-3β-ol sebagai senyawa identitas ekstrak kental daun jati belanda.
4.Uji kandungan kimia senyawa identitas ekstrak meliputi uji kualitatif untuk mengetahui adanya kandungan senyawa friedelin-3β-ol menggunakan
metode Kromatografi Lapis Tipis (KLT) serta uji kuantitatif sebagai gambaran mengenai kadar senyawa friedelin-3β-ol di dalam ekstrak menggunakan metode
C. Alat
Alat yang digunakan dalam penelitian ini adalah:
Blender (Retsch bv), Furnace / pemijar (Carbolite), Vacuum rotary evaporator (Janke & Kunkel Ika Labortechnik), oven (Memmert), TLC Scanner (Camag TLC Scanner 3), timbangan analitik (Model AB-204, Mettler Toledo), krus platina, penjepit, hot plate (Heidolph MR 2002), pompa vacuum (Robinair High Vacuum Pump Model 15110 seri 11026), corong Buchner, eksikator, penangas air, alat-alat gelas (pyrex).
D. Bahan
Bahan baku pembuatan ekstrak kental etanolik daun jati belanda adalah daun jati belanda yang diambil dari Kebun Tanaman Obat Fakultas Farmasi Universitas Sanata Dharma saat pagi hari pada bulan Juni 2009.
E. Jalannya Penelitian
1. Determinasi tanaman
Determinasi tanaman jati belanda dilakukan di Laboratorium Farmakognosi-Fitokimia Fakultas Farmasi Universitas Sanata Dharma Yogyakarta, secara makroskopik dengan cara membandingkan tanaman jati belanda dengan yang ada di buku acuan untuk mendeterminasi. Determinasi dilakukan dengan cara membandingkan ciri-ciri morfologi tanaman jati belanda yang digunakan dengan buku acuan (Backer dan Bakhuizen van den Brink, 1963). 2. Pengumpulan bahan
Daun jati belanda diambil dari satu pohon di kebun tanaman obat Fakultas Farmasi Universitas Sanata Dharma pada bulan Juni 2009. Waktu pengambilan daun dilakukan antara pukul 9 hingga 10 pagi. Daun yang diambil adalah daun tua atau yang telah membuka sempurna, kurang lebih daun ke-4 sampai ke-8 dari pucuk daun.
3. Pembuatan serbuk daun
Daun jati belanda dicuci dengan air mengalir lalu ditiriskan dan
diangin-anginkan. Kemudian daun dikeringkan menggunakan oven dengan suhu 45ºC
selama 2 hari. Daun yang telah kering dibuat serbuk dengan blender hingga diperoleh serbuk kering daun jati belanda. Selanjutnya, serbuk daun jati belanda diayak dengan ayakan nomor mesh 12/50.
4. Pembuatan ekstrak kental daun jati belanda
dalam erlenmeyer, kemudian ditambah 10 bagian etanol 95% yaitu 150,0 ml, direndam selama 6 jam sambil diaduk, kemudian didiamkan sampai 24 jam. Maserat dipisahkan dan proses diulangi dua kali dengan jenis dan jumlah pelarut yang sama. Semua maserat dikumpulkan dan diuapkan dengan penguap vakum kemudian dilanjutkan menguapkan sisa pelarut menggunakan oven hingga diperoleh ekstrak kental. Rendemen yang diperoleh ditimbang dan dicatat.
5. Uji organoleptik ekstrak
Dilakukan dengan penggunaan pancaindera, meliputi deskripsi bentuk, warna, bau, dan rasa ekstrak.
6. Identitas ekstrak
Dilakukan dengan studiliteratur meliputi deskripsi tata nama ekstrak dan senyawa identitas ekstrak.
7. Penetapan kadar air
Kurang lebih 2,0 g ekstrak kental etanolik daun jati belanda ditimbang saksama dalam wadah yang telah ditara. Dikeringkan pada suhu 105oC selama 5 jam dalam oven, didinginkan lalu ditimbang. Pengeringan dilanjutkan dan ditimbang pada pada jarak 1 jam sampai perbedaan antara dua penimbangan berturut-turut tidak lebih dari 0,25%.
8. Penetapan kadar abu total
arang habis, didinginkan, dan ditimbang sampai bobot konstan. Jika dengan cara ini arang tidak dapat dihilangkan, maka ditambahkan air panas, disaring melalui kertas saring bebas abu. Dipijarkan sisa dan kertas saring dalam krus, diuapkan, dipijarkan hingga bobot tetap, ditimbang. Dihitung kadar abu terhadap bahan yang dikeringkan di udara.
9. Penetapan kadar abu larut air
Abu yang diperoleh pada penetapan kadar abu, dididihkan dengan 25,0 ml aquades selama 5 menit, bagian yang larut air dikumpulkan, disaring melaui krus kaca masir atau kertas saring bebas abu, kemudian dipijarkan selama 1 jam pada suhu tidak lebih dari 450oC, hingga bobot tetap, ditimbang. Dihitung kadar abu yang larut dalam air terhadap bahan yang telah dikeringkan di udara.
10. Penetapan kadar abu tidak larut asam
Abu yang diperoleh pada penetapan kadar abu, dididihkan dengan 25,0 ml asam klorida selama 5 menit, bagian yang tidak larut dalam asam dikumpulkan, disaring melalui krus kaca masir atau kertas saring bebas abu, kemudian dicuci dengan air panas dan dipijarkan selama 1 jam pada suhu tidak lebih dari 4500C, hingga bobot tetap, ditimbang. Dihitung kadar abu yang tidak larut dalam asam terhadap bahan yang telah dikeringkan di udara.
11. Penetapan kadar sari larut air
30,0 ml filtrat hingga kering dalam cawan dangkal berdasar rata yang telah ditara, panaskan sisa pada suhu 105oC hingga bobot tetap. Hitung kadar dalam persen sari yang larut dalam air, dihitung terhadap bahan yang telah dikeringkan di udara.
12. Penetapan kadar sari larut etanol
Sebanyak 2,0 g ekstrak kental etanolik daun jati belanda dimaserasi dengan 40,0 ml etanol 95%, menggunakan labu bersumbat sambil berkali-kali dikocok selama 6 jam pertama kemudian dibiarkan selama 18 jam. Saring cepat untuk menghindarkan penguapan etanol (95%), uapkan 20,0 ml filtrat hingga kering dalam cawan dangkal berdasar rata yang telah ditara, panaskan sisa pada suhu 105oC hingga bobot tetap. Hitung kadar dalam persen sari yang larut dalam etanol, dihitung terhadap bahan yang telah dikeringkan di udara.
13. Uji kandungan kimia senyawa identitas ekstrak etanolik daun jati belanda secara kualitatif dan kuantitatif
Uji kandungan kimia senyawa identitas ekstrak berupa analisa kualitatif dan kuantitatif. Analisa kualitatif dilakukan dengan metode Kromatografi Lapis Tipis (KLT) sedangkan analisa kuantitatif dilakukan dengan perhitungan kadar kandungan kimia senyawa identitas ekstrak etanolik daun jati belanda yaitu friedelin-3β-ol dengan metode KLT densitometri.
a. Analisis kualitatif dilakukan dengan menotolkan larutan standar dan larutan sampel ekstrak pada plat kromatografi lapis tipis.
1. Preparasi standar
2. Preparasi sampel
Sebanyak 4,0 g ekstrak disari dengan 40,0 ml etanol 95 % menggunakan labu bersumbat sambil berkali-kali dikocok selama 6 jam pertama kemudian dibiarkan selama 18 jam. Larutan sampel ditotolkan untuk masing-masing replikasi ( 3 replikasi) sebanyak 20 μl.
Komponen yang digunakan dalam analisis kualitatif meliputi : fase diam : silika gel GF254
fase gerak : heksan : etil asetat (3:2 v/v)
Deteksi : (1) pengamatan di bawah UV 254 nm dan UV 365 nm
(2) disemprot dengan larutan antimon (III) klorida 20 % dalam kloroform (pereaksi Carr Price) kemudian dipanaskan selama 5-6 menit menggunakan oven pada suhu 100oC.
b. Analisis kuantitatif dilakukan dengan cara : hasil KLT yang diperoleh dari uji kualitatif baik standar maupun sampel diukur kadarnya dengan menggunakan alat densitometer.
1. Penentuan panjang gelombang maksimum
Panjang gelombang maksimum diperoleh dengan cara menelusuri bercak pada panjang gelombang 200 nm sampai 380 nm. Panjang gelombang maksimum dicapai pada saat terjadi serapan maksimum yang ditunjukkan dengan terbentuknya puncak kurva. Pada penentuan panjang gelombang ini digunakan friedelin-3β-ol murni.
2. Pembuatan kurva baku
dalam kloroform. Larutan tersebut ditotolkan pada plat fase diam silika gel GF254 sebanyak 10 μl, 15 μl, 20 μl, 25 μl, 30 μl menggunakan pipet mikroliter dan dikembangkan dalam bejana KLT yang telah jenuh dengan uap fase gerak heksan:etil asetat (3:2 v/v), selanjutnya dilakukan elusi hingga jarak rambatan fase gerak 10,0 cm dari totolan. Keringkan lempeng dan deteksi dengan lampu UV pada panjang gelombang 254 nm dan 365 nm. Apabila bercak tidak terdeteksi, dilakukan penyemprotan dengan antimon (III) klorida (pereaksi Carr Price). Kemudian dilakukan pengukuran dengan TLC Scanner sehingga diperoleh data AUC. Berdasarkan data AUC dihitung secara regresi linier sehingga diperoleh nilai a, b, r. Nilai r menunjukkan kelinieritasan garis yang terbentuk ( korelasi liniear antara x dan y). Nilai a dan b tersebut kemudian dimasukkan ke dalam persamaan y = bx + a, dimana y adalah area di bawah kurva (AUC), a adalah koefisien regresi dan b adalah tetapan regresi, sedangkan x adalah konsentrasi zat yang ingin diketahui.
3. Penetapan kadar sampel secara KLT densitometri
Dari hasil pengukuran diperoleh harga AUC dari sampel ekstrak yang selanjutnya dimasukkan ke dalam persamaan regresi linier yang diperoleh pada pembuatan kurva baku. Kadar masing-masing kandungan kimia dihitung menggunakan persamaan kurva baku tersebut, sehingga diperoleh harga x (konsentrasi sampel).
F. Analisis Hasil
Hasil yang diperoleh dari karakterisasi ekstrak etanolik daun jati belanda dianalisis dengan metode deskriptif dan deskriptif komparatif. Analisis dilakukan dengan memaparkan nilai-nilai hasil pengukuran yang diperoleh dari penelitian. Pada analisis deskriptif akan dipaparkan hasil pengujian identitas ekstrak, nilai pengukuran kadar abu larut air, kadar sari larut air, kadar sari larut etanol, dan hasil uji kandungan kimia senyawa identitas friedelin-3β-ol secara kuantitatif
dalam ekstrak kental etanolik daun jati belanda. Sedangkan pada analisis deskriptif komparatif akan dipaparkan hasil pengujian organoleptik ekstrak, kadar air, kadar abu total, kadar abu tidak larut asam, serta hasil uji kandungan kimia senyawa identitas friedelin-3β-ol secara kualitatif dalam ekstrak etanolik daun jati
30 BAB IV
HASIL DAN PEMBAHASAN
A. Determinasi Tanaman
Determinasi tanaman perlu dilakukan untuk memperoleh kepastian bahwa tanaman yang digunakan dalam penelitian merupakan tanaman yang ingin diuji yaitu Guazuma ulmifolia Lamk., sehingga dapat menghindari kesalahan pemilihan bahan tanaman yang digunakan dalam penelitian.
Determinasi tanaman dilakukan di Laboratorium Farmakognosi-Fitokimia, Fakultas Farmasi, Universitas Sanata Dharma, secara makroskopik dengan cara membandingkan ciri-ciri morfologi tanaman jati belanda yang digunakan dengan buku acuan yang ada. Buku acuan yang digunakan yaitu Flora of Java edisi I karangan Backer dan Backhuizen van den Brink (1963).
Berdasarkan hasil determinasi dapat dipastikan tanaman yang digunakan dalam penelitian ini adalah benar-benar tanaman jati belanda dengan nama latin Guazuma ulmifolia Lamk. (Lampiran 1).
B. Pengumpulan Bahan
hingga 10. Pengambilan daun jati belanda dilakukan pada pagi hari agar daun yang diambil masih segar karena turgor daun yang paling tinggi terjadi saat dua jam sebelum matahari tinggi atau sebelum matahari bersinar paling terik. Daun yang diambil adalah daun yang telah membuka sempurna, kurang lebih pada posisi daun ke-4 sampai ke-8 dari pucuk daun. Pemilihan ini karena untuk tanaman jati belanda yang dipanen adalah daun yang tua, yaitu pada saat kandungan kimia atau senyawa aktif yang diinginkan berada pada kadar maksimal di dalam daun. Daun yang dipetik adalah daun ke-4 hingga ke-8 dari pucuk daun karena bagian ini merupakan bagian yang memiliki usia yang tua (matang). Bila daun yang dipetik berada pada posisi kurang dari daun ke-4 dari pucuk daun dikhawatirkan usia daun masih muda sehingga belum memiliki kandungan kimia yang maksimal. Demikian pula bila dipetik daun pada posisi lebih dari daun ke-8 dari pucuk daun dikhawatirkan usia daun terlalu tua sehingga kadar kandungan kimia tidak maksimal.
C. Pembuatan Serbuk Daun
Daun jati belanda yang telah dipetik kemudian dibersihkan dan dicuci dengan air mengalir. Pencucian dimaksudkan untuk menghilangkan kotoran yang melekat pada daun seperti debu dan tanah. Daun yang telah benar-benar bersih ditiriskan dan diangin-anginkan untuk menghilangkan air, lalu dikeringkan menggunakan oven dengan suhu 45ºC selama 2 hari. Suhu ini dipilih karena suhu
mudah rusak dan lebih tahan lama dalam penyimpanan.
Daun jati belanda yang telah kering dibuat serbuk dengan blender hingga diperoleh serbuk kering daun jati belanda. Tujuan pembuatan serbuk adalah memperkecil ukuran partikel agar luas permukaan partikel menjadi semakin besar, sehingga kontak serbuk dengan penyari akan semakin besar. Hal ini menyebabkan kandungan kimia tersari lebih cepat dan lebih banyak sehingga penyarian berlangsung efektif dan efisien.
Pada umumnya penyarian akan bertambah baik bila permukaan serbuk simplisia yang bersentuhan dengan cairan penyari makin luas. Hal ini berarti bahwa semakin halus serbuk simplisia seharusnya penyarian akan semakin baik. Namun ternyata tidak selalu demikian dalam pelaksanaanya, karena penyarian masih tergantung juga pada sifat fisik dan kimia simplisia yang bersangkutan. Simplisia yang terlalu halus akan menyulitkan proses penyaringan, karena butir-butir halus akan membentuk suspensi yang sulit dipisahkan dengan hasil penyarian yang menyebabkan hasil penyarian menjadi tidak murni lagi tetapi tercampur dengan partikel-partikel halus. Pembuatan serbuk yang terlalu halus akan menyebabkan banyak dinding sel yang pecah, padahal dinding sel merupakan saringan, sehingga zat yang tidak larut masih terdapat di dalam sel. Apabila banyak dinding sel yang pecah, maka tidak ada lagi saringan yang mampu menahan zat yang tidak larut, sehingga zat yang tidak diinginkan tersebut dapat bercampur dengan hasil penyarian. Oleh sebab itu, perlu ditetapkan derajat halus serbuk yang paling tepat untuk memperoleh hasil penyarian yang baik.
derajat halus serbuk adalah 4/18. Jenis pengayak yang digunakan dinyatakan dengan nomor mesh, dan nomor mesh diperoleh melalui konversi angka derajat halus 4/18 dikali dengan 2, 54 (1 inchi). Hasil konversi menunjukkan nomor mesh yang seharusnya digunakan adalah 10/45, namun karena terbatasnya alat yang tersedia maka pada penelitian ini digunakan ayakan nomor 12/50.
Setelah serbuk diayak dengan ayakan 12/50 diperoleh serbuk yang homogen. Pembuatan serbuk homogen sesuai derajat halus serbuk dimaksudkan untuk mendapatkan ukuran butiran serbuk daun yang optimal sehingga penarikan kandungan kimia dalam butiran serbuk daun oleh pelarut pada proses maserasi yang akan dilakukan dapat berlangsung maksimal. Ukuran butiran serbuk menentukan keefektifan maserasi karena dibutuhkan luas permukaan yang optimum agar pelarut mampu menembus butiran serbuk dan menarik kandungan kimia yang terdapat di dalamnya. Semakin besar luas permukaan serbuk semakin besar luas permukaan kontak serbuk dengan cairan pelarut, maka semakin banyak kandungan kimia yang dapat terlarut.
D. Pembuatan Ekstrak Kental Etanolik Daun Jati Belanda
maupun tidak langsung seminimal mungkin. Hal ini dapat ditemukan pada proses maserasi, karena serbuk simplisia hanya mengalami perendaman dalam jangka waktu tertentu tanpa perlakuan pemanasan.
yang tidak diperlukan tetapi ikut terlarut dalam cairan penyari.
Dari hasil penyarian diperoleh ekstrak cair etanolik daun jati belanda yang dikentalkan menggunakan vacuum rotary evaporator pada suhu 50°C. Tujuan ekstrak cair dikentalkan adalah untuk mendapatkan ekstrak berbentuk kental sesuai dengan bentuk ekstrak yang terdapat pada Monografi Ekstrak Tumbuhan Obat Indonesia. Penurunan tekanan di bawah tekanan normal akan menurunkan titik didih etanol sehingga dengan pemanasan yang tidak terlalu tinggi proses penguapan etanol dapat berlangsung cepat. Suhu pengentalan yang tinggi dikhawatirkan dapat membuat kandungan kimia yang terdapat dalam ekstrak menjadi tidak stabil bahkan rusak. Hasil pengentalan kemudian dilanjutkan dengan menguapkan cairan pengekstraksi yang tersisa menggunakan oven dengan suhu 45°C hingga diperoleh ekstrak kental dengan konsistensi yang liat dan tidak dapat dituang. Ekstrak inilah yang dinamakan ekstrak kental etanolik daun jati belanda. Dari hasil penelitian diperoleh ekstrak kental etanolik daun jati belanda dengan rendemen sebesar 24, 32 %.
Gambar hasil ekstrak cair dan ekstrak kental etanolik daun jati belanda dari penelitian ditunjukkan pada gambar berikut.
(a) (b)
E. Uji Organoleptik Ekstrak
Uji organoleptik bertujuan untuk pengenalan awal secara sederhana dan seobjektif mungkin. Uji ini dilakukan dengan menggunakan indera untuk dapat mendeskripsikan bentuk, warna, bau, dan rasa ekstrak.
Dari hasil pengujian ekstrak cair etanolik daun jati belanda memiliki bentuk cair, berwarna hijau tua, berbau khas etanol, dan rasa agak kelat. Sedangkan ekstrak kental etanolik daun jati belanda memiliki bentuk kental, berwarna coklat tua kehitaman, tidak berbau, dan rasa agak kelat. Hasil uji organoleptik ini memberikan manfaat bagi peneliti untuk mengenali ekstrak tersebut sebagai ekstrak kental etanolik daun jati belanda. Hal ini karena setelah diuji dan dibandingkan dengan Monografi Ekstrak Tumbuhan Obat Indonesia ciri-ciri yang telah diperoleh di atas sesuai dengan yang telah ditetapkan untuk ekstrak kental daun jati belanda, yaitu berbentuk kental, berwarna cokelat tua, tidak berbau, dan rasa agak kelat.
F. Identitas Ekstrak 1. Deskripsi tata nama
a. Nama ekstrak :Ekstrak Kental Daun Jati Belanda (Extractum Guazumae ulmifoliae
Folii Spissum)
b. Nama latin tanaman : Guazuma ulmifolia Lamk. c. Bagian tanaman yang digunakan : daun
d. Nama Indonesia tanaman : jati belanda
Tujuan dilakukan penentuan identitas ekstrak adalah untuk memperoleh identitas objektif dan spesifik dari ekstrak. Ekstrak dapat mengandung senyawa identitas artinya senyawa tertentu yang menjadi petunjuk spesifik dengan metode tertentu (Anonim, 2000).Secara umum suatu senyawa atau sekelompok senyawa dapat menjadi senyawa identitas bahan tumbuhan obat jika senyawa tersebut stabil, dapat diidentifikasi dan dianalisa secara kuantitatif, serta unik untuk tanaman yang bersangkutan (Sinambela, 2002).
Pada proses standarisasi bahan baku obat tradisional hasil penetapan senyawa senyawa identitas yang dapat berupa senyawa tunggal atau kelompok kelas senyawa dalam tanaman obat akan berguna sebagai acuan kontrol kuantitatif tanpa memperhatikan apakah senyawa atau kelompok senyawa tersebut memiliki aktivitas terapi atau tidak.
Kandungan kimia utama yang terdapat dalam tanaman jati belanda adalah tanin dan lendir atau muscilago. Sedangkan senyawa identitas yang khas pada ekstrak daun jati belanda adalah friedelin-3β-ol.
G. Penetapan Kadar Air
yang diperbolehkan pada penetapan kadar air ini terkait dengan kemurnian bahan baku dan kontaminasi selama proses pembuatan ekstrak.
Penetapan kadar air dalam ektrak kental etanolik daun jati belanda dilakukan dengan metode gravimetri yaitu dengan menimbang selisih bobot ekstrak sebelum dan sesudah pengeringan. Pengeringan dilakukan dengan menggunakan oven selama 5 jam pada suhu 105°C yaitu suhu optimal untuk menguapkan air yang terkandung dalam ekstrak etanolik daun jati belanda. Lalu ekstrak didinginkan dan ditimbang. Pengeringan dilanjutkan dan ditimbang pada pada jarak 1 jam sampai perbedaan antara dua penimbangan berturut-turut tidak lebih dari 0,25%
Diperoleh kadar air ekstrak kental etanolik daun jati belanda pada penelitian adalah 17,67 % b/b. Nilai tersebut telah memenuhi syarat Monografi
Ekstrak Tumbuhan Obat Indonesia yang ditetapkan oleh BPOM RI untuk ekstrak kental daun jati belanda yaitu tidak lebih dari 18,1%.
H. Penetapan Kadar Abu Total
dengan kemurnian bahan baku dan dijadikan sebagai salah satu indikator kualitas dan keamanan bahan baku tersebut sebagai komponen penyusun jamu.
Penetapan kadar abu dilakukan dengan memijarkan ekstrak pada suhu tinggi yaitu 400oC-600oC. Diharapkan pada suhu ini seluruh senyawa organik yang memiliki unsur karbon terdestruksi dan menguap sehingga yang tertinggal hanya bahan anorganik yang tidak akan terdestruksi oleh suhu tinggi. Setelah seluruh ekstrak menjadi abu kemudian dilakukan penimbangan setiap jam sambil terus dipijarkan sampai didapatkan bobot konstan, yaitu bobot dimana dua kali penimbangan berturut-turut berbeda tidak lebih dari 0,5 mg tiap g sisa yang ditimbang.
Hasil penetapan kadar abu total dalam ekstrak kental etanolik jati belanda adalah 1,77 % b/b. Nilai tersebut memberikan gambaran bahwa kandungan bahan
anorganik dalam ekstrak tersebut berada di bawah nilai maksimal yang ditetapkan, artinya bahan baku pembuatan ekstrak tersebut murni dan aman dari segi cemaran bahan anorganik.
I. Penetapan Kadar Abu Larut Air
Penetapan kadar abu larut air bertujuan untuk mengetahui jumlah kandungan abu dalam ekstrak etanolik daun jati belanda yang dapat terlarut dalam air.
hingga diperoleh bobot konstan. Selanjutnya dapat dihitung jumlah abu yang larut dalam air. Dari hasil pengujian diperoleh kadar abu yang larut air sebesar 4,47 % b/b. Hasil penetapan kadar abu larut air yang diperoleh dari penelitian ini tidak dibandingkan dengan standar karena belum ditetapkan standar kadar abu larut air untuk ekstrak kental daun jati belanda pada Monografi Ekstrak Tumbuhan Obat Indonesia.
J. Penetapan Kadar Abu Tidak Larut Asam
Penetapan kadar abu tidak larut asam bertujuan untuk mengetahui kandungan cemaran silika pada ekstrak etanolik daun jati belanda. Kadar abu tidak larut asam yang tinggi menunjukkan adanya kontaminasi residu nonlogam yang tidak dapat larut dalam asam pada ekstrak, seperti silika (Si) yang terdapat di alam sebagai kuarsa, batu dan pasir. Menurut Monografi Ekstrak Tumbuhan Obat
Indonesia yang ditetapkan oleh BPOM RI kadar abu tidak larut asam ekstrak etanolik daun jati belanda tidak lebih dari 1,5 %.
K. Penetapan Kadar Sari Larut Air
Tujuan ditetapkannya kadar sari larut air adalah untuk memberikan gambaran awal jumlah kandungan senyawa dalam ekstrak etanolik daun jati belanda yang dapat larut dalam pelarut air.
Penetapan kadar sari larut air dilakukan dengan metode gravimetri, yaitu dengan menimbang selisih bobot ekstrak sebelum dan sesudah pengeringan. Pelarut yang digunakan adalah air kloroform. Kloroform ditambahkan dalam penyari untuk mencegah terjadinya pembusukan ekstrak selama maserasi, karena di dalam air terkandung mikroba yang dapat menyebabkan pembusukan zat. Ekstrak etanolik daun jati belanda yang telah dilarutkan dalam air kloroform kemudian digojog selama 6 jam pertama dan kemudian didiamkan selama 18 jam. Prinsipnya adalah seperti pada proses maserasi, dimana pelarut diusahakan dapat menarik senyawa yang dapat terlarut semaksimal mungkin melalui perendaman dan penggojogan. Suhu pemanasan yang digunakan saat penetapan kadar sari larut air adalah 105oC karena suhu ini merupakan suhu optimal untuk menguapkan pelarut air yang digunakan. Dari hasil pengujian diperoleh kadar sari larut air ekstrak etanolik daun jati belanda sebesar 25,83 % b/b. Nilai tersebut belum dapat dibandingkan dengan nilai standar karena belum ditetapkan standar kadar sari larut air untuk ekstrak kental daun jati belanda pada Monografi Ekstrak Tumbuhan Obat Indonesia.
L. Penetapan Kadar Sari Larut Etanol
dapat larut dalam pelarut etanol.
Seperti penetapan kadar sari larut air, penetapan kadar sari larut etanol juga menggunakan metode gravimetri. Dari hasil pengujian diperoleh kadar sari larut etanol ekstrak etanolik daun jati belanda sebesar 39,71 % b/b. Nilai tersebut belum dapat dibandingkan dengan nilai standar karena belum ditetapkan standar kadar sari larut etanol untuk ekstrak kental daun jati belanda pada Monografi Ekstrak Tumbuhan Obat Indonesia.
Apabila hasil penetapan kadar sari larut etanol tersebut dibandingkan dengan hasil yang diperoleh dari penetapan kadar sari larut air, maka kadar sari larut etanol memberikan nilai kadar sari yang lebih tinggi. Hal ini menunjukkan bahwa kandungan senyawa kimia yang terdapat dalam ekstrak etanolik daun jati belanda lebih banyak terlarut dalam pelarut etanol daripada pelarut air. Hasil ini dapat memberikan manfaat bagi peneliti selanjutnya untuk memilih menggunakan pelarut etanol bila akan mengisolasi kandungan senyawa kimia dalam ekstrak daun jati belanda.
M.Uji Kandungan Kimia Senyawa Identitas Ekstrak Etanolik Daun Jati Belanda Secara Kualitatif dan Kuantitatif
Uji kandungan kimia senyawa identitas ekstrak etanolik daun jati belanda yang dilakukan berupa analisis kualitatif menggunakan metode Kromatografi Lapis Tipis dan analisis kuantitatif menggunakan instrumen TLC Scanner (KLT Densitometer).
kualitatif ini dilakukan dengan pengamatan nilai Rf dan warna bercak sampel yang dibandingkan dengan standar friedelin-3β-ol. Fase diam yang digunakan adalah silika gel GF254 karena diketahui sampel yang akan dirambatkan tidak berfluoresensi pada panjang gelombang 254 nm, sehingga bila dilihat di bawah sinar UV dengan panjang gelombang 254 nm silika gel akan berfluoresensi dengan warna hijau kebiruan dan kromatogram sampel dan standar akan berwarna gelap. Hal ini disebabkan karena bercak hasil elusi meredam fluoresensi yang terjadi pada silika gel GF254 sehingga warnanya menjadi lebih gelap dari sekitarnya. Sedangkan pada panjang gelombang 365 nm, silika berwarna ungu dan bercak standar serta sampel akan berpendar. Pada panjang gelombang ini, silika tidak berfluoresensi sehingga berwarna ungu, sedangkan bercak ekstrak etanolik daun jati belanda dan standar mengalami fluoresensi.
terendam oleh fase gerak yang terdapat di dalam bejana. Fase gerak yang digunakan dalam penelitian adalah heksan : etil asetat ( 3 : 2 v/v). Kemudian pengembangan dilakukan hingga mencapai batas 10,0 cm dari batas awal penotolan. Selanjutnya kromatogram dikeluarkan dari bejana dan dikeringkan untuk menguapkan fase gerak yang masih terdapat pada plat KLT kemudian dideteksi di bawah lampu UV 254 nm dan 365 nm.
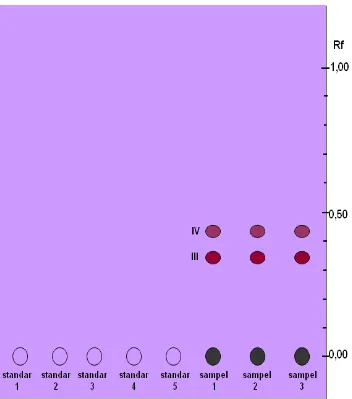
Deteksi di bawah lampu UV 254 nm dapat dilihat pada gambar berikut.
Gambar 3. Kromatogram larutan standar friedelin-3β-ol dan sampel ekstrak
Keterangan :
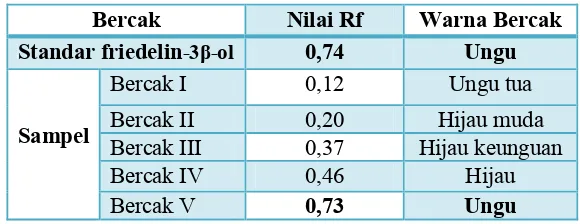
Dari Gambar 3 tampak bercak standar friedelin-3β-ol meredam fluoresensi berwarna ungu, sedangkan bercak sampel ekstrak etanolik daun jati belanda pada ketiga replikasi menunjukkan pemisahan 5 bercak dengan nilai Rf dan warna yang berbeda-beda. Nilai Rf dan warna tersebut ditampilkan pada tabel berikut.
Tabel I. Hasil KLT standar friedelin-3β-ol dan sampel ekstrak
etanolik daun jati belanda pada deteksi lampu UV 254 nm
Bercak Nilai Rf Warna Bercak Standar friedelin-3β-ol 0,74 Ungu
Sampel
Bercak I 0,12 Ungu tua
Bercak II 0,20 Hijau muda Bercak III 0,37 Hijau keunguan
Bercak IV 0,46 Hijau
Bercak V 0,73 Ungu
Dari tabel I dapat dilihat bahwa bercak sampel ekstrak etanolik daun jati belanda pada pemisahan kelima (bercak V) memiliki nilai Rf yang mendekati dan warna bercak yang sama dengan bercak standar senyawa identitas friedelin-3β-ol.
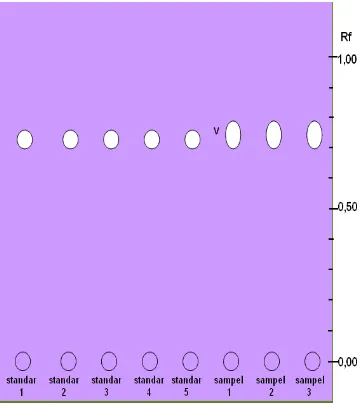
Gambar 4. Kromatogram larutan standar friedelin-3β-ol dan sampel ekstrak
etanolik daun jati belanda pada deteksi lampu UV λ 365 nm
Keterangan :
Fase gerak : heksan : etil asetat (3:2) Fase diam : silika gel GF254
Bercak tersebut kemudian diperjelas dengan melakukan penyemprotan dengan pereaksi antimon (III) klorida. Pereaksi yang lebih dikenal sebagai pereaksi Carr Price ini merupakan pereaksi yang digunakan untuk mendeteksi glikosida, saponin dan terpenoid. Senyawa identitas friedelin-3β-ol termasuk
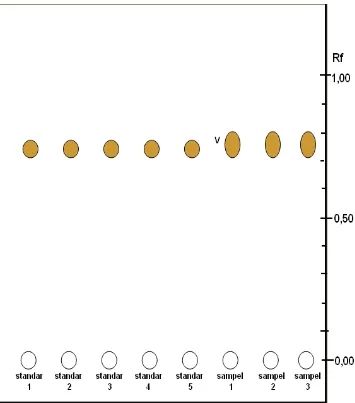
dalam golongan triterpenoid maka dapat dideteksi dengan pereaksi tersebut. Plat lalu dipanaskan selama 6 menit pada suhu 100oC. Tujuan pemanasan plat KLT adalah untuk mempercepat reaksi kimia yang terjadi antara bercak dan larutan penyemprot sehingga menghasilkan warna. Setelah pemanasan plat KLT diperoleh bercak standar dan sampel bercak kelima berwarna coklat sangat muda ketika dilihat dengan sinar visibel atau tanpa menggunakan lampu UV(Gambar 5) dan berpendar putih di bawah sinar UV 365 nm (Gambar 6).
Gambar 5. Kromatogram larutan standar friedelin-3β-ol dan sampel ekstrak
etanolik daun jati belanda setelah disemprot pereaksi antimon (III) kloridapada
deteksi sinar tampak
Keterangan :
Fase gerak : heksan : etil asetat (3:2) Fase diam : silika gel GF254
Gambar 6. Kromatogram larutan standar friedelin-3β-ol dan sampel ekstrak etanolik daun jati belanda setelah disemprot pereaksi antimon (III) klorida pada
deteksi lampu UV λ 365 nm
Keterangan :
Fase gerak : heksan : etil asetat (3:2) Fase diam : silika gel GF254
2. Analisis kuantitatif senyawa identitas friedelin-3β-ol dengan KLT- densitometer
Analisa kuantitatif bertujuan untuk memberikan gambaran kadar kandungan senyawa identitas friedelin-3β-ol di dalam sampel ekstrak etanolik
daun jati belanda. Analisis dilakukan dengan menghitung kadar sampel menggunakan persamaan kurva baku friedelin-3β-ol dan nilai AUC (luas daerah
di bawah kurva) pada kromatogram masing-masing replikasi sampel yang diperoleh melalui pengukuran dengan KLT-densitometer.
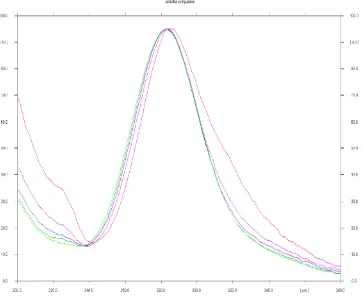
a.Penentuan panjang gelombang maksimum
Gambar 7. Spektra penelusuran panjang gelombang maksimum standar
friedelin-3β-ol pada λ 200 nm – 380 nm
b.Pembuatan kurva baku
tersebut adalah luas daerah di bawah kurva. Nilai AUC yang diperoleh untuk masing-masing konsentrasi standar terdapat pada tabel II.
Tabel II. Data pembuatan kurva baku friedelin-3β-ol
Standar Konsentrasi
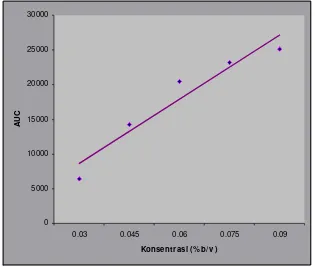
Dengan membuat kurva hubungan konsentrasi standar friedelin-3β-ol
yang ditotolkan (x) dan luas area di bawah kurva (y), maka diperoleh persamaan garis lurus y = bx + a yang dapat digunakan untuk menghitung kadar senyawa identitas friedelin-3β-ol dalam sampel ekstrak etanolik daun jati belanda.
peningkatan konsentrasi standar friedelin-3β-ol terjadi pula peningkatan luas
0.03 0.045 0.06 0.075 0.09
Konsentrasi (% b/v )
AU
C
Gambar 8. Kurva baku hubungan konsentrasi standar friedelin-3β-ol Vs AUC
Keterangan
Instrumen : TLC Scanner Fase diam : Silika gel GF254
Fase gerak : heksan : etil asetat (3:2)
Detektor : UV 283 nm
c.Penetapan kadar friedelin-3β-ol dalam sampel dengan KLT- densitometer
Sejumlah larutan sampel (μl) replikasi I, II, dan III yang telah diketahui
konsentrasinya ditotolkan pada lempeng yang sama, kemudian dikembangkan pada fase gerak heksan : etil asetat ( 3 : 2 v/v ). Keberhasilan metode densitometri sangat dipengaruhi keberhasilan teknik pemisahannya. Karena itu dipilih fase gerak yang sesuai agar terjadi pemisahan ekstrak etanolik daun jati belanda yang baik menjadi komponen-komponennya. Hasil yang didapat setelah pemisahan adalah bercak sampel terdiri atas lima bercak. Bercak paling atas (bercak V) memiliki warna yang sama dan nilai Rf yang mendekati dengan nilai Rf standar friedelin -3β-ol. Bercak inilah yang kemudian diukur intensitasnya dengan TLC Scanner sehingga diperoleh nilai AUC. Selanjutnya kadar friedelin-3β-ol dalam sampel dapat dihitung menggunakan persamaan kurva baku yang telah diperoleh sebelumnya.
Perhitungan kadar senyawa identitas friedelin-3β-ol dalam ekstrak etanolik daun jati belanda secara lengkap termasuk konversinya dari persentase b/v menjadi persentase b/b dapat dilihat pada lampiran 10.
Dari penelitian diperoleh kadar senyawa identitas friedelin-3β-ol dalam
sampel ekstrak etanolik daun jati belanda seperti pada tabel berikut.
Tabel III. Kadar senyawa identitas friedelin-3β-ol dalam sampel ekstrak etanolik
daun jati belanda
Sampel AUC Kadar (% b/v)
Replikasi I 8.025, 9 0,028 Replikasi II 7.309,7 0,026 Replikasi III 7.306,6 0,026
55 BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
Dari hasil penelitian yang telah dilakukan dapat diambil kesimpulan, yaitu: karakter ekstrak etanolik daun jati belanda adalah organoleptis ekstrak berbentuk kental, berwarna coklat tua kehitaman, tidak berbau, dan rasa agak kelat, kadar air 17,67 % b/b, kadar abu total 1,77 % b/b, kadar abu larut air 4,47 % b/b, kadar abu tidak larut asam 1,37 % b/b, kadar sari larut air 25,83 % b/b, kadar sari larut etanol 39,71 % b/b, dan rata-rata kadar senyawa identitas friedelin-3β-ol dalam sampel ekstrak etanolik daun jati belanda adalah (0,027 ± 1,15 x 10-3) % b/v.
B. Saran
DAFTAR PUSTAKA
Anonim, 1977, Materia Medika, jilid I, xx, 136-137, Departemen Kesehatan Republik Indonesia, Jakarta
Anonim, 1978, Materia Medika, jilid II, 42-47, Departemen Kesehatan Republik Indonesia, Jakarta
Anonim, 1986, Sediaan Galenik, 2-40, Departemen Kesehatan Republik Indonesia, Jakarta
Anonim, 1995, Materia Medika, jilid VI, 313, Departemen Kesehatan Republik Indonesia, Jakarta
Anonim, 2000, Parameter Standar Umum Ekstrak Tumbuhan Obat, cetakan pertama, Badan Pengawas Obat dan Makanan Republik Indonesia, Jakarta Anonim, 2004 a, Monografi Ekstrak Tumbuhan Obat Indonesia, Volume I, 29-31,
Badan Pengawas Obat dan Makanan Republik Indonesia, Jakarta
Anonim, 2004 b, Mutamba (Guazuma ulmifolia) Monograph, Raintree Nutrition, Inc. Carson City, Nevada
Anonim, 2005 a, Peraturan Kepala Badan Pengawas Obat dan makanan Republik Indonesia No. HK.00.05.4.1380 tentang Pedoman Cara Pembuatan Obat Tradisional Yang Baik, Badan Pengawas Obat dan Makanan Republik Indonesia, Jakarta
Anonim, 2005 b, Standarisasi Ekstrak Tumbuhan Obat Indonesia, Salah Satu Tahapan Penting Dalam Pengembangan Obat Asli Indonesia, Info POM, Vol. 6, No.4, Jakarta
Backer, C.A., and Backhuizen van den Brink, R. C., 1963, Flora Of Java, Vol I, 3-7, 402-404, 408, N.V.P Noordhoff-Groningen-The Netherlands
Farida dan Monica, W.S., 2000, Pengaruh Ekstrak Daun Jati Belanda (Guazuma ulmifolia Lamk.) terhadap Penurunan Kadar Kolesterol Kelinci, Warta Tumbuhan Obat Indonesia, Vol.6, No.2, 12-13
Joshita, D., Azizahwati, Wahyuditomo, 2000, Pengaruh Daun Jati Belanda terhadap Kerja Enzim Lipase secara In Vitro, Warta Tumbuhan Obat Indonesia, Vol.6, No.2, 6-8
Gritter, R.J., Bobbitt, J.M., and Schwarting, A.E., 1985, Introduction to
Chromatography, diterjemahkan oleh Kosasih Padmawinata, Edisi II, ITB, Bandung
Mintarsih, 1990, E. R. R., Penetapan Kadar Alkaloid Kinina dalam Akar, Batang, dan Daun Chinchona Succirubra Pavon et Klotzsch dari Daerah Kaliurang secara Spektrodensitometri (TLC-scanner), Skripsi, Fakultas Farmasi, UGM, Yogyakarta.
Noegrohati, S., 1994, Pengantar Kromatografi, dalam Noegrohati, S. dan Narsito, (Eds.), Risalah Prinsip dan Aplikasi Beberapa Teknik Analisis Instrumental, Laboratorium Analisis Kimia dan Fisika Pusat UGM, Yogyakarta
Nurwati, 1984, Pengaruh Daun Jati Belanda terhadap Berat Badan dan Gambaran Hematologik Darah Tikus Betina Serta Identifikasi Komponen Lendirnya, Skripsi, Fakultas Farmasi UGM, Yogyakarta
Pramono, S.,Nurwati, S., Sugiyanto, 2000, Pengaruh Lendir Daun Jati Belanda (Guazuma ulmifolia Lamk.) terhadap Bobot Tikus Putih Betina, Warta Tumbuhan Obat Indonesia, Vol.6, No.2, 14-15
Rahardjo S.S., Ngatijan, Pramono, S., 2005, Aktivitas Lipase Pankreas Rattus Norvegicus Akibat Pemberian Ekstrak Etanol Daun Jati Belanda(Guazuma ulmifolia Lamk.), Berkala Ilmu Kedokteran, Vol.38, No.1, 15-23
Sinambela, 2002, Standarisasi Sediaan Obat Herba,Seminar Nasional Tumbuhan Obat Indonesia XXII, Fakultas Farmasi Universitas Muhammadiyah, Purwokerto
Suharmiati dan Maryani, 2003, Khasiat dan Manfaat Jati Belanda Si Pelangsing dan Peluruh Kolesterol, 8, 21-24, PT. Agromedia, Jakarta
Sulaksana, J., dan Jayusman, D. I., 2005, Kemuning dan Jati Belanda, 18, Penebar Swadaya, Jakarta
Supardjan, A. M., 1987, Pemisahan Tetrasiklin dan Hasil Pemisahannya dalam Sediaan Tetrasiklin secara KLT-densitometri, Lembaga Penelitian, UGM, Yogyakarta
Syamsuhidayat S.S., dan Hutapea J.R., 1991, Inventaris Tanaman Obat Indonesia, Jilid I, Departemen Kesehatan Republik Indonesia, Badan Penelitian dan Pengembangan Kesehatan, Jakarta
Wijayanti, 2007, Pengaruh Pemberian Infusa Daun Jati Belanda (Guazuma ulmifolia Lamk.) terhadap Kadar Trigliserida dalam Plasma Tikus Putih Jantan Galur Wistar, Skripsi, Fakultas Farmasi Universitas Sanata Dharma, Yogyakarta
Wulandari, R., 1996, Ekstraksi dan Identifikasi secara Kromatografi Lapis Tipis (KLT) dan Spektrofotometer UV Senyawa Alkaloid Tumbuhan Jati Belanda (Guazuma ulmifolia Lamk.), Skripsi, Fakultas Farmasi UGM, Yogyakarta Yeniwati, 1984, Pengaruh Jamu Galian Singset dan Daun Jati Belanda terhadap
Kunci determinasinya adalah sebagai berikut.
1b, 2b, 3b, 12b, 13b, 14b, 17b, 18b, 19b, 20b, 21b, 22b, 23b, 24b, 25b, 26b, 27b, 28b, 29b, 30b, 31a, 32a, 33a, 34a, 35a, 36d, 37b, 38b, 39b, 41b, 42b, 44b, 45b, 46e,50a………...94(Sterculiaceae) 1b, 6b, 10b, 12b, 15b, 171, 18b………....….10(Guazuma ulmifolia Lamk.)
Lampiran 2 : Data Pengentalan Ekstrak Cair
Vacuum Rotary Evaporator Ekstrak etanolik daun jati belanda (Guazuma ulmifolia
Tekanan untuk menguapkan air (mbar)
Hasil ekstrak kental (g)
Replikasi I 25,6
Replikasi II 24,8
Replkasi III 26,2
Total ekstrak kental 76,6
- Perhitungan rendemen = BeratEkstrakKentalYangDiperoleh 100%
- Total berat ekstrak kental Replikasi I = 12, 8 g + 13,4 g = 26,2 g
- Perhitungan rendemen = BeratEkstrakKentalYangDiperoleh 100% BeratSerbukAwal ×
Rendemen replikasi III = 26, 2 100% 24, 95% 105
g
g × =
Rata – rata rendemen ketiga replikasi = 24, 38% 23, 62% 24,95% 24, 32% 3
+ + =
0, 67 SD=
0, 67
100% 100% 2, 75%
24,32 SD
CV x
Lampiran 3 : Data Identitas dan Organoleptik Ekstrak
A. Identitas Ekstrak 3. Deskripsi tata nama
a. Nama ekstrak : Ekstrak Etanolik Daun Jati Belanda (Extractum Guazumae
ulmifoliae Folii Spissum)
b. Nama latin tanaman : Guazuma ulmifolia Lamk. c. Bagian tanaman yang digunakan : daun
d. Nama Indonesia tanaman : jati belanda 2. Senyawa identitas ekstrak : friedelin-3β-ol
B. Organoleptik Ekstrak
Identifikasi Ekstrak Cair Ekstrak Kental Warna Hijau tua Coklat tua kehitaman
Bau Khas etanol Tidak berbau
Rasa Agak kelat Agak kelat
Lampiran 4: Perhitungan Penetapan Kadar Air
Uraian Replikasi I (g) II (g) III (g)
Berat krus 51,3502 49,1153 49,7381
Berat krus + ekstrak kental
53,3507 51,1155 51,7385
Berat ekstrak kental awal
2,0005 2,0002 2,0004
Berat krus + ekstrak kering
52,9994 50,7593 51,3859
Berat ekstrak kering (oven 105oC, 5 jam sampai bobot tetap)
1,6492 1,6440 1,6478
Lampiran 5 : Perhitungan Penetapan Kadar Abu Total
Uraian I (g) II (g) III (g)
Berat krus awal 51,3502 49,1153 49,7381 Berat krus + ekstrak
kental
53,3507 51,1155 51,7385
Berat ekstrak kental 2,0005 2,0002 2,0004 Berat krus + abu
konstan
51,3862 49,1502 49,7738
Berat abu konstan 0,0360 0,0349 0,0357