BAB II
TINJAUAN PUSTAKA 2.1 Uraian Bahan
2.1.1 Kloramfenikol
Menurut Ditjen POM (1995), Rumus struktur :
Gambar 2.1 Struktur Kloramfenikol.
Nama Kimia : D-treo-(-)-2,2-Dikloro-N-[β-hidroksi-α -(hidroksimetil)-p-nitrofenetil]asetamida
Rumus Molekul : C11H12Cl2N2O5 Berat Molekul : 323,13
Pemerian : Hablur halus berbentuk jarum atau lempeng memanjang; putih hingga putih kelabu atau putih kekuningan;larutan
praktis netral terhadap lakmus P; stabil dalam larutan netral atau larutan agak asam
Kelarutan : Sukar larut dalam air; mudah larut dalam etanol, dalam propilenglikol, dalam aseton, dan dalam etil asetat.
Kloramfenikol mempunyai efek samping umum berupa gangguan lambung-usus, neuropati optis, radang lidah dan mukosa mulut. Tetapi yang sangat berbahaya adalah depresi sumsum tulang (myelodepresi) yang dapat berwujud dua bentuk anemia (Tan dan Rahardja, 2007).
2.1.2 Prednisolon
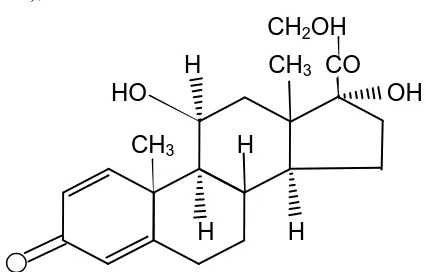
Menurut Ditjen POM (1995), Rumus struktur : CH2OH
H CH3 CO
HO OH
CH3 H
H H
Gambar 2.2 Struktur Prednisolon
Nama Kimia : 11β,17,21-Trihidroksipregna-1,4-diena-3,20-dion[50-24-8] Rumus Molekul : C21H28O5
Berat Molekul : 360,45
Pemerian : Serbuk hablur, putih sampai praktis putih; tidak berbau. Kelarutan : Sangat sukar larut dalam air; larut dalam metanol dan dalam
dioksan; sukar larut dalam kloroform.
Efek samping dari prenisolon jika penggunaanya dilakukan jangka panjang menyebabkan hipokalemia, tukak lambung, penekanan pertumbuhan, osteoporosis, muka bulat, penekanan sekresi kortikotropin, atropi kulit, memperberat penyakit diabetes melitus, mudah terkena infeksi, glaukoma, hipertensi, gangguan menstruasi, dan perubahan mental atau tingkah laku (Siswandono dan Soekardjo, 2000).
Saat ini, sangat banyak beredar produk obat yang mengandung kombinasi dua atau lebih bahan aktif. Kombinasi dimaksudkan agar obat dapat lebih efektif mencapai sasaran terapi. Salah satunya adalah kombinasi antara kloramfenikol dan prednisolon, yang digunakan untuk meringankan efek antiradang seperti dermatologis yang berat dan sebagai antibiotik.
2.2. Spektrofotometri
Spektrofotometer adalah alat untuk mengukur transmitan atau serapan suatu sampel sebagai fungsi panjang gelombang. Spektrofotometer merupakan penggabungan dari dua fungsi alat yang terdiri dari spektrometer yang menghasilkan sinar dari spektrum dengan panjang gelombang tertentu dan fotometer sebagai alat pengukur intensitas cahaya yang ditransmisikan atau yang diabsorpsi. Ketika cahaya (monokromatik atau heterogen) mengenai medium homogen, suatu bagian dari cahaya yang ada akan dipantulkan, sebagian diserap medium, dan sisanya ditransmisikan atau diteruskan (Day dan Underwood, 1998).
Bagian molekul yang bertanggung jawab terhadap penyerapan cahaya disebut kromofor dan terdiri atas ikatan rangkap dua atau rangkap tiga, terutama jika ikatan rangkap tersebut terkonjugasi. Semakin panjang ikatan rangkap dua atau rangkap tiga terkonjugasi di dalam molekul, molekul tersebut akan lebih mudah menyerap cahaya (Cairns, 2008).
Gugus fungsi seperti –OH, -O, -NH2 dan –OCH3 yang memberikan transisi n → π* disebut gugus auksokrom. Gugus ini adalah gugus yang tidak dapat menyerap radiasi ultraviolet-sinar tampak, tetapi apabila gugus ini terikat pada gugus kromofor mengakibatkan pergeseran panjang gelombang ke arah yang lebih besar atau pergeseran batokromik (Gandjar dan Rohman, 2007). Efek hipsokromik atau pergeseran biru adalah pergeseran absorban ke daerah panjang gelombang yang lebih pendek karena adanya substitusiatau efek pelarut. Efek hipokromik adalah efek yang menyebabkan penurunan intensitas absorban (Dachriyanus, 2004).
Radiasi ultraviolet diabsorpsi oleh molekul organik aromatik, molekul yang mengandung elektron-π terkonjugasi atau atom yang mengandung elektron -n, menyebabkan transisi elektron di orbit terluarnya dari tingkat energi elektron dasar ke tingkat energi tereksitasi lebih tinggi. Besarnya absorbansi radiasi tersebut berbanding dengan banyaknya molekul analit yang mengabsorpsi dan dapat digunakan untuk analisis kuantitatif (Satiadarma, dkk., 2004)
2.2.1. Hukum Lambert-Beer
Lambert-Beer, sehingga diperoleh bahwa serapan berbanding lurus terhadap konsentrasi dan ketebalan sel, hukum Lambert-Beer menyatakan bahwa intensitas yang diteruskan oleh larutan zat penyerap berbanding lurus dengan tebal dan konsentrasi larutan (Gandjar dan Rohman, 2007).
Hukum Lambert-Beer umumnya dikenal dengan persamaan sebagai berikut:
A = abc
Keterangan: A = absorbansi a = absorptivitas b = tebal kuvet (cm) c = konsentrasi
Absorptivitas (a) merupakan suatu konstanta yang tidak tergantung pada konsentrasi, tebal kuvet dan intensitas radiasi yang mengenai larutan sampel. Absorptivitas tergantung pada suhu, pelarut, struktur molekul dan panjang gelombang radiasi (Gandjar dan Rohman, 2007).
2.2.2. Komponen Spektrofotometer
Menurut Day dan Underwood (1998), unsur - unsur terpenting suatu spektrofotometer adalah sebagai berikut:
b. Monokromotor: digunakan untuk memperoleh sumber sinar yang monokromatis. Alatnya berupa prisma untuk mengarahkan sinar monokromatis yang diinginkan dari hasil penguraian.
c. Kuvet (sel): digunakan sebagai wadah sampel untuk menaruh cairan ke dalam berkas cahaya spektrofotometer. Kuvet itu haruslah meneruskan energi radiasi dalam daerah spektrum yang diinginkan. Pada pengukuran di daerah sinar tampak, kuvet dapat digunakan, tetapi untuk pengukuran pada daerah ultraviolet kita harus menggunakan sel kuarsa karena gelas tidak tembus cahaya pada daerah ini. Kuvet tampak dan ultraviolet yang khas mempunyai ketebalan 1 cm.
d. Detektor: Peranan detektor penerima adalah memberikan respon terhadap cahaya pada berbagai panjang gelombang.
2.2.3. Kegunaan Spektofotometri
Kegunaan spektrofotometri ultraviolet dalam analisis kualitatif sangat terbatas karena rentang daerah radiasi yang relatif sempit hanya dapat mengakomodasi sedikit sekali puncak absorpsi maksimum dan minimum, karena itu identifikasi senyawa yang tidak diketahui tidak memungkinkan untuk dilakukan (Satiadarma, dkk., 2004).
Spektrofotometri derivatif menawarkan berbagai keuntungan. Pertama pada spektra derivatif ditekankan gambaran ini lebih jelas bila meningkat dari spektra derivatif peringkat pertama hingga ke peringkat keempat (Munson, 1984).
(Cairns, 2008), dimana konsentrasi zat dalam sampel dihitung dengan rumus sebagai berikut:
Cs
Ct
As
At
=
Keterangan: As = absorbansi baku pembanding At = absorbansi zat dalam sampel Cs = konsentrasi baku pembanding Ct = konsentrasi zat dalam sampel
Penentuan kadar senyawa organik yang mempunyai struktur kromofor atau mengandung gugus kromofor, serta mengabsorpsi radiasi ultraviolet penggunaanya cukup luas (Satiadarma, dkk., 2004).
2.3. Spektrofotometri Derivatif
Konsep derivatif telah diperkenalkan pertama kali pada tahun 1950, dimana terlihat memberikan banyak keuntungan. Aplikasi utama spektrofotometri derivatif ultraviolet–visibel adalah untuk identifikasi kualitatif dan analisis senyawa dalam sampel. Metode spektrofotometri derivatif sangat cocok untuk analisis pita absorpsi yang overlapping atau tumpang tindih (Owen, 1995).
Spektrum derivatif diperoleh dengan membuat absorban atau transmitan derivatif orde pertama atau orde lebih tinggi yang terkait dengan panjang gelombang (ΔA / Δλ) sebagai fungsi dari panjang gelombang. Spektrum dapat
dilakukan dengan men-scan monokromator yang terpasang pada panjang gelombang tetap, tetapi dengan perbedaan panjang gelombang yang sedikit, sehingga berguna jika analit adalah dua komponen yang mengabsorpsi radiasi pada sisi pita absorpsi dari komponen yang mengganggu (Satiadarma, dkk., 2004).
Jika kita berasumsi bahwa spektrum orde-nol memenuhi hukum Beer, maka ada hubungan linear yang sama antara konsentrasi dan amplitudo untuk semua turunan:
Orde nol Orde pertama
Orde ke-n
Keterangan: λ = panjang gelombang A = absorbansi
ε = absorptivitas
b = tebal kuvet
c = konsentrasi sampel
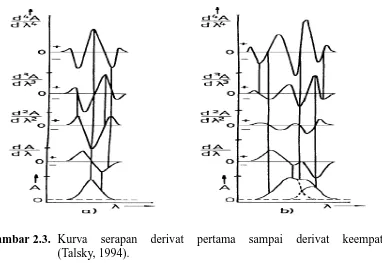
Kurva serapan derivat pertama sampai derivat keempat dapat dilihat pada Gambar 2.3.
Gambar 2.3. Kurva serapan derivat pertama sampai derivat keempat (Talsky, 1994).
Ada tiga aplikasi spektrofotometri derivatif yang sering digunakan dalam anlisa kuantitatif antara lain metode zero crossing, metode peak to peak dan metode multivariate spectrophotometric calibration (Talsky, 1994).
Panjang gelombang zero crossing adalah panjang gelombang dimana senyawa tersebut mempunyai serapan nol dan menjadi panjang gelombang analisis untuk zat lain dalam campurannya. Metode zero crossing memisahkan campuran dari spektrum derivatifnya pada saat panjang gelombang komponen pertama tidak ada sinyal (Nurhidayati, 2007).
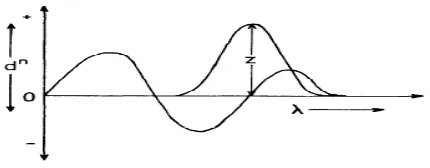
Bila campuran analit memiliki panjang gelombang zero-crossing lebih dari satu, maka yang dipilih untuk dijadikan panjang gelombang analisis adalah panjang gelombang zero crossing yang serapan pasangannya dan campurannya persis sama, karena pada panjang gelombang tersebut dapat secara selektif mengukur serapan senyawa pasangannya dan memiliki serapan yang paling besar. Pada serapan yang paling besar, serapannya lebih stabil sehingga kesalahan analisis dapat diperkecil (Nurhidayati, 2007). Kurva sederhana aplikasi zero crossing dapat dilihat pada Gambar 2.4.
Gambar 2.4. Kurva sederhana aplikasi zero crossing (Talsky, 1994).
Metode spektrofotometri derivatif atau metode kurva turunan adalah salah satu metode spektrofotometri yang dapat digunakan untuk analisis campuran beberapa zat secara langsung tanpa harus melakukan pemisahan terlebih dahulu meskipun dengan panjang gelombang yang berdekatan (Nurhidayati, 2007).
Beberapa keuntungan dari spektrofotometri derivatif antara lain yaitu spektrum derivatif memberikan gambaran struktur yang terinci dari spektrum serapan dan gambaran ini makin jelas dari spektum derivatif pertama ke derivatif keempat (Munson, 1984).
biaya operasionalnya lebih murah dan waktu analisisnya lebih cepat (Nurhidayati, 2007).
2.4. Validasi Metode Analisis
Tujuan utama yang harus dicapai dari suatu kegiatan analisis kimia adalah dihasilkannya data hasil uji yang absah (valid). Secara sederhana hasil uji yang absah dapat digambarkan sebagai hasil uji yang mempunyai akurasi (accuracy) dan presisi (precission) yang baik. Validasi adalah suatu tindakan penilaian terhadap parameter tertentu pada prosedur penetapan yang dipakai untuk membuktikan bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya (Harmita, 2004).
Validasi metode analisis dilakukan dengan uji laboratorium, dengan demikian dapat ditunjukkan bahwa karakteristik kinerjanya telah memenuhi persyaratan untuk diterapkan dalam analisis senyawa atau sediaan yang bersangkutan. Parameter analisis yang ditentukan pada validasi adalah akurasi, presisi, limit deteksi, limit kuantitasi, kelinieran dan rentang (Satiadarma, dkk., 2004).
2.4.1. Akurasi
Dalam metode simulasi, sejumlah analit bahan murni (senyawa pembanding kimia) ditambahkan kedalam campuran bahan sediaan farmasi (plasebo), lalu campuran tersebut dianalisis dan hasilnya dibandingkan dengan kadar standar yang ditambahkan atau kadar sebenarnya. Jika plasebo tidak memungkinkan untuk disiapkan, maka sejumlah analit yang telah diketahui konsentrasinya dapat ditambahkan langsung ke dalam sediaan farmasi. Ini dinamakan metode penambahan baku standar (Harmita, 2004).
Menurut Harmita (2004) dalam metode adisi (penambahan bahan baku), sejumlah sampel yang dianalisis ditambah analit dengan konsentrasi biasanya 98% sampai 102% dari kadar analit yang diperkirakan, dicampur dan dianalisis kembali. Selisih kedua hasil dibandingkan dengan kadar yang sebenarnya. Dalam kedua metode tersebut, persen perolehan kembali dinyatakan sebagai rasio antara hasil yang diperoleh dengan hasil yang sebenarnya:
Keterangan: CF = kadar zat dalam sampel setelah penambahan larutan baku
CA = kadar zat dalam sampel sebelum penambahan larutan baku C A * = kadar larutan baku zat yang ditambahkan
2.4.2. Presisi
Parameter-parameter seperti simpangan baku (SB), simpangan baku relatif (Relative Standard Deviation) dan derajat kepercayaan haruslah dikalkulasi untuk mendapatkan tingkat presisi tertentu (Ermer dan Miller, 2005). Nilai standar deviasi relatif (RSD) dinyatakan memenuhi persyaratan jika < 2% (Gandjar dan Rohman, 2007).
Standar deviasi relatif = ×100% X
SB
2.4.3. Batas Deteksi dan Batas Kuantitasi
Batas deteksi adalah nilai parameter, yaitu konsentrasi analit terendah yang dapat dideteksi yang masih memberikan respon signifikan dibandingkan dengan blanko (Harmita, 2004).
Batas deteksi merupakan batas uji yang secara spesifik menyatakan apakah analit yang dianalisis berada di atas atau di bawah nilai tertentu (Gandjar dan Rohman, 2007). Batas deteksi dapat dihitung dengan rumus sebagai berikut (Harmita, 2004):
Menurut Harmita (2004), batas kuantitasi adalah jumlah analit terkecil dalam sampel yang masih dapat diukur dalam kondisi percobaan yang sama dan memenuhi kriteria cermat dan seksama.
LOQ =
slope
2.4.4. Linearitas
Linieritas merupakan kemampuan suatu metoda untuk memperoleh hasil-hasil uji yang secara langsung proporsional dengan konsentrasi analit pada kisaran yang diberikan. Linieritas suatu metode merupakan ukuran seberapa baik kurva kalibrasi yang menghubungkan antara respon (y) dengan konsentrasi (x). Data yang diperoleh selanjutnya diproses dengan metode kuadrat terkecil, untuk selanjutnya dapat ditentukan nilai kemiringan (slope), intersep, dan koefisien korelasinya (Gandjar dan Rohman, 2007).
Kelinieran suatu metode analisis adalah kemampuan untuk menunjukkan bahwa nilai hasil uji langsung atau setelah diolah secara matematika, proporsional dengan konsentrasi analit dalam sampel dalam batas rentang konsentrasi tertentu (Satiadarma, dkk., 2004).
2.4.5. Rentang