21
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
Uraian tumbuhan meliputi sistematika tumbuhan, nama daerah, nama asing, morfologi tumbuhan dan khasiat tumbuhan.
2.1.1 Sistematika tumbuhan
Sistematika tumbuhan poguntano adalah sebagai berikut (Anonim, 2009): Kingdom : Plantae
Divisi : Spermatophyta Subdivisi : Angiospermae Kelas : Dicotyledonae Subkelas : Asteridae Ordo : Scrophulariales Famili : Scrophulariaceae Genus : Picria
Spesies : Picria fel-terrae Lour.
Sinonim : Curanga amara Vahl., Curanga amara Juss., Curania amara R&S., Gratiola amara Roxb., Curanga fel-terrae Lour., dan Torenia cardiosepala Benth.
2.1.2 Nama daerah
Nama daerah dari tumbuhan ini adalah poguntano, pugun tana, pogon tanoh (Dairi), tamah daun kukurang, raheut (Sunda), (Maluku) dan papaita (Ternate) (Anonim, 2009).
22
2.1.3 Nama asing
Pada beberapa negara lain tumbuhan ini dikenal dengan nama hempedu tanah, gelumak susu, rumput kerak nasi (Malaysia), sagai-uak (Filipina), kong sadden (Laos) dan thanh (Vietnam) (Anonim, 2007).
2.1.4 Morfologi tumbuhan
Herba tahunan, tinggi lebih dari 40 cm, batang dengan cabang yang jarang, tegak atau melata, segiempat, berakar di buku-buku, berbulu halus yang padat. Daun tunggal berhadapan, bundar telur, pangkal daun membaji sampai membundar, ujung daun agak melancip, tepi daun beringgitan, berbulu halus. Pembungaan berupa tandan di ujung atau di batang, jumlah bunga 2-16, daun gagang kecil, melanset, mahkota bunga menabung, berbibir rangkap, gundul bagian luar, bagian dalam ada kelenjar bulu, bibir atas berwarna coklat kemerah-merahan, bibir bagian bawah berwarna putih. Buah kapsul lonjong, padat, berkatup dua, dengan beberapa biji. Biji membulat, diameter sekitar 0,6 mm (Anonim, 2009).
2.1.5 Khasiat tumbuhan
Tumbuhan ini digunakan sebagai obat pencahar, mengobati kolik (mulas mendadak dan hebat), malaria, diuretik, demam, amenorrhea dan gangguan pada kulit (Perry, 1980). Di Cina Selatan puguntano digunakan untuk pengobatan demam, infeksi herpes, kanker dan inflamasi (Zhong, et al., 1979).
2.2 Ekstraksi
Ekstraksi adalah kegiatan penarikan kandungan kimia yang dapat larut sehingga terpisah dari bahan yang tidak dapat larut dari pelarut cair. Simplisia yang diekstraksi mengandung senyawa aktif yang dapat larut. Ada beberapa
23
metode yang umum digunakan, diantaranya maserasi, perkolasi, sokletasi dan refluks. Salah satu metode yang banyak digunakan adalah maserasi.
2.2.1 Maserasi
Maserasi digunakan untuk penyarian simplisia yang bersifat lunak seperti daun dan bunga tetapi banyak juga yang menggunakan metode ini untuk menyari simplisia yang keras seperti akar dan korteks karena cara pengerjaan dan peralatan yang digunakan sederhana dan mudah diperoleh. Pada penyarian dengan cara maserasi perlu dilakukan pengadukan untuk menghomogenkan konsentrasi larutan di luar serbuk simplisia, sehingga dengan pengadukan tersebut tetap terjaga adanya derajat perbedaan kosentrasi yang sekecil-kecilnya antara larutan di dalam sel dengan larutan di luar sel.
Maserasi adalah proses penyarian simplisia dengan menggunakan pelarut melalui beberapa kali pengocokan atau pengadukan pada temperatur ruangan. Cairan penyari akan menembus dinding sel simplisia dan akan masuk ke dalam rongga sel yang mengandung zat aktif. Zat aktif akan larut karena adanya perbedaan konsentrasi antara larutan zat aktif di dalam sel dengan di luar sel, sehingga larutan yang terpekat didesak ke luar. Peristiwa tersebut terjadi secara berulang sehingga terjadi keseimbangan konsentrasi antara larutan di luar sel dan di dalam sel.
Maserasi dapat dilakukan dengan cara menurut Farmakope Indonesia Edisi III (1979):
Sebanyak 10 bagian simplisia dengan derajat halus yang cocok dimasukkan kedalam sebuah bejana, kemudian dituangi dengan 75 bagian cairan penyari, ditutup dan dibiarkan selama 5 hari terlindung dari cahaya, sambil sering
24
diaduk. Setelah 5 hari sari diserkai, ampas diperas dan dicuci dengan cairan penyari secukupnya hingga diperoleh 100 bagian. Sari dipindahkan ke dalam bejana tertutup, dibiarkan ditempat sejuk dan terlindung dari cahaya selama 2 hari. Dienaptuangkan dan disaring.
Maserasi dilakukan juga secara umum dengan merendam serbuk simplisia dalam cairan penyari yang sesuai selama 3-5 hari pada temperatur kamar terlindung dari cahaya, sambil diaduk berulang-ulang lalu filtrat disaring dan diuapkan. Demikian seterusnya dilakukan sampai filtrat jernih.
2.3 Kanker
Kanker adalah istilah umum untuk pertumbuhan sel yang tidak normal, yaitu suatu kondisi dimana sel telah kehilangan pengendalian dan mekanisme normal sehingga mengalami pertumbuhan yang tidak normal, cepat dan tidak terkendali. Kanker dapat menyusup ke jaringan tubuh normal dan menekan jaringan tubuh normal sehingga mempengaruhi fungsi tubuh (Diananda, 2009). Ciri-ciri yang menggambarkan perubahan tumor jinak menjadi kanker ganas adalah kemampuan menyerang sel secara lokal, menyebarkan melalui sel limfa, dam metastatis dari organ ke seluruh tubuh (Ruddon, 2007).
Adapun ciri-ciri sel kanker secara khusus yang membedakan dengan sel normal, antara lain sebagai berikut.
a. Sel kanker mampu mencukupi kebutuhan sinyal pertumbuhannya sendiri
Sinyal pertumbuhan eksternal (mitogenic growth factor) dibutuhkan oleh sel normal untuk berproliferasi. Pada kondisi normal terdapat mekanisme regulasi terhadap rangsangan sinyal pertumbuhan sehingga proses perkembangan sel dapat dikontrol. Namun, sel kanker dapat memproduksi growth factor sendiri sehingga
25
tidak bergantung pada rangsangan sinyal pertumbuhan dari luar untuk melakukan proliferasi. Mutasi yang terjadi pada sel kanker memungkinkan sel tersebut untuk memperpendek growth factor pathway. Dengan demikian, sel kanker dapat tumbuh menjadi tidak terkendali (Pecorino, 2005; Kumar, 2005).
b. Sel kanker tidak sensitif terhadap sinyal antiproliferatif
Sinyal antiproliferatif adalah sinyal anti pertumbuhan yang dibutuhkan oleh sel untuk mengontrol dan menjaga keteraturan sel serta homeostasis jaringan. Pada keadaan normal, regulasi sinyal pertumbuhan ini menjadi faktor penentu bagi sel untuk berproliferasi atau istirahat. Sinyal ini akan mengatur perkembangan sel dengan memblok proliferasi melalui dua mekanisme, yaitu sel dipaksa keluar dari fase proliferasi yang aktif menuju fase istirahat G0 atau sel diinduksi untuk melepaskan potensi proliferasi secara permanen dengan diinduksi untuk memasuki fase post mitotic. Sel kanker memiliki kemampuan untuk menghindar dari sinyal anti pertumbuhan yang berhubungan dengan daur sel. Hal ini disebabkan oleh adanya mutasi pada beberapa gen (proto-onkogen) (Pecorino, 2005; Kumar, 2005).
c. Sel kanker mampu menghindar dari mekanisme apoptosis
Apoptosis merupakan suatu mekanisme fisiologis pengurangan sel untuk perbaikan jaringan dan pelepasan sel yang rusak yang dapat membahayakan tubuh (Ruddon, 2007). Resistensi kanker terhadap mekanisme apoptosis dapat terjadi dengan melibatkan protein regulator apoptosis antara lain: p53 dan Bcl-2. Protein ini memiliki kemampuan untuk mencegah replikasi DNA yang rusak dan mendorong penghancuran sel yang mengandung DNA abnormal. Mutasi gen pada
26
protein regulator ini menyebabkan sel kehilangan kontrol proliferasi (Kumar, et al., 2005).
d. Kemampuan angiogenesis yang dimiliki oleh sel kanker
Sel kanker memiliki kemampuan untuk memacu pertumbuhan pembuluh darah baru yang disebut angiogenesis. Kemampuan tersebut diinisiasi oleh sinyal Vascular Endothelial Growth Factor (VEGF) dan Fibroblas Growth Factor (FGF). Faktor-faktor angiogenensis dapat mengaktifkan angiogenic switch, sehingga pertumbuhan pembuluh darah baru menjadi tidak terkendali (Kumar, et al., 2005).
e. Sel kanker mampu menginvasi jaringan di sekitarnya dan membentuk anak sebar (metastasis)
Kebanyakan kanker pada manusia akan membentuk massa tumor primer yang mampu membebaskan diri dari jaringan awalnya untuk memasuki aliran darah atau pembuluh limfa dan membentuk tumor sekunder (metastasis) di bagian tubuh yang lain. Hal ini dapat terjadi akibat mutasi yang memungkinkan peningkatan aktivitas enzim-enzim yang terlibat dalam invasi sel kanker dan berkurangnya adhesi antar sel oleh molekul addisi sel (Pecorino, 2005).
f. Sel kanker memiliki potensi yang tak terbatas untuk mengadakan replikasi Adanya kemampuan untuk memenuhi kebutuhan sinyal pertumbuhan dan kemampuan menghindar dari mekanisme apoptosis, sel kanker memiliki kemampuan tak terbatas untuk bereplikasi. Kemampuan replikasi tak terbatas ini berkaitan dengan adanya enzim telomerase yang menjaga integritas telomer pada kromosom, sehingga sel tetap memiliki kemampuan untuk membelah diri. Pada kondisi normal, telomer akan mengalami degradasi (pemotongan) pada saat sel
27
mengalami replikasi. Ketidakmampuan sel untuk meregulasi degradasi telomer inilah yang menyebabkan sel kanker memiliki kemampuan tidak terbatas untuk bereplikasi (Kumar, et al., 2005).
2.3.1 Siklus sel
Siklus sel merupakan proses perkembangbiakan sel yang memperantarai pertumbuhan dan perkembangan makhluk hidup. Setiap sel baik sel normal maupun sel kanker mengalami siklus sel. Siklus sel memiliki dua fase utama, yakni fase S (sintesis) dan fase M (mitosis). Fase S merupakan fase terjadinya replikasi DNA kromosom dalam sel, sedangkan pada fase M terjadi pemisahan 2 set DNA kromosom tersebut menjadi 2 sel (Nurse, 2000).
Selain itu, terdapat fase yang membatasi kedua fase utama tersebut yang dinamakan Gap. G1 (Gap-1) terdapat sebelum fase S dan setelah fase S dinamakan G-2 (Gap-2). Pada fase G1, sel melakukan persiapan untuk sintesis DNA. Fase ini merupakan fase awal cell cycle progression yang diatur oleh faktor ekstraselular seperti mitogen dan molekul adhesi. Penanda fase ini adalah adanya ekspresi dan sintesis protein sebagai persiapan memasuki fase S. Pada fase G2, sel melakukan sintesis lebih lanjut yang memadai untuk proses pembelahan, sehingga sel siap melakukan pembelahan pada fase M (Ruddon, 2007).
Siklus sel dikontrol oleh beberapa protein yang bertindak sebagai regulator positif dan negatif. Kelompok cyclin khususnya cyclin D, E, A dan B merupakan protein yang levelnya fluktuatif selama proses siklus sel. Cyclin bersama dengan kelompok cyclin dependent kinase (CDK), khususnya CDK 4, 6 dan 2, bertindak sebagai regulator positif yang memacu terjadinya siklus sel. Pada mamalia ekspresi kinase (CDK4, CDK2 dan CDC2/CDK1) terjadi bersamaan dengan
28
ekspresi cyclin (D, E, A dan B) secara berurutan seiring dengan jalannya siklus sel (G1-S-G2-M) (Nurse, 2000). Aktivasi CDK dihambat oleh regulator negatif siklus sel, yakni CDK inhibitor (CKI), yang terdiri dari Cip/Kip protein (meliputi p21, p27, p57) dan keluarga INK4 (meliputi p16, p18, p19). Selain itu, tumor suppressor protein yaitu p53 dan pRb juga bertindak sebagai protein regulator negatif (Foster, et al., 2001).
Aktivasi CDK memerlukan ekspresi cyclin (Cyc). Kompleks Cyclin-CDK dengan protein CKI dan adanya fosforilasi oleh Wee1 (tyrosin15)/ Myt1 (threonin14) dapat menyebabkan inaktivasi CDK. Aktivasi kompleks Cyc-CDK diawali dengan proteolisis CKI oleh ubiquitin, kemudian fosforilasi CDK oleh CDK-activating kinase (CAK) pada threonin161 dan penghilangan fosfat (defosforilasi) oleh Cdc25 fosfatase pada target fosforilasi Wee1 (tyrosin15)/Myt1 (threonin14). CDK bekerja pada awal G1 untuk mengaktifkan E2F-dependent transcription gen yang diperlukan untuk fase S (di akhir G1 untuk menginisiasi fase S) dan juga di akhir G2 untuk menginisiasi mitosis (M) (Nurse, 2000).
Checkpoint pada G2 terjadi ketika ada kerusakan DNA yang akan mengaktivasi beberapa kinase termasuk ataxia telangiectasia mutated (ATM) kinase. Hal tersebut menginisiasi dua kaskade untuk menginaktivasi Cdc2-CycB baik dengan jalan memutuskan kompleks Cdc2-CycB maupun mengeluarkan kompleks Cdc-CycB dari nukleus atau aktivasi p21.
Checkpoint pada fase G1 akan dapat dilalui jika (1) ukuran sel memadai; (2) ketersediaan nutrien mencukupi; dan (3) adanya faktor pertumbuhan (sinyal dari sel yang lain). Checkpoint pada fase G2 dapat dilewati jika ukuran sel memadai dan replikasi kromosom terselesaikan dengan sempurna, sedangkan
29
checkpoint pada metaphase (M) terpenuhi bila semua kromosom dapat menempel pada gelendong (spindle) mitotik (Ruddon, 2007).
Checkpoint ini akan menghambat progresi siklus sel ke fase mitosis, sedangkan checkpoint pada fase M (mitosis) terjadi jika benang spindle tidak terbentuk atau jika semua kromosom tidak dalam posisi yang benar dan tidak menempel dengan sempurna pada spindle. Checkpoint tersebut bekerja dengan memonitor apakah kinetokor dan mikrotubul terhubung secara benar. Jika tidak, kohesi kromatid akan tetap berlangsung dan mikrotubul gagal untuk memendek sehingga kromatid tidak bergerak menjauh ke kutub yang berlawanan (Ruddon, 2007).
Kontrol checkpoint sangat penting untuk menjaga stabilitas genomik. Kesalahan pada checkpoint akan meloloskan sel untuk berkembang biak meskipun terdapat kerusakan DNA atau replikasi yang tidak lengkap atau kromosom tidak terpisah sempurna sehingga akan menghasilkan kerusakan genetik. Hal ini kritis bagi timbulnya kanker. Oleh karena itu, proses regulasi siklus sel mampu berperan dalam pencegahan kanker (Ruddon, 2007).
2.3.2 Karsinogenesis
Karsinogenesis merupakan suatu proses terjadinya kanker melalui mekanisme multitahap dengan adanya perubahan neoplastik pada jaringan normal yang disebabkan oleh akumulasi multimutasi genetik dan menyebabkan transformasi progresif sel normal menjadi sel malignan (ganas) (Tsao, et al., 2004). Perubahan ini diawali dari mutasi somatik satu sel tunggal yang mengakibatkan perubahan dari normal menjadi hiperplastik, displastik dan pada akhirnya menjadi suatu keganasan atau malignansi (memiliki kemampuan
30
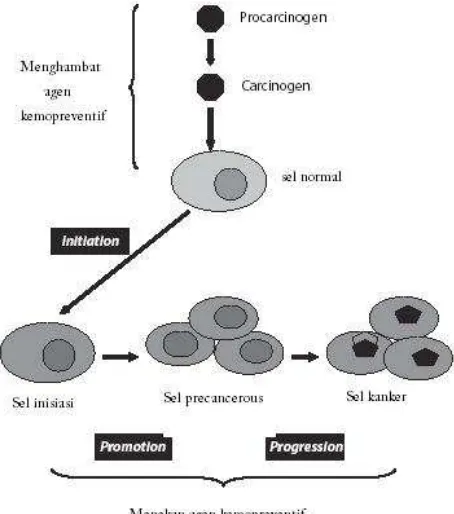
metastasis atau menginvasi jaringan di sekelilingnya). Perubahan genetik ini termasuk perubahan seluler mendasar pada sel kanker yang dipengaruhi oleh beberapa gen seperti: tumor suppresor genes (pRb, p53,PTEN, E-cadherin) dan proto-oncogenes (ras, c-myc, Bcl-2). Karsinogenesis dapat dibagi menjadi empat tahap utama, yaitu tahap inisiasi, promosi, progresi dan metastasis (Gambar 2.1).
Tahap inisiasi adalah tahap pertama pada karsinogenesis ketika sel normal mulai mengalami mutasi oleh karsinogen (Diandana, 2009). Tahap karsinogenesis selanjutnya adalah promosi, merupakan tingkat lanjutan dari tahap inisiasi. Pada tahap ini, sel mulai mengalami hiperplastik pada inti sel. Sel-sel akan memperoleh beberapa keuntungan selektif untuk tumbuh sehingga pertumbuhannya menjadi cepat dan berubah menjadi tumor jinak. Tahap promosi tidak melibatkan perubahan struktural dari genom secara langsung, tetapi biasanya terjadi perubahan ekspresi gen yang terinisiasi (Tsao, et al., 2004)
Gambar 2.1. Multitahap karsinogenesis (dimodifikasi dari Tsao, et al., 2004)
31
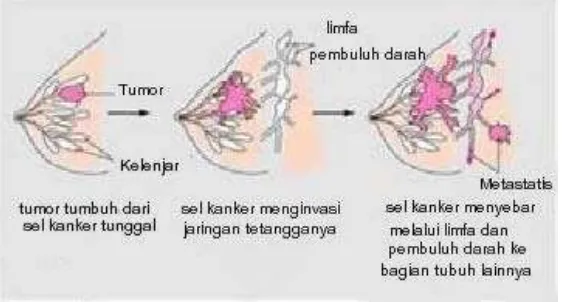
Pada tahap progresi, kemampuan pembelahan yang tinggi menuntun terbentuknya koloni sel yang lebih besar melalui perubahan genetik lebih lanjut dan munculnya keistimewaan-keistimewaan lain seperti peningkatan mobilitas dan angiogenesis (Kumar, et al., 2005). Pada tahap ini, sel-sel tumor dikatakan sebagai sel malignan. Pada fase ini juga akan terjadi karsinoma dan metastasis melalui aktivasi onkogen dan malfungsi dari enzim topoisomerase (Pecorino, 2005). Tahap metastasis merupakan tahap akhir dalam karsinogenesis. Pada tahap ini, sel kanker melakukan invasi ke jaringan-jaringan lain di dalam tubuh melalui pembuluh darah, pembuluh limpa, atau rongga tubuh (Gambar 2.2) (Kumar, et al., 2005). Sel malignan yang bermetastasis ini masuk melalui basement membran menuju saluran limpoid. Sel tersebut akan berinteraksi dengan sel limpoid yang digunakan sebagai inangnya. Selanjutnya, sel kanker akan masuk ke jaringan lainnya membentuk tumor sekunder dengan didukung kemampuan neoangiogenesis yang dimilikinya (Kumar, et al., 2005).
Payudara normal Kanker payudara
Gambar 2.2 Kanker payudara (dimodifikasi dari Kumar, et al., 2002). Tahap metastasis dapat berlangsung karena melemahnya ikatan antarsel yang disebabkan oleh terdegradasinya CAMs (Cell-cell Adhesion Molocules) dan
32
E-cadherin sebagai molekul yang menjaga pertautan antarsel. Molekul-molekul tersebut diketahui sudah sangat sedikit bahkan tidak ditemukan lagi pada sel kanker, sehingga proses metastasis dapat terus terjadi (Kumar, et al., 2005). Adanya mutasi pada satu sel tunggal normal sebagai akibat terpapar oleh karsinogen (inisiasi), akan menyebabkan progresi sel menjadi hiperplasi (promosi), diplasi (progresi) dan pada akhirnya memiliki kemampuan invasi ke jaringan sekitarnya (metastasis) (Tsao, et al., 2004).
2.3.3 Kanker payudara
Kanker payudara merupakan kanker yang menyerang jaringan epitelial payudara, yaitu membran mukosa dan kelenjar, sehingga kanker payudara tergolong pada karsinoma. Kanker payudara merupakan kanker yang paling umum diderita oleh wanita, di samping kanker serviks. Penyebab kanker payudara sangat beragam, antara lain (Torosian, 2002):
a. Kerusakan pada DNA yang menyebabkan mutasi genetik. Kerusakan ini dapat disebabkan oleh radiasi yang berlebihan
b. Kegagalan immune surveillance dalam pencegahan proses malignan pada fase awal
c. Faktor pertumbuhan yang abnormal
d. Malfungsi DNA repairs seperti : BRCA1, BRCA2 dan p53.
Kanker payudara terjadi ketika sel-sel pada payudara tumbuh tidak terkendali dan dapat menginvasi jaringan tubuh yang lain baik yang dekat dengan organ tersebut maupun bermetastasis ke jaringan tubuh yang letaknya berjauhan. Semua tipe jaringan pada payudara dapat berkembang menjadi kanker, namun pada umumnya kanker muncul baik dari saluran (ducts) maupun kelenjar
33
(glands). Perkembangannya memerlukan waktu berbulan-bulan atau bertahun-tahun sampai tumor tersebut cukup besar untuk dirasakan pada payudara. Deteksi dapat dilakukan dengan mammograms yang kadang-kadang dapat mendeteksi tumor sejak dini (Dolinsky, 2002).
Faktor resiko kanker payudara dapat dibedakan menjadi faktor yang dapat diubah (reversible) dan yang tidak dapat diubah (irreversible). Faktor-faktor yang tidak dapat diubah termasuk jenis kelamin, bertambahnya umur, ada-tidaknya riwayat keluarga menderita kanker, pernah-tidaknya menderita kanker payudara, pernah-tidaknya mendapat terapi radiasi pada bagian dada, suku bangsa Kaukasian, orang yang mengalami menstruasi pertama pada usia sangat muda (sebelum 12 tahun), yang mengalami menopause terlambat (setelah 50 tahun), yang tidak pernah melahirkan atau melahirkan di usia lebih dari 30 tahun dan yang mengalami mutasi genetik. Dari berbagai macam faktor tersebut, 3%-10% penyebab kanker payudara diduga berkaitan dengan perubahan baik gen BRCA1 maupun gen BRCA2 (Dolinsky, 2002).
Beberapa faktor yang menaikkan resiko menderita kanker payudara yang dapat diubah, yakni mendapatkan terapi pengganti hormon (penggunaan estrogen dan progesteron dalam jangka waktu lama untuk mengatasi gejala menopause), menggunakan pil antikontrasepsi (pil KB), tidak menyusui, mengonsumsi minuman beralkohol 2-5 gelas per hari, menjadi gemuk terutama setelah menopause dan tidak berolahraga (Dolinsky, 2002). Perlu diingat bahwa faktor-faktor resiko tersebut hanyalah berdasarkan pada kemungkinan. Seseorang tetap dapat terkena kanker payudara walaupun ia tidak mempunyai satu pun faktor
34
resiko tersebut. Menghindari faktor resiko tersebut dan deteksi awal adalah cara terbaik untuk mengurangi kematian berkaitan dengan kanker ini.
Peningkatan insidensi kanker payudara disebabkan oleh kegagalan terapi terhadap kanker itu sendiri. Kegagalan ini diakibatkan oleh adanya multidrug resistance (MDR) dan terjadi hingga 71% dibandingkan dengan faktor penyebab lainnya (Mechetner, et al., 1998). Multidrug resistance atau resistensi obat ini diakibatkan oleh adanya breast cancer resistance protein (BCRP) yang salah satunya adalah P-glycoprotein (P-gp) (Imai, et al., 2005). Aktivasi P-gp dan peningkatan ekspresinya dapat menurunkan efikasi dari beberapa agen kemoterapi seperti taxol dan doxorubicin (Mechetner, et al., 1998). Penekanan aktivitas P-gp dan ekspresinya mampu meningkatkan efektivitas agen kemoterapi (Zhou, et al., 2006).
Selain itu, paparan estrogen endogen yang berlebihan juga dapat berkontribusi sebagai penyebab kanker payudara. Sekitar 50% kasus kanker payudara merupakan kanker yang bergantung pada estrogen dan sekitar 30% kasus merupakan kanker yang positif mengekspresi HER-2 berlebihan (Gibbs, 2000). Kedua protein tersebut selain berperan dalan metastasis, juga berperan dalam perkembangan kanker payudara (early cancer development).
Proses metastase kanker payudara diinisiasi oleh adanya aktivasi/ekspresi berlebih beberapa protein, misalnya Estrogen Reseptor (ER) dan c-erbB-2 (HER- 2) yang merupakan protein predisposisi kanker payudara (Fuqua, 2001; Eccles, 2001). Aktivasi reseptor estrogen melalui ikatan kompleks dengan estrogen akan memacu transkripsi gen yang mengatur proliferasi sel. Estrogen dapat memacu ekspresi protein yang berperan dalam siklus sel seperti cyclin D1, CDK4
35
dependent kinase 4), cyclin E dan CDK2. Selain itu, aktivasi reseptor estrogen mampu mengaktivasi beberapa onkoprotein yang berperan utama dalam sinyal pertumbuhan, misalnya Ras, Myc dan cycD1 (Foster, et al., 2001). Aktivasi protein ini mengakibatkan adanya pertumbuhan yang berlebihan melalui aktivasi onkoprotein yang lain seperti P13K, AKT, Raf, ERK dan MAP kinase (Hahn, et al., 2002). Di lain pihak, kompleks estrogen dengan reseptornya juga akan memacu transkripsi beberapa gen tumor suppressor, seperti BRCA1, BRCA2 dan p53.
2.3.4 Sel MCF-7
Sel MCF-7 pertama kali diperoleh pada tahun 1973 di Michigan Cancer Foundation. Sel ini banyak dimanfaatkan secara luas sebagai sel yang sensitif terhadap kehadiran hormon esterogen (ER), sehingga menjadi model yang ideal untuk penelitian (Holliday, et al., 2011). Sel ini berasal dari pleural effusion breast adenocarcinoma seorang pasien wanita Kaukasian berumur 69 tahun, golongan darah O (Crawford, 2002). Sel ini termasuk sel adherent (melekat) yang dapat ditumbuhkan dalam media penumbuh DMEM yang mengandung foetal bovine serum (FBS) 10% dan antibiotik penisilin-streptomicin 1% (Anonim, 2008). Sel ini mengekspresikan reseptor estrogen alfa (ER-α), memiliki sifat resisten terhadap doxorubicin (Zampieri, et al., 2002) dan tidak mengekspresikan caspase-3 (Bouker, 2005). Pada sel MCF-7, P-gp diekspresikan tinggi, sehingga sensitivitas terhadap agen kemoterapi seperti doxorubicin rendah (Wong, et al., 2006). Penurunan konsentrasi ini dapat mengurangi efektivitas senyawa kemoterapi pada sel MCF-7. Salah satu cara untuk meningkatkan sensitivitas
36
MCF-7 adalah dengan menghambat ekspresi dan aktivasi P-gp (Zhou, et al., 2006).
2.3.5 Sel T47D
Sel T47D (Human ductal breast epithelial tumor cell line) adalah sel yang mengekspresikan tumor yang telah termutasi pada protein p53. Sel ini dapat kehilangan estrogen reseptor (ER) apabila kekurangan esterogen pada jangka waktu lama selama percobaan in vitro (Anonim, 2013). Sel ini berasal dari ductal carcinoma dan mengekspresikan caspase 3 (Mooney, et al., 2002). Oleh karena itu sel ini digunakan pada model untuk penelitian resistensi obat pada pasien dengan tumor payudara p53 mutan (Anonim, 2013).
2.3.6 P-glycoprotein
P-glycoprotein (P-gp) merupakan protein ABC-transporter pada manusia yang termasuk dalam subfamili MDR/TAP (Allen, et al., 2002) P-gp dikenal dalam beberapa sebutan yakni ABCB1, ATP-binding cassette sub-family B member 1, MDR1 dan PGY1 (Choi, 2005). ABCD1 atau P-gp termasuk dalam ATP-dependent efflux pump yang memiliki substrat spesifik antara lain: obat (colchicine dan tacrolimus), agen kemoterapi (etoposide, adrimycin dan vinblastine), lipid, steroid, xenobiotik, peptide, bilirubin, cardiac glycoside (digoxin), glucocorticoids (dexamethasone) dan agen terapi HIV tipe 1 (inhibitor protease dan nonnucleoside reverse transcriptase) (Kitagawa, 2006). Di dalam tubuh, P-gp ini dapat ditemukan pada sel usus, hati, tubula ginjal dan capillary endothelial (Deng, et al., 2001).
P-glycoprotein adalah sebuah glikoprotein transmembran yang memiliki 10 - 15 kDa N-terminal glycosylation dengan bobot 170-kDa dikode oleh gen
37
MDR1 (Kitagawa, 2006). Gen ini dicirikan dengan pompa efflux obat dan anggota dari keluarga ATP-binding transport (Choi, 2005). Dalam sistem organ, P-gp berpengaruh terhadap absorbsi, distribusi dan eliminasi obat (Matheny, et al., 2001). Kemampuan P-gp sebagai pompa efflux berguna dalam detoksifikasi senyawa-senyawa yang masuk ke dalam sel. Senyawa yang termasuk substrat dari P-gp akan diikat dan dikeluarkan dari dalam sel (Gambar 2.3). Aktivitas P-gp sangat bergantung pada aktivasi P-gp oleh ATP melalui pembentukkan kompleks P-gp-ATP. Hidrolisis ATP oleh ATPase memberikan energi aktivasi pada P-gp (Choi, et al., 2005). Aktivasi P-gp akan menurunkan intake agen kemoterapi sehingga menurunkan efikasi agen tersebut terhadap sel kanker. Pada kondisi ekspresi yang berlebihan, P-gp dapat menyebabkan resistensi obat terutama agen kemoterapi pada kanker payudara seperti doxorubicin (Mechetner, et al., 1998). P-gp akan mengikat doxorubicin sebagai salah satu substratnya untuk dikeluarkan dari dalam sel (Wong, et al., 2006). P-gp atau ABCD1 pertama kali diujikan sebagai multidrug resistance dan terbukti sebagai penyebab resistensi obat kemoterapi (Juliano, 1976).
Penghambatan aktivasi dan ekspresi P-gp memegang peranan penting dalam keberhasilan terapi kanker (Zhou, et al., 2006). Penghambatan aktivitas P-gp dapat melalui dua mekanisme yakni dengan menghambat substrat P-P-gp secara langsung dengan berikatan pada P-gp-binding domain dan menghambat hidrolisis ATP oleh ATase melalui ikatan substrat dengan ATP (Kitagawa, 2006). Penghambatan ini dapat dilakukan menggunakan senyawa flavonoid dan polifenol melalui dua sisi ikatan pada ATP-binding sites dan steroid interacting region dimana ATPase berikatan dengan P-gp cytosolic domain (Kitagawa, 2006).
38
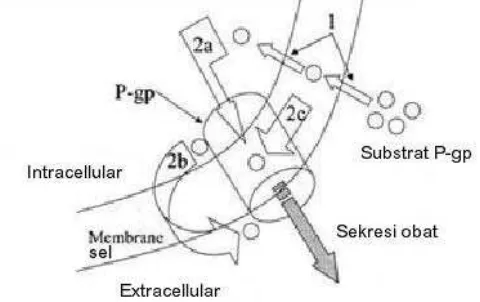
Gambar 2.3 Mekanisme pemompaan oleh P-gp (dimodifikasi dari Matheny, et al., 2001).
P-gp memompa senyawa-senyawa (2a, 2b, 2c) yang termasuk substratnya untuk dikeluarkan dari dalam sel. Ekspresi berlebih dari P-gp ini dapat menyebabkan resistensi obat pada terapi kanker payudara (Matheny, et al., 2001). Penekanan ekspresi P-gp dapat dilakukan melalui berbagai mekanisme antara lain aktivasi jalur sinyal transduksi c-Jun NH2-terminal kinase (JNK) dan inaktivasi NF-κB transcriptional factor, c-Jun NH2-terminal kinase (JNK) merupakan protein kinase yang berikatan dengan NH2-terminal yang merupakan sisi aktif pada c-Jun transcriptional factor dan protein ini mampu memfosforilasi c-Jun. Fosforilasi c-Jun akan menstimulasi pembentukan ikatan dengan AP-1, suatu elemen pada gen MDR1. Pembentukan ikatan ini akan mencegah ekspresi mRNA MDR1 dan pada akhirnya akan menghambat ekspresi P-gp. Fosforilasi c-Jun tersebut dapat dilakukan oleh salvicine (quinine diterpenoid sintetik) (Zhou, et al., 2006). Penelitian yang dilakukan oleh Deng, et al., (2001), melaporkan bahwa aktivasi NF-κB sebagai akibat adanya stimulus dari lingkungan berupa stress, paparan agen sitotoksik, heat shock, iradiasi, genotoxic stress, inflamasi, paparan sitokin dan faktor pertumbuhan dapat meningkatkan ekspresi P-gp. NF-κB yang
39
aktif mampu berikatan dengan promoter gen MDR1 sehingga proses ekspresi P-gp dapat berjalan. Inaktivasi NF-κB mampu menghambat ekspresi P-gp.
2.3.7 Resistensi doxorubicin terhadap sel kanker payudara
Doxorubicin adalah golongan antibiotik antrasiklin sitotoksik yang diisolasi dari Streptomyces peucetius var. caesius. Doxorubicin telah digunakan secara luas untuk mengobati kanker payudara dan menunjukkan kemampuan yang kuat dalam melawan kanker. Senyawa ini telah digunakan sebagai obat kemoterapi kanker sejak akhir tahun 1960-an (Singal, et al., 1998; Rock, et al., 2003).
Doxorubicin memiliki aktivitas antineoplastik dan spesifik untuk fase S dalam siklus sel. Mekanisme aktivitas antineoplastiknya belum diketahui dengan pasti. Mekanisme aksi doxorubicin kemungkinan melibatkan ikatan dengan DNA melalui interkalasi di antara pasangan basa serta menghambat sintesis DNA dan RNA melalui pengkacauan template dan halangan sterik. Kemungkinan mekanisme yang lain adalah melibatkan ikatan dengan lipid membran sel, yang akan mengubah berbagai fungsi selular dan berinteraksi dengan topoisomerase II membentuk kompleks pemotong DNA (Rock, et al., 2003).
Aplikasi doxorubicin yang telah digunakan secara klinis untuk berbagai jenis tumor ini dibatasi oleh timbulnya efek samping (Tyagi, et al., 2004). Efek samping yang timbul segera setelah pengobatan dengan doxorubicin adalah mual, imunosupresi dan aritmia yang sifatnya revesibel serta dapat dikontrol dengan obat-obat lain. Efek samping yang paling serius akibat pengobatan dengan doxorubicin dalam jangka waktu yang lama adalah cardiomyopathy yang diikuti dengan gagal jantung (Tyagi, et al., 2004). Berdasarkan hasil penelitian restrospektif diketahui bahwa toksisitas kardiak akibat pemberian doxorubicin
40
merupakan efek samping yang bergantung pada dosis. Mekanisme yang memperantarai toksisitas kardiak tersebut diduga disebabkan oleh terbentuknya spesies oksigen reaktif, meningkatnya kadar anion superoksida dan pengurasan ATP yang kemudian menyebabkan perlukaan jaringan kardiak (Wattanapitayakul, et al., 2005).
Permasalahan yang sering timbul dalam terapi kanker terutama kanker payudara menggunakan doxorubicin adalah resistensi obat dan menjadi penyebab kegagalan terapi kanker payudara (Mechetner, et al., 1998). Resistensi ini diperantarai oleh berbagai mekanisme antara lain: mutasi pada target obat, kegagalan inisiasi apoptosis dan pengeluaran obat oleh protein transporter pada membran sel (Notobartolo, et al., 2005). Pengeluaran obat yang disebabkan oleh adanya pompa efflux P-gp menjadi salah satu sebab utama resistensi obat ini (Mechetner, et al., 1998).
Doxorubicin termasuk obat golongan antrasiklin yang merupakan substrat P-gp (Mechetner, et al., 1998; Wong et al., 2006). Doxorubicin akan dikenali oleh P-gp dan selanjutnya segera dikeluarkan dari dalam sel sehingga menurunkan konsentrasi efektif doxorubicin dalam sel kanker. Mekanisme pemompaan oleh gp sangat bergantung pada aktivasi protein tersebut dan penekanan ekspresi P-gp (Zhou, et al., 2006). Oleh karena itu, inaktivasi P-P-gp dan penekanan ekspresinya mampu mengatasi permasalahan resistensi sel kanker terhadap doxorubicin (Mechetner, et al., 1998; Zhou, et al., 2006).
2.3.8 Uji sitotoksik menggunakan metode MTT
Uji sitotoksisitas dilakukan secara in vitro, yaitu untuk menentukan potensi sitotoksik suatu senyawa seperti obat antikanker. Toksisitas merupakan
41
kejadian kompleks secara in vivo yang menimbulkan kerusakan sel akibat penggunaan obat antikanker yang bersifat sitotoksik. Respon sel terhadap agen-agen sitotoksik dipengaruhi oleh kerapatan sel (Kupcsik, 2011).
Metode MTT [3-(4,5-dimetiltiazol-2-il)-2,5-difenil tetrazolium bromida] adalah salah satu uji sitotoksisitas yang bersifat kuantitatif. Uji ini berdasarkan pengukuran intensitas warna (kolorimetri) yang terjadi sebagai hasil metabolisme suatu substrat oleh sel hidup menjadi produk berwarna (Kupcsik, 2011).
Pada uji ini digunakan garam MTT. Garam ini akan terlibat pada kerja enzim dehidrogenase. MTT akan direduksi menjadi formazan oleh sistem reduktase suksinat tetrazolium, yang termasuk dalam mitokondria dari sel hidup (Kupcsik, 2011).
Formazan merupakan zat berwarna ungu yang tidak larut dalam air sehingga dilarutkan menggunakan HCl 0,04 N dalam isopropanool atau 10% SDS dalam HCl 0,01 N. Intensitas warna ungu terbentuk dapat ditetapkan dengan spektrofotometri dan berkorelasi langsung dengan jumlah sel yang aktif melakukan metabolisme, sehingga berkorelasi dengan viabilitas sel. Persentase viabilitas dapat dihitung dengan persamaan sebagai berikut.
2.3.9 Combination Index (CI)
Terapi pengobatan kanker pada umumnya menggunakan terapi kombinasi (ko-kemoterapi) dengan agen-agen yang memiliki efek sinergis terhadap sel kanker, bersifat spesifik dan memiliki efek toksik seminimal mungkin. Terapi kombinasi hingga saat ini dikembangkan secara empiris. Namun demikian,
42
sampai saat ini belum ada terapi pengobatan untuk kanker payudara yang telah metastasis. Selain itu, berbagai permasalahan seperti resistensi obat dan timbulnya toksisitas yang tinggi pada jaringan normal oleh beberapa agen kemoterapi, menjadi semakin sulit menemukan terapi kanker payudara yang efektif. Hal tersebut menuntut pengembangan cara pengobatan baru bagi kanker payudara (Tyagi, et al., 2004).
Pemanfaatan senyawa alam yang non-toksik dengan efektivitas tinggi melawan kanker dapat menjadi pilihan pengembangan terapi kombinasi dengan agen kemoterapi (Sharma, et al., 2004, Tyagi, et al., 2004). Oleh karena itu, berbagai metode dapat dilakukan untuk mengembangkan dan mengevaluasi kombinasi terapi yang tepat.
Isobologram dan combination index (CI) merupakan metode yang umum digunakan untuk mengevaluasi kombinasi obat. Metode ini dikemukakan pertama kali oleh Chou dan Talalay pada tahun 1984 (Zhao, et al., 2004).
Analisis isobologram mengevaluasi interaksi dua obat dengan jalan menentukan terlebih dahulu konsentrasi efektif (IC50) dari masing-masing obat ketika diaplikasikan sebagai agen tunggal kemudian diplotkan pada sumbu X dan Y. Garis yang menghubungkan kedua titik disebut dengan garis aditif. Selanjutnya, konsentrasi kombinasi kedua obat untuk menghasilkan efek yang sama digambarkan pada plot yang sama. Efek sinergis, aditif, atau antagonis diindikasikan oleh letak titik plot tersebut, yaitu apakah (secara berurutan) di bawah, pada, atau di atas garis aditif (Zhao, et al., 2004).
Selain dengan isobologram, interaksi antara dua obat dapat dianalisis dengan CI (combination index). Analisis CI menghasilkan suatu nilai parameter
43
kuantitatif yang menggambarkan efikasi dari kombinasi dengan menggunakan persamaan sebagai berikut.
I= (D)1/(Dx)1 + (D)2/(Dx)2
I adalah CI. Dx adalah konsentrasi dari satu senyawa tunggal yang dibutuhkan untuk memberikan efek, dalam hal ini adalah IC50 terhadap pertumbuhan sel kanker payudara. (D)1 dan (D)2 adalah besarnya konsentrasi kedua senyawa untuk memberikan efek yang sama. Nilai CI kurang, sama, atau lebih dari 1 mengindikasikan efek (secara berurutan) sinergis, aditif, atau antagonis (Zhao, et al., 2004; Reynolds, et al., 2005).
Uji efek kombinasi dengan kedua metode tersebut biasanya dilakukan secara in vitro. Metode uji in vitro dapat digunakan sebagai uji praklinik awal untuk menggambarkan interaksi kombinasi, sehingga ketika dilakukan uji in vitro hasilnya akan lebih efisien.
2.3.10 Apoptosis dan nekrosis
Kematian sel dapat didefinisikan sebagai kehilangan irreversibel dari suatu membran plasma. Secara historis, ada tiga jenis kematian sel pada sel mamalia dengan kriteria morfologi. Type I, dikenal sebagai apoptosis. Apoptosis adalah perubahan karakteristik dalam morfologi, termasuk kondensasi kromatin (pyknosis) dan fragmentasi (karyorrhexis), perubahan minor dalam organel sitoplasma dan penyusutan sel secara keseluruhan. Pecahnya membran plasma dan pembentukan badan-badan apoptosis yang mengandung inti sel atau sitoplasma. Semua perubahan ini terjadi sebelum membran plasma lisis.
Tipe II ditandai dengan akumulasi besar dua membran vakuola dalam sitoplasma. Kematian sel tipe III dikenal sebagai nekrosis, sering didefinisikan
44
secara negatif seperti kematian yang tidak memiliki ciri-ciri proses tipe I dan tipe II. Nekrosis didasarkan pada kriteria morfologi kehancuran membran plasma secara awal dan dilatasi organel sitoplasma, khususnya mitokondria (Golstein, 2006).
a. Apoptosis
Apoptosis adalah kematian sel melalui mekanisme genetik dengan kerusakan/fragmentasi kromosom atau DNA. Apoptosis dibedakan menjadi dua kelompok, yaitu:
1. Apoptosis fisiologis
Apoptosis fisiologis adalah kematian sel yang diprogram (programmed cell death). Proses kematian sel erat kaitannya dengan enzim telomerase. Pada sel embrional, enzim ini mengalami aktivasi sedangkan pada sel somatik enzim ini tidak mengalami aktivasi, kecuali sel bersangkutan mengalami transformasi menjadi ganas. Telomer yang terletak pada ujung kromosom merupakan faktor yang sangat penting dalam melindungi kromosom. Pada sel normal, telomer akan memendek pada saat pembelahan diri. Apabila ukuran telomer mencapai ukuran tertentu (level kritis) akibat pembelahan berulang, maka sel tersebut tidak dapat melakukan pembelahan diri lagi. Selanjutnya sel akan mengalami apoptosis secara fisiologis. Pada sel ganas, pemendekan telomerase sampai pada level kritis tidak terjadi karena pada sel ganas terjadi aktivasi dari enzin ribonukleoprotein (telomerase) secara terus menerus. Enzim ini sangat berperan pada sintetis telomeric DNA, sehingga berbagai elemen yang dibutuhkan pada pembentukan telomer dapat dibentuk secara terus menerus dan ukuran telomer pada ujung
45
kromosom dapat dipertahankan. Oleh karena itu, sel ganas dapat bersifat immortal (Sudiana, 2011).
2. Apoptosis patologis
Apoptosis patologis adalah kematian sel karena adanya suatu rangsangan. Proses kematian sel (apoptosis) dapat melalui beberapa jalur, antara lain sebagai berikut: a) Aktivitas p-53
Apoptosis ini dipicu oleh aktivitas p-53 karena sel yang bersangkutan memiliki gen yang cacat (gene defect) yang dipicu oleh bangak faktor, antara lain bahan kimia, radikal bebas, maupun virus (oncovirus). Gen yang cacat dapat memicu aktivitas beberapa enzim seperti PKC (protein kinase-C) dan CPK-K2 (cystein protein kinase-K2), dimana kedua enzim in dapat memicu aktivitas p-53. p-53 adalah fraktor transkripsi terhadap pembentikan p-21. Peningkatan p-21 akan menekan semua CDK (Cyclin Dependent-protein Kinase) dengan cyclin, dimana siklus pembelahan sel sangat tergantung pada ikatan kompleks antara CDK dengan cyclin.
Apabila terjadi pengikatan p21, maka semua CDK akan ditekan, baik pada CDK-1 pada fase M, CDK-4 dan CDK-6 pada fase S. Dengan terjadinya penekanan semua CDK pada semua fase siklus sel, maka siklus sel akan berhenti sehingga p-53 akan memicu aktivitas BAX. Protein BAX akan menekan aktivitas BCL-2 sehingga terjadi peribahan membran permeabilitas dari mitokondria. Perubahan ini mengakibatkan terjadinya pelepasan cytokrom-C ke sitosol sehingga akan mengaktivasi kaskade kaspase dan kaspase aktif ini akan mengaktifkan DNA-se. DNA-se yang aktif akan menembus membran inti dan merusak DNA, sehingga DNA sel akan terfragmentasi dan mengalami apoptosis.
46 b) Jalur sitotoksik
Apoptosis dipicu oleh adanya sel yang memiliki gen cacat (gene defect) sehingga sel akan mengekspresiakn protein asing. Protein asing yang dhasilkan dapat bersifat imunogenik sehingga memicu pembentukan antibodi. Antibodi akan menempel di permukaan sel killer dan akan memicu pelepasan enzim yang disebut sebagai sitotoksin. Sitotoksin tersebut mengandung perforin dan granzyme, dimana perforin dapat memperforasi membran sel yang memiliki gen cacat sedangkan granzyme akan masuk ke dalam sel dan mengaktivasi kaspase kaspade. Kaspase yang aktif ini akan mengaktivasi DNA-se sehingga sel mengalami kematian (apoptosis).
c) Disfungsi mitokondria
Disfungsi mitokondria adalah gangguan ekspresi protein pada mitokondria yang tidak seimbang baik ekspresinya yang berlebihan, maupun protein yang diekspresikan adalah protein abnormal.
d) Kompleks fas dan ligan
Terjadinya apoptosis melalui jalur ligan dan fas dapat terjadi karena dipicu oleh adanya sel yang terinveksi virus, dimana di permukaan sel terekspresi suatu protein yang disebut fas. Fas yang terdapat pada membran sel yang terinfeksi virus akan diikat oleh ligan yang berada di permukaan NK-cell atau CTL (cytotoxic T lymfosit). Adanya ikatan antar fas-ligan akan mengaktifase suatu protein yang disebut Fas Associated Protein Death Domain (FADD) yang dapat mengaktivasi kaspase kaskade. Selanjutnya, kaspase yang aktif akan mengaktifkan DNA-se sehingga sel akan mengalami apoptosis (Sudiana, 2011).
47 b. Nekrosis
Nekrosis didefinisikan sebagai kematian sel yang tidak memiliki ciri-ciri seperti apoptosis dan autophagy. Nekrosis sering dihubungkan dengan sesuatu yang bersifat negatif, namun nekrosis dapat mencakup tanda-tanda proses yang terkontrol seperti disfungsi mitokondria, peningkatkan generasi spesies oksigen reaktif, pengurangan ATP, proteolisis oleh calpains dan cathepsins dan kerusakan membran plasma awal. Selain itu, penghambatan spesifik protein yang terlibat dalam mengatur apoptosis atau autophagy dapat mengubah jenis kematian sel menjadi nekrosis (Golstein, 2006).
2.3.11 Selectivity index
Untuk memperoleh nilai selectivity index digunakan sel yang berasal dari ginjal monyet hijau afrika (vero) menggunakan 3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyltetrazolium bromide (MTT). Selektivitas indeks (SI) diperoleh dari rasio IC50 sel Vero sel dibandingkan dengan sel kanker yang diuji. Nilai SI lebih tinggi dari 3 menunjukkan bahwa obat atau ekstrak memiliki selektivitas yang tinggi (Prayong, 2008).