a. Senyawa lemak rantai terbuka atau alifatik, seperti asam-asam lemak, gula-gula, dan hampir semua asam amino
b. Senyawa sikloalifatik atau alisiklik, seperti terpenoid, steroid, dan beberapa alkaloid
c. Senyawa benzenoid atau aromatik, seperti fenol dan kuinon.
d. Senyawa heterosiklik, seperti alkaloid, flavonoid, dan basa-basa nukleat.
2. Klasifikasi Berdasarkan Aktivitas Fisiologi
Biasanya pengembangan bahan alam didahului dengan pengamatan dan pengalaman empirik khasiat bahan alam tersebut untuk menyembuhkan penyakit tertentu. Oleh karena itu, salah satu cara penyelidikan bahan obat dari tumbuhan atau bahan alam lainnya adalah melalui ekstraksi dan penetapan khasiat farmakologi ekstrak, diikuti dengan isolasi komponen murni.
Sebagai contoh, berbagai steroid dengan struktur yang berbeda, aktivitas kardiotoniknya (kardenolida dan bufadienolida) ditunjukkan secara spesifik oleh (a) ikatan cis cincin A/B, (b) adanya gugus gula pada C3, dan (c) gugus lakton
(dengan 5 atau 6 atom karbon) terkonjugasi pada C17.
O
3. Klasifikasi Berdasarkan Taksonomi
telah dapat diisolasi dari berbagai genus, spesies, suku, atau ordo. Bahkan di dalam satu spesies terdapat sejumlah komponen yang memiliki struktur dasar yang berkaitan. Sebagai contoh, opium dari Papaver somniferum mengandung lebih dari 20 alkaloid seperti morfin, kodein, tebain dan narkotin yang semuanya merupakan hasil biosintesis dari prekursor 11-benzilisokuinolin dengan kopling oksidatif.
Pengetahuan tentang kandungan komponen tumbuhan berkembang dengan sangat pesat karena berkembangnya metode ekstraksi, isolasi dan karakterisasinya. Hal ini mendorong berkembangnya suatu bidang baru yang disebut kemotaksonomi (chemotaxonomy) atau sistematik kimia (chemosystematic) yang mengarah ke pembagian kandungan tumbuhan berdasarkan taksa tumbuhan. Dengan kata lain, isi kandungan tumbuhan dianggap sebagai tanda bagi evolusi dan kalsifikasi tumbuhan.
N R
4. Klasifikasi Berdasarkan Biogenesis
Biogenesis dan biosintesis memiliki arti yang sama dan sering kali digunakan tanpa perbedaan. Namun, istilah biogenesis biasanya digunakan untuk reaksi pembentukan yang masih dalam taraf hipotesis, sedangkan jika reaksi tersebut telah dibuktikan secara eksperimen, digunakan istilah biosintesis.
Berbagai teori tentang pembentukan senyawa metabolit primer dan metabolit sekunder telah dikemukakan di dalam berbagai publikasi. Diawali dengan teori aturan isoprena pada tahun 1930, yang menyatakan bahwa semua terpenoid dibentuk dari unit isoprena 5-C, dilanjutkan dengan teori poliketometilena untuk senyawa fenolik, yang merupakan saran pertama bagi biosintesis asetogenin (poliketida). Komponen pembangun utama untuk atom-atom karbon dan nitrogen di dalam semua senyawa bahan alam berasal dari 5 kelompok prekursor, yaitu:
Asetil ko-A
Malonil ko-A unit 2C(Me-C
O
) poliketida (asetogenin)
a.
b. asam sikimat unit 6C-3C (6C-1C atau 6C-2C) senyawa fenolik
c. asam mevalonat unit prenil isoprenoid
CH2=C-CH2-CH2
Me
d. unit asam amino seperti fenilanalina, tirosina, ornitina, lisina, dan triptofan
alkaloid
e. 5-5'-deoksiadenilmetionina unit 1C
2.3 Senyawa Flavonoida
Senyawa flavonoida diturunkan dari unit C6-C3 (fenil propana) yang bersumber
dari asam sikimat (via fenilalanin) dan unit C6 yang diturunkan dari jalur
poliketida. Fragmen poliketida ini disusun dari tiga molekul malonil-KoA yang bergabung dengan unit C6-C3 (sebagai KoA tioester) untuk membentuk unit awal
-C3teroksidasi (tidak jenuh) untuk menghasilkan gugus flavon, atau dihidroksilasi
pada posisi C3 cincin piranon untuk menghasilkan gugus flavanol pada flavonoid.
Sistem penomoran untuk turunan senyawa flavonoid diberikan di bawah :
O
Flavanol ini selanjutnya dioksidasi untuk menghasilkan antosianin, yang memberikan warna biru terang pada bunga dan warna anggur merah gelap. Senyawa flavonoid juga berperan dalam memberikan banyak warna lain di alam, terutama daun mahkota kuning dan jingga, bahkan flavonoid yang tidak berwarna menyerap cahaya pada spektrum UV (karena banyak gugus kromofor) dan dapat dilihat oleh banyak serangga. Senyawa ini diduga memiliki manfaat ekologi yang besar di alam berkat warnanya sebagai penarik serangga dan burung untuk membantu penyerbukan tanaman. Flavonoid tertentu juga mempengaruhi rasa makanan secara signifikan, misalnya beberapa tanaman memiliki rasa pahit dan kesat seperti glikosida flavanon naringin.
O
itu. Oleh karena itu, makanan kaya flavonoid dianggap penting untuk mengobati penyakit-penyakit, seperti kanker dan penyakit jantung (yang dapat memburuk akibat oksidasi lipoprotein densitas-rendah) (Heinrich et al, 2009).
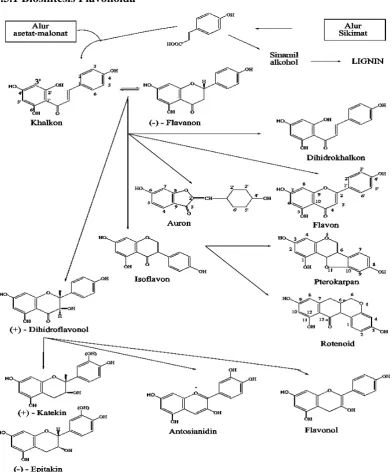
2.3.1 Biosintesis Flavonoida
Gambar 2.1Biosintesa hubungan antara jenis monomer flavonoida dari alur asetat-malonat dan alur sikimat (Markham, 1998).
Kerangka C15 yang dihasilkan, telah mempunyai substituen oksigen
sehubungan dengan pembentukan cincin A (jalur poliketida) dan dengan cincin B yang berasal dari sikimat (fenilalanina---asam sikimat). Setelah terjadi berbagai perubahan enzimatik dari ketiga atom karbon sentral dari kerangka 1,3-diaril propana dapat mempunyai berbagai gugus fungsional, misalnya hidroksil, ikatan rangkap, karbonil dan sebagainya.
2.3.2 Klasifikasi Senyawa Flavonoida
Dalam tumbuhan, flavonoid terdapat dalam berbagai bentuk struktur. Keragaman struktur flavonoid ini disebabkan karena perbedaan tahap modifikasi lanjutan dari struktur dasar flavonoid, antara lain:
1. Flavonoid O-glikosida.
Flavonoid biasanya terdapat sebagai flavonoid O-glikosida, pada senyawa tersebut satu gugus hidroksi flavonoid (atau lebih) terikat pada satu gula (atau lebih) dengan ikatan hemiasetal yang tak tahan asam. Pengaruh glikosilasi meyebabkan flavonoid menjadi kurang reaktif dan lebih mudah larut dalam air (cairan). Glukosa merupakan gula yang paling umum terlibat, walaupun galaktosa, ramnosa, xilosa, dan arabinosa sering juga terdapat. Gula lain yang ditemukan adalah alosa, manosa, fruktosa, apiosa dan asam glukuronat serta galakturonat.
2. Flavonoid C-glikosida.
3. Flavonoid Sulfat
Gabungan flavonoid lain yang mudah larut dalam air yang mungkin ditemukan hanya flavonoid sulfat. Senyawa ini mengandung satu ion sulfat atau lebih, yang terikat pada hidroksil fenol atau gula.
4. Biflavonoid
Biflavonod adalah flavonoid dimer, walau pun prosianidin dimer (satuan dasarnya katekin) biasanya tidak dimasukkan ke dalam golongan ini. Flavonoid yang biasanya terlibat adalah flavon dan flavanon yang secara biosintesis mempunyai pola oksigenasi yang sederhana 5,7,4’ (atau kadang-kadang 5,7,3’,4’) dan ikatan antar-flavonoid berupa ikatan karbon-karbon atau kadang-kadang ikatan eter. Biflavonoid jarang ditemukan sebagai glikosida, dan penyebarannya terbatas, terdapat terutama pada gimnospermae.
5. Aglikon flavonoid yang aktif-optik
Aglikon flavonoid mempunyai atom karbon asimetrik dan dengan demikian menunjukkan keaktifan optik (yaitu memutar cahaya terpolarisasi-datar). Yang termasuk dalam golongan flavonid ini ialah flavanon, dihidroflavonol, katekin, pterokarpan, rotenoid, dan beberapa biflavonoid. (Markham, 1988)
Menurut Robinson (1995), flavonoid dapat dikelompokkan berdasarkan tahanan oksidasi dan keragaman lain pada rantai C3 :
1. Flavon
O
O A C
B
2. Flavonol
Flavonol sangat tersebar luas di dalam tumbuhan, baik sebagai kopigmen antosianin dalam daun bunga maupun dalam daun tumbuhan tinggi. Dalam tumbuhan terdapat banyak sekali glikosida flavonol.Sampai saat ini yang paling umum adalah kuersetin 3-rutinosida yang dikenal sebagai rutin.
O
O
OH A C
B
3. Isoflavon
Isoflavon merupakan senyawa yang tidak begitu mencolok, tetapi senyawa ini penting sebagai fitoaleksin (senyawa pelindung) dalam tumbuhan untuk pertahanan terhadap penyakit.Isoflavon menunjukkan aktivitas sebagai estrogenik, insektisida, dan antifungi.Beberapa diantaranya berguna untuk racun tikus.
O
O
A C
B
4. Flavanon
dengan serbuk Mg dan HClpekat.Diantara flavonoida hanya flavon yang menghasilkan warna merah ceri kuat.
O
O A C
B
5. Flavanonol
Flavanonol (atau dihidroflavonol) barangkali merupakan flavonoid yang paling kurang dikenal, dan tidak dapat diketahui apakah senyawa ini terdapat sebagai glikosida. Senyawa ini stabil dalam asam klorida panas tetapi terurai oleh udara (Harborne, 1987).
O
O
OH A C
B
6. Antosianin
Antosianin adalah pigmen daun bunga merah sampai biru yang biasa, banyaknya sampai 30% bobot kering dalam beberapa bunga. Antosianin terdapat juga dalam bagian lain tumbuhan tinggi kecuali fungus. Antosianin selalu terdapat dalam bentuk glikosida.
O
OH A C
B +
7. Katekin
O
Merupakan monomer flavan 3,4-diol, leukoantosianidin jarang terdapat sebagai glikosida, namun beberapa bentuk glikosida yang dikenal adalah apiferol, dan peltoginol.
Khalkon adalah pigmen fenol kuning yang berwarna coklat tua dengan sinar UV bila dikromatografi kertas. Aglikon khalkon dapat dibedakan dari glikosidanya karena hanya pigmen dalam bentuk glikosida yang dapat bergerak pada kromatografi kertas dalam pengembang air (Harborne, 1987).
A
O
B
10.Auron
O
O
CH
A
B
2.4Skrining Fitokimia
Banyak reagen yang dapat digunakan untuk mengetahui keberadaan dari flavonoid, meskipun beberapa juga akan bereaksi positif dengan senyawa polifenol. Reagen yang biasa digunakan adalah :
1. Shinoda Test, yaitu dengan menambahkan serbuk magnesium pada ekstrak sampel dan beberapa tetes HCl pekat, warna orange, pink, merah sampai ungu akan terjadi pada senyawa flavon, flavonol, turunan 2,3-dihidro dan xanton. Penggunaan zinc sebagai pengganti magnesium dapat dilakukan, dimana hanya flavanonol yang memberikan perubahan warna merah pekat sampai magenta, flavanon dan flavonol akan memberi warna merah muda yang lemah sampai magenta.
2. H2SO4(p), flavon dan flavonol akan memberikan perubahan larutan kuning
pekat. Kalkon dan auron menghasilkan larutan berwarna merah atau merah kebiru-biruan. Flavanon memberikan warna orange sampai merah.
3. NaOH 10% , menghasilkan larutan biru violet
4. FeCl3 5% telah digunakan secara luas untuk mengidentifikasi senyawa
fenol, tetapi tidak dapat digunakan untuk membedakan macam-macam golongan flavonoid. Pereaksi ini memberi warna kehijauan, warna biru, dan warna hitam-biru (Sarker, 2006).
2.5Teknik Pemisahan
Ada 2 jenis teknik pemisahan:
1. Pemisahan kimia adalah suatu teknik pemisahan yang berdasarkan adanya perbedaan yang besar dari sifat-sifat fisika komponen dalam campuran yang akan dipisahkan.
2. Pemisahan fisika adalah suatu teknik pemisahan yang didasarkan pada perbedaan-perbedaan kecil dari sifat-sifat fisik antara senyawa-senyawa yang termasuk dalam satu golongan. (Muldja, 1995)
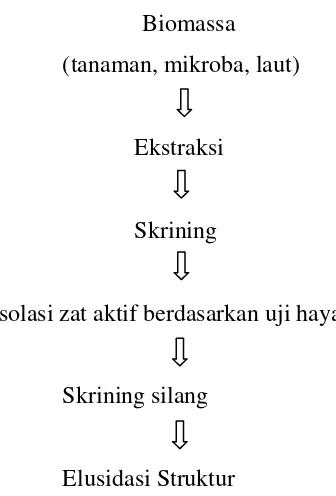
Biomassa (tanaman, mikroba, laut)
Ekstraksi
Skrining
Isolasi zat aktif berdasarkan uji hayati
Skrining silang
Elusidasi Struktur
Gambar 2.3 Skema Teknik Pemisahan Metabolit Sekunder
2.5.1 Ekstraksi
Jika telah dikeringkan, biomassa kemudian digiling menjadi partikel-partikel kecil menggunakan blender atau penggilingan. Proses penggilingan ini penting karena ektraksi efektif pada partikel kecil, dikarenakan memiliki luas permukaan yang lebih besar.
Pemilihan pelarut ekstraksi sangat penting. Jika tanaman diteliti dari sudut pandang etnobotani, ektraksi harus mengikuti pemakaiannya secara tradisional. Kegagalan mengekstraksi biomassa dapat menyebabkan kehilangan akses untuk mendapatkan zat aktif.
Terdapat sejumlah metode ekstraksi, yang paling sederhana adalah ekstraksi dingin (dalam labu besar berisi biomassa), dengan cara ini bahan kering hasil gilingan diekstraksi pada suhu kamar secara berturut-turut dengan pelarut yang kepolarannya makin tinggi. Keuntungan utama cara ini adalah merupakan metode ekstraksi yang mudah karena ekstrak tidak dipanaskan sehingga kemungkinan kecil bahan alam terurai. Penggunaan pelarut dengan peningkatan kepolaran secara berurutan memungkinkan pemisahan bahan alam berdasarkan kelarutannya (dan polaritasnya) dalam ektraksi. Hal ini sangat mempermudah proses isolasi. Ekstraksi dingin memungkinkan banyak senyawa terekstraksi, meskipun beberapa senyawa memiliki kelarutan terbatas dalam pelarut ekstraksi pada suhu kamar. (Heinrich et al, 2009)
Ekstraksi dianggap selesai bila tetesan terakhir memberikan reaksi negatif terhadap senyawa yang diekstraksi. Untuk mendapatkan larutan ekstrak pekat, biasanya pelarut ekstrak diuapkan dengan menggunakan alat rotari evaporator. (Harborne, 1996)
2.5.2 Partisi
dilakukan secara terus menerus dengan menggunakan dua pelarut yang tak bercampur yang kepolarannya meningkat. Partisi biasanya dilakukan melalui dua tahap:
1. Air/petroleum eter ringan (heksana) untuk menghasilkan fraksi nonpolar di lapisan organik
2. Air/diklorometan atau air/kloroform atau air/etil asetat untuk membuat fraksi agak polar di lapisan organik. Ini merupakan metode pemisahan yang mudah dan mengandalkan kelarutan bahan alam dan bukan interaksi fisik dengan medium lain (Heinrich et al, 2009).
2.5.3 Hidrolisis
Prosedur yang digunakan untuk hidrolisis asam dari flavonoid glikosida adalah, sebanyak 2 mg sampel flavonoid glikosida dicampur dengan asam klorida 6% sebanyak 5 ml dengan jumlah metanol yang sangat sedikit pada sampel untuk membuat proses hidrolisis menjadi sempurna. Larutan dipanaskan selama 45 menit lalu didinginkan, kemudian ekstrak sepenuhnya dilarutkan dengan eter. Penguapan dari larutan akan mengendapkan ramnosa dan glukosa. Lapisan eter, setelah dikeringkan dengan menggunakan natrium sulfat akan didapatkan aglikon flavonoid setelah diuapkan (Mabry et al, 1970).
2.5.4 Kromatografi
Kromatografi pertama kali dikembangkan oleh seorang ahli botani Rusia Michael Tswett pada tahun 1903 untuk memisahkan pigmen berwarna dalam tanaman dengan cara perkolasi ekstrak petroleum eter dalam kolom gelas yang berisi kalsium karbonat (CaCO3). Kromatografi merupakan suatu teknik pemisahan
Kromatografi dapat dibedakan atas berbagai macam tergantung pada pengelompokkannya. Berdasarkan pada mekanisme pemisahannya, kromatografi dibedakan menjadi: kromatografi adsorbsi, kromatografi partisi, kromatografi pasangan ion, kromatografi penukar ion, kromatografi eksklusi ukuran. Berdasarkan pada alat yang digunakan, kromatografi dapat dibagi atas: kromatografi kertas, kromatografi lapis tipis (disebut juga kromatografi planar), kromatografi cair kinerja tinggi, dan kromatogtrafi gas. Bentuk kromatografi yang paling awal adalah kromatografi kolom yang digunakan untuk pemisahan sampel dalam jumlah yang besar.
Pemisahan pada kromatografi planar pada umumnya dihentikan sebelum semua fase gerak melewati seluruh permukaan fase diam. Solut pada kedua kromatografi ini dikarakterisasi dengan jarak migrasi solut terhadap jarak ujung fase geraknya. Nilai faktor retardasi solut (Rf) dapat dihitung dengan menggunakan perbandingan dalam persamaan:
Rf= Jarak yang ditempuh solut Jarak yang ditempuh fase gerak
Nilai maksimum Rf adalah 1 dan ini dicapai ketika solut mempunyai perbandingan distribusi (D) dan faktor retensi sama dengan 0 yang berarti solut bermigrasi dengan kecepatan yang sama dengan fase gerak. Nilai minimum Rf adalah 0 dan ini teramati jika solut tertahan pada posisi titik awal di permukaan fase diam.
Proses Sorpsi
atau lebih mekanisme ini terlibat dalam satu jenis kromatografi. Keempat jenis tersebut adalah adsorpsi, partisi, pertukaran ion, dan eksklusi ukuran.
Adsorben
Silika gel merupakan jenis adsorben (fase diam) yang penggunaannya paling luas. Permukaan silika gel terdiri atas gugus Si-O-Si dan gugus silanol (Si-OH). Gugus silanol bersifat sedikit asam dan polar karenanya gugus ini mampu membentuk ikatan hidrogen dengan solut-solut yang agak polar sampai sangat polar.
Adanya air dari atmosfer yang diserap oleh permukaan silika gel mampu mendeaktifkan permukaan silika gel karena air akan menutup sisi aktif silika gel. Hal seperti ini dapat diatasi dengan memanaskan pada suhu 1050C, meskipun demikian reprodusibilitasnya sulit dicapai kecuali jika suhu dan kelembapan benar-benar dijaga secara hati-hati. Semakin polar solut maka akan semakin tertahan kuat ke dalam adsorben silika gel ini (Gandjar dkk, 2007).
Tabel 2.1 Daftar Adsorben pada Kromatografi
Jenis adsorben Kepolaran
Alumina
Karbon aktif (Charcoal) Silika gel
Magnesium silikat Selulosa
Resin-resin polimerik (stiren/difenil benzen)
(paling polar)
(paling non polar)
2.5.4.1Kromatografi Lapis Tipis
dengan menggunakan pipa mikrokapilaritas. Plat dikembangkan dengan meletakkannya didalam botol ataupun chamber pengembang yang berisi sejumlah kecil pelarut. Pelarut akan menaiki plat dengan adanya gaya kapilar, dan membawa senyawa dari sampel dengan itu. Senyawa yang berbeda dipisahkan dari dasarnya pada saat interaksi mereka dengan lapisan adsorben.
Plat KLT yang biasa digunakan adalah plat dengan ukuran pori silika 60 Å dan ketebalan lapisan 25 µm dalam penyangga poliester atau aluminium, beberapa dengan menggunakan atau tanpa menggunakan indikator fluorosensi yang sesuai untuk analisa cepat dari ekstrak kasar tanaman dan digunakan sebagai dasar dari langkah preparatif. Plat biasa dapat digunting dengan menggunakan gunting atau kertas cutter untuk mengambil ukuran yang diinginkan. Deteksi noda yang dihasilkan dapat menggunakan lampu ultraviolet ataupun dengan menyemprot dengan menggunakan reagen yang sesuai (Cseke et al, 2006).
2.5.4.2 Kromatografi Kolom
Kolom kromatografi atau tabung untuk pengaliran karena gaya tarik bumi (gravitasi) atau sistem bertekanan rendah biasanya terbuat dari kaca yang dilengkapi keran jenis tertentu pada bagian bawahnya untuk mengatur aliran pelarut. Ukuran keseluruhan kolom sungguh beragam, tetapi biasanya panjangnya sekurang-kurangnya 10 kali garis tengah dalamnya dan mungkin saja sampai 100 kalinya. Ukuran kolom dan banyaknya penjerap yang dipakai ditentukan oleh bobot campuran sampel yang akan dipisahkan.
Fraksi kolom yang mengandung senyawa yang sama (diperiksa dengan KLT) atau tampaknya berasal dari satu puncak (memakai pendeteksian sinambung) digabungkan, dan pelarutnya diuapkan, lebih baik dengan tekanan rendah. Jika pelarut dan penjerap murni. Maka fraksi-fraksi pun murni (Gritter dkk, 1991).
2.5.4.3 Kromatografi Lapis Tipis Preparatif
Sebagian besar pemakaian kromatografi lapis tipis preparatif hanya dalam jumlah miligram. Kromatografi lapis tipis preparatif bersama-sama dengan kromatografi kolom terbuka, dijumpai sebagian besar dalam isolasi bahan alam. Penjerap yang paling umum digunakan adalah silika gel dan dipakai untuk pemisahan campuran senyawa lipofil maupun campuran senyawa hidrofil. Ukuran partikel dan porinya kurang lebih sama dengan ukuran tingkat KLT.
Cuplikan sebanyak 10-100 mg dapat dipisahkan pada lapisan silika gel atau aluminium oksida 20 x 20 cm yang tebalnya 1 mm. Pengembangan plat KLTP biasanya dilakukan dalam bejana kaca yang dapat menampung beberapa plat. Bejana dijaga tetap jenuh dengan pelarut pengembang dengan bantuan sehelai kertas saring yang tercelup ke dalam pengembang.
2.6 Teknik Spektroskopi
Teknik analisis modern mencakup berbagai teknik analisis instrumen elektronika yang dikembangkan untuk mengukur parameter fisika dan kimia alami yang khas dan tetap dari atom atau molekul. Parameter khas yang bermakna untuk analisis adalah absorpsi dan emisi energi radiasi elektromagnet oleh atom atau molekul.
Teknik analisis spektroskopi berasaskan antaraksi radiasi elektromagnet dengan komponen atom atau molekul yang menghasilkan fenomena bermakna sebagai parameter analisis. Karena pada setiap teknik spektroskopi antaraksi radiasi elektromagnet dengan komponen atom/ molekul khas dan tidak semuanya sama, uraian teknik analisis didahului dengan mekanisme antaraksi tersebut, serta fenomena yang dipakai sebagai parameter analisisnya (Satiadarma dkk, 1995).
2.6.1 Spektroskopi Ultraviolet (UV-Vis)
Senyawa polifenol memiliki dua karakteristik pita penyerapan Ultraviolet dengan maksimal jarak 240 sampai 285 nm dan 300 sampai 550 nm. Berbagai macam golongan flavonoid dapat dikenali dari spektrum UV mereka masing-masing, karakteristik spektra UV dari masing-masing flavonoid yang mengandung jumlah dari golongan hidroksil aglikon, pola substituen glikosida, dan golongan asil aromatik bahan alam.
Saat ini penggunaan Spektroskopi UV-Visible paling sering digunakan dalam aplikasi untuk analisa kuantitatif, dan nilai dari metode ini dapat mengurangi perbandingan informasi yang banyak dari teknik spektroskopi yang lainnya seperti NMR dan MS (Andersen, 2006).
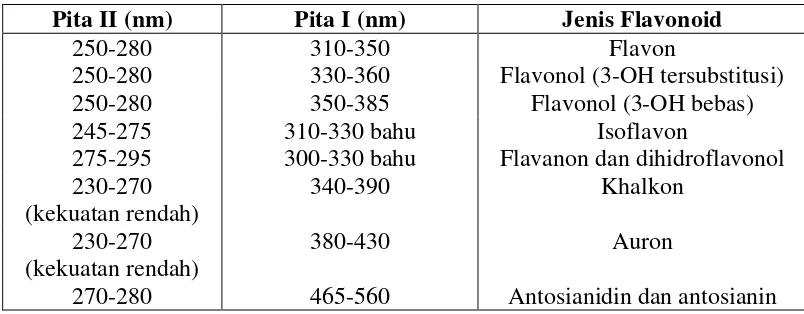
Ciri spektrum khas jenis flavonoid utama dengan pola oksigenasi yang setara disajikan pada tabel dibawah :
Tabel 2.2 Rentangan Serapan Spektrum UV-Visible golongan Flavonoida
Pita II (nm) Pita I (nm) Jenis Flavonoid
250-280 310-350 Flavon
250-280 330-360 Flavonol (3-OH tersubstitusi)
250-280 350-385 Flavonol (3-OH bebas)
245-275 310-330 bahu Isoflavon
275-295 300-330 bahu Flavanon dan dihidroflavonol 230-270
270-280 465-560 Antosianidin dan antosianin
Perubahan penyulihan pada cincin A cenderung tercerminkan pada serapan pita II, sedangkan perubahan penyulihan pada cincin B dan C cenderung lebih jelas tercermin pada serapan pita I (Markham, 1988).
2.6.2 Spektroskopi Inframerah (FT-IR)
Spektrum inframerah suatu molekul adalah hasil transisi antara tingkat energi getaran (vibrasi) yang berlainan. Inti-inti atom yang terikat oleh ikatan kovalen mengalami getaran (vibrasi) atau osilasi (oscillation) dengan cara serupa dengan dua bola yang terikat oleh suatu pegas.
diserap. Ikatan nonpolar (seperti C-H atau C-C) menyebabkan absorpsi lemah, sedangkan ikatan polar (seperti misalnya O-H, N-H, dan C=O) menunjukkan absorpsi yang lebih kuat.
Suatu ikatan dalam sebuah molekul dapat mengalami berbagai vibrasi molekul. Secara umum terdapat dua tipe vibrasi molekul:
1. Streching (vibrasi regang/ulur): vibrasi sepanjang ikatan sehingga terjadi perpanjangan atau pemendekan ikatan.
2. Bending (vibrasi lentur/tekuk): vibrasi yang disebabkan oleh sudut ikatan sehingga terjadi pembesaran atau pengecilan sudut ikatan.
Oleh karena itu suatu ikatan tertentu dapat menyerap energi lebih dari satu panjang gelombang. Contohnya, ikatan O-H menyerap energi pada frekuensi 3330 cm-1, energi pada panjang gelombang ini menyebabkan kenaikan vibrasi regang ikatan O-H itu. Suatu ikatan O-H itu juga menyerap pada kira-kira 1250 cm-1, energi pada panjang gelombang ini menyebabkan kenaikan vibrasi lentur. Tipe vibrasi yang berlain-lainan ini disebut cara vibrasi fundamental (Supratman, 2010).
2.6.3 Spektroskopi Resonansi Magnetik Inti Proton (1H-NMR)
Setelah spektroskopi inframerah, spektroskopi resonansi magnetik inti (NMR) adalah yang metode yang paling penting digunakan dalam kimia organik. Dalam spektroskopi inframerah mengandung infromasi mengenai adanya gugus fungsi pada molekul, sedangkan spektroskopi NMR memberikan informasi mengenai jumlah dari masing-masing hidrogen.
Pergeseran kimia dalam unit δ ditunjukkan dalam jumlah resonansi proton yang
bergeser dari TMS dalam bagian per juta (ppm) dari frekuensi dasar spektroskopi
δ= pergeseran dalam Hz
frekuensi spektrometer dalam MHz
Unsur dasar dari spektrometer nmr adalah ilustrasi skematis. Sampel dilarutkan dalam pelarut yang tidak memiliki proton (biasanya CCl4) dan dalam
jumlah yang kecil dari TMS yang ditambahkan sebagai pusat referensi internal.
Semua proton dalam molekul yang identik dalam lingkungan kimia akan memiliki pergerseran kimia yang sama. Dengan demikian, semua proton dari TMS atau semua proton dalam benzena, siklopentana, atau aseton memiliki nilai