Hasil dan Pembahasan Ikatan Ion pada Kristal A. ELF Topologi dan Senyawa Ionik
Untuk mengkarakterisasi fitur utama dari pasangan elektron dalam Kristal ionic, kita akan fokus pada rocksalt (B1) tahap LiF sebagai patokan. Kesimpulan yang sama berasal untuk semua senyawa keluarga Kristal AX.
Hasil untuk identifikasi penarikan ELF dan bips yang ditunjukkan pada tabel 1. Seperti yang telah diamati oleh Savin et al, pasangan elektron
didistribusikan ke atom elektron sekitar inti (terdekat), dimana satu kulit untuk litium (inti kulit-K, K (Li)) dan dua untuk flour (inti kulit K, K (F) dan valensi kulit L, L (F)). Tidak ada elektron yang berhubungan dengan cekungan ikatan. Kulit hampir bulat sempurna mengisi peralihan yang diamati sehingga
menimbulkan dua kulit di F dan satu kulit di L+.
1. Titik Kritis dan Kulit Pasangan Elektron
Beberapa valensi maxima terjadi dalam kulit kedua F-, dimana kita menemukan
Tabel 2 merangkum pengaturan SEP untuk alkil halide lainnya. Jumlah dan distribusi valensi SEP penarik mengungkapkan polarisasi ion dan kuatnya interaksi dalam Kristal. Distribusi penarik SEP di Kristal alkil halida dibedakan menjadi 3 pola : octahedral (oh), kubik (c), dan pola yang lebih rumit (v). Semua kation menunjukkan pengaturan SEP kubik. Untuk anion, ketika kation berukuran kecil yang terlibat, polarisasi muncul didaerah tetangga terdekat terdekat (6 kation) sehingga menimbulkan suatu pengaturan octahedral (misalnya LiCl pada gambar 1). Pola ikatan mereka didominasi oleh interaksi kation-anion. Sebagai anion menjadi lebih terpolarisasi, sedangkan pola muncul lebih kompleks untuk topologi valensi yang menunjukkan sebagai V (untuk berbagai bentuk). Misalnya Br- di LiBr. Sehingga, jika kedua ion memiliki
kekerasan yang sama, tidak satu pun dari mereka mampu mempolarisasi ion lawannya. Sehingga, apabila SEP muncul pada daerah tetangga kedua dominasi yang tersorot yaitu interaksi antara ion –ion contohnya pada gambar 1 bagian b (untuk KF).
2. Valensi
Seperti yang diharapkan , pada penelitian ini telah diamati (pada tabel 2) bahwa perbedaan terbesar muncul untuk kulit terluar baik kation maupun anion. Dalam kasus Li+ dan Na+, nilai-nilai ΔELF sangat rendah dan sangat berbeda
(kecuali dalam NaF) dari nilai-nilai ΔELF dari anion (Tabel 2). Dalam kasus ini, kulit terluar anion ini, yaitu kristal valensi, terutama bertanggung jawab untuk kristal menanggapi tekanan fisik dan kimia. Sebagai kation menjadi lebih lembut dan atau deformasi kation menjadi mirip dengan salah satu anion, baik ion berkontribusi pada kristal valensi (misalnya, di NaF). kristal ini adalah orang-orang yang menimbulkan pengaturan C-C dari SEP.
3. Jari-Jari Ion
4. Ionik polyhedra
The Wigner-Seitz sel dalam struktur rocksalt yang dapat mengadopsi dua bentuk. Jika rA / rX cukup dekat dengan kesatuan, kedua ion diasumsikan menunjukkan bentuk kubik (bentuk II). Jika rasio jelas berbeda dari satu, ion yang lebih besar mengadopsi bentuk cuboctahedron, sedangkan ion yang lebih kecil mengisi kiri-atas lubang kubik (bentuk I).
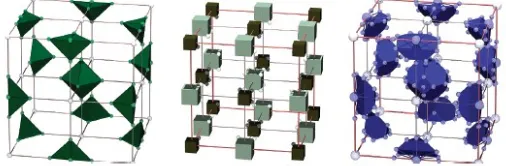
Contoh ditunjukkan di bagian a-c Gambar 4, di mana bola kecil menunjukkan posisi ELF minimum dan tetap hijau gelap menunjukkan sel-sel ionic yang sesuai. Hasil untuk keseluruhan set dikumpulkan pada Tabel 3. Semua kecuali dua dari halida alkali menunjukkan bentuk I.
bentuk polyhedral diambil oleh ion-ion dalam kerangka ELF secara langsung mereka berhubungan dengan ukuran 3D, tidak hanya untuk jari-jari mereka.
5. Volume ion