VALIDASI METODE THIN-LAYER CHROMATOGRAPHY
(TLC)-DENSITOMETRI PADA PENETAPAN KADAR KAFEIN DALAM
KOPI
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
i
VALIDASI METODE THIN-LAYER CHROMATOGRAPHY
(TLC)-DENSITOMETRI PADA PENETAPAN KADAR
KAFEIN DALAM KOPI
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
iv
HALAMAN PERSEMBAHAN
Karya ini kupersembahkan kepada Tuhan Yesus Kristus, yang selalu merancang hal indah diluar ekspektasiku, yang selalu menyediakan hal-hal luar biasa yang
tidak pernah dilihat, didengar maupun timbul dari dalam hati. Kepada Papi, Mami, dan Adik sebagai bentuk pencapaian atas doa dan dukungan. Kepada keluarga dan sahabat setia yang selalu mendukung. Serta almamater Universitas
vi PRAKATA
Puji dan syukur penulis panjatkan kepada Tuhan Yesus Kristus atas segala berkat dan karunia-Nya sehingga penelitian dan penyusunan skripsi yang berjudul “Validasi Metode Thin-Layer Chromatography (TLC)-Densitometri pada Penetapan Kadar Kafein dalam Kopi” dapat selesai dengan baik. Skripsi ini disusun sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi (S.Farm) di Fakultas Farmasi, Universitas Sanata Dharma, Yogyakarta.
Selama proses penelitian berlangsung hingga selesai penulis mendapat banyak dukungan dan bantuan dari berbagai pihak. Oleh karena itu, penulis ingin menyampaikan terima kasih kepada:
1. Ibu Yustina Sri Hartini, M.Si., Apt. selaku Dekan Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
2. Ibu Christine Patramurti, M.Si., Apt. selaku Ketua Program Studi Fakultas Farmasi Universitas Sanata Dharma Yogyakarta, sekaligus selaku dosen pembimbing yang telah bersedia membimbing dengan kesabaran, dukungan, arahan, serta saran selama proses penelitian hingga berakhirnya skripsi.
3. Bapak Maywan Hariono, M.Sc., Ph.D., Apt.selaku dosen penguji untuk segala masukan, kritik, dan saran hingga skripsi tersusun.
4. Bapak Michael Raharja Gani M.Farm., Apt. selaku dosen penguji untuk untuk segala masukan, kritik, dan saran hingga skripsi tersusun.
5. Ibu Rita Suhadi M.Si., Apt. selaku Dosen Pembimbing Akademik atas bimbingannya selama ini.
6. Ibu Damiana Sapta Candrasari S.Si. M.Sc. selaku Kepala Penanggung jawab Laboratorium Fakultas Farmasi yang telah memberikan izin penggunaan laboratorium untuk kepentingan penelitian.
7. Laboran Mas Bimo, Pak Kayat, Pak Parlan yang baik hati membantu, menemani, dan mendukung proses penelitian di laboratorium.
vii
9. Rekan penelitian Cinna Cindy dan Galung Istri Setyoningsih, untuk dukungan, pengertian, dan bantuan sehingga mampu melewati suka-duka proses penelitian untuk menyelesaikan skripsi.
ix DAFTAR ISI
Halaman
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
PERNYATAAN PERSETUJUAN PUBLIKASI ... v
PRAKATA ... vi
PERNYATAAN KEASLIAN KARYA ... vii
DAFTAR ISI ... viii
HASIL DAN PEMBAHASAN ... 9
KESIMPULAN ... 18
SARAN ... 18
DAFTAR PUSTAKA ... 19
LAMPIRAN ... 21
x
DAFTAR TABEL
Tabel I. Nilai recovery yang diterima untuk berbagai konsentrasi sampel ... 8
Tabel II. Nilai presisi yang diharapkan untuk bermacam konsentrasi sampel ... 8
Tabel III. Data resolusi kafein ... 12
Tabel IV. Data perolehan AUC dari enam seri baku kafein ... 14
Tabel V. Data akurasi dan presisi larutan seri baku kafein ... 16
xi
DAFTAR GAMBAR
xii
DAFTAR LAMPIRAN
Lampiran 1. Sertifikat analisis standar kafein ... 21
Lampiran 2. Kemasan sampel kopi bubuk ... 22
Lampiran 3. Contoh perhitungan konsentrasi larutan kafein ... 24
Lampiran 4. Spektrum panjang gelombang kafein ... 25
Lampiran 5. Hasil kromatogram kurva baku 3x replikasi... 27
Lampiran 6. Kromatogram seri baku kafein – linearitas ... 38
Lampiran 7. Kromatogram seri baku kafein – akurasi dan presisi ... 42
xiii INTISARI
Kafein atau 1,3,7-trimetilksantin adalah senyawa alkaloid yang ditemukan dalam tanaman kopi, teh, yerba mate, dsb. Kafein dapat meningkatkan kinerja, kewaspadaan, dan kinerja seseorang. Namun penggunaan kafein berlebihan yakni, ≥200mg dapat menyebabkan insomnia, sakit kepala, gugup, sehingga diperlukan penetapan kadar kafein pada kopi. Penelitian ini bertujuan untuk memvalidasi metode TLC-Densitometri pada penetapan kadar kafein dalam kopi bubuk murni.
Penelitian ini bersifat non-eksperimental deskriptif. Metode yang digunakan yaitu Kromatografi Lapis Tipis (KLT)-Densitometri dengan menggunakan fase diam silika gel 60 GF254, komposisi fase gerak metanol:
etil asetat: ammonia 25% (13:77:10), volume yang dianalisis 2µ L, dan panjang gelombang pengamatan 275nm.
Parameter validasi metode yang digunakan pada penelitian meliputi selektivitas, linearitas dan rentang, akurasi, dan presisi. Hasil yang diperoleh menunjukkan hasil selektivitas yang baik dengan nilai resolusi (Rs) 4,545 pada sampel kopi, dan 5,400 pada sampel kopi dengan penambahan baku kafein (150ppm) serta linearitas yang baik dengan nilai koefisien korelasi (r) 0,9980. Nilai akurasi dan koefisien variasi yang baik untuk baku kafein pada konsentrasi 350 ppm dan 450 ppm secara berturut-turut adalah 10,943; 3,1554% dan 15,925; 3,6898%. Rentang pengukuran pada konsentrasi 150-750 ppm. Berdasarkan hasil tersebut, maka metode ini memiliki validitas yang baik untuk penetapan kadar kafein dalam kopi bubuk.
xiv ABSTRACT
Caffeine also known as 1,3,7 trimethylxanthine is an alkaloid compound that can be found in coffee, tea, and yerba mate plant. Caffeine in body has effect in enhancing both performance and allertness. The excessive intake of caffeine more than 200mg/day would cause many effect such as insomnia, headache, and nervous. So, it is necessary to determine caffeine concentration in coffee. This study aims to validate the Thin-Layer Chromatography-Densitometry method to determine caffeine concentration in coffee powder.
This is non-experimental descriptive research using TLC-Densitometry method by using silica gel 60 GF254 as stationary phase, methanol-ethyl
acetate-ammonia 25% (13:77:10) as the mobile phase, sample volume 2µL, solvent front within 75mm and wavelength detection at 275nm.
Validity parameter is defined basing on selectivity, linearity and range, accuracy, and precission. The result shows that the method has good selectivity with the resolution (Rs) of coffee sample was 4,545 and coffee sample with caffeine addition (150ppm) was 5,400, a good linearity with coefficient correlation (r) 0,9980. Recovery value and coefficient variation of caffeine standard at the concentration 350 ppm and 450 ppm were 10,943; 3,1554% and 15,925; 3,6898% respectively. The series of standard curve concentration was within 150-750 ppm. In conclusion, this method is valid to determine caffeine concentration in coffee powder.
1 PENDAHULUAN
Kopi adalah tumbuhan yang hidup di tempat tropis dan subtropis, terlebih pada bagian ekuator dengan kondisi ketinggian di antara 200-2000 meter pada suhu 18-22℃. Ada banyak jenis spesies kopi, contohnya yang terkenal adalah kopi arabika (Coffea arabica L.)dan kopi robusta (Coffea robusta L.) (Patay, Bencsik, Papp, 2016).
Kopi mengandung senyawa alkaloid kafein, serta beberapa antioksidan. Kafein atau 1,3,7-trimethylxanthine terdapat di lebih dari 60 spesies tanaman subtropis seperti pada teh, biji kakao, kopi, dan tanaman yerba mate. Secara farmakologis kafein diketahui dapat mengatasi berbagai penyakit seperti asma, hidung tersumbat, serta pusing atau sakit kepala (Preedy, 2012). Kafein juga diketahui dapat meningkatkan daya ingat, meningkatkan tingkat kewaspadaan, serta memperbaiki suasana hati/psikorelaksan (Alsunni, 2015). Oleh karena itu kopi banyak dimanfaatkan oleh masyarakat, bukan hanya sekedar minuman, tapi guna mendapatkan efek yang membantu mengoptimalkan produktivitas sehari-hari.
2
adalah dengan menetapkan kadar kafein yang terdapat dalam satu bungkus kopi agar tiap kali penyajian kopi memenuhi batas konsumsi kafein harian.
Beberapa penelitian kafein menggunakan metode TLC-Densitometri telah dilakukan, di antaranya adalah Palacios, et al (2017) yang meneliti tentang kadar kafein dengan sampel tablet parasetamol-kafein; serbuk kopi; dan minuman berenergi; menggunakan fase diam silika gel 60 G; komposisi fase gerak etil asetat-metanol-ammonium hidroksida (85:10:5), Torres, et al (2015) menggunakan sampel minuman berenergi; fase gerak metanol-etil asetat (3:1); fase diam polyester backed silica gel, Bochenska (2013) menggunakan sampel tablet; fase gerak heksana-aseton-asam asetat glasial (5:5:1); fase diam silika gel 60 F254.
Penelitian oleh Isnindar, dkk (2016) melakukan metode optimasi isolasi “Optimization Method of Caffeine Isolation of Merapi Green Coffee beans” menggunakan komposisi fase gerak kloroform : etil asetat (1:3), fase diam silika gel F254 mampu menghasilkan pemisahan yang baik pada kafein kopi. Selain itu,
penelitian oleh Riswanto, dkk (2015) tentang “Validasi dan determinasi piridoksin, nikotinamid, dan kafein pada minuman berenergi menggunakan TLC-Densitometri”, telah memberikan hasil yang memenuhi parameter akurasi, presisi, linearitas, selektivitas, dan rentang.
3 METODE PENELITIAN
Bahan
Bahan yang digunakan yaitu sampel kopi bubuk merek “X”, baku kafein (Certificate of Analysis no. 001/WS/I/2018), plat silika gel F254, metanol (analytical
grade), etil asetat (analytical grade), ammonia 25% (analytical grade),
aquadestilata.
Alat dan instrumentasi
Alat yang digunakan yaitu seperangkat alat densitometer (CAMAG TLC Scanner 3 CAT. No. 0277.6485 SER. No. 160602), autosampler (CAMAG Linomat 5 CAT. No. 027.7808. SER. No. 170610), neraca kasar, neraca analitik (Scaltec SBC 22 max 60/210 g; min 0,001 g; d=0,01/0,1 mg; e=1 mg), seperangkat komputer merk Dell B6RDZ1S Connexant System RD01-D850 A03-0382 JP France S.A.S, peralatan gelas (gelas beaker, labu takar), pipet volume, CAMAG
flat bottom chamber, oven (POSTBUS 7018-3502 KA Ultretch), mikrotube, mikropipet 100-1000μL (Socorex ACURA 825).
Metode Penelitian Pembuatan fase gerak
Fase gerak yang digunakan terdiri dari metanol, etil asetat & ammonia 25%. Fase gerak ini dipilih dengan mengacu pada penelitian Riswanto, dkk (2015). Pencampuran fase gerak dilakukan di dalam labu takar 100mL dengan perbandingan metanol : etil asetat : ammonia 25% (13:77:10) v/v.
Penjenuhan chamber/bejana
Fase gerak yang akan digunakan metanol : etil asetat : ammonia 25% (13:77:10) dituang ke dalam dasar bejana/chamber, dicelupkan kertas saring pada fase gerak. Bejana ditutup, lalu fase gerak dibiarkan menguap hingga membasahi kertas saring selama kurang lebih 1 jam atau bila fase gerak telah mencapai tujuh perdelapan tinggi kertas saring (FI V, 2014).
Aktivasi plat KLT silika gel F254
Plat silika gel 60 GF254 dengan ukuran 20x20cm disiapkan, kemudian
4 Pembuatan larutan stok kafein
Baku kafein ditimbang seksama lebih kurang 50,0mg. Kafein dilarutkan dengan metanol (pro analysis grade) hingga batas tanda di dalam labu takar 50mL sehingga didapat konsentrasi larutan stok kafein 1000ppm.
Preparasi larutan seri kafein
Larutan seri kafein dibuat dengan mengambil masing-masing 200, 250, 300, 350, 400, dan 450µL larutan stok kafein yang dimasukkan kedalam mikrotube berbeda. Ditambahkan metanol pada masing-masing konsentrasi berturut-turut sebanyak 800, 750, 700, 650, 600, dan 550µL sehingga volume akhir yang diperoleh 1 mL dan didapat larutan seri baku kafein dengan konsentrasi 200, 250, 300, 350, 400, dan 450ppm.
Penentuan panjang gelombang maksimal
Larutan seri kafein konsentrasi200, 250, 300, 350, 400 dan 450ppmditotol menggunakan instrument autosampler linomat sebanyak 2µ l pada plat KLT yang telah diaktivasi pada suhu 120℃ selama ±45 menit. Tiap totolan diberi jarak 1cm, jarak dari samping kanan-kiri 1cm, dan jarak dari bawah 2cm. Plat KLT tersebut dielusi hingga jarak 75mm pada chamber yang telah dijenuhkan dengan fase gerak (metanol : etil asetat : ammonia 25%). Plat dikeringkan, kemudian dibaca serapan pada rentang panjang gelombang 200-400nm menggunakan instrument
densitometer. Panjang gelombang maksimal yang diperoleh dari nilai serapan paling optimal (tinggi) digunakan untuk menganalisis kafein pada sistem KLT-Densitometri (Kromatografi Lapis Tipis-KLT-Densitometri).
Penentuan kurva baku
5
didapatkan sebelumnya. Dibuat persamaan garis y=bx+a hubungan antara konsentrasi dengan respon (AUC).
Preparasi sampel kopi robusta dan arabika i. Kopi robusta
Sampel kopi bubuk robusta ditimbang seksama lebih kurang 2,0 gram kemudian dilarutkan dalam 150,0mL aquadestilata suhu 100°C. Larutan kopi robusta siap digunakan untuk analisis kadar dengan metode Kromatografi Lapis Tipis - Densitometri.
ii. Kopi arabika
Sampel kopi bubuk arabika ditimbang seksama lebih kurang 10,0 gram kemudian dilarutkan dalam 150,0 mL aquadestilata suhu 100℃. Larutan kopi arabika disaring menggunakan kertas saring untuk menghilangkan sisa endapan serbuk kopi. Larutan kopi arabika siap digunakan untuk analisis kadar dengan metode Kromatografi Lapis Tipis - Densitometri.
Validasi metode analisis
i. Penentuan selektivitas dan spesifitas
Nilai resolusi dihitung dari hasil pengukuran baku kafein konsentrasi 150ppm, sampel kopi, dan sampel kopi yang ditambah dengan baku kafein konsentrasi 150ppm dengan cara menghitung jarak puncak yang dihasilkan senyawa kafein dengan puncak terdekat yang timbul pada densitogram. Nilai Rf (retention factor) antara senyawa kafein dengan Rf senyawa lain yang terdapat di dalam sampel kopi, sehingga didapatkan nilai resolusi senyawa kafein.
ii. Penentuan linearitas dan rentang
6
didapatkan sebelumnya. Dibuat persamaan garis kurva baku hubungan antara konsentrasi dengan respon (AUC).
iii. Penentuan akurasi dan presisi
Larutan seri kafein dibuat dengan mengambil sebanyak 200, 350, dan 450µL larutan baku kafein kemudian dimasukkan ke dalam mikrotube berbeda, setelah itu ditambahkan pelarut metanol pada masing-masing seri berturut-turut sebanyak 800, 650, dan 550 µL, didapatkan volume akhir 1 mL sehingga didapat larutan seri baku kafein dengan konsentrasi 200, 350, dan 450 ppm. Masing-masing ditotol menggunakan instrument autosampler Linomat sebanyak 2µL pada plat KLT yang telah diaktivasi pada suhu 120℃ selama ±45 menit.Tiap totolan diberi jarak 1cm, jarak dari samping kanan-kiri 1cm, dan jarak dari bawah 2cm. Plat KLT tersebut dielusi hingga jarak 75mm pada chamber yang telah dijenuhkan dengan fase gerak (metanol : etil asetat : ammonia 25%). Plat dikeringkan kemudian dibaca serapan menggunakan densitometer pada panjang gelombang maksimal. Hasil AUC diplotkan terhadap persamaan garis kurva baku (y=bx+a) yang telah diperoleh, dilakukan 3x replikasi. Dihitung nilai akurasi dan presisi yang berupa nilai SD, %perolehan kembali, dan CV kemudian dibandingkan dengan nilai akurasi dan presisi mengacu Association of Official Analytical Chemist (AOAC). iv. Validasi metode dengan adisi baku kafein
Larutan sampel kopi yang telah dipreparasi dipindahkan pada 4 mikrotube berbeda, masing-masing sebanyak 400µL. Pada mikrotube pertama ditambahkan aquadestilata sebanyak 600µL. Mikrotube kedua ditambahkan baku kafein sebanyak 50µL (50ppm), kemudian ditambahkan aquadestilata sebanyak 550µL. Mikrotube ketiga ditambahkan baku kafein sebanyak 100µL (100ppm), kemudian ditambahkan aquadestilata sebanyak 500µL. Mikrotube keempat ditambahkan baku kafein sebanyak 150µL (150ppm), kemudian ditambahkan
7 Analisis Hasil
i. Selektivitas dan spesifitas
Selektivitas dilihat berdasarkan hasil resolusi pada densitogram, antara senyawa kafein dan senyawa lain dalam sampel yang memiliki puncak berdekatan. Syarat resolusi yang baik yakni Rs≥2,00 (AOAC, 2013). Spesifitas dilihat dari kedekatan nilai Rf yang dihasilkan antar senyawa kafein yang dianalisis.
ii. Linearitas
Nilai linearitas ditentukan dari koefisien korelasi (r) yang diperoleh dari AUC baku kafein yang diplotkan terhadap konsentrasi baku kafein. Linearitas ditentukan dengan nilai koefisien korelasi ≥0,99 (AOAC, 2013).
iii. Rentang
Konsentrasi larutan seri diplotkan terhadap respon AUC masing-masing seri, kemudian diperoleh persamaan y=bx+a. Rentang ditentukan dari konsentrasi terendah dan tertinggi dari seri baku kafein yang memiliki linearitas yang baik, ditunjukkan dengan nilai koefisien korelasi ≥ 0,99 (AOAC, 2013).
iv. Akurasi dan recovery
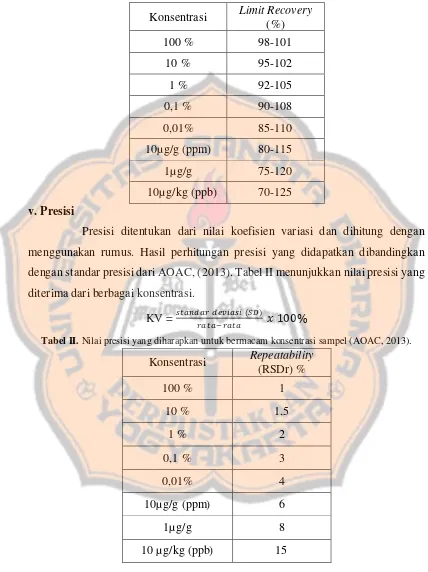
Akurasi ditentukan dari hasil kadar yang diuji dengan kadar baku dan dinyatakan dalam bentuk persen. Hasil akurasi yang didapatkan dibandingkan dengan standar akurasi dari AOAC, (2013). Perolehan kembali ditentukan dari metode adisi baku kafein pada sampel. Kadar penambahan baku kafein dihitung dan dibandingkan dengan standar perolehan kembali dari AOAC (2013). Tabel I menunjukkan nilai recovery yang diterima untuk berbagai konsentrasi sampel.
Akurasi = 𝑘𝑎𝑑𝑎𝑟 𝑡𝑒𝑟𝑢𝑘𝑢𝑟
𝑘𝑎𝑑𝑎𝑟 𝑠𝑒𝑏𝑒𝑛𝑎𝑟𝑛𝑦𝑎 𝑥 100%
Perolehan kembali = 𝑘𝑎𝑑𝑎𝑟 𝑠𝑒𝑏𝑒𝑛𝑎𝑟𝑛𝑦𝑎−𝑘𝑎𝑑𝑎𝑟 𝑡𝑒𝑟𝑢𝑘𝑢𝑟
8
Tabel I. Nilai recovery yang diterima untuk berbagai konsentrasi sampel (AOAC, 2013)
Konsentrasi LimitRecovery
Presisi ditentukan dari nilai koefisien variasi dan dihitung dengan menggunakan rumus. Hasil perhitungan presisi yang didapatkan dibandingkan dengan standar presisi dari AOAC, (2013). Tabel II menunjukkan nilai presisi yang diterima dari berbagai konsentrasi.
KV = 𝑠𝑡𝑎𝑛𝑑𝑎𝑟 𝑑𝑒𝑣𝑖𝑎𝑠𝑖 (𝑆𝐷)
𝑟𝑎𝑡𝑎−𝑟𝑎𝑡𝑎 𝑥 100%
Tabel II. Nilai presisi yang diharapkan untuk bermacam konsentrasi sampel (AOAC, 2013).
9 HASIL DAN PEMBAHASAN
Validasi metode dilakukan untuk menjamin sebuah metode penetapan kadar dapat dipertanggungjawabkan kesahihannya, dibuktikan dengan beberapa parameter validasi yang dilakukan meliputi selektivitas, spesifitas, linearitas, rentang, akurasi, dan presisi. Validasi metode penetapan kadar kafein dilakukan secara Kromatografi Lapis Tipis-Densitometri dengan menggunakan kopi bubuk arabika dan robusta sebagai sampel. Penelitian ini menggunakan instrument
CAMAG TLC Scanner 3 sebagai densitometer untuk melakukan analisis, serta CAMAG Linomat 5 sebagai autosampler untuk melakukan penotolan baku kafein dan sampel kopi pada plat KLT (Kromatografi Lapis Tipis). Fase gerak yang digunakan yakni, metanol; etil asetat; dan ammonia 25% dengan perbandingan berturut-turut 13:77:10 (v/v) mengacu pada penelitian dari Riswanto, dkk (2015) Plat KLT yang digunakan berjenis silika gel 60 GF254. Plat silika gel 60 GF254
digunakan karena merupakan plat yang umum digunakan untuk metode Kromatografi Lapis Tipis (Spangenberg, et al 2011). Plat silika gel 60 GF254
memiliki ukuran pori-pori 60Å, simbol F254 menunjukkan bahwa plat dapat
berfluorosensi dibawah sinar ultraviolet yang mempermudah uji kualitatif senyawa dibawah sinar ultraviolet pada panjang gelombang 254nm. Aktivasi plat KLT silika gel 60 GF254 dilakukan di dalam oven pada suhu 120℃ selama 45 menit untuk
10
(2015). Pada penelitian digunakan sampel kopi bubuk instant jenis arabika dan robusta.
Penentuan panjang gelombang optimal kafein
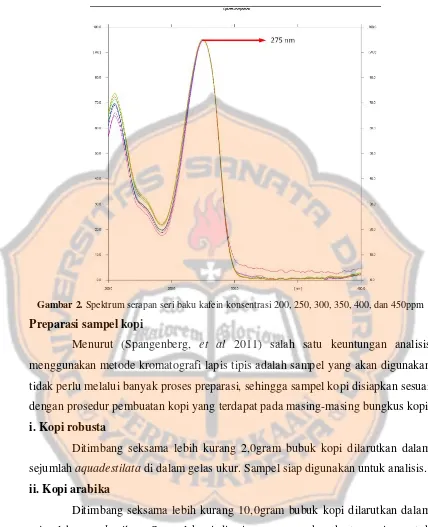
Senyawa kafein memiliki gugus kromofor dan auksokrom, sehingga dapat dilakukan analisis dengan densitometer, dengan prinsip memantulkan intensitas cahaya yang dipancarkan oleh analit. Penentuan panjang gelombang maksimal dilakukan pada larutan seri baku kafein sebelum tahap penentuan linearitas. Larutan seri baku kafein konsentrasi 200, 350, dan 450ppm ditotol menggunakan instrument autosampler Linomat sebanyak 2µL dan dilakukan elusi hingga jarak 75mm dengan fase gerak metanol-etil asetat-ammonia 25% (13:77:10) kemudian dilakukan pembacaan absorbansi pada rentang panjang gelombang 200-400nm.
Gambar 1. Struktur kafein dan auksokrom-kromofor
11
Gambar 2. Spektrum serapan seri baku kafein konsentrasi 200, 250, 300, 350, 400, dan 450ppm
Preparasi sampel kopi
Menurut (Spangenberg, et al 2011) salah satu keuntungan analisis menggunakan metode kromatografi lapis tipis adalah sampel yang akan digunakan tidak perlu melalui banyak proses preparasi, sehingga sampel kopi disiapkan sesuai dengan prosedur pembuatan kopi yang terdapat pada masing-masing bungkus kopi. i. Kopi robusta
Ditimbang seksama lebih kurang 2,0gram bubuk kopi dilarutkan dalam sejumlah aquadestilata di dalam gelas ukur. Sampel siap digunakan untuk analisis. ii. Kopi arabika
Ditimbang seksama lebih kurang 10,0gram bubuk kopi dilarutkan dalam sejumlah aquadestilata. Sampel kopi disaring menggunakan kertas saring untuk menghilangkan sisa endapan bubuk yang tidak larut air. Sampel siap digunakan untuk analisis.
12
sebelumnya sehingga suhu aquadestilata kurang lebih 100℃. Pada sampel kopi arabika terdapat sisa bubuk yang tidak larut air, maka dilakukan penyaringan menggunakan kertas saring untuk menghilangkan sisa-sisa bubuk kopi yang dapat menyumbat pori-pori plat dan mengganggu proses elusi yang terjadi. Pada sampel kopi robusta tidak terdapat sisa endapan bubuk, maka tidak dilakukan penyaringan. Penentuan selektivitas
Proses penentuan selektivitas dilakukan dengan menambahkan sejumlah baku kafein ke dalam sampel kopi yang telah dipreparasi, kemudian ditotol menggunakan instrumentautosampler Linomat sejumlah 2µL pada plat. Selektivitas digunakan untuk melihat kemampuan metode mengukur analit di dalam sebuah sampel atau matriks.
Tabel III. Data resolusi kafein
Keterangan Data resolusi Nilai Rf
Baku kafein 150ppm - 0,70
Sampel kopi 4,545 0,74
Sampel kopi + baku kafein 150ppm 5,400 0,74
Menurut (AOAC, 2013) selektivitas yang baik ditunjukkan dengan nilai resolusi (Rs) ≥2. Menurut (Spangenberg, et al 2011) nilai resolusi ≥1,25 dapat
13
(a)
(b)
(c)
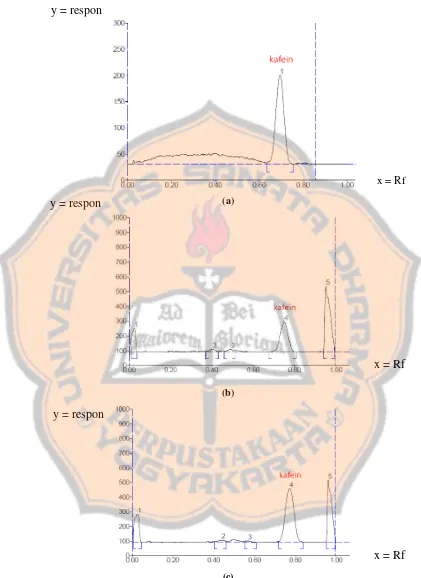
Gambar 3. Kromatogram kafein pada larutan baku 150ppm (a), sampel kopi tanpa adisi baku (b), dan sampel kopi dengan adisi baku kafein 150ppm (c)
14
Dari kromatogram (Gambar 3) dapat diketahui bahwa nilai Rf baku kafein 150ppm, sampel kopi tanpa adisi baku kafein, dan sampel kopi dengan adisi baku kafein 150ppm berturut-turut 0,70; 0,74; dan 0,74. Dari metode didapatkan nilai Rf ≥0,33 menunjukkan analit mampu terelusi dengan baik karena ikatan yang terjadi antara analit dengan fase diam lebih kecil dibanding ikatan yang terjadi antara analit dengan fase gerak, sehingga pemisahan analit kafein dengan senyawa lain optimal. Penentuan kurva baku
Kurva baku dalam sebuah metode menunjukkan hubungan antara konsentrasi seri baku dengan respon dari sebuah instrument. Respon ditunjukkan dengan nilai AUC (Area Under Curve). Pada penelitian, penetapan kurva baku dilakukan dengan seri baku kafein konsentrasi 200, 250, 300, 350, 400, dan 450ppm dilakukan 3x replikasi dan dilakukan elusi pada waktu yang sama, kemudian dari ketiga replikasi didapatkan nilai AUC yang setara dengan konsentrasi dan menunjukkan regresi linear terbaik.
Tabel IV. Data perolehan AUC dari enam seri baku kafein
Konsentrasi
15
persamaan garis kurva baku y = 32,239x + 777,25 digunakan untuk menghitung kadar kafein dalam sampel kopi.
Gambar 4. Kurva hubungan antara konsentrasi kafein (200,250,300,350,400, dan 450ppm)
dengan respon (AUC)
Penentuan akurasi dan presisi
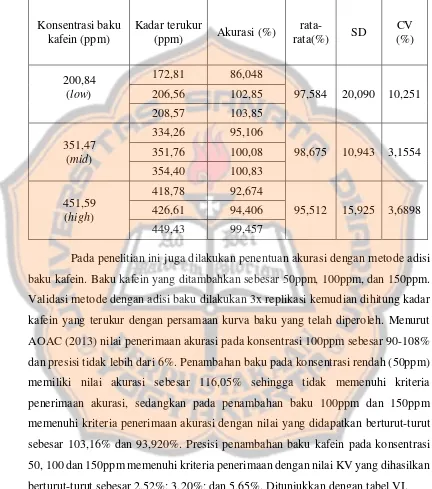
Akurasi adalah ketepatan suatu metode analisis yang ditunjukkan dengan kedekatan nilai yang dihasilkan dan diterima dibandingkan dengan nilai/kadar sesungguhnya (Spangenberg, et al 2011). Presisi adalah kemampuan suatu metode analisis untuk menunjukkan hasil yang mendekati sebenarnya, dengan proses pengukuran yang berulang dan hasilnya dinyatakan dengan CV (Koefisien variasi) (Spangenberg, et al 2011). Dari penelitian dilakukan penentuan akurasi dan presisi dari larutan seri baku kafein dan adisi baku kafein ke dalam sampel (perolehan kembali). Untuk penetapan akurasi dan presisi dari larutan seri baku dilakukan dengan 3x replikasi. Nilai AUC yang dihasilkan kemudian diplotkan pada persamaan garis kurva baku yang sudah diperoleh sebelumnya, sehingga diperoleh konsentrasi terukur dan konsentrasi yang sebenarnya. Menurut AOAC (2013) kriteria akurasi pada konsentrasi 100ppm yakni 90-108%. Konsentrasi low, mid, dan
high (200, 350 dan 450ppm) memenuhi kriteria akurasi dengan nilai yang dihasilkan berturut-turut dari konsentrasi rendah ke tinggi sebesar 97,58%; 98,67%; dan 95,51%. Menurut AOAC (2013) kriteria penerimaan presisi pada konsentrasi 100ppm tidak lebih dari 6%. Presisi konsentrasi mid, dan high (350 dan 450ppm) memenuhi kriteria yang diharapkan dengan nilai KV yang dihasilkan dari konsentrasi tengah ke tinggi berturut-turut 3,1544%; dan 3,6898%, sedangkan
16
konsentrasi rendah (200ppm) tidak memenuhi kriteria penerimaan presisi dengan nilai KV 10,251%
Tabel V. Data akurasi dan presisi larutan seri baku kafein
Konsentrasi baku
17
Tabel VI. Data %penerimaan kembali dan presisi dengan adisi baku kafein
Penambahan
Rentang sebuah metode menunjukkan konsentrasi terendah dan tertinggi yang dapat memenuhi parameter validasi metode (linearitas, akurasi dan presisi). Pada penelitian didapatkan bahwa rentang pengukuran seri baku kafein dari konsentrasi 150 hingga 750ppm memiliki nilai koefisien korelasi (r) 0,9982 dan nilai koefisien determinasi (r2) 0,9965. Maka pada penelitian ini pengukuran kafein dinyatakan linear pada rentang 150-750ppm.
18 KESIMPULAN
Metode penetapan kadar kafein dalam kopi bubuk dengan metode TLC-Densitometri memenuhi parameter validasi yang baik dengan selektivitas Rs >2; linearitas r = 0,9980; memenuhi kriteria %perolehan kembali pada konsentrasi 350ppm (tengah) dan 450ppm (tinggi); memenuhi kriteria penerimaan akurasi pada 50ppm (rendah), 100ppm (tengah), dan 150ppm (tinggi); memenuhi kriteria presisi pada konsentrasi 50, 100, 150, 250, 350, dan 450ppm; serta rentang pengukuran kadar pada konsentrasi 150 hingga 750ppm.
SARAN
19 DAFTAR PUSTAKA
Alsunni, A.A., 2015. Energy Drink Consumption : Beneficial and Adverse Health Effects. International Journal of Health Sciences., 9 (4), 469-471.
AOAC, 2013. Guideline for dietary supplements and botanicals. Association of Official Analytical Chemists.
Anonim, 2014. Farmakope Indonesia.
Bochenska, P, and Alina, P. 2013. Use Of Tlc For The Quantitative Determination Of Acetylsalicylic Acid, Caffeine, And Ethoxybenzamide In Combined Tablets. Journal of Liquid Chromatography & Related technologies. 37 (20), 2929-2941.
BPOM RI, 2004. Ketentuan Pokok Pengawasan Suplemen Makanan. Keputusan Kepala Badan Pengawas Obat dan Makanan.
Isnindar, Wahyuono, S., Widyarini, S., Yuswanto., 2016. Optimization Method of Caffeine Isolation of Merapi Green Coffee Beans. International Journal of Pharmtech Research. 9 (5) 255-259.
Moffat, A. C., Osselton, M. D., Widdop, B. Clarke’s Analysis of Drugs and Poisons.
Palacios, C., Salatino, M.L.F., Salatino, A. 2017. TLC Procedure for Determination of Approximate Contents of Caffeine in Food and Beverages. World Journal of Chemical Education. 5 (5). 148- 152. Patay, E.B., Bencsik, T., Papp, N., 2016. Phytochemical overview and
medicinal importance of Coffea species from past until now. Asian Pacific Journal of Tropical Medicine. 9 (12). 1127-1135
Patil, P.N., 2012. Caffeine in Various Samples and Their Analysis with HPLC – A Review. Int. J. Pharm. Sci. Rev. Res. 16 (2). 76–83.
Preedy, V.R., 2012. Caffeine : Chemistry, Analysis, Function and Effects. The Royal Society of Chemistry.
Pubchem, 2018. Caffeine. (Online),
https://pubchem.ncbi.nlm.nih.gov/compound/caffeine#section=Top Acessed 5 Mei 2018.
Riswanto, F.D.O., Lukitaningsih, RR. E., Martono, S., 2015. Analytical Method Validation and Determination of Pyridoxine, Nicotinamide, and Caffeine in Energy Drinks Using Thin Layer Chromatography-Densitometry.
Indones. J. Chem. 15 (1), 9-15.
Spangenberg, B., Poole, C.F., and Weins, C., 2011. Quantitative Thin Layer Chromatography: A Practical Survey.
21 Lampiran 2. Kemasan sampel kopi bubuk
23
Lampiran 3. Contoh perhitungan konsentrasi larutan kafein a. Perhitungan konsentrasi larutan stok kafein
Sejumlah 50,0mg kafein dilarutkan dengan pelarut hingga 50 mL
Konsentrasi larutan stok kafein 50,0mg/50mL = 1000µg/mL = 1000ppm b. Perhitungan larutan seri kafein
Sejumlah 200µL larutan stok kafein (1000ppm) diencerkan dengan pelarut hingga 1mL
Konsentrasi larutan seri kafein (1000ppm x 200µL) / 1000µL = 200ppm Perhitungan lainnya dilakukan sama seperti contoh sesuai dengan jumlah larutan stok kafein yang diambil.
24
26
28 Kurva baku replikasi 1
1. Konsentrasi 200ppm
29 3. Konsentrasi 300 ppm
30 5. Konsentrasi 400 ppm
31 Kurva baku replikasi 2
1. Konsentrasi 200 ppm
32 3. Konsentrasi 300 ppm
33 5. Konsentrasi 400 ppm
6. Konsentrasi 450 ppm
34 Kurva baku replikasi 3
1. Konsentrasi 200 ppm
35 3. Konsentrasi 300 ppm
36 5. Konsentrasi 400 ppm
37
Lampiran 6. Kromatogram seri baku kafein – linearitas 1. Konsentrasi 150 ppm
38 3. Konsentrasi 350 ppm
39 5. Konsentrasi 550 ppm
41
Lampiran 7. Kromatogram seri baku kafein – akurasi dan presisi 1. Konsentrasi 200ppm replikasi 1
42 3. Konsentrasi 200ppm replikasi 3
43 5. Konsentrasi 250ppm replikasi 2
44 7. Konsentrasi 300ppm replikasi 1
45 9. Konsentrasi 300ppm replikasi 3
46 11. Konsentrasi 350ppm replikasi 2
47 13. Konsentrasi 400ppm replikasi 1
48 15. Konsentrasi 400ppm replikasi 3
49 17. Konsentrasi 450ppm replikasi 2
18. Konsentrasi 450ppm replikasi 3
50
Lampiran 8. Kromatogram adisi baku kafein (replikasi 9x) – presisi dan akurasi 1. Non adisi replikasi 1
51 3. Non adisi replikasi 3
52 5. Non adisi replikasi 5
53 7. Non adisi replikasi 7
54 9. Non adisi replikasi 9
55 11. Adisi baku kafein 50ppm replikasi 2
56 13. Adisi baku kafein 50ppm replikasi 4
57 15. Adisi baku kafein 50ppm replikasi 6
58 17. Adisi baku kafein 50ppm replikasi 8
59 19. Adisi baku kafein 100ppm replikasi 1
60 21. Adisi baku kafein 100ppm replikasi 3
61 23. Adisi baku kafein 100ppm replikasi 5
62 25. Adisi baku kafein 100ppm replikasi 7
63 27. Adisi baku kafein 100ppm replikasi 9
64 29. Adisi baku kafein 150ppm replikasi 2
65 31. Adisi baku kafein 150ppm replikasi 4
66 33. Adisi baku kafein 150ppm replikasi 6
67 35. Adisi baku kafein 150ppm replikasi 8
68
BIOGRAFI PENULIS