i
OPTIMASI CLEAN UP EKSTRAK METANOL AIR TEH HIJAU DENGAN MENGGUNAKAN METODE SOLID PHASE EXTRACTION
(SPE) UNTUK MENDUKUNG PENETAPAN KADAR KUERSETIN DALAM TEH HIJAU DENGAN KROMATOGRAFI CAIR KINERJA
TINGGI
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Farmasi
Oleh:
Adi Wirasaputra NIM : 088114059
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
ii
Persetujuan Pembimbing
OPTIMASI CLEAN UP EKSTRAK METANOL AIR TEH HIJAU DENGAN MENGGUNAKAN METODE SOLID PHASE EXTRACTION
(SPE) UNTUK MENDUKUNG PENETAPAN KADAR KUERSETIN DALAM TEH HIJAU DENGAN KROMATOGRAFI CAIR KINERJA
TINGGI
Skripsi yang diajukan oleh: Adi Wirasaputra NIM : 088114059
telah disetujui oleh :
Pembimbing Utama
iii
Pengesahan Skripsi Berjudul
OPTIMASI CLEAN UP EKSTRAK METANOL AIR TEH HIJAU DENGAN MENGGUNAKAN METODE SOLID PHASE EXTRACTION
(SPE) UNTUK MENDUKUNG PENETAPAN KADAR KUERSETIN DALAM TEH HIJAU DENGAN KROMATOGRAFI CAIR KINERJA
TINGGI
oleh: Adi Wirasaputra NIM : 088114059
Dipertahankan di hadapan Panitia Penguji Skripsi Fakultas Farmasi
Ipang Djunarko, M. Sc., Apt.
Panitia Penguji Tanda tangan :
1. Prof. Dr. Sri Noegrohati, Apt. ... 2. Prof. Dr. C. J. Soegihardjo, Apt. ...
iv
“Ketika jiwaku letih lesu di dalam aku, teringatlah aku kepada TUHAN, dan sampailah doaku kepada-Mu, ke
dalam bait-Mu yang kudus.” (Yunus 2:7)
“Usaha yang sedang – sedang saja membuahkan hasil yang sedang – sedang saja. Tetapi usaha yang luar biasa membuahkan hasil yang luar biasa pula.”
(Toyotomi Hideyoshi)
“Terbayangkan berarti terjangkau.” (Toyotomi Hideyoshi)
Skripsi ini aku persembahkan kepada :
Bapak, Mama, Bagus, dan Candra,
yang selalu mendukungku dan menerimaku apa adanya
v
PERNYATAAN KEASLIAN KARYA
Penulis menyatakan dengan sesungguhnya bahwa skripsi yang ditulis ini tidak memuat karya atau bagian karya orang lain, kecuali yang telah disebutkan dalam kutipan dan daftar pustaka, sebagaimana layaknya karya ilmiah.
Apabila dikemudian hari ditemukan indikasi plagiarisme dalam naskah ini, maka penulis bersedia menanggung segala sanksi sesuai peraturan perundang-undangan yang berlaku.
vi
(Adi Wirasaputra)
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI ILMIAH UNTUK
KEPENTINGAN AKADEMIS
Yang bertandatangan dibawah ini, saya mahasiswa Universitas Sanata Dharma:
Nama : Adi Wirasaputra No Mahasiswa : 088114059
Demi pengembangan ilmu pengetahuan, saya memberikan kepada perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul:
OPTIMASI CLEAN UP EKSTRAK METANOL AIR TEH HIJAU
DENGAN MENGGUNAKAN METODE SOLID PHASE EXTRACTION
(SPE) UNTUK MENDUKUNG PENETAPAN KADAR KUERSETIN
DALAM TEH HIJAU DENGAN KROMATOGRAFI CAIR KINERJA
TINGGI
Beserta perangkat yang diperlukan (bila ada). Dengan demikian saya memberikan kepada perpustakaan Universitas Sanata Dharma hak untuk menyimpan, mengalihkan dalam bentuk media lain, mengelolanya dalam bentuk pangkalan data, mendistribusikan secara terbatas, dan mempublikasikan di Internet atau media lain untuk kepentingan akademis tanpa perlu meminta ijin dari saya maupun memberikan royalty kepada saya selama tetap mencantumkan nama saya sebagai penulis.
vii
PRAKATA
Segala pujian dan syukur penulis haturkan kepada Tuhan karena hanya dengan anugerah, berkat, cinta, kasih, dan pertolongan-Nya, penulis dapat menyelesaikan penelitian dan penyusunan skripsi yang berjudul ”Optimasi Clean
Up Ekstrak Metanol Air Teh Hijau dengan Menggunakan Metode Solid
Phase Extraction (SPE) untuk Mendukung Penetapan Kadar Kuersetin
dalam Teh Hijau dengan Kromatografi Cair Kinerja Tinggi”. Skripsi ini disusun guna memenuhi salah satu syarat untuk memperoleh gelar Sarjana Strata Satu Program Studi Farmasi (S.Farm).
Terselesaikannya penulisan laporan akhir ini tidak lepas dari bantuan berbagai pihak, karena itu penulis mengucapkan terima kasih kepada:
1. Bapak Ipang Djunarko, M.Sc., Apt. selaku Dekan dan segenap staf serta karyawan Laboratorium Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
2. Prof. Dr. Sri Noegrohati, Apt. selaku Dosen Pembimbing yang telah memberikan petunjuk, saran, arahan, dan bimbingan kepada penulis dalam proses penyusunan skripsi ini.
3. Prof. Dr. C. J. Soegihardjo, Apt. dan Bapak Jeffry Julianus, M. Si. selaku Dosen Penguji skripsi yang telah memberikan saran dan masukan demi kesempurnaan skripsi ini.
viii
5. Pak Sanjaya dan Pak Acang atas bantuan selama menghadapi masalah dalam penelitian dan mau membagi ilmu yang tidak didapatkan selama kuliah. 6. Keluarga Wirasaputra tercinta Bapak, Mama, Bagus, dan Candra terima kasih
atas dukungan doa yang selalu membanjir tulus untukku yang membuatku berani bangkit lagi di kala terpuruk.
7. Keluarga Mbah Putri yang selalu mendoakan segala perjuanganku Mbah Putri, Bulik Etik, Mas Hagai, Heraldi, Kezia, dan Brian.
8. Alfonsus Rosario Heppy Dwiyoga, Paulus Setya Dharma dan Anastasia Filipa Veritas da Silva teman seperjuangkanku yang telah dengan sabar menghadapi semua kemalasanku, mendukung dan menyemangati aku selama masa-masa terpuruk di lab.
9. Kawan-kawan seperjuangan di lab dan grup antistress: Eka Riusinta Wati, Melisa Dharmawan, Vinsensia Vica, M.G. Rosita Secoadi, Dhimas B.K., Novi Imoliana, Meiske Munda, Wilfrida Maria Dua, Margaretha Efa Putri, Yuni Rogan, dan Elisa atas kerja sama dan kebersamaan, dukungan dan keceriaan di lab selama penelitian ini.
10. Monica Satya Resmi Yunita untuk momen – momen kebersamaan kita dulu dan terima kasih atas dukungan doa selama ini.
ix
12. Antonius Pandu W., Albertus Djanu Rombang, Alexius Ario P.W., dan Yosef Himawan Yudha terima kasih atas keluangan waktu untuk bersama pergi sejenak dari penatnya skripsi.
13. Teman – teman FKK 2008 yang mau membantu dan selalu memberi dukungan untuk selesainya skripsi ini : Adityawarman, Perthy Melati Kasih, Ellen Sinaga, Paulina Marcellina, Pratiwi Setyaningsih, Gina Vinrensia, Marsyani, dan Tia.
14. Serta semua pihak yang telah banyak membantu penyusunan skripsi ini yang tidak dapat disebutkan satu per satu.
Penulis menyadari bahwa penulisan skripsi ini masih banyak kekurangan dan kelemahan karena keterbatasan pikiran, tenaga, dan waktu penulis. Untuk itu penulis mengharapkan saran dan kritik yang membangun dari semua pihak. Akhir kata semoga skripsi ini dapat berguna dan bermanfaat bagi pembaca semua.
x
DAFTAR ISI
Halaman
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
PERNYATAAN KEASLIAN KARYA ... v
HALAMAN PERSETUJUAN PUBLIKASI ... vi
xi
G. Kromatografi Cair Kinerja Tinggi (KCKT) ... 10
1. Definisi dan instrumentasi KCKT... 10
2. Kromatografi partisi fase terbalik... 12
H. Landasan Teori ... 12
I. Hipotesis... 13
BAB III METODE PENELITIAN ... 14
A. Jenis dan Rancangan Penelitian ... 14
B. Variabel Penelitian... 14
C. Definisi Operasional... 15
D. Bahan Penelitian ... 15
E. Alat Penelitian ... 16
F. Tata Cara Penelitian ... 17
1. Pembuatan serbuk daun teh ... 17
2. Ekstraksi denga menggunakan metode sokhlet sekaligus hidrolisis 17 3. Skrining metode clean up ... 17
xii
5. Optimasi volume fase gerak (eluen) ... 20
6. Penentuan kapasitas kolom SPE ... 21
G. Analisis Hasil Optimasi ... 22
BAB IV HASIL DAN PEMBAHASAN ... 24
A. Pembuatan Serbuk Daun Teh ... 24
B. Ekstraksi denga menggunakan metode sokhlet sekaligus hidrolisis 24 C. Skrining metode clean up ... 27
D. Optimasi jenis fase diam dan fase gerak SPE... 29
E. Optimasi volume fase gerak (eluen) ... 44
F. Penentuan kapasitas kolom SPE ... 46
BAB V KESIMPULAN DAN SARAN... 49
A. Kesimpulan ... 49
B. Saran ... 49
DAFTAR PUSTAKA ... 50
LAMPIRAN ... 52
xiii
DAFTAR TABEL
Halaman
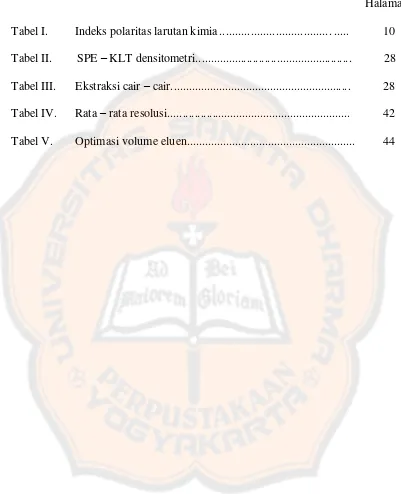
Tabel I. Indeks polaritas larutan kimia ... ... 10
Tabel II. SPE – KLT densitometri... 28
Tabel III. Ekstraksi cair – cair... 28
Tabel IV. Rata – rata resolusi... 42
xiv
DAFTAR GAMBAR
Halaman
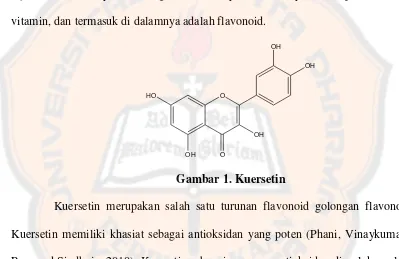
Gambar 1. Kuersetin ... 1
Gambar 2. Sisi aktif kuersetin ... 6
Gambar 3. Interaksi antara kuersetin dengan pelarut metanol-air(90:10) ... 26
Gambar 4. Reaksi hidrolisis pada suatu kuersetin glikon ... 27
Gambar 5. Kromatogram baku kuersetin 65 ppm ... 32
Gambar 6. Kromatogram hasil elusi dengan n-heksana (silika)... 32
Gambar 7. Kromatogram hasil elusi dengan etil asetat (silika)... 33
Gambar 8. Kromatogram hasil elusi dengan metanol... 33
Gambar 9. Kromatogram hasil elusi dengan n-heksana (diol) ... 36
Gambar 10. Kromatogram hasil elusi dengan etil asetat (diol) ... 36
Gambar 11. Kromatogram hasil elusi dengan metanol (diol) ... 37
Gambar 12. Kromatogram baku kuersetin 14 ppm (C18) ... 39
Gambar 13. Kromatogram hasil elusi dengan HCl 0,002 N (C18) ... 39
Gambar 14. Kromatogram hasil elusi dengan metanol ... 40
Gambar 15. Kromatogram baku kuersetin 10 ppm ... 41
Gambar 16. Kromatogram fraksi metanol ... 41
Gambar 17. Kromatogram sampel sebelum SPE ... 43
Gambar 18. Kurva volume eluen vs AUC ... 45
xv
Gambar 20. Kromatogram fraksi HCl 0,002 N pada pengisian 0,1 ml
sampel... ... 47 Gambar 21. Kromatogram fraksi HCl 0,002 N pada pengisian 0,2 ml
xvi
DAFTAR LAMPIRAN
Lampiran 1. Kromatogram optimasi jenis fase gerak pada fase diam
C18 ... 53
Lampiran 2. Kromatogram optimasi jenis fase gerak pada fase diam diol... 55
Lampiran 3. Kromatogram optimasi jenis fase gerak pada fase diam silika ... 58
Lampiran 4. Kromatogram optimasi volume ... 61
Lampiran 5. Kromatogram kapsitas ... 64
Lampiran 6. Contoh cara perhitungan resolusi ... 70
Lampiran 7. Contoh cara perhitungan efisiensi clean up ... 70
xvii
INTISARI
Kuersetin merupakan senyawa berkhasiat yang terdapat dalam daun teh (Camelia sinensis). Senyawa flavonoid golongan flavonol ini dikenal memilki khasiat sebagai antioksidan kuat. Di dalam daun teh terdapat bermacam – macam senyawa dari golongan fenolik, tanin, pektin, katekin, dan vitamin. Tentunya ekstrak metanol air dari teh hijau mengandung senyawa – senyawa lain yang bisa mengganggu determinasi kuersetin dalam teh hijau. Oleh karena itu dalam penelitian ini digunakan metode Solid Phase Extraction (SPE) untuk mengurangi berbagai senyawa yang ikut terekstraksi agar kuersetin dapat dideterminasi tanpa adanya gangguan dari senyawa – senyawa tersebut.
Penelitian ini bertujuan untuk mendapatkan sistem SPE optimal yang bisa mengurangi berbagai senyawa yang ikut terekstraksi sehingga dapat digunakan untuk determinasi kuersetin dalam ekstrak teh hijau. Optimasi dilakukan dengan pemilihan jenis fase diam (diol, silika, dan C18) dan fase gerak (aquabidest, metanol, etil asetat, n-heksana) serta volume fase gerak untuk mengelusi kuersetin.
Sistem SPE terpilih adalah SPE kolom C18 dengan larutan pencuci 6 ml HCl 0,002 N dan larutan pengelusi 5 – 10 ml metanol. Kondisi tersebut cukup efisien dalam memisahkan kuersetin dari koekstraktan dengan nilai resolusi 2,994 dan nilai efisiensi clean up 37,5 – 43,75%.
xviii
ABSTRACT
Quercetin is a pharmacologic component in green tea (Camelia sinensis). This flavonol flavonoid has a potential antioxidant effect. There are many components in green tea leaves such as phenolic components, tannin, pectin, cathecin, and vitamin. Aqueous methanolic green tea extract has many other components which can disturb the determination of quercetin in green tea sampel. Therefore Solid Phase Extraction is used in this study to reduce the number of co-extractants so it can support the determination of quercetin.
This study is to determine the optimum conditions of Solid Phase Extraction system that fit for purpose. Optimation could be done by choosing the type of stationary phase (diol, silica, and C18) and the mobile phase (aquabidest, methanol, aethyl acetic, n-hexane) and the volume of mobile phase to eluting quercetin.
The chosen SPE system is SPE C18 coloumn with 6 ml HCl 0,002 N as the washing solvent and 5 – 10 ml methanol as the eluting solvent. That condition is enough efficient to separate quercetin from co-extractants which resolution value 2,994 and clean up efficiency value 37,5 – 43,75%.
1
BAB I
PENGANTAR
A. Latar Belakang
Teh sudah tak asing lagi bagi masyarakat Indonesia. Menikmati teh bisa dengan dijadikan teh seduh, teh celup, hingga teh siap saji dalam kemasan. Teh hijau memiliki banyak kandungan di dalamnya, di antaranya adalah pektin, tanin, vitamin, dan termasuk di dalamnya adalah flavonoid.
O
Kuersetin merupakan salah satu turunan flavonoid golongan flavonol. Kuersetin memiliki khasiat sebagai antioksidan yang poten (Phani, Vinaykumar, Rao, and Sindhuja, 2010). Kuersetin sebagai senyawa antioksidan diperlukan oleh tubuh untuk menetralkan radikal bebas dan mencegah kerusakan sel normal oleh adanya radikal bebas. Senyawa antioksidan menstabilkan radikal bebas dengan mendonorkan protonnya untuk berpasangan dengan elektron yang dimiliki radikal bebas sehingga reaksi berantai dari pembentukan radikal bebas dapat dihambat.
Kandungan flavonoid golongan lain dalam daun teh hijau (Camellia sinensis L.) adalah katekin. Katekin tidak berwarna, larut dalam air, dan memberi
adalah epigalokatekin galat (log P = 2,38), epigalokatekin (log P = 1,2), epikatein galat, epikatekin (log P = 1,02), dan katekin (log P = 1,02). Epigalokatekin galat juga mempunyai aktivitas antioksidan (Kodama, Goncalves, Lajolo, and Genovese, 2010).
Upaya mendapatkan fraksi analit yang bersih dari senyawa lain (clean up) bisa ditempuh dengan cara Liquid – Liquid Extraction (LLE) maupun Solid
Phase Extraction (SPE). LLE berdasarkan pada koefisien distribusi analit pada
suatu pelarut dengan prinsip partisi. Pelarut yang digunakan untuk menghilangkan senyawa lain selain analit tidak boleh bercampur. SPE merupakan kromatografi kolom, dimana senyawa yang memiliki kepolaran mirip dengan fase diam atau dapat berinteraksi dengan fase diam akan tertahan sedangkan senyawa yang lain akan ikut terelusi. Dengan mempertimbangkan log P dari senyawa – senyawa selain kuersetin dan log P kuersetin sendiri (log P = 1,82), maka fase gerak SPE yang dipilih juga diharapkan mampu mengelusi kuersetin dengan sedikit mengelusi senyawa – senyawa lain.
diinjeksikan pada alat Kromatografi Cair Kinerja Tinggi (KCKT) fase terbalik yang metodenya telah dioptimasi oleh Dwiyoga (2012).
Pemilihan fase diam (C18, diol, dan silika) dan komposisi pelarut dalam metode SPE perlu dioptimasi untuk mendapatkan hasil yang optimum. Kondisi metode SPE dikatakan optimum jika memenuhi parameter – parameter berikut yaitu berkurangnya jumlah peak senyawa – senyawa lain yang terikut dalam ekstraksi yang dinyatakan dengan nilai efisiensi clean up, Area Under Curve
(AUC) kuersetin terbesar dan didapatkan nilai Rs ≥ 1,5.
Telah dilakukan penelitian tentang pemisahan kuersetin menggunakan metode SPE fase terbalik dalam tablet Ginkgo biloba (Mokgadi, Mmualefe, and Torto, 2009), namun bukan dalam teh hijau. Dengan tetap mengacu pada penelitian tersebut, optimasi dilakukan dengan mengubah – ubah komposisi atau jenis pelarut dan pemilihan fase diam (C18, diol, dan silika) serta menentukan volume pengelusi. Ketiga faktor tersebut dapat mempengaruhi parameter – parameter clean up yang optimum.
1. Permasalahan
2. Keaslian penelitian
Penelitian terhadap kuersetin dengan metode SPE telah dilakukan dalam suatu sediaan obat. Penelitian dengan judul “SampliQ OPT Solid Phase Extraction Sorbent in the Cleanup of Flavonoids in Ginkgo Biloba by
HPLC-DAD” dilakukan dengan menggunakan fase diam C18 dan larutan pengelusi metanol:air (5:95 v/v) serta metanol:amonium asetat (30:70 v/v) untuk memisahkan kuersetin dalam tablet Ginkgo Biloba (Mokgadi, Mmualefe, and Torto, 2009). Demikian, maka dapat dipastikan bahwa optimasi metode SPE kuersetin dalam teh hijau ini belum pernah dilakukan sebelumnya.
3. Manfaat penelitian
a. Manfaat metodologis. Penelitian ini diharapkan dapat memberikan informasi mengenai penggunaan metode SPE pada proses ekstraksi kuersetin untuk penetapan kadar kuersetin dalam ekstrak metanol air teh hijau.
b. Manfaat praktis. Penelitian ini diharapkan dapat memberikan informasi terkait dengan pemilihan jenis fase diam, jenis fase gerak, dan volume eluen SPE yang terbaik untuk proses ekstraksi kuersetin untuk penetapan kadar kuersetin dalam ekstrak metanol air teh hijau.
B. Tujuan Penelitian
5
BAB II
PENELAAHAN PUSTAKA
A. Kandungan Daun Teh Hijau (Camellia sinensis L.)
Daun teh hijau (Camellia sinensis L.) mengandung substansi fenol dan substansi bukan fenol. Substansi fenol terdiri dari katekin yang punya empat turunan, yaitu epikatekin (EC), epikatekin galat (ECG), epigalokatekin (EGC) dan epigalokatekin galat (EGCG) serta flavonol terdiri dari kaempferol, kuersetin, dan mirisetin. Subtansi bukan fenol terdiri dari pektin, alkaloid, karbohidrat, klorofil, mineral, protein, dan asam amino (Soraya, 2007).
Flavonol utama yang ada di dalam daun teh adalah kuersetin, kaempferol dan myrycetin. Flavonol ini, terutama terdapat dalam bentuk glikosidanya (berikatan dengan molekul gula) dan sedikit dalam bentuk aglikonnya (Hartoyo, 2003).
B. Flavonoid
Adanya gula yang terikat pada flavonoid, cenderung menyebabkan falvonoid mudah larut dalam air dan dengan demikian campuran pelarut di atas dengan air merupakan pelarut yang lebih baik untuk glikosida. Sebaliknya, aglikon yang kurang polar seperti flavonol yang termetoksilasi cenderung lebih mudah larut dalam pelarut seperti eter dan kloroform (Markham, 1988).
C.Kuersetin
Kuersetin merupakan senyawa berwarna kuning dan menjadi anhidrat pada suhu 95 - 97° C. Kelarutan : larut dalam asam asetat glasial, dalam larutan aqueous alkaline dan praktis tidak larut dalam air (The Merck Index, 1989). Kuersetin memiliki gugus fungsi karbonil dan hidroksil sehingga dapat membentuk kompleks dengan beberapa ion logam (Makasheva, 2005).
Kuersetin memiliki aktivitas antioksidan yang kuat karena memiliki tiga ciri pada strukturnya, yaitu 3’,4’-dihidroksi pada cincin B; 2,3-ikatan rangkap
pada cincin C dan sebuah gugus 5-hidroksil pada cincin A. Ketiga ciri ini secara umum ditunjukkan pada gambar di bawah ini (Sibuea, 2006).
O
D. Ekstraksi
Ekstrak adalah sediaan pekat yang diperoleh dengan mengekstraksi zat aktif dari simplisia nabati atau hewani menggunakan pelarut yang sesuai, kemudian semua atau hampir semua pelarut diuapkan dan massa atau serbuk yang tersisa diperlakukan sedemikian sehingga memenuhi baku yang telah ditetapkan (DirJen POM, 1995).
Ekstraksi adalah proses pemisahan satu atau lebih komponen dari suatu campuran homogen menggunakan pelarut cair (solven) sebagai separating agent (Harborne, 1987). Pemilihan pelarut dan cara ekstraksi yang tepat dapat dipermudah dengan mengetahui terlebih dahulu zat aktif yang dikandung simplisia (DirJen POM, 1986).
E. Soxhlet
Soxhlet adalah ekstraksi menggunakan pelarut yang selalu baru yang dilakukan dengan alat khusus sehingga terjadi ekstraksi kontinyu dengan jumlah pelarut relatif konstan dengan adanya pendingin balik. Penyarian dengan alat soxhlet menggunakan larutan yang dipanaskan terus menerus sehingga zat aktif yang tidak tahan pemanasan kurang cocok (DirJen POM, 2010).
F. Solid-Phase Extraction (SPE)
1. Prosedur SPE
semua analit yang dituju pada penjerap yang digunakan, sementara senyawa – senyawa penganggu akan terelusi. Analit yang dituju (yang tertahan pada penjerap ini) selanjutnya dielusi dengan sejumlah kecil pelarut organik yang akan mengambil analit yang tertahan ini. Strategi ini beramanfaat jika analit yang dituju berkadar rendah. Strategi lain adalah dengan mengusahakan supaya analit yang tertuju keluar (terelusi), sementara senyawa penganggu tertahan pada penjerap (Rohman, 2009).
Tahap pertama menggunakan SPE adalah dengan mengkondisikan penjerap dengan pelarut yang sesuai. Penjerapa nonpolar seperti C18 dan penjerap
penukar ion dikondisikan dengan mengalirinya menggunakan metanol lalu dengan akuades. Pencucian yang berlebihan dengan air akan mengurangi recovery analit. Penjerap – penjerap polar seperti diol, siano, amino, dan silika harus dibilas dengan pelarut nonpolar seperti metilen klorida (Rohman, 2009).
Ada empat tahap dalam prosedur SPE, yaitu: a. Pengkondisian
Cartridge (penjerap) dialiri dengan pelarut sampel untuk membasahi
permukaan penjerap dan untuk menciptakan nilai pH yang sama, sehingga perubahan – perubahan kimia yang tidak diharapkan ketika sampel dimasukkan dapat dihindari.
b. Retensi (tertahannya) sampel
c. Pembilasan
Tahap ini penting untuk menghilangkan seluruh komponen yang tidak tertahan oleh penjerap selama tahap retensi.
d. Elusi
Tahap ini merupakan tahap terakhir untuk mengambil analit yang dituju jika analit tersebut tertahan pada penjerap (Rohman, 2009).
2. Fase SPE
Tabel I. Indeks polaritas larutan kimia (Snyder, 1978)
Fase gerak adalah medium angkut yang terdiri atas satu atau beberapa pelarut. Fase gerak bergerak di dalam fase diam, yaitu lapisan berpori karena ada gaya kapiler (Stahl, 1985).
G. Kromatografi Cair Kinerja Tinggi
1. Definisi dan instrumentasi KCKT
Kromatografi merupakan teknik yang mana solut terpisah oleh perbedaan kecepatan elusi, dikarenakan solut – solut ini melewati suatu kolom kromatografi (Gandjar dan Rohman, 2009).
a. Fase diam
Oktadesil silika (ODS atau C18) merupakan fase diam yan paling banyak
digunakan karena mampu memisahkan senyawa – senyawa dengan kepolaran yang rendah, sedang, maupun tinggi. Oktil atau rantai alkil yang lebih pendek lagi lebih sesuai untuk solut yang polar (Gandjar dan Rohman, 2009).
b. Fase gerak
Kemampuan KCKT dalam memisahkan banyak senyawa terutama tergantung pada jenis fase gerak. Fase gerak dapat mempengaruhi pemisahan komponen dalam campuran (Munson, 1991).
Fase gerak yang paling sering digunakan untuk pemisahan dengan fase terbalik adalah campuran larutan bufer dengan metanol atau campuran air dengan asetonitril (Gandjar dan Rohman, 2009).
c. Detektor
Detektor UV-Vis didasarkan pada adanya penyerapan ultraviolet (UV) dan sinar tampak (Vis) pada kisaran panjang gelombang 190 – 800 nm oleh spesies oleh spesies solut yang mempunyai struktur – struktur atau gugus – gugus kromoforik (Gandjar dan Rohman, 2009).
2. Kromatografi partisi fase terbalik
Konsep dasar kromatografi partisi, yaitu perlakuan sampel dalam kondisi cair-cair tergantung pada kelarutannya di dalam kedua cairan yang terlibat (Gritter et al., 1991). Partisi analit di antara dua fase yang tidak saling campur, karena
adanya perbedaan koefisien distribusi dari masing-masing senyawa (Munson, 1991).
H. Landasan Teori
Kuersetin merupakan turunan flavonoid golongan flavonol. Kuersetin adalah aglikon yang terlepas dari gugus glikosidanya sehingga kepolarannya menurun namun larut dalam pelarut metanol.
Salah satu kandungan ekstrak teh hijau adalah flavonoid. Kandungan flavonoid dalam ekstrak teh hijau tidak hanya kuersetin, namun masih ada turunan flavonoid golongan lain ataupun polifenol lain yang larut dalam pelarut ekstrak yang sama. Oleh karena itu, diperlukan Solid Phase Extraction (SPE) dengan harapan didapatkan ekstrak teh hijau yang bersih dari turunan flavonoid lain ataupun polifenol lain.
Solid Phase Extraction merupakan teknik pemisahan analit dari
dengan SPE dilakukan untuk memperoleh ekstrak yang bersih dari senyawa lainnya (selain kuersetin) dan didaptkan kandungan kuersetin terbanyak. Hasil ekstraksi diinjeksikan pada sistem KCKT fase terbalik yang sudah teroptimasi dan dilihat kromatogramnya. Parameter pemisahan dengan SPE yang menunjukkan hasil optimum yaitu berkurangnya puncak – puncak senyawa selain kuersetin, Area Under Curve (AUC) kuersetin yang terbesar, dan resolusi tercapai ≥ 1,5
pada kromatogram.
I. Hipotesis
14
BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Jenis dan rancangan penelitian ini adalah eksperimental karena terdapat perlakuan terhadap subjek uji.
B. Variabel Penelitian
1. Variabel bebas
Variabel bebas dalam penelitian ini adalah :
a. Fase diam C18 dengan fase gerak HCl 0,002 N dan metanol.
b. Fase diam diol dengan fase gerak n-heksana, etil asetat, dan metanol. c. Fase diam silika dengan fase gerak n-heksana, etil asetat, dan metanol. d. Volume eluen yang digunakan
2. Variabel tergantung
Variabel tergantung dalam penelitian ini adalah nilai efisiensi clean up, nilai resolusi, dan AUC kuersetin.
3. Variabel pengacau terkendali
C. Definisi Operasional
1. Kuersetin yang dianalisis merupakan senyawa aktif yang berada dalam sampel ekstrak teh hijau.
2. Sistem SPE yang digunakan adalah seperangkat alat SPE menggunakan fase diam C18 dengan fase gerak aquabidest HCl 0,002 N, dan metanol; fase diam diol dengan fase gerak n-heksana, etil asetat, dan metanol; serta fase diam silika dengan fase gerak n-heksana, etil asetat, dan metanol.
3. Optimasi jenis fase diam dan fesa gerak dilakukan dengan menggunakan fase diam yang berbeda dan fase gerak yang berbeda pada tiap fase diam, optimasi volume fase gerak dilakukan dengan mengubah volume fase gerak, dan optimasi kapasitas kolom dilakukan dengan mengubah volume sampel yang masuk pada kolom SPE.
4. Parameter pemisahan komponen dengan metode SPE dilanjutkan dengan KCKT fase terbalik adalah kromatogram dengan jumlah impurities yang sedikit dan AUC kuersetin terbesar.
D. Bahan Penelitian
Bahan yang digunakan dalam penelitian adalah baku kuersetin (Pcode:100910390), metanol p.a. (E, Merck), aquabidest, etil asetat p.a. (E, Merck), n-heksana p.a. (E, Merck), akuades yang disaring yang diperoleh dari
konsentrasinya adalah 11,32 M, teh hijau dengan merk ”Sigma” yang diperoleh dari PT. Pagilaran Samigaluh, Kulon Progo.
E. Alat Penelitian
Alat yang digunakan dalam penelitian ini adalah seperangkat alat soxhlet 100 ml dan refluks, waterbath (merk “Marius” dan “Hedolph), termometer, kantong sokhlet, rotary evaporator, neraca analitik (OHAUS Carat Series PAJ 1003, max 60/120 g, min 0,001 g, d = 0,01/0,1 mg, e = 1 mg), densitometer (CAMAG TLC Scanner 3 CAT. No. 027.6485 SER. No. 160602), autosampler (Linomat 5 No. 170610), perangkat lunak WinCats (V.1.4.4), bejana kromatografi, seperangkat alat KCKT fase terbalik dengan sistem gradien dan isokratik dengan detektor ultraviolet, Shimadzu LC-2010C, kolom C-18 merek KNAUER C-18 (No. 25EE181KS (B115Y620), Dimensi 250 x 4,6 mm), seperangkat komputer (merk Dell B6RDZ1S Connexant Sistem RD01-D850 A03-0382 JP France S.A.S, printer HP Deskjet D2566 HP-024-000 625730), alat ultrasonikasi (Retsch tipe T640 No.935922013), kertas saring Whatman 0,45 μm, alat vacuum, hair dryer “Q2 External Beauty”, milipore, seperangkat cartridge Solid Phase Extraction (SPE) dengan fase diam C18, diol, silika merek E-Merck,
F. Tata Cara Penelitian
1. Pembuatan serbuk daun teh
Sejumlah tujuh bungkus kemasan teh hijau yang diambil dari PT Pagilaran dengan nomor batch yang sama dicampur menjadi satu kemudian dihomogenkan, lalu diserbuk dan disaring. Hasil serbuk kemudian disimpan dalam wadah yang kering, kemudian diberi silika gel.
2. Ekstraksi dengan menggunakan metode Soxhlet sekaligus hidrolisis
Serbuk daun teh ditimbang 8 gram kemudian dimasukkan ke dalam tea bag. Tea bag dimasukkan ke dalam tabung soxhlet kemudian disoxhlet dengan
240 ml larutan metanol : aquabidest (90:10) yang mengandung HCl 1,85 M dan Butyl Hidroxy Toluene (BHT) 0,1% b/v pada suhu 90OC. Proses soxhletasi dihentikan setelah mencapai 18 kali sirkulasi larutan penyari. Hasil soxhlet atau ekstrak didiamkan selama beberapa saat pada suhu kamar hingga suhunya kurang lebih sama dengan suhu kamar. Ekstrak dipindahkan ke dalam labu takar 250 ml lalu diencerkan dengan ditambahkan larutan metanol : aquabides (90:10) hingga tanda. Sejumlah 25 ml ekstrak diuapkan dengan rotary evaporator hingga 5 ml.
3. Skrining metode clean up
Dilakukan metode clean up dengan cara partisi, yaitu ekstraksi cair – cair antara larutan metanol:air (90:10) dengan n-heksana, air dengan etil asetat. Fraksi
– fraksi tersebut ditotolkan pada KLT-densitometri yang telah dioptimasi.
4. Optimasi jenis fase diam dan fase gerak SPE
a. Pembuatan HCl 0,002 N. Sejumlah 2,21 ml HCl 32% dimikropipet dan dipindahkan pada labu takar 25 ml, diencerkan dengan aquabidest hingga batas tanda menjadi HCl 1 N. Sejumlah 200 µl larutan HCl 1 N dimikropipet dan dipindahkan ke labu takar 100 ml, diencerkan dengan aquabidest hingga batas tanda menjadi HCl 0,002 N.
b. Fase diam diol
1) Pengkondisian (conditioning). Sejumlah 2 ml metanol p.a. dialirkan pada kolom SPE diol kemudian tetesan ditampung pada tabung reaksi. Selanjutnya dialirkan berturut – turut 2 ml etil asetat p.a. dan 2 ml n-heksana p.a. ke dalam kolom SPE diol.
2) Pengisian (loading) sampel. Sejumlah 0,3 ml sampel pekat dimasukkan ke dalam kolom SPE diol.
3) Pengelusian (eluting). Sejumlah 4 ml n-heksana p.a. dialirkan melalui kolom, tetesan eluen ditampung pada tabung reaksi. Berturut – turut 4 ml etil asetat p.a. dan metanol p.a. dialirkan ke dalam kolom dan eluen ditampung pada tabung reaksi.
dalam labu takar 5 ml dan diencerkan hingga batas tanda. Fraksi – fraksi tersebut di-milipore dan di-ultrasonikasi selama 10 menit.
c. Fase diam silika
1) Pengkondisian (conditioning). Sejumlah 2 ml metanol p.a. dialirkan pada kolom SPE silika kemudian tetesan ditampung pada tabung reaksi. Selanjutnya dialirkan berturut – turut 2 ml etil asetat p.a. dan 2 ml n-heksana p.a. ke dalam kolom SPE silika.
2) Pengisian (loading). Sejumlah 0,3 ml sampel pekat dimasukkan ke dalam kolom SPE.
3) Pengelusian (eluting). Sejumlah 4 ml n-heksana p.a. dialirkan melalui kolom, tetesan eluen ditampung pada tabung reaksi. Berturut – turut 4 ml etil asetat p.a. dan metanol p.a. dialirkan ke dalam kolom dan eluen ditampung pada tabung reaksi.
4) Preparasi sampel. Fraksi n-heksana, etil asetat, dan metanol diuapkan dengan rotary evaporator lalu dilarutkan pada metanol p.a. Sejumlah tertentu metanol p.a. dari fraksi n-heksana, etil asetat, dan metanol dipindahkan ke dalam labu takar 5 ml dan diencerkan hingga batas tanda. Fraksi – fraksi tersebut di-milipore dan di-ultrasonikasi selama 10 menit.
d. Fase diam C18
2) Pengisian (loading). Sejumlah 0,2 ml sampel pekat dimasukkan ke dalam kolom SPE C18.
3) Pengelusian (eluting). Sejumlah 6 ml HCl 0,002 N dialirkan melalui kolom, tetesan eluen ditampung pada tabung reaksi. Sejumlah 5 ml metanol p.a. dialirkan ke dalam kolom dan eluen ditampung pada tabung reaksi.
4) Preparasi sampel. Fraksi HCl 0,002 N diuapkan dengan rotary evaporator lalu dilarutkan pada metanol p.a., dipindahkan pada labu takar
5 ml dan ditmbahkan metanol hingga batas tanda. Sejumlah 5 ml fraksi metanol diencerkan dengan labu takar 10 ml hingga batas tanda. Fraksi – fraksi tersebut di-milipore dan di-ultrasonikasi selama 10 menit.
5. Optimasi volume fase gerak (eluen)
a. Pengkondisian (conditioning). Berturut – turut 2 ml metanol p.a. dan 2 ml HCl 0,002 N dialirkan pada kolom SPE C18 kemudian tetesan ditampung pada tabung reaksi.
b. Pengisian (loading). Sejumlah 0,1 ml sampel pekat dimasukkan ke dalam kolom SPE C18.
c. Pencucian (washing). Sejumlah 6 ml HCl 0,002 N dialirkan melalui kolom, tetesan eluen ditampung pada tabung reaksi.
d. Pengelusian (eluting).
1) Sejumlah 5 ml metanol p.a. dialirkan ke dalam kolom dan eluen ditampung pada tabung reaksi.
3) Sejumlah 10 ml metanol p.a. dialirkan ke dalam kolom dan eluen ditampung pada tabung reaksi.
e. Preparasi sampel. Fraksi metanol sejumlah 7,5 ml dan 10 ml diuapkan dengan rotary evaporator. Setelah teruapkan diencerkan dengan metanol p.a. di dalam labu takar 5 ml hingga tanda batas, lalu milipore dan di-ultrasonikasi selama 10 menit.
6. Penentuan kapasitas kolom SPE
a. Pengkondisian (conditioning). Berturut – turut 2 ml metanol p.a. dan 2 ml HCl 0,002 N dialirkan pada kolom SPE C18 kemudian tetesan ditampung pada tabung reaksi.
b. Pengisian (loading).
1) Sejumlah 0,05 ml sampel pekat dimasukkan ke dalam kolom SPE C18.
2) Sejumlah 0,1 ml sampel pekat dimasukkan ke dalam kolom SPE C18.
3) Sejumlah 0,2 ml sampel pekat dimasukkan ke dalam kolom SPE C18.
c. Pengelusian (eluting). Sejumlah 6 ml HCl 0,002 N dialirkan melalui kolom, tetesan eluen ditampung pada tabung reaksi. Sejumlah 6 ml metanol p.a. dialirkan ke dalam kolom dan eluen ditampung pada tabung reaksi.
d. Preparasi sampel. Fraksi HCl 0,002 N diuapkan dengan rotary evaporator lalu dilarutkan pada metanol p.a., dipindahkan pada labu takar 5 ml
diuapkan dengan rotary evaporator. Setelah teruapkan, diencerkan dengan metanol p.a. di dalam labu takar 5 ml hingga tanda batas, lalu milipore dan di-ultrasonikasi selama 10 menit.
7. Identifikasi kuersetin
Analit yang diperoleh dari hasil SPE kemudian diinjeksikan pada sistem KCKT fase terbalik yang sudah teroptimasi dengan kolom C18 detektor UV pada panjang gelombang 370 nm, flow rate 1 mL, komposisi fase gerak aquabidest-metanol-asam fosfat 1% (55:45:1).
G. Analisis Hasil Optimasi
Data kromatogram yang diperoleh pada baku diamati sehingga dapat diketahui sistem SPE yang memberikan hasil optimal, yaitu dengan menghitung nilai resolusi dan menghitung nilai efisiensi clean up.
1. Analisis kualitatif
Analisis kualitatif dilakukan dengan cara membandingkan waktu retensi antara kromatogram baku kuersetin dengan kromatogram fraksi hasil elusi SPE.
2. Nilai resolusi
Nilai resolusi pemisahan peak dihitung terhadap peak terdekat dengan
rumus: Rs = 𝑡𝑅1 − 𝑡𝑅2 (𝑤2+𝑤1)/2
Keterangan : tR1 dan tR2 = waktu retensi komponen
W1 dan W2 = lebar alas puncak
3. Nilai efisiensi clean up
Nilai efisiensi clean up dihitung dengan membandingkan jumlah peak sebelum SPE dengan jumlah peak sesudah SPE dengan rumus:
Efisiensi clean up= 𝑗𝑢𝑚𝑙𝑎 ℎ𝑝𝑢𝑛𝑐𝑎𝑘 𝑠𝑒𝑏𝑒𝑙𝑢𝑚 𝑆𝑃𝐸−𝑗𝑢𝑚𝑙𝑎 ℎ𝑝𝑢𝑛𝑐𝑎𝑘 𝑠𝑒𝑠𝑢𝑑𝑎 ℎ𝑆𝑃𝐸
24
BAB IV
HASIL DAN PEMBAHASAN
A. Pembuatan Serbuk Daun Teh
Sebelum dilakukan ekstraksi dengan metode sokhletasi, sampel daun teh kering yang diperoleh dari PT. Pagilaran diserbuk dahulu. Tujuan dari proses penyerbukan ini adalah untuk memperluas area kontak antara pelarut dengan sampel sehingga ketika proses ekstraksi, pelarut akan lebih banyak berinteraksi dengan sel tanaman. Dengan proses penyerbukan sampel ini diharapkan proses ekstraksi bisa berlangsung maksimal.
Setelah diperoleh serbuk daun teh, dilakukan penyaringan dan pencampuran serbuk daun teh. Dalam proses penyaringan ini serbuk akan terpisah berdasarkan ukuran partikelnya. Ukuran partikel serbuk yang diambil adalah serbuk yang berukuran partikel kecil karena memiliki luas area kontak dengan pelarut yang lebih besar. Tujuan pencampuran serbuk daun teh adalah untuk menghomogenkan sampel.
B. Ekstraksi dengan Menggunakan Metode Soxhlet Sekaligus Hidrolisis
Metode ekstraksi yang digunakan adalah soxhletasi. Soxhletasi adalah ekstraksi menggunakan pelarut yang selalu baru umumnya dilakukan dengan alat khusus sehingga terjadi ekstraksi kontinyu dengan jumlah pelarut yang relatif konstan dengan adanya pendingin balik (DirJen POM, 2010). Dikatakan “pelarut
selalu baru” karena pelarut yang berada di dalam labu akan menguap dan
terkondensasi oleh adanya pendingin balik sehingga menetes mengisi tabung sifon dan membasahi tea bag di dalamnya. Pelarut yang membawa ekstrak, akan memenuhi tabung sifon dan kembali ke dalam labu yang nantinya akan menguap dan terkondensasi lagi sehingga bisa dikatakan terjadi ekstaksi secara kontinyu (berkesinamungan).
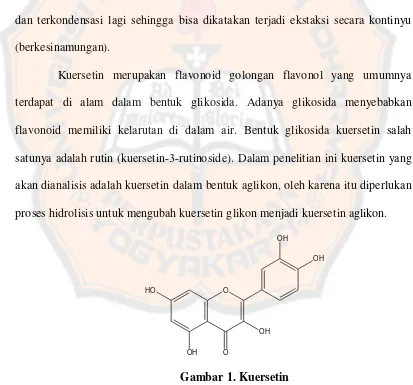
Kuersetin merupakan flavonoid golongan flavonol yang umumnya terdapat di alam dalam bentuk glikosida. Adanya glikosida menyebabkan flavonoid memiliki kelarutan di dalam air. Bentuk glikosida kuersetin salah satunya adalah rutin (kuersetin-3-rutinoside). Dalam penelitian ini kuersetin yang akan dianalisis adalah kuersetin dalam bentuk aglikon, oleh karena itu diperlukan proses hidrolisis untuk mengubah kuersetin glikon menjadi kuersetin aglikon.
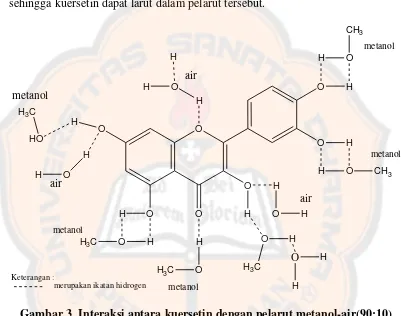
Pada proses ekstraksi yang disertai hidrolisis ini digunakan larutan penyari metanol:air (90:10) yang mengandung HCl 1,85 M. Pelarut yang dipilih adalah metanol:air (90:10) karena adanya gugus - gugus hidroksil pada kuersetin menyebabkan larutan metanol-air mampu berinteraksi secara hidrogen bonding sehingga kuersetin dapat larut dalam pelarut tersebut.
O
Gambar 3. Interaksi antara kuersetin dengan pelarut metanol-air(90:10).
Gambar 4. Reaksi hidrolisis pada suatu kuersetin glikon
Suhu yang digunakan dalam proses sokhletasi sekaligus hidrolisis ini adalah 90°C. Pada suhu tersebut metanol akan menguap dan mengalami kondensasi sehingga menetes dan membasahi tea bag mengisi ruang sifon.
C. Skrining Metode Clean Up
Tabel II. SPE – KLT densitometri
SPE pengelusi hasil keterangan
diol
kuersetin karena terelusi oleh metanol
metanol ada kuersetin
mengelusi hampir semua senyawa selain kuersetin, masih ada kuersetin yang terjerap kuat pada diol
aseton ada
kuersetin karena terelusi oleh metanol
metanol ada kuersetin
Tabel III. Ekstraksi cair – cair
Ekstraksi Cair – Cair Hasil
Sampel dalam pelarut metanol-air (90:10) diuapkan metanolnya dan ditambahkan aquabidest. Paritsi antara
aquabidest dengan etil asetat analit larut dalam etil asetat. Etil asetat diuapkan dan pelarutnya diganti dengan
metanol.
Beberapa senyawa yang polar (larut dalam air)
berkurang
Sampel dalam pelarut metanol-air (90:10) dipartisi dengan n-heksana analit berada dalam fraksi metanol-aquabidest(90:10). Metanol diuapkan dan ditambahkan aquabidest. Paritsi antara aquabidest dengan etil asetat
Optimasi metode SPE dengan menggunakan Kromatografi Cair Kinerja Tinggi (KCKT) akhirnya dipilih karena KCKT lebih sensitif dalam mendeteksi analit dibadingkan dengan Kromatografi Lapid Tipis Densitometri (KLT-Densitometri). Selain itu, ekstraksi cair – cair secara partisi tidak lagi dipilih karena tidak efektif dan tidak efisien dalam mendapatkan analit. Hal ini terkait dengan banyaknya pelarut yang digunakan dan koefisien distribusi kuersetin pada dua pelarut yang digunakan saat proses partisi.
Metode KLT Densitometri yang digunakan untuk skrining metode clean up berdasarkan penelitian Dharma (2012) dimana menggunakan fase diam silika,
fase gerak toluen-etil asetat-asam format (14:5:1). Sedangkan metode KCKT yang digunakan untuk optimasi jenis fase diam dan fase gerak SPE yang akan dibahas pada subbab selanjutnya adalah metode KCKT optimal dari penelitian Dwiyoga (2012), yaitu dengan menggunakan fase diam C8, fase gerak aquabidest-metanol (52,5:47,5) suhu kolom 30°C, dan flow rate 1,2 ml/menit.
D. Optimasi Jenis Fase Diam dan Fase Gerak SPE
Adapun tahap – tahap yang dilakukan dalam SPE adalah sebagai berikut : a. Pengkondisian
Cartridge (penjerap) dialiri dengan pelarut sampel untuk membasahi
permukaan penjerap dan untuk menciptakan nilai pH yang sama, sehingga perubahan – perubahan kimia yang tidak diharapkan ketika sampel dimasukkan dapat dihindari.
b. Retensi (tertahannya) sampel
Larutan sampel dilewatkan ke cartridge baik untuk menahan analit yang dituju, sementara komponen lain terelusi atau untuk menahan komponen yang tidak diharapkan sementara analit yang dituju terelusi.
c. Pembilasan
Tahap ini penting untuk menghilangkan seluruh komponen yang tidak tertahan oleh penjerap selama tahap retensi.
d. Elusi
Tahap ini merupakan tahap terakhir untuk mengambil analit yang dituju jika analit tersebut tertahan pada penjerap (Rohman, 2009).
1. Fase diam (cartridge) silika. Fase diam silika merupakan sistem kromatografi fase normal. Dikatakan demikian karena fase diam yang digunakan lebih polar daripada fase geraknya.
Pengkondisian dilakukan dengan mengalirkan metanol, etil asetat, dan n-heksana secara berturut – turut. Digunakan etil asetat sebelum dialirkan n-heksana karena metanol dan n-heksana tidak saling bercampur dalam volume yang sama karena tidak terjadi interaksi antara n-heksana dengan metanol, serta adanya perbedaan indeks polaritas yang jauh antara metanol (5,1) dan n-heksana (0,1). Oleh karena itu, dibutuhkan fase gerak yang tingkat kepolarannya menengah yang mampu berinteraksi dengan dua fase gerak tadi yaitu etil asetat dimana memiliki nilai indeks polaritas 4,4. Dengan demikian tidak ada molekul metanol yang tertinggal di cartridge saat dialiri n-heksana karena sudah terelusi oleh adanya etil asetat.
Sejumlah 0,3 ml sampel dimasukkan ke dalam cartridge SPE silika kemudian berturut – turut dielusi dengan 4 ml n-heksana, 4 ml etil asetat, dan 4 ml metanol. Kuersetin larut dalam etil asetat dan metanol, namun tidak dalam heksana. Dengan demikian fase gerak yang digunakan sebagai pembilas adalah n-heksana. Fraksi – fraksi tersebut kemudian diinjeksikan pada KCKT yang telah dioptimasi oleh Dwiyoga (2012) yaitu dengan menggunakan fase diam C8, fase gerak aquabidest-metanol (52,5:47,5) suhu kolom 30°C, dan flow rate 1,2 ml/menit.
dari kolom hingga sampai ke detektor. Adapun kromatogram yang didapatkan sebagai berikut.
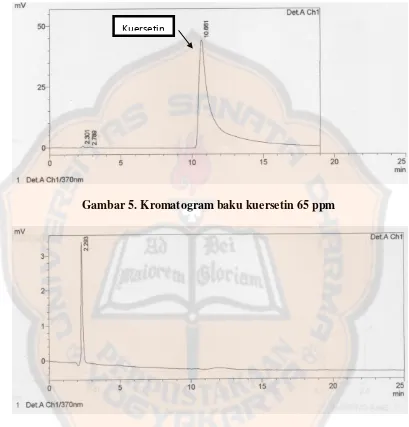
Gambar 5. Kromatogram baku kuersetin 65 ppm
Gambar 6. Kromatogram hasil elusi dengan n-heksana (silika)
Berdasarkan hasil kromatogram di atas menunjukkan bahwa fraksi hasil elusi dengan n-heksana tidak menunjukkan adanya kuersetin. Hal ini ditunjukkan dengan tidak munculnya puncak kuersetin pada sekitar menit 10. N-heksana tidak melarutkan kuersetin sehingga n-heksana tidak mampu mengelusi kuersetin dari fase diam, kuersetin lebih teradsorpsi pada fase diam silika.
Gambar 7. Kromatogram hasil elusi dengan etil asetat (silika)
Pada kromatogram fraksi etil asetat terdapat puncak dengan tR 10,428 menit. Puncak tersebut adalah puncak kuersetin karena memiliki tR yang mirip dengan tR baku kuersetin. Etil asetat mampu mengelusi kuersetin karena kuersetin larut dalam etil asetat dan juga etil asetat mampu berinteraksi dengan kuersetin.
Gambar 8. Kromatogram hasil elusi dengan metanol
Pada kromatogram fraksi metanol terdapat puncak dengan tR 10,429 menit yang merupakan puncak kuersetin karena kemiripan tR-nya dengan baku
Kuersetin
kuersetin. Metanol mampu mengelusi kuersetin karena kuersetin larut dalam metanol dan metanol mampu berinteraksi dengan kuersetin.
Dari kromatogram di atas tampak bahwa etil asetat dan metanol mampu mengelusi kuersetin. Area Under Curve kuersetin pada fraksi metanol lebih kecil daripada AUC kuersertin pada fraksi etil asetat karena kuersetin yang tersisa dalam cartridge tinggal sedikit, sebagian besar terlusi oleh etil asetat. Jumlah puncak yang ada dalam kromatogram fraksi etil asetat dan metanol sama, yaitu 14 puncak.
Etil asetat mampu mengelusi kuersetin dengan jumlah besar, namun demikian juga koekstraktan yang terikut juga banyak. Nilai resolusi kuersetin dengan puncak di sebelah kirinya sebesar 0,5666 dan nilai resolusi kuersetin dengan puncak di sebelah kanannya sebesar 1,3716. Hal ini menunjukkan bahwa etil asetat tetap mengelusi koekstraktan yang memiliki kepolaran yang mirip dengan kuersetin. Dengan sistem SPE ini nilai resolusi yang baik tidak tercapai,
nilai resolusi yang baik adalah RS ≥ 1,5.
2. Fase diam (cartridge) diol. Fase diam diol yang dipakai dalam sistem ini merupakan sistem kromatografi fase normal. Dikatakan demikian karena fase diam yang digunakan lebih polar daripada fase geraknya.
Oleh karena itu, dibutuhkan fase gerak yang semi polar yang mampu berinteraksi dengan dua fase gerak tadi yaitu etil asetat dimana memiliki nilai indeks polaritas 4,4. Dengan demikian tidak ada molekul metanol yang tertinggal di cartridge saat dialiri n-heksana karena sudah terelusi oleh adanya etil asetat.
Sejumlah 0,3 ml sampel dimasukkan ke dalam cartridge SPE silika kemudian berturut – turut dielusi dengan 4 ml n-heksana, 4 ml etil asetat, dan 4 ml metanol. Kuersetin larut dalam etil asetat dan metanol, namun tidak dalam heksana. Dengan demikian fase gerak yang digunakan sebagai pembilas adalah n-heksana.
Analisis kualitatif yang dilakukan adalah dengan membandingkan waktu retensi (tR) baku kuersetin dengan puncak kromatogram fraksi n-heksana, fraksi etil asetat, dan fraksi metanol yang memiliki tR yang mirip dengan kuersetin. Adapun kromatogram yang didapatkan sebagai berikut.
Gambar 5. Kromatogram baku kuersetin 65 ppm
Gambar 9. Kromatogram hasil elusi dengan n-heksana (diol)
Gambar 10. Kromatogram hasil elusi dengan etil asetat (diol)
Gambar 11. Kromatogram hasil elusi dengan metanol (diol)
Dilihat dari kromatogram fraksi n-heksana, etil asetat, dan metanol memiliki kemiripan profil kromatogram dengan kromatogram hasil SPE menggunakan cartridge silika. Hal ini karena diol memiliki sistem kromatogrfi fase normal seperti pada penggunaan cartridge silika.
Nilai resolusi puncak kuersetin yang didapatkan pada kromatogram fraksi etil asetat juga tidak memenuhi parameter resolusi yang baik. Nilai resolusi puncak kuersetin dengan puncak di sebelah kirinya adalah 0,4796, sedangkan nilai resolusi puncak kuersetin dengan puncak di sebelah kanannya adalah 1,4549. Hal ini menunjukkan bahwa etil asetat mengelusi senyawa lain yang memiliki kepolaran yang mirip dengan kuersetin, yaitu senyawa yang memiliki tR yang berdekatan dengan kuersetin.
3. Fase diam (cartridge) C18. Fase diam kolom SPE C18 merupakan sistem kromatografi fase terbalik. Hal ini karena fase gerak yang digunakan lebih polar daripada fase diamnya.
Pengkondisian dilakukan dengan mengalirkan metanol kemudian dialirkan HCl 0,002 N. Digunakan metanol karena metanol memiliki viskositas yang rendah sehingga bisa membasahi seluruh partikel C18 pada kolom. Kemudian HCl 0,002 N dialirkan agar suasana kolom menjadi asam. Digunakan HCl 0,002 N karena pH-nya 3 sehingga masih masuk dalam range pH yang aman untuk fase diam C18. Karena suasana asam maka kuersetin yang berada dalam kolom akan berubah menjadi bentuk molekul sehingga kuersetin akan mengalami retensi pada kolom C18.
Gambar 12. Kromatogram baku kuersetin 14 ppm
Gambar 13. Kromatogram hasil elusi dengan HCl 0,002 N
Pada kromatogram di atas tampak bahwa senyawa kuersetin masih ada yang ikut terelusi oleh fase gerak HCl 0,002 N. Hal ini karena kuersetin memang memiliki kelarutan pada aquabidest. Jumlah kuersetin yang terelusi tidak sebanyak pada fase gerak metanol.
Gambar 14. Kromatogram hasil elusi dengan metanol
Pada fraksi ini tampak bahwa terdapat puncak kuersetin dilihat dari tR puncak yang muncul pada menit 10,418. Kuersetin larut dalam metanol sehingga kuersetin bisa terelusi oleh metanol. Nilai resolusi puncak kuersetin dengan puncak di sebelah kirinya adalah 1,6773. Dengan demikian parameter resolusi tercapai yaitu nilai resolusi lebih besar dari 1,5. Hal ini menunjukkan bahwa kolom SPE C18 mampu menahan senyawa yang memiliki kepolaran mirip dengan kuersetin yang ditunjukkan dengan tidak munculnya puncak dengan tR dekat dengan kuersetin.
Metode SPE dengan larutan pembilas (washing) 0,002 N HCl dan pengelusi metanol juga diaplikasikan pada sistem KCKT optimum yang didapatkan oleh Dwiyoga (2012). Sistem KCKT tersebut menggunakan fase diam oktildesilsilan (C18), campuran fase gerak metanol-aquabidest-asam fosfat 5% (54:45:1), kecepatan alir 1,0 mL/menit, suhu oven 30° C dengan sistem gradien. Adapun kromatogram yang didapatkan adalah sebagai berikut.
Gambar 15. Kromatogram baku kuersetin 10 ppm
Gambar 16. Kromatogram fraksi metanol
Kromatogram di atas merupakan hasil dari sistem KCKT elusi gradien. Konsentrasi fase gerak metanol meningkat mulai menit ke-20 sehinga baseline berubah menjadi naik. Tujuan memakai sistem elusi gradien agar puncak terakhir cepat terelusi sehingga tidak memakan waktu lama untuk menunggu waktu retensinya.
Dari kromatogram di atas didapatkan tR baku kuersetin pada menit 15,963 sehingga puncak yang memiliki tR 15,557 pada kromatogram fraksi
Kuersetin
metanol dipastikan menjadi puncak kuersetin. Dengan demikian puncak kuersetin muncul di sekitar menit ke-15.
Resolusi yang didapatkan dari fraksi metanol dengan cartridge SPE C18 sejumlah 3x replikasi yaitu :
Tabel IV. Rata – rata resolusi
replikasi kiri puncak kuersetin Rs puncak kuersetin w (menit) tR (menit) w (menit) tR (menit) demikian metode SPE cartridge C18 dengan larutan pengelusi metanol memenuhi parameter resolusi. Dengan tertahannya senyawa yang memiliki tR dekat dengan kuersetin pada cartridge SPE C18, maka proses clean up ini menunjang tercapainya resolusi yang baik pada sistem KCKT tersebut.
Efisiensi clean up merupakan kemampuan suatu metode SPE dalam mengurangi jumlah senyawa selain analit yang ikut terekstraksi. Senyawa – senyawa selain analit yang ikut terekstraksi tersebut disebut koekstraktan. Koekstraktan bisa menganggu proses determinasi suatu analit, oleh karena itu sebisa mungkin jumlah koekstraktan dikurangi.
Gambar 17. Kromatogram sampel sebelum SPE
Pada kromatogram fraksi metanol SPE C18 dari kromatogram – kromatogram sebelumnya didapatkan 9 – 10 puncak dan dari kromatogram sampel sebelum SPE di atas terdapat 16 puncak. Hal ini menunjukkan bahwa metode SPE mampu mengurangi jumlah koekstraktan. Adapun perhitungannya
adalah (𝑗𝑢𝑚𝑙𝑎 ℎ𝑝𝑢𝑛𝑐𝑎𝑘 𝑠𝑒𝑏𝑒𝑙𝑢𝑚 𝑆𝑃𝐸−𝑗𝑢𝑚𝑙𝑎 ℎ𝑝𝑢𝑛𝑐𝑎𝑘 𝑠𝑒𝑠𝑢𝑑𝑎 ℎ𝑆𝑃𝐸)
𝑗𝑢𝑚𝑙𝑎 ℎ𝑝𝑢𝑛𝑐𝑎𝑘 𝑠𝑒𝑏𝑒𝑙𝑢𝑚 𝑆𝑃𝐸 𝑥 100% =
(16−9)
16 𝑥 100% = 43,75%. Karena ada puncak kromatogram berjumlah 10
puncak maka didapatkan juga hasil perhitungan efisiensi clean up sebesar 37,5%. Dengan demikian nilai efisiensi clean up metode ini adalah 37,5 – 43,75%. Angka tersebut menunjukkan bahwa metode ini kurang efisien.
E. Optimasi Volume Fase Gerak (Eluen)
Tujuan dilakukannya optimasi volume fase gerak pengelusi adalah untuk mendapatkan berapa volume fase gerak pengelusi (metanol) yang dibutuhkan agar semua analit terelusi dari kolom SPE. Dengan mendapatkan kepastian seberapa jumlah volume metanol yang dibutuhkan maka diharapkan mampu mengefisienkan penggunaan sejumlah metanol sebagai eluen. Jika penggunaan fase gerak efisien maka tidak akan membuang – buang metanol berlebih atau pun sebaliknya yaitu volume eluen tidak kurang untuk menarik analit.
Tabel V. Optimasi volume eluen
volume eluen (ml) AUC (dalam 100000) replikasi 1 replikasi 2 rata - rata
5 2,51277 2,4758 2,494285
7,5 2,92801 2,87266 2,900335 10 2,60228 2,62976 2,61602
Volume sampel yang dimasukkan ke dalam kolom SPE C18 adalah 0,1 ml. Kemudian dibilas (washing) menggunakan HCl 0,002 N sejumlah 6 ml yang selanjutnya dielusi dengan metanol sejumlah 5 ml; 7,5 ml; dan 10 ml. Respon
Area Under Curve (AUC) pada masing – masing volume berbeda – beda dengan
AUC pada volume 7,5 ml disebabkan karena kesalahan pada saat pengisian sampel yang tidak pas 0,1 ml sehingga terjadi kenaikan AUC.
Gambar 18. Kurva volume eluen vs AUC
Volume eluen dan respon AUC yang didapatkan kemudian diplotkan untuk mengetahui hubungan antara penambahan volume eluen dengan respon AUC dan didapatkan persamaan y = 0,024x + 2,487. Dengan menggunakan one sample t-test, nilai slope 0,024 dibandingkan dengan nilai 0 untuk mengetahui ada
atau tidaknya perbedaan yang bermakna antara kedua nilai tersebut. Didapatkan bahwa t hitung = 1,0496 < t tabel = 4,30. Dengan demikian tidak ada perbedaan signifikan antara antara nilai slope dengan 0. Hal ini menunjukkan penambahan volume eluen tidak akan memberikan perbedaan berarti pada nilai AUC. Oleh karena itu volume metanol pengelusi yang dipakai adalah 5 – 10 ml. Namun lebih dipilih volume pengelusi tidak lebih dari 10 ml agar koekstraktan yang terjerap pada fase diam C18 tidak ikut terelusi.
y = 0,024x + 2,487
F. Penentuan Kapasitas Kolom SPE C18
Penentuan kapasitas kolom SPE bertujuan untuk mengetahui kemampuan cartridge SPE dalam menahan (retensi) sampel dalam jumlah tertentu. Dalam hal
ini bertujuan untuk mencari batasan volume sampel yang boleh dimasukkan ke dalam kolom SPE agar mampu tertahan di kolom.
Penentuan kapasitas kolom ini dilakukan dengan mengubah volume sampel yang dimasukkan ke dalam kolom SPE dari 0,05 ml; 0,1 ml; dan 0,2 ml. Kemudian sampel dielusi pertama dengan HCl 0,002 N lalu dielusi dengan metanol. Jika ada kuersetin yang terelusi oleh HCl 0,002 N maka hal itu menunjukkan bahwa cartridge SPE tidak bisa menahan sampel.
Gambar 20. Kromatogram fraksi HCl 0,002 N pada pengisian 0,1 ml sampel
Gambar 21. Kromatogram fraksi HCl 0,002 N pada pengisian 0,2 ml sampel
0,005 – 0,2 ml pada cartridge SPE C18, kuersetin masih bisa ditahan. Batas sampai dimana analit tidak tertahan lagi di cartridge SPE tidak diketahui, karena hanya dilakukan pengisian sampel hingga volume 0,2 ml.
49
BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
Berdasarkan hasil penelitian, dapat diambil kesimpulan bahwa metode SPE kolom C18 dapat digunakan untuk mengurangi jumlah senyawa – senyawa lain (koekstraktan) pada ekstrak teh hijau dengan menggunakan larutan pencuci 6 ml HCl 0,002 N dan larutan pengelusi 5 - 10 ml metanol pada volume pengisian sampel 0,1 ml dengan parameter optimum resolusi 2,994 namun didapatkan efisiensi clean up yang kurang baik, yaitu 37,5 – 43,75%.
B. Saran
50
DAFTAR PUSTAKA
Dharma, P.S., 2012, Optimasi Proses Ekstraksi Kuersetin Total pada Teh Hijau dengan Metode Kromatografi Lapis Tipis-Densitometri, Skripsi, Universitas Sanata Dharma, Yogyakarta.
Direktorat Jenderal Pengawasan Obat dan Makanan, 1986, Sediaan Galenik, Departemen Kesehatan Republik Indonesia, Jakarta, pp. 3-7, 26.
Direktorat Jenderal Pengawasan Obat dan Makanan RI, 1995, Farmakope Indonesia, edisi IV, Departemen Kesehatan Republik Indonesia, Jakarta, 299, 1009-1010.
Direktorat Jenderal Pengawasan Obat dan Makanan RI, 2010, Acuan Sediaan
Herbal, volume kelima, edisi I, Departemen Kesehatan Republik
Indonesia, Jakarta, 299, 64-65.
Dwiyoga, A.R.H., 2012, Optimasi dan Validasi Penetapan Kadar Kuersetin Menggunakan Kromatografi Cair Kinerja Tinggi (KCKT) fase Terbalik dalam Teh Hijau (Camelia sinensis O.K.), Skripsi, Universitas Sanata Dharma Yogyakarta.
Gandjar, I.G. dan Rohman, A., 2009, Kimia Farmasi Analisis, Pustaka Pelajar, Yogyakarta, pp. 379.
Hendayana, S., 2006, Kimia Pemisahan Metode Kromatografi dan Elektroforesis Modern, PT. Remaja Rosdakarya, Bandung, 21-25.
Kodama, D.H., Goncalves, A.E.d.S.S., Lajolo, F.M., and Genovese, M.I., 2010, Flavonoids, Total Phenolics and Antioxidant Capacity: Comparison between Commercial Green Tea Preparations, Ciencia e Technologia de Alimentos, 1077.
Markham, K.R., 1988, Techniques of Flavonoid Identification, diterjemahkan oleh Kosasih Padmawinata, hal. 15, Penerbit ITB, Bandung.
Mokgadi, J., Mmualefe, L.C., and Torto, N., 2009, SampliQ OPT Solid Phase Extraction Sorbent in the Cleanup of Flavonoids in Ginkgo Biloba by HPLC-DAD, Agilent Technologies, 1 – 8.
Munson, J. W., 1991, Pharmaceutical Analysis Modern Methods, diterjemahkan oleh Harjana, Parwa B., Volume II, hal. 13-5, 8Airlangga University Press, Surabaya.
Pescok, R. L., Shields, L. D., and Cains, T., 1976, Modern Methods of Chemical Analysis, 2nd ed, John Wiley & Sons, Canada, pp. 51.
Phani, Ch. R. S., Vinaykumar, Ch., Rao, K.U., and Sindhuja, G., 2010, Quantitative Analysis of Quercetin in Natural Sources by RP-HPLC, IJRPBS, 19.
Rohman, A., 2009, Kromatografi untuk Analisis Obat, edisi 1, Graha Ilmu, Yogyakarta, pp. 36 – 38.
Sibuea, P., 2006, Makan Sehat Hidup Sehat, hal 162-165, diakses tanggal 3 april 2011.
Silva, A. F. V. D., 2012, Validasi Metode dalam Penetapan Kadar Kuersetin Total dalam Daun Teh Segar (Camellia sinensis O.K.), Teh Hijau, dan Teh Hitam Menggunakan Metode Kromatografi Cair Kinerja Tinggi (KCKT) Fase Terbalik, Skripsi, Universitas Sanata Dharma, Yogyakarta.
Snyder, L.R., Kirkland, J.J., and Glajch, J.L., 1997, Practical HPLC Method Development, 2nd Edition, JohnWiley & Sons, Inc., New York, pp. 690.
Soraya, N., 2007, Sehat dan Cantik Berkat Teh Hijau, diakses tanggal 3 April 2011.
Stahl, E., 1985, Drug Analysis by Chromatography and Microscopy, Penerbit ITB, Bandung, pp. 1-8.
52
Lampiran 1. Kromatogram optimasi jenis fase gerak pada fase diam C18
1. Kromatogram fase diam C18 dengan fase gerak 0,002 N HCl replikasi 1
3. Kromatogram fase diam C18 dengan fase gerak 0,002 N HCl replikasi 2
Lampiran 2. Kromatogram optimasi jenis fase gerak pada fase diam diol
1. Kromatogram fase diam diol dengan fase gerak n-heksan replikasi 1
3. Kromatogram fase diam diol dengan fase gerak metanol replikasi 1
5. Kromatogram fase diam diol dengan fase gerak etil asetat replikasi 2
Lampiran 3. Kromatogram optimasi jenis fase gerak pada fase diam silika
1. Kromatogram fase diam silika dengan fase gerak n-heksan replikasi 1
3. Kromatogram fase diam silika dengan fase gerak metanol replikasi 1
5. Kromatogram fase diam silika dengan fase gerak etil asetat replikasi 2
Lampiran 4. Kromatogram optimasi volume
1. Volume eluen 5 ml metanol replikasi 1
3. Volume eluen 7,5 ml metanol replikasi 1
5. Volume eluen 10 ml metanol replikasi 1
Lampiran 5. Kromatogram kapsitas
1. Fraksi air pada 0,05 ml sampel replikasi 1
3. Fraksi air pada 0,05 ml sampel replikasi 2
5. Fraksi air pada 0,1 ml sampel replikasi 1
7. Fraksi air pada 0,1 ml sampel replikasi 2
9. Fraksi air pada 0,2 ml sampel replikasi 1
11.Fraksi air pada 0,2 ml sampel replikasi 2
Lampiran 6. Contoh cara perhitungan resolusi
Lampiran 7. Contoh cara perhitungan efisiensi clean up
Rumus :
Lampiran 8. Contoh cara perhitungan t-test
Rumus : t = (rata – rata –nilai yang diketahui) x √jumlah sampel/standar deviasi Diketahui persamaan : y = 0,02435x + 2,48761
derajat kebebasan = n-1 = 3-1 = 2 t tabel untuk tingkat kepercayaan 95% = 4,30
72
BIOGRAFI PENULIS
Penulis skripsi yang berjudul “Optimasi Clean Up Ekstrak Metanol Air The Hijau dengan Menggunakan Metode Solid Phase Extraction (SPE) Untuk Determinasi Kuersetin dalam
Teh Hijau” bernama lengkap Adi Wirasaputra. Penulis lahir di Klaten pada tanggal 20 Oktober 1989 sebagai anak pertama dari pasangan Tri Setiyo Widiyanto dan Yuniati Dewi Dyah Kuswandari. Penulis telah menyelesaikan pendidikannya di SD Maria Assumpta Klaten (2002), di SMP Pangudi Luhur 1 Klaten (2005), SMA Kolese De Britto Yogyakarta (2008). Penulis melanjutkan pendidikannya di Fakultas Farmasi Universitas Sanata Dharma Yogyakarta pada tahun 2008. Selama menempuh pendidikan di Fakultas Farmasi Universitas Sanata Dharma Yogyakarta, penulis aktif dalam kegiatan seperti menjadi panitia Pharmacy Performances and Event Cup 2008, panitia TITRASI 2009, menjadi panitia
Pharmacy Performances and Event Cup 2010, kegiatan donor darah, dan panitia