INTISARI
Sinar UV menimbulkan Reactive Oxygen Species (ROS) yang dapat ditanggulangi dengan antioksidan. Kelopak bunga rosella (Hibiscus sabdarifa L.) mengandung senyawa antioksidan antosianin namun rentan terhadap kerusakan, sehingga perlu diformulasikan dalam sediaan yang dapat menjerap yaitu multiemulsi A/M/A dan suspensi liposom. Penelitian bertujuan untuk memperoleh formula optimum dan kondisi penyimpanan multiemulsi A/M/A, serta mengetahui pengaruh penyimpanan terhadap stabilitas antosianin ekstrak rosella dalam multiemulsi A/M/A dan suspensi liposom yang ditunjukkan dengan laju disipasi dan entrapment efficiency.
Formula optimum diperoleh dengan optimasi formula kemudian diuji sifat dan stabilitas fisiknya. Laju disipasi ditetapkan slope persamaan ln jumlah antosianin ekstrak kelopak bunga rosella total dan fase luar multiemulsi A/M/A dan suspensi liposom. Entrapment efficiency dihitung dengan mengukur persentase selisih antosianin ekstrak kelopak bunga rosella total dan fase luar kedua sediaan dengan menggunakan metode spektrofotometer visibel derivatif. Analsis statistik dilakukan dengan t-test.
- wadah terlindung dari cahaya dengan penambahan gas nitrogen, serta multiemulsi A/M/A dengan kondisi penyimpanan optimum memiliki laju disipasi dan entrapment efficiency antosianin ekstrak kelopak bunga rosella lebih tinggi daripada suspensi liposom.
ABSTRACT
UV light could induced production of Reactive Oxygen Spesies (ROS) which can solved by using antioxidant. Roselle (Hibiscus sabdariffa L.) was contained anthocyanin as an antioxidant agent, but this compound was less stable in environmental conditions, so it needs to be formulated in a dosage form that could entrapped and protect it. The aim of this study were to determine optimum formula of multiple emulsion and storage condition, stability of anthocyanin roselle extract in W/O/W multiple emulsion and liposome suspension by evaluating the rate of dissipation and entrapment efficiency.
Optimum formula were obtain by optimize formula then was tested physical charateristic and stability. Rate of dissipation was determine by calculated slope ln amount of anthocianin roselle extract in entrapped and outer phase multi emulsion and liposome suspension. Entrapment efficiency was calculated by separating the total extract and the extract that not entrapped in both of dosage form, then was analyzed by derivative visible spectrophotometry. Statistical analyze was conducted by t-test.
The result showed that optimum multiple emulsion was produced, optimum storage condition are low temperature (-4ºC), in fotoprotective continer with adding nitrogen gas, W/O/W multiple emulsion in optimum storage condition has higher rate of dissipation and entrapment efficeincy than liposome suspension.
PENGARUH PENYIMPANAN TERHADAP STABILITAS EKSTRAK KELOPAK BUNGA ROSELLA (Hibiscus sabdariffa L.) DALAM SEDIAAN
MULTIEMULSI A/M/A DAN SUSPENSI LIPOSOM
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh: Me Li NIM : 118114177
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
i
PENGARUH PENYIMPANAN TERHADAP STABILITAS EKSTRAK KELOPAK BUNGA ROSELLA (Hibiscus sabdariffa L.) DALAM SEDIAAN
MULTIEMULSI A/M/A DAN SUSPENSI LIPOSOM
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh: Me Li NIM : 118114177
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iv
HALAMAN PERSEMBAHAN
There are three methods to gaining wisdom.
The first is reflection, which is the highest.
The second is limitation, which is the easiest.
The third is experience, which is the bitterest.
Confucius
I hear and I Forget
I See and I Remember
I do and I understand
Confucius
We keep moving forward, opening new doors, and doing new things,
Because we‟re curious and curiosity keep leading us down new paths
Walt Disney
Kupersembahakan karya ini kepada:
vii PRAKATA
Puji dan syukur kepada Tuhan Yang Maha Esa atas kasih dan karunia yang telah dilimpahkan sehingga saya dapat meyelesaikan skripsi dengan judul
“Pengaruh Penyimpanan terhadap Stabilitas Ekstrak Kelopak Bunga Rosella
(Hibiscus Sabdariffa L.) dalam Sediaan Multiemulsi A/M/A dan Suspensi Liposom” dengan baik. Skripsi ini merupakan salah satu syarat untuk memperoleh gelar Sarjana Farmasi (S.Farm.) di Fakultas Sanata Dharma Yogyakarta.
Selama proses perkuliahan, penelitian, penyusunan dan penyelesaian skripsi ini, penulis mendapakan motivasi, dorongan, doa, semangat, dukungan, saran serta kritik dari berbagai pihak. Oleh Karena itu, penulis ingin mengucapkan terima kasih kepada:
1. Ibu Aris Widyawati, M.Si., Ph.D selaku Dekan Fakultas Farmasi Universitas Sanata Dharma Yogyakarta
2. Ibu Prof. Dr. Sri Noegrohati, Apt., selaku Dosen Pembimbing yang telah banyak meluangkan waktu, bimbingan, diskusi, kritik, dan saran kepada penulis mulai dari proposal hingga selesainya skripsi ini.
3. Ibu Beti Pudyastuti, M.Sc., Apt. dan Dr. Yustina Sri Hartini, M.Sc., Apt. selaku Dosen Penguji yang telah bersedia meluangkan waktu untuk menjadi dosen penguji, serta memberikan pengarahan saran dan ktitik kepada penulis.
viii
5. Bapak Budiono dan Ibu Yuliana selaku orang tua penulis yang telah melahirkan, membesarkan penulis dengan penuh kasih sayang, edukasi informal, dan doa tiada henti sehingga penulis diperkenankan melanjutkan studi dan melakukan penelitian ini.
6. Drs. Sanjayadi, M.Sc., selaku dosen permbimbing pendamping yang telah banyak membimbing, dan memberikan banyak ilmu dan pengetahuan serta motivasi selama penelitian dan penyusunan skripsi.
7. Yohanes Dwiatmaka, M.Si. selaku dosen pembimbing akademik atas pendamping dan perhatian atas perkembangan saya selama perkuliahan. 8. Eva Mayangsari dan Yolana Kwartono sebagai sahabat dan keluarga satu
penelitian atas kerja sama, bantuan, kebersamaan dan berbagi dalam suka dan duka selama proses penelitian ini.
9. Ibu Sonia Chang, saudari Yessi Harianti, dan saudari Van-Ni selaku tante dan adik-adik dari penulis yang selalu memberikan motivasi dan mendukung penulis dalam menyelesaikan penelitian.
10. Han‟s Junidar, S.E., atas dukungan, motivasi, serta bantuan baik dalam bentuk semangat, sahabat cerita berbagi suka dan duka serta penyedia alat kepada peneliti sehingga dapat menyelesaikan penelitian ini.
ix
12. Tim Udang (Yolanda dan Adit), tim melon (Kiki, Lika, Devi, dan Miko), dan tim PPD (Verni, Shiro, Canly dan Erita) selaku teman dengan pembimbing yang sama, atas bantuan berupa sarana dan motivasi.
13. Seluruh dosen, teman-teman FSM D, teman-teman FST B 2011 dan Teman-teman satu angkatan 2011 Fakultas Farmasi Sanata Dharma, dan Teman- teman-teman KKN yang telah mendukung dan berbagi keceriaan untuk menyelesaikan penelitian ini.
14. Keluarga besar Pusdiklat Sukhawati Maitreiya, Vihara Bodhicitta Maitreya, teman-teman seperantauan 2011, atas doa, nasihat, dukungan selama peneiltian ini.
15. Semua pihak yang tidak dapat disebutkan satu persatu dalam bentuk doa, dukungan, dan nasihat sehingga penulis dapat menyelesaikan tugas akhir dengan baik.
Penulis menyadari bahwa penulis masih dalam proses pembelajaran sehingga penulis berharap kritik dan saran dari semua pihak demi kemajuan di masa yang akan datang. Semoga tugas akhir ini dapat bermanfaat bagi semua pihak terutama di bidang ilmu Farmasi.
x DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PERSERTUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
LEMBAR PERNYATAAN KEASLIAN KARYA ... v
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ... vi
PRAKATA ... vii
3. Keaslian Penelitian... 4
B. Tujuan ... 4
BAB II PENELAAHAN PUSTAKA... 6
A. Photoaging ... 6
B. Antioksidan ... 7
C. Kelopak Bunga Rosella (Hibiscus sabdariffa L.) ... 7
D. Antosianin ... 9
E. Multiemulsi A/M/A ... 11
F. Stabilitas Multiemulsi A/M/A ... 12
G. Bahan- Bahan Tambahan dalam Multiemulsi A/M/A ... 15
H. Suspensi Liposom ... 21
xi
J. Spektrofotometer Visibel Metode Derivatif ... 24
K. Laju Disipasi ... 25
L. Entrapment efficiency ... 26
M. Landasan Teori ... 27
N. Hipotesis ... 29
BAB III METODOLOGI PENELITIAN... 30
METODOLOGI PENELITIAN ... 30
A. Jenis Rancangan Penelitian ... 30
B. Variabel Penelitian dan Definisi Operasional ... 30
C. Bahan ... 32
D. Alat ... 33
E. Tata Cara Penelitian ... 33
1. Ekstrasi Kelopak Bunga Rosella ... 33
2. Karakterisasi fisika-kimia ekstrak kelopak bunga rosella ... 34
3. Penetapan bobot tetap ekstrak kelopak bunga rosella... 34
4. Optimasi multiemulsi A/M/A ... 34
5. Cara pembuatan multiemulsi A/M/A hasil optimasi ... 36
6. Evaluasi sediaan multiemulsi A/M/A ... 37
7. Evaluasi sediaan suspensi liposom ... 38
8. Pembuatan kurva baku ... 39
9. Optimasi Preparasi Multiemulsi A/M/A ... 41
10. Preparasi multiemulsi A/M/A ... 42
11. Preparasi Suspensi Liposom ... 43
F. Analisis Hasil ... 45
BAB IV HASIL DAN PEMBAHASAN ... 47
A. Penetapan Bobot Tetap Ekstrak Kelopak Bunga Rosella ... 48
B. Formulasi Multiemulsi A/M/A ... 49
C. Evaluasi Multiemulsi A/M/A ... 54
D. Evaluasi Suspensi Liposom ... 62
E. Kurva Baku Ekstrak Kelopak Bunga Rosella ... 63
xii
G. Penetapan Laju Disipasi ... 70
H. Penetapan Entrapment efficiency ... 76
BAB V KESIMPULAN DAN SARAN ... 81
A. Kesimpulan ... 81
B. Saran ... 81
DAFTAR PUSTAKA ... 83
LAMPIRAN ... 87
xiii
DAFTAR TABEL
Tabel I. Formula emulsi primer A/M ... 52 Tabel II. Formula multiemulsi A/M/A ... 54 Tabel III. Laju disipasi dan waktu paruh antosianin dalam multiemulsi
A/M/A dan suspensi liposom ... 73 Tabel IV. Hasil t-test laju disipasi antosianin multiemulsi A/M/A dan
suspensi liposom total... 75 Tabel V. Entrapment efficiency antosianin ekstrak kelopak bunga rosella
dalam multiemulsi A/M/A ... 76 Tabel VI. Tabel t-test entrapment efficiency antosianin pada multiemulsi
xiv
DAFTAR GAMBAR
Gambar 1. Kelopak bunga rosella ... 8
Gambar 2. Struktur dasar antosianin ... 10
Gambar 3. Stuktur antosianin pada pH yang berbeda ... 11
Gambar 4. Droplet multiemulsi A/M/A ... 12
Gambar 5. Struktur Tween 80® ... 17
Gambar 6. Struktur Span 80 ... 18
Gambar 7. Struktur setil alkohol ... 19
Gambar 8. Struktur dimethicone ... 20
Gambar 9. Struktur xanthan gum ... 20
Gambar 10. Struktur liposom ... 21
Gambar 11. Spektra derivatif orde ke-nol sampai orde ke-dua ... 25
Gambar 12. Spektra antosianin ekstrak kelopak bunga rosella ... 48
Gambar 13. Penampilan emulsi A/M dan multiemulsi A/M/A... 56
Gambar 14. Pengamatan uji fase emulsi primer dalam minyak dan multiemulsi dalam aquadest ... 57
Gambar 15. Hasil pengamatan mikroskopik emulsi A/M dan multiemulsi A/M/A pada hari pertama dengan perbesaran 40 kali ... 60
Gambar 16. Hasil pengamatan mikroskopik multiemulsi A/M/A kontrol dan multiemulsi A/M/A perlakuan pada hari ke-28 dengan perbesaran 40 kali ... 60
Gambar 17. Hasil pengujian mekanik dengan sentrifugasi ... 61
Gambar 18. Persentase pemisahan pada multiemulsi A/M/A ... 61
Gambar 19. Hasil pengamatan mikroskopik suspensi liposom pada hari pertama dengan perbesaran 40 kali ... 63
Gambar 20. Spektra kurva baku antosianin ektrak kelopak bunga rosella dalam metanol ... 64
Gambar 21. Spektra derivat kurva baku antosianin ekstrak kelopak bunga rosella dalam metanol ... 65
xv
Gambar 23. Kurva baku konsentrasi antosianin ekstrak kelopak bunga rosella dengan pelarut aquadest terhadap tinggi derivat ... 66 Gambar 24. Kurva baku konsentrasi antosianin ekstrak kelopak bunga
rosella:pelarut Triton 10% (1:1) metanol terhadap tinggi derivat ... 66 Gambar 25. Tinggi derivat optimasi lama ultrasonifikasi multiemulsi
A/M/A ekstrak kelopak bunga rosella ... 68 Gambar 26. Hasil optimasi lama sentrifugasi pada multiemulsi A/M/A ... 69 Gambar 27. Hasil sentrifugasi supernatan yang telah ditambahkan metanol ... 70 Gambar 28. Pengaruh lama penyimpanan terhadap antosianin ekstrak
kelopak bunga rosella total pada sediaan multiemulsi A/M/A ... 71 Gambar 29. Pengaruh lama penyimpanan terhadap antosianin kelopak
bunga rosella yang berada di fase luar multiemulsi A/M/A ... 71 Gambar 30. Pengaruh lama penyimpanan terhadap antosainin ekstrak
kelopak bunga rosella total dan berada di fase luar pada suspensi liposom ... 73 Gambar 31. Pengaruh waktu penyimpanan terhadap entrapment efficiency
antosianin ekstrak kelopak bunga rosella dalam sediaan multiemulsi A/M/A kontrol dan perlakuan ... 78 Gambar 32. Pengaruh waktu penyimpanan terhadap entrapment efficiency
xvi
DAFTAR LAMPIRAN
Lampiran 1. Serangkaian alat spektrofotometer UV-Vis ... 88
Lampiran 2. Perhitungan bobot tetap ... 88
Lampiran 3. Hasil optimasi HLB pada emulsi primer ... 88
Lampiran 4. Hasil optimasi kecepatan pencampuran emulsi A/M ... 90
Lampiran 5. Hasil optimasi lama pencampuran emulsi A/M ... 90
Lampiran 6. Hasil optimasi setil alkohol sebagai stiffening agent pada emulsi A/M ... 91
Lampiran 7. Hasil optimasi konsentrasi dimethicone sebagai antifoaming agent pada emulsi A/M ... 91
Lampiran 8. Hasil optimasi ratio fase emulsi A/M dengan fase air multiemulsi A/M/A ... 92
Lampiran 9. Hasil optimasi konsentrasi Tween 80® sebagai emusifier pada multiemulsi A/M/A ... 92
Lampiran 10. Hasil optimasi lama pencampuran pada multiemulsi A/M/A ... 93
Lampiran 11. Hasil pengukuran mikromeritik ... 93
Lampiran 12. Penentuan persentase pemisahan multiemulsi A/M/A ... 96
Lampiran 13. Kurva baku antosianin ekstrak kelopak bunga rosella dengan pelarut metanol ... 96
Lampiran 14. Kurva baku antosianin ekstrak kelopak bunga rosella dengan pelarut aquadest... 97
Lampiran 15. Kurva baku antosianin ekstrak kelopak bunga rosella : Triton X-100 10% (1:1) dengan pelarut metanol ... 98
Lampiran 16. Sampel uji multiemulsi A/M/A kontrol dan multiemulsi A/M/A perlakuan ... 99
Lampiran 17. Sampel uji suspensi liposom ... 100
Lampiran 18. Optimasi volume metanol pada supernatan sediaan multiemulsi A/M/A ekstrak kelopak bunga rosella ... 100
Lampiran 19. Perhitungan laju disipasi antosianin ekstrak kelopak bunga rosella pada multiemulsi A/M/A ... 101
xvii
Lampiran 21. Perhitungan entrapment efficiency antosianin ekstrak kelopak bunga rosella pada multiemulsi A/M/A kontrol ... 103 Lampiran 22. Perhitungan entrapment efficiency antosianin ekstrak kelopak
bunga rosella pada multiemulsi A/M/A perlakuan ... 105 Lampiran 23. Perhitungan entrapment efficiency antosianin ekstrak kelopak
bunga rosella pada suspensi liposom ... 106 Lampiran 24. Perhitungan t-test laju disipasi antosianin ekstrak kelopak
bunga rosella multiemulsi A/M/A kontrol dan multiemulsi A/M/A perlakuan serta multiemulsi A/MA perlakuan dan suspensi liposom ... 107 Lampiran 25. Perhitungan t-test entrapment efficiency antosianin
xviii INTISARI
Sinar UV menimbulkan Reactive Oxygen Species (ROS) yang dapat ditanggulangi dengan antioksidan. Kelopak bunga rosella (Hibiscus sabdarifa L.) mengandung senyawa antioksidan antosianin namun rentan terhadap kerusakan, sehingga perlu diformulasikan dalam sediaan yang dapat menjerap yaitu multiemulsi A/M/A dan suspensi liposom. Penelitian bertujuan untuk memperoleh formula optimum dan kondisi penyimpanan multiemulsi A/M/A, serta mengetahui pengaruh penyimpanan terhadap stabilitas antosianin ekstrak rosella dalam multiemulsi A/M/A dan suspensi liposom yang ditunjukkan dengan laju disipasi dan entrapment efficiency.
Formula optimum diperoleh dengan optimasi formula kemudian diuji sifat dan stabilitas fisiknya. Laju disipasi ditetapkan slope persamaan ln jumlah antosianin ekstrak kelopak bunga rosella total dan fase luar multiemulsi A/M/A dan suspensi liposom. Entrapment efficiency dihitung dengan mengukur persentase selisih antosianin ekstrak kelopak bunga rosella total dan fase luar kedua sediaan dengan menggunakan metode spektrofotometer visibel derivatif. Analsis statistik dilakukan dengan t-test.
Hasil penelitian menunjukkan pada multiemulsi A/M/A diperoleh formula optimum, kondisi penyimpanan optimum yaitu pada suhu rendah -4 C dalam wadah terlindung dari cahaya dengan penambahan gas nitrogen, serta multiemulsi A/M/A dengan kondisi penyimpanan optimum memiliki laju disipasi dan entrapment efficiency antosianin ekstrak kelopak bunga rosella lebih tinggi daripada suspensi liposom.
xix ABSTRACT
UV light could induced production of Reactive Oxygen Spesies (ROS) which can solved by using antioxidant. Roselle (Hibiscus sabdariffa L.) was contained anthocyanin as an antioxidant agent, but this compound was less stable in environmental conditions, so it needs to be formulated in a dosage form that could entrapped and protect it. The aim of this study were to determine optimum formula of multiple emulsion and storage condition, stability of anthocyanin roselle extract in W/O/W multiple emulsion and liposome suspension by evaluating the rate of dissipation and entrapment efficiency.
Optimum formula were obtain by optimize formula then was tested physical charateristic and stability. Rate of dissipation was determine by calculated slope ln amount of anthocianin roselle extract in entrapped and outer phase multi emulsion and liposome suspension. Entrapment efficiency was calculated by separating the total extract and the extract that not entrapped in both of dosage form, then was analyzed by derivative visible spectrophotometry. Statistical analyze was conducted by t-test.
The result showed that optimum multiple emulsion was produced, optimum storage condition are low temperature (-4ºC), in fotoprotective continer with adding nitrogen gas, W/O/W multiple emulsion in optimum storage condition has higher rate of dissipation and entrapment efficeincy than liposome suspension.
1 BAB I PENDAHULUAN
A. Latar Belakang
Indonesia merupakan negara beriklim tropis. Sebagai negara tropis, Indonesia mendapat intensitas sinar matahari lebih besar. Penyinaran sinar matahari dapat memberikan efek positif maupun negatif (Depkes RI, 1985). Secara in vitro dari matahari yang merupakan inisiator pembentukan Reactive Oxygen Species (ROS) pada kulit. Berdasarkan panjang gelombangnya, sinar UV dibedakan atas ultraviolet aging (UVA 320-400 nm), ultraviolet burning (UVB 290-320 nm), dan ultraviolet c (200-290 nm). UVA dapat menyebabkan kerusakan melalui Reactive Oxygen Species (ROS) yang dapat menyebabkan photoaging atau penuaan kulit yang disebabkan sinar matahari (Ardhie, 2011).
aktif ekstrak rosella yang bersifat polar dapat stabil dalam kondisi asam sehingga perlu diformulasikan dalam pembawa yang juga bersifat asam yang sesuai sehingga dapat menjaga kestabilan antosianin. Ekstrak kelopak bunga rosella diformulasikan dalam multiemulsi A/M/A (air dalam minyak dalam air) dan suspensi liposom yang memiliki kemampuan untuk melindungi zat aktif di dalam sistemnya terhadap lingkungan eksternal (Shasi, Satinder, dan Bharat, 2012). Multiemulsi dengan tipe A/M/A dikarenakan antosianin yang bersifat polar.
Multiemulsi dapat digunakan sebagai sediaan yang dapat melindungi senyawa aktif dalam partikel ganda. Multiemulsi merupakan suatu sistem dispersi kompleks cairan yang dikenal dengan „emulsi dalam emulsi‟, di mana droplet suatu dispersi cairan (air dalam minyak atau minyak dalam air) didispersikan ke cairan lainnya (air atau minyak) untuk menghasilkan multiemulsi A/M/A atau M/A/M (Lutz dan Aserin, 2008). Dalam penyimpanan, fenomena yang sering terjadi yaitu koalesensi fase internal emulsi sekunder dan micellar transport yang dapat mengakibatkan zat aktif fase internal keluar ke fase luar. Fenomena tersebut disebabkan karena tekanan osmosis dan tekanan Laplace (Myers, 2006). Jika antosianin yang berada di fase internal keluar ke fase eksternal, maka dapat mengalami kerusakan terutama teroksidasi akibat pengaruh suhu dan oksigen.
stabil disimpan dalam jangka panjang. Fenomena ketidakstabilan liposom, salah satunya yaitu fusi, yaitu penggabungan partikel liposom sehingga menyebabkan perbesaran ukuran dapat menyebabkan ketidakstabilan (Kumar, Kumar, dan Mahadevan, 2011).
1. Perumusan Masalah
a. Bagaimana sifat dan stabilitas fisis formula optimum multiemulsi A/M/A ekstrak kelopak bunga rosella (Hibiscus sabdariffa L.)?
b. Bagaimana kondisi penyimpanan yang optimum untuk multiemulsi A/M/A dalam menjaga stabilitas antosianin pada ekstrak kelopak bunga rosella (Hibiscus sabdariffa L.)?
c. Bagaimana pengaruh kondisi dan lama penyimpanan terhadap stabilitas ekstrak kelopak bunga rosella (Hibiscus sabdariffa L.) dalam multiemulsi A/M/A yang optimum sifat fisis dan kimianya dan suspensi liposom yang ditinjau dari laju disipasi dan entrapment efficiency antosianin ekstrak kelopak bunga rosella?
2. Manfaat Penelitian a. Manfaat teoritis
b. Manfaat praktis
Penelitian ini memberikan informasi tentang waktu dan kondisi penyimpanan yang sesuai untuk sediaan multiemulsi A/M/A dan suspensi liposom ekstrak kelopak bunga rosella.
3. Keaslian Penelitian
Penelitian terkait ekstrak rosella yang pernah dilakukan yaitu: Liposom-Containing Hibiscus sabdariffa Calyx Extract Formulation with Increased Antioxidant Activity, Improved Dermal Penetration and Reduce Dermal Toxicity Testing oleh Pinsuwan, Amnuaikit, Ungphaiboon, dan Ithara, 2010. Penelitian tersebut belum melakukan uji stabilitas ekstrak kelopak bunga rosella dalam sediaan liposom selama penyimpanan sejauh penelusuran pustaka oleh peneliti, belum ada penelitian mengenai pengaruh penyimpanan terhadap stabilitas ekstrak kelopak bunga rosella dalam multiemulsi A/M/A dan suspensi liposom yang ditinjau dari laju disipasi dan entrapment efficiecy.
B. Tujuan
1. Memperoleh formula optimum multiemulsi A/M/A yang mengandung ekstrak kelopak bunga rosella (Hibiscus sabdariffa L.) dengan sifat dan stabilitas fisik yang baik
2. Mengetahui kondisi penyimpanan multiemusi A/M/A optimum yang mengandung ekstrak kelopak bunga rosella (Hibiscus sabdariffa L.)
6 BAB II
PENELAAHAN PUSTAKA
A. Photoaging
Photoaging adalah bentuk utama kerusakan kulit akibat paparan sinar matahari, frekuensi berlebih sering dibandingkan dengan kanker kulit. Paparan UV kronis dapat mengakibatkan penuaan dini kulit yang disebut dengan premature skin aging, ditandai dengan kerutan halus dan kasar oleh kulit, dispigmentasi, warna pucat, perubahan tekstur, kehilangan elastisitas, dan premalignant actinic keratoses. Sebagian besar tanda-tanda klinis disebabkan oleh perubahan dermal (Draelos, 2010).
B. Antioksidan
Antioksidan merupakan suatu inhibitor reaksi radikal bebas. Kerja antioksidan akan bereaksi dengan radikal bebas sehingga akan membentuk radikal bebas baru yang bersifat kurang reaktif dan relatif stabil (Fessenden dan Fessenden, 1986).
Antioksidan dikategorikan menjadi antioksidan enzimatik dan nonenzimatik. Antioksidan enzimatik mencakup superoksida dismutase (SOD), katalase, dan glutation peroksidase. Antioksidan nonenzimatik mencakup vitamin c, vitamin e, glutation, asam urat, dan albumin (Fouad, 2005). Selain digolongkan di atas, antioksidan juga dapat dikategorikan dari perolehannyayaitu dikenal juga antioksidan alami yang biasa terdapat pada buah-buahan, teh, sayuran, dan bir. Terdapat pula antioksidan sintetik misalnya BHA (butylated hydroxyanisole) dan BHT (butylated hydroxytoluene) (Sofia, 2005).
C. Kelopak BungaRosella (Hibiscus sabdariffa L.) 1. Taksonomi
Kingdom : Plantae
Divisi : Magnoliophyta Kelas : Magnoliopsida Bangsa : Malvales Suku : Malvaceae Marga : Hibiscus
2. Deskripsi tanaman rosela
Rosella dapat tumbuh dengan baik di daerah beriklim tropis dan subtropis. Rosella (Hibiscus Sabdariffa L.) merupakan anggota famili Malvaceae. Tanaman ini mempunyai habitat asli di daerah yang terbentang dari India sampai Malaysia. Rosella merupakan herba tahunan yang bisa mencapai ketinggian 0,5-3 meter. Batangnya bulat, tegak, berkayu, dan berwarna merah. Daunnya tunggal, berbentuk bulat telur, pertulangan menjari, ujung tumpul, tepi bergerigi, dan pangkal berlekuk. Panjang daun 6-15 cm dan lebarnya 5-8 cm (Backer dan Brink, 1965).
menyerupai ginjal, berbulu, dengan panjang 5 mm dan lebar 4 mm (Backer dan Brink, 1965).
3. Fitokimia kelopak bunga rosella
Kelopak bunga rosella mengandung flavonoid seperti flavonoid
gosipetin, hibisetin, dan sabdatin. Selain itu juga mengandung alkaloid, β
-sitosterol, antosianin, asam sitrat, sianidin-3-rutinosa, delfinidin, galaktosa, pektin, protocatechuic acid, kuersetin, asam stearik dan lilin (Mahadevan dkk., 2008)
Pigmen warna rosella bertanggung jawab atas warna merah dan sumber utama kapasitas antioksidan. Namun pigmen warna tersebut tidak stabil pada perubahan suhu, lama penyimpanan, dan variasi bunga rosella (Tsai, McIntosh, Pearce, Camden, dan Jordan, 2002).
D. Antosianin
membentuk cincin heterosiklik (cincin C) dengan gugus gula yang terikat pada atom karbon pada posisi C-3 atau A-5 (gambar 2).
Gambar 2. Struktur dasar antosianin (Miguel, 2011)
Antosianin merupakan golongan senyawa yang bersifat polar dan dengan kelarutan yang lebih tinggi dalam metanol daripada etanol dan air (Bridger, Chinn dan Truong, 2010). Kestabilan warna senyawa antosianin dipengaruhi oleh tingkat keasaman, suhu, lama penyimpanan, oksigen dan cahaya. Laju kerusakan (degredasi) antosianin cenderung meningkat selama proses penyimpanan yang diiringi kenaikan suhu. Degredasi termal menyebabkan hilangnya warna pada antosianin. Laju penurunan termal antosianin mengukuti kinetika orde pertama (Hermawan dkk,2010).
Gambar 3. Stuktur antosianin pada pH yang berbeda (Hermawan dkk., 2010)
E. Multiemulsi A/M/A
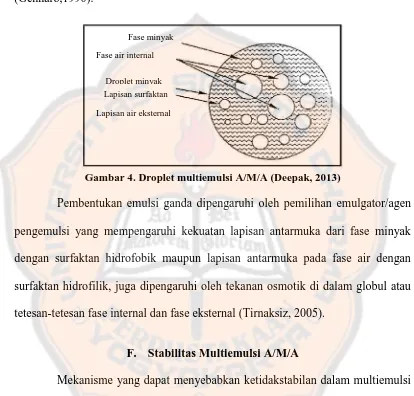
Salah satu inovasi terbaru dalam teknologi emulsi adalah pengembangan emulsi ganda yakni emulsi yang fase terdispersinya mengandung tetesan-tetesan kecil atau globul. Emulsi ganda (gambar 4) terbagi atas dua tipe emulsi yakni emulsi tipe M/A/M artinya emulsi M/A terdispersi pada fase air, dan tipe emulsi A/M/A dengan emulisi A/M terdispersi pada fase air (Gennaro, 1990).
Ukuran droplet multiemulsi lebih besar daripada ukuran partikel emulsi biasa sehingga emulsi ganda kurang stabil secara termodinamika. Pelepasan zat aktif dari fase dalam ke fase luar atau sebaliknya, sering tidak terkendali. Stabilitas serta mekanisme pelepasan multiemulsi saling berhubungan dan memiliki keterkaitan (Lutz dan Aserin, 2008).
Penggunaan multiemulsi memiliki keuntungan yakni menutupi rasa yang tidak enak saat penggunaan, meningkatkan absorbsi obat, memperpanjang pelepasan obat, serta dapat memisahkan dua bahan hidrofilik yang tidak saling
bercampur (incompatible) yakni pada fase air internal dan fase air eksternal yang dipisahkan oleh fase pertengahan minyak pada emulsi ganda tipe A/M/A (Gennaro,1990).
Gambar 4. Droplet multiemulsi A/M/A (Deepak, 2013)
Pembentukan emulsi ganda dipengaruhi oleh pemilihan emulgator/agen pengemulsi yang mempengaruhi kekuatan lapisan antarmuka dari fase minyak dengan surfaktan hidrofobik maupun lapisan antarmuka pada fase air dengan surfaktan hidrofilik, juga dipengaruhi oleh tekanan osmotik di dalam globul atau tetesan-tetesan fase internal dan fase eksternal (Tirnaksiz, 2005).
F. Stabilitas Multiemulsi A/M/A
Mekanisme yang dapat menyebabkan ketidakstabilan dalam multiemulsi yang utama adalah disebabkan oleh reduksi energi bebas sistem melalui penurunan area antarmuka. Surfaktan memiliki peran dalam mereduksi energi antar permukaan melalui proses adsorpsi. Sistem multiemulsi, mekanisme utama yang menyebabkan stabilitas jangka pendek adalah koalesensi droplet pada emulsi primer. Maka dari itu, pemilihan emulsifier berupa surfaktan tunggal atau campuran menjadi penting agar dapat menghasilkan stabilitas optimum untuk
Droplet minyak Lapisan surfaktan
Lapisan air eksternal Fase air internal
sistem tersebut, baik untuk emulsi A/M maupun M/A. Mekanisme lain penyebab ketidakstabilan adalah hilangnya droplet-droplet emulsi fase internal yang disebabkan oleh pecahnya lapisan yang memisahkan droplet-droplet kecil fase internal dari fase eksternal. Perbedaan tekanan osmotik antara fase internal dan eksternal dalam suatu sistem sediaan menyebabkan material yang terkandung pada fase internal berpindah ke fase eksternal (micellar transport). Tekanan tinggi dalam droplet yang lebih kecil dapat menghasilkan energi atas hilangnya material dari droplet tersebut (Myers, 2006).
Efek tekanan osmotik pada stabilitas beberapa emulsi telah diselidiki selama hampir empat dekade. Pada multiemulsi A/M/A komponen fase minyak dapat berfungsi sebagai membran yang memisahkan fase air internal dan eksternal. Ketebalan membran minyak bervariasi dengan perubahan komposisi dan proses multiemulsi. Air dapat melewati membran pada fase minyak dari fase internal ke fase eksternal atau dari fase eksternal ke fase internal bergantung pada tekanan osmosis. Apabila tekanan osmotik fase air internal lebih tinggi dibandingkan dengan fase air eksternal menyebabkan air masuk ke dalam fase air internal, sehingga terjadi pembengkakan droplet fase internal sehingg akhirnya meledak dan melepaskan isinya ke fase eksternal. Apabila tekanan osmotik lebih tinggi di fase air luar dibandingkan fase air internal, air akan keluar dari fase internal ke fase eksternal, menyebabkan penyusutan droplet fase internal dan fase minyak (Jiao dan Burgess, 2008).
akan masuk ke dalam fase internal sehingga menyebabkan droplet internal membengkak hingga pada akhirnya pecah dan fase air internal ke fase eksternal. Transfer air dari fase internal dapat meyebabkan penyusutan tetesan internal yang terjadi jika gradien sebaliknya ada sehingga mempengaruhi destabilitas (Florence and Whitehill, 1985). Tegangan antarmuka pada dua cairan pada antarmuka yang melengkung ketika salah satu cairan tersebar sebagai droplet ke fase cair lain disebut tekanan Laplace. Tekanan Laplace berbanding terbalik dengan jari-jari kelengkungan. Pemberian sejumlah kecil elektrolit dalam fase air internal dapat menangkal efek tekanan Laplace. Tekanan Laplace dalam proses emulsifikasi menyebabkan emulsi menjadi tidakefektif secara termodinamikan. Pembentukan emulsi dengan droplet kecil (tetesan sangat melengkung), dibutuhkan energi yang lebih untuk mengatasi tekanan Laplace yang besar pada droplet. Tekanan Laplace selama penyimpanan terjadi sepanjang permukaan antar droplet. Droplet yang dipengaruhi tekanan Lapalce menjadi berbentuk memanjang dan berbentuk silindris, untuk mengurangi tekanan Laplace dari droplet berbentuk bola, yang menyebabkan ketidakstabilan. Kehadiran elektrolit dengan jumlah yang tidak tepat dapat berdampak negatif terhadap stabilitas multiemulsi. Jumlah elektrolit yang diformulasikan harus cukup tinggi untuk melawan tekanan Laplace namun cukup rendah untuk menghindari efek osmotik (Jiao dan Burgess, 2008).
kekentalan atau pemadatan antar fase (Blinks dan Rocher, 2009). Dalam konteks aplikasi obat seperti pelepasan obat terkontol, yang mana mekanisme penghantarannya adalah difusi terkontrol, mekanisme ketidakstabilan dapat merugikan terhadap aksi dari sistem, karena dapat menyebabkan pelepasan yang cepat dari zat aktif dengan kemungkinan efek yang berbahaya. Mekanisme ketidakstabilan emulsi harus dimengerti dan dikontrol dalam sistem multiemulsi. Dalam semua kasus, stabilitas akhir sistem sangat bergantung pada sifat dari fase minyak dan air, karakteristik dari emulsifier primer dan sekunder dalam sistem, serta hubungan antara fase internal dan eksternal (Myers, 2006).
G. Bahan- Bahan Tambahan dalam Multiemulsi A/M/A 1. Surfaktan (emulsifying agent)
Surfaktan adalah rantai asam lemak pendek yang bersifat amfifilik atau amfifatik, yang memiliki bagian dengan afinitas polar dan nonpolar. Surfaktan merupakan molekul yang dapat berorientasi dengan menurunkan tegangan permukaan pada media dispersi. Sifat hidrofilik terdapat pada bagian kelompok kepala dan lipofilik terdapat pada rantai (atau ekor) pada molekul surfaktan (Schramm, 2000).
Menurut ionisasi dalam air, surfaktan di klasifikasikan menjadi:
b. Surfaktan nonionik. Surfaktan nonionik merupakan surfaktan yang tidak mengalami ionisasi pada larutan air, karena gugus hidrofobik merupakan tipe dissociable, seperti alkohol, fenol, eter, ester, atau amida. Surfaktan nonionik terbentuk dari hidrofobik yang terdiri dari rantai polietilen glikol. Surfaktan nonionik merupakan detergen, wetting agent dan emulsifier yang baik.
c. Surfaktan kationik. Surfaktan kationik merupakan surfaktan yang terionisasi dalam air menjadi kation yang umumnya berupa halogen dan anion.
(Salager, 2002). Surfaktan memiliki rentang dari komponen larut minyak untuk menstabilkan emulsi A/M hingga material larut air yang memberikan produk M/A. Surfaktan biasa digunakan dalam kombinasi surfaktan larut air dan larut minyak untuk mengurangi tegangan antarmuka pada lapisan antarmuka yang penting dalam stabilitas emulsi yang optimum. Surfaktan nonionik memiliki toksisitas dan iritasi yang rendah (Billany, 2002).
emulsi. Cara menstabilkan emulsi adalah dengan adanya gugus polar dari surfaktan yang terhidrasi dan bulky, yang menyebabkan halangan sterik antar droplet dan mencegah koalesen (Kim, 2005).
Surfaktan nonionik merupakan emulgator yang memiliki kesetimbangan hidrofilik-lipofilik yang seimbang di dalam molekulnya. Tidak seperti emulgator anionik dan kationik, emulgator nonionik tidak mudah di-pengaruhi oleh perubahan pH dan adanya elektrolit (Gennaro, 1990).
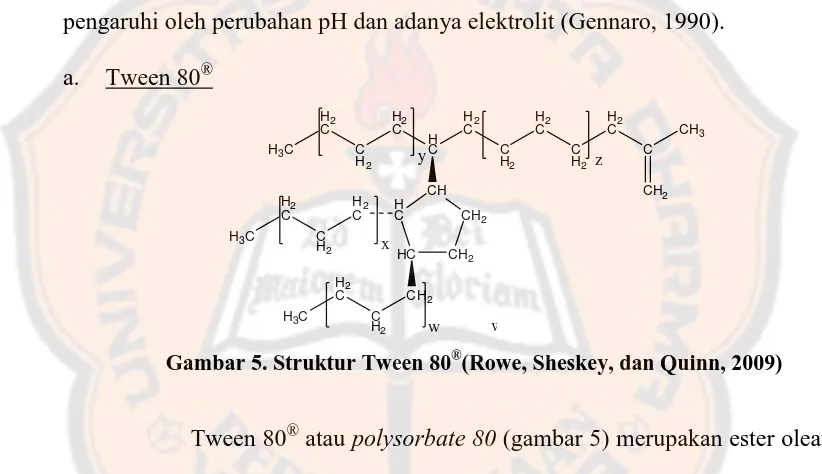
a. Tween 80®
Gambar 5. Struktur Tween 80®(Rowe, Sheskey, dan Quinn, 2009)
dalam air dan etanol (95%), namun tidak larut dalam mineral oil dan vegetable oil (Rowe dkk., 2009).
b. Span 80®
Span 80® (gambar 6) mempunyai nama lain sorbitan monooleat dengan nilai HLB 4,3. Pemeriannya berupa warna kuning gading, cairan seperti minyak kental, bau khas tajam, terasa lunak. Kelarutannya tidak larut tetapi terdispersi dalam air, bercampur dengan alkohol, tidak larut dalam propilen glikol, larut dalam hampir semua minyak mineral dan nabati, dan sedikit larut dalam eter (Rowe dkk.., 2009).
HC
Gambar 6. Struktur Span 80 (Rowe dkk., 2009)
2. Parafin cair
Dalam formulasi topikal parafin cair umumnya digunakan untuk
formulasi krim dan salep karena tidak menyebabkan iritasi kulit. Parafin cair
berbentuk berupa cairan kental bening tidak berwarna. Konsentrasi parafin cair
yang digunakan dalam sediaan topikal adalah 1,0 - 32,0% (Rowe dkk., 2009).
3. Setil alkohol
Setil alkohol (gambar 7) dengan nama lain alcohol cetylicus. Setil alkohol berupa butiran putih, tidak larut air yang secara luas digunakan dalam formulasi kosmetik dan farmasetis seperti supositoria, modifield-realease solid dosage form, emulsi, lotion, krim, dan salep. Aplikasi setil alcohol bidang farmasetis berfungsi sebagai coating agent, emulsifer, stiffening agent dan meningkatkan konsistensi pada emulsi A/M. Setil alkohol memiliki titik lebur
45–52 C dan stabil terhadap keberadaan asam, basa, cahaya dan pada udara
tidak mengumpal. Konsentrasi setil alkohol sebagai stiffening agent adalah 2-10% (Rowe dkk., 2009).
Gambar 7. Struktur setil alkohol (Rowe dkk., 2009)
4. Dimethicone
dimethicone dalam sediaan krim, lotion, dan ointment adalah 10%-30% (Rowe dkk., 2009).
Gambar 8. Struktur dimethicone (Rowe dkk., 2009)
5. Xanthan gum
Gambar 9. Struktur xanthan gum (Rowe dkk., 2009)
Xanthan gum (gambar 9) merupakan golongan gum polisakarida yang
memiliki molekul besar. Xanthan gum memiliki warna krem keputih-putihan,
tidak berbau, mudah mengalir, dan berbentuk berupa serbuk halus. Xanthan gum
sedikit larut dalam etanol dan eter, dan larut dalam air dingin dan panas. Xanthan
dan agen peningkat viskositas karena berbentuk hidrokoloid. Xanthan gum dapat
memberikan peningkatan viskositas atau pengental, penstabil dalam
penyimpanan jangka panjang dengan temperatur tinggi (Rowe dkk., 2009).
6. Aquadest
Aquadest merupakan air yang telah mengalami proses destilasi. Aquadest, digunakan secara luas sebagai bahan baku, dan bahan pelarut selama proses produksi dan formulasi produk farmasetis, bahan aktif farmasi (API) dan intermediet, dan reagen analitis (Rowe dkk., 2009).
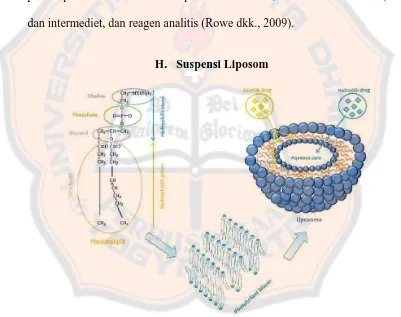
H. Suspensi Liposom
Gambar 10. Struktur liposom (Laouini, Jaafar-Maalej, Blouza, Sfar, Charcosset, dan Fessi, 2012).
uang memiliki kelarutan berbeda dan secara spontan membentuk lapisan tunggal atau ganda, yang kemudian membentuk vesikel tertutup dengan adanya larutan air. Kemampuan liposom dalam menjerap dan mempertahankan obat secara luas serta fleksibilitas struktur adalah elemen utama untuk mengontrol aksi obat (Krowczynski, 1987). Liposom terbentuk ketika lipid yang terdiri dari kepala yang bersifat hidrofilik dan ekor yang bersifat hidrofilik didispersikan ke dalam air, dan membentuk lapisan tipis berupa lipid bimolekuler. Selama agregasi, lapisan lipid bimolekuler tipis terhidrasi akan terpisah kemudian masing-masing lapisan tersebut akan bergabung membentuk vesikel yang dapat mencegah interaksi lapisan lipid hidrokarbon dengan air sekitarnya (Laouini dkk., 2012).
berukuran 20–100 nm, Large Unilamellar Vesicles (LUV) berukuran >100 nm, dan Giant Unilamellar Vesicles (GUV) berukuran >1000 nm. Lamellar Vesicles (LV) terdiri dari lebih dari 1 lapis bilayer yang diklasifikasikan berdasarkan ukuran yaitu Oligolamellar Vesicles (OLV) berukuran 100 – 500 nm dan Multilamellar Vesicles (MLV) berukuran >500 nm (Laouini dkk., 2012).
I. Stabilitas suspensi liposom
Liposom dapat menjadi sediaan yang stabil disimpan dalam jangka panjang (Kumar dkk., 2011). Berdasarkan pemilihan dan konsentrasi dari zat aktif, vesikel liposom dapat menjadi stabil atau tidak stabil. Masalah stabilitas liposom diketahui berasal dari vesikel unilamelar karena dapat berfusi dengan vesikel lain membentuk vesikel unilamelar dengan ukuran besar atau Large Unilamelar Vesicle (LUV) (Meier dan Schreiber, 2005).
Parameter yang harus dipertimbangkan untuk menstabilkan sistem liposom dalam suatu formulasi, yaitu:
1. Membuat liposom dengan lipid murni karena lipid yang tidak murni (teroksidasi/terhidrolisis atau lipid yang tersuspensi pada minyak/trigliserida) akan mendestabilisasi liposom.
2. Hindari penggunaan surfaktan ionik dalam fase di mana liposom akan ditambahkan.
4. pH produk dipertahankan mendekati pH netral karena kecepatan hidrolisis terendah pada pH 6,5.
5. Produk yang mengandung liposom idealnya disimpan dalam suhu lemari pendingin. Namun, jika produk akhir dibuat dengan viskositas tertentu menggunakan gum atau pengental yang netral maka produk tersebut dapat disimpan pada suhu ruangan.
6. Wadah produk yang mengandung liposom berupa wadah dengan bahan opaque untuk menghindari/mengurangi kerusakan oleh cahaya pada liposom.
(Kulkami, 2005).
J. Spektrofotometer Visibel Metode Derivatif
Prinsip spektrofotometri adalah radiasi pada panjang gelombang 400-800 nm yang melalui larutan yang mengandung molekul tertentu akan menyebabkan elektron pada ikatan antar molekul tereksitasi. Eksitasi menyebabkan molekul memiliki bilangan kuantum yang lebih tinggi dan mengabsorbsi energi yang melewati larutan (Watson, 1999).
Kekurangan utama dari spektrofotometri UV-Vis adalah kurangnya selektifitas. Pengukuran absorbansi sering kali merupakan pengakumulasian dari interfensi yang berasal dari komponen sampel yang lain seperti matriks (reagen atau senyawa lain). Salah satu metode yang paling sederhana untuk meningkatkan selektifitas yang dapat mengatasi overlapping secara kuantitatif adalah dengan derivatisasi spektra (Karpinska, 2010).
Metode spektrofotometri derivatif atau metode kurva turunan adalah salah satu metode spektrofotometri yang dapat digunakan untuk analisis campuran beberapa zat secara langsung tanpa harus melakukan pemisahan terlebih dahulu walaupun dengan panjang gelombang yang berdekatan (Nurhidayati, 2007).
Gambar 11. Spektra derivatif orde ke-nol sampai orde ke-dua (Nurhidayati, 2007)
K. Laju Disipasi
suhu. Laju disipasi sebenarnya membentuk laju pseudoplastik (NAFTA, 2006). Antosianin ekstrak kelopak bunga rosella mengikuti reaksi orde pertama (Hermawan dkk., 2010). Integrasi persamaan laju disipasi dapat menggunakan ln dan logaritma. Laju disipasi menghubungkan berkurangnya konsentrasi dengan waktu (Martin dkk., 1993).
Waktu paruh merupakan waktu yang dibutuhkan agar suatu substansi terdegradasi atau terdisipasi yang dideskripsikan dengan kinetika orde pertama dan diikuti dengan konsep eksponensial yang bergantung pada konsentrasi dan waktu. Waktu paruh (t1/2) yang berhubungan dengan degredasi dan disipasi (k) dihitung menggunakan rumus berikut:
t1/2 = ...(2)
(NAFTA, 2006)
L. Entrapment efficiency
Entrapment adalah proses penjerapan zat aktif ke dalam cangkang atau matriks berupa padat atau cait yang bertujuan untuk melindungi zat aktif, mengendalikan pelepasan dan imobilisasi. Entrapment efficiency didefinisikan sebagai persentase zat aktif dalam mikrokapsulasi dari total jumlah zat aktif yang ditambahkan selama proses penjerapan. Entrapment efficiency merupakan parameter penting pada sediaan vesikel (Vladisavljević dan Holdich, 2012).
selanjutnya rendah, kelarutan polimer dalam pelarut nonorganik rendah, dan kelarutan pelarut organik terhadap air rendah (Dhakar, 2010).
M. Landasan Teori
Indonesia merupakan negara tropis sehingga mendapatkan intensitas sinar matahari yang lebih besar. Kulit merupakan organ tubuh yang secara langsung terpejan langsung sinar ultraviolet (UV) dari matahari. Kulit secara berkesinambungan terpapar oxidative stress menyebabkan terbentuknya ROS (Reactive Oxygen Species) dan pada akhirnya menyebabkan kerusakan kulit. Antioksidan diperlukan untuk menanggulangi ROS.
Rosella merupakan salah satu tanaman yang dapat berfungsi sebagai antioksidan. Salah satu antioksidan yang banyak terkandung dalam kelopak bunga rosella adalah antosianin. Kestabilan warna senyawa antosianin yang mngindikasikan kestabilan ekstrak kelopak bunga rosella dipengaruhi oleh tingkat keasaman, suhu, lama penyimpanan, oksigen dan cahaya (Hermawan dkk., 2010). Rosella perlu diformulasikan ke dalam sediaan yang dapat melindungi dari pengaruh lingkungan seperti multiemulsi A/M/A dan suspensi liposom. Multiemulsi A/M/A dapat melindungi ekstrak kelopak bunga rosella dengan membentuk droplet pelindung berupa fase minyak, sedangkan liposom berupa vesikel yang terdiri fosfolipid. Evaluasi stabilitas ekstrak kelopak bunga rosella dievaluasi dari laju disipasi dan entrapment efficiency.
ketidakstabilan sediaan emulsi dan kerusakan antosianin ekstrak kelopak bunga rosella. Suhu yang tinggi memicu ketidakstabilan multiemulsi A/M/A karena meningkatkan energi kinetik dan tekanan osmotik. Energi kinetik dan tekanan osmotik yang memicu fenomena ketidakstabilan seperti koalesensi dan micellar transport yang dapat mengakibatkan ekstrak rosella keluar dari droplet minyak dan berada di fase luar dan mengalami kerusakan. Suhu rendah meningkatkan kekentalan sediaan sehingga memperlambat terjadinya fenomena ketidakstabilan. Suhu tinggi dan keberadaan oksidator dapat mengoksidasi antosianin yang bersifat antioksidan dalam ekstrak kelopak bunga rosella. Keberadaaan oksidator seperti oksigen dapat dikurangi dengan pemberian gas nitrogen. Kondisi penyimpanan suspensi liposom telah dioptimasi oleh Juniarka (2010) yaitu dengan penyimpanan suhu 4ºC dengan pemberian dengan nitrogen.
Multiemulsi A/M/A merupakan sediaan yang secara termodinamika tidak stabil. Formulasi multiemulsi A/M/A optimum diperlukan untuk memberikan stabilitas antosianin ekstrak kelopak bunga rosella yang lebih lama dan entrapment efficiency yang optimum dan stabil, sehingga diperlukan optimasi formula dan cara pembuatan multiemulsi A/M/A. Liposom dapat menjadi sediaan yang dapat stabil disimpan dalam jangka panjang. Fenomena ketidakstabilan liposom umumnya berupa agregasi dan fusi.
efficiency suspensi liposom ekstrak kelopak bunga adalah 65±9,4% dengan ukuran partikel 0,673±0,084 µm. Multiemulsi A/M/A yang memiliki diameter internal dan entrapment efficiency lebih besar memungkinkan menjerap ekstrak rosella lebih tinggi. Penjerapan yang lebih tinggi yang ditunjukkan dengan entrapment efficiency meningkatkan perlindungan terhadap ekstrak kelopak bunga rosella dari kerusakan akibat pengaruh lingkungan.
N. Hipotesis
1. Multiemulsi A/M/A mempunyai sifat fisik yaitu pH sesuai pH kulit dan memiliki kemampuan menjerap ekstrak kelopak bunga rosella serta stabilitas fisis yang baik ditunjukan dengan memiliki dengan persentase pemisahan yan kecil.
2. Stabilitas ekstrak kelopak bunga rosella (Hibiscus sabdariffa L.) dengan kondisi penyimpanan pada suhu rendah dan dengan pemberian gas nitrogen lebih baik daripada multiemulsi A/M/A pada kondisi penyimpanan pada suhu ruangan tanpa pemberian gas nitrogen yang ditinjau dari laju disipasi yang lebih kecil dan entrapment efficiency lebih besar.
30 BAB III
METODOLOGI PENELITIAN
A. Jenis Rancangan Penelitian
Jenis rancangan penelitian ini adalah eksperimental murni yaitu untuk mendapatkan formula multiemulsi A/M/A yang optimum, mengetahui kondisi penyimpanan optimum pada multiemulsi A/M/A serta mengetahui stabilitas ekstrak kelopak bunga rosella (Hibiscus sabdariffa L.) dalam multiemulsi air dalam minyak dalam air (A/M/A) dan dalam suspensi liposom dengan menggunakan metode spektrofotometri visibel selama penyimpanan.
B. Variabel Penelitian dan Definisi Operasional 1. Variabel utama
a. Variabel bebas. Variabel bebas pada penelitian ini adalah konsentrasi bahan dan HLB pada multiemulsi A/M/A dan konsentrasi bahan-bahan pada suspensi liposom serta waktu penyimpanan
b. Variabel tergantung. Variabel tergantung pada penelitian ini adalah sifat fisis, stabilitas fisis, laju disipasi, entrapment efficiency antosianin pada ekstrak kelopak bunga rosella dalam multiemulsi A/M/A dan suspensi liposom
2. Variabel pengacau
b. Variabel pengacau tak terkendali. Variabel pengacau tak terkendali pada penelitian ini adalah ukuran droplet multiemulsi A/M/A dan suspensi liposom, udara, tekanan osmotik, serta kelembaban selama pembuatan dan penyimpanan.
3. Definisi operasional
a. Ekstrak kelopak bunga rosella adalah sediaan kental hasil ekstraksi 5 kg kelopak bunga rosella segar dengan menggunakan metode maserasi
menggunakan pelarut metanol dan kemudian disimpan pada suhu -4C
dengan pemberian gas nitrogen dan wadah tertutup rapat yang telah dilapisi aluminium foil.
b. Antosianin adalah senyawa golongan flavonoid yang memilliki pigment warna kuat pada ekstrak kelopak bunga rosella dan memiliki panjang gelombang 490-550 nm, yang memberikan efek sebagai antioksidan. c. Surfaktan adalah emulsifier berupa Tween 80® dan Span 80® pada emulsi
A/M dan Tween 80® pada pembuatan multiemulsi A/M/A, yang berfungsi mengurangi tegangan antarmuka fase internal dan fase eksternal.
d. Multiemulsi A/M/A kontrol adalah multiemulsi A/M/A yang disimpan pada suhu ruangan (27ºC) dengan wadah tidak tembus cahaya tanpa penggunaan gas nitrogen.
f. Lama penyimpanan adalah rentang waktu pengujian yaitu pada multiemulsi A/M/A selama 1,3,7,14 dan 28 hari sedangkan suspensi liposom 1 dan 14 hari.
g. Suspensi liposom adalah sediaan cair yang mengandung 500 µL ekstrak kelopak bunga rosella yang terjerap oleh fosfolipid berupa lesitin dan dispersikan ke dalam medium dispersi aquadest.
h. Spektofotometri visibel derivat adalah spektra yang telah diderivatisasi kedua dan delta lambda 40 nm, kemudian diukur tinggi derivat dengan menggunakan penggaris rotring Ziegel.
i. Entrapment efficiency adalah persentase ekstrak kelopak bunga rosella yang terjerap dalam sediaan multiemulsi A/M/A dan dalam suspensi liposom yang diperoleh dengan menggunakan metode spektrofotometri visibel derivatisasi.
j. Laju disipasi adalah laju kehilangan ekstrak rosella yang ditunjukkan dengan derajat kemiringan atau slope pada persamaan antosianin ekstrak kelopak bunga rosella total dan yang berada di fase luar dalam sediaan multiemulsi A/M/A dan dalam suspensi liposom.
C. Bahan
diperoleh dari Sanjayadi, aquadest, metanol (kualitas pro analisis, Merck), Triton X-100 (kualitas pro analisis, Merck), dan gas nitrogen teknis yang diperoleh dari CV. Perkasa Yogyakarta.
D. Alat
Alat yang digunakan dalam penelitian ini adalah mixer (Miyako), waterbath (Elbanton), labu takar (Pyrex®), beaker (Pyrex®), cawan porselin, termometer, tabung sentrifuge, sentrifuge (Top Sentrifuge model PLC-03), mikroskop (Olympus), timbangan analitik digital (Mettler Toledo), batang pengaduk, cawan porselin, sonikasi (Retsch), pH indikator universal, seperangkat alat spektrofotometer UV-Vis Shimadsu UV-1800 (lampiran A), mikropipet (Secorex), flakon, parafilm, aluminium foil, dan penggaris (Rotring Ziegel Germany).
E. Tata Cara Penelitian 1. Ekstrasi Kelopak Bunga Rosella
2. Karakterisasi fisika-kimia ekstrak kelopak bunga rosella
Ekstrak yang diperoleh dari Sanjayadi dilakukan karakterisasi secara organoleptis, pengukuran pH, dan kandungan kimia dengan menggunakan spektrofotometer visibel.
3. Penetapan bobot tetap ekstrak kelopak bunga rosella
Sebanyak 500 µ L ekstrak metanol rosella diuapkan dalam cawan porselin kering yang telah ditimbang dengan menggunakan waterbath pada suhu 40-50ºC kemudian ditimbang kembali hingga memperoleh bobot dua kali berturut tidak lebih dari 0,5 mg tiap gram sisa yang ditimbang (Depkes RI, 1975).
4. Optimasi multiemulsi A/M/A
a. Optimasi HLB emulsi primer A/M
Emulsi primer dibuat dengan menggunakan komposisi Span 80® dan Tween 80® dengan HLB 5; 5,3; 5,5; dan 5,8. HLB optimal dipilih berdasarkan persentase pemisahan dari 25 ml emulsi A/M selama 24 jam penyimpanan.
b. Optimasi kecepatan pencampuran emulsi A/M
Pembuatan emulsi A/M dilakukan dengan pembuatan emulsi A/M dengan kecepatan mixer 4 dan 5. Kecepatan optimal dipilih berdasarkan persentase pemisahan dari 25 mL selama 24 jam penyimpanan.
c. Optimasi setil alkohol sebagai stiffening agent
optimal dipilih dengan melihat persentase pemisahan dari 25 mL emulsi A/M selama 24 jam.
d. Optimasi dimethicone sebagai antifoaming agent
Konsentrasi dimethicone yang dioptimasi adalah 2; 4; 6; dan 8%. Konsentrasi dimethicone optimal dipilih dengan melihat kestabilan dari persentase pemisahan dari 25 mL emulsi A/M selama 24 jam.
e. Optimasi rasio fase emulsi primer A/M dalam multiemulsi A/M/A
Emulsi primer A/M yang ditambahkan dalam multiemulsi A/M/A dioptimasi sejumlah 27,8; 37,8; dan 47,8 g. Jumlah optimal emulsi primer A/M yan dimasukkan dalam multiemulsi A/M/A dipilih berdasarkan persentase pemisahan minimal dari 25 mL yang dihasilkan setelah penyimpanan 24 jam.
f. Optimasi konsentrasi Tween 80® dalam multiemulsi A/M/A
Surfaktan pada multiemulsi A/M/A berupa Tween 80® dioptimasi dengan konsentrasi 2; 4; dan 6%. Konsentrasi surfaktan optimal dipilih berdasarkan persentase pemisahan dari 25 mL multiemulsi A/M/A selama penyimpanan 24 jam.
g. Optimasi lama pencampuran multiemulsi A/M/A
5. Cara pembuatan multiemulsi A/M/A hasil optimasi a. Pembuatan emulsi primer A/M
Ekstrak kental metanol Rosella yang telah diuapkan, Tween 80®, dan MgSO4 dilarutkan dalam aquadest internal. Span 80®, setil alkohol, dan dimethicone dilarutkan dalam parafin cair yang merupakan fase minyak. Kedua fase tersebut dipanaskan hingga suhu 50º±3C, fase air kemudian ditambahkan sedikit demi sedikit ke dalam fase minyak, diaduk selama 10 menit dengan menggunakan mixer dengan dialiri gas nitrogen. b. Pembuatan multiemulsi A/M/A
Tween 80® dan xanthan gum dilarutkan dalam aquadest sekunder hingga homogen sebagai fase air eksternal. Emulsi primer (A/M) dan fase air yang telah tercampur masing-masing dipanaskan hingga 50ºC. Emulsi primer ditambahkan sedikit demi sedikit dalam fase air yang telah mengandung Tween 80® dan xanthan gum sambil dicampur dengan menggunakan mixer selama 10 menit dengan dialiri gas nitrogen.
6. Evaluasi sediaan multiemulsi A/M/A a. Pengamatan organoleptis
Multiemulsi A/M/A kontrol dan perlakuan diamati bau, warna, dan homogenitas pada hari ke 1, 3, 7, 14 dan 28 setelah pembuatan. b. Penetapan pH
Sejumlah multiemulsi A/M/A dioleskan pada kertas indikator pH universal dan dibandingkan dengan warnanya dengan standar (Direktrorat Jenderal Pengawasan Obat dan Makanan, 1975).
c. Penentuan tipe emulsi
Pengujian fase dilakukan dengan memasukkan sejumlah emulsi primer A/M dan multiemulsi A/M/A ke dalam air dan minyak. Tipe A/M ditunjukkan apabila secara visual emulsi primer atau multiemulsi A/M/A larut dalam fase minyak dan tidak larut dalam fase air. Sedangkan tipe M/A ditunjukkan apabila emulsi primer atau multiemulsi A/M/A larut dalam air dan tidak larut dalam minyak (Billany, 2001). Air yang digunakan berupa aquadest dan fase minyak berupa parafin cair.
d. Pengukuran mikromeritik
menggunakan mikroskop dengan perbesaran 400 kali yang terhubung dengan software OptiLab, ukuran partikel diperoleh dengan mengukur diameter partikel menggunakan sofware ImageJ.
e. Uji mekanik
Sediaan multiemulsi A/M/A dimasukkan kedalam tabung sentrifugasi, kemudian disentrifugasi pada kecepatan 5000 rpm selama 20 menit. Hasil sentrifugasi diamati dengan melihat ada atau tidaknya pemisahan fase dari 25 mL multiemulsi A/M/A (Mahmmod, Akhtar, dan Manickam, 2014).
f. Uji persentase creaming
Multiemulsi A/M/A dengan kondisi penyimpanan kontrol dan perlakuan ditempatkan tabung reaksi berskala kemudian diamati secara berkala selama rentang waktu pengujian apabila terjadi perubahan tinggi akibat pemisahan. Multiemulsi A/M/A kontrol disimpan pada suhu 27ºC tanpa pemberian gas nitrogen dan multiemulsi A/M/A perlakuan disimpan pada suhu -4ºC dengan penambahan gas nitrogen. Tabung reaksi berskala 25 mL ditempatkan dalam wadah tertutup rapat dan terlindung dari cahaya (Billany, 2001).
7. Evaluasi sediaan suspensi liposom
a. Pengamatan organoleptis
Suspensi liposom diamati bau, warna, dan homogenitas pada hari ke-1 dan 14 setelah pembuatan.
b. Penetapan pH
Sejumlah suspensi liposom dioleskan pada kertas indikator pH universal dan dibandingkan dengan warnanya dengan standar (Direktrorat Jenderal Pengawasan Obat dan Makanan, 1975).
c. Pengukuran mikromeritik
Sampel suspensi liposom pada hari pertama dioleskan pada preparat cekung, lalu diletakan pada meja objek mikroskop cahaya yang dilengkapi dengan lensa okuler mikrometer yang telah terkalibrasi dan seperangkat kamera (Martin dkk., 1993). Ukuran droplet suspensi liposom diamati dengan menggunakan mikroskop dengan perbesaran 400 kali yang terhubung dengan software OptiLab, ukuran partikel diperoleh dengan mengukur diameter partikel menggunakan sofware ImageJ.
8. Pembuatan kurva baku
a. Kurva baku ekstrak kelopak bunga rosella dengan pelarut metanol
dilarutkan dengan metanol pro analisis ke dalam labu takar 10 mL, lalu di encerkan hingga batas tanda.
b. Kurva baku ekstrak kelopak bunga rosella dengan pelarut aquadest
Pembuatan kurva baku dilakukan dengan membuat larutan stok kemudian diencerkan dan diukur. Larutan stok diambil dari 100 µ L ekstrak kental rosella dilarutkan dalam aquadest dan encerkan dalam labu takar 10 mL hingga batas tanda. Larutan stok diambil sejumlah 0,08 ; 0,09; 0,1; 0,2; 0,3; 0,4; 0,5; 0,6; 0,7; 0,8; 0,9; dan 1 mL, larutan kemudian dilarutkan dengan aquadest dalam labu takar 5 mL, dan diencerkan hingga batas tanda
c. Kurva baku ekstrak kelopak bunga rosella : Triton X-100 10% (1:1) dengan pelarut metanol
9. Optimasi Preparasi Multiemulsi A/M/A
a. Optimasi lama ultrasonifikasi multiemulsi A/M/A ekstrak kelopak bunga rosella
Sebanyak 8,5 g multiemulsi AM/A dilakukan ultrasonifikasi selama 0; 15; dan 30 menit. Bagian supernatan diambil dan ditambahkan metanol pro analisis 5 mL dan disentrifugasi selama 20 menit. Hasil tinggi spektra derivat optimum yang dihasilkan kemudian digunakan sebagai lama ultrasonifikasi pada multiemulsi A/M/A untuk memperoleh ekstrak kelopak bunga rosella dalam total sediaan dan hasil minimun digunakan untuk memperoleh ekstrak kelopak bunga rosella yang berada pada fase luar multiemulsi A/M/A.
b. Optimasi lama sentrifugasi sediaan multiemulsi A/M/A
Sebanyak 8,5 g multiemulsi A/M/A di ultrasonifikasi selama 30 menit. Multiemulsi A/M/A tersebut selanjutnya sentrifugasi selama 0; 20; dan 40 menit dengan kecepatan 5000 rpm. Lama sentrifugasi optimum ditentukan dari volume supernatan multiemulsi A/M/A optimum.
c. Optimasi volume metanol pada supernatan sediaan multiemulsi A/M/A ekstrak kelopak bunga rosella
d. Optimasi lama sentrifugasi supernatan yang telah ditambahkan metanol Bagian supernatan yang telah ditambahkan metanol dan di vortex, selanjutnya di sentrifugasi selama 10 dan 20 menit dengan kecepatan 5000 rpm. Lama sentrifugasi optimum ditentukan dari volume optimum supernatan yang telah jernih.
10. Preparasi multiemulsi A/M/A
a. Preparasi sampel penetapan laju disipasi dan entrapment efficiency multiemulsi A/M/A
b. Penetapan laju disipasi pada multiemulsi A/M/A
Laju disipasi ditetapkan dengan slope (b) persamaan y = bx+a fungsi ln dari jumlah antosianin ekstrak kelopak bunga rosella total dan berada pada fase luar multiemulsi A/M/A ada rentang pengujian yaitu 1, 3, 7, 14 dan 28 hari. Penetapan laju disipasi dilakukan pada multiemulsi dengan kondisi penyimpanan kontrol dan perlakuan.
c. Penetapan entrapment efficiency multiemulsi A/M/A
Entrapment efficiency diukur dengan menghitung selisih jumlah antosianin total ekstrak kelopak bunga rosella (dengan ultrasonifikasi) dengan jumlah antosianin ekstrak kelopak bunga rosella yang berada pada fase luar dari jumlah antosianin total multiemulsi A/M/A.
Selain itu, dilakukan pengukuran entrapment efficeiency pada multiemulsi A/M/A yang dilakukan pada penyimpanan perlakuan dan kontrol dengan waktu hari ke 1,3, 7, 14, dan 28.
11. Preparasi Suspensi Liposom
a. Preparasi sampel penetapan laju disipasi dan entrapment efficiency suspensi liposom
tambahkan dalam labu takar 5 mL dengan metanol pro analisis. Jumlah antosianin ekstrak kelopak bunga rosella suspensi liposom yang berada pada fase luar suspensi liposom diperoleh dari 500 µ L suspensi liposom ditambahkan aquadest sebanyak 500 µL dan ditambahkan labu takar 5 mL dengan aquadest.
b. Penetapan laju disipasi pada suspensi liposom
Laju disipasi ditetapkan dengan slope (b) persamaan y = bx+a fungsi ln dari jumlah antosianin ekstrak kelopak bunga rosella total dan berada pada fase luar suspensi liposom pada hari ke-1 dan 14. Laju disipasi diukur dengan membandingkan kandungan total ekstrak kelopak bunga rosella dalam suspensi liposom total dengan kandungan ekstrak kelopak bunga rosella yang berada di fase luar suspensi liposom pada hari pertama dan hari ke-14 pada penyimpanan suhu rendah (4ºC) dengan penambahan gas nitrogen (Juniarka, 2012).
c. Penetapan entrapment efficiency suspensi liposom
F. Analisis Hasil Analisis hasil pada penelitian ini yaitu: 1. Kurva baku
Kurva baku diperoleh dari hubungan konsentrasi ekstrak kelopak bunga rosella dengan tinggi spektra derivat dan diperoleh nilai linieritas (r), slope (b) dan intersep (a) selanjutnya digunakan untuk membuat persamaan kurva baku y = bx+a.
2. Penetapan laju disipasi dan entrapment efficiency ekstrak kelopak bunga rosella dalam multiemulsi A/M/A dan suspensi liposom
Spektra hasil analisis menggunakan spektrofotometri visibel dilakukan derivatisasi kedua dengan delta lambda 40 nm. Jumlah antosianin ekstrak kelopak bunga rosella total dalam multiemulsi A/M/A dan suspensi liposom diperoleh dengan:
a. Plot nilai tinggi derivat ekstrak kelopak bunga rosella total dalam multiemulsi A/M/A pada persamaan kurva baku ekstrak kelopak bunga rosella dalam metanol
b. Plot nilai tinggi derivat ekstrak kelopak bunga rosella total dalam suspensi liposom pada persamaan kurva baku ekstrak kelopak bunga rosella : TritonX-100 10% (1:1) dalam metanol.
Laju disipasi multiemulsi A/M/A dibandingkan dengan laju disipasi suspensi liposom berdasarkan nilai slope (b) persamaan regresi linier antara lama penyimpanan dan ln jumlah ekstrak rosella.
Waktu Paruh ditetapkan berdasarkan konstanta laju disipasi, yang dihitung dengan menggunakan rumus berikut:
...(2) (Martin dkk., 1993). Entrapment efficiency multiemulsi A/M/A dihitung pada hari ke-1, 3, 7, 14, dan 28, dan dibandingkan dengan entrapment efficiency suspensi liposom yang dihitung pada hari ke-1 dan 14. Entrapment efficiency dihitung berdasarkan rumus berikut:
47 BAB IV
HASIL DAN PEMBAHASAN
Tujuan dari penelitian ini yaitu untuk memperoleh formula multiemulsi A/M/A optimum dan mengetahui stabilitas ekstrak kelopak bunga rosella dalam sediaan multiemulsi A/M/A dan suspensi liposom selama penyimpanan. Kelopak rosella dipilih karena memiliki kemampuan sebagai antioksidan dengan kandungan seperti antosianin, gossipetin, flavonoid, riboflavin, asam askorbat, niacin, karoten, vitamin, dan mineral (Al-Hashimi, 2012). Antosianin dalam ekstrak metanol rosella meliputi 3-sambubiosida, sianidin-3-sambiosia, delphinidin,-3 glukosida dan sianidin 3-glukosida (Kalima , Ramg, Chove, dan Wicklund, 2014). Antioksidan antosianin mudah mengalami kerusapak terutapa karena pengaruh lingkungan untuk mengatasi kekurangan tersebut ekstrak kelopak bunga rosella perlu diformulasikan dalam bentuk sediaan vesikel (Pinswuan dkk., 2010). Formulasi multiemulsi dan liposom merupakan contoh sediaan vesikel sehingga dapat melindungi antosianin yang terkandung dalam ekstrak kelopak bunga rosella. Tipe multiemulsi A/M/A digunakan karena ekstrak kelopak bunga rosella yang cenderung bersifat polar.
(Susmiyanto, Wibowo, dan Sutresno, 2013). Pengukuran ekstrak kelopak bunga rosella selanjutnya merupakan pengukuran antosianin.
Gambar 12. Spektra antosianin ekstrak kelopak bunga rosella
A. Penetapan Bobot Tetap Ekstrak Kelopak Bunga Rosella
Formulasi multiemulsi A/M/A menggunakan ekstrak metanol kelopak rosella. Fraksi metanol dipilih untuk menghasilkan recovery antosianin yang lebih tinggi. Pelarut polar seperti metanol direkomendasikan untuk mengektraksi komponen fenolik dari bahan tanaman (Halima, 2014).