BAB II
TINJAUAN KEPUSTAKAAN
2.1. Red Cell Distribution Width (RDW)
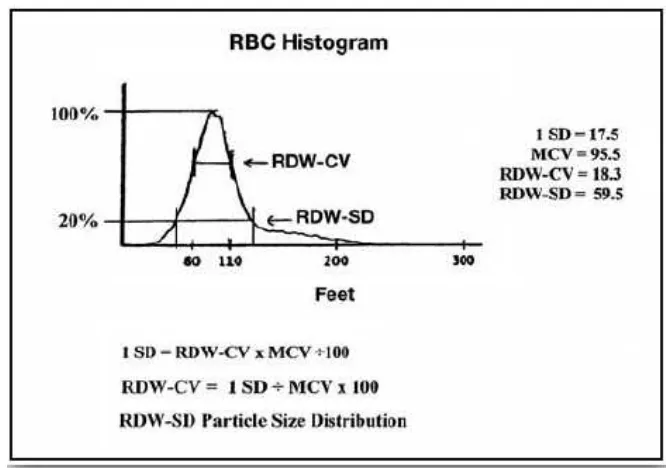
RDW merupakan suatu hitungan matematis yang menggambarkan jumlah anisositosis (variasi ukuran sel) dan pada tingkat tertentu menggambarkan poikilositosis (variasi bentuk sel) sel darah merah pada pemeriksaan darah tepi. RDW adalah cerminan dari nilai koefisien variasi dari distribusi volume sel darah merah. Baik MCV dan RDW keduanya dinilai dari histogram eritrosit (RBC). MCV dihitung dari seluruh luas area dibawah kurva, sedangkan RDW dihitung hanya dari basis tengah histogram.Ada 2 metode yang dikenal untuk mengukur nilai RDW, yaitu RDW-CV (Coefficient Variation) dan RDW-SD (Standard Deviation).15,16
Nilai RDW-CV dapat diukur dengan formula:16
RDW = !"#$%#&% %()*#+* ,-. (0!1)
3(#$ 3.4 x 100
Nilai normal berkisar antara 11.5 % - 14.5%. Sedangkan RDW-SD merupakan nilai aritmatika lebar dari kurva distribusi yang diukur pada frekwensi 20%. Nilai normal RDW-SD adalah 39 sampai 47 fL. Semakin tinggi nilai RDW maka semakin besar variasi ukuran sel.17
Gambar 2.1. Histogram distribusi ukuran sel normal. Ukuran sel lebih kecil dari normal distribusi kekiri; Ukuran sel lebih besar dari
normal distribusi kekanan.16
Gambar 2.2. Histogram penilaian RDW. RDW dinilai dari lebar histogram pada 1 standard deviasi (1SD) dibagi nilai rerata MCV. Nilai
normal RDW-CV adalah 11,5% sampai 14,5%. RDW-SD adalah nilai aritmatika lebar dari kurva distribusi yang diukur pada frekwensi 20%.
Nilai normal RDW-SD adalah 39 sampai 47 fL.15
yang normal akan bercampur dengan yang ukurannya lebih kecil atau yang lebih besar yang terbentuk saat terjadi defisiensi. Kenaikan serupa juga terjadi selama mendapatkan terapi pengganti besi, B12, dan folat ketika jumlah retikulosit meningkat. Nilai RDW juga meningkat setelah mendapatkan tranfusi darah, seperti halnya juga pada penderita anemia hemolitik dan trombotik dimana eritrosit terfragmentasi dalam sirkulasi. Peningkatan RDW juga berhubungan dengan penyakit hati, pecandu alkohol, keadaan inflamasi, dan penyakit ginjal, namun mekanisme dibalik timbulnya variasi eritrosit ini masih sangat kompleks.18
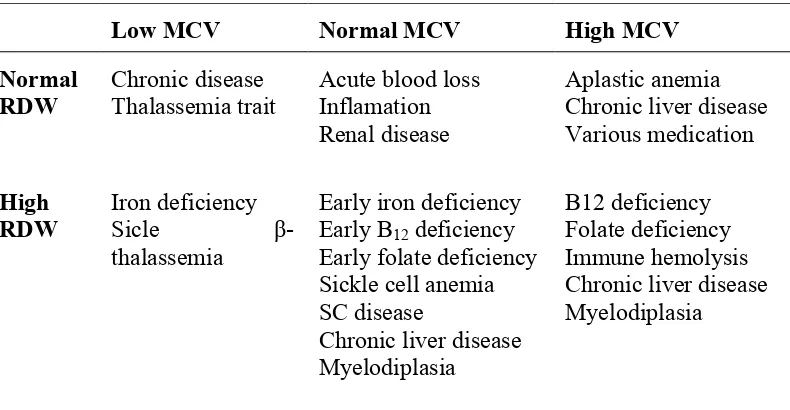
Tabel 2.1. Hubungan RDW dengan MCV.19
Low MCV Normal MCV High MCV
Gauer tahun 1950an menunjukkan adanya hubungan humoral antara jantung dan ginjal dimana dilatasi atrium kanan jantung menimbulkan natriuresis dan diuresis. Hal ini dibuktikan oleh Flynn et al, dimana senyawa aktifnya adalah Atrial Natriuretic Peptide (ANP). Kemudian pada tahun 1988, Sudoh et al mendapatkan Brain Natriuretic Peptide (BNP) dari otak babi yang ditemukan pula pada miosit ventrikel jantung.20
peptida natriuretik tersebut mempunyai kesamaan struktur yaitu adanya cincin residu 17 asamamino yang dibentuk dengan jembatan disulfida antara 2 residu sistein, disertai 2 rantai cabang masing-masing dengan ujung aminodan karboksil.20,21,22,23
2.2.1. Sekresi
Dalam keadaan normal, hormon pre-proBNP disimpan dalam jumlah sedikit di granula atrium. Setelah ada stimulus, terjadi pergeseran produksinya dari atrium ke ventrikel yang dibentuk dengan cepat dan dikeluarkan sebagai pancaran (burst). Stimulus utama sintesis dan sekresi hormon pre-proBNP adalah adanya stres dinding jantung berupa regangan dinding ventrikel (cardiac wall stretching) dan peningkatan tekanan pengisiannya (filling pressure). Misalnya
seperti pada gagal jantung kronik dimana terjadi regangan kronik miosit ventrikel terutama ventrikel kiri.2,20,21,24
Semua anggota peptide natriuretik di keluarkan dalam bentuk prohormon. Adanya stres pada dinding jantung menyebabkan miosit mengeluarkan hormon pre-proBNP yang mengandung asam amino rantai 134 termasuksinyal rantai peptida dari 26 asam amino pada ujung terminal NH2. Selanjutnya, pre-proBNP diubah melalui pemecahan peptida sinyalnya menjadi hormon proBNP yang mengandung asam amino rantai 108. Di sirkulasi, enzim proteolitik furin memecah proBNP menjadi hormon aktif BNP yang mempunyai 32 asam amino (asam amino 77-108), terpisah dari NT-proBNP (fragmen terminal NH dari proBNP) dengan 76 asam amino (asam amino 1-76) yang merupakan metabolit tidak aktif.21,24,25
Peningkatan kadar peptida natriuretik khususnya NT-proBNP juga dijumpai pada pasca infark miokard yang mungkin disebabkan oleh regangan daerah sekitar infark dan berkaitan dengan aktivasi sistem neurohormonal. Regangan mekanik dapat mengaktifkan jalur JAK/STAT (Jannus Kinase/Signal Transducer and Activators of Transcription), menstimulasi sekresi BNP, dan
memperbesar ekspresi gen Interleukin-6 dan cardiotrophin-1. Kemungkinan lain Cardiotrophin-1 sendiri dapat secara langsung meningkatkan transkripsi gen
Peningkatan kadar BNP dan NT-proBNP tidak hanya mencerminkan stres dinding ventrikel kiri yang meningkat tetapi dapat juga akibat langsung dari iskemia miokard walaupun mekanismenya masih belum jelas. Diduga iskemia dapat meningkatkan regangan dinding ventrikel regional.23,28
2.2.2. Degredasi
Mekanisme utama bersihan peptida natriuretik dari sirkulasi adalah melalui pengikatan terhadap Natriuretic Peptide Receptors-C (NPR-C) lewat proses endositosis. Neutral Endopeptidases (NEPs), suatu enzim metallopeptidase yang mengandung zink, juga berpengaruh dalam degradasi
peptida natriuretik yaitu melalui hidrolisis. BNP relatif lebih resisten terhadap NEPS dibandingkan dengan ANP. Tetapi NT-proBNP secara biologi tidak aktif dan tidak terikat dengan NPRs dan juga tidak mengalami degradasi oleh NEPs. Mekanisme bersihan NT-proBNP belum diketahui tetapi diduga sebagian besar sepertinya melalui ekskresi ginjal yaitu filtrasi glomerulus. Fungsi ginjal mempengaruhi kadar NT-proBNP pada gagal jantung akut. Peningkatan nyata NT-proBNP pada pasien gagal ginjal menunjukkan ginjal mungkin berperan penting untuk bersihan NT-proBNP.22,25 Pasien dengan insufisiensi ginjal sedang dan berat memerlukan penyesuaian kadar NT-proBNP yaitu 1200 ng/mL.29,30
2.2.3. Fisiologi Dalam Tubuh Manusia
Peptida natriuretik mempunyai reseptor untuk berinteraksi terhadap sel target yakni Natriuretic Peptide Receptors-A (NPR-A), Natriuretic Peptide Receptors-B (NPR-B) dan NPR-C yang merupakan keluarga reseptor guanylyl
cyclase. Reseptor ini memediasi aktifitas biologik peptida natriuretik melalui sintesa dan akumulasi intraseluler dari cyclic guanosine monophosphate (cGMP). Efek biologis yang ditimbulkan adalah diuresis dan natriuresis, vasodilatasi, inhibisi sistem nervus simpatis dan sistem renin-angiotensin- aldosteron, serta inhibisi pertumbuhan miosit kardiak dan vaskular.21,24,31
dapat mempengaruhi konsentrasi peptida natriuretik jantung diantaranya miokard infark akut dan gagal ginjal.24,32
2.3. Gagal Jantung 2.3.1. Defenisi
Gagal jantung adalah satu gejala klinis pada pasien mengalami kelainan struktur atau fungsi jantung yang disebabkan oleh kelainan bawaan atau acquired heart disease sehingga jantung tidak mampu untuk memompakan darah dalam
jumlah yang memadai untuk memenuhi kebutuhan metabolit tubuh (forward failure) atau kemampuan tersebut hanya dapat terjadi dengan tekanan pengisian
jantung yang tinggi (backward failure) atau kedua-duanya.33
2.3.2. Patofisiologi
Penyebab tersering terjadinya gagal jantung adalah gangguan/kerusakan fungsi miokard ventrikel kiri di samping adanya penyakit pada perikardium, miokardium, endokardium, ataupun pembuluh darah besar. Penurunan fungsi ventrikel kiri mengakibatkan terjadinya penurunan curah jantung yang selanjutnya menyebabkan teraktivasinya mekanisme kompensasi neurohormonal yang bertujuan mengembalikan kinerja jantung dalam memenuhi kebutuhan jaringan.
Aktivasi sistem simpatis menimbulkan peningkatan denyut jantung dan vasokontriksi perifer sehingga curah jantung dapat meningkat kembali. Aktivasi renin-angiotensin-aldosteron system (RAAS) menyebabkan vasokontriksi
(angiotensin) dan peningkatan volume darah melalui retensi air dan natrium (aldosteron). Mekanisme kompensasi yang terus berlangsung ini akan menyebabkan stress pada miokardium sehingga menyebabkan terjadinya remodeling yang progresif, dan pada akhirnya dengan mekanisme kompensasi pun jantung tidak dapat lagi memenuhi kebutuhan jaringan (dekompensasi).34
2.3.3. Gejala Klinis
dapat memompa darah lebih banyak. Akibatnya, otot jantung akan menebal untuk membantu meningkatkan kekuatan pompa. Hal tersebut membutuhkan semakin banyak suplai darah dari arteri koronaria yang menyebabkan jantung juga akan berdenyut lebih cepat untuk memompa lebih sering lagi. Pada keadaan ini, kadar hormon yang menstimulasi jantung akan meningkat.3
Manifestasi klinis yang timbul menunjukkan adanya tanda-tanda gagal jantung kongestif yaitu dispnu dan fatique yang dapat menghambat toleransi latihan dan retensi cairan yang dapat menimbulkan kongesti paru dan edema perifer. Kedua abnormalitas tersebut akan mengurangi kapasitas fungsional dan kualitas hidup.3
2.3.4. Klasifikasi Gagal Jantung
New York Heart Association (NYHA) pertama kali membuat klasifikasi
gagal jantung yang berdasarkan pada derajat keterbatasan fungsional. Pembagian fungsional NYHA sering digunakan untuk menentukan progresifitas gagal jantung. Sistem ini membagi pasien atas 4 kelas fungsional yang bergantung pada gejala yang muncul, yaitu asimptomatis (kelas I), gejala muncul pada aktifitas ringan (kelas II), gejala muncul pada aktifitas berat (kelas III), dan gejala muncul pada saat istirahat (kelas IV). Kelas fungsional pada penderita gagal jantung cenderung berubah-ubah. Bahkan perubahan ini dapat terjadi walaupun tanpa perubahan pengobatan, dan tanpa perubahan pada fungsi ventrikel yang dapat diukur.3
American College of Cardiology/ American Heart Association
kembali lagi ke stadium A, hal yang mana dapat terjadi bila menggunakan klasifikasi menurut NYHA.3
2.3.5. Diagnosis
Diagnosis dibuat berdasarkan anamnesis, pemeriksaan fisik, elektrokardiografi, foto toraks, ekokardiografi-doppler, kateterisasi jantung dan uji latih.1
Kriteria Framingham dapat pula dipakai untuk diagnosis gagal jantung yaitu dengan terpenuhinya 2 kriteria mayor atau 1 kriteria mayor dan 2 kriteria minor. Adapun kriteria Framingham sebagai berikut:1
- Kriteria mayor:
a. Paroksismal nokturnal dispnu b. Distensi vena leher
c. Ronki paru d. Kardiomegali e. Edema paru akut f. Gallop S3
g. Peninggian tekanan vena jugularis h. Refluks hepatojugular
- Kriteria minor: a. Edema ekstremitas b. Batuk malam hari c. Dispnea d’effort
d. Hepatomegali e. Efusi pleura
f. Penurunan kapasitas vital 1/3 dari normal g. Takikardia (> 120 x/menit)
- Kriteria mayor atau minor:
Gagal jantung dapat disertai spektrum abnormalitas fungsi ventrikel yang luas, mulai dari ukuran ventrikel kiri dan fraksi ejeksi yang normal sampai dengan dilatasi berat dan/atau fraksi ejeksi yang sangat rendah.1
2.4. Hubungan RDW dengan Gagal Jantung
Selama satu dekade terakhir, telah terjadi lonjakan jumlah penelitian yang meneliti tentang biomarker prognostik berbagai penderita gagal jantung. Beberapa biomarker seperti natriuretik peptida secara langsung mencerminkan proses patofisiologi dalam prognosis, sedangkan biomarker lainnya masih kurang baik dalam menggambarkan prognosis.11
Setelah publikasi awal oleh Felker et al12 pada tahun 2007 secara tidak sengaja menemukan bahwa RDW dapat menjadi prediktor prognosis yang sangat independen pada penderita gagal jantung (dan yang lebih penting, lebih unggul dibandingkan parameter anemia yang lain termasuk konsentrasi hemoglobin), RDW menjadi subjek yang menarik bagi berbagai peneliti klinis di lapangan. Dengan cakupan yang luas dari penyakit kardiovaskuler, termasuk gagal jantung, RDW ditemukan dapat menjadi prediktor outcome yang konsisten dan independen.11
Dalam artikel yang diterbitkan di Revista Espanola de Cardiologia, Bonaque et al35 menyajikan data yang menunjukkan peran prognostik dari RDW pada 698 orang penderita gagal jantung kronik. Dalam analisis yang disesuaikan, RDW dapat memprediksi tingkat mortalitas dan hospitalisasi pada penderita gagal jantung kronik. Penelitian mereka semakin menegaskan hubungan antara RDW dengan morbiditas dan mortalitas pada penderita penyakit kardiovaskular yang sudah ada sebelumnya.11
bahwa RDW merupakan pemeriksaan “gratis” yang memiliki nilai prognostik yang baik pada penderita gagal jantung meski dibandingkan dengan pemeriksaan lain yang relatif lebih mahal seperti NT-proBNP.
Förhécz et al37 pada tahun 2009 melakukan pengamatan terhadap mekanisme yang mendasari timbulnya peningkatan nilai RDW pada penderita gagal jantung kronik yang sudah diteliti sebelumnya. Dari hasil pengamatan disimpulkan bahwa adanya hubungan antara peningkatan RDW dengan marker inflamasi, eritropoiesis yang tidak efektif, nutrisi yang kurang, dan gangguan fungsi ginjal. Penelitian ini sejalan dengan temuan oleh Allen et al38 tahun 2010. Allen juga menemukan adanya hubungan antara peningkatan RDW pada penderita gagal jantung dengan marker defisiensi besi, inflamasi, dan gangguan fungsi ginjal.
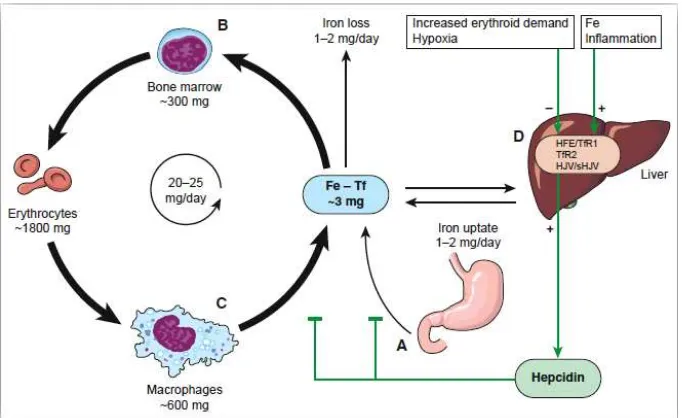
Gambar 2.3. Jalur pertukaran besi.16
Pada penelitian yang dilakukan oleh Okonko et al40 yang melakukan studi pada 157 pasien gagal jantung sistolik (left ventricular ejection fraction < 45%) baik dengan anemia maupun non anemia, kemudian pada pasien tersebut dilakukan pemeriksaan profil status zat besi (feritin, saturasi transferin, TIBC) lalu dihubungkan dengan tingkat keparahan gagal jantung dinilai dari New York Heart Association (NYHA) functional class. Penelitian ini dilakukan di Wexham
Part Hospital (Slough United Kingdom) dan Royal Brompton Hospital (London,
United Kingdom). Diagnosa gagal jantung kronik ditegakan berdasarkan adanya
tanda dan gejala yang dialami lebih dari 6 bulan dan nilai Left Ventricular Ejection Fraction (LVEF) ≤ 45%. Dari penelitian tersebut dapat disimpulkan adanya gangguan metabolisme besi yang berhubungan dengan tingkat keparahan dari NYHA functional class pada penderita gagal jantung kronik.
2.5. Hubungan NT-proBNP dengan Gagal Jantung
NT-proBNP diindikasikan sebagai alat bantu menegakkan diagnosis gagal jantung atau bentuk ringan disfungsi jantung, membantu dalam menilai keparahan gagal jantung yang ditandai dengan kelas NYHA dan juga menilai keberhasilan terapi pasien dengan disfungsi ventrikel kiri. NT-proBNP juga bermanfaat dalam menyingkirkan gejala dengan penyebab kardiak atau non kardiak pada sesak nafas. Kadar NT-proBNP akan meningkat sebanding dengan peningkatan kelas NYHA dan menggambarkan tingkat keparahan dari gangguan jantung. Sensitifitas yang tinggi dari NT-proBNP juga memungkinkan untuk mendeteksi bentuk ringan dari disfungsi jantung pada pasien asimptomatis.42,43
Sebuah penelitian mendapatkan bahwa median konsentrasi NT-proBNP pada gambaran klinis menurut kelas NYHA II, III dan IV berturut-turut adalah 3512 pg/mL, 5610 pg/mL, dan 6196 pg/mL. Sedangkan median konsentrasi NT-proBNP pada eksaserbasi gagal jantung akut adalah 4639 pg/mL dibandingkan 108 pg/mL tanpa gagal jantung akut.42
Sebuah penelitian melaporkan bahwa kadar NT-proBNP 5 kali di atas normal mempunyai sensitifitas dan nilai prediksi negatif > 90% untuk mendeteksi LVEF < 40%. Selain itu juga ditetapkan batasan normal NT-proBNP untuk mendeteksi gagal jantung adalah 68-112 pg/mL (8,2-13,3 pmol/L).44 Konsentrasi cut point NT-proBNP yang direkomendasikan di Eropa untuk mendeteksi gagal jantung adalah 100 pg/mL untuk laki-laki dan 150 pg/mL untuk perempuan. Sementara di Amerika Serikat untuk kedua jenis kelamin ditetapkan 125 pg/mL.45
Studi COPERNICUS9 (Carvedilol Prospective Randomized Cumulative Survival) 2004, menyatakan penderita gagal jantung kronik dengan kadar
NT-proBNP >1767 pg/mL memiliki tingkat hospitalisasi dan kematian dalam 1 tahun dua kali lipat lebih besar daripada pendeita dengan nilai NT-proBNP yang lebih rendah. Demikian halnya data dari ADHERE10 studi 2007 (Acute Decompensated Heart Failure National Registry) dengan jumlah sampel yang lebih besar lagi
2.6. Hubungan RDW dengan NT-ProBNP pada Gagal Jantung
Studi yang dilakukan oleh Al Najjar et al14 pada tahun 2009 mencoba
mengidentifikasi hubungan antara nilai RDW dan nilai NT-proBNP pada
penderita gagal jantung kronik. Peneliti mendapati bahwa RDW memiliki
korelasi positif yang signifikan dengan tingkat kekuatan korelasi moderat
terhadap angka NT-proBNP dengan p value < 0,01. Nilai RDW dan NT-proBNP
keduanya sama sama meningkat secara signifikan pada pasien yang meninggal
dalam satu tahun pertama sejak diagnosis ditegakkan dengan tingkat signifikansi
p < 0,001 kemaknaan 95%.
Studi yang dilakukan oleh Celik et al46 pada tahun 2012 mencoba
menjelaskan keterkaitan RDW dengan NT-proBNP pada penderita gagal jantung
tidak terkompensasi. Mereka menyimpulkan bahwa RDW akan meningkat
seiring dengan peningkatan NT-proBNP dan seiring dengan peningkatan tekanan
pengisian ventrikel kiri. Terdapat beberapa hipotesis yang mencoba menjelaskan
mengapa RDW dapat mencerminkan peranan NT-proBNP sebagai petanda
biologis keadaan gagal jantung kronik. Kebanyakan hipotesis tersebut
mengaitkan RDW dengan keadaan inflamasi kronis, gangguan fungsi ginjal,
ketidakefektifan proses eritropoiesis, malnutrisi, dan gangguan jalur
neurohormonal yang terjadi pada penderita gagal jantung kronik.46
Akan tetapi, studi yang dilakukan oleh Van Kimmenade et al36
menunjukkan bahwa peningkatan RDW pada penderita gagal jantung kronik
yang tidak terkompensasi ternyata tidaklah dipengaruhi oleh status nutrisi pasien,
riwayat transfusi darah ataupun oleh inflamasi. Hal ini dibuktikan dengan tidak
cukup signifikannya korelasi angtara RDW dengan CRP (C-Reactive Protein)
yang merupakan marker inflamasi. Temuan ini semakin mempertegas bahwa
kemungkinan kaitan antar RDW dengan NT-proBNP terletak pada aktivasi jalur
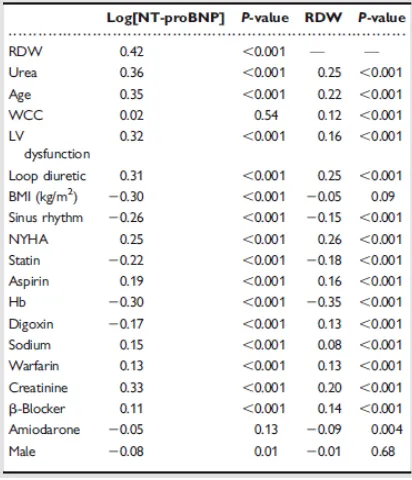
Tabel 2.2. Korelasi Spearman antara RDW dengan NT-proBNP.13
Hasil yang berbeda dikemukakan oleh studi terkini dari Allen et al38 yang
menyebutkan bahwa terjadi gangguan proses mobilisasi simpanan besi di hati
pada pasien gagal jantung kronik yang tidak terkompensasi, dan hal inilah yang
kemungkinan menyebabkan terjadinya peningkatan nilai RDW pada
pasien-pasien tersebut. Diduga hal ini pula yang menjelaskan mengapa terjkadi
peningkatan hepsidin pada penderita gagal jantung kronik. Hepsidin mencegah
tubuh menyerap zat besi dari yang diperlukan baik yang berasal dari makanan atau suplemen dan menahan pengambilan zat besi dari sel, yang pada akhirnya berakibat pada gangguan pembentukan sel darah merah sehingga menyebabkan ukuran sel darah merah yang beredar menjadi sangat beragam dan pada akhirnya meningkatkan nilai RDW.38
Sungguhpun begitu, tidak dapat serta merta disimpulkan bahwa
peningkatan RDW pada pasien gagal jantung kronik ini murni dikarenakan oleh
gangguan mobilisasi besi saja. Karena hal yang sedikit berbeda dikemukakan
oleh penelitian Patel et al47 pada tahun 2009 yang menemukan bahwa pada
pasein gagal jantung kronik terjadi pula peningkatan berbagai sitokin-sitokin
proinflamatorik. Hal ini mungkin semakin memperkuat alasan mengapa RDW
dapat mencerminkan peranaan NT-proBNP sebagai indikator prognosis pasien