Informasi Dokumen
- Penulis:
- Giri Seno Aji K7113190
- Jafar Shidiq K7113118
- Maryana K7113136
- Maya Al Fattah K7113139
- Maya Fatmalasari F K7113140
- Nisa Romadhoni K7113153
- Riana Resty K7113182
- Sekolah: Universitas
- Mata Pelajaran: Kimia
- Topik: Asam Basa
- Tipe: Presentasi
- Tahun: 2023
- Kota: Tidak Diketahui
Ringkasan Dokumen
I. Pendahuluan
Pendahuluan memberikan gambaran umum mengenai topik asam dan basa dalam konteks kimia. Ini mencakup pentingnya pemahaman konsep asam dan basa dalam berbagai aplikasi sehari-hari, seperti dalam reaksi kimia, industri, dan kesehatan. Pemahaman ini tidak hanya bermanfaat bagi pelajar dalam bidang kimia tetapi juga bagi masyarakat umum yang berinteraksi dengan bahan kimia dalam kehidupan sehari-hari.
II. Asam Basa
Bagian ini menjelaskan definisi asam dan basa, serta karakteristik masing-masing. Asam didefinisikan sebagai senyawa yang menghasilkan ion hidrogen (H+) dalam larutan, sedangkan basa menghasilkan ion hidroksida (OH-). Pemahaman ini penting untuk mencapai tujuan pembelajaran, yang mencakup pengenalan sifat-sifat kimia dasar dan reaksi antara asam dan basa.
2.1. Pengertian Asam
Asam adalah senyawa yang dapat melepaskan ion H+ ketika larut dalam air. Karakteristik asam meliputi rasa asam, kemampuan mengubah warna indikator, dan sifat korosif. Pemahaman ini penting dalam konteks reaksi kimia dan aplikasi praktis dalam laboratorium.
2.2. Pengertian Basa
Basa adalah senyawa yang dapat menghasilkan ion OH- dalam larutan. Sifat-sifat basa termasuk rasa pahit dan licin. Pemahaman tentang basa sangat penting dalam penentuan pH dan interaksi dengan asam.
III. Teori Asam Basa
Bagian ini membahas berbagai teori yang menjelaskan konsep asam dan basa, seperti teori Arrhenius, Bronsted-Lowry, dan Lewis. Setiap teori memberikan perspektif yang berbeda tentang bagaimana asam dan basa berinteraksi, yang penting untuk memahami reaksi kimia di berbagai tingkat pendidikan.
3.1. Teori Arrhenius
Teori ini mendefinisikan asam sebagai zat yang menghasilkan ion H+ dan basa sebagai zat yang menghasilkan ion OH- dalam larutan. Ini adalah dasar pemahaman kimia yang digunakan dalam banyak eksperimen.
3.2. Teori Bronsted-Lowry
Teori ini memperluas definisi asam dan basa sebagai donor dan akseptor proton, yang lebih fleksibel dan aplikatif dalam berbagai reaksi kimia.
3.3. Teori Lewis
Teori ini mendefinisikan asam sebagai akseptor pasangan elektron dan basa sebagai donor pasangan elektron. Pendekatan ini sangat berguna dalam pemahaman reaksi organik dan kompleks.
IV. Tata Nama Asam Basa
Bagian ini menjelaskan cara penamaan asam dan basa, termasuk aturan untuk senyawa yang mengandung oksigen dan tanpa oksigen. Memahami tata nama ini penting untuk komunikasi yang jelas dalam dunia kimia.
4.1. Penamaan Senyawa Asam
Penamaan senyawa asam yang tidak mengandung oksigen mengikuti aturan tertentu, seperti menambahkan akhiran '-ida'. Ini membantu dalam mengidentifikasi jenis asam dengan cepat.
4.2. Penamaan Senyawa Basa
Basa biasanya dinamai berdasarkan logam yang terlibat diikuti oleh hidroksida. Memahami nama-nama ini penting untuk studi lebih lanjut dalam kimia anorganik.
V. Garam
Bagian ini menjelaskan pembentukan garam dari reaksi asam dan basa. Memahami bagaimana garam terbentuk dan sifatnya sangat penting dalam berbagai aplikasi, termasuk industri makanan dan farmasi.
5.1. Pengertian Garam
Garam terbentuk ketika asam bereaksi dengan basa. Pemahaman ini penting untuk aplikasi praktis dalam kehidupan sehari-hari, seperti dalam proses pengawetan makanan.
5.2. Pembentukan Garam
Pembentukan garam dapat bervariasi tergantung pada kekuatan asam dan basa yang terlibat, yang mempengaruhi sifat akhir garam yang dihasilkan.
VI. Penentuan Skala Keasaman
Bagian ini membahas cara menentukan kekuatan asam dan basa melalui pH. Memahami pH sangat penting dalam berbagai aplikasi, termasuk laboratorium dan industri.
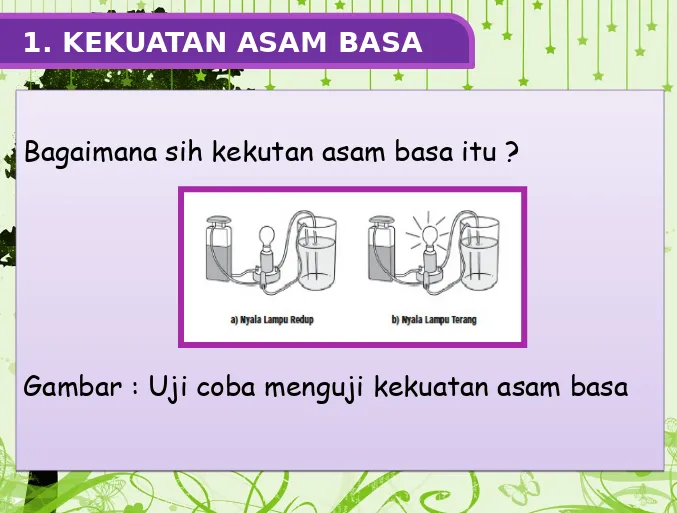
6.1. Kekuatan Asam Basa
Kekuatan asam dan basa dapat diukur dengan pH, yang merupakan indikator penting dalam banyak reaksi kimia.
6.2. Indikator pH
Berbagai jenis indikator, termasuk indikator universal dan pH meter, digunakan untuk menentukan pH larutan, yang penting dalam eksperimen laboratorium.
VII. Aplikasi Asam Basa
Bagian ini menjelaskan berbagai aplikasi praktis dari asam dan basa dalam kehidupan sehari-hari, termasuk penggunaan dalam makanan, obat-obatan, dan pembersih. Ini menunjukkan relevansi materi dalam konteks kehidupan nyata.
7.1. Aplikasi Sifat Asam
Contoh penggunaan asam dalam makanan dan pengawetan menunjukkan bagaimana konsep kimia diterapkan dalam industri makanan.
7.2. Aplikasi Sifat Basa
Penggunaan basa dalam produk pembersih dan obat-obatan menunjukkan pentingnya pemahaman asam dan basa dalam berbagai bidang.