BAB II
TINJAUAN UMUM INDUSTRI FARMASI
P.T. KIMIA FARMA (PERSERO) TBK. PLANT MEDAN
2.1 Sejarah Perusahaan
Sejarah industri farmasi di Indonesia diawali dengan berdirinya pabrik farmasi pertama yang didirikan di Hindia Timur pada tahun 1817, yaitu Naamloze Vennootschap (N.V.) Chemicalien Handle Rathkamp & Co. Setelah perang kemerdekaan usai, pada tahun 1957-1959, perusahaan-perusahaan
farmasi milik Belanda, yaitu perusahaan Bovasta Bandoengsche Kinine Fabriek
yang memproduksi pil Kina, dan Onederneming Jodium, yang memproduksi Yodium, dinasionalisasi oleh pemerintah Indonesia yang pada perkembangan
selanjutnya menjadi P.T. Kimia Farma (Persero). P.T. Kimia Farma (Persero) Tbk. sebagai Badan Usaha Milik Negara (BUMN) dibentuk sebagai
Perusahaan Perseroan Terbatas (P.T.) pada tanggal 16 Agustus 1971. Sejak berdirinya hingga sekarang ini P.T. Kimia Farma (Persero) Tbk. telah mengalami beberapa perubahan, yaitu:
1. Periode I (1957-1959)
Periode ini adalah periode dimana pemerintah melaksanakan
nasionalisasi perusahaan farmasi milik bangsa Belanda yang ada di
Indonesia. Program nasionalisasi ini dikoordinasi oleh Badan Pengambil
Alihan Perusahaan Farmasi (BAPPHAR). Adapun perusahaan farmasi milik
a. Naamloze Vennootschap (N.V.) Rathkamp dan Naamloze
Vennootschap (N.V.) Bavosta di Jakarta
b. Naamloze Vennootschap (N.V.) Bandoengsche Kinine Febriek di
Bandung
c. Naamloze Vennootschap (N.V.) Ordeneming Iodium Watadakon di
Mojokerto
d. Naamloze Vennootschap (N.V.) Industri Tella di Surabaya
e. Commanditaire Vennootschap (C.V.) Apotek Malang di Malang
f. Drogistry Van Belem dan Naamloze Vennootschap (N.V.) Sari Delle
di Yogyakarta
2. Periode II (1960-1968)
Periode ini adalah periode pembentukan Perusahaan Negara Farmasi
(PNF) dan perusahaan-perusahaan farmasi milik Belanda yang telah
dinasionalisasikan sebelumnya. Perusahaan Negara Farmasi (PNF) ini
berdasarkan Peraturan Pemerintah Nomor 60 tahun 1961 dibawah
koordinasi Badan Pimpinan Umum Farmasi Negara sebagai peleburan
Badan Pengambil Alihan Perusahaan Farmasi (BAPPHAR) yang bernaung
dibawah Departemen Kesehatan.
Perusahaan-perusahaan yang didirikan adalah :
a. Perusahaan Negara Farmasi (PNF) Radja Farma (yang dahulunya
Naamloze Vennootschap (N.V.) Rathkamp) di Jakarta
b. Perusahaan Negara Farmasi (PNF) Nurani Farma (yang dahulunya
c. Perusahaan Negara Farmasi (PNF) Nakula Farma (yang dahulunya
Naamloze Vennootschap (N.V.) Bavosta) di Jakarta
d. Perusahaan Negara Farmasi (PNF) Bhinneka Kimia Farma di
Bandung
e. Perusahaan Negara Farmasi (PNF) Sari Husada (yang dahulunya
Naamloze Vennootschap (N.V.) Sari Delle) di Yogyakarta
f. Perusahaan Negara Farmasi (PNF) Kasa Husada (yang dahulunya
Naamloze Vennootschap (N.V.) Varbanstaffen)
g. Perusahaan Negara Farmasi (PNF) Biofarma (yang dahulunya
Naamloze Vennootschap (N.V.) Pasteur Institute) di Bandung
3. Periode III (1969-1970)
Untuk meningkatkan efisiensi setiap Badan Usaha Milik Negara
(BUMN), dikeluarkan Intruksi Presiden Nomor 17 tahun 1967 sehingga
Departemen Kesehatan melebur perusahaan-perusahaan milik negara
tersebut ke dalam Perusahaan Negara Farmasi (PNF) dan Alat-Alat
Kesehatan Bhinneka Kimia Farma serta Perusahaan Negara Farmasi (PNF)
Kasa Husada di Surabaya dirubah menjadi Perusahaan Umum dan
Perusahaan Daerah, kemudian Perusahaan Negara Farmasi (PNF) Sari
Husada di Yogyakarta berdiri sendiri sebagai anak perusahaan.
4. Periode IV (1971-2001)
Periode IV dimulai tahun 1971 ditandai dengan dikeluarkannya
Peraturan Pemerintah Nomor 116 tahun 1971 yang berlaku sejak tanggal 19
Maret 1971. Perusahaan Negara Farmasi (PNF) dan Alat-Alat Kesehatan
menjadi Perseroan Terbatas (P.T.) yang selanjutnya disahkan pada tanggal
16 Agustus 1971 sebagai P.T. Kimia Farma (Persero) Tbk. dengan akta
notaris dan diumumkan dalam berita negara.
5. Periode V (2001-sekarang)
Pada periode ini tepatnya tanggal 28 Juni 2001 P.T. Kimia Farma
(Persero) menjadi Perusahaan Terbuka (Tbk.) dengan nama P.T. Kimia
Farma (Persero) Tbk. dimana untuk privatisasi tahap I saham yang lepas
adalah sebanyak 9% dengan rincian 3% untuk program Kepemilikan Saham
Karyawan dan Manajemen (KSKM) P.T. Kimia Farma (Persero) Tbk., dan
sebanyak 6% untuk masyarakat umum.
Pada tanggal 4 Januari 2003 P.T. Kimia Farma membentuk 2 anak
perusahaan yaitu:
a. P.T. Kimia Farma Health & Care
b. P.T. Kimia Farma Trading & Distribution
Sedangkan pabrik sebagai P.T. Kimia Farma Holding Company.
Sejak tanggal 4 Juli 2001 pula P.T. Kimia Farma (Persero) Tbk.
tercatat sebagai perusahaan publik di Bursa Efek Jakarta dan Bursa Efek
Surabaya. Berbekal tradisi industri yang panjang selama lebih dari 187
tahun dan nama yang identik dengan mutu, hari ini P.T. Kimia Farma
(Persero) Tbk. telah berkembang menjadi sebuah perusahaan pelayanan
kesehatan utama di Indonesia yang kian memainkan peranan penting dalam
pengembangan dan pembangunan bangsa dan masyarakat.
Dengan dukungan kuat Penelitian dan Pengembangan, segmen usaha yang
yodium, kina dan produk-produk turunannya, serta minyak nabati. Lima fasilitas
produksi yang tersebar di Indonesia merupakan tulang punggung dari industri.
Plant Jakarta memproduksi sediaan tablet, tablet salut, kapsul, sirup kering,
suspensi, sirup, tetes mata, krim, antibiotika dan injeksi. Unit ini merupakan
satu-satunya pabrik obat di Indonesia yang mendapat tugas dari pemerintah untuk
memproduksi obat golongan narkotika. Industri formulasi ini telah memperoleh
sertifikat, yaitu: Cara Pembuatan Obat yang Baik (CPOB) dan ISO (International Organization for Standardization) 9001:2008.
Plant Bandung memproduksi bahan baku kina dan turunan-turunannya,
rifampisin, obat asli indonesia dan Alat Kontrasepsi Dalam Rahim (AKDR).
Selain itu, Plant Bandung juga memproduksi tablet, sirup, serbuk, dan produk
kontrasepsi Pil Keluarga Berencana (Pil KB). Unit produksi ini telah menerima
sertifikat Cara Pembuatan Obat yang Baik (CPOB) dan ISO (International Organization for Standardization) 9002.
Plant Semarang mengkhususkan diri pada minyak jarak, minyak nabati,
serta bedak. Untuk menjamin kualitas produksi, unit ini secara konsisten
menerapkan Sistem Manajemen Mutu (SMM) ISO (International Organization for Standardization) 9001:2008 serta telah memperoleh sertifikat Cara Pembuatan Obat yang Baik (CPOB).
Plant Watudakon di Jawa Timur merupakan satu-satunya pabrik yang
mengolah tambang yodium di Indonesia. Unit ini memproduksi yodium dan
garam-garamnya, bahan baku ferro sulfat sebagai bahan utama pembuatan tablet
besi untuk obat tambah darah, dan kapsul lunak ”Yodiol” yang merupakan obat
produksi formulasi seperti tablet, tablet salut, kapsul lunak, salep, sirup, dan
cairan obat. Unit ini telah memperoleh sertifikat Cara Pembuatan Obat yang Baik
(CPOB), ISO (International Organization for Standardization) 9002 dan ISO (International Organization for Standardization) 14001.
Plant Medan di Tanjung Morawa, Sumatera Utara, dikhususkan untuk
memasok kebutuhan obat di wilayah Sumatera. Produk yang dihasilkan oleh
pabrik yang telah memperoleh sertifikat Cara Pembuatan Obat yang Baik (CPOB)
untuk tablet, krim dan kapsul serta ISO (International Organization for Standardization) 9001:2008.
P.T. Kimia Farma (Persero) Tbk. Plant Medan berdiri pada tahun 1967
dengan nama Perusahaan Negara Farmasi (PNF) Radja Farma dan dulunya juga
merupakan perusahaan farmasi milik Belanda yang dinasionalisasikan oleh
pemerintah Indonesia. Pada tahun 1971 perusahaan ini berubah nama menjadi
P.T. Kimia Farma (Persero) Tbk. dan menjadi perusahaan cabang dari P.T. Kimia
Farma (Persero) Tbk. Jakarta. Dengan adanya Surat Keputusan Direksi Nomor
14/DIR/VI/2004 pada tanggal 14 Juni 2004 maka P.T. Kimia Farma (Persero)
cabang Medan berubah menjadi P.T. Kimia Farma (Persero) Tbk. Plant Medan.
Distribusi obat-obatan dikelola oleh Unit Logistik Sentral (ULS) yang berada di
Jakarta. Unit Logistik Sentral (ULS) ini nantinya yang mendistribusikannya
2.2 Visi dan Misi
Visi P.T. Kimia Farma (Persero) Tbk. adalah: Komitmen pada
peningkatan kualitas kehidupan kesehatan dan lingkungan. Untuk mewujudkan
visi tersebut, P.T. Kimia Farma (Persero) Tbk. memiliki misi, diantaranya:
1. Mengembangkan industri kimia dan farmasi dengan melakukan penelitian
dan pengembangan produk yang inovatif.
2. Mengembangkan bisnis Pelayanan Kesehatan Terpadu (Health Care Provider) yang berbasis jaringan distribusi dan jaringan apotek.
3. Meningkatkan kualitas sumber daya manusia dan mengembangkan sistem
informasi perusahaan.
Misi ini diwujudkan melalui strategi perusahaan, yakni:
1. Meningkatkan sinergi antar unit usaha dengan menggunakan salah satu unit
usaha yang kuat untuk mengembangkan unit usaha lain.
2. Meningkatkan efektifitas pemasaran dengan penyusunan program
pemasaran yang lebih fokus dan perluasan cakupan daerah pemasaran yang
ada.
3. Memperkuat struktur bisnis distribusi dengan melakukan intensifikasi dan
ekstensifikasi kegiatan distribusi.
4. Melakukan diversifikasi dan pengembangan produk, baik yang berasal dari
pengembangan sendiri maupun kerja sama dengan pihak luar.
5. Melakukan pengembangan usaha yang terkait dengan pelayanan kesehatan
yang dilakukan sendiri, kerja sama dengan pihak luar ataupun melalui
6. Mengembangkan sumber daya manusia untuk memperoleh sumber daya
manusia yang mempunyai komitmen-komitmen tinggi, melalui pelatihan
dan pendidikan yang terencana dan berkesinambungan.
7. Mengembangkan sistem dan prosedur operasi ditunjang dengan sistem ilmu
teknologi yang memadai untuk peningkatan efisiensi dan menuju
Operasional yang Baik (Excellence Operational).
2.3 Lokasi dan Sarana Produksi
P.T. Kimia Farma (Persero) Tbk. Plant Medan berada pada jalan
Sisingamangaraja Kilometer 9 No.59, Kotamadya Medan, Provinsi Sumatera
Utara, Indonesia. Perusahaan ini berdiri di atas lahan dengan luas 20.269 meter
persegi yang terdiri dari:
1. Ruang perkantoran.
2. Ruang laboratorium pengelolaan mutu (Ruang Asisten Manager
Pengelolaan Mutu, Ruang Mikrobiologi, Ruang Pengawasan Mutu, Ruang
Instrumen, Ruang Contoh Pertinggal) dan Pengawasan Selama Proses (In Process Control/IPC).
3. Ruang produksi tablet/kapsul.
4. Ruang produksi krim/salep.
5. Ruang penimbangan sentral.
6. Gudang bahan baku.
7. Gudang bahan kemas.
8. Gudang etiket.
10. Bangunan penunjang seperti tempat pencucian, dapur, mushola, dan tempat
olahraga.
Konstruksi bangunan P.T. Kimia Farma (Persero) Tbk. Plant Medan telah
dibuat sesuai dengan persyaratan Cara Pembuatan Obat yang Baik (CPOB)
dimana dinding dan langit-langit memiliki permukaaan licin dan tidak terdapat
sambungan. Lantai dan dinding di dalam ruangan produksi dilapisi dengan epoksi, ruang produksi untuk masing-masing bentuk sediaan terletak terpisah. Sistem
pengaturan udara pada ruang produksi menggunakan Unit Pengatur Udara (Air Handling Unit/AHU) dengan Peyejuk Udara (Air Conditioner/AC) sentral.
2.3.1 Struktur Organisasi P.T. Kimia Farma (Persero) Tbk. Plant Medan
Dalam melaksanakan kegiatanya P.T. Kimia Farma (Persero) Tbk. Plant
Medan menggunakan struktur organisasi yang disusun sedemikian rupa sehingga
jelas terlihat batas-batas tugas, wewenang dan tanggung jawab dari setiap personil
dalam organisasi. Struktur organisasinya dapat dilihat pada Lampiran 1, dimana di dalamnya mencakup tingkat manager sampai pada tingkat asisten manager dan
tingkat supervisor, sedangkan untuk level karyawan tidak digambarkan.
2.3.2 Sediaan-Sediaan Obat yang Diproduksi P.T. Kimia Farma (Persero) Tbk. Plant Medan
1. Betametason 0,1% krim.
2. Betason-N® krim.
3. Betason® krim.
5. Fungoral® krim tube 5 gram dan 10 gram.
6. Virules® krim tube 5 gram.
7. Hidrokortison 2,5% krim.
8. Kloramfenikol 250 miligram kapsul (1000 kapsul per botol dan 250 kapsul
per botol).
9. Kalsium Laktat 500 miligram tablet (1000 tablet per botol).
10. Parasetamol 500 miligram tablet (kemasan 10 tablet per strip dalam 10 strip
per kotak dan 1000 tablet per botol).
11. Gliseril Guaiakolat 200 miligram (1000 tablet per botol).
12. Gentamisin salep kulit.
13. Antalgin 500 mg tablet (kemasan 10 tablet per strip dalam 10 strip per kotak
dan 1000 tablet per botol).
14. Vitamin B kompleks tablet (1000 tablet per botol).
2.3.3 Perencanaan Produksi dan Pengendalian Inventaris (PPPI)
Tugas dan fungsi dari Perencanaan Produksi dan Pengendalian Inventaris
(PPPI) (Plan Production And Inventory Control/PPIC) yaitu: 1. Merencanakan kebutuhan bahan produksi.
2. Mengontrol jalannya pembuatan obat.
3. Merencanakan pengiriman obat jadi.
4. Melakukan stok opname ke gudang pada setiap akhir triwulan.
Dasar perencanaan adalah pemesanan pemasaran yang berasal dari
konversikan per Bets (Batch) karena tiap produk memiliki ukuran Bets (Batch) yang berbeda.
Untuk pemesanan bahan, Perencanaan Produksi dan Pengendalian
Inventaris (PPPI) memperhatikan stok bahan baku yang ada di gudang, stok
produk ruahan atau setengah jadi dan stok produk jadi di gudang, sehingga dapat
diketahui beberapa bahan yang akan dipesan.
Setelah semua jumlah bahan yang diperlukan untuk produksi dihitung, maka
Perencanaan Produksi dan Pengendalian Inventaris (PPPI) mengeluarkan Surat
Permintaan Pembelian Bahan (SPPB) ditujukan kepada bagian pembelian.
Pembelian ada dua cara yaitu: secara terpusat di Jakarta dan secara lokal di
Medan. Bagian pembelian ini akan memilih pemasok yang paling murah tetapi
memenuhi spesifikasi bahan yang diminta, kemudian bagian pembelian
menerbitkan Surat Pemesanan (SP) (Purchase Order/PO) dan ditandatangani Manager Plant. Dibuat tembusan satu lembar arsip pesanan ke bagian gudang agar
disiapkan tempatnya.
Bahan pesanan yang datang diterima oleh bagian gudang dimana bagian
gudang akan memeriksa kecocokan Nomor Pesanan, Jumlah, Spesifikasi Bahan
yang diminta pada Surat Pemesanan dengan bahan yang akan diantarkan. Bahan
tersebut akan dikarantina dan diberi label kuning sementara bagian gudang
membuat surat permohonan periksa ke Bagian Pengawasan Mutu untuk
melakukan sampling dan pemeriksaan terhadap bahan tersebut. Bila bahan
memenuhi syarat akan diberi label hijau disertai Hasil Pemeriksaan Laboratorium
Pemeriksaan Laboratorium (HPL) untuk nantinya akan dikembalikan ke pihak
pemasok.
Setelah semua bahan yang dipesan lengkap, maka Perencanaan Produksi
dan Pengendalian Inventaris (PPPI) membuat Surat Perintah Kerja (SPK) ke
bagian produksi yang ditandatangani pimpinan. Pada Surat Perintah Kerja (SPK)
tersebut ditulis Nomor Surat Perintah Kerja (Nomor SPK), Nama Sediaan, Nomor
Bets (Batch), dan kapan obat tersebut diharapkan siap diproduksi. Surat Perintah Kerja (SPK) dari Perencanaan Produksi dan Pengendalian Inventaris (PPPI) yang
dikirim ke bagian produksi dilampiri Catatan Pengolahan Bets (Batch), Catatan Pengemasan Bets (Batch), Surat Perintah Pengeluran Bahan Baku (SPPBB) dan Surat Perintah Pengeluran Bahan Kemas (SPPBK). Surat Perintah Kerja (SPK)
dibuat rangkap 4 dengan distribusi ke bagian Produksi, bagian Gudang, bagian
Laboratorium dan sebagai Arsip.
Obat jadi yang telah siap diproduksi dan dikemas kemudian dikirim ke
gudang penyimpanan obat jadi setelah dilakukan Analisis Kemasan Akhir
(Finished Pack Analysis) oleh petugas pengawasan mutu. Obat jadi tersebut akan dikirimkan dari gudang oleh Perencanaan Produksi dan Pengendalian Inventaris
(PPPI) ke Unit Logistik Sentral (ULS) Jakarta, maka Perencanaan Produksi dan
Pengendalian Inventaris (PPPI) membuat Surat Pengeluaran Produk Jadi (SPPJ)
ke bagian gudang untuk menyiapkan obat jadi tersebut untuk dikirimkan ke
Jakarta dan akan dilakukan stock opname. Pada bahan yang telah di stockopname
2.3.4 Produksi
Produksi adalah semua kegiatan pembuatan mulai dari penerimaan bahan
awal, pengolahan sampai dengan menghasilkan obat jadi. Kegiatan produksi ini
dilakukan di area tertutup dan tidak berhubungan langsung dengan bagian gudang
ataupun perkantoran.
Tugas dari bagian produksi PT Kimia Farma (Persero) Tbk. Plant Medan:
1. Melaksanakan pembuatan obat sesuai dengan Surat Perintah Kerja (SPK)
dari bagian Perencanaan Produksi dan Pengendalian Inventaris (PPPI),
mulai dari permintaan bahan baku ke gudang, penimbangan, pengolahan,
pengemasan, sampai pengiriman obat jadi ke gudang obat jadi sesuai
dengan prosedur tertulis yang telah ditetapkan pada Prosedur Tetap
(ProTap).
2. Melaksanakan dokumentasi atas semua tindakan yang dilakukan selama
proses pengolahan dan pengemasan dengan berpedoman pada Prosedur
Tetap (ProTap). Sebelum dimulainya kegiatan produksi, petugas yang
terlibat dalam kegiatan produksi ataupun yang memasuki area produksi
harus memakai pakaian bersih, masker, penutup kepala, dan melakukan
desinfeksi tangan dengan desinfektan yang tersedia sebelum memakai
sarung tangan.
Produksi dilaksanakan setelah adanya Surat Perintah Kerja (SPK) dari
bagian Perencanaan Produksi dan Pengendalian Inventaris (PPPI) ke bagian
Produksi dan dilakukan Produksi sesuai dengan Prosedur Tetap (ProTap) yang
telah ditetapkan serta mendokumentasi setiap tindakan yang dilakukan selama
Bets (Batch), Tahapan Proses, Operator, Tanggal, Jam, Hasil, Pengawasan yang berguna untuk mengetahui berapa lama waktu yang dibutuhkan untuk
menghasilkan suatu Bets (Batch) sediaan dan kualitas sediaan yang dihasilkan. Laporan proses produksi ini diisi oleh petugas yang melakukan suatu tahapan
proses produksi dan diketahui oleh supervisor produksi.
Hal-hal yang harus diperhatikan sebelum memulai kegiatan produksi:
1. Ruang produksi harus tetap terjaga kebersihan, dimana kegiatan
pembersihan dilakukan tiap pagi sebelum dimulai kegiatan produksi dan
sore hari sesudah selesai kegiatan produksi.
2. Temperatur dan kelembaban tiap ruangan produksi diatur sedemikan rupa
menggunakan Unit Pengatur Udara (Air Handling Unit/AHU) yaitu Penyejuk Udara (Air Conditioner/AC) sentral.
3. Peralatan yang digunakan harus dipastikan selalu dalam keadaan bersih
sebelum dan sesudah dilakukan kegiatan produksi.
4. Ruangan produksi harus mendapat penerangan dan pertukaran udara yang
cukup agar kegiatan produksi berjalan lancar.
Selama proses produksi berlangsung dilakukan Pengawasan Selama Proses
(In Process Control/IPC). Pengawasan Selama Proses (In Process Control/IPC) yang dilakukan ada 2 macam, yaitu:
1. Dilakukan oleh pihak produksi, yaitu setiap 15 menit sekali dilakukan
pemeriksaan keseragaman bobot.
2. Dilakukan oleh pihak pengawasan mutu, antara lain: uji kekerasan, waktu
Obat yang telah selesai diproduksi akan dilakukan pengemasan primer di
bagian produksi yang selanjutnya diserahkan ke bagian pengemasan melalui
Kotak Hantar (Passing Box) untuk dilakukan pengemasan sekunder sampai dihasilkan obat jadi. Obat jadi yang telah selesai dikemas, ditimbang dan dicatat
selanjutnya dibuat permohonan periksa ke Bagian Pemastian Mutu untuk
dilakukan Analisis Kemasan Akhir (Finished Pack Analysis). Obat jadi yang lulus pemeriksaan selanjutnya diserahkan ke gudang penyimpanan obat jadi.
Bagian Produksi pada PT Kimia Farma (Persero) Tbk. Plant Medan terdiri
dari beberapa jalur, diantaranya:
1. Jalur Produksi Krim dan Salep.
Jalur produksi krim terpisah dari jalur produksi yang lain dimana pada
jalur produksi ini terdiri dari beberapa ruangan. Ruangan tersebut telah
diatur suhu, kelembaban dan tekanan dengan Unit Pengatur Udara (Air Handling Unit/AHU). Adapun ruangan pada jalur produksi krim terdiri dari: a. Ruangan penimbangan.
Pada rungan ini dilengkapi dengan beberapa alat timbangan
digital (elektrik), lemari asam, Pengumpul Debu (Dust Collector), Unit Pengatur Udara (Air Handling Unit/AHU). Bahan-bahan yang telah ditimbang akan di tempatkan pada area antara (staging area) untuk kemudian diambil oleh petugas produksi lain untuk dilakukan
proses produksi selanjutnya. Ruangan penimbangan dipakai untuk
menimbang bahan sediaan krim, salep, tablet dan kapsul.
Pada ruangan ini dilengkapi dengan alat Double Jacket Tank
untuk memanaskan air, alat Ultra Turrax untuk mencampur bahan aktif dengan bahan dasar krim, alat Pencampur (Mixer) untuk pengadukan sehingga diperoleh produk ruahan. Alat-alat tersebut
dibersihkan setiap pagi hari sebelum digunakan dan sore hari sesudah
selesai digunakan. Bila tidak ada kegiatan produksi maka pembersihan
dilakukan seminggu sekali. Selama proses produksi Pengawasan
Selama Proses (In Process Control/IPC) oleh Bagian Pengawasan Mutu.
c. Ruangan pengisian.
Ruangan untuk melakukan pengisian sediaan krim ada 3 yaitu:
• Ruangan pengisian I: dilengkapi dengan mesin pengisian krim
(Elemech) dengan kapasitas 2400 tube per jam dan dilengkapi juga dengan neraca analitik.
• Ruang pengisian II: dilengkapi dengan mesin pengisian krim
(Pharmech) dengan kapasitas 900 tube per jam sampai 2000 tube per jam dan dilengkapi juga dengan neraca analitik.
• Ruang pengisian III: dilengkapi dengan mesin pengisian krim
(Pharmech) dengan kapasitas 1600 tube per jam dan dilengkapi juga dengan neraca analitik.
Sebelum pengisian krim, tube kosong yang telah dibersihkan di
bagian pengemasan di masukkan ke Kotak Hantar (Passing Box),
dibawa oleh petugas produksi ke ruang pengisian dan disusun ke
dilakukan pengisian. Setiap 15 menit dilakukan pemeriksaan bobot
oleh operator dan pada awal dan akhir pengisian dilakukan
pemeriksaan oleh Bagian Pengawasan Mutu.
d. Ruangan karantina.
Pada ruang ini disimpan produk ruahan untuk menunggu
pemeriksaan laboratorium. Produk ruahan yang telah selesai diperiksa
akan dikirim ke bagian pengemasan melalui Kotak Hantar (Passing Box) untuk dilakukan pengemasan sekunder. Bagan Alur proses Produksi krim dan salep dapat dilihat pada Lampiran 4.
2. Jalur Produksi Tablet.
Jalur produksi tablet terletak terpisah dari jalur produksi krim untuk
menghindari terjadinya pencemaran silang. Pada unit tablet juga terdapat
beberapa jalur. Ruangan tersebut telah diatur suhu, kelembaban dan tekanan
dengan Unit Pengatur Udara (Air Handling Unit/AHU). Juga dilengkapi dengan Pengumpul Debu (Dust Collector) sentral. Adapun ruangan pada produksi tablet terdiri dari:
a. Ruangan pencampuran.
Semua bahan tambahan dan bahan aktif dimasukkan ke dalam
Super Mixer dan dicampur hingga homogen, pengecualian untuk bahan pelicin dan bahan penghancur luar. Massa di atas digranulasi
dengan menggunakan alat Rotary Wet Granulator sehingga didapat granul basah. Untuk selanjutnya granul basah tersebut di pindah ke
ruang pengeringan.
Granul basah yang dihasilkan dikeringkan di dalam oven dengan
suhu 50oC sampai dengan 60oC selama 10 jam (tergantung pada bahan
yang akan dikeringkan). Kapasitas oven tersebut 450 kg per hari.
Setelah kering dilakukan pemeriksaan laboratorium dan selanjutnya
dipindahkan ke ruangan granulasi untuk pengayakan.
c. Ruang granulasi.
Massa granul yang telah dikeringkan digranulasi dengan alat
Communiting Fitz Mill, kemudian hasil granulasi dibawa ke ruang pencampuran akhir.
d. Ruang pencampuran akhir.
Massa yang telah digranulasi dimasukkan ke dalam alat V-Mixer
dan ditambahkan dengan bahan pelicin dan bahan penghancur luar.
Hasil yang diperoleh kemudian dilakukan pemeriksaan Pengawasan
Selama Proses (In Process Control/IPC). Massa disimpan di ruang karantina.
e. Ruang pencetakan.
Ruang untuk pencetakan ada 5, masing-masing terdapat 1 alat
cetak dan juga terdapat Pengumpul Debu (Dust Collector), neraca analitis, dan Unit Pengatur Udara (Air Handling Unit/AHU). Pencetakan dilakukan dengan menggunakan mesin cetak tablet merek
Cadmach CU dengan kecepatan mesin 50000 tablet per jam. Setiap 15 menit operator harus memeriksa keseragaman bobot. Bagian
Pengawasan Mutu di dalam ruang produksi melakukan pemeriksaan
friabilitas, waktu hancur, kekerasan tablet, disolusi dan keseragaman
bobot.
f. Ruang sortir.
Tablet yang dihasilkan disortir oleh petugas, tablet disortir dari
debu dan juga untuk disortir dari bentuk tablet yang tidak bagus atau
pecah. Kemudian dipindahkan ke ruangan pengemasan.
g. Ruang pengemasan.
Tablet yang telah diluluskan oleh Bagian Pengawasan Mutu
dibawa ke ruang pengemasan primer dan dikemas dalam kantong
plastik atau diblister. Tiap kantong berisi 1000 tablet dengan
menggunakan mesin penghitung dan diberi silika gel. Pada kemasan
strip atau blister masing-masingnya berisi 10 tablet dan dikemas ke
dalam kotak yang setiap kotak berisi 10 strip atau blister. Setelah
selesai dilakukan pengemasan primer dipindahkan ke ruangan melalui
Kotak Hantar (Passing Box) untuk dilakukan pengemasan sekunder. Bagan alur produksi tablet dapat dilihat pada Lampiran 2.
3. Jalur Produksi Kapsul.
Sediaan kapsul yang diproduksi oleh P.T. Kimia Farma (Persero) Tbk.
Plant Medan adalah Kloramfenikol Kapsul. Seperti jalur produksi krim,
salep dan tablet, jalur produksi Kapsul juga terletak terpisah untuk
menghindari terjadinya pencampuran atau pencemaran silang (Mix Up atau
Cross Contamination). Pada jalur produksi kapsul juga terdapat beberapa ruangan dimana setiap ruangan tersebut diatur suhu, kelembaban dan
Unit/AHU), juga dilengkapi Pengumpul Debu (Dust Collector) sentral. Adapun ruangan pada unit kapsul terdiri dari:
a. Ruang pengeringan.
Bahan yang akan dipakai untuk pembuatan kapsul ditimbang di
ruang penimbangan sesuai dengan Surat Perintah Kerja (SPK). Untuk
bahan pengisi (Avicel) dikeringkan terlebih dahulu di dalam oven
selama kurang lebih 12 jam pada suhu 85oC. Setelah itu semua bahan
dipindahkan ke ruang pencampuran.
b. Ruang pencampuran.
Pada ruang ini dilakukan pencampuran bahan aktif, bahan
pengisi dan bahan tambahan lainnya dengan menggunakan alat
Pencampur-V (V-Mixer) selama kurang lebih 15 menit. Setelah homogen, dilakukan pemeriksaan massa oleh Bagian Pengawasan
Mutu dan kemudian dipindahkan ke ruang pengisian kapsul.
c. Ruang pengisian kapsul.
Massa yang telah homogen dimasukkan ke dalam mesin
pengisian kapsul (Kwang Dah). Pada awal dan akhir pengisian dilakukan pemeriksaan laboratorium dan setiap 15 menit dilakukan
pemeriksaan keseragaman bobot oleh operator. Setelah itu
dipindahkan ke ruang seleksi kapsul.
d. Ruang sortir.
Kapsul yang dihasilkan disortir oleh petugas, Kapsul disortir
dari debu dan juga untuk disortir dari bentuk kapsul yang tidak bagus.
e. Ruang pengemasan.
Kapsul yang telah diluluskan oleh Bagian Pengawasan Mutu
dibawa ke ruang pengemasan primer dan dikemas dalam kantong
plastik. Tiap kantong berisi 250 kapsul dan 1000 kapsul dengan
menggunakan mesin penghitung dan diberi silika gel. Setelah selesai
dilakukan pengemasan primer dipindahkan ke ruangan pengemasan
melalui Kotak Hantar (Passing Box) untuk dilakukan pengemasan sekunder. Bagan alur produksi kapsul dapat dilihat pada Lampiran 3.
2.3.5 Pengawasan Mutu dan Pemastian Mutu
Pengawasan mutu obat harus dilaksanakan melalui sistem pengawasan
yang terencana dan terpadu. Semua unsur yang terlibat dalam pembuatan obat,
baik personalia maupun kelengkapan sarana industri farmasi harus dapat
menunjang maksud pembuatan obat itu dan mendukung sepenuhnya persyaratan
yang diinginkan sehingga obat yang dihasilkan senantiasa memenuhi spesifikasi
mutu yang telah ditetapkan. Pengawasan mutu adalah semua pengawasan yang
dilakukan selama pembuatan dan dirancang untuk menjamin agar produk obat
yang dihasilkan senantiasa memenuhi spesifikasi, identifikasi, kekuatan,
kemurnian dan karakteristik lain yang telah ditetapkan.
Bagian/Departemen Pengawasan Mutu (QC) di industri farmasi
bertanggung jawab untuk memastikan, bahwa:
1. Bahan awal memenuhi spesifikasi yang ditetapkan untuk identitas,
2. Tahapan produksi obat telah dilaksanakan sesuai prosedur yang ditetapkan
dan telah divalidasi.
3. Semua Pengawasan Selama Proses (In Process Control/IPC) dan pemeriksaan selama proses dan pemeriksaan laboratorium terhadap suatu
Bets (Batch) obat telah dilaksanakan dan Bets (Batch) tersebut memiliki spesifikasi yang ditetapkan sebelum didistribusi.
4. Suatu Bets (Batch) obat memenuhi persyaratan mutunya selama waktu peredaran yang ditetapkan. Setiap bahan baku yang dikarantina dilakukan
pengujian oleh Bagian Pengawasan Mutu yang mencakup: spesifikasi
identitas, kualitas, kekuatan/potensi dan persyaratan lain yang ditentukan.
2.3.6 Pemeriksaan Mutu Bahan Baku dan Bahan Pengemas
Bahan baku dan bahan pengemas datang dari pemasok ke bagian gudang,
kemudian petugas laboratorium melakukan sampling dan pemeriksaan terhadap:
1. Bahan baku dan bahan tambahan.
Pemeriksaan terhadap bahan baku dan bahan tambahan meliputi
pemeriksaan:
a. Pemeriksaan organoleptis, meliputi bentuk, warna, bau dan rasa.
b. Pemeriksaan kimia, meliputi pemeriksaan kualitatif, kuantitatif dan
pH.
c. Pemeriksaan fisika, meliputi titik lebur, kelarutan dan berat jenis.
2. Bahan pengemas.
Pemeriksaan terhadap bahan pengemas meliputi pemeriksaan:
b. Pemeriksaan etiket, meliputi ukuran, kebenaran tulisan dan lambang,
desain dan warna.
2.3.7 Pengawasan Selama Proses (In Process Control/IPC)
Pengawasan selama berlangsungnya proses produksi bertujuan untuk
mencegah terlanjur diproduksinya obat yang tidak memenuhi spesifikasi.
Pengawasan dilakukan dengan cara mengambil contoh dan mengadakan
pemeriksaan dan pengujian terhadap produk yang dihasilkan pada
langkah-langkah tertentu dari proses pengolahan.
Pengawasan dalam proses pengolahan yang dilaksanakan oleh bagian
Produksi dilakukan guna menjamin bahwa mesin dan peralatan produksi serta
proses yang digunakan akan menghasilkan produk yang memenuhi spesifikasi
yang ditetapkan. Sedangkan pengawasan dalam proses produksi yang
dilaksanakan oleh bagian Pengawasan Mutu meyakinkan bahwa produk yang
dihasilkan pada tahap tertentu telah memenuhi spesifikasi yang telah ditetapkan
sebelum dilanjutkan pada proses berikutnya. Bagian Pengawasan Mutu
menentukan apakah tahap lanjutan dari proses pengolahan dapat dilaksanakan
berdasarkan hasil pengujian yang dilakukan.
Pengawasan Selama Proses (In Process Control/IPC) hendaklah meliputi pengujian parameter kualitas, antara lain:
1. Tablet: pemerian, kadar air, bobot rata-rata, bobot satuan, kadar bahan aktif,
kekerasan, friabilitas, waktu hancur dan disolusi.
2. Kapsul: pemerian, bobot rata-rata, bobot satuan, kadar bahan aktif, waktu
3. Krim dan Salep: pemerian, pH, bobot rata-rata, homogenitas dan kadar
bahan aktif.
2.3.8 Pengawasan Selama Pengemasan
Pengawasan dalam proses pengemasan hendaklah meliputi pemeriksaan
parameter kualitas, antara lain:
1. Kerapatan tutup wadah seperti tutup botol dan tutup tube.
2. Jumlah satuan produk dalam kemasan.
3. Kebenaran dan kebersihan bahan pengemas yang dipakai.
4. Kerapian pengemasan, penulisan Nomor Bets (Batch), tanggal kadaluarsa. 5. Kebocoran produk yang dikemas dalam strip.
2.3.9 Uji Stabilitas
Pengujian stabilitas adalah serangkaian uji yang didesain untuk
mendapatkan jaminan stabilitas suatu produk, yaitu pemeliharaan spesifikasi suatu
produk yang dikemas dalam bahan pengemas yang telah ditentukan dan disimpan
dalam kondisi penyimpanan yang telah ditetapkan pada rentang waktu tertentu.
Maksud pengujian stabilitas adalah untuk memberikan bukti mengenai bagaimana
mutu bahan atau produk berubah sepanjang waktu karena pengaruh berbagai
faktor lingkungan seperti suhu, kelembapan dan cahaya. Pengujian stabilitas
memungkinkan ditetapkannya cara penyimpanan yang direkomendasikan, periode
uji ulang, masa edar bahan baku aktif atau produk serta kelebihan jumlah yang
Pengujian stabilitas produk obat hendaklah dilakukan dengan cara:
1. Pengujian jangka panjang mutu produk obat untuk suatu jangka waktu yang
ditentukan, terbagi dalam beberapa interval: minimal setiap tiga bulan untuk
tahun pertama, setiap enam bulan untuk tahun kedua, serta selanjutnya
sekali setiap tahun dan dengan kondisi penyimpanan tertentu, misalnya suhu
30oC kurang lebih 2oC, kelembaban relatif 60% kurang lebih 5%.
Khususnya bahan baku aktif/produk jadi yang peka terhadap panas
hendaklah disimpan pada suhu yang lebih rendah, yang pada akhirnya akan
ditetapkan menjadi suhu penyimpanan jangka panjang. Lama periode
pengujian biasanya ditentukan oleh masa edar yang diperkirakan bagi
produk tersebut.
2. Pengujian dipercepat mutu produk selama 3 sampai 6 bulan terbagi
sedikitnya dalam empat interval waktu dengan kondisi yang diperberat,
seperti temperatur dan kelembaban tinggi, pemaparan cahaya dan
sebagainya. Dengan cara pengujian stabilitas dipercepat, laju penguraian
obat dapat diperkirakan dan stabilitas produk dapat diramalkan untuk
kondisi penyimpanan tertentu, yakni 10oC di atas suhu penyimpanan jangka
panjang dengan kelembaban yang sesuai, misalnya 40oC kurang lebih 2oC,
kelembaban relatif 75% kurang lebih 5%.
2.3.10 Pengolahan Limbah
Pengolahan limbah yang ada di Industri P.T. Kimia Farma (Persero) Tbk.
1. Pengolahan Limbah Cair
Sumber limbah cair berasal dari air cucian atau bilasan di ruang
produksi dan air cucian atau bilasan alat-alat di laboratorium.
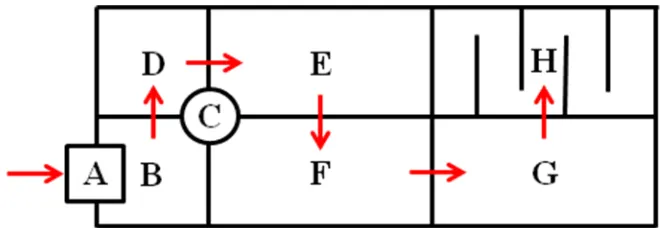
Gambar 2.1 Denah bak pengolahan limbah cair P.T. Kimia Farma (Persero) Tbk. Plant Medan.
Keterangan gambar:
A = Saluran masuk
B = Bak penampung
C = Mesin pompa
D = Bak Netralisasi
E = Bak Aerasi I
F = Bak Aerasi II
G = Bak Sedimentasi
H = Bak Biokontrol
Proses pengolahan limbah cair yaitu:
a. Limbah cair yang dikeluarkan dari ruangan melalui Saluran Masuk
(A) ditampung dalam Bak Penampungan (B)
b. Selanjutnya dipompakan dengan Mesin Pompa (C) ke Bak Netralisasi
c. Pada Bak Netralisasi (D) bila perlu, ditambahkan air kapur untuk
menetralkan limbah cair yang dikeluarkan. Selanjutnya limbah cair
yang telah netral dialirkan ke Bak Aerasi I (E)
d. Pada Bak Aerasi I (E) dilakukan aerasi dengan menggunakan aerator
yang bertujuan untuk menginjeksikan udara ke dalam bak tersebut
supaya bakteri aerob yang terdapat dalam bak tersebut dapat
melakukan penguraian bahan-bahan organik yang terdapat dalam
limbah cair tersebut. Selanjutnya juga dialirkan ke Bak Aerasi II (F).
e. Pada Bak Aerasi II (F) juga mendapat perlakuan yang sama dimana
dilakukan aerasi dengan menggunakan aerator yang bertujuan untuk
menginjeksikan udara ke dalam bak tersebut supaya bakteri aerob
yang terdapat dalam bak tersebut dapat melakukan penguraian
bahan-bahan organik yang terdapat dalam limbah cair tersebut. Lalu
dialirkan ke Bak Sedimentasi (G).
f. Pada Bak Sedimentasi (G), limbah cair tersebut didiamkan atau
diendapkan beberapa hari selanjutnya dialirkan ke Bak Biokontrol
(H).
g. Pada Bak Biokontrol (H), dilakukan pengujian terhadap hasil
2. Pengolahan Limbah Padat
Sumber limbah padat berasal dari:
a. Debu yang pada Pengumpul Debu (Dust Collector) di ruang produksi.
b. Debu yang berasal dari Pembersih Vakum (Vacuum Cleaner) yang digunakan untuk membersihkan ruangan produksi dan alat
produksi.
c. Wadah dan etiket yang rusak dari bagian pengemasan. Untuk tube
sebelum dimusnahkan harus digunting terlebih dahulu.
d. Bahan-bahan yang tidak memenuhi spesifikasi ataupun yang telah
rusak yang berasal dari bagian gudang.
Semua limbah padat tersebut dibakar oleh petugas dan sisa
pembakaran tersebut dibuang ke tempat pembuangan akhir.
2.4 Cara Pembuatan Obat yang Baik (CPOB) 2.4.1 Manajemen Mutu (Pemastian Mutu)
Pemastian mutu adalah keseluruhan sistem yang dibuat dengan tujuan agar
seluruh produk industri farmasi yang dihasilkan memenuhi persyaratan mutu yang
telah ditetapkan. Secara konseptual, Pemastian Mutu adalah pola pikir, kerja team
dan tanggung jawab setia orang dalam perusahaan sehingga tujuan mutu tercapai.
Tujuan mutu adalah jaminan terhadap khasiat, keamanan dan mutu dari produk
yang dihasilkan itu sendiri. Agar tujuan tersebut dapat tercapai, maka perlu ada
pengelolaan terhadap seluruh komponen (sumber daya) dalam industri farmasi
Pemastian mutu mencakup Cara Pembuatan Obat yang Baik (CPOB)
ditambah dengan faktor lain di luar pedoman ini seperti desain dan pengembangan
produk. Sistem pemastian mutu yang benar dan tepat bagi industri farmasi
hendaklah memastikan bahwa:
1. Desain dan pengembangan obat dilakukan dengan memperhatikan
persyaratan Cara Pembuatan Obat yang Baik (CPOB) dan semua langkah
produksi dan pengendalian diuraikan secara jelas.
2. Tanggung jawab manajerial diuraikan dengan jelas dalam uraian jabatan.
3. Pengaturan disiapkan untuk pembuatan pasokan dan penggunaan bahan
awal dan pengemas yang benar.
4. Semua pengawasan terhadap produk antara dan Pengawasan Selama Proses
(In Process Control/IPC) lainnya memenuhi persyaratan yang ditetapkan. 5. Pengkajian terhadap semua dokumen yang terkait dengan proses
pengemasan dan pengujian Bets (Batch) dilakukan sebelum memberikan pengesahan pelulusan untuk distribusi. Penilaian hendaklah meliputi semua
faktor yang relevan termasuk kondisi pembuatan, hasil dan Pengawasan
Selama Proses (In Process Control/IPC), pengkajian dokumen produksi termasuk pengemasan, pengkajian penyimpangan dari prosedur yang telah
ditetapkan, pemenuhan persyaratan dari spesifikasi produk jadi dan
pemeriksaan produk dalam kemasan akhir.
6. Obat tidak dijual atau dipasok sebelum Kepala Bagian Manajemen Mutu
peraturan lain yang berkaitan dengan aspek produksi, pengawasan mutu dan
pelulusan produk.
7. Tersedia pengaturan yang memadai untuk memastikan bahwa sedapat
mungkin produk disimpan, didistribusikan dan selanjutnya ditangani
sedemikian rupa agar mutu tetap dijaga selama masa edar atau masa simpan
obat.
8. Tersedia prosedur inspeksi diri dan audit mutu yang secara berkala
mengevaluasi efektivitas dan penerapan sistem pemastian mutu.
9. Pemasok bahan awal dan bahan pengemas dievaluasi dan disetujui untuk
memenuhi spesifikasi mutu yang telah ditentukan oleh perusahaan.
10. Penyimpangan dilaporkan, diselidiki dan dicatat.
11. Tersedia sistem persetujuan terhadap perubahan yang berdampak pada mutu
produk.
12. Prosedur pengolahan ulang dievaluasi dan disetujui.
13. Evaluasi mutu produk berkala dilakukan untuk verifikasi konsistensi proses
dan memastikan perbaikan proses yang berkesinambungan.
Cara Pembuatan Obat yang Baik (CPOB) adalah bagian dari Pemastian
Mutu yang memastikan bahwa obat dibuat dan dikendalikan secara konsisten
untuk mencapai standar mutu yang sesuai dengan tujuan penggunaan dan
dipersyaratkan dalam izin edar dan spesifikasi produk.
Persyaratan dasar dari Cara Pembuatan Obat yang Baik (CPOB) adalah:
1. Semua proses pembuatan obat dijabarkan dengan jelas, dikaji secara
menghasilkan obat yang memenuhi persyaratan mutu dan spesifikasi yang
telah ditetapkan.
2. Tahap proses yang kritis dalam pembuatan, pengawasan proses dan sarana
penunjang serta perubahannya yang signifikan divalidasi.
3. Tersedia semua sarana yang diperlukan dalam Cara Pembuatan Obat yang
Baik (CPOB) termasuk:
a. Personil yang terkualifikasi dan terlatih.
b. Bangunan dan sarana dengan luas yang memadai.
c. Peralatan dan sarana penunjang yang sesuai.
d. Bahan, wadah dan label yang benar.
4. Prosedur dan instruksi yang disetujui dan tempat penyimpanan serta sarana
transportasi yang memadai.
5. Prosedur dan instruksi ditulis dalam bentuk instruksi dengan bahasa yang
jelas, tidak bermakna ganda, dapat diterapkan secara spesifik pada sarana
yang tersedia.
6. Operator memperoleh pelatihan untuk menjalankan prosedur secara benar.
7. Pencatatan dilakukan secara manual atau dengan alat pencatat selama
pembuatan yang menunjukkan bahwa semua langkah yang dipersyaratkan
dalam prosedur dan instruksi yang ditetapkan benar-benar dilaksanakan dan
jumlah serta mutu produk yang dihasilkan sesuai dengan yang diharapkan.
8. Tiap penyimpangan dicatat secara lengkap dan diinvestigasi.
9. Catatan pembuatan termasuk distribusi yang memungkinkan penelusuran
10. Penyimpanan dan distribusi obat yang dapat memperkecil risiko terhadap
mutu obat.
11. Tersedia sistem penarikan kembali Bets (Batch) obat manapun dari peredaran.
12. Keluhan terhadap produk yang beredar dikaji, penyebab cacat mutu
diinvestigasi serta dilakukan tindakan perbaikan yang tepat dan pencegahan
pangulangan kembali keluhan.
2.4.2 Personalia
Struktur organisasi perusahaan hendaklah disusun dengan baik, sehingga
bagian produksi dan bagian pengawasan mutu dipimpin oleh orang yang berbeda
yang mempunyai tanggung jawab masing-masing. Industri farmasi bertanggung
jawab untuk menyediakan personil yang terkualifikasi dalam jumlah yang
memadai untuk melaksanakan semua tugas. Tiap personil hendaklah memahami
tanggung jawab masing-masing dan dicatat. Seluruh personil hendaklah
memahami prinsip Cara Pembuatan Obat yang Baik (CPOB) dan memperoleh
pelatihan awal dan berkesinambungan, termasuk instruksi mengenai higiene yang
berkaitan dengan pekerjaan.
Personil Kunci mencakup Kepala Bagian Produksi, Kepala Bagian
Pengawasan Mutu dan Kepala Bagian Manajemen Mutu (Pemastian Mutu). Posisi
utama tersebut dijabat oleh personil purna waktu. Kepala Bagian Produksi dan
Kepala Bagian Manajemen Mutu (Pemastian Mutu) serta Kepala Bagian
Kepala Bagian Produksi hendaklah seorang Apoteker yang terdaftar dan
terkualifikasi, memperoleh pelatihan yang sesuai, memiliki pengalaman praktis
yang memadai dalam bidang pembuatan obat dan keterampilan Manajerial
sehingga memungkinkan untuk melaksanakan tugas secara profesional. Kepala
Bagian Produksi hendaklah diberi kewenangan dan tanggung jawab penuh dalam
produksi obat.
Kepala Bagian Pengawasan Mutu hendaklah seorang Apoteker yang
terdaftar dan terkualifikasi, memperoleh pelatihan yang sesuai, memiliki
pengalaman praktis yang memadai dan keterampilan Manajerial sehingga
memungkinkan untuk melaksanakan tugas secara profesional. Kepala Bagian
Pengawasan Mutu hendaklah diberi kewenangan dan tanggung jawab penuh untuk
melaksanakan tugas yang berhubungan pengawasan mutu obat selama proses
produksi.
Kepala Bagian Manajemen Mutu (Pemastian Mutu) hendaklah seorang
Apoteker yang terdaftar dan terkualifikasi, memperoleh pelatihan yang sesuai,
memiliki pengalaman praktis yang memadai dan keterampilan Manajerial
sehingga memungkinkan untuk melaksanakan tugas secara profesional. Kepala
Bagian Manajemen Mutu (Pemastian Mutu) hendaklah diberi kewenangan dan
tanggung jawab penuh untuk melaksanakan tugas yang berhubungan dengan
sistem mutu atau pemastian mutu.
Setiap karyawan yang langsung ikut serta dalam kegiatan pembuatan obat
dan yang karena tugasnya harus memasuki daerah pembuatan obat, hendaklah
diberikan pelatihan yang sesuai dengan tugasnya maupun pelatihan Cara
berkesinambungan dengan program tertulis yang disetujui oleh Manajer Produksi,
Manajer Pengawasan Mutu dan Manajer Manajemen Mutu (Pemastian Mutu).
Pelatihan khusus diberikan kepada karyawan yang bekerja di daerah steril, di
daerah bersih, atau bagi mereka yang bekerja menggunakan bahan yang beresiko
tinggi, toksis atau yang menimbulkan alergi. Pelatihan hendaknya diberikan oleh
orang yang cakap. Dokumen pelatihan harus disimpan dengan baik dan efektifitas
program pelatihan hendaknya dinilai secara berkala.
2.4.3 Bangunan dan Fasilitas
Bangunan industri farmasi harus didirikan di daerah yang tidak ada
sumber pencemaran, misalnya bekas timbunan sampah, bahan kimia dan lain-lain.
Sumber pencemaran lainnya adalah debu jalan, debu industri lain dan partikel
pestisida. Apabila oleh karena adanya perubahan struktur tanah atau perencanaan
kota maka perlu dilakukan langkah pencegahan yang sesuai, agar pencemaran
tersebut tidak memengaruhi kualitas produk yang dibuat.
Bangunan dan fasilitas untuk pembuatan obat hendaklah memiliki desain,
konstruksi dan letak yang memadai, serta disesuaikan kondisinya dan dirawat dengan
baik untuk memudahkan pelaksanaan operasi yang benar. Tata letak dan desain
ruangan harus dibuat sedemikian rupa untuk memperkecil risiko terjadinya
kekeliruan, pencemaran silang dan kesalahan lain, dan memudahkan pembersihan,
sanitasi dan perawatan yang efektif untuk menghindari pencemaran silang,
penumpukan debu atau kotoran dan dampak lain yang dapat menurunkan mutu
Hal-hal penting yang harus dieprhatikan dalam menentukan desain dan
tata ruang bangunan industri farmasi, antara lain:
1. Kesesuaian dengan kegiatan lain, yang mungkin dilakukan dalam sarana
yang sama atau dalam sarana yang berdampingan.
2. Luasnya ruang kerja, yang memungkinkan penempatan peralatan dan
bahan-bahan secara teratur dan logis serta memungkinkan terlaksananya
kegiatan, kelancaran arus kerja, komunikasi dan pengawasan yang efektif
maupun untuk mencegah kesesakan dan ketidakteraturan.
3. Pencegahan terjadinya penggunaan kawasan produksi sebagai lalu lintas
umum bagi karyawan atau bahan-bahan ataupun sebagai tempat
penyimpanan kecuali untuk bahan-bahan yang sedang dalam proses.
4. Tata ruang harus didesain sedemikian rupa sehingga memungkinkan
kegiatan produksi dilakukan secara efektif dan efisien, mengikuti urutan
tahap produksi dan menurut kelas kebersihan yang disyaratkan.
5. Terdapat pemisahan jalan (pintu) masuk bagi karyawan dengan
bahan/barang yang dapat menyebabkan resiko pencemaran silang.
Bangunan hendaklah mendapatkan penerangan yang efektif dan mempunyai
ventilasi dengan fasilitas Sistem Pengatur Udara (Air Handling Sistem/AHS) (termasuk suhu, kelembaban dan penyaring) yang sesuai untuk kegiatan dalam
Untuk menghindari resiko terjadinya pencemaran silang antar produk,
berikut adalah hal-hal yang perlu diperhatikan sebagai persyaratan bangunan
industri farmasi, antara lain:
1. Permukaan bagian dalam ruangan harus kedap air, tidak terdapa tsambungan
atau rekatan yang dapat menyebabkan pelepasan atau pengumpulan partikel,
tidak merupakan media pertumbuhan mikroba, mudah dibersihkan serta
tahan terhadap metode pembersihan, bahan pembersih dan desinfectant yang digunakan berulang kali dengan memperhatikan faktor kepadatan, porositas,
tekstur dan sifak elektrostatik.
2. Untuk daerah pengolahan dan pengemasan harus dihindari pemakaian bahan
dari kayu
3. Pipa saluran udara dipasang di atas langit-langit atau di koridor untuk
menghindari penumpukan debu.
4. Lampu penerangan harus dipasang rata dengan langit-langit dan diberi
lapisan untuk mencegah kebocoran udara.
2.4.4 Peralatan
Peralatan yang digunakan dalam pembuatan obat harus memiliki rancang
bangun dan konstruksi yang tepat, ukuran yang memadai, ditempatkan dengan
tepat dan harus terkualifikasi sehingga mutu setiap obat terjamin secara seragam
untuk setiap bets. Hal ini berguna untuk mempermudah pembersihan dan
perwatannya.
Peralatan hendaknya dirawat menurut jadwal agar tetap berfungsi dengan
pemeliharaan dan pemakaian suatu peralatan utama hendaklah dicakup dalam
buku catatan harian yang menunjukkan Tanggal, Waktu, Kekuatan, Nomor Bets
(Batch) produk dan Jumlah Produk yang Dihasilkan yang diolah dengan peralatan tersebut serta pelaksana pembersihan.
Peralatan yang digunakan untuk menimbang, mengukur, dan menguji
harus diperiksa ketelitiannya secara teratur serta dikalibrasi menurut program dan
prosedur yang tepat. Pemasangan dan penempatan alat harus dapat mencegah
terjadinya kontaminasi silang dan cukup renggang untuk memberikan keleluasaan
kerja. Saluran air, uap dan udara bertekanan harus diatur dengan baik sehingga
kualitas ruangan dan sediaan yang baik dicapai selama kegiatan berlangsung.
2.4.5 Sanitasi dan Higiene 2.4.5.1Higiene Perorangan
1. Tiap personil yang masuk ke area pembuatan hendaklah mengenakan
pakaian pelindung yang sesuai dengan kegiatan yang dilaksanakan.
2. Prosedur higiene perorangan termasuk persyaratan untuk mengenakan
pakaian pelindung hendaklah diberlakukan bagi semua personil yang
memasuki area produksi, baik karyawan purna waktu, paruh waktu atau
bukan karyawan yang berada di area pabrik, misalnya karyawan kontraktor,
pengunjung anggota manajemen senior dan inspektur.
3. Untuk menjamin perlindungan produk dari pencemaran dan untuk
keamanan personil, hendaklah personil mengenakan pakaian pelindung yang
kotor (yang dapat dipakai ulang) hendaklah disimpan dalam wadah tertutup
hingga saat pencucian.
4. Program higiene yang rinci hendaklah dibuat dan diadaptasikan terhadap
berbagai kebutuhan di dalam area pembuatan. Program tersebut hendaklah
mencakup prosedur yang berkaitan dengan kesehatan, praktik higiene dan
pakaian pelindung personil. Prosedur hendaklah dipahami dan dipatuhi
secara ketat oleh setiap personil yang bertugas di area produksi dan
pengawasan serta pengemasan. Program higiene hendaklah dipromosikan
oleh manajemen dan dibahas secara luas selama sesi pelatihan.
5. Semua personil hendaklah menjalani pemeriksaan kesehatan pada saat
direkrut. Industri harus bertanggung jawab agar tersedia instruksi yang
memastikan bahwa keadaan kesehatan personil yang dapat mempengaruhi
mutu produk diberitahukan kepada manajemen industri. Harus dilakukan
pemeriksaan kesehatan personil secara berkala. Petugas pemeriksa visual
hendaklah menjalani pemeriksaan mata secara berkala.
6. Semua personil hendaklah menerapkan higiene perorangan yang baik.
Hendaklah mereka dilatih mengenai penerapan higiene perorangan. Semua
personil yang berhubungan dengan proses pembuatan hendaklah
memperhatikan tingkat higiene perorangan yang tinggi.
7. Tiap personil yang mengidap penyakit atau menderita luka terbuka yang
dapat merugikan mutu produk hendaklah dilarang menangani bahan awal,
bahan pengemas, bahan yang sedang diproses dan obat jadi sampai dia
8. Semua personil hendaklah diperintahkan dan didorong inisiatifnya untuk
melaporkan kepada atasan langsung tiap keadaan (pabrik, peralatan atau
personil) yang menurut penilaian mereka dapat merugikan produk.
9. Hendaklah dihindarkan persentuhan langsung antara tangan operator dengan
bahan awal, produk antara dan produk ruahan yang terbuka dan juga dengan
bagian peralatan yang bersentuhan dengan produk.
10. Personil hendaklah diinstruksikan supaya menggunakan sarana mencuci
tangan dan mencuci tangannya sebelum memasuki area produksi. Untuk
tujuan itu perlu dipasang poster yang sesuai.
11. Merokok, makan, minum, mengunyah, memelihara tanaman, menyimpan
makanan, minuman, bahan untuk merokok atau obat pribadi hanya
diperbolehkan di area tertentu dan dilarang dalam area produksi,
laboratorium, area gudang dan area lain yang mungkin berdampak terhadap
mutu produk.
2.4.5.2Sanitasi Bangunan dan Fasilitas
1. Bangunan yang digunakan untuk pembuatan obat hendaklah didesain dan
dikonstruksi dengan tepat untuk memudahkan sanitasi yang baik.
2. Hendaklah tersedia dalam jumlah yang cukup sarana toilet dengan ventilasi
yang baik dan tempat cuci bagi personil yang letaknya mudah diakses dari
area pembuatan.
3. Hendaklah disediakan sarana yang memadai untuk penyimpanan pakaian
4. Penyiapan, penyimpanan dan konsumsi makanan dan minuman hendaklah
dibatasi di area khusus, misalnya kantin. Sarana ini hendaklah memenuhi
standar sanitasi.
5. Sampah tidak boleh dibiarkan menumpuk. Sampah hendaklah dikumpulkan
di dalam wadah yang sesuai untuk dipindahkan ke tempat penampungan di
luar bangunan dan dibuang secara teratur dan berkala dengan mengindahkan
persyaratan sanitasi.
6. Rodentisida, insektisida, agen fumigasi dan bahan sanitasi tidak boleh
mencemari peralatan, bahan awal, bahan pengemas, bahan yang sedang
diproses dan/atau produk jadi.
7. Hendaklah ada prosedur tertulis untuk pemakaian rodentisida, insektisida,
agen fumigasi, pembersih dan sanitasi yang tepat. Prosedur tertulis tersebut
hendaklah disusun dan dipatuhi untuk mencegah pencemaran terhadap
peralatan, bahan awal, wadah obat, tutup wadah, bahan pengemas dan label
atau produk jadi. Rodentisida, insektisida dan fungisida hendaklah tidak
digunakan kecuali yang sudah terdaftar dan digunakan sesuai peraturan
terkait.
8. Hendaklah ada prosedur tertulis yang menunjukkan penanggung jawab
untuk sanitasi serta menguraikan dengan cukup rinci mengenai jadwal,
metode, peralatan dan bahan pembersih yang harus digunakan untuk
pembersihan sarana dan bangunan. Prosedur tertulis terkait hendaklah
9. Prosedur sanitasi hendaklah berlaku untuk pekerjaan yang dilaksanakan oleh
kontraktor atau karyawan sementara maupun karyawan purna waktu selama
pekerjaan operasional biasa.
10. Segala praktik tidak higiene di area pembuatan atau area lain yang dapat
berdampak merugikan terhadap mutu produk, hendaklah dilarang.
2.4.5.3Pembersihan dan Sanitasi Peralatan
1. Setelah digunakan, peralatan hendaklah dibersihkan baik bagian luar
maupun bagian dalam sesuai dengan prosedur yang telah ditetapkan, serta
dijaga dan disimpan dalam kondisi yang bersih. Tiap kali sebelum dipakai,
kebersihannya diperiksa untuk memastikan bahwa semua produk atau bahan
dari Bets (Batch) sebelumnya telah dihilangkan.
2. Metode pembersihan dengan cara vakum atau cara basah lebih dianjurkan.
Udara bertekanan dan sikat hendaklah digunakan dengan hati-hati dan
sedapat mungkin dihindari karena menambah risiko pencemaran produk.
3. Pembersihan dan penyimpanan peralatan yang dapat dipindah-pindahkan
dan penyimpanan bahan pembersih hendaklah dilaksanakan dalam ruangan
yang terpisah dari ruangan pengolahan.
4. Prosedur tertulis yang cukup rinci untuk pembersihan dan sanitasi peralatan
serta wadah yang digunakan dalam pembuatan obat hendaklah dibuat,
divalidasi dan ditaati. Prosedur ini hendaklah dirancang agar pencemaran
peralatan oleh agen pembersih atau sanitasi yang dicegah. Prosedur ini
setidaknya meliputi penanggung jawab pembersihan, jadwal, metode,
pembongkaran dan perakitan kembali peralatan yang mungkin diperlukan
untuk memastikan pembersihan yang benar terlaksana. Jika perlu, prosedur
juga meliputi sterilisasi peralatan, penghilangan identitas Bets (Batch) sebelumnya serta perlindungan peralatan yang telah bersih terhadap
pencemaran sebelum digunakan.
5. Catatan mengenai pelaksanaan pembersihan, sanitasi dan inspeksi sebelum
penggunaan peralatan hendaklah disimpan secara benar.
6. Disinfektan dan deterjen hendaklah dipantau terhadap pencemaran mikroba;
enceran disinfektan dan deterjen hendaklah disimpan dalam wadah yang
sebelumnya telah dibersihkan dan hendaklah disimpan untuk jangka waktu
tertentu kecuali bila disterilkan.
2.4.5.4Validasi Prosedur Pembersihan dan Sanitasi
Prosedur pembersihan sanitasi dan higiene hendaklah divalidasi dan
dievaluasi secara berkala untuk memastikan efektivitas prosedur memenuhi
persyaratan.
2.4.6 Produksi
Produksi hendaklah dilaksanakan dengan mengikuti prosedur yang telah
ditetapkan dan memenuhi ketentuan Cara Pembuatan Obat yang Baik (CPOB)
yang menjamin senantiasa menghasilkan produk yang memenuhi persyaratan
mutu serta memenuhi ketentuan izin pembuatan dan izin edar (registrasi).
Prosedur produksi hendaklah dibuat oleh penanggung jawab produksi
telah ditetapkan hendaknya dicatat pada Catatan Bets (Batch) dan bila perlu proses produksi setiap Bets (Batch) sebelumnya dievaluasi kembali.
2.4.6.1Bahan Awal
1. Setiap pemasukan, pengeluaran dan sisa bahan harus dilakukan pencatatan.
2. Pada saat diterima harus diperiksa keutuhan kemasan dan kebenaran label
dari bahan tersebut.
3. Setiap bahan awal, sebelum dinyatakan lulus untuk digunakan hendaklah
memenuhi spesifikasi bahan awal yang sudah ditetapkan yang diberi label
dengan nama yang dinyatakan dalam spesifikasi.
4. Bahan awal yang mengalami kerusakan oleh suhu disimpan di tempat yang
suhu udaranya diatur.
5. Bahan awal yang mudah terurai atau menurun potensinya harus dinyatakan
batas waktu penggunaannya.
6. Penyimpanan hendaklah dilakukan dalam ruangan atau tempat yang
suhunya diatur dan disesuaikan dengan sifat fisik dan kimia bahan tersebut.
7. Persediaan bahan awal diperiksa dalam selang waktu tertentu untuk
menyakinkan bahwa wadahnya tertutup rapat, bertanda yang benar dan
dalam kondisi yang baik pemeriksaan laboratorium kembali dilakukan
sesuai prosedur yang ditentukan.
8. Semua bahan awal yang tidak memenuhi syarat ditandai dengan jelas, di
tempatkan terpisah dan secepatnya dikembalikan ke pemasok atau
2.4.6.2 Validasi Prosedur
Studi validasi hendaklah memperkuat pelaksanaan CPOB dan dilakukan
sesuai dengan prosedur yang telah ditetapkan. Hasil validasi dan kesimpulan
hendaklah dicatat. Sebelum suatu Prosedur Pengolahan Induk ditetapkan,
hendaklah diambil langkah untuk membuktikan prosedur tersebut cocok untuk
pelaksanaan produksi rutin, dan bahwa proses yang telah ditetapkan dengan
menggunakan bahan dan peralatan yang telah ditentukan, akan senantiasa
menghasilkan produk yang memenuhi persyaratan mutu.
2.4.6.3 Pencegahan Pencemaran Silang
Pencemaran bahan awal atau produk oleh bahan atau produk lain harus
dihindarkan. Risiko pencemaran silang ini dapat timbul akibat tidak terkendalinya
debu, gas, uap, percikan atau organisme dari bahan atau produk yang sedang
diproses, dari sisa yang tertinggal pada alat dan pakaian kerja operator. Tingkat
resiko pencemaran ini tergantung dari jenis pencemar dan produk yang tercemar.
Di antara pencemar yang paling berbahaya adalah bahan yang dapat menimbulkan
sensitisasi kuat, preparat biologis yang mengandung mikroba hidup, hormon
tertentu, bahan sitotoksik dan bahan lain berpotensi tinggi. Produk yang paling
terpengaruh oleh pencemaran adalah sediaan parenteral, sediaan yang diberikan
dalam dosis besar dan/atau sediaan yang diberikan dalam jangka waktu panjang.
2.4.6.4 Sistem Penomoran Bets (Batch)
Sistem penomoran bets yang digunakan pada tahap pengolahan dan tahap
secara rinci untuk memastikan bahwa produk antara, produk ruahan, dan produk
jadi dapat dikenali dengan Nomor Bets (Batch) tertentu. Sistem penomoran ini hendaknya menjamin bahwa Nomor Bets (Batch) yang sama tidak digunakan secara berulang. Tidak diperkenankan memakai Nomor Bets (Batch) yang sama selama periode tertentu yaitu paling sedikit 10 tahun. Untuk Bets (Batch) yang diolah ulang hendaklah diberikan kode tambahan terhadap Nomor Bets (Batch) tersebut.
2.4.6.5 Penimbangan dan Penyerahan
Penimbangan atau penghitungan dan penyerahan bahan awal, bahan
pengemas, produk antara dan produk ruahan dianggap sebagai bagian dari siklus
produksi dan memerlukan dokumentasi serta rekonsiliasi yang lengkap.
Pengendalian terhadap pengeluaran bahan dan produk tersebut untuk produksi,
dari gudang, area penyerahan atau antar bagian produksi, adalah sangat penting.
Untuk menghindari terjadinya campur baur, pencemaran silang, hilangnya
identitas dan keragua-raguan, maka hanya bahan awal, produk antara dan produk
ruahan yang terkait dari satu bets saha yang boleh ditempatkan dalam area
penyerahan. Setelah penimbangan, penyerahan dan penandaan, bahan awal,
produk antara dan produk ruahan hendaklah diangkut dan disimpan dengan cara
yang benar sehingga keutuhannya tetap terjaga sampai saat pengolahan
2.4.6.6 Pengolahan
Hendaklah tidak memasukkan bahan lain selain bahan untuk Bets (Batch) yang sedang diolah tersebut. Pemantauan kondisi area pengolahan dan langkah
yang harus dilakukan sebelum memulai proses pengolahan sebaiknya
menggunakan suatu daftar periksa yang mencakup, antara lain: kondisi daerah
pengolahan harus dipantau dan dikendalikan sesuai persyaratan yang telah
ditetapkan dan peralatan harus dinyatakan bersih secara tertulis sebelum
digunakan. Kegiatan pengolahan harus mengikuti Prosedur Tetap (ProTap), dan
tiap penyimpangan harus segera dilaporkan kepada supervisor dan
didokumentasikan di dalam catatan pengolahan Bets (Batch). Semua bahan yang digunakan dalam pengolahan harus diperiksa lebih dahulu.
2.4.6.7 Pengawasan Selama Proses (In Process Control/IPC)
Pengawasan selama proses meliputi pemeriksaan terhadap proses yaitu
produk antara dan produk ruahan. Bagian pengawasan mutu akan mengawasi
bahan produk yang akan diperiksa. Pengawasan selama proses ini bertujuan untuk
mencegah terlanjur diproduksinya obat yang tidak memenuhi spesifikasi.
Pengawasan mutu selama proses produksi atau Pengawasan Selama Proses
(In Process Control/IPC) dilakukan untuk:
1. Sediaan padat, meliputi: pemeriksaan kadar zat aktif, pemeriksaan
keseragaman bobot untuk tablet dan kapsul, dilakukan beberapa kali selama
proses produksi, pemeriksaan waktu hancur, kekerasan tablet (kadar air),
sample diambil pada waktu permulaan, pertengahan, dan akhir pencetakan
2. Sediaan setengah padat, meliputi: keseragaman dan homogenitas obat,
pemeriksaan ukuran partikel, pemeriksaan tampilan, viskositas, berat jenis,
pemeriksaan berat, pemeriksaan kebocoran tube (wadah).
2.4.6.8 Pengemasan
Kegiatan pengemasan berfungsi mengemas produk ruahan menjadi produk
jadi. Proses pengemasan hendaklah dilaksanakan dibawah pengawasan ketat
untuk menjaga identitas, keutuhan, dan kualitas barang yang sudah dikemas.
Sebelum kegiatan pengemasan dimulai hendaklah dilakukan pemeriksaan untuk
memastikan bahwa peralatan dan ruang kerja dalam keadaan bersih dan bebas dari
produk dan sisa produk lain atau dokumen yang tidak diperlukan untuk kegiatan
yang dilakukan.
Sebelum menempatkan bahan pengemas pada jalur pengemasan hendaklah
diadakan pemeriksaan kesiapan jalur pengemasan yang bersangkutan oleh petugas
yang ditunjuk sesuai dengan prosedur tertulis yang ditentukan.
Pada penyelesaian proses pengemasan produk yang sudah dikemas
hendaklah diperiksa dengan teliti untuk memastikan bahwa produk obat tersebut
sesuai dengan persyaratan dalam prosedur pengemasan induk. Hanya obat jadi
yang berasal dari satu Bets (Batch) pengemasan saja yang boleh di tempatkan pada satu area. Bila ada karton yang tidak penuh maka jumlah yang ada di
dalamnya hendaklah dituliskan pada karton tersebut.
Produk dalam status karantina hendaklah diberi label “Karantina” dan
disimpan dalam rak khusus untuk karantina atau di tempat yang diberi tanda
2.4.6.9 Penyimpanan Bahan Awal, Produk Antara, Produk Ruahan dan Obat Jadi
Setiap bahan awal, produk antara, produk ruahan, dan obat jadi yang
disimpan hendaklah mempunyai kartu persediaan yang senantiasa dirujuk dan jika
terdapat penyimpangan hendaklah dicatat disertai penjelasan. Semua bahan
hendaklah disimpan secara rapi dan teratur untuk mencegah resiko tercampur atau
beresiko terjadinya pencemaran serta memudahkan pemeriksaan dan
pemeliharaan.
Semua bahan ini disimpan dengan jarak yang cukup terhadap bahan lainnya
maupun terhadap dinding, tidak diletakkan di lantai, dan dalam kondisi
lingkungan yang sesuai. Penyimpanan di luar gudang diperbolehkan bagi bahan
yang dikemas dalam wadah kedap yang mutunya tidak terpengaruh oleh suhu,
kelembaban dan faktor lainnya. Bahan yang mudah terbakar hendaklah disimpan
di gudang khusus yang letaknya terpisah sesuai dengan peraturan yang berlaku.
2.4.7 Pengawasan Mutru
Pengawasan mutu obat harus dilaksanakan melalui sistem pengawasan
yang terencana dan terpadu. Semua unsur yang terlibat dalam pembuatan obat,
baik personalia maupun kelengkapan sarana industri farmasi harus dapa
tmenunjang maksud pembuatan obat itu dan mendukung sepenuhnya persyaratan
yang diinginkan sehingga obat yang dihasilkan senantiasa memenuhi spesifikasi
Bagian Pengawasan Mutu di industri farmasi bertanggung jawab untuk
memastikan, bahwa:
1. Bahan awal untuk produksi obat memenuhi spesifikasi identitas, kekuatan,
kemurnian, kualitas dan keamanan, yang telah ditetapkan.
2. Tahapan produksi obat telah dilaksanakan sesuai dengan prosedur yang telah
ditetapkan dan telah divalidasi sebelumnya, antara lain melalui evaluasi
dokumentasi produksi terdahulu.
3. Semua pengawasan selama proses dan pemeriksaan laboratorium terhadap
suatu bets obat telah dilaksanakan dan bets tesebut memenuhi spesifikasi
yang telah ditetapkan sebelum didistribusikan.
4. Suatu bets obat memenuhi persyaratan mutunya selama waktu peredaran yang
telah ditetapkan.
Sesuai dengan ketentuan dalam Pedoman CPOB, maka Bagian
Pengawasan Mutu memiliki kewenangan khusus untuk memberikan keputusan
akhir meluluskan atau menolak atas mutu bahan baku atau produk obat maupun
hal lain yang mempengaruhi mutu obat.
2.4.8 Inspeksi Diri dan Audit Mutu
Tujuan inspeksi diri adalah untuk melakukan penilaian apakah seluruh
aspek produksi dan pengendaliaan mutu senantiasa memenuhi persyaratan Cara
Pembuatan Obat yang Baik (CPOB). Program inspeksi diri dirancang untuk
mencari kelemahan dalam pelaksanaan Cara Pembuatan Obat yang Baik (CPOB)
dan untuk menetapkan tindakan perbaikannya. Tindakan perbaikan yang
inspeksi yang mampu menilai secara objektif pelaksanaan Cara Pembuatan Obat
yang Baik (CPOB). Prosedur dan catatan mengenai inspeksi diri hendaklah
dibuat.
Untuk mendapatkan standar inspeksi diri yang maksimal dan seragam maka
disusun daftar pemeriksaan selengkap mungkin. Daftar pemeriksaan hendaklah
meliputi pertanyaan mengenai hal-hal berikut:
1. Karyawan.
2. Bangunan termasuk fasilitas untuk karyawan.
3. Penyimpanan bahan awal dan bahan jadi.
4. Peralatan.
5. Produksi.
6. Pengawasan mutu.
7. Dokumentasi.
8. Pemeliharaan gedung dan peralatan.
Manajemen hendaklah membentuk tim inspeksi diri yang paling sedikit
terdiri dari tiga anggota yang berpengalaman dalam bidangnya masing-masing
dan memahami CPOB.
2.4.9 Penanganan Keluhan Terhadap Produk, Penarikan Kembali Produk dan Produk Kembalian
Hendaklah tersedia prosedur tertulis yang merinci penyelidikan, evaluasi,
tindak lanjut yang sesuai, termasuk pertimbangan untuk penarikan kembali
produk, dalam menanggapi keluhan terhadap obat yang diduga cacat. Keluhan dan