PEMANFAATAN LIMBAH CAIR BIOETANOL MENJADI
PUPUK ORGANIK CAIR (POC)
Rommy Adeputra Lamuri, Apolonaris Ama Maran, Suratno Lourentius*, Setiyadi Jurusan Teknik Kimia, Fakultas Teknik, Universitas Katolik Widya Mandala Surabaya,
Jalan Kalijudan 37 Surabaya *E-mail: [email protected]
ABSTRAK
Pada proses pembuatan bioetanol 95% dari bahan baku tetes nira, karbohidrat atau lignoselulosa akan menghasilkan limbah cair dengan perbandingan 1 liter bioetanol:10 liter limbah cair. Perbandingan tersebut menunjukkan banyaknya limbah yang dihasilkan dengan kandungan senyawa organik yang berpotensi pada penurunan kualitas lingkungan apabila dibuang ke lingkungan tanpa dilakukan penanganan terlebih dahulu. Oleh karena itu, diperlukan suatu pengolahan yang baik dan benar, salah satunya dengan memanfaatkan EM-4 guna mendegradasi senyawa organik sehingga dapat diolah menjadi pupuk organik cair.
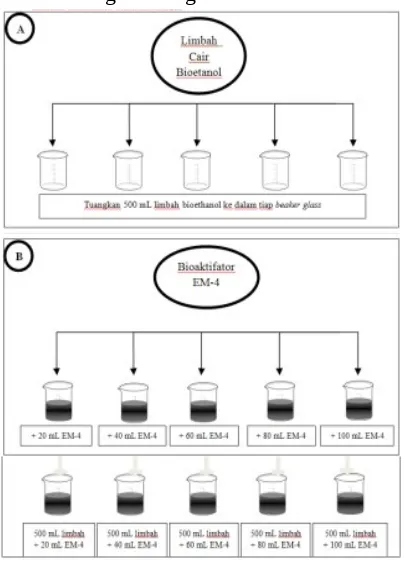
Bahan baku limbah bioetanol diperoleh dari pabrik bioetanol yakni PT. Agro Nusantara dan EM-4 (effective microorganism) diperoleh dari PT Sanggulangit Persada. Pembuatan pupuk organik cair dilakukan dengan mencampur limbah cair bioetanol sebanyak 500 mL dengan EM-4 pada volume yang divariasikan yakni; 20, 40, 60, 80 dan 100 mL, kemudian dilakukan fermentasi dengan variasi waktu 3, 6, 9, 12 dan 15 hari. Fermentasi dilakukan untuk memberi kesempatan effective microorganism (EM-4) mendegradasi senyawa-senyawa organik menjadi yang lebih sederhana, sehingga dapat meningkatkan kadar N, P dan K. Pengukuran kadar N, P, dan K dilakukan sebelum dan sesudah proses fermentasi untuk mengetahui adanya perubahan kadar. Sebelum fermentasi, kadar N diperoleh sebesar o,2447%, P2O5 sebesar 0,0733%, dan K2O sebesar 1,9188%. Setelah dilakukan fermentasi menggunakan EM-4, diperoleh kadar N, P, dan K tertinggi yaitu pada hari ke-9 dengan penambahan EM-4 sebanyak 100 mL denga kadar N sebesar 0,4178%, kadar P2O5 sebesar 0,1782% dan kadar K2O sebesar 2,1636%. Hasil tersebut menunjukkan bahwa kadar nitrogen, fosfor dan kalium sudah memenuhi syarat kadar SNI.
Kata kunci:limbah bioethanol, effective microorganism (EM-4), kadar NPK
I. Pendahuluan
Seiring dengan perkembangan teknologi, pertumbuhan penduduk dan jumlah industri yang meningkat, mengakibatkan bertambahnya jenis dan volume limbah. Salah satu industri yang limbahnya bermasalah adalah industri bioetanol. Limbah bioetanol merupakan salah satu penyebab pencemaran lingkungan yang membawa dampak buruk bagi kesehatan masyarakat. Pencemaran ini diakibatkan oleh senyawa–senyawa organik dalam limbah bioetanol yang mengalami proses penguraian oleh mikroorgsnisme dan menimbulkan pembusukan. Di daerah Bekonang Solo, limbah industri bioetanol dialirkan ke selokan mengakibatkan pencemaran terhadap lingkungan (Isroi, 2007).
Limbah bioetanol biasa disebut dengan vinasse atau stillage memiliki kandungan senyawa-senyawa organik yang
dapat dimanfaatkan dalam bidang pertanian seperti pembuatan pupuk organik. Pupuk organik merupakan jenis pupuk dengan kandungan unsur hara makro dan mikro yang tinggi sehingga dapat dimanfaatkan untuk meningkatkan produktivitas komoditas pertanian. Pupuk organik cair adalah jenis pupuk yang berbentuk cair yang mudah meresap ke dalam tanah dan mengandung unsur-unsur penting bagi kesuburan tanah. Keunggulan pupuk organik cair adalah tidak akan terjadi kelebihan kapasitas pupuk pada tanah, maka tanaman akan mudah mengatur pemupukan lebih merata (Slamet, 2005).
II. Tujuan Percobaan
Tujuan dari penelitian ini adalah mempelajari pengaruh waktu fermentasi dan penambahan Effective Microorganism 4
III. Tinjauan Pustaka
III.1. Vinasse
Pada industri bioetanol dihasilkan produk samping berupa limbah cair yang
disebut sebagai vinasse
atau stillage. Limbah vinasse pada industri bioetanol cukup melimpah tergantung kapasitas produksinya. Secara estimasi untuk memproduksi 1 liter etanol akan menghasilkan vinasse atau stillage kurang lebih 10 liter (Sumada 2013).
Menurut Khanal (2010) komposisi Unsur-unsur N, P dan K yang terkandung di dalamnya dapat dimanfaatkan sebagai pupuk cair yang memiliki harga jual lebih tinggi dari harga bioetanol.
III.2. Bioaktifator EM-4
Effective Microorganism-4
merupakan campuran mikroorganisme pengurai yang dapat membantu proses pengomposan bahan organik. EM-4 berupa larutan berwarna coklat dengan pH 3,5-4,0 dan mengandung mikroorganisme yang terdiri dari jamur fermentasi
(Aspergillus dan Penicilium), bakteri asam
laktat (Lactobacillus sp), bakteri fotosintetik (Rhodopseudomonas sp),
Actinomycetes, dan ragi (Saccharomyces
Penicilium) berperan menghasilkan
alkohol, ester dan zat-zat anti mikroba. Pertumbuhan jamur ini membantu menghilangkan bau dan mencegah serbuan serangga dan ulat-ulat merugikan dengan cara menghilangkan penyediaan makanannya.
2. Bakteri asam laktat (Lactobacillus sp) berperan dalam menekan pertumbuhan mikroorganisme yang merugikan; meningkatkan percepatan perombakan bahan organik; menghancurkan bahan organik seperti lignin dan selulosa serta membantu proses fermentasi tanpa menimbulkan senyawa beracun yang ditimbulkan dari pembusukan bahan organik.
3. Bakteri fotosintetik ( Rhodopseudo-monas sp) menghasilkan zat-zat yang bermanfaat seperti, asam amino, asam nukleat dan zat bioaktif yang berguna bagi pertumbuhan dan perkembangan tanaman.
4. Actinomycetes menghasilkan zat-zat
anti mikroba dari asam amino yang dihasilkan bakteri fotosintetik. Zat-zat anti mikroba ini menekan pertumbuhan jamur dan bakteri berbahaya.
5. Ragi/yeast (Saccharomyces sp) akan menghasilkan senyawa-senyawa yang bermanfaat bagi pertumbuhan tanaman dari asam amino dan gula yang dikeluarkan oleh bakteri fotosintetik dan bahan organic. Ragi menghasilkan zat-zat bioaktif seperti hormon dan enzim untuk meningkatkan jumlah sel aktif dan perkembangan akar. Sekresi ragi adalah substrat yang baik untuk bakteri asam laktat dan Actinomycetes.
Secara umum, EM-4 bermanfaat untuk mempercepat pengomposan sampah organik dan kotoran hewan, memperbaiki sifat fisik, kimia dan biologis tanah, serta meningkatkan ketersediaan nutrisi dan senyawa organik dalam tanah. Pengomposan atau penguraian tersebut akan menghasilkan bahan organik seperti; asam amino, protein, karbohidrat dan vitamin yang mudah diserap oleh akar tanaman (Utomo, 2007).
Mikroorganisme yang ada di dalam EM-4 mengurai bahan organik dan substrat yang berasal dari proses pembuatan bioetanol dengan reaksi sebagai berikut:
CxHyOzN2S+mikroorganisme+O2
CO2+H2O+NH3 + CxHyOzN (1)
3(NH4)2SO4+ mikroorganisme
6H2O + N2 + 4NH3 + 3SO2 (2)
2NaH2PO4 +mikroorganisme
P2O5 + 2NaOH + H2O (3)
K2SO4 + mikroorganisme
K2O + SO3 (4)
Reaksi dekomposisi senyawa organik atau subtrat tersebut menghasilkan NH3
yang menunjukan lingkungan bersifat basa serta K2O dan P2O5 (Effendi, 2003).
III.3. Pupuk Organik
Pupuk organik adalah pupuk yang sebagian besar atau seluruhnya terdiri atas senyawa-senyawa organik yang pada umumnya berasal dari tanaman dan dalam jumlah sedikit dapat ditemukan dalam kotoran. Dalam proses pengolahannya, pupuk organik dapat berupa padat maupun cair dan dapat digunakan sebagai agen pensuplai bahan organik untuk memperbaiki sifat fisik, kimia dan biologi tanah (Simanungkalit, 2006).
Menurut Fitri dkk (2007) Pupuk organik cair mempunyai beberapa manfaat diantaranya adalah:
1. Dapat mendorong dan meningkatkan pembentukan klorofil daun dan pembentukan bintil akar pada tanaman
leguminosae, sehingga meningkatkan
kemampuan fotosintesis tanaman dan penyerapan nitrogen dari udara; 2. Dapat meningkatkan vigor tanaman
sehingga tanaman menjadi kokoh dan kuat, meningkatkan daya tahan tanaman terhadap kekeringan dan serangan patogen penyebab penyakit; 3. Merangsang pertumbuhan cabang
tanaman;
4. Meningkatkan pembentukan bunga dan bakal buah;
5. Mengurangi gugurnya daun, bunga dan bakal buah.
III.4. Nitrogen
Nitrogen (N) merupakan unsur hara yang penting bagi tumbuhan karena
bermanfaat merangsang pertumbuhan bagian vegetatif tanaman yaitu akar, batang dan daun. Kandungan nitrogen pada tanaman dalam jumlah berlebih dalam tanaman dapat mengakibatkan
terhambatnya pembungaan dan
pembuahan tanaman. Selain itu, nitrogen juga mempunyai fungsi sebagai peningkat kadar protein (Sutedjo, 2002).
III.5. Fosfor
Fosfor (P) merupakan unsur hara yang diperlukan tumbuhan dalam jumlah besar (hara makro). Dalam tubuh tumbuhan, fosfor dapat dijumpai dalam bentuk phitin, nuklein dan fostide yang merupakan bagian dari protoplasma dan inti sel. Biasanya fosfor diambil tanaman dari tanah dalam bentuk H2PO4- dan
HPO42-. Fosfor bermanfaat dalam
mempercepat pertumbuhan akar semai, mempercepat pertumbuhan tanaman muda menjadi tanaman dewasa, mempercepat pembungaan dan pemasakan buah biji serta meningkatkan produksi biji-biji (Sutedjo, 2002).
III.6. Kalium
Kalium merupakan unsur hara kedua terbanyak setelah nitrogen. Kalium mempunyai valensi satu dan diserap tanaman dari tanah dalam bentuk ion K+.
Unsur K sangat berlimpah dan mempunyai energi hidrasi rendah sehingga tidak menyebabkan polarisasi molekul air. Peran kalium bagi tanaman adalah membentuk protein dan karbohidrat, meningkatkan ketahanan tanaman terhadap penyakit serta meningkatkan kualitas biji maupun buah (Sutedjo, 2002).
III.7. Metode Kjeldahl
Metode Kjeldahl merupakan metode yang sederhana untuk penetapan nitrogen total pada asam amino, protein dan senyawa yang mengandung nitrogen.
ammonia. Selanjutnya jumlah nitrogen yang terlepas sebagai amonia dihitung dan dikonversikan ke dalam kadar protein dengan mengalikan konstanta tertentu.
III.8. Analisis Spektrofotometri
Spektrofotometri merupakan suatu metode analisis yang didasarkan pada pengukuran serapan sinar monokromatis oleh suatu larutan berwarna pada panjang gelombang spesifik dengan menggunakan radiasi maupun pengukuran absorbsi terisolasi pada suatu panjang gelombang tertentu (Clark, 1993).
Penentuan kadar Fosfor (P) dilakukan dengan menggunakan alat spektrofotometri UV-VIS. Absorbansi dari larutan sampel yang diukur dengan spektrofotometer UV-Vis digunakan untuk mengukur intensitas sinar yang dilalui menuju sampel (I) dan membadingkannya dengan intensitas sinar sebelum dilewatkan ke sampel tersebut (Io). Rasio I/Io disebut transmitansi (T), sedangkan Lambert Beer (Underwood, 2002).
Penentuan kadar kalium dilakukan menggunakan metode spektrofotometri dengan alat spektrofotometer serapan atom (SSA). Alat ini biasa digunakan dalam penentuan unsur-unsur logam dan metaloid yang prinsip pengukurannya berdasarkan penyerapan cahaya dengan panjang gelombang tertentu oleh atom logam dalam keadaan bebas. Metode ini sangat tepat untuk analisis zat pada konsentrasi rendah (Skoog, 2002).
III.8. Standar Nasional Indonesia (SNI) Pupuk Organik
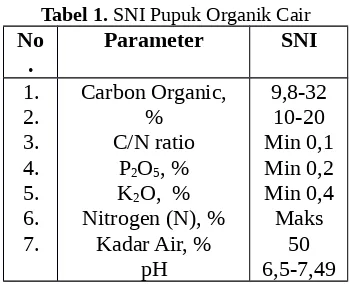
Menurut Wahyuningsih (2009), Standar Nasional Indonesia pada tahun 2004 untuk Pupuk Organik Cair adalah sebagai berikut:
Tabel 1. SNI Pupuk Organik Cair No
Variabel berubah pada penelitian ini adalah volume bioaktifator EM-4 (20, 40, 60, 80 dan 100 mL) dan waktu fermentasi (3, 6, 9, 12 dan 15 hari).
IV.2. Prosedur Penelitian
Limbah cair bioetanol sebagai bahan baku utama pada penelitian ini disaring untuk memisahkan kotoran padat dan dilakukan analisis kadar N, P, K pada limbah tersebut sebagai faktor pembanding terhadap kadar N, P, K setelah difermentasi.
mL. Masing-masing sampel diaduk dengan menggunakan pengaduk hingga
tercampur sempurna.
Sampel akan mengalami proses fermentasi oleh mikroorganisme yang terkandung di dalam EM-4 selama beberapa hari, kemudian dihitung kadar N, P dan K pada hari ke 3, 6, 9, 12 dan 15. Analisis kadar N pada sampel dengan menggunakan metode Kjeldahl, kadar
P2O5 dengan menggunakan
Spektrofotometer UV-Vis, dan kadar K2O
menggunakan Spekrofotometer Serapan Atom. Kadar N, P, K hasil penelitian dibandingkan dengan kadar SNI.
Gambar 1. Prosedur Percobaan
V. Hasil Penelitian dan Pembahasan V.1. Analisis Pretreatment
Pada tahap awal penelitian ini dilakukan analisis mengenai karakteristik
dan kualitas limbah yakni berkaitan dengan warna, tekstur, bau, pH, dan kadar kandungan hara (N, P, dan K). Analisis ini dijadikan sebagai parameter atau pembanding sifat dan karakteristik limbah setelah dilakukan pengomposan.
Tabel 2. Hasil analisis karakteristik limbah cair bioethanol
Selain itu dilakukan analisis kadar hara N, P, dan K yang terkandung dalam limbah bioetanol sebelum dilakukan pengomposan.
Tabel 3. Hasil analisis kadar hara NPK sebelum fermentasi
V.2.Hasil Analisis Kadar N, P2O5, dan K2O
pada Penambahan EM-4 60 mL
Hasil analisis kadar N, P2O5, dan K2O
pada penambahan EM-4 60 mL ditunjukan pada table berikut:
Tabel 4. Hasil Analisis Kadar N, P2O5, dan K2O pada Penambahan EM-4 60 mL
Karakteristi
k Hasil Analisis
Warna Bau Tekstur
pH
coklat tua kurang sedap pekat, tidak terlalu kental
8,53
Kandungan Hara Kadar (%) Nitrogen (N)
Fosfor dalam P2O5
Kalium dalam K2O
0,2447 0,0733 0,9188
Sampel Hari
ke-Kadar N (%)
Kadar P2O5
(%)
Kadar K2O
(%) Limbah
bioetanol 0 0,2447 0,0733 1,9188
(500 mL limbah boetanol + 60 mL EM-4)
3 0,2907 0,0883 2,1153
6 0,3506 0,1274 2,3177
9 0,3643 0,1694 2,0102
12 0,3290 0,1371 1,9681
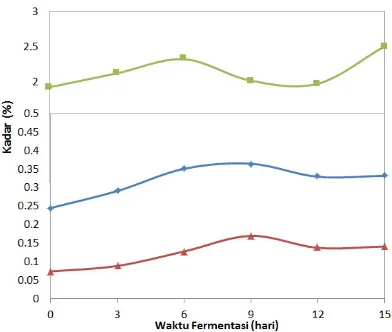
Gambar 2. Hasil Analisis Kadar N, P2O5, dan K2O pada Penambahan EM-4 60 mL
Dari hasil di atas, terlihat bahwa kadar N, P2O5 dan K2O mengalami
perubahan setelah ditambahkan effective
microorganism (EM-4). Hal ini
menunjukkan adanya pengaruh EM-4 dalam meningkatkan kadar N, P2O5, dan
K2O. Perubahan kadar tersebut akan
semakin jelas terlihat dengan adanya pengaruh waktu fermentasi, seperti yang ditunjukkan pada tabel 4 atau pada gambar 2 di atas.
Kadar N dan P2O5 mengalami
kenaikan pada hari ke-3 dan terus berlanjut hingga hari ke-9. Namun, pada hari ke-12 mengalami penurunan dan meningkat lagi pada hari ke-15 meskipun kadar yang diperoleh lebih kecil daripada perolehan pada hari ke-9. Perolehan kadar N dan P2O5
tertinggi yaitu pada hari ke-9 yang menunjukkan bahwa mikroorganisme bekerja secara optimal pada hari ke-9 dan menurunnya kadar pada hari ke-12 disebabkan karena makanan untuk mikroorganisme mulai berkurang sehingga kinerja mikrorganisme juga akan semakin menurun.
Kadar K2O mengalami kenaikkan
hingga hari 6 dan menurun pada hari ke-9 dan 12, namun meningkat lagi pada hari ke-15. Perolehan kadar K2O yang tidak
stabil tersebut menunjukkan adanya kinerja mikroorganisme yang masih berlanjut meskipun sempat mengalami penurunan.
Hasil menunjukan kadar N dan P2O5
megalami penurunan pada hari ke-12, bukan berarti kinerja semua mikroorganisme menurun melainkan masih ada beberapa mikroorganisme yang bekerja terutama dalam meningkatkan kadar K2O.
Oleh karena itu, secara keseluruhan, kadar N, P2O5 dan K2O terbaik diperoleh pada
hari ke-9, sehingga hari ke-9 dapat ditetapkan sebagai waktu optimum untuk menghasilkan kadar N, P2O5 dan K2O
dengan kadar N sebesar 0,3643%, kadar P2O5 sebasar 0,1694% dan kadar K2O
sebesar 2,0102%.
V.3. Hasil Pengukuran Kadar N, P2O5, dan K2O
pada Hari ke-9
Hasil Pengukuran Kadar N, P2O5, dan
K2O pada Hari ke-9 ditunjukan pada table
berikut:
Tabel 5. Hasil Analisis Kadar N, P2O5, dan K2O pada Penambahan EM-4 60 mL
Sampel
Penambahan Volume
EM-4
Kadar N (%) Limbah
bioetanol 0 0,2447
Hari ke-9
20 40 60 80 100
0,2667 0,3071 0,3643 0,4001 0,4178
Lanjutan table 5. Sampel Kadar P2O5
(%)
Kadar K2O
(%) Limbah
bioetanol 0,0733 1,9188
Hari ke-9
0,1820 0,1825 0,1694 0,1698 0,1782
2,1701 2,0485 2,0102 2,0536 2,1636
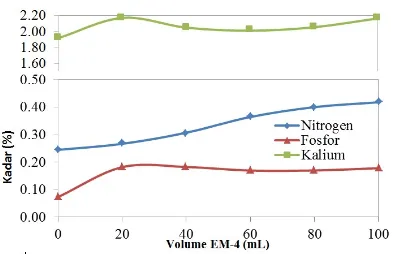
Gambar 3. Hasil Analisis Kadar N, P2O5, dan K2O pada Penambahan EM-4 60 mL
Dari hasil pengukuran di atas, terlihat bahwa setiap perlakuan pada sampel limbah bioetanol mengalami perubahan kadar baik N, P2O5, maupun K2O. Perubahan tersebut
menunjukkan adanya aktivitas
mikroorganisme dalam mendegradasi atau mengurai senyawa organik. Pada dasarnya, semakin banyaknya EM-4 yang ditambahkan maka semakin banyak mikroorganisme yang mendegradasi senyawa organik sehingga perolehan kadar N, P2O5 dan K2O akan semakin meningkat.
Perolehan kadar N selalu mengalami peningkatan seiring dengan semakin banyaknya EM-4 yang ditambahkan. Namun, hal tersebut berbedah dengan perolehan kadar P2O5 dan K2O. Kadar P2O5
meningkat pada penambahan EM-4 sebanyak 20 mL dan 40 mL, menurun pada penambahan 40 mL dan 80 mL, dan meningkat lagi pada penambahan 100 mL. Sedangkan, kadar K2O meningkat pada
penambahan EM-4 sebanyak 20 mL, menurun pada penambahan 40 mL dan 60 mL, namun meningkat lagi pada penambahan 80 mL dan 100 mL. Perolehan kadar P2O5 dan K2O yang kurang stabil
tersebut menunjukkan adanya aktivitas mikroorganisme yang tidak hanya mendegradasi senyawa organik dan meningkatkan kadar N, P2O5 dan K2O
melainkan juga mengkonsumsi senyawa organik tersebut karena dianggap sebagai nutrisi sehingga dapat mengurangi kadar P2O5 dan K2O.
Secara keseluruhan, kadar N, P2O5 dan
K2O terbaik diperoleh pada penambahan
EM-4 sebanyak 100 mL. Hal ini menunjukkan bahwa proses fermentasi limbah bioetanol untuk menghasilkan kadar N, P2O5, dan K2O tertinggi diperoleh pada
hari ke-9 dengan penambahan EM-4 sebanyak 100 mL, dengan kadar N sebesar 0,4178%, kadar P2O5 sebesar 0,1782% dan
kadar K2O sebesar 2,1636%. Hasil yang
diperoleh tersebut sudah memenuhi syarat kadar SNI, yakni untuk N minimal 0,4%, P2O5 minimal 0,1%, dan K2O minimal 0,2%.
Kesimpulan
Dari hasil penelitian yang telah dilakukan, kesimpulan yang diperoleh adalah sebagai berikut:
1. Adanya pengaruh waktu terhadap peningkatan kadar N,P, dan K dalam pengomposan limbah bioetanol dan diperoleh kadar N, P, dan K tertinggi pada fermentasi hari ke-9 dengan kadar N sebesar 0,3643%, kadar P2O5 sebasar 0,1694% dan kadar K2O
sebesar 2,0102%.
2. Adanya pengaruh penambahan Effective
Microorganism-4 (EM-4) terhadap
peningkatan kadar N, P dan K dalam pengomposan limbah bioetanol dan diperoleh kadar N,P dan K tertinggi pada penambahan EM-4 sebanyak 100 mL dengan kadar N sebesar 0,4178%, kadar P2O5 sebesar
0,1782% dan kadar K2O sebesar 2,1636%.
Daftar Pustaka
Badan Standarisasi Nasional. 2010. Pupuk NPK Padat. SNI 2803:2010.
Clark, B.J. 1993. UV Spectroscopy Techniques Instrumentations, Data Handling.Chapman & Hall.London.
Day, R. A. and A. L. Underwood. 2002. Analisis Kimia Kuantitatif. Edisi Keenam. Jakarta: Erlangga.
Djuarnani dkk. 2005. Cara Cepat Membuat Kompos. Jakarta: AgroMedia Pustaka. Effendi, H. 2003. Telaan Kualitas Air Bagi
Isroi. 2007. Pupuk Organik Cair (POC) dari Limbah Bioetanol. http://isroi.com/2009 / 07/29/pupuk-organik-cair-POC-dari-limbah-bioetanol. [30 September 2015]. Mengel, K and A, Kirby. 1987. Principles of
plant nutrition. 4th ed. Switzerland :International Potash Inst.
Risqiani, Nur Fitri dkk. 2007. Pengaruh Dosis dan Frekuensi Pemberian Pupuk Organik Cair Terhadap Pertumbuhan dan Hasil Buncis (Phaseolus vulgaris.) Dataran Rendah: Jurnal Ilmu Tanah dan Lingkungan Vol. 7 No.1 (2007).
Skoog. D. A., Donald M. West, F. James Holler, Stanley R. Crouch, 2000. Fundamentals of Analytical Chemistry. Hardcover. Publisher: Brooks Cole.
Slamet, Widyati, E.D Purbayanti, C.I. Sutrisno. 2005. Pemanfaatan Limbah Rumah Potong Hewan (RPH) dan Limbah Industri Minuman Teh untuk Kompos. Tropika Jurnal Penelitian Pertanian. Fakultas Pertanian Universitas Muhammadiyah. Malang.
Sumada, Ketut.2013. Pemanfaatan Limbah Cair Indrustri Etanol (Vinasse) sebagai Pupuk. http://ketutsumada.blogspot .co.id/2013/01/ pemanfaatan-vinasse-limbah-cair.html, [28 November 2015].
Suriadikarta dan Simanungkalit, 2006. Pupuk Organik dan Pupuk Hayati. Balai Besar Penelitian dan Pengembangan Sumberdaya
Lahan Pertanian. Bogor.
http//balittanah.litbang.deptan.go.id. [01 oktober 2015].
Sutedjo, M. 2002. Pupuk dan Cara Pemupukan. Jakarta: Rineka Cipta.
Utomo, A.S.W. 2007. Pembuatan Kompos dengan Limbah Organik. Jakarta;Sinar Cemerlang Abadi.
Wahyuningsih dan Supriyo. 2009. Teknologi Produksi Pupuk Organik Cair dari Limbah Sampah Rumah Tangga di Kelurahan Lempongsari, Lodya Semarang dengan Komposer EM-4