PENGARUH PENAMBAHAN CAHAYA KONTINU
TERHADAP PRODUKTIVITAS TANAMAN
KARET RAKYAT (Hevea Brasiliensis Muell Arg.)
DI TANJUNG JABUNG BARAT, PROVINSI JAMBI
ENDANG RUSPARYATI
DEPARTEMEN AGRONOMI DAN HORTIKULTURA
FAKULTAS PERTANIAN
INSTITUT PERTANIAN BOGOR
2012
ABSTRACT This research is to know the relations of continous light to rubber plants’ productivity, located in West Tanjung Jabung, Jambi. This is an uncontrolled research with research spots taken at 225 m, 275 m, 325 m, 375 m, 425 m, 475 m, 525 m, 600 m, 700 m, and 800 m distances from flare. There are four rubber plants taken on each spots and flare is the light source researched. The variables observed on this research are rubbers production, light (illuminations, irradiations, UV, and quantum) splitted to day observation to the sunlight and night observation to the flare light. Other observation done on this research are weeds’ vegetation analysis, soil and air temperature observation, and soil analysis. Results on this research is the increase of contionus flare has no impact to the rubber plants productivity, because the observe value on the night observations show that illumination value is about 0,001-0,004 watt/m2, but the value of UV, irradiations and quantum shows zero point. Productivity of rubber plant is affected by the age of the plant and klon used as a seed, no treatment, no weeds’ control, and soil structure.The most influential factors in the production rubber clones GT and AVROS is the nutrient content of the soil, soil texture, soil pH, the amount of weeds, and the growth of rubber trees. In clone LCB factors affecting production are soil nutrient content, soil texture, soil pH, the amount of weeds, and the growth of rubber trees. Keyword : rubber, light, flare, illumination, irradiation , UV, dan Quantum
RINGKASAN
ENDANG RUSPARYATI. Pengaruh Penambahan Cahaya Kontinu
Terhadap Produktivitas Tanaman Karet Rakyat (Hevea Brasiliensis Muell
Arg.) Di Tanjung Jabung Barat, Provinsi Jambi. (Dibimbing oleh
HERDATA AGUSTA)
Percobaan ini dilaksanakan untuk mengetahui hubungan antara penambahan cahaya kontinu dan produktivitas tanaman karet. Cahaya kontinu berasal dari flare. Flare perupakan cerobong panjang yang dialiri gas dan dibakar diatasnya. Penelitian dilaksanakan di Tanjung Jabung Barat, Jambi. Penelitian dilaksanakan dari bulan Februari sampai Juni 2011. Percobaan yang dilakukan di lapang bukan merupakan percobaan yang terkontrol, tetapi merupakan bentuk percobaan observasional. Contoh tanaman yang diamati diambil sesuai dengan jarak tanaman dengan flare. Percobaan dilakukan pada jarak 225m, 275m, 325m, 375m, 425m, 475m, 525m, 600m, 700m, dan 800m dari flare. Setiap titik diambil empat tanaman, sehingga terdapat 40 tanaman contoh. Selain mengambil contoh tanaman, juga dilakukan pengamatan nilai cahaya matahari dan cahaya api biru dari flare. Pengamatan cahaya flare dilakukan pada titik 10 m, 25 m, 50 m, 75 m, 100 m, 125 m, dan 150 m dari flare. Rata-rata nilai iluminasi pada bulan Februari sebesar 21 166 lux, pada bulan Maret sebesar 16 568 lux, dan untuk bulan Juni sebesar 18 684 lux, nilai iluminasi yang paling besar pada bulan Februari. Rata-rata nilai UV pada bulan Februari sebesar 1 mw/cm2, pada bulan Maret sebesar 1.38 mw/cm2, dan untuk bulan Juni sebesar 1.5 mw/cm2, nilai UV yang paling besar adalah pada bulan Juni. Nilai ilumnasi berbeda dengan nilai UV. Rata-rata nilai iradiasi pada bulan Februari sebesar 34 watt/m2/menit, pada bulan Maret sebesar 28.67 watt/m2/menit, dan untuk bulan Juni sebesar 32.72 watt/m2/menit, nilai iradiasi yang paling besar adalah pada bulan Juni. Rata-rata nilai kuantum pada bulan Februari sebesar 563 µEinstein s-1m-2, pada bulan Maret sebesar 572.6 µEinstein s-1m-2, sedangkan pada bulan juni tidak dilakukan pengukuran nilai kuantum
karena tidak tersedianya peralatan alat. Nilai iradiasi cahaya flare pada malam hari pada jarak 10 – 150 m dari cerobong flare sebesar 0.001 watt/m2, sedangkan pada jarak 225 m nilai irradiasi sebesar 0 watt/m2. Hal ini menunjukan bahwa iradiasi cahaya tidak berpengaruh terhadap tanaman karet. Lahan yang digunakan dalam penelitian merupakan kebun karet rakyat yang berada di Betara Tanjung Jabung Barat, Provinsi Jambi. Tinggi permukaan tanah adalah 17 meter diatas permukaan laut, sehingga tanah banyak mengandung pasir. Jenis tanah berkolerasi positif terhadap permeabilitas air, sehingga penguapan air lebih cepat dan pada musim kemarau mengalami kekeringan. Terdapat 3 varietas yang ditanam di perkebunan karet rakyat ini, yaitu GT (Gondang Tapen), Avros (Algemene Vereniging Rubber Planters Oostkust Sumatra), dan LCB. Pada klon GT produksi tanaman karet termasuk rendah, hanya berkisar antara 3.12 – 17.80 kg / ha / hari. jika dibandingkan dengan produktivitas klon GT sebesar 20 kg/ha/hari. Produksi pada klon AVROS juga terbilang rendah dengan produksi anara 4.08 – 6.94 kg/ha/hari dibandingkan dengan produktivitas klon AVROS yang dapat mencapai 15 kg/ha/hari. Pada klon LCB dikatakan rendah dengan produksi sebesar 0.58 dan 1.54 kg/ha/hari jika dibandingkan dengan produktivitas klon LCB sebesar 15 kg/ha/hari. Produksi yang rendah pada klon LCB karena karet belum matang sadap, sehingga lateks yang dihasilkan belum maksimal. Faktor yang berpengaruh terhadap produksi lateks tiga klon tersebut adalah kandungan hara tanah, tekstur tanah , pH tanah, jumlah gulma, dan pertumbuhan tanaman karet.
PENGARUH PENAMBAHAN CAHAYA KONTINU
TERHADAP PRODUKTIVITAS TANAMAN
KARET RAKYAT (Hevea Brasiliensis Muell Arg.)
DI TANJUNG JABUNG BARAT, PROVINSI JAMBI
Skripsi sebagai salah satu syarat untuk memperoleh gelar Sarjana Pertanian pada Fakultas Pertanian Institut pertanian BogorENDANG RUSPARYATI
A24070061
DEPARTEMEN AGRONOMI DAN HORTIKULTURA
FAKULTAS PERTANIAN
INSTITUT PERTANIAN BOGOR
2012
Judul : PENGARUH PENAMBAHAN CAHAYA KONTINU TERHADAP
PRODUKTIVITAS TANAMAN KARET RAKYAT (Hevea
Brasiliensis Muell Arg.) DI TANJUNG JABUNG BARAT, PROVINSI JAMBI Nama : Endang Rusparyati NIM : A24070061 Menyetujui, Pembimbing Dr. Ir. Herdhata Agusta NIP. 19590813 198303 1 003 Mengetahui, Ketua Departemen Agronomi dan Hortikultura Dr. Ir. Agus Purwito, MSc. Agr. NIP. 1961110 198703 1 003 Tanggal Lulus:……..
RIWAYAT HIDUP
Penulis dilahirkan di kota Pamekasan pada tanggal 24 Januari 1989 sebagai anak pertama dari dua bersaudara dari Bapak Hafid dan ibu Hairiyah. Tingkat pendidikan dasar ditempuh oleh penulis selama 6 tahun dan selesai pada tahun 2001 di Sekolah Dasar Tobungan II, Galis, Pamekasan. Selain Sekolah dasar, penulis juga bersekolah di Madrasah Ibtidaiyah Nasyatus Sibyan yang ditempuh selama 7 tahun dan lulus pada tahun 2002. Pendidikan lanjut tingkat pertama diselesaikan di SLTP 5 Pamekasan pada tahun 2004. Pendidikan tingkat menengah diselesaikan pada tahun 2007 di SMA Negeri 2 Pamekasan. Penulis menjadi pengurus OSIS SMA tahun 2006 sebagai ketua divisi Demokrasi, HAM, Pendidikan Politik, Lingkungan Hidup, Kepekaan dan Toleransi. Penulis diterima di Institut Pertanian Bogor pada tahun 2007 melalui Undangan Seleksi Masuk IPB (USMI). Penulis memilih jurusan Agronomi dan Hortikultura. Penulis juga mengikuti beberapa kegiatan yang dilaksanakan oleh departemen Agronomi dan Hortikultura seperti TEGAR II sebagai seksi LKTI. Saat ini penulis menjadi salah satu staf pengajar di bimbingan belajar Mitra Siswa.KATA PENGANTAR
Puji syukur penulis panjatkan kehadirat Alah SWT. atas rahmat dan karunia-Nyalah penulis dapat menyelesaikan skipsi yang berjudul “Pengaruh Penambahan Cahaya Kontinu Terhadap Produktivitas Tanaman Karet Rakyat (Hevea Brasiliensis Muell Arg.) Di Tanjung Jabung Barat, Provinsi Jambi”. Pada kesempatan ini penulis juga ingin mengucapkan terimakasih kepada: 1. Dr. Ir. Herdhata Agusta sebagai dosen pembimbing skripsi yang telah memberikan masukan, saran, dan dana selama Penulis melakukan penelan. 2. Bapak Tarmidzi, Amroni, Mbak Devi serta seluruh staf Betara Gas Plant, Jambi yang telah banyak membantu Penulis dalam melakukan penelitian. 3. Bapak, Ibu, Adik dan saudara-saudara penulis yang telah meberikan doa dan kasih sayang selama penulis menyelesaikan studi. 4. Teman-teman AGH 44 dan semua yang telah membantu penelitian ini yang berupa bantuan tenaga dan dukungan dan pikiran selama percobaan berlangsung. 5. Warga Whardhatul Jannah dan para anggota GASISMA yang telah memberikan dukungan dan semangat untuk segera menyelesaikan skripsi. Penulis berharap semoga skripsi ini memberi manfaat bagi ilmu pengetahuan dan bagi pembacanya. Bogor, Juli 2012 PenulisDAFTAR ISI
Halaman DAFTAR ISI... i DAFTAR TABEL... ii DAFTAR GAMBAR ... iii DAFTAR LAMPIRAN ... iv PENDAHULUAN ... 1 Latar Belakang ... 1 Tujuan... 2 Hipotesis ... 2 TINJAUAN PUSTAKA ... 3 Karakteristik Karet ... 3 Lateks ... 3 Cahaya Kontinu ... 5 Analisis Komponen Utama ... 6 BAHAN DAN METODE ... 8 Tempat dan Waktu Percobaan... 8 Bahan dan Alat ... 8 Metode Pelaksanaan ... 13 Pelaksanaan Penelitian ... 14 HASIL DAN PEMBAHASAN... 24 Kondisi Umum ... 24 Parameter Cahaya Pada Siang Hari... 27 Pengamatan Bulan Februari... 27 Pengamatan Bulan Maret... 29 Pengamatan Bulan Juni... 32 Pengamatan Pada Malam Hari ... 35 Pengukuran Suhu Tanah dan Udara Pada Siang Hari... 36 Pengukuran Suhu Tanah Pada Malam Hari ... 37 Kecepatan Angin ... 38 Jumlah gas yang dibakar ... 39 Pengamatan Gulma... 40 Pengamatan Tanah ... 43 Produktifitas Tanaman Karet... 46 Analisis Komponen Utama ... 50 KESIMPULAN DAN SARAN... 57 Kesimpulan... 57 Saran ... 57 DAFTAR PUSTAKA ... 58 LAMPIRAN ... 61DAFTAR TABEL
Nomor Halaman 1. Deret Standar Campuran Kepekatan K, Na, Ca, dan Mg... 11 2. Populasi Tanaman Setiap Titik Sampel ... 26 3. Kondisi Gulma pada Klon GT ... 41 4. Kondisi Gulma pada Klon Avros... 42 5. Kondisi Gulma pada Klon LCB... 43 6. Hasil Analisis Hara Mikro Tanah ... 44 7. Hasil Analisis Fisika Tanah (Titik 225) ... 46 8. Hasil Produksi Tanaman Karet ... 48 9. Nilai Ciri 5 Komponen Utama dari 26 Karakter pada Klon GT ... 50 10. Nilai Ciri 5 Komponen Utama dari 26 Karakter pada Klon AVROS... 53 11. Nilai Ciri 3 Komponen Utama dari 26 Karakter pada Klon LCB ... 55DAFTAR GAMBAR
Nomor Halaman 1. Flare Api Biru ... 24 2. Penampakan Batang Karet ... 25 3. Nilai Iluminasi Bulan Februari 2011 ... 28 4. Nilai Sinar UV Bulan Februari 2011 ... 28 5. Iradiasi Cahaya Bulan Februari 2011... 29 6. Kuantum Cahaya Bulan Februari 2011... 29 7. Nilai Iluminasi Bulan Maret 2011 ... 30 8. Nilai Cahaya UV Bulan Maret 2011 ... 30 9. Nilai Iradiasi Cahaya Bulan Maret 2011... 31 10. Nilai Kuantum Cahaya Bulan Maret 2011... 32 11. Nilai Iluminasi Cahaya 14 Juni 2011 ... 33 12. Nilai UV Pada Tanggal 14 Juni 2011 ... 33 13. Nilai Iradiasi Pada Tanggal 14 Juni 2011 ... 34 14. Iradiasi Cahaya Api Flare Pada Malam Hari ... 35 15. Suhu Tanah Siang Hari Pada Jarak 225 m Dari Flare api biru ... 36 16. Pengamatan Suhu Tanah Pada Malam Hari... 37 17. Suhu Api Flare ... 38 18. Kecepatan Angin ... 39 19. Jumlah Gas Yang Dibakar pada Bulan Februari sampai Mei 2011... ...40 20. Penyadapan Sistem 1/2 S dan Penyadapan Sistem V ... 47 21. Konsumsi Kulit Karet (a), Pemulihan Kulit Karet(b) ... 47 22. Produksi Lateks Tanaman Karet ... 49 23. Plot 2 Dimensi Analisis Komponen Utama GT (kesuburan tanah x produksi) ... 51 24. Plot 2 Dimensi Analisis Komponen Utama GT (produksi x jumlah gulma) .. 52 25. Plot 2 Dimensi Analisis Komponen Utama AVROS (kesuburan tanah x produksi) ... 53 26. Plot 2 Dimensi Analisis Komponen Utama AVROS (Pertumbuhan tanaman x gulma) ... 54 27. Plot 2 Dimensi Analisis Komponen Utama LCB (Kesuburan tanah x gulma)55 28. Plot 2 Dimensi Analisis Komponen Utama LCB (Kesuburan tanah x Produksi) ... 56DAFTAR LAMPIRAN
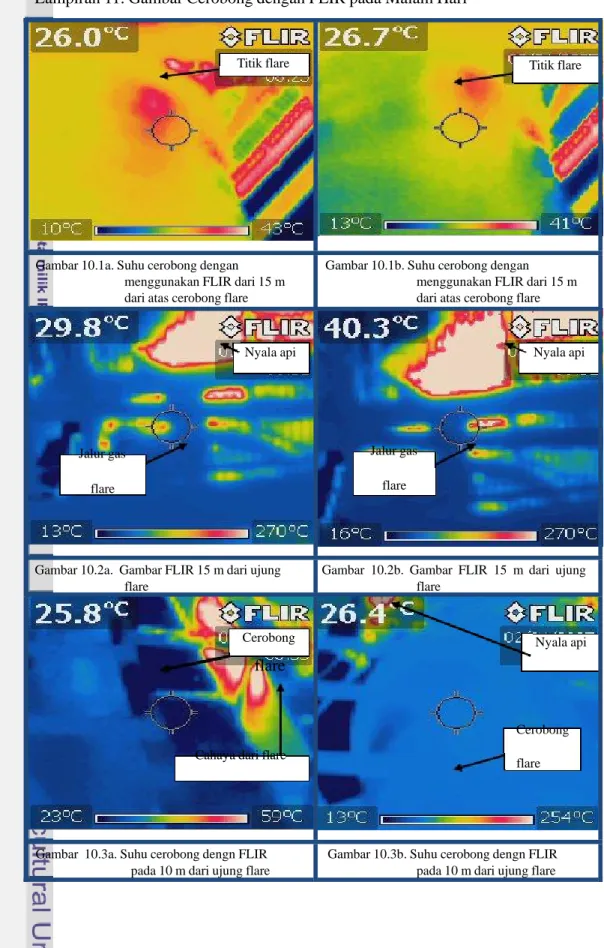
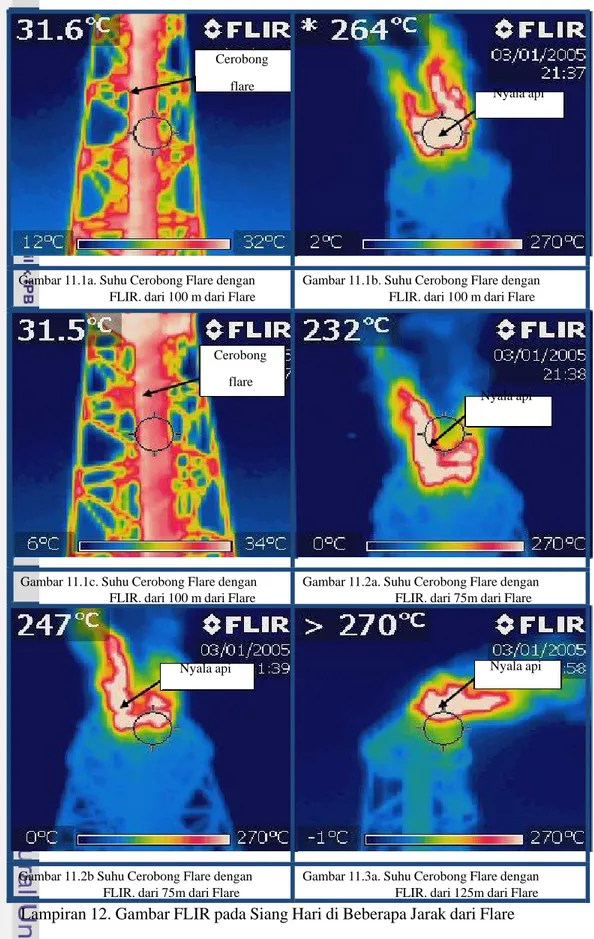
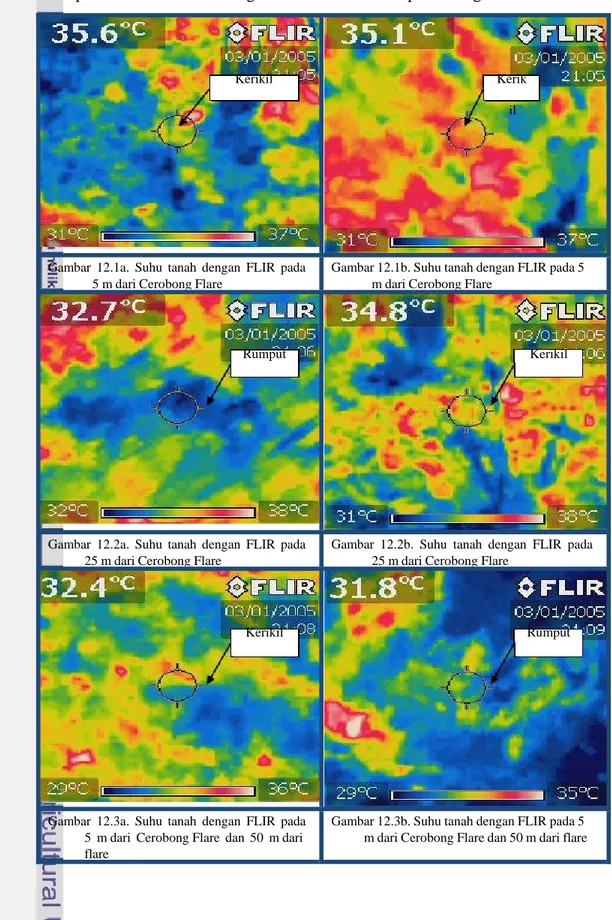
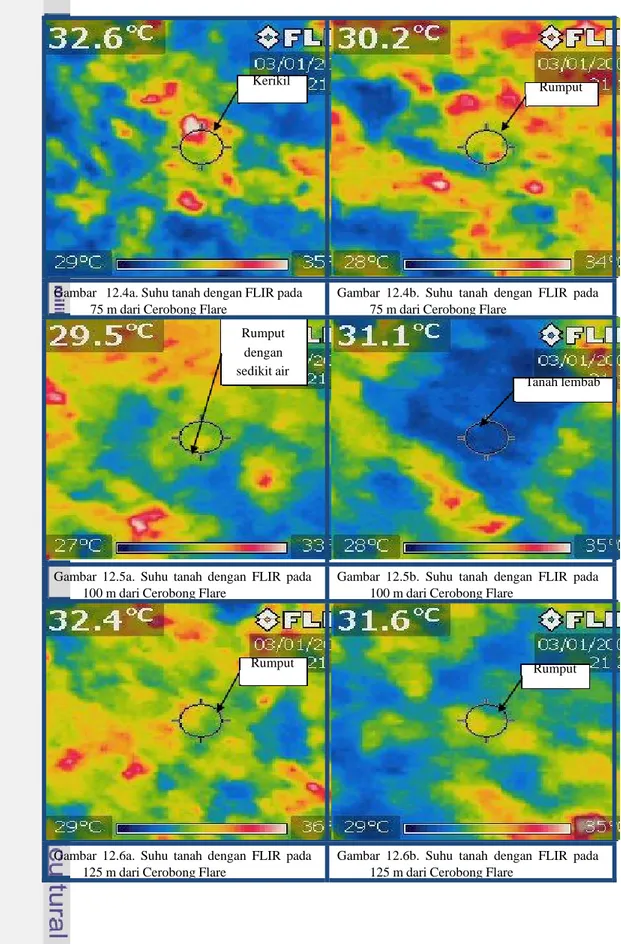
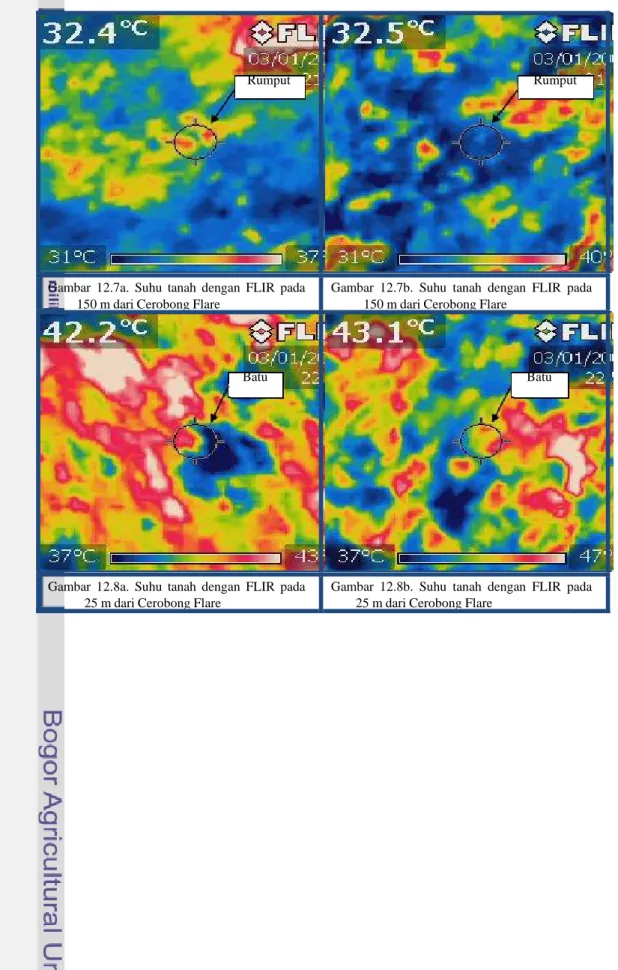
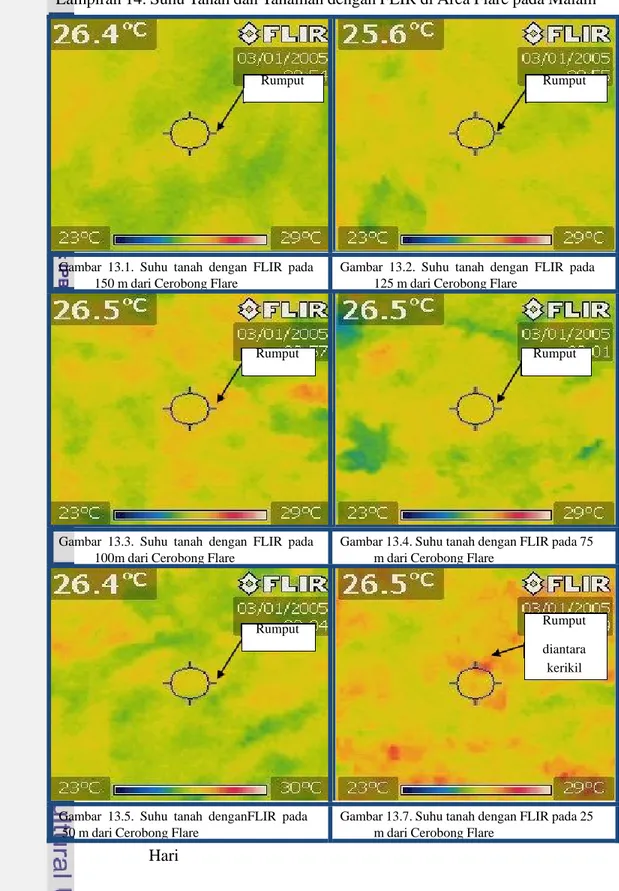
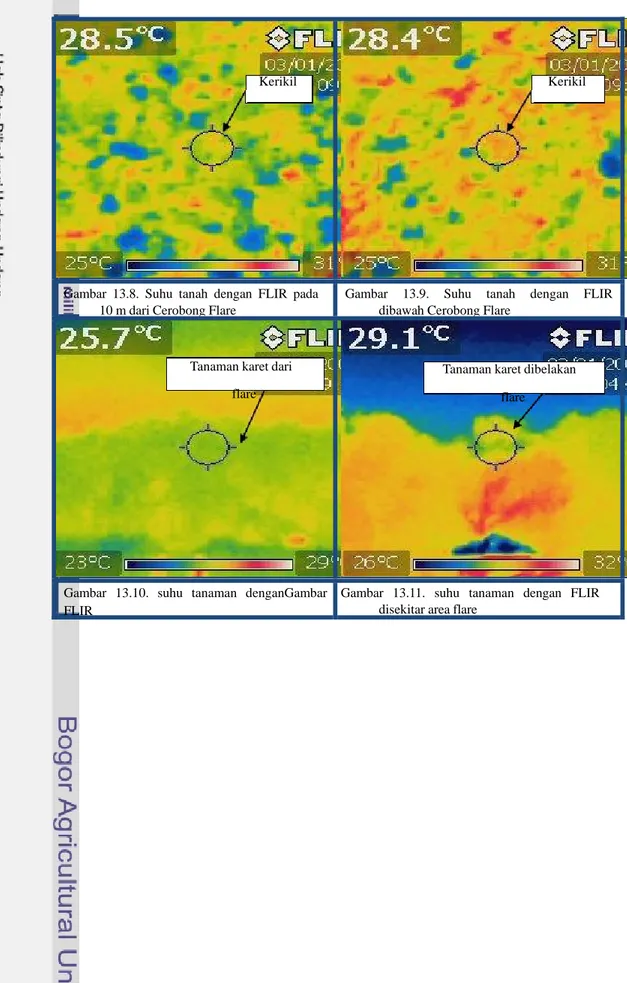
Nomor Halaman 1. Denah Penelitian ... 62 2. Gambar Alat Untuk Pengukuran di Lapang... 63 3. Hasil Analisis Tanah ... 64 4. Komposisi Tanah ... 66 5. Data Curah Hujan Jambi ... 67 6. Keragaman Gulma ... 68 7. Pengukuran Cahaya Matahari ... 69 8. Pengukuran Iradiasi Cahaya Api Flare ... 71 9. Pengukuran Suhu Tanah, Udara dan Kecepatan Angin ... 72 10. Pengukuran Suhu Tanah Malam Hari ... 73 11. Gambar Cerobong dengan FLIR pada Malam Hari ... 74 12. Gambar FLIR pada Siang Hari di Beberapa Jarak dari Flare ... 75 13. Suhu Tanah dengan FLIR di Area Flare pada Siang Hari ... 77 14. Suhu Tanah dan Tanaman dengan FLIR di Area Flare pada Malam Hari... 80 15. Suhu Batang Karet dan Kanopi dengan Menggunakan FLIR... 82 16. Hasil Analisis Komponen Utama Klon GT ... 83 17. Hasil Analisis Komponen Utama Klon AVROS ... 84 18. Hasil Analisis Komponen Utama Klon LCB ... 85PENDAHULUAN
Latar Belakang Karet alam merupakan komoditi pertanian yang penting untuk lingkup nasional maupun internasional. Indonesia merupakan produsen karet terbesar kedua setelah Thailand. Di Indonesia karet merupakan salah satu hasil pertanian yang menunjang perekonomian Negara. Tidak sedikit masyarakat yang menggantungkan penghasilannya dari hasil produksi karet. Perkebunan karet lebih banyak ditemukan di pulau Sumatera dan Kalimantan. Direktorat Jendral Perkebunan (2011) mencatat luas lahan karet di Indonesia mengalami peningkatan setiap tahunnya (Lampiran 1). Peningkatan yang signifikan lebih didominasi oleh perkembangan kebun karet rakyat. Pada tahun 2011 diperkirakan luas lahan perkebunan karet mencapai 3.5 juta hektar. Produksi karet juga mengalami peningkatan hingga 2.6 juta ton. Tercatat luas lahan perkebunan karet rakyat diperkirakan mencapai 2.9 juta ha dan menghasilkan produksi karet sebesar 2.1 juta ton. Hasil produksi karet pada tahun 1998 dengan luas lahan 3.6 juta ha menghasilkan karet sebanyak 1.6 juta ton. Perkebunan karet rakyat pada tahun tersebut seluas 3.1 juta ha dan sisanya merupakan perkebunan karet swasta dan perkebunan karet pemerintah, sedangkan hasil produksi perkebunan rakyat mencapai 1.2 juta ton. Telihat penurunan lahan karet rakyat, akan tetapi hasil karet meningkat. Semakin lama produksi karet dari perkebunan rakyat semakin menurun. Penurunan produktivitas ini disebabkan oleh beberapa faktor, diantaranya adalah perawatan yang kurang intensif dan bibit yang digunakan bukan merupakan bibit yang berkualitas. Perawatan yang dilakukan pada perkebunan rakyat hanya dengan mengurangi jumlah vegetasi disekitar tanaman. Sebagian besar masyarakat tidak melakukan pemupukan atau perawatan lainnya. Bibit yang digunakan merupakan bibit yang tumbuh dari biji tanaman sebelumnya. Penyadapan juga dilakukan setiap hari pada saat matahari telah terik. Hal ini mengakibatkan tekanan turgor tanaman berkurang sehingga karet yang dihasilkan hanya sedikit (Kiswara, 2007).Perkebunan karet rakyat yang terletak di Betara, Kabupaten Tanjung Jabung Barat Provinsi Jambi terletak di sekitar area produksi gas. Di area ini terdapat cerobong gas yang dibakar. Pembakaran gas menghasilkan cahaya biru yang menyala sepanjang hari. Cerobong gas ini lebih dikenal dengan sebutan flare. Flare hanya dimatikan pada saat shut down pada bulan Mei. Penelitian ini dilatar belakangi oleh anggapan penduduk setempat yang menyatakan bahwa adanya cahaya dari flare mengakibatkan penurunan produksi karet. Hal ini cukup menarik perhatian peneliti untuk melakukan penelitian ini. Penelitian ini mengacu pada penelitian sebelumnya tentang pengaruh pemberian cahaya kontinu terhadap kedelai di Tuban pada tahun 2000. Api pada lahan yang akan diteliti sudah di modifikasi dari api merah - kuning menjadi api biru. Modifikasi cahaya ini bertujuan agar nilai iradiasi dan iluminasi cahaya yang dihasilkan menjadi lebih kecil, sehingga dapat meminimalkan efek negatif yang ditimbulkan. Tujuan Penelitian ini bertujuan mengetahui hubungan antara iradiasi cahaya flare dengan produktivitas kebun karet rakyat dan vegetasi disekitarnya di instalasi industri minyak dan gas Tanjung Jabung, Provinsi Jambi. Hipotesis Hipotesis yang diajukan dalam penelitian ini adalah radiasi flare api biru memberikan pengaruh terhadap produktifitas tanaman karet dan vegetasi disekitarnya.
TINJAUAN PUSTAKA
Karakteristik Karet Karet (Havea brasiliensis) merupakan tanaman asli dari Amerika Selatan. karet merupakan tanaman berkayu yang memiliki tinggi dan diameter mencapai 40 m dan 35 cm (Anwar, 2010). batang tanaman ini mengandung getah yang disebut dengan lateks dan merupakan sumber karet alam dunia. Karet memiliki struktur daun majemuk yang terdiri atas tangkai daun utama dan tangkai anak daun. Panjang tangkai daun utama sekitar 3–20 cm dan panjang anak daun sekitar 3-10 cm dengan jumlah anak daun biasanya 3 anak daun. Anak daun berbentuk oval, memanjang, dan daunnya meruncing. Karet mempunyai biji yang terdapat dalam setiap buah. Jumlah biji sekitar 3–6 sesuai dengan jumlah ruang buah. Warna biji coklat kehitaman dengan bercak-bercak berpola yang khas. Karet memiliki akar tunggang dengan banyak akar-akar lateral. Anwar (2010) menyatakan bahwa karet tumbuh baik pada daerah dengan ketinggian kurang dari 1200 m dpl dengan kemiringan lahan 0–70 m. Kondisi tanah yang optimum adalah tanah-tanah dengan kedalaman mencapai 1 m, mempunyai drainase yang baik dan dengan kisaran pH 4.0–8.0, tetapi tumbuh lebih baik pada kondisi tanah masam. Omokhafe dan Emoedo (2010) juga menyatakan iklim yang sesuai untuk karet adalah yang memiliki suhu udara sekitar 22–30OC, kelembaban relatif tidak melampaui 70–80 %, curah hujan setiap tahunnya antara 1500–3000 mm dengan panjang bulan kering maksimum 3-4 bulan. Pada musim kering, karet akan menggugurkan daun setiap tahunnya. Pertumbuhan karet yang optimum dicapai dengan populasi 400–500 tanaman setiap hektar. Lateks Lateks merupakan hasil dari penyadapan karet. Penyadapan karet merupakan sistim pengambilan lateks dengan mengikuti aturan-aturan tertentu untuk memperoleh produksi tinggi, secara ekonomis menguntungkan danberkesinambungan dengan memperhatikan kesehatan tanaman (Setyamidjaja, 1993). Setelah penyadapan, maka hasil karet akan dikumpulkan untuk dijual. Hasil lateks tidak selalu tetap setiap harinya, banyak hal yang mempengaruhi volume lateks yang didapatkan. Lateks yang dihasilkan dipengaruhi oleh klon karet, umur karet (Khasanah et al, 2007), lilit batang karet, intensitas pengambilan dan cara penyadapan (Joshi et al, 2002), keadaan tanah, dan waktu penyadapan (Omokhafe dan Emoedo, 2010). Klon‐klon lama yang telah dilepas yaitu GT 1, AVROS 2037, PR 255, PR 261, PR 300, PR 303, RRIM 600, RRIM 712, BPM 1, BPM 24, BPM 107, BPM 109, PB 260, RRIC 100. Tahun 2006 telah diliris klon-klon karet baru yaitu: IRR 5, IRR 32, IRR 39, IRR 42, IRR 104, IRR 112, dan IRR 118 (Anwar, 2010). Klon‐klon tersebut menunjukkan produktivitas dan kinerja yang baik pada berbagai lokasi, tetapi memiliki variasi karakter agronomi dan sifat‐sifat sekunder lainnya. Oleh karena itu, pengguna harus memilih dengan cermat klon‐klon yang sesuai agroekologi wilayah pengembangan dan jenis‐jenis produk karet yang akan dihasilkan. Karet yang siap sadap juga bergantung pada umur tanaman. Pertambahan umur sebanding dengan pertambahan lilit batang karet. Lilit batang karet betambah 0 – 2 cm setiap bulannya (Chandrasekhar et al, 2005). Omokhafe dan Emoedo (2010) menyatakan produksi lateks dari tanaman karet disamping ditentukan oleh keadaan tanah dan pertumbuhan tanaman, klon unggul, juga dipengaruhi oleh teknik dan manajemen penyadapan. Apabila ketiga kriteria tersebut dapat terpenuhi, maka diharapkan tanaman karet pada umur 5 ‐ 6 tahun telah memenuhi kriteria matang sadap. Kriteria matang sadap antara lain apabila keliling lilit batang pada ketinggian 100 cm dari permukaan tanah telah mencapai minimum 45 cm. Jika 60% dari populasi tanaman telah memenuhi kriteria tersebut, maka areal pertanaman sudah siap dipanen. Omokhafe (2004) menyatakan Tinggi bukaan sadap, baik dengan sistem sadapan ke bawah (Down ward tapping system, DTS) maupun sistem sadap ke atas (Upward tapping system, UTS) adalah 130 cm diukur dari permukaan tanah. Waktu bukaan sadap adalah 2 kali setahun yaitu, pada (a) permulaan musim hujan (Juni) dan (b) permulaan masa intensifikasi sadapan (bulan Oktober). Oleh karena itu, tidak secara otomatis tanaman yang sudah matang sadap lalu langsung
disadap, tetapi harus menunggu waktu tersebut di atas tiba. Secara umum, permulaan sadapan dimulai dengan sudut kemiringan irisan sadapan sebesar 40o dari garis horizontal (Cornish, 2001). Pada sistem sadapan bawah, besar sudut irisan akan semakin mengecil hingga 30o bila mendekati "kaki gajah" (pertautan bekas okulasi). Sistem sadapan ke atas sudut irisan akan semakin membesar. Secara teoritis, apabila didukung dengan kondisi pertumbuhan yang sehat dan baik, tanaman karet telah memenuhi kriteria matang sadap pada umur 5-6 tahun. Dengan mengacu pada patokan tersebut, berarti mulai pada umur 6 tahun tanaman karet dapat dikatakan telah merupakan tanaman menghasilkan atau TM. Nafri (2008) menambahkan bahwa tebalnya irisan sadap ± 1.5-2 mm, penyadapan dilakukan 2 hari sekali (pemakaian kulit hanya 2.5 cm / bulan), biasanya pembuluh lateks terletak pada ketebalan 7 mm, penyadapan jangan sampai terkena lapisan kambium (±1-1.5 mm dari lapisan kambium), dan waktu penyadapan yang terbaik antara pukul 05.00-07.00 pagi. Setelah dilakukan penyadapan tanaman karet maka kulit yang telah dipotong akan melakukan regenerasi (Kongsawadworakul et al., 2009). Regenerasi akan berlangsung sejak kulit mulai disadap dan akan kembali normal pada tahun kedua setelah penyadapan. Gulma juga merupakan komponen yang dapat mepengaruhi produksi lateks. Keberadaan gulma yang tumbuh pada area kebun dapat menjadi saingan tanaman karet dalam menyerap unsur hara. Pengendalian gulma sangat penting, karena pengurangan unsur hara yang diserap tanaman akan berpengaruh terhadap produksi tanaman (Priyadarshan et al., 2005). Gulma yang menjadi pesaing karet adalah alang-alang, Mikania cordorata, Axonopus sp, puspalum konjugatum, Imperata cylindrical, Melastoma malabathricum, Borreria alata (Yeoh and Taib, 1979 dan Anwar 2010). Pengendalian gulma dapat dilakukan secara manual ataupun kimia. Cahaya Kontinu Karet menyukai intensitas cahaya matahari yang rendah (Chandrasekhar et al., 2005). Hal ini disebabkan pada saat musim hujan dan intensitas cahaya
matahari menurun maka daun tanaman karet melebar dan membantu peningkatan proses fotosintesis. Intensitas matahari yang terlalu besar dapat mengakibatkan pengguguran daun. Musim kering (panas) berturut-turut selama dua bulan akan menyebabkan stress pada tanaman karena penguapan yang besar dan pasokan air yang sedikit. Sehingga proses fotosintesis terganggu. Jumlah panjang hari sangat mempengaruhi produktifitas karet. Jumlah panjang hari yang dibutuhkan oleh tanaman karet adalah 12 jam setiap hari (Yeang, 2007). Radiasi cahaya matahari dapat mempengaruhi fotosintesis karet. Cahaya yang efisien digunakan oleh tanaman karet adalah 0.17 – 0.31 g MJ-1 (Khasanah et al, 2007). Agusta dan Santosa (2005) menyatakan bahwa penambahan cahaya yang terus menerus (fotoperiodisitas 24 jam setiap hari) dengan nilai iradiasi sebesar 0.61 cal/cm2/menit dengan nilai iluminasi sebesar 59 lux mampu melakukan penekanan proses pembungaan dan pembentukan polong, pengisian biji, serta produksi kacang hijau kultivar Betet. Hal ini dapat menyatakan bahwa penambahan cahaya dapat memberikan efek negatif terhadap tanaman. Penambahan cahaya kontinu pada tingkat 0.01 cal/cm2/menit dengan nilai iluminasi sebesar 2 lux tidak mempengaruhi produksi kacang hijau (Agusta, 2008). Tanaman karet tidak terlalu terpengaruh terhadap suhu dingin pada malam hari. Blohm and Gehrels (2007) menyatakan bahwa tanaman karet dipengaruhi suhu dingin yang berkisar 10oC pada malam hari. Analisis Komponen Utama Analisis komponen utama merupakan bagian dari analisis multivariat yang melibatkan lebih dari dua variabel. Pola hubungannya dapat bersifat dependen maupun independen. Jika pola hubungan dependen maka dalam analisisnya diperlukan variabel bebas dan variabel tergantung. Salah satu tantangan dalam analisis data peubah ganda adalah mereduksi dimensi dari segugus peubah data yang besar. Hal ini sering kali dilakukan dengan cara mereduksi gugus peubah tersebut menjadi gugus peubah yang lebih kecil atau gugus peubah yang baru yang banyaknya lebih sedikit. Peubah-peubah baru tersebut merupakan fungsi dari peubah asal atau peubah asal itu sendiri
memiliki proporsi informasi yang signifikan mengenai gugus data tersebut. Pereduksian dimensi ini sangat diperlukan saat melakukan eksplorasi data menggunakan plot-plot untuk memberikan informasi secara visual. Penggunaan komponen utama merupakan fungsi linier tertentu dari peubah asal. Sering disarankan untuk digunakan dalam proses mereduksi banyak peubah. Analisi komponen utama adalah prosedur statistik untuk mendapatkan komponen utama yang mampu mempertahankan sebagian besar informasi yang terkandung pada data asal (Sartono, et all. 2003). Komponen utama mampu mempertahankan sebagian besar informasi yang diukur menggunakan keragaman total hanya menggunakan sedikit komponen utama saja. Analisis komponen utama juga dapat dipandang sebagai sebuah kasus proyeksi data dari dimensi besar ke dimensi yang lebih rendah. Analisis komponen utama adalah salah satu teknik ekplorasi data yang digunakan sangat luas ketika menghadapi data peubah ganda. Metode yang digunakan untuk menentukan banyaknya komponen utama yaitu bedasarkan pada kumulatif proporsi keragaman total yang mampu dijelaskan. Minimum persentasi di entukan terlebih dulu, dan selanjutnya banyaknya komponen yang paling kecil sehingga batas itu terpenuhi dijadikan sebagai banyaknya komponen utama. Tidak ada patokan yang baku berapa batas minimum tersebut.
BAHAN DAN METODE
Tempat dan Waktu Percobaan Penelitian akan dilaksanakan di kebun karet rakyat di daerah Betara Kabupaten Tanjung Jabung Barat, Provinsi Jambi. Waktu pelaksanaan penelitian dimulai dari bulan Februari 2011 sampai dengan Juli 2011. Bahan dan Alat Penelitian ini akan menggunakan sampel dari perkebunan karet rakyat yang terdapat disekitar salah satu perusahaan minyak dan gas yang tedapat di daerh Betara, Tanjung Jabung Barat, Provinsi Jambi. Bahan yang dihugunakan dibagi menjadi dua, yaitu bahan untuk pembekuan karet dan bahan yang digunakan untuk analisis tanah secara kimia. Bahan yang digunakan untuk pembekuan karet adalah cuka karet yang biasa digunakan oleh petani karet setempat. Jumlah cuka karet yang digunakan tergantung pada berat lateks yang sudah di dapatkan. Perbandingan antara cuka karet dan lateks yaitu 1 : 10. Bahan yang digunakan untuk analisis tanah dibagi berdasarkan parameter tanah yang dianalisis. pH tanah. Bahan untuk analisis tanah yaitu Air bebas ion, Larutan buffer pH 7,0 dan pH 4.0, KCl 1 M, Larutkan 74,5 g KCl p.a. dengan air bebas ion hingga 1 liter. Peralatan yang digunakan Neraca analitik, Botol kocok 100 ml, Dispenser 50 ml gelas ukur-1, Mesin pengocok, Labu semprot 500 ml, pH meter. C-Organik. Bahan yang digunakan adalah Asam sulfat pekat, Kalium dikromat 1 N (Larutkan 98,1 g kalium dikromat dengan 600 ml air bebas ion dalam piala gelas, tambahkan 100 ml asam sulfat pekat, panaskan hingga larut sempurna, setelah dingin diencerkan dalam labu ukur 1 l dengan air bebas ion sampai tanda garis), Larutan standar 5.000 ppm C (Larutkan 12,510 g glukosa p.a. dengan air suling di dalam labu ukur 1 l dan diimpitkan). Alat yang digunakanadalah Neraca analitik, Spektrofotometer, Labu ukur 100 ml, Dispenser 10 ml, Pipet volume 5 ml. N-Total. Bahan yang digunakan untuk analisis tanah untuk destruksi contoh adalah Asam sulfat pekat (95-97 %), Campuran selen p.a. (tersedia di pasaran) atau buat dengan mencampurkan 1,55 g CuSO4 anhidrat, 96,9 g Na2SO4 anhidrat dan 1,55 g selen kemudian dihaluskan. Bahan untuk pengukuran secara destilasi yaitu, Asam borat 1% (Larutkan 10 g H3BO3 dengan 1 l air bebas ion), Natrium Hidroksida 40 % (Larutkan 400 g NaOH dalam piala gelas dengan air bebas ion 600 ml, setelah dingin diencerkan menjadi 1 l), Batu didih (Buat dari batu apung yang dihaluskan), Penunjuk Conway (Larutkan 0,100 g merah metil (metil red) dan 0,150 g hijau bromkresol (bromcresol green) dengan 200 ml etanol 96 %), Larutan baku asam sulfat 1N (Titrisol) 32, H2SO4 4 N(Masukan 111 ml H2SO4 p.a. pekat (95-97 %) sedikit demi sedikit melalui dinding labu labu ukur 1000 ml yang telah berisi sekitar 700 ml air bebas ion, kocok dan biarkan menjadi dingin. Tambahkan lagi air bebas ion hingga 1000 ml, kocok), Larutan baku asam sulfat 0,050 N (Pipet 50 ml larutan baku H2SO4 1 N Titrisol ke dalam labu ukur 1 liter. Encerkan dengan air bebas ion hingga 1 l. Atau: Pipet 12,5 ml asam sulfat 4 N ke dalam labu ukur 1 l. Diencerkan sampai 1 l dengan air bebas ion, kocok. Kenormalannya ditetapkan dengan bahan baku boraks). Alat yang digunakan untuk penetapan N-Total adalah neraca analitik, tabung digestion & blok digestion, labu didih 250 ml, erlenmeyer 100 ml bertera, buret 10 ml, pengaduk magnetic, dispenser, tabung reaksi, pengocok tabung, dan alat destilasi. P-Bray 1. Peralatan yang digunakan adalah Neraca analitik, Dispenser 25 ml, Dispenser 10 ml, Tabung reaksi, Pipet 2 ml, Kertas saring, Botol kocok 50 ml, Mesin pengocok, Spektrofotometer. Pereaksi yang digunakan adalah HCl 5 N (Sebanyak 416 ml HCl p.a. pekat (37 %) dimasukkan dalam labu ukur 1.000 ml yang telah berisi sekitar 400 ml air bebas ion, kocok dan biarkan menjadi dingin. Tambahkan lagi air bebas ion hingga 1.000 ml. Pengekstrak Bray dan Kurts I (larutan 0,025 N HCl + NH4F 0,03
N) (Timbang 1,11 g hablur NH4F, dilarutkan dengan lebih kurang 600 ml air bebas ion, ditambahkan 5 ml HCl 5 N, kemudian diencerkan sampai 1 l). Pereaksi P pekat (Larutkan 12 g (NH4)6 Mo7O24.4H2O dengan 100 ml air bebas ion dalam labu ukur 1 liter. Tambahkan 0,277 g K (SbO)C4H4O6 0,5 H2O dan secara perlahan 140 ml H2SO4 pekat. Jadikan 1 l dengan air bebas ion). Pereaksi pewarna P (Campurkan 1,06 g asam askorbat dan 100 ml pereaksi P pekat, kemudian dijadikan 1 liter dengan air bebas ion. Pereaksi P ini harus selalu dibuat baru). Standar induk 1.000 ppm PO4 (Titrisol) (Pindahkan secara kuantitatif larutan standar induk PO4 Titrisol di dalam ampul ke dalam labu ukur 1 l. Impitkan dengan air bebas ion sampai dengan tanda garis, kocok). Standar induk 100 ppm PO4 (Pipet 10 ml larutan standar induk 1.000 ppm PO4 ke dalam labu 100 ml. Impitkan dengan air bebas ion sampai dengan tanda garis lalu kocok). Deret standar PO4 (0-20 ppm) (Pipet berturut-turut 0; 2; 4; 8; 12; 16; dan 20 ml larutan standar 100 ppm PO4 ke dalam labu ukur 100 ml, diencerkan dengan pengekstrak Olsen hingga 100 ml). K, Na, Ca, dan Mg. Peralatan yang digunakan adalah Neraca analitik 3 desimal, Tabung digestion & blok digestion, Pengocok tabung, Dispenser, Tabung reaksi, Spektrophotometer UV-VIS, AAS, Flamephotometer, Spektrofotometer.
Bahan yang digunakan adalah HNO3 pekat (65 %) p.a., HClO4 pekat (60 %) p.a. Standar 0 (larutan HClO4 0,6 %) (Dipipet 1 ml HClO4 pekat (60 %) ke dalam labu ukur 100 ml yang telah berisi air bebas ion kira-kira setengahnya, goyangkan dan tambahkan lagi air bebas ion hingga tepat 100 ml (pengenceran 100 x). Larutan BaCl2-Tween Ditimbang 3 g serbuk BaCl2 p.a. ke dalam botol kocok 250 ml, tambahkan 4 ml Tween 80 dan botol digoyangkan agar campuran merata. Campuran dibiarkan semalam, selanjutnya ditambah 100 ml air bebas ion dan dikocok selama 2 jam hingga serbuk BaCl2 terlarut sempurna. Biarkan semalam sebelum digunakan). Larutan asam campur (Ke dalam labu ukur 1 l yang berisi air bebas ion kira-kira setengahnya, tambahkan secara perlahan berturut- turut 50 ml CH3COOH glasial (100 %) p.a., 20 ml HCl pekat (37 %) p.a. dan 20 ml H3PO4 pekat (70 %) p.a., kemudian diimpitkan dengan air bebas ion menjadi 1 l). Standar campur 250 ppm K, 100 ppm Na, 50 ppm Mg, 250 ppm Ca. Pipet
masing-masing: 25,0 ml standar pokok 1.000 ppm K, 10,0 ml standar pokok 1.000 ppm Na, 25,0 ml standar pokok 1.000 ppm Ca, 5,0 ml standar pokok 1.000 ppm Mg kemudian Campurkan dalam labu ukur 100 ml, tambahkan perlahan 1 ml HClO4 pekat, kemudian diimpitkan dengan air bebas ion hingga tepat 100 ml. Deret standar campur K (0-250 ppm), Na (0-100 ppm), Ca (0-250 ppm) dan Mg (0-50 ppm). Pipet standar campur sebanyak 0; 1; 2; 4; 6; 8; dan 10 ml, masing- masing dimasukkan ke dalam tabung reaksi dan dijadikan 10 ml dengan larutan HClO4 0,6 % (Tabel 1). Tabel 1. Deret Standar Campuran Kepekatan K, Na, Ca, dan Mg S0 S1 S2 S3 S4 S5 S6 0 25 50 100 150 200 250 ppm K 0 10 20 40 60 80 100 ppm Na 0 25 50 100 150 200 250 ppm Ca 0 5 10 20 30 40 50 ppm Mg Kapasitas Tukar Kation dan Kejenuhan Basa. Peralatan yang digunakan adalah Neraca analitik, Tabung perkolasi, Labu ukur 50 ml, Labu ukur 100 ml, Labu semprot, Spektrofotometer, Flamefotometer, Atomic absorption spectrophotometer (AAS). Untuk perkolasi, bahan yang digunakan adalah Amonium asetat 1 M, pH 7,0 (Timbang 77,08 g serbuk NH4-Asetat p.a. ke dalam labu ukur 1 l. Tambahkan air bebas ion hingga serbuk melarut dan tepatkan 1 l. Atau dapat pula dibuat dengan cara berikut: Campurkan 60 ml asam asetat glasial dengan 75 ml ammonia pekat (25%) dan diencerkan dengan air bebas ion hingga sekitar 900 ml. pH campuran diatur menjadi 7,00 dengan penambahan amonia atau asam asetat, kemudian diimpitkan tepat 1 l). Etanol 96 %, HCl 4 N (Sebanyak 33,3 ml HCl p.a. 37 % dimasukkan ke dalam labu ukur 100 ml yang telah berisi sekitar 50 ml air bebas ion, kocok dan biarkan dingin. Tambahkan lagi air bebas ion hingga tepat 100 ml). NaCl 10% (Timbang 100 g NaCl, kemudian dilarutkan dengan air bebas ion. Tambahkan 4 ml HCl 4 N dan diimpitkan tepat 1l). Pasir kuarsa bersih, Filter pulp (Kation-kation dapat ditukar). Amonium asetat 4 M, pH 7,0 Buat dengan cara yang sama seperti amonium asetat 1 M, namun menggunakan 4 x 77,08 g NH4-Asetat p.a. Standar pokok 1.000 ppm K, Standar pokok 1.000 ppm Na,
Standar pokok 1.000 ppm Ca, Standar pokok 1.000 ppm Mg, Standar campur 200 ppm K, 100 ppm Na, 50 ppm Mg, 250 ppm Ca (Pipet masing-masing : 25,0 ml standar pokok 1.000 ppm K, 10,0 ml standar pokok 1.000 ppm Na, 5,0 ml standar pokok 1.000 ppm Mg, 25,0 ml standar pokok 1.000 ppm Ca Campurkan dalam labu ukur 100 ml, ditambah 25 ml NH4-asetat 4 N, pH 7,0, kemudian diimpitkan). Deret standar campur K (0-250 ppm), Na (0-100 ppm), Ca (0-250 ppm) dan Mg (0-50 ppm), (Pipet standar campuran sebanyak 0; 1; 2; 4; 6; 8 dan 10 ml, masing- masing dimasukkan ke dalam tabung reaksi dan dijadikan 10 ml dengan larutan NH4-Ac 1 M, pH 7). Larutan La 2,5 % (Timbang 66,8376 gram LaCl3.7H2O, dilarutkan dengan air bebas ion ditambahkan 10 ml HCl 25% kemudian diimpitkan tepat 1 l). Larutan La 0,125 % (Larutan La 2,5 % diencerkan 20 x dengan air bebas ion). Bahan KTK cara destilasi yaitu Asam borat 1% (Larutkan 10 g H3BO3 dengan 1 l air bebas ion). Natrium Hidroksida 40 % (Larutkan 400 g NaOH dalam piala gelas dengan air bebas ion 600 ml, setelah dingin diencerkan menjadi 1 l). Batu didih (Buat dari batu apung yang dihaluskan). Penunjuk Conway (Larutkan 0,100 g merah metil (metil red) dan 0,150 g hijau bromkresol (bromcresol green) dengan 200 ml etanol 96 %). Larutan baku asam sulfat 1N (Titrisol). H2SO4 4 N (Masukkan 111 ml H2SO4 p.a. pekat (95-97 %) sedikit demi sedikit melalui dinding labu labu ukur 1.000 ml yang telah berisi sekitar 700 ml air bebas ion, kocok dan biarkan menjadi dingin. Tambahkan lagi air bebas ion hingga 1.000 ml, kocok). Larutan baku asam sulfat 0,050 N (Pipet 50 ml larutan baku H2SO4 1 N Titrisol ke dalam labu ukur 1 l. Encerkan dengan air bebas ion hingga 1 l. Atau: Pipet 12,5 ml asam sulfat 4 N ke dalam labu ukur 1 l. Encerkan sampai 1 l dengan air bebas ion, kocok. Kenormalannya ditetapkan dengan bahan baku boraks). Peralatan yang digunakan untuk mengukur cahaya adalah : Li-cor LI-250 Light Meter, sensor Pyranometer LI-200, sensor Photometer LI-210, sensor Kuantum LI-190, UV Light Meter (YK-35UV), Light Meter (LX-1128SD), Anemometer untuk mengukur kecepatan angin dan suhu udara, Infra Red Thermal Imager (FLIR I3) untuk mengetahui suhu api, tanaman dan perbedaan suhu disekitarnya, Ring Tanah untuk analisis fisika tanah, GPS (76 CSX) untuk menentukan tanaman yang akan digunkan sebagai tanaman contoh, Timbangan
(ketelitian 0.01g untuk karet), Timbangan (ketelitian 0.1g untuk gulma), Oven mengeringkan gulma dan karet, , Kamera, Infra red Thermometer Gun (Raytex, Minitep) untuk mengukur suhu tanah. Gambar peralatan dapat dilihat pada lampiran 2. Metode Pelaksanaan Percobaan ini bukan merupakan percobaan yang terkontrol, akan tetapi merupakan bentuk percobaan observasional. Contoh tanaman yang diamati diambil sesuai dengan radius yang telah ditentukan dengan menggunakan GPS dan keberadaan tanaman karet itu sendiri. Pengambilan contoh karet hanya pada arah utara saja, karena pada sekeliling flare hanya pada arah utara yang terdapat hutan karet rakyat (lampiran 1). Pada arah barat, timur, dan selatan ditumbuhi tanaman bukan karet. Radius yang di ambil adalah jarak tanaman karet dari flare yaitu: 225 m (03o 24.057’ S, 98o 76.909’ E), 275 m (03o 24.048’ S, 98o 76.979’ E), 325 m (03o 24,021’ S, 98o 77,011’ E) , 375 m (03o 23,994’ S, 98o 77,043’ E), 425 m (03o 23,999’ S, 98o 77,104’ E), 475 m (03o 24.158’ S, 98o 77.185’ E), 525 m (03o 24.257’ S, 98o 77.219’ E), 600 m (03o 24.392’ S, 98o 77.292’ E), 700 m (03o 24,489’ S, 98o 77,418’ E), dan 800 m (03o 24,579’ S, 98o 77,406’ E). Setiap titik akan diambil empat tanaman contoh yang di anggap dapat mewakili tanaman karet lain disekitarnya. Denah percobaan dapat dilihat pada lampiran 1. Pengamatan cahaya matahari meliputi UV, Iradiasi, Iluminasi, dan Kuantum. Selain itu, dilakukan pengamatan suhu tanah dan suhu udara pada siang dan malam hari. Pengamatan pada cahaya flare dilakukan pada radius 0 m, 10 m, 25 m, 50 m, 75 m, 100 m, 125 m, dan 150 m. Pengamatan cahaya ini dilakukan pada malam hari yang meliputi UV, Iradiasi, Ilminasi, dan Kuantum. Pengamatan
lingkungan meliputi kondisi gulma (jumlah gulma, bobot basah gulma, bobot kering gulma, dan kadar air Gulma) dan kondisi fisika dan kimia tanah (Kadar air tanah, pasir, debu, Liat, pH tanah, C organik tanah, N total tanah, Ca tanah, Mg tanah, K Tanah, Na Tanah, KTK Tanah, dan P tanah). Pengamatan produksi meliputi lilit batang, tinggi batang, tinggi bidang sadap, panjang daun, lebar daun, Berat Basah karet, Berat Kering karet, dan kadar karet kering. Data akan diolah menggunakan analisis komponen utama dengan menggunakan SAS 17. Pelaksanaan Penelitian Lahan yang digunakan merupakan perkebunan rakyat yang sudah dalam fase matang sadap. Tanaman contoh yang diambil merupakan tanaman yang dianggap dapat mewakili keseluruhan penampakan tanaman karet yang berada dilapangan. Pengamatan dilakukan pada siang dan malam hari mulai pukul 06.00 WIB – 18.00 WIB dan 19.00 WIB – 03.00 WIB dini hari. Pengamatan yang dilakukan antara lain: Analisis tanah. Sampel tanah diambil pada jarak 225 m, 275 m, 325 m, 375 m, 425 m, 475 m, 525 m, 600 m, 700 m, dan 800 m dari flare dengan empat kedalaman 0 - 10 cm, 10 - 20 cm, 20 - 30 cm, 30 - 40 cm dari permukaan tanah. Pengambilan sampel tanah pada setiap titik dilakukan di tengah-tengah titik tersebut. Tanah dilapangan kemudian ditimbang 50 gram untuk menentukan kadar air, dan 250 gram untuk menentukan sifat fisik tanah. Pengukuran kadar air tanah dilakukan dengan cara mengoven tanah di Laboratorium Pasca Panen IPB. tanah kering udara dalam pinggan aluminium yang telah diketahui bobotnya. Keringkan dalam oven pada suhu 105 oC selama 3 jam. Angkat pinggan dengan penjepit dan masukkan ke dalam eksikator. Setelah contoh dingin kemudian timbang. Bobot yang hilang adalah bobot air dengan perhitungan: Kadar Air (%) = (kehilangan bobot / bobot contoh) x 100 Faktor koreksi kadar air (fk) = 100 / (100 – kadar air) Pengambilan sempel untuk sifat fisika tanah diambil pada jarak 225 m dari flare dengan empat kedalaman 0 - 10 cm, 10 - 20 cm, 20 - 30 cm, 30 - 40 cm dari
Cr yang berwarna jingga menjadi Cr3+yang berwarna hijau dalam suasana asam. permukaan tanah. Cara pengambilan sampel tanah untuk uji sifat fisika tanah berbeda dengan pengambilan sampel tanah untuk uji kimia tanah. Pengambilan sampel tanah untuk uji fisika tanah dilakukan dengan menggunakan ring khusus tanah. Pengambilan sampel tanah hanya dilakukan satu kali pada tanggal 12 Februari 2011. Tanah kemudian di uji di Laboratorium Tanah untuk mengetahui sifat kimia dan fisika tanah Penentuan pH. Nilai pH menunjukkan konsentrasi ion H+ dalam larutan
tanah, yang dinyatakan sebagai –log[H+]. Peningkatan konsentrasi H+ menaikkan potensial larutan yang diukur oleh alat dan dikonversi dalam skala pH. Elektrode gelas merupakan elektrode selektif khusus H+, hingga memungkinkan untuk hanya mengukur potensial yang disebabkan kenaikan konsentrasi H+. Potensial yang timbul diukur berdasarkan potensial elektrode pembanding (kalomel atau AgCl). Biasanya digunakan satu elektrode yang sudah terdiri atas elektrode pembanding dan elektrode gelas (elektrode kombinasi). Konsentrasi H+ yang diekstrak dengan air menyatakan kemasaman aktif (aktual) sedangkan pengekstrak KCl 1 N menyatakan kemasaman cadangan (potensial). Langkah kerjanya yaitu Timbang 10,00 g contoh tanah sebanyak dua kali, masing-masing dimasukkan ke dalam botol kocok, ditambah 50 ml air bebas ion ke botol yang satu (pH H2O) dan 50 ml KCl 1 M ke dalam botol lainnya (pH KCl). Kocok dengan mesin pengocok selama 30 menit. Suspensi tanah diukur dengan pH meter yang telah dikalibrasi menggunakan larutan buffer pH 7,0 dan pH 4,0. Laporkan nilai pH dalam 1 desimal. Penentuan C-Organik. Karbon sebagai senyawa organik akan mereduksi 6+ Intensitas warna hijau yang terbentuk setara dengan kadar karbon dan dapat diukur dengan spektrofotometer pada panjang gelombang 561 nm. Langkah kerja untuk menentukan C-Organik tanah yaitu Timbang 0,500 g contoh tanah ukuran <0,5 mm, dimasukkan ke dalam labu ukur 100 ml. Tambahkan 5 ml K2Cr2O7 1 N, lalu dikocok. Tambahkan 7,5 ml H2SO4 pekat, dikocok lalu diamkan selama 30 menit. Diencerkan dengan air bebas ion, biarkan dingin dan diimpitkan. Keesokan
harinya diukur absorbansi larutan jernih dengan spektrofotometer pada panjang gelombang 561 nm. Sebagai pembanding dibuat standar 0 dan 250 ppm, dengan memipet 0 dan 5 ml larutan standar 5.000 ppm ke dalam labu ukur 100 ml dengan perlakuan yang sama dengan pengerjaan contoh. Catatan: Bila pembacaan contoh melebihi standar tertinggi, ulangi penetapan dengan menimbang contoh lebih sedikit. Ubah faktor dalam perhitungan sesuai berat contoh yang ditimbang. Cara penghitungan penetapa C-organik (%) adalah: C-Organik (%) = ppm kurva x ml ekstrak 1.000 ml-1 x 100 mg contoh-1 x fk = ppm kurva x 100 1.000-1 x 100 500-1 x fk = ppm kurva x 10 500-1 x fk Keterangan: ppm kurva = kadar contoh yang didapat dari kurva hubungan antara kadar deret standar dengan pembacaannya setelah dikoreksi blanko. 100 = konversi ke % fk = faktor koreksi kadar air = 100/(100 – % kadar air) Penentuan N-Total. Senyawa nitrogen organik dioksidasi dalam lingkungan asam sulfat pekat dengan katalis campuran selen membentuk (NH4)2SO4. Kadar amonium dalam ekstrak dapat ditetapkan dengan cara destilasi atau spektrofotometri. Pada cara destilasi, ekstrak dibasakan dengan penambahan larutan NaOH. Selanjutnya, NH3 yang dibebaskan diikat oleh asam borat dan dititar dengan larutan baku H2SO4 menggunakan penunjuk Conway. Cara spektrofotometri menggunakan metode pembangkit warna indofenol biru. Langkah kerja yang dilakukan untuk menentukan kandungan N-Total dalam tanah yaitu Destruksi contoh Timbang 0,500 g contoh tanah ukuran <0,5 mm, masukan ke dalam tabung digest. Tambahkan 1 g campuran selen dan 3 ml asam sulfat pekat, didestruksi hingga suhu 350 oC (3-4 jam).
Destruksi selesai bila keluar uap putih dan didapat ekstrak jernih (sekitar 4 jam). Tabung diangkat, didinginkan dan kemudian ekstrak diencerkan dengan air bebas ion hingga tepat 50 ml. Kocok sampai homogen, biarkan semalam agar partikel mengendap. Ekstrak digunakan untuk pengukuran N dengan cara destilasi atau cara kolorimetri. Pengukuran N dengan cara destilasi yaitu pindahkan secara
kualitatif seluruh ekstrak contoh ke dalam labu didih (gunakan air bebas ion dan labu semprot). Tambahkan sedikit serbuk batu didih dan aquades hingga setengah volume labu. Disiapkan penampung untuk NH3 yang dibebaskan yaitu erlenmeyer yang berisi 10 ml asam borat 1% yang ditambah 3 tetes indikator Conway (berwarna merah) dan dihubungkan dengan alat destilasi. Dengan gelas ukur, tambahkan NaOH 40% sebanyak 10 ml ke dalam labu didih yang berisi contoh dan secepatnya ditutup. Didestilasi hingga volume penampung mencapai 50–75 ml (berwarna hijau). Destilat dititrasi dengan H2SO4 0,050 N hingga warna merah muda. Catat volume titar contoh (Vc) dan blanko (Vb). Cara menghitung kadar N- Total adalah: Kadar nitrogen (%) = (Vc - Vb) x N x bst N x 100 mg contoh-1 x fk = (Vc - Vb) x N x 14 x 100 500-1 x fk = (Vc - Vb) x N x 2,8 x fk Keterangan : Vc, Vb = ml titar contoh dan blanko N = normalitas larutan baku H2SO4 14 = bobot setara nitrogen 100 = konversi ke % fk = faktor koreksi kadar air = 100/(100 – % kadar air) Penentuan P-Bray 1. Dasar penetapan P-Bray 1 adalah Fosfat dalam suasana asam akan diikat sebagai senyawa Fe, Al-fosfat yang sukar larut. NH4F yang terkandung dalam pengekstrak Bray akan membentuk senyawa rangkai dengan Fe & Al dan membebaskan ion PO43-. Pengekstrak ini biasanya digunakan pada tanah dengan pH <5,5. Cara kerja Penentuan P-Bray 1 yaitu Timbang 2,500 g contoh tanah <2 mm, ditambah pengekstrak sebanyak 25 ml, kemudian dikocok selama 5 menit. Saring dan bila larutan keruh dikembalikan ke atas saringan semula (proses penyaringan maksimum 5 menit). Dipipet 2 ml ekstrak jernih ke dalam tabung reaksi. Contoh dan deret standar masing-masing ditambah pereaksi pewarna fosfat sebanyak 10 ml, dikocok dan dibiarkan 30 menit. Diukur absorbansinya dengan spektrofotometer pada panjang gelombang 693 nm. perhitungannya adalah:
Kadar P2O5 tersedia (ppm) = ppm kurva x ml ekstrak/1.000 ml x 1.000g/g contoh x fp x 142/190 x fk = ppm kurva x 25/1.000 x 1.000/2,5 x fp x 142/190 x fk = ppm kurva x 10 x fp x 142/190 x fk Keterangan: ppm kurva = kadar contoh yang didapat dari kurva hubungan antara kadar deret standar dengan pembacaannya setelah dikoreksi blanko. fp = faktor pengenceran (bila ada) 142/190 = faktor konversi bentuk PO4 menjadi P2O5 fk = faktor koreksi kadar air = 100/(100 – % kadar air) Penentuan K, Na, Ca, dan Mg. Dasar penetapannya adalah Unsur makro dan mikro total dalam tanah dapat diekstrak dengan cara pengabuan basah menggunakan campuran asam pekat HNO3 dan HClO4. Kadar makro dan mikro dalam ekstrak diukur menggunakan AAS, flamefotometer dan spektrofotometer. Timbang 0,500 g contoh tanah <0,5 mm ke dalam tabung digestion. Tambahkan 5 ml HNO3 p.a. dan 0,5 ml HClO4 p.a. dan biarkan satu malam. Besoknya dipanaskan dalam digestion blok dengan suhu 100 oC selama satu jam , kemudian suhu ditingkatkan menjadi 150 oC. Setelah uap kuning habis suhu digestion blok ditingkatkan menjadi 200 oC. Destruksi selesai setelah keluar asap putih dan sisa ekstrak kurang lebih 0,5 ml. Tabung diangkat dan dibiarkan dingin. Ekstrak diencerkan dengan air bebas ion hingga volume tepat 50 ml dan kocok dengan pengocok tabung hingga homogen. Pipet 1 ml ekstrak dan deret standar masing- masing ke dalam tabung kimia dan ditambahkan 9 ml larutan La 0,25 %. Kocok dengan menggunakan pengocok tabung sampai homogen. Ca dan Mg diukur dengan AAS sedangkan K dan Na diukur dengan alat flamephotometer dengan deret standar sebagai pembanding. Penghitungan Kadar K, Ca, Mg, dan Na (%) = ppm kurva x ml ekstrak 1.000 ml-1 x 100 mg contoh-1 x fp x fk = ppm kurva x 50/1.000 x 100/500 x 10 x fk = ppm kurva x 0,1 x fk Keterangan:
ppm kurva = kadar contoh yang didapat dari kurva hubungan antara kadar deret standar dengan pembacaannya setelah dikoreksi blanko. 100 = konversi ke % (pada satuan %) fk = faktor koreksi kadar air = 100/(100 – % kadar air) fp = faktor pengenceran Kapasitas Tukar Kation dan Kejenuhan Basa. Dasar penetapannya adalah koloid tanah (mineral liat dan humus) bermuatan negatif, sehingga dapat menyerap kation-kation. Kation-kation dapat ditukar (dd) (Ca2+, Mg2+, K+ dan Na+) dalam kompleks jerapan tanah ditukar dengan kation NH4+ dari pengekstrak dan dapat diukur. Untuk penetapan KTK tanah, kelebihan kation penukar dicuci dengan etanol 96%. NH4+ yang terjerap diganti dengan kation Na+ dari larutan NaCl, sehingga dapat diukur sebagai KTK. Kation-kation dapat ditukar (Ca2+, Mg2+, K+ dan Na+) ditetapkan dengan Flamefotometer dan AAS. NH4+ (KTK) ditetapkan secara kolorimetri dengan metode Biru Indofenol. Cara menentukan KTK tanah adalah Timbang 2,500 g contoh tanah ukuran >2 mm, lalu dicampur dengan lebih kurang 5 g pasir kuarsa. Dimasukkan ke dalam tabung perkolasi yang telah dilapisi berturut-turut dengan filter flock dan pasir terlebih dahulu (filter pulp digunakan seperlunya untuk menutup lubang pada dasar tabung, sedangkan pasir kuarsa sekitar 2,5 g) dan lapisan atas ditutup dengan penambahan 2,5 g pasir. Ketebalan setiap lapisan pada sekeliling tabung diupayakan supaya sama. Siapkan pula blanko dengan pengerjaan seperti contoh tapi tanpa contoh tanah. Kemudian diperkolasi dengan amonium acetat pH 7,0 sebanyak 2 x 25 ml dengan selang waktu 30 menit. Filtrat ditampung dalam labu ukur 50 ml, diimpitkan dengan amonium acetat pH 7,0 untuk pengukuran kationdd: Ca, Mg, K dan Na (S). Tabung perkolasi yang masih berisi contoh diperkolasi dengan 100 ml etanol 96 % untuk menghilangkan kelebihan amonium dan perkolat ini dibuang. Sisa etanol dalam tabung perkolasi dibuang dengan pompa isap dari bawah tabung perkolasi atau pompa tekan dari atas tabung perkolasi. Selanjutnya diperkolasi dengan NaCl 10 % sebanyak 50 ml, filtrat ditampung dalam labu ukur 50 ml dan diimpitkan dengan larutan NaCl 10 %. Filtrat ini digunakan untuk pengukuran KTK dengan cara destilasi atau
kolorimetri. Pengukuran KTK Pengukuran KTK dapat dilakukan dengan cara destilasi langsung, destilasi perkolat NaCl dan kolorimetri perkolat NaCl. Pada cara destilasi langsung dikerjakan seperti penetapan N-Kjeldahl tanah, isi tabung perkolasi (setelah selesai tahap pencucian dengan etanol) dipindahkan secara kuantitatif ke dalam labu didih. Gunakan air bebas ion untuk membilas tabung perkolasi. Tambahkan sedikit serbuk batu didih dan aquades hingga setengah volume labu. Siapkan penampung untuk NH3 yang dibebaskan yaitu erlenmeyer yang berisi 10 ml asam borat 1 % yang ditambah 3 tetes indicator Conway (berwarna merah) dan dihubungkan dengan alat destilasi. Dengan gelas ukur, tambahkan NaOH 40% sebanyak 10 ml ke dalam labu didih yang berisi contoh dan secepatnya ditutup. Destilasi hingga volume penampung mencapai 50– 75 ml (berwarna hijau). Destilat dititrasi dengan H2SO4 0,050 N hingga warna merah muda. Catat volume titar contoh (Vc) dan blanko (Vb). Cara Pengukuran kationdd (Ca, Mg, K, Na) yaitu Perkolat NH4-Ac (S) dan deret standar K, Na, Ca, Mg masing-masing dipipet 1 ml ke dalam tabung reaksi, kemudian ditambahkan 9 ml larutan La 0,25 %. Diukur dengan AAS (untuk Ca dan Mg) dan flamefotometer (untuk pemeriksaan K dan Na) menggunakan deret standar sebagai pembanding. Cara pengukuran Kationdd (cmol (+) kg-1) (S) = (ppm kurva/bst kation) x ml ekstrak 1.000 ml-1 x1.000 g g contoh-1 x0,1x fp x fk = (ppm kurva/bst kation) x 50 ml 1.000 ml-1 x 1.000 g 2,5 g-1 x 0,1 x fp x fk = (ppm kurva/bst kation) x 2 x fp1 x fk Cara Perhitungan destilasi langsung: KTK (cmol (+) kg-1) = (Vc - Vb) x N H2SO4 x 0,1 x 1.000 g/2,5 g x fk = (Vc - Vb) x N H2SO4 x 40 x fk Cara Perhitungan kejenuhan basa: Kejenuhan basa = jumlah kation dd (S)/KTK (T) x 100 % Keterangan: ppm kurva = kadar contoh yang didapat dari kurva hubungan antara kadar deret standar dengan pembacaannya setelah dikoreksi blanko. 0,1 = faktor konversi dari mmol ke cmol bst kation = bobot setara: Ca : 20, Mg: 12,15, K: 39, Na: 23 fp1 = faktor pengenceran (10)
fp2 = faktor pengenceran (20) fk = faktor koreksi kadar air = 100/(100 – % kadar air) S = jumlah basa-basa tukar (cmol(+) kg-1) T = kapasitas tukar kation (cmol(+) kg-1) Jumlah latek. Latek diambil dari tanaman karet yang telah ditentukan yaitu pada radius 225 m, 275 m, 325 m, 375 m, 425 m, 475 m, 525 m, 600 m, 700 m, 800 m dari flare. Penyadapan dilakukan pada pukul 7.00 WIB sesuai dengan kegiatan penyadapan petani. Pada setiap titik terdapat empat tanaman karet yang akan disadap, sehingga terdapat 40 sampel lateks setiap hari pengambilan. Tipe penyadapan disesuaikan dengan tipe sadap petani. Tipe sadap yang dilakukan adalah ½ S, yaitu setengah keliling batang karet dengan arah kiri atas kekanan bawah. Latek yang telah terkumpul kemudian ditimbang dan dicampur dengan cuka karet untuk mengumpalkan lateks sehingga lateks dan air yang terkandung dalam lateks. Lateks kemudian di bawa ke Laboratirium Pasca Panen IPB untuk dikeringkan dengan menggunakan oven selama 3 hari dengan suhu 80 oC sampai benar-benar kering. Pengambilan getah karet disesuaikan dengan kegiatan para penyadap karet. Penyadapan dilakukan pada tanggal 11 Februari 2011, 20 – 21 Maret 2011, dan pada tanggal 13 -14 Juni 2011. Setiap hari dilakukan penyadapan karet Analisis vegetasi. Analisis vegetasi dilakukan dengan mengambil vegetasi disekitar tanaman karet pada radius 225 m, 275 m, 325 m, 375 m, 425 m, 475 m, 525 m, 600 m, 700 m, 800 m dari flare dengan menggunakan kuadran ukuran 1 m x 1 m. Pada setiap titik terdapat empat pengulangan pengambilan vegetasi sehingga terdapat 40 sampel gulma. Kuadran dilempar disekiar tanaman contoh, sehingga mendapatkan vegetasi yang mewakili sekitar tanaman contoh. Analisis vegetasi dilakukan satu kali pada tanggal 11 Februari 2011. Gulma kemudian di timbang untuk mendapatkan bobot awal. Setelah itu gulma kemudian dipisahkan berdasarkan jenisnya. Gulma kemudian di oven dengan suhu 80 oC selama 2 hari agar gulma benar-benar kering.
Klon Karet. Klon tanaman ditentukan dengan memperbandingkan dengan koleksi plasma nutfah Institut Pertanian Bogor (IPB). Daun dari setiap sempel akan dibandingkan dengan plasma yang dimiliki kampus IPB karena tanaman di perkebunan karet rakyat memiliki jenis yang berbeda. Data yang demikian akan sangat membantu dalam pengolahan data. Pengamatan tanaman karet. Pengamatan tanaman karet dilakukan dengan mengamati tinggi tanaman karet yaitu dengan menggunakan distometer. Tinggi tanaman karet dihitung dari permukaan tanah sampai percabangan pertama tanaman karet. lilit batang dilakukan dengan menggunakan meteran. Pengukuran lilit batang dilakukan pada ketinggian 100 cm dari permukaan tanah. Pengamatan tinggi bidang sadap dilakukan dengan menggunakan meteran yaitu dengan mengukur tinggi tanaman karet dari permukaan tanah sampai pada bidang sadap karet. Terdapat juga pengamatan konsumsi kulit karet, yaitu dengan mengukur tebalnya potongan kulit karet. Pengamatan cahaya. Pengamatan cahaya dilakukan dengan pengamatan pada siang hari dan malam hari. Pengamatan pada siang hari (07.00 WIB - 18.00 WIB) meliputi kuantum yaitu pengukuran dengan menggunakan quantum yang disambungkan dengan Li-cor LI-250 Light Meter. Pengukuran nilai iluminasi mengggunakan Photometer yang disambungkan dengan Li-cor LI-250 Light Meter. Pengukuran nilai iradiasi mengggunakan Pyranometer yang disambungkan dengan Li-cor LI-250 Light Meter. Pengamatan yang dilakukan pada malam hari (19.00 WIB– 05.00 WIB) tidak berbeda dengan pengamatan yang dilakukan pada siang hari. Pengamatan cahaya dilakukan setiap 15 menit sekali. Pengamatan di dalam area flare akan dilakukan pada radius 0 m, 10 m, 25 m, 50 m, 75 m, 100 m, 125 m, 150 m dan 225 m jarak dari flare. Suhu. Pengamatan suhu dilakukan pada siang hari dan malam hari dengan
menngunakan satuan oC. pengukuran suhu dilakukan dengan mengukur suhu tanah dan suhu udara. Pengukuran suhu udara menggunakan anemometer sedangkan untuk pengukuran suhu tanah menggunakan Infa Red Thermometer
gun. Pengamatan suhu dilakukan dengan mengikuti pengamatan cahaya. Pengamatan dilakukan setiap 15 menit sekali. Pengamatan pada malam hari dilakukan pada radius 0 m, 10 m, 25 m, 50 m, 75 m, 100 m, 125 m, 150 m dan 225 m dari flare. Kecepatan angin. Kecepatan angin di ukur pada radius 0 m, 10 m, 25 m, 50 m, 75 m, 100 m, 125 m, 150 m dan 225 m dari flare. Pengukuran kecepatan angin menggunakan Anemometer dengan satuan meter persekon. Pengamatan kecepata angin dilakukan bersamaan dengan pengamatan cahaya dan pengamatan suhu tanah. Analisis data. Analisis data dilakukan untuk mengetahui hubungan antara besarnya nyala api flare dengan produksi tanaman karet dan tumbuhan disekitarnya dengan membuat histogram atara jarak tanaman karet dan produksi tanaman karet. Nyala api yang kecil sehingga nilai irradiasi, iluminasi, kuantum dan UV mendekati nol, maka anlisis data tidak akan mengacu terhadap jarak tanaman terhadap flare. Analisis data akan dilakukan dengan membagi tanaman berdasarkan klon yang terdapat dilapangan. Variabel yang digunakan merupakan variabel terukur selain variabel cahaya flare maupun cahaya matahari. Tanaman yang akan dibandingkan harus memiliki klon dan umur yang relatif sama, sehingga pembahasan akan dilakukan berdasarkan kliasifikasi klon dan umur tanaman. Analisis berupa analisis komponen utama dengan menggunakan SAS 17.