UJI DAYA ANTIBAKTERI EMULGEL ANTIACNE MINYAK SERAI WANGI JAWA (Cymbopogon winterianus) TERHADAP Staphylococcus
epidermidis
SKRIPSI
Disusun untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm)
Program Studi Farmasi
Oleh:
Bernadetta Arum Wijayanti
NIM :098114007
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
i
UJI DAYA ANTIBAKTERI EMULGEL ANTIACNE MINYAK SERAI WANGI JAWA (Cymbopogon winterianus) TERHADAP Staphylococcus
epidermidis
SKRIPSI
Disusun untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm)
Program Studi Farmasi
Oleh:
Bernadetta Arum Wijayanti
NIM : 098114007
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
vi
HALAMAN PERSEMBAHAN
Karya ini kupersembahkan kepada:
Ayahku Antonius Wijayadi (Alm) & Ibuku Maria Aluisia Siti Suwarni
Budheku Ceacilia Sitti Wardani
Masku Andreas Wibowo Nugroho
Adikku Klara Tyas Cahyawati
dan Alamamaterku yang kubanggakan
“
“
N
N
a
a
l
l
a
a
r
r
h
h
a
a
n
n
y
y
a
a
a
a
k
k
a
a
n
n
m
m
e
e
m
m
b
b
a
a
w
w
a
a
m
m
u
u
d
d
a
a
r
r
i
i
A
A
m
m
e
e
n
n
u
u
j
j
u
u
B
B
,
,
n
n
a
a
m
m
u
u
n
n
i
i
m
m
a
a
j
j
i
i
n
n
a
a
s
s
i
i
m
m
a
a
m
m
p
p
u
u
m
m
e
e
m
m
b
b
a
a
w
w
a
a
m
m
u
u
d
d
a
a
r
r
i
i
A
A
k
k
e
e
m
m
a
a
n
n
a
a
p
p
u
u
n”
n
”
-
-A
A
l
l
b
b
e
e
r
r
t
t
E
E
i
i
n
n
s
s
t
t
e
e
i
i
n
n
.
.
“
“
A
A
p
p
a
a
b
b
i
i
l
l
a
a
d
d
i
i
d
d
a
a
l
l
a
a
m
m
d
d
i
i
r
r
i
i
s
s
e
e
s
s
e
e
o
o
r
r
a
a
n
n
g
g
m
m
a
a
s
s
i
i
h
h
a
a
d
d
a
a
r
r
a
a
s
s
a
a
m
m
a
a
l
l
u
u
d
d
a
a
n
n
t
t
a
a
k
k
u
u
t
t
u
u
n
n
t
t
u
u
k
k
b
b
e
e
r
r
b
b
u
u
a
a
t
t
s
s
u
u
a
a
t
t
u
u
k
k
e
e
b
b
a
a
i
i
k
k
a
a
n
n
,
,
m
m
a
a
k
k
a
a
j
j
a
a
m
m
i
i
n
n
a
a
n
n
b
b
a
a
g
g
i
i
o
o
r
r
a
a
n
n
g
g
t
t
e
e
r
r
s
s
e
e
b
b
u
u
t
t
a
a
d
d
a
a
l
l
a
a
h
h
t
t
i
i
d
d
a
a
k
k
a
a
k
k
a
a
n
n
b
b
e
e
r
r
t
t
e
e
m
m
u
u
n
n
y
y
a
a
i
i
a
a
d
vii
PRAKATA
Puji dan syukur penulis haturkan kepada Tuhan Yesus Kristus dan Bunda
Maria atas rahmat dan penyertaan sehingga penulis dapat menyelesaikan
penelitian skripsi yang berjudul “Uji Daya Antibakteri Emulgel Antiacne Minyak
Serai Wangi Jawa (Cymbopogon winterianus) terhadap Staphylococcus
epidermidis” dengan baik dan lancar.
Penulis menyadari selama penyusunan skripsi ini, penulis telah
mendapatkan bantuan doa, bimbingan, arahan, saran dan kritik yang membangun
dari berbagai pihak. Pada kesempatan ini, penulis hendak menyampaikan
ungkapan terima kasih yang sebesar-besarnya kepada:
1. Ibu Maria Aluisia Siti Suwarni atas kerja keras dan kasih sayangnya
kepada penulis sebagai putrinya dan senantiasa menemani selama
penelitian di Balai Laboratorium Kesehatan Yogyakarta.
2. Bapak Ipang Djunarko, M. Sc., Apt. selaku Dekan Fakultas Farmasi
Universitas Sanata Dharma.
3. Ibu Agustina Setiawati, M. Sc., Apt. selaku dosen pembimbing yang selalu
memberikan arahan dan evaluasi semenjak pembuatan proposal penelitian
hingga selesainya penulisan skripsi ini.
4. Prof. Dr. C. J. Soegihardjo, Apt.selaku dosen penguji atas masukan, saran
dan kritik yang membangun kepada penulis.
5. Rini Dwiastuti, M.Sc., Apt.selaku dosen penguji atas masukan, saran dan
viii
6. Ibu Maria Dwi Budi Jumpowati, S. Si., atas masukan dan arahan dalam
bidang Mikrobiologi kepada penulis.
7. Bapak Musrifin, Bapak Agung, Bapak Wagiran, Bapak Parlan, Bapak
Kayat, dan Bapak Darto yang telah membantu selama penelitian
berlangsung.
8. Budhe, kakak, dan adik penulis yang telah memberikan motivasi
sepenuhnya hingga penulisan skripsi ini selesai.
9. Jenny Marina, Hermawan Deny, Johanes Putra Wicaksono, Wanda
Indriani dan Ina Juni Natasia atas dukungan selama penelitian.
10.Teman – teman Farmasi Sains dan Teknologi 2009 A Fakultas Farmasi
Universitas Sanata Dharma atas doa dan dukungan kepada penulis.
11.Victor Purnama Agung FanggidaE atas motivasi dan dukungan kepada
penulis.
12.Semua pihak yang tidak dapat penulis sebutkan satu per satu yang telah
memberikan doa, bantuan, dan dukungan selama penelitian dan
penyusunan skripsi.
Penulis menyadari begitu banyak kekurangan dalam naskah skripsi ini
mengingat keterbatasan pengetahuan dan kemampuan penulis. Oleh karena itu,
penulis mengharapkan saran dan kritik yang membangun untuk kemajuan
selajutnya.
ix
DAFTAR ISI
Halaman
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
PERNYATAAN PERSETUJUAN PUBLIKASI ... vi
PERNYATAAN KEASLIAN KARYA ... v
HALAMAN PERSEMBAHAN ... vi
PRAKATA ... vii
DAFTAR ISI ... ix
DAFTAR TABEL ... xiii
DAFTAR GAMBAR ... xv
DAFTAR LAMPIRAN ... xvii
INTISARI ... xix
ABSTRACT ... xx
BAB I. PENGANTAR ... 1
A. Latar Belakang ... 1
1. Rumusan Masalah ... 3
2. Keaslian Penelitian ... 3
3. Manfaat Penelitian ... 4
B. Tujuan Penelitian ... 4
BAB II. TINJAUAN PUSTAKA ... 5
x
B. Jerawat (Acne) ... 6
C. Staphylococcus epidermidis ... 8
D. Uji Potensi Antibakteri ... 10
1. Metode difusi ... 10
2. Metode dilusi ... 11
E. Gel dan Emulgel ... 12
1. Parafin cair ... 13
2. Aquades (air suling) ... 14
3. Carbopol 940 ... 14
4. Tween 80 dan Span 80 ... 17
5. Gliserin ... 20
6. Trieathanolamine (TEA) ... 21
7. Metil paraben ... 21
8. Propil paraben ... 22
F. Sifat Fisik Sediaan Topikal ... 22
1. Viskositas ... 22
2. Daya Sebar ... 23
G. Landasan Teori ... 23
H. Hipotesis ... 25
BAB III. METODE PENELITIAN ... 26
A. Jenis dan Rancangan Penelitian ... 26
B. Variabel Penelitian dan Definisi Operasional ... 26
xi
2. Definisi Operasional ... 27
C. Bahan dan Alat Penelitian ... 28
1. Bahan peneltian ... 28
2. Alat penelitian ... 29
D. Tatacara Penelitian ... 29
1. Identifikasi dan verifikasi minyak serai wangi Jawa ... 29
2. Pembuatan stok dan suspensi bakteriStaphylococcus epidermidis .... 30
3. Penanaman bakteri Staphylococcus epidermidis secara pour plate ... 31
4. Uji daya antibakteri minyak serai wangi Jawa terhadap Staphylococcus epidermidis dengan metode difusi sumuran ... 32
5. Penentuan Kadar Hambat Minimum (KHM) dan Kadar Bunuh Minimum (KBM) minyak serai wangi Jawa terhadap Staphylococcus epidermidis dengan metode dilusi padat ... 32
6. Pembuatan emulgel antiacne minyak serai wangi Jawa ... 33
7. Uji sifat fisik emulgel antiacne minyak serai wangi Jawa ... 35
8. Uji daya antibakteri emulgel antiacne minyak serai wangi Jawa terhadap Staphylococcus epidermidis dengan metode difusi sumuran 36 E. Analisis Hasil ... 36
BAB IV. HASIL DAN PEMBAHASAN ... 37
A. Identifikasi dan Verifikasi Minyak Serai Wangi Jawa ... 37
xii
C. Penentuan Kadar Hambat Minimum (KHM) dan Kadar Bunuh Minimum
(KBM) Minyak Serai Wangi Jawa terhadap Staphylococcus epidermidis
dengan Metode Dilusi Padat ... 43
D. Pembuatan Emulgel Antiacne Minyak Serai Wangi Jawa ... 46
E. Uji Sifat Fisik Emulgel Antiacne Minyak Serai Wangi Jawa ... 49
F. Uji Daya Antibakteri Emulgel Antiacne Minyak Serai Wangi Jawa terhadap Staphylococcus epidermidis dengan Metode Difusi Sumuran .. 51
BAB V. KESIMPULAN DAN SARAN ... 55
A. Kesimpulan ... 55
B. Saran ... 55
DAFTAR PUSTAKA ... 56
LAMPIRAN ... 60
xiii
DAFTAR TABEL
Halaman
Tabel 1. Hubungan rentang nilai HLB dengan penggunaan surfaktan ... 18
Tabel 2. Formula kontrol basis emulgel antiacne dan emulgel antiacne minyak
serai wangi Jawa dalam 200 g ... 34
Tabel 3. Hasil verifikasi minyak serai wangi Jawa ... 38
Tabel 4. Diameter zona hambat pertumbuhan Staphylococcus epidermidis yang
terbentuk oleh minyak serai wangi Jawa... 40
Tabel 5. Nilai probabilitas uji Shapiro-Wilk diameter zona hambat
pertumbuhan Staphylococcusepidermidis yang terbentuk oleh minyak
serai wangi Jawa... 41
Tabel 6. Hasil uji Wilcoxon diameter zona hambat pertumbuhan
Staphylococcus epidermidis yang terbentuk oleh minyak serai wangi
Jawa ... 42
Tabel 7. Hasil uji daya antibakteri minyak serai Jawa terhadap Staphylococcus
epidermidis secara dilusi padat ... 44
Tabel 8. Hasil penegasan uji daya antibakteri minyak serai Jawa terhadap
Staphylococcus epidermidis secara streakplate ... 45
Tabel 9. Hasil uji sifat fisik emulgel antiacne minyak serai wangi Jawa ... 50
Tabel 10. Diameter zona hambat yang terbentuk oleh emulgel antiacne minyak
serai wangi Jawa terhadap Staphylococcus epidermidis dengan metode
xiv
Tabel 11. Hasil uji Wilcoxon diameter zona hambat pertumbuhan
Staphylococcus epidermidis yang terbentuk oleh emulgel antiacne
xv
DAFTAR GAMBAR
Halaman
Gambar 1. Staphylococcus epidermidis dan infeksi akibat Staphylococcus
epidermidis pada kulit ... 8
Gambar 2. Staphylococcus epidermidis ATCC 12228 dan Staphylococcus epidermidis ATCC 35894 ... 9
Gambar 3. Struktur monomer dari carbopol ... 14
Gambar 4. Gambaran skematik crosslink dari polimer akrilik ... 15
Gambar 5. Gambaran skematik molekul carbopol dalam kondisi terurai dengan ikatan higrogen ... 16
Gambar 6. Gambaran skematik molekul carbopol dalam kondisi terurai setelah dinetralkan dengan suatu basa ... 16
Gambar 7. Struktur molekul dari tween 80 dan span 80 ... 17
Gambar 8. Gambaran skematik droplet minyak pada emulsi minyak dalam air 20 Gambar 9. Struktur molekul dari gliserin. ... 20
Gambar 10. Struktur molekul dari TEA ... 21
Gambar 11. Struktur molekul dari metil paraben ... 21
Gambar 12. Struktur molekul dari propil paraben ... 22
Gambar 13. Zona hambat pertumbuhan Staphylococcus epidermidis yang terbentuk oleh minyak serai wangi Jawa... 40
xvi
Gambar 15. Emulgel antiacne minyak serai wangi Jawa dengan konsentrasi 15%;
17,5%; dan 20% ... 49
Gambar 16. Zona hambat pertumbuhan Staphylococcus epidermidis yang
xvii
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Sertifikat analisis minyak serai wangi Jawa... 60
Lampiran 2. Sertifikat hasil uji Staphylococcus epidermidis ATCC 12228 .. 61
Lampiran 3. Verifikasi minyak serai wangi Jawa ... 62
Lampiran 4. Gambar uji daya antibakteri minyak serai wangi Jawa terhadap
Staphylococcus epidermidis dengan metode difusi padat ... 64
Lampiran 5. Pengukuran diameter zona hambat minyak serai wangi Jawa
terhadap Staphylococcus epidermidis ... 65
Lampiran 6. Hasil perhitungan statistik zona hambat minyak serai wangi Jawa
terhadap Staphylococcus epidermidis dengan metode difusi
sumuran ... 66
Lampiran 7. Hasil uji daya antibakteri minyak serai wangi Jawa terhadap
Staphylococcus epidermidis dengan metode dilusi padat ... 73
Lampiran 8. Hasil uji penegasan daya antibakteri minyak serai wangi Jawa
terhadap Staphylococcus epidermidis ... 75
Lampiran 9. Perhitungan rHLB sistem emulsi ... 76
Lampiran 10. Emulgel antiacne minyak serai wangi Jawa ... 78
Lampiran 11. Daya sebar dan viskositas emulgel antiacne minyak serai wangi
Jawa ... 80
Lampiran 12. Hasil uji daya antibakteri emulgel antiacne minyak serai wangi
Jawa terhadap Staphylococcus epidermidis dengan metode difusi
xviii
Lampiran 13. Hasil perhitungan statistik zona hambat emulgel antiacne minyak
serai wangi Jawa terhadap Staphylococcus epidermidis dengan
xix
INTISARI
Sitronelal, geraniol, sitronelol merupakan kandungan utama dalam minyak serai wangi Jawa yang berpotensi sebagai antibakteri. Minyak serai wangi Jawa dapat diformulasikan menjadi emulgel untuk meningkatkan penerimaan dan kenyamanan pengguna. Penelitian ini bertujuan untuk mengetahui adanya daya antibakteri minyak serai wangi Jawa dan emulgel antiacne minyak serai wangi Jawa terhadap pertumbuhan Staphylococcus epidermidis (salah satu penyebab jerawat) serta mengetahui kualitas sediaan emulgel minyak serai wangi Jawa berdasarkan sifat fisiknya.
Penelitian ini merupakan penelitian eksperimental murni dengan rancangan penelitian acak lengkap pola searah. Tahapan penelitian meliputi pengujian antibakteri minyak serai wangi Jawa dengan metode difusi sumuran (variasi konsentrasi 100%; 50%; 20%; 10% dan 5%); penentuan nilai KHM dan KBM minyak serai wangi Jawa terhadap Staphylococcus epidermidis dengan metode dilusi padat. Penelitian dilanjutkan dengan memformulasikan minyak serai wangi Jawa dalam emulgel dengan variasi konsentrasi 15%; 17,5%; dan 20%. Selanjutnya, dilakukan pengujian sifat fisik berupa viskositas dan daya sebar serta pengujian daya antibakteri emulgel antiacne minyak serai wangi Jawa dengan metode difusi sumuran. Daya antibakteri diukur berdasarkan diameter zona hambat yang dihasilkan dan dianalisis secara statistik dengan uji Kruskal-wallis dilanjutkan uji Wilcoxon. Data dianalisis menggunakan software R 2.14.1.
Hasil penelitian menunjukkan nilai KHM dan KBM minyak serai wangi Jawa terhadap Staphylococcus epidermidis berturut-turut 12,5% dan 15%. Emulgel antiacne minyak serai wangi Jawa memiliki sifat fisik 48 jam setelah formulasi serta memiliki daya antibakteri pada konsentrasi 15%. Hasil analisis statistik menggunakan uji Kruskal-wallis dilanjutkan uji Wilcoxon menunjukkan tidak adanya perbedaan yang bermakna antara daya antibakteri emulgel antiacne
minyak serai wangi Jawa terhadap Staphylococcus epidermidis pada variasi konsentrasi 15%; 17,5%; dan 20%.
xx
ABSTRACT
Citronellal, geraniol, and citronellol are the major chemical compounds of Java citronella oil that have potential as an antibacterial. Java citronella oil can be formulated into emulgel to enhance acceptance and convenience of users. This study aimed to determine the antibacterial potency of Java citronella oil and Java citronella oil antiacne emulgel against Staphylococcus epidermidis (one cause of acne) and to determine the quality of emulgel based on its physical properties.
This study is a purely experimental study with randomized study design complete unidirectional pattern. Stages of research were involving the evaluation of antibacterial potency of Java citronella oil against Staphylococcus epidermidis
which was done by using diffusion method (variations concentration are 100%; 50%; 20%; 10% and 5%); determine MIC and MBC value of Java citronella oil against Staphylococcus epidermidis which was done by using dillution method. Java citronella oil then formulated into emulgel with variations concentration to 15%; 17,5%, and 20%. Furthermore, the quality of emulgel based on its physical properties and the antibacterial potency of emulgel are determined. The data of measurement result of inhibition zones statistically analyzed with the Kruskal-Wallis test followed the Wilcoxon test. Data were analyzed using the R 2.14.1 software.
The results showed the value of MIC and MBC Java citronella oil against Staphylococcus epidermidis respectively 12.5% and 15%. Java citronella oil antiacne emulgel had good physical properties in 48-hours-storage and showed antibacterial activity at a concentration of 15%. Statistical analysis using the Kruskal-Wallis test followed Wilcoxon test showed no significant difference between the antibacterial potency of Java citronella oil antiacne emulgel against
Staphylococcusepidermidis at various concentration of 15%, 17.5% and 20%.
Keyword: antibacterial potency, Java citronella oil, emulgel,
BAB I PENGANTAR A. Latar Belakang
Jerawat (acne) merupakan salah satu masalah kulit yang pernah dialami
oleh sebagian besar masyarakat. Menurut Herawati dan Presley (2012) dalam
Pusat Informasi Obat dan Layanan Kefarmasian (PIOLK) Universitas Surabaya
menyebutkan catatan kelompok studi dermatologi kosmetika Indonesia yang
menunjukkan terdapat 60% penderita jerawat di Indonesia pada tahun 2006 dan
80% pada tahun 2007. Jerawat dapat terjadi hampir 85% pada remaja dan usia 12
– 25 tahun. Jerawat biasa terdapat pada area wajah, punggung, dada bagian atas,
dan bahu. Jerawat dapat mengurangi rasa kepercayaan diri seseorang sebab
memperburuk penampilannya sehingga perlu dilakukan suatu terapi jerawat.
Salah satu cara dalam terapi jerawat adalah dengan menggunakan suatu
antibakteri untuk menekan pertumbuhan bakteri flora normal penyebab jerawat
yang berlebihan. Bakteri-bakteri tersebut berkembang biak dengan baik dalam
kondisi lingkungan yang dihasilkan dari perpaduan sebum yang berlebihan dan
keratinosit sehingga menghasilkan mediator proinflamasi penyebab peradangan
(Breedlove, Bruck, Comerford, Donofrio, Labus, Mayer et al., 2006).
Penggunaan antibakteri yang sama dalam waktu yang cukup lama dengan
frekuensi yang tinggi menimbulkan mekanisme resistensi sekunder sehingga
diperlukan sumber antibakteri baru yang dapat digunakan untuk menghambat
pertumbuhan bakteri flora normal penyebab jerawat.
Adanya tren “back to nature” di kalangan masyarakat menyebabkan
terapi menggunakan bahan alam lebih diminati dibandingkan dengan bahan kimia
yang sintetis maupun semisintetis. Minyak serai wangi Jawa atau disebut juga
Java citronella oil disuling dari Cymbopogon winterianus Jowitt memiliki
kandungan utama sitronelal (monoterpen aldehida) dan geraniol serta sitronelol
(monoterpen alkohol) yang dapat dimanfaatkan sebagai antibakteri
(Lertsatitthanakorn, Taweechaisupapong, Arunyanart, Aromdee dan Khunkitti
(2010). Flora normal yang dapat menimbulkan jerawat antara lain
Propionibacterium acnes dan Staphylococcus epidermidis (Dunkin, 2013).
Menurut penelitian yang dilakukan oleh Lertsatitthanakorn et al. (2010), minyak
serai wangi Jawa memiliki Kadar Bunuh Minimum terhadap Propionibacterium
acnes sebesar 0,625 µL/mL dan Kadar Hambat Minimum sebesar 0,078 µL/mL.
Penelitian lain yang dilakukan oleh Diaz, Rossi, Mendonça, Silva, Ribon, Aguilar
et al. (2010) ekstrak etanol 80% serai wangi memiliki Kadar Hambat Minimum
terhadap Staphylococcus aureus sebesar 0,5 mg/mL. Penelitian mengenai aktivitas
antibakteri minyak serai wangi Jawa terhadap Staphylococcus epidermidis sampai
saat ini belum pernah dilakukan. Pada penelitian ini dilakukan penelitian
pendahuluan berupa uji daya antibakteri minyak serai wangi Jawa terhadap
Staphylococcus epidermidis secara in vitro dengan metode difusi sumuran.
Penggunaan minyak serai wangi Jawa secara langsung pada kulit
menimbulkan sensasi berminyak yang menurunkan kenyamanan pengguna.
Minyak serai wangi Jawa diformulasikan ke dalam emulgel untuk mengatasi hal
minyak dalam sistemnya pada tipe minyak dalam air dan gel yang dapat
memberikan sensasi dingin pada saat pengaplikasian. Terkait formulasi sediaan
emulgel antiacne minyak serai wangi Jawa perlu dilakukan uji sifat fisik dan daya
antibakteri emulgel antiacne minyak serai wangi Jawa terhadap Staphylococcus
epidermidis untuk melihat kualitas dari sediaan.
1. Rumusan Masalah
a. Apakah minyak serai wangi Jawa memiliki daya antibakteri terhadap
pertumbuhan Staphylococcus epidermidis?
b. Berapa Kadar Hambat Minimum (KHM) dan Kadar Bunuh Minimum
(KBM) minyak serai wangi Jawa terhadap pertumbuhan Staphylococcus
epidermidis?
c. Apakah sediaan emulgel antiacne minyak serai wangi Jawa memiliki
daya antibakteri terhadap pertumbuhan Staphylococcus epidermidis?
d. Apakah sediaan emulgel antiacne minyak serai wangi Jawa memiliki
kualitas yang baik berdasarkan sifat fisiknya?
2. Keaslian Penelitian
Sejauh penelusuran pustaka yang dilakukan penulis, penelitian mengenai
uji daya antibakteri emulgel antiacne minyak serai wangi Jawa terhadap
3. Manfaat Penelitian
a. Manfaat teoritis
Menambah informasi bagi ilmu pengetahuan mengenai
perkembangan formulasi emulgel antiacne minyak serai wangi Jawa untuk
menghambat pertumbuhan Staphylococcus epidermidis.
b. Manfaat praktis
Menyediakan alternatif formula emulgel antiacne minyak serai
wangi Jawa untuk mengatasi jerawat.
B. Tujuan Penelitian
1. Mengetahui adanya daya antibakteri minyak serai wangi Jawa terhadap
pertumbuhan Staphylococcus epidermidis.
2. Mengetahui Kadar Hambat Minimum (KHM) dan Kadar Bunuh Minimum
(KBM) minyak serai wangi Jawa terhadap pertumbuhan Staphylococcus
epidermidis.
3. Memastikan adanya daya antibakteri pada sediaan emulgel antiacne minyak
serai wangi Jawa terhadap pertumbuhan Staphylococcus epidermidis.
4. Mengetahui bahwa sediaan emulgel antiacne minyak serai wangi Jawa
5
BAB II
TINJAUAN PUSTAKA A. Minyak Serai Wangi Jawa
Minyak atsiri atau yang biasa dikenal sebagai essential oil merupakan
minyak hasil penyulingan uap/air yang larut dalam lemak, hidrofobik, dan
benar-benar menguap dari tempat aplikasi tanpa menghilangkan tanda yang terlihat atau
warna bahkan jika minyak asli berwarna. Minyak serai wangi (citronella oil)
diperoleh dari hasil penyulingan tanaman serai. Citronella oil dibagi menjadi 2
tipe yaitu Ceylon citronella oil dari Cymbopogon nardus dan Java citronella oil
dari Cymbopogon winterianus. Minyak serai wangi berwarna kuning pucat hingga
gelap (Balchin, 2006).
Minyak serai wangi Jawa mengandung sitronelal 32 – 45%, geraniol 12 –
18%, sitronelol 11 – 15%, geranil asetat 3,8%, sitronelil asetat 2 – 4%, limonene 2
– 5%, elemol dan alkohol sisquiterpen yang lain 2 – 5%, α-elemene dan α
-cadinene 2 – 5%, dan juga cubebene, calamenene, bourbonene, bisabolene,
eugenol, metil eugenol, isopulegol, nerol, linalool, metil heptanon, myrcene dan
α-pinene. Minyak serai wangi Jawa yang berkualitas baik biasanya mengandung
sitronelal, geraniol, dan sitrinelol masing-masing dari 38%, 16%, dan 12% (Peter,
2007). Standar mutu minyak serai menurut ketentuan EOA (Essential Oil
Association) USA No. 14 yaitu berat jenis ( ) 0,877 – 0,893; indeks bias
(nD20): 1,466 – 1,473; warna: kuning muda – kuning (Panda, 2003).
Minyak serai wangi Jawa biasanya digunakan sebagai bahan dalam
berupa pewangi dalam pembuatan deodorant, sabun, detergen, pembersih,
insektisida dan produk lainnya (Peter, 2007). Terlepas dari sifat repelan terhadap
serangga, minyak serai wangi (citronella oil) juga diketahui memiliki aktivitas
antibakteri melawan Propionibacterium acnes yang dapat menyebabkan jerawat.
Sebuah studi in vitro menunjukkan bahwa minyak serai wangi Jawa memiliki
aktivitas penangkapan radikal bebas yang sangat baik dan aksi antiinflamasi.
Sebagai tambahan, uji sensitifitas pada kulit dengan local lymph node assay
menyatakan bahwa minyak serai wangi pada konsentrasi 50% b/v diklasifikasikan
tidak sensitif. The United State of America Food and Administration (FDA)
mengelompokkan minyak serai wangi Jawa dalam kategori GRAS (Generally
RecognizedAsSafe) (Lertsatitthanakorn et al., 2010).
B. Jerawat (Acne)
Jerawat (acne) biasanya berhubungan dengan peningkatan sekresi sebum
yang berlebihan dan terjadi pada bagian tubuh yang memiliki kelenjar sebasea
seperti kepala, leher, dada, punggung, dan bahu (Breedlove et al., 2006). Setiap
tanda pada kulit yang dihasilkan oleh jerawat merupakan jenis lesi. Kasus yang
paling ringan, yaitu jerawat menghasilkan blackheads dan whiteheads.
Blackheads merupakan jerawat naik ke permukaan kulit dan terlihat hitam
sedangkan whiteheads merupakan jerawat yang tinggal di bawah permukaan kulit.
Lesi jerawat yang lebih bermasalah lainnya, yaitu papula (lesi meradang yang
biasanya muncul dengan bentuk kecil, benjolan merah muda); pustula (pimple,
menyakitkan, lesi padat berada jauh di dalam kulit); kista (dalam, menyakitkan,
lesi berisi nanah yang bisa menyebabkan bekas luka) (Anonim a, 2010).
Salah satu penyebab utama jerawat adalah peningkatan hormon seks,
terutama androgen seperti testosteron, yang terjadi selama masa pubertas.
Testosteron dikonversi dalam kulit menjadi dihidrotestosteron (DHT) oleh α
-reduktase, yang merangsang kelenjar sebasea untuk memperbesar dan
memproduksi lebih banyak sebum. Semakin banyak sebum yang diproduksi,
semakin buruk jerawat yang ditimbulkan. Selanjutnya, sebuah studi oleh Lee et al.
(2010) menunjukkan DHT yang juga diperkirakan terlibat dalam produksi sitokin
proinflamasi di jerawat (Chaudhuri dan Marchio, 2011).
Keratinisasi folikel abnormal juga terlibat dalam perkembangan jerawat
(Chaudhuri dan Marchio, 2011). Campuran keratinosit dan sebum dalam folikel
memberikan peluang untuk flora normal berkembang biak (DiPiro, Talbert, Yee,
Matzke, Wells, Posey, 2005). Bakteri flora normal tersebut mensekresi lipase
yang kemudian bereaksi dengan sebum menghasilkan asam lemak bebas yang
menginduksi adanya peradangan (Durkin, 2013). Persentase keberadaan
Staphylococcus epidermidis di kulit sekitar 85 – 100% menunjukkan bahwa
Staphylococcus epidermidis merupakan flora normal alami yang ada di kulit
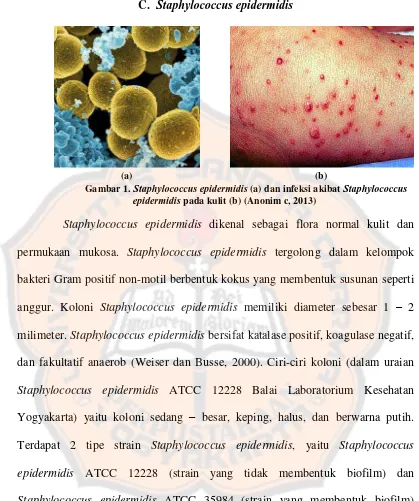
C. Staphylococcus epidermidis
(a) (b)
Gambar 1. Staphylococcus epidermidis (a) dan infeksi akibat Staphylococcus epidermidis pada kulit (b) (Anonim c, 2013)
Staphylococcus epidermidis dikenal sebagai flora normal kulit dan
permukaan mukosa. Staphylococcus epidermidis tergolong dalam kelompok
bakteri Gram positif non-motil berbentuk kokus yang membentuk susunan seperti
anggur. Koloni Staphylococcus epidermidis memiliki diameter sebesar 1 – 2
milimeter. Staphylococcus epidermidis bersifat katalase positif, koagulase negatif,
dan fakultatif anaerob (Weiser dan Busse, 2000). Ciri-ciri koloni (dalam uraian
Staphylococcus epidermidis ATCC 12228 Balai Laboratorium Kesehatan
Yogyakarta) yaitu koloni sedang – besar, keping, halus, dan berwarna putih.
Terdapat 2 tipe strain Staphylococcus epidermidis, yaitu Staphylococcus
epidermidis ATCC 12228 (strain yang tidak membentuk biofilm) dan
Staphylococcus epidermidis ATCC 35984 (strain yang membentuk biofilm)
(Motoyama, Yamaguchi, Matsumoto, Ichijo, Nagumo, Kagami et al., 2009).
Biofilm merupakan multiseluler ditunjukkan dengan adanya aglomerasi
permukaan suatu mikroorganisme. Biofilm berfungsi dalam resistensi terhadap
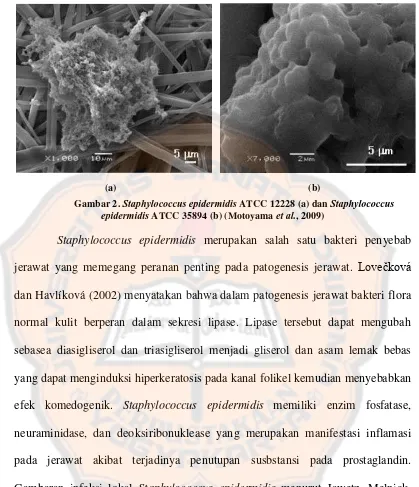
(a) (b)
Gambar 2. Staphylococcus epidermidis ATCC 12228 (a) dan Staphylococcus epidermidis ATCC 35894 (b) (Motoyama et al., 2009)
Staphylococcus epidermidis merupakan salah satu bakteri penyebab
jerawat yang memegang peranan penting pada patogenesis jerawat. Lovečková
dan Havlíková (2002) menyatakan bahwa dalam patogenesis jerawat bakteri flora
normal kulit berperan dalam sekresi lipase. Lipase tersebut dapat mengubah
sebasea diasigliserol dan triasigliserol menjadi gliserol dan asam lemak bebas
yang dapat menginduksi hiperkeratosis pada kanal folikel kemudian menyebabkan
efek komedogenik. Staphylococcus epidermidis memiliki enzim fosfatase,
neuraminidase, dan deoksiribonuklease yang merupakan manifestasi inflamasi
pada jerawat akibat terjadinya penutupan susbstansi pada prostaglandin.
Gambaran infeksi lokal Staphylococcus epidermidis menurut Jawetz, Melnick,
dan Adelberg (1986) yaitu suatu pimple, infeksi folikel rambut, atau suatu abses,
biasanya suatu peradangan yang hebat, terlokalisir, dan mengalami pernanahan
D. Uji Potensi Antibakteri
Menurut Farmakope Indonesia IV (1995), antibakteri adalah obat
pembasmi bakteri, khususnya bakteri yang merugikan manusia. Uji potensi
antibakteri digunakan dalam rangka pemilihan obat antimikroba yang efektif
untuk pengobatan atau pengendalian penyakit yang disebabkan oleh bakteri.
Menurut Agbor, Ma’ori, dan Opajobi (2011) metode yang umum dilakukan
adalah sebagai berikut:
1. Metode difusi
Berikut termasuk dalam metode difusi:
a. Metode disc diffusion.Metode ini paling banyak yang digunakan dalam
laboratorium klinis. Dalam uji ini, disk yang terbuat dari kertas diresapi
dengan sejumlah tertentu agen antibakteri yang diketahui konsentrasinya
dengan tepat. Disk tersebut diletakkan pada medium agar yang telah
diinokulasikan dengan bakteri uji. Senyawa antibakteri berdifusi ke dalam
medium sekitarnya membentuk gradien konsentrasi sekitar disk.
Pertumbuhan bakteri uji dihambat hingga terbentuk jarak dari disk dengan
konsentrasi dari senyawa tersebut kurang lebih sama dengan Konsentrasi
Hambat Minumum (KHM). Penghambatan pertumbuhan bakteri tampak
sebagai zona melingkar pada cawan agar. Diameter zona hambat yang
terbentuk proposional terhadap aktivitas antibakterinya.
b. Metode ditch.Metode ini dilakukan dengan cara menghilangkan potongan
agar dari cawan dan mengisi lubang yang terbentuk dengan agar yang telah
sedemikian hingga beberapa bakteri dapat diinokulasikan secara streak plate
tegak lurus pada agar yang telah mengandung antibakteri tersebut. Metode ini
cocok untuk uji suatu senyawa terhadap sejumlah besar bakteri. Kerugiannya
plat harus selalu baru tiap harinya. Metode ini tidak lagi digunakan dalam
laboratorium.
c. Metode punch hole diffusion. Metode ini terdiri dari pembuatan lubang
sumuran atau meletakkan suatu tabung dengan lobang di kedua sisinya pada
cawan agar. Agar tersebut sebelumnya telah diinokulasikan bakteri uji.
Masing-masing sumuran diisi dengan senyawa uji dengan konsentrasi yang
berbeda.
2. Metode dilusi
Metode dilusi digunakan untuk mengukur Kadar Hambat Minimum
(KHM) dan Kadar Bunuh Minimum (KBM). Kadar Hambat Minimal (KHM)
merupakan kadar minimal yang diperlukan untuk menghambat pertumbuhan
bakteri sedangkan Kadar Bunuh Minimum (KBM) merupakan kadar minimal
yang diperlukan untuk membunuh bakteri.
Berikut termasuk dalam metode dilusi (Anonim b, 2012) :
a. Broth dilution. Broth dilution merupakan sebuah teknik yang di dalamnya
terdapat suspensi bakteri uji pada konsentrasi optimal atau sesuai diuji dengan
berbagai konsentrasi dari suatu senyawa antibakteri dalam medium cair yang
telah ditentukan.
b. Agardilution. Agardilution meliputi penggabungan berbagai konsentrasi dari
koloni bakteri pada permukaan agar. Hasilnya sering dianggap paling dapat
diandalkan dalam penentuan nilai Kadar Hambat Minimum (KHM).
Kemampuan antibakteri dikatakan kuat apabila memiliki nilai KHM
antara 0,05 – 0,50 mg/mL, sedang apabila nilai KHM antara 0,6 – 1,50 mg/mL
dan lemah apabila di atas 1,50 mg/mL (Diaz et al., 2010). Pengukuran adanya
kekuatan antibiotik dan antibakteri berdasarkan besarnya zona hambat menurut
Suryawiria (1978) cit Moerfiah dan Supomo (2011) dipergunakan metode Davis
Stout dengan ketentuan sebagai berikut:
1) Sangat kuat (daerah hambat 20 mm atau lebih)
2) Kuat (daerah hambat 10 – 20 mm)
3) Sedang (daerah hambat 5 – 10 mm)
4) Lemah (daerah hambat kurang dari 5 mm).
E. Gel dan Emulgel
Menurut Farmakope Indonesia IV (1995), gel merupakan sistem
semipadat yang terdiri dari suspensi yang dibuat dari partikel anorganik yang kecil
atau molekul organik yang besar, terpenetrasi oleh suatu cairan. Gel dapat
digunakan untuk obat yang diberikan secara topikal atau yang dimasukkan ke
dalam lubang tubuh. Kelemahan utama pada gel adalah dalam penghantaran obat
yang bersifat hidrofobik kemudian dilakukan pendekatan berbasis emulsi untuk
mengatasi kelemahan tersebut. Ketika gel dan emulsi dikombinasikan bersama
menjadi suatu sediaan, sediaan tersebut dikenal sebagai emulgel (Panwar,
Emulgel (emulsion in gel) merupakan emulsi baik tipe oil-in-water
maupun water-in-oil yang dimodifikasikan dengan gelling agent. Emulgel
memiliki tingkat penerimaan yang tinggi sebagai sediaan topikal sebab memiliki
gabungan kelebihan dari gel dan emulsi (Bhanu, Shanmugam, Lakshmi, 2011).
Gel pada penggunaan topikal memiliki beberapa kelebihan menurut Voigt (1994)
yaitu kemampuan penyebaran pada kulit baik; efek dingin yang dijelaskan melalui
penguapan lambat dari kulit; kemudahan pencucian dengan air; dan pelepasan
obat yang baik sedangkan kelebihan emulsi memiliki kemampuan terpenetrasi
pada kulit yang tinggi (Bhanu et al., 2011). Monografi bahan yang digunakan
sebagai bahan tambahan emulgel adalah sebagai berikut.
1. Parafin cair
Parafin cair pada umumnya digunakan pada sediaan topikal. Dalam
emulsi parafin cair digunakan sebagai bahan tambahan pada tipe emulsi minyak
dalam air dengan konsentrasi 1,0 – 32,0%. Pemerian dari parafin cair yaitu
transparan, tidak berwarna, cairan berminyak yang kental, tidak berfluoresensi di
siang hari, hambar, tidak berbau ketika didinginkan, dan berbau samar ketika
dipanaskan. Titih didih > 360oC. Viskositas 110 – 230 mPas pada 20oC. Kelarutan
parafin cair yaitu praktis larut dalam etanol (95%), gliserin dan air; larut dalam
aseton, bensen, kloroform, karbon disulfida, eter, dan petroleum; mudah larut
dalam minyak atsiri dan minyak; pengecualian pada minyak jarak (Rowe,
Sheskey, Owen, 2006). Nilai rHLB parafin cair adalah 11,8 (Meher, Yadav, Sahu,
2. Aquades (air suling)
Bobot molekul air suling adalah 18,02. Air suling dibuat dengan
menyuling air yang dapat diminum. Pemerian dari air suling yaitu cairan jernih,
tidak berwarna, tidak berbau, dan tidak berasa (Direktorat Jendral Pengawas Obat
dan Makanan, 1979).
3. Carbopol 940
Gellingagent untuk keperluan farmasi dan kosmetik idealnya harus inert,
aman dan tidak reaktif dengan komponen formulasi lainnya. Dimasukkannya
gelling agent dalam formulasi harus menyediakan matriks seperti solid yang baik
selama penyimpanan, dapat dipecah dengan mudah ketika mengalami gaya geser
yang dihasilkan ketika dikeluarkan dari botol atau ketika tube diremas dan selama
aplikasi topikal (Liberman, Rieger, Banker, 1996). Gellingagent dapat digunakan
untuk menghasilkan berbagai macam konsistensi dari yang agak mengental
[image:35.595.102.516.221.598.2]hingga yang sangat keras (Winfield dan Richard, 2004).
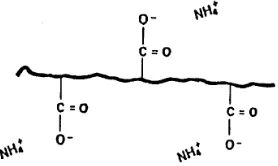
Gambar 3. Struktur monomer dari carbopol (Rowe et al., 2006)
Carbopol (carbomer) merupakan polimer sintetik dengan bobot molekul
yang tinggi dari asam akrilat yang membentuk ikatan silang (crosslink) dengan
sukrosa alil atau eter alil dari pentaeritritol. Pemerian dari carbopol yaitu berwarna
sediaan topikal carbopol digunakan sebagai gelling agent pada konsentrasi 0,5 –
2% (Rowe et al., 2006). Carbopol 940 memiliki sifat sangat kental dan sifat alir
[image:36.595.99.511.211.614.2]yang sangat singkat (Braun dan Rosen, 2000).
Gambar 4. Gambaran skematik crosslink dari polimer akrilik (Braun dan Rosen, 2000)
Pada kondisi kering, polimer carbopol berada dalam konfigurasi
gulungan (coiled) yang erat. Ketika didispersikan dalam air, terjadi sedikit
penguraian molekul disertai pengentalan yang minimal pada sistem (Braun dan
Rosen, 2000). Terdapat dua mekanisme yang dapat menyebabkan carbopol
menjadi benar-benar dalam keadaan terurai (uncoiled), pengentalan yang
maksimum, pembentukan dan stabilitasi emulsi, dan kinerja bioadhesi. Dua
mekanisme pengentalan dalam carbopol, yaitu:
a. Donor hidrosil Curteis (1991). Sistem ini menunjukkan penggunaan pelarut
yang mampu menyumbangkan gugus hidroksil. Ikatan higrogen yang
dihasilkan antara gugus karboksil dari carbopol dan gugus donor hidroksil
dari pelarut menyebabkan molekul menjadi terurai dan terjadilah proses
biasa digunakan sebagai donor hidroksil adalah gugus-gugus poliol (seperti
gliserin, propilenglikol, PEG dan sebagainya), gula alkohol (seperti mannitol,
sorbitol dan sebagainya), surfaktan nonionik dengan lima atau lebih
[image:37.595.99.516.214.622.2]gugus-gugus etoksi, dan sebagainya.
Gambar 5. Gambaran skematik molekul carbopol dalam kondisi terurai dengan ikatan hidrogen (Curteis, 1991)
b. Netralisasi (Chikhalikar dan Moorkath, 2002). Metode netralisasi merupakan
metode yang paling umum digunakan dengan cara menetralkan polimer
dengan suatu basa yang cocok. Netralisasi mengionisasi carbopol,
menghasilkan muatan negatif di sepanjang rantai polimer. Tolakan muatan
negatif menyebabkan molekul terurai sepenuhnya menjadi struktur yang
diperpanjang (extended structure). Reaksi ini berlangsung cepat dan
menghasilkan kinerja yang efisien. Beberapa agen penetral yang dapat
digunakan adalah natrium hidroksida, TEA, dan amonia.
[image:37.595.244.383.638.721.2]
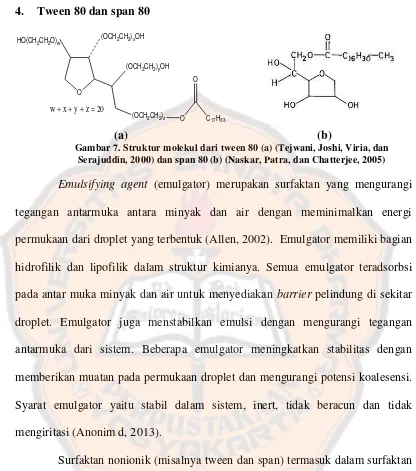
4. Tween 80 dan span 80
O
(OCH2CH2)z
HO(CH2CH2O)w (OCH2CH2)xOH
(OCH2CH2)yOH
O C17H33
O
w + x + y + z = 20
[image:38.595.98.514.123.594.2](a) (b)
Gambar 7. Struktur molekul dari tween 80 (a) (Tejwani, Joshi, Viria, dan Serajuddin, 2000) dan span 80 (b) (Naskar, Patra, dan Chatterjee, 2005)
Emulsifying agent (emulgator) merupakan surfaktan yang mengurangi
tegangan antarmuka antara minyak dan air dengan meminimalkan energi
permukaan dari droplet yang terbentuk (Allen, 2002). Emulgator memiliki bagian
hidrofilik dan lipofilik dalam struktur kimianya. Semua emulgator teradsorbsi
pada antar muka minyak dan air untuk menyediakan barrier pelindung di sekitar
droplet. Emulgator juga menstabilkan emulsi dengan mengurangi tegangan
antarmuka dari sistem. Beberapa emulgator meningkatkan stabilitas dengan
memberikan muatan pada permukaan droplet dan mengurangi potensi koalesensi.
Syarat emulgator yaitu stabil dalam sistem, inert, tidak beracun dan tidak
mengiritasi (Anonim d, 2013).
Surfaktan nonionik (misalnya tween dan span) termasuk dalam surfaktan
sintetik. Tipe ini digunakan dalam pembuatan baik tipe emulsi minyak dalam air
maupun tipe emulsi air dalam minyak pada penggunaan internal dan eksternal.
Kelebihan tipe nonionik dibandingkan dengan tipe anionik dan katioik yaitu tidak
rentan pada perubahan pH dan penambahan elektrolit. Hal ini menyebabkan
terhadap perubahan pH (Winfield dan Richard, 2004; Swarbrick, Rubino, dan
Rubino, 2006).
Kelarutan emulgator pada suatu fase dapat mempengaruhi tipe emulsi
yang dihasilkan. Jika emulgator lebih larut dalam air (hidrofilik) maka air menjadi
fase luar dan emulsi tipe minyak dalam air terbentuk. Sebaliknya, jika emulgator
lebih larut dalam minyak (lipofilik) maka minyak menjadi fase luar dan emulsi
tipe air dalam minyak terbentuk. Hal ini menyebabkan konsep bahwa tipe emulsi
berkaitan dengan keseimbangan antara sifat hidrofilik dan lipofilik dari surface
active emulsifying agent (Winfield dan Richard, 2004; Swarbrick et al., 2006).
Hidrophile-Lipophile Balances (HLB) merupakan perhitungan polaritas
surfaktan. Semakin rendah nilai HLB maka surfaktan bersifat lipofilik sebaliknya
semakin tinggi nilai HLB maka surfaktan bersifat hidrofilik (Kim, 2004). Nilai
HLB suatu surfaktan dihitung berdasarkan formula empiris. Rentang nilai HLB
[image:39.595.101.514.330.639.2]untuk surfaktan nonionik adalah 0 sampai 20 (Florence dan Attwood, 2006).
Tabel 1. Hubungan rentang nilai HLB dengan penggunaan surfaktan(Swarbrick et al., 2006)
Rentang HLB Penggunaan
0 – 3 Antifoamingagent
4 – 6 Emulgator A/M 7 – 9 Zat Pembasah 8 – 18 Emulgator M/A 13 – 15 Deterjen 10 – 18 Zat Pelarut
Tween 80 atau polisorbat 80 merupakan ester oleat dari sorbitol di mana
tiap molekul anhidrida sorbitolnya berkopolimerisasi dengan 20 molekul
etilenoksida. Tween 80 berupa cairan kental berwarna kuning dan agak pahit.
mineral dan minyak sayur. Tween 80 dapat digunakan sebagai emulgator pada
kosmetik dan sediaan farmasetis secara tunggal maupun kombinasi. Nilai HLB
tween 80 yaitu 15,0 (Rowe et al., 2006).
Span 80 atau sorbitan monooleat banyak digunakan dalam kosmetik,
produk makanan, dan sediaan farmasetis sebagai surfaktan nonionik lipofilik.
Umumnya, digunakan dalam formulasi farmasi sebagai pengemulsi agen dalam
penyusunan krim, emulsi, dan salep untuk aplikasi topikal. Ketika digunakan
sendiri, ester sorbitan menghasilkan emulsi dan mikroemulsi air dalam minyak
yang stabil tetapi sering digunakan dalam kombinasi dengan polisorbat pada
berbagai proporsi untuk menghasilkan variasi konsistensi emulsi atau krim. Span
80 berupa cairan kental berwarna kuning yang umumnya larut atau terdispersi
dalam minyak; juga larut pada sebagian besar pelarut organik. Dalam air,
walaupun tidak larut span umumnya dapat terdispersi. Nilai HLB span 80 yaitu
4,3 (Rowe et al., 2006).
Atlas-ICI menganjurkan untuk mengkombinasikan tween yang hidrofilik
dengan span yang lipofilik, dengan menggunakan variasi perbandingannya untuk
menghasilkan emulsi yang diinginkan. Misalnya, penggabungan molekul tween
40 dan span 80 dalam menstabilkan emulsi. Bagian hidrokarbon span 80 (sorbitan
monooleat) berada dalam droplet minyak dan radikal sorbitan berada dalam fase
air. Kepala sorbitan yang besar pada molekul span mencegah ekor-ekor
hidrokarbon bergabung rapat pada fase minyak. Ketika tween 40 (polioksietilen
sorbitan monopalmitat) ditambahkan, senyawa ini mengarah pada antarmuka
bersama dengan cincin sorbitan dan rantai polioksietilen, bersama dalam fase air.
Rantai hidrokarbon molekul tween 40 berada dalam globul minyak di antara rantai
span 80, dan menghasilkan gaya tarik menarik Van der Waals yang efektif.
Dengan cara ini, selaput antarmuka diperkuat dan stabilitas emulsi minyak dalam
[image:41.595.101.492.241.597.2]air ditingkatkan terhadap penggabungan partikel (Sinko, 2006).
Gambar 8. Gambaran skematik droplet minyak pada emulsi minyak dalam air, menunjukkan orientasi molekul tween dan span pada antarmukanya (Sinko, 2006)
5. Gliserin
Gambar 9. Struktur molekul dari gliserin (Rowe et al., 2006)
Gliserin digunakan sebagai humektan dalam sediaan topikal pada
konsentrasi ≤ 30%. Pemerian dari gliserin yaitu jernih, tidak berwarna, tidak
berbau, kental, larutan higroskopis, dan memiliki rasa manis. Kelarutan gliserin
yaitu larut dalam air, etanol, dan metanol; sedikit larut dalam aseton; dan praktis
6. Triethanolamine (TEA)
Gambar 10. Struktur molekul dari TEA (Rowe et al., 2006)
Dalam sediaan emulgel, TEA digunakan untuk menetralkan formula
yang mengandung carbopol hingga pH berada di antara 5,6 – 6,5 dan
menyebabkan terurainya rantai polimer dan membentuk struktur gel. Kisaran pH
tersebut ditentukan agar sesuai pH kulit (pH 5) dan mencapai stabilitas maksimum
carbopol dalam air (pH 6 – 8) (Shahin, Hady, Hammad, dan Mortada, 2011).
Pemerian dari TEA yaitu jernih, cairan kental tidak berwarna sampai kuning
pucat, memiliki sedikit bau amonia (Rowe et al., 2006).
7. Metil paraben
Gambar 11. Struktur molekul dari metil paraben (Rowe et al., 2006)
Metil paraben digunakan sebagai pengawet antimikroba dalam kosmetik,
produk makanan, dan sediaan farmasetis. Konsentrasi metil paraben dalam
sediaan topikal pada kisaran 0,02 – 0,3%. Pemerian dari metil paraben yaitu
[image:42.595.101.511.263.610.2]berbau; dan memiliki rasa sedikit terbakar. Metil paraben dapat digunakan secara
tunggal ataupun dikombinasikan dengan pengawet yang lain (Rowe et al., 2006).
[image:43.595.102.514.197.579.2]8. Propil paraben
Gambar 12. Struktur molekul dari propil paraben (Rowe et al., 2006)
Propil paraben digunakan sebagai pengawet antimikroba dalam
kosmetik, produk makanan, dan sediaan famasetis. Konsentrasi propil paraben
dalam sediaan topikan pada kisaran 0,01 – 0,6%. Pemerian dari propil paraben
yaitu putih, kristal, tidak berasa, dan tidak berbau. Propil paraben dapat digunakan
secara tunggal ataupun dikombinasikan dengan pengawet yang lain (Rowe et al.,
2006).
F. Sifat Fisik Sediaan Topikal 1. Viskositas
Viskositas merupakan tahanan suatu sistem untuk mengalir pada suatu
tekanan yang diberikan. Makin kental suatu cairan, makin besar gaya yang
diperlukan untuk membuat cairan tersebut dapat mengalir dengan laju tertentu
(Sinko, 2006). Viskositas termasuk faktor yang penting dalam karakteristik
sediaan semisolid, viskositas suatu sediaan menentukan lama tinggal sediaan pada
kulit sehingga obat dapat terpenetrasi dengan baik (Garg, Aggarwal, Garg, dan
2. Daya sebar
Daya sebar (spreadability) merupakan istilah yang digunakan untuk
menunjukkan luasnya wilayah dimana sediaan topikal mudah menyebar pada
aplikasi di kulit atau bagian yang terkena (Mishra, Murthy, Pasa, dan Nayak,
2011). Daya sebar, pada prinsipnya, berkaitan dengan sudut kontak dari setetes
cairan atau sediaan semipadat pada substrat terstandar dan berkaitan dengan
koefisien gesekan. Daya sebar merupakan karakteristik penting dari formulasi ini
dan bertanggung jawab untuk transfer dosis yang tepat ke tempat target,
kemudahan aplikasi pada substrat, pengeluaran dari kemasan, dan yang paling
penting, kenyamanan konsumen (Garg et al., 2002).
Parallel-plate method adalah metode yang paling banyak digunakan
untuk menentukan dan mengukur daya sebar sediaan semipadat. Keuntungan dari
metode ini adalah sederhana dan relatif murah. Selain itu, dapat dirancang dan
dibuat sesuai dengan kebutuhan peneliti mengenai jenis data yang dibutuhkan,
rute administrasi, luas permukaan yang dibahas, dan membran model untuk
dipertimbangkan. Di sisi lain, metode ini kurang tepat dan sensitif, dan data yang
dihasilkannya harus ditafsirkan secara manual dan disajikan (Garg et al., 2002).
G. Landasan Teori
Jerawat disebabkan oleh produksi sebum yang berlebihan serta adanya
hiperkeratinasi yang menyebabkan folikel tersumbat sehingga menciptakan
lingkungan yang kondusif bagi flora normal kulit seperti Staphylococcus
berinteraksi dengan sebum menghasilkan suatu asam lemak bebas. Asam lemak
bebas berlebih inilah selanjutnya mempromotori adanya peradangan pada kulit
yang menyebabkan terbentuknya jerawat.
Salah satu usaha untuk menyembuhkan jerawat adalah dengan
mengurangi jumlah bakteri penyebab jerawat yang berkembang biak secara
berlebihan. Tiga komponen utama yang terkandung pada minyak serai wangi
Jawa berupa sitronelal, geraniol dan sitronelol berpotensi untuk membunuh
bakteri termasuk bakteri penyebab jerawat, yaitu Staphylococcus epidermidis.
Oleh karenanya, minyak serai wangi Jawa berpotensi untuk diformulasikan ke
dalam suatu sediaan antiacne. Pengujian daya antibakteri ditunjukkan dengan
diameter zona hambat dengan metode difusi sumuran serta Konsentrasi Hambat
Minimum (KHM) dan Konsentrasi Bunuh Minimum (KBM) dengan metode
dilusi padat. Pengujian ini dilakukan untuk memastikan bahwa minyak serai
wangi Jawa dapat menghambat pertumbuhan Staphylococcus epidermidis.
Penggunaan emulgel diharapkan dapat menutupi ketidaknyamanan dalam
penggunaan minyak serai wangi Jawa secara langsung. Hal ini dikarenakan
minyak serai wangi yang memiliki sensasi berminyak tertutupi dalam sistem
emulsi tipe minyak dalam air kemudian dengan adanya suatu gelling agent dapat
memberikan sensasi dingin pada saat pengaplikasian. Pembuatan emulgel diawali
dengan pembentukan emulsi tipe minyak dalam air dengan minyak serai wangi
Jawa dan parafin sebagai fase minyak. Emulgator yang digunakan berupa
gelling agent yang ditambahkan pada emulsi terurai polimernya sehingga
konsistensinya mengental setelah ditambahkan TEA.
H. Hipotesis
Emulgel antiacne minyak serai wangi Jawa memiliki daya antibakteri
BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini merupakan penelitian eksperimental murni dengan
rancangan penelitian acak lengkap pola searah. Penelitian ini dilakukan di
Laboratorium Teknologi dan Formulasi Padat Fakultas Farmasi Universitas
Sanata Dharma, serta Balai Laboratorium Kesehatan Yogyakarta.
B. Variabel Penelitian dan Definisi Operasional 1. Variabel penelitian
a. Variabel bebas. Minyak serai wangi Jawa dengan variasi konsentrasi
100%; 50%; 20%; 10%; dan 5%. Konsentrasi minyak serai wangi Jawa
dalam emulgel.
b. Variabel tergantung. Daya antibakteri minyak serai wangi Jawa dan
emulgel antiacne minyak serai wangi Jawa diukur dari diameter zona
hambat yang terbentuk terhadap Staphylococcus epidermidis. Sifat fisik
emulgel antiacne minyak serai wangi Jawa meliputi viskositas dan daya
sebar.
c. Variabel Pengacau Terkendali. Asal bahan (minyak serai wangi Jawa
Indaroma), wadah penyimpanan (botol kaca), diameter sumuran (6 mm),
bakteri uji (Staphylococcus epidermidis ATCC 12228 Balai Laboratorium
Kesehatan Yogyakarta) konsentrasi suspensi bakteri uji setara dengan
kekeruhan larutan standar Mac. Farland 0,5 (1 x 108 CFU/mL), volume
suspensi bakteri uji yang diinokulasikan ke dalam media (1 mL), waktu
penyimpanan sediaan emulgel (48 jam), volume minyak serai Jawa yang
dimasukkan ke dalam lubang sumuran (50 L), waktu inkubasi (24 jam),
suhu inkubasi (37oC).
d. Variabel Pengacau Tak Terkendali. Kriteria tanaman serai wangi Jawa
yang digunakan produsen sebagai sumber minyak serai wangi Jawa serta
metode destilasinya.
2. Definisi Operasional
a. Minyak serai wangi Jawa merupakan minyak atsiri dari tanaman serai
wangi Jawa (Cymbopogon winterianus) yang diperoleh dari CV Indaroma.
b. Emulgel antiacne minyak serai wangi Jawa merupakan sediaan topikal
semipadat yang dibuat dengan bahan aktif berupa minyak serai wangi
Jawa sesuai formula yang ditentukan dan dibuat sesuai prosedur
pembuatan emulgel pada penelitian ini.
c. Kontrol basis emulgel antiacne adalah sediaan topikal semipadat yang
dibuat tanpa bahan aktif minyak serai sesuai prosedur pembuatan emulgel
pada penelitian ini.
d. Daya antibakteri sediaan emulgel antiacne minyak serai wangi Jawa
adalah kemampuan sediaan emulgel antiacne minyak serai wangi Jawa
untuk menghambat atau membunuh Staphylococcus epidermidis yang
ditunjukkan oleh zona hambat yang dihasilkan kemudian dengan
e. Staphylococcus epidermidis merupakan kultur murni bakteri uji
Staphylococcus epidermidis ATCC 12228 yang diperoleh dari Balai
Laboratorium Kesehatan Yogyakarta.
f. Zona hambat merupakan zona jernih di sekitar sumuran yang telah
dimasukkan dengan minyak serai wangi Jawa atau emulgel yang dapat
menghambat pertumbuhan atau membunuh Staphylococcus epidermidis
dibandingkan dengan kontrol negatif.
g. Daya sebar merupakan kemampuan emulgel untuk tersebar merata pada
kulit saat diaplikasikan, sehingga obat dapat terpenetrasi dengan baik.
Daya sebar dinyatakan dalam diameter penyebaran sediaan. Rentang
diameter daya sebar yang diharapkan 3 – 5 cm.
h. Viskositas emulgel merupakan tingkat kekentalan emulgel yang dapat
diaplikasikan dengan baik di kulit. Rentang viskositas yang diharapkan
150 – 250 d.Pa.s.
C. Bahan dan Alat Penelitian 1. Bahan penelitian
Bahan yang digunakan dalam penelitian ini adalah minyak serai wangi
Jawa yang diperoleh dari CV Indaroma, bakteri uji Staphylococcus epidermidis
ATCC 12228 yang diperoleh dari Balai Laboratorium Kesehatan Yogyakarta,
Media MHA (Muller-Hinton Agar), media BHIB (Brain Heart Infusion Broth),
(Bratachem), carbopol 940 (Bratachem), TEA (Bratachem), parafin cair
(Bratachem), tween 80 (Bratachem), span 80 (Bratachem), dan aquades.
2. Alat penelitian
Alat yang digunakan dalam penelitian ini adalah hand refractometer,
piknometer, cawan petri (Pyrex), Biological Safety Cabinet (ESCO), jarum ose,
pelubang sumuran, cutton bud steril, autoklaf, neraca analitik, densichek (Vitek),
mixer (Philip Type 1500/A), viscometer Rion seri VT O4 (RION-JAPAN),
lempeng kaca pengukur daya sebar, jangka sorong, mikropipet, waterbath, dan
alat-alat gelas lainnya.
D. Tatacara Penelitian 1. Identifikasi dan verifikasi minyak serai wangi Jawa
Bahan yang diidentifikasi pada penelitian ini, yaitu: minyak serai wangi
Jawa yang merupakan minyak atsiri dari tanaman serai wangi Jawa (Cymbopogon
winterianus) diperoleh dari CV Indaroma Yogyakarta dan telah diuji identitasnya.
Verifikasi minyak serai wangi Jawa meliputi:
a. Pengamatan organoleptis. Pengamatan organoleptis berupa pengamatan
bentuk dan warna minyak serai wangi Jawa.
b. Indeks bias. Indeks bias minyak serai wangi Jawa diukur dengan
menggunakan hand refractometer. Penutup prisma dibuka kemudian minyak
serai wangi Jawa diteteskan 1 atau 2 tetes sampel pada prisma utama, penutup
atau “3” diatur dengan memutar knob hingga tanda “•” tergantung dari
konsentrasi sampel yang diuji. Berikut adalah jarak jangkauan:
“1”: 1,333 – 1,404 (skala sebelah kiri)
“2”: 1,404 – 1,468 (skala tengah)
“3”: 1,468 – 1,520 (skala sebelah kanan)
Ujung refraktometer diarahkan ke arah cahaya yang terang, dilihat
melalui lensa sambil diputar-putar sampai skala terlihat jelas. Tampak garis
batas yang memisahkan sisi yang terang dan gelap pada bagian atas dan bawah.
Jika garis batas berwarna atau tidak jelas, maka ring diputar untuk
menghilangkan warna hingga garis batas terlihat jelas.
c. Bobot Jenis. Piknometer 10 mL ditimbang dalam keadaan kosong dan bersih.
Piknometer 10 mL diisi air suling. Suhu diturunkan hingga 23oC kemudian
dinaikkan perlahan hingga 25oC. Permukaan air diatur sampai puncak kapiler
kemudian pipa kapiler ditutup. Setelah mencapai suhu kamar, dinding luar
piknometer diusap dan ditimbang. Hal yang sama dilakukan pada minyak
serai wangi Jawa. Bobot jenis minyak atsiri serai sama dengan
kerapatan minyak serai wangi Jawa dibagi kerapatan air pada suhu 25oC.
2. Pembuatan stok dan suspensi bakteri Staphylococcus epidermidis
Sebelum pembuatan stok perlu dilakukan pengaktifan Staphylococcus
epidermidis. Media BHIB dilarutkan dan disterilkan dengan menggunakan
autoklaf pada suhu 121oC selama 15 menit. Setelah steril, media BHIB
dimasukkan dalam tabung sebanyak 5 mL. Biakan murni Staphylococcus
suhu 37oC dalam inkubator. Langkah ini dilakukan sekali lagi setelah 24 jam
inkubasi.
Media TSA dilarutkan dan disterilkan dengan menggunakan autoklaf pada
suhu 121oC selama 15 menit. Setelah steril, media TSA dimasukkan dalam tabung
sebanyak 5 mL, dibiarkan memadat dalam keadaan miring. Diambil 1 ose biakan
murni Staphylococcus epidermidis dan diinokulasikan, diinkubasi selama 24 jam
pada suhu 37oC dalam inkubator. Hasil kultur digunakan sebagai stok bakteri
Staphylococcus epidermidis.
Pembuatan suspensi bakteri dilakukan dengan cara diambil 1 ose koloni
bakteri Staphylococcus epidermidis dari stok bakteri, dimasukkan ke dalam
tabung reaksi yang telah berisi media BHIB steril, inkubasi selama 24 jam pada
suhu 37oC dalam inkubator. Selanjutnya, kekeruhan suspensi bakteri
Staphylococcus epidermidis disesuaikan dengan standar Mac Farland 0,5 dengan
pengencer NaCl fisiologis steril (konsentrasi bakteri 108 CFU/mL).
3. Penanaman bakteri Staphylococcus epidermidis secara pour plate
Suspensi bakteri diinokulasikan sebanyak 1 mL pada MHA steril cair.
Setelah di-vortex, campuran tersebut dimasukkan ke cawan petri. Media yang
telah memadat dilubangi menggunakan pelubang sumuran dengan diameter 6 mm
secara aseptis sebagai tempat kontrol positif, kontrol negatif, dan minyak serai
wangi Jawa dengan berbagai variasi konsentrasi. Pembuatan lubang sumuran
dilakukan hingga dasar petri kemudian dilakukan penambalan dengan
4. Uji daya antibakteri minyak serai wangi Jawa terhadap Staphylococcus epidermidis dengan metode difusi sumuran
a. Penentuan konsentrasi minyak serai wangi Jawa. Minyak serai wangi Jawa
dibuat dalam beberapa seri konsentrasi yaitu 100%; 50%; 20%; 10%; dan
5% dengan menggunakan pelarut parafin cair.
b. Uji daya antibakteri minyak serai wangi Jawa terhadap Staphylococcus
epidermidis secara difusi sumuran. Minyak serai wangi Jawa dengan
berbagai konsentrasi sebanyak 50 L diletakkan pada masing-masing
lubang sumuran yang tersedia secara aseptis. Kontrol positif yang
digunakan adalah Klindamisin fosfat 0,06% dan kontrol negatif yang
digunakan adalah parafin cair. Diinkubasi selama 24 jam pada suhu 37oC,
kemudian diamati hasilnya. Zona hambat diukur dengan jangka sorong
dengan cara mengukur zona jernih yang terbentuk dikurangi dengan
diameter dari sumuran. Diameter zona hambat yang dihasilkan sebagai
dasar untuk mengamati daya antibakteri yang dibandingkan dengan
kontrol positif dan kontrol negatif. Dilakukan replikasi sebanyak tiga kali.
5. Penentuan Kadar Hambat Minimum (KHM) dan Kadar Bunuh Minimum (KBM) minyak serai wangi Jawa terhadap Staphylococcus epidermidis dengan metode dilusi padat
Minyak serai wangi Jawa dengan kadar tertentu, sesuai dengan hasil pada
uji sebelumnya, sebanyak 1 mL ditambahkan pada 1 mL suspensi bakteri uji yang
telah disetarakan dengan standar Mac Farland 0,5. Kemudian ditambahkan pada
20 mL media MHA steril cair. Selanjutnya, dituang dalam cawan petri steril
secara pour plate. Pengamatan dilakukan setelah diinkubasikan selama 24 jam
KHM dan KBM dapat diketahui dengan membandingkan kejernihan media yang
diinokulasikan larutan uji dengan kontrol negatif parafin cair dan kontrol
pertumbuhan bakteri secara visual. Setelah didapatkan media pertumbuhan yang
jernih, dilakukan pengujian berikutnya dengan melakukan menginokulasikan
bakteri dari setiap media yang jernih ke media steril yang baru secara streak plate.
KHM merupakan konsentrasi terkecil yang mampu menghambat pertumbuhan
bakteri yang ditunjukkan dengan media pertumbuhan yang jernih tetapi masih ada
pertumbuhan pada hasil streak. KBM merupakan konsentrasi terkecil yang dapat
membunuh bakteri, ditandai dengan tidak adanya pertumbuhan dari hasil streak
yang menandakan bahwa bakteri uji mati karena larutan uji dengan konsentrasi
tersebut. Kontrol sterilitas dibuat dengan cara menuangkan media MHA steril cair
tanpa penambahan Staphylococcus epidermidis pada cawan petri steril dan setelah
dibiarkan memadat dilakukan pelubangan pada tengah media. Kontrol
pertumbuhan bakteri dibuat dengan cara parafin cair sebanyak 1 mL ditambahkan
pada suspensi bakteri uji yang telah disetarakan dengan standar Mac Farland 0,5.
Ditambahkan pada 20 mL media MHA steril cair. Selanjutnya, dituang dalam
cawan petri steril secara pourplate.
6. Pembuatan emulgel antiacne minyak serai wangi Jawa
a. Formula. Formula yang digunakan pada penelitian ini mengacu pada
formula emulgel chlorphenesin (Mohamed, 2004). Formula untuk 100 g
R/ Chlorphenesin 0,50 g
Carbopol 934 1,00 g
Parafin cair 5,00 g
Tween 20 0,60 g
Span 20 0,90 g
Propilen glikol 5,00 g
Etanol 2,50 g
Metil paraben 0,03 g
Propil paraben 0,01 g
Aquades ad 100,00 g
[image:55.595.101.515.95.682.2]Formula tersebut dilakukan modifikasi sebagai berikut.
Tabel 2. Formula kontrol basis emulgel antiacne dan emulgel antiacne minyak serai wangi Jawa dalam 200 g
Material (dalam 200 gram) Kontrol basis emulgel antiacne Emulgel antiacne minyak serai wangi Jawa 15% Emulgel antiacne minyak serai wangi Jawa 17,5% Emulgel antiacne minyak serai wangi Jawa 20% Minyak serai
wangi Jawa - 30,00 g 35,50 g 40,00 g Parafin cair 40,00 g 10,00 g 5,50 g -
Carbopol 940 1,00 g 1,00 g 1,00 g 1,00 g Tween 80 31,20 g 31,20 g 31,20 g 31,20 g Span 80 8,80 g 8,80 g 8,80 g 8,80 g Gliserin 4,00 g 4,00 g 4,00 g 4,00 g TEA 1,50 g 1,50 g 1,50 g 1,50 g Metil paraben 0,36 g 0,36 g 0,36 g 0,36 g Propil paraben 0,04 g 0,04 g 0,04 g 0,04 g Aquades 113,60 g 113,60 g 113,60 g 113,60 g
b. Pembuatan Emulgel. Carbopol 940 dikembangkan dalam 70 mL aquades
cair, dan span 80) dan fase air (sisa aquades, metil paraben, gliserin, dan
tween 80) disiapkan secara terpisah dengan mencampurkan
masing-masing komponennya pada suhu 60oC. Fase minyak ditambahkan pada
fase air kemudian dicampur dengan menggunak