PENGARUH VARIASI KOMPOSISI PEG 400 - PEG 4000 PADA AKTIVITAS ANTIBAKTERI SALEP MINYAK SEREH WANGI JAWA
(Cymbopogon winterianus) TERHADAP BAKTERI Staphylococcus epidermidis ATCC 12228
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat
Memperoleh Gelar Sarjana Farmasi (S. Farm)
Program Studi Farmasi
Oleh :
Fransiskus Asisi Dian Kristianto NIM 108114067
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
2014
i
PENGARUH VARIASI KOMPOSISI PEG 400 - PEG 4000 PADA AKTIVITAS ANTIBAKTERI SALEP MINYAK SEREH WANGI JAWA
(Cymbopogon winterianus) TERHADAP BAKTERI Staphylococcus epidermidis ATCC 12228
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat
Memperoleh Gelar Sarjana Farmasi (S. Farm)
Program Studi Farmasi
Oleh :
Fransiskus Asisi Dian Kristianto NIM 108114067
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
2014
ii
iii
Pengesahan Skripsi Berjudul
iv
v
vi
HALAMAN PERSEMBAHAN
Karya ini kupersembahkan untuk: Tuhanku Yesus Kristus, Kedua orang tuaku Thomas Dwi Heru Santosa dan Yohana Parjinah, Saudaraku Filipus Cahyo Kristianto,
Celly Brita dan SemuaTeman-teman dan kerabatku
dan Almamaterku tercinta.
vii PRAKATA
Puji syukur kepada Tuhan atas segala berkat, kasih karunia dan penyertaan-Nya sehingga penyusunan skripsi dengan judul “Pengaruh Variasi Komposisi PEG 400 - PEG 4000 Pada Aktivitas Antibakteri Salep Sereh Wangi Jawa (Cymbopogon winterianus) Terhadap Bakteri Staphylococcus epidermidis ATCC 12228” dapat diselesaikan dengan baik. Skripsi ini disusun untuk memenuhi persyaratan dalam meraih gelar Sarjana Farmasi (S.Farm.) di Fakultas Farmasi, Universitas Sanata Dharma, Yogyakarta.
Dalam mengerjakan penelitian hingga terselesaikannya skripsi ini, penulis telah mendapatkan banyak bantuan doa, semangat, arahan, saran, serta kritik yang membangun dari berbagai pihak. Oleh karena itu, dalam kesempatan ini, penulis ingin menyampaikan ungkapan terima kasih kepada :
1. Orang tua, Bapak Thomas Dwi Heru santoso dan Ibu Yohana Fransisca Parjinah, atas pengertian, dukungan doa, dan segala bantuan yang tak terhingga yang telah diberikan kepada penulis selama ini dan hingga detik ini. 2. Dekan Fakultas Farmasi Universitas Sanata Dharma.
3. Ibu Christofori Maria Ratna Rini Nastiti, M.Pharm., Apt. selaku Dosen Pembimbing yang dengan sabar memberikan arahan, saran, serta semangat kepada penulis selama penelitian hingga terselesaikannya skripsi ini.
4. Ibu Erna dan Ibu Damiana sebagai dosen penguji atas segala saran dan masukan mengenai penelitian ini.
viii
5. Ibu Maria Dwi Budi Jumpowati, S.Si. selaku Dosen Fakultas Farmasi Universitas Sanata Dharma atas waktunya untuk memberikan masukan dan arahannya dalam bidang mikrobiologi kepada penulis selama penelitian. 6. Seluruh Dosen Fakultas Farmasi Universitas Sanata Dharma, Yogyakarta
yang telah mendampingi dan berbagi ilmu selama penulis menempuh pendidikan di Fakultas Farmasi Universitas Sanata Dharma, Yogyakarta. 7. Seluruh staf laboratorium, staf kebersihan, dan staf keamanan Fakultas
Farmasi Universitas Sanata Dharma, Yogyakarta, terutama Bapak Mukminin dan Bapak Musrifin yang telah membantu penulis selama penelitian hingga selesainya skripsi ini.
8. Filipus Cahyo Kristianto selaku saudara kandung penulis atas doa, kasih sayang, dan dorongan, serta motivasi membangun kepada penulis. Terima kasih.
9. Eva Monalisa selaku saudara sepupu atas segala motivasi dan doanya sehingga penulis selalu semangat dalam menjalankan proses skripsi.
10.Angga Zakharia, Sekar Wulan dan Felicia Aniska selaku teman satu kelompok atas kerja sama, motivasi dan semangat yang diberikan saat menyelesaikan penelitian ini.
11.Celly Brita atas kasih sayang, semangat, dan motivasi yang telah diberikan serta selalu ada dalam suka maupun duka.
ix
serta kebersamaan yang luar biasa kepada penulis selama lebih dari empat tahun. Kalian adalah keluarga kedua selama penulis hidup sebagai mahasiswa di Fakultas Farmasi Universitas Sanata Dharma Yogyakarta
13.Semua pihak yang tidak dapat disebutkan satu per satu yang telah membantu penulis dalam menyelesaikan pendidikan di perguruan tinggi ini.
Penulis menyadari bahwa masih banyak kekurangan dalam penyusunan skripsi ini, sehingga kritik dan saran yang membangun untuk perubahan yang lebih baik. Semoga skripsi ini dapat bermanfaat bagi pembaca.
x DAFTAR ISI
Halaman
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
PERNYATAAN KEASLIAN KARYA ... iv
PERNYATAAN PERSETUJUAN PUBLIKASI ... v
xi
B. Minyak Atsiri ... 8
C. Minyak Sereh Wangi Jawa ... 9
D. Sitronelal ... 11
E. Geraniol ... 11
F. Staphylococcus epidermidis ... 12
G. Anti bakteri ... 13
A. Jenis dan Rancangan Penelitian ... 22
B. Variabel Penelitian dan Definisi Operesional ... 22
C. Alat dan Bahan ... 24
D. Skema Kerja ... 24
E. Analisis Hasil ... 33
BAB IV. HASIL DAN PEMBAHASAN ... 34
A. Identifikasi dan Verifikasi Minyak Sereh Wangi Jawa ... 34
B. Uji Aktivitas Antibakteri Minyak Sereh Wangi Jawa ... 36
C. Formulasi Sediaan Salep Minyak Sereh Wangi Jawa ... 40
xii
E. Uji Sterilitas Salep Minyak Sereh Wangi Jawa ... 47
F. Uji Aktivitas Antibakteri Salep Minyak Sereh Wangi Jawa ... 48
BAB V. KESIMPULAN DAN SARAN ... 53
A. Kesimpulan ... 53
B. Saran ... 53
DAFTAR PUSTAKA ... 54
LAMPIRAN ... 58
xiii
DAFTAR TABEL
Halaman Tabel I. Formula Sediaan Salep Sereh Wangi Jawa ... 27 Tabel II. Hasil Verifikasi Minyak Sereh Wangi Jawa ... 35 Tabel III. Hasil Pengukuran Rerata Diameter Zona Hambat Minyak
Sereh Wangi Jawa Terhadap Staphyloccus epidermidis ... 38 Tabel IV. Sifat Fisik Salep Minyak Sereh Wangi Jawa ... 44 Tabel V. Hasil Uji Statistik Stabilitas Fisik dan Pergeseran Viskositas
Salep Minyak Sereh Wangi Jawa ... 46 Tabel VI. Hasil Pengukuran Rerata Diameter Zona Hambat Salep Minyak
Sereh Wangi Jawa Terhadap Staphyloccus epidermidis ... 49 Tabel VII. Hasil Uji Statistik ... 51
xiv
DAFTAR GAMBAR
Halaman
Gambar 1. Struktur Setronelal ... 11
Gambar 2. Struktur Geraniol ... 12
Gambar 3. Struktur PEG ... 18
Gambar 4. Minyak Sereh Wangi Jawa ... 35
Gambar 5. Diagram Hasil Pengukuran Rerata Diameter Zona Hambat Minyak Sereh Wangi Jawa ... 39
Gambar 6. Salep Sereh wangi Jawa Formula I dan Formula II ... 43
Gambar 7. Uji Sterilitas Sediaan ... 48
Gambar 8. Diagram Hasil Pengukuran Rerata Diameter Zona Hambat Minyak Sereh Wangi Jawa ... 50
xv
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Certificate of Analysis ... 59
Lampiran 2. Surat Keterangan S. Epidermidis ... 60
Lampiran 3. Uji karakteristik Minyak Sereh Wangi Jawa ... 61
Lampiran 4. Uji Aktivitas Anti bakteri Minyak Sereh Wangi Jawa ... 62
Lampiran 5. Uji Formulasi Salep Minyak Sereh Wangi Jawa ... 63
Lampiran 6. Uji Sifat Fisik Salep Minyak Sereh Wangi Jawa ... 64
Lampiran 7. Uji Aktivitas Anti bakteri Minyak Sereh Wangi Jawa ... 65
Lampiran 8. Uji Sterilitas Salep Minyak Sereh Wangi Jawa ... 66
xvi INTISARI
Penelitian tentang pengaruh variasi komposisi dari PEG 400 dan PEG 4000 pada aktivitas antibakteri dalam salep minyak atsiri sereh wangi Jawa terhadap Staphylococcus epidermidis telah dilakukan. Selain untuk mengamati pengaruh komposisi PEG pada aktivitas antibakteri terhadap Staphylococcus epidermidis, penelitian ini juga bertujuan untuk membuat formulasi sediaan salep minyak atsiri sereh wangi Jawa dan mengetahui sifat fisiknya.
Penelitian ini merupakan penelitian eksperimental murni dengan rancangan penelitian acak lengkap pola dua arah. Salep minyak atsiri sereh wangi Jawa dibuat dalam 2 formula dimana sifat fisik dan zona hambat sebagai respon dari variasi komposisi PEG 400 dan PEG 4000. Dalam penelitian ini sifat fisik sediaan salep minyak atsiri sereh wangi Jawa diteliti. Hasil penelitian dianalisis secara statistik menggunakan metode ANAVA dua arah, dimana diikuti dengan uji Tukey untuk mengetahui perbedaan tiap formula dan kelompok kontrol menggunakan software R 2.14.1.1.
Hasil penelitian menunjukkan salep minyak atsiri sereh wangi Jawa menghasilkan aktivitas antibakteri terhadap Staphyloccous epidermidis. Aktivitas antibakteri salep minyak atsiri sereh wangi Jawa tidak terpengaruh oleh variasi komposisi dari PEG 400 dan PEG 4000.
Keywords: Cymbopogon winterianus, salep, aktivitas antibakteri, diameter zona hambat.
xvii ABSTRACT
The study of effect of variation composition of PEG 4000 and PEG 400 on the antibacterial activity of Citronella Java oil ointment against Staphylococcus epidermidis had been done. Beside to observe the effect of PEG composition on the antibacterial activity against Staphylococcus epidermidis, this study also aimed to provide ointment formulation for Citronella Java oil which met physical ointment.
This study was a pure experimental study using randomized study design complete two directional pattern. The Citronella Java oil ointment was designed into 2 formulas which physical ointment and inhibition zone as response of variance composition of PEG 400 and PEG 4000.
In this study, the physical properties of Citronella Java oil ointment were investigated. The result were analyzed statistikally by using two-way ANAVA method, which was then followed by Tukey's test to observe the differences between each formula and the control group using the software R 2.14.1.1
The results showed that the Citronella Java oil ointment provided antibacterial activity againt Staphylococcus epidermidis. The antibacterial activity of Citronella Java oil ointment was not affected by the variation composition of PEG 400 and PEG 4000.
Keywords: Cymbopogon winterianus, ointments, antibacterial activity, inhibition zone diameter.
1 BAB I PENGANTAR
A. Latar Belakang
Kesehatan merupakan salah satu kebutuhan dasar manusia, itulah sebabnya upaya untuk mencapai tingkat kesehatan yang optimal sangat diperlukan. Namun seiring dengan kemajuan zaman yang ditandai dengan globalisasi di segala bidang telah menyebabkan pergeseran berbagai penyakit. Salah satu contoh penyakit yang masih menjadi masalah kesehatan masyarakat Indonesia adalah penyakit kulit. Menurut Direktur Jenderal Pelayanan Medik Departemen Kesehatan Republik Indonesia tahun 2006 penyakit kulit dan jaringan subkutan berdasarkan prevalensi 10 penyakit terbanyak pada masyarakat Indonesia menduduki peringkat kedua setelah infeksi saluran pernapasan akut dengan jumlah 501.280 kasus atau 3,16% (Astriyanti, Lerik, Sahdan, 2010).
Penyakit kulit yang disebabkan karena infeksi merupakan penyakit yang paling umum terjadi pada orang-orang dari segala usia (Indrayatna, 2010). Infeksi kulit dapat disebabkan oleh bakteri gram negatif maupun bakteri gram positif (Djuanda, 1999). Staphylococcus epidermidis adalah salah satu flora normal pada kulit, merupakan spesies bakteri gram positif dari genus Staphylococcus yang diketahui menjadi penyebab utama terjadinya infeksi, terutama infeksi oportunistik (menyerang individu dengan sistem kekebalan tubuh yang lemah). Pemberian antibakteri merupakan salah satu pilihan dalam menangani penyakit infeksi. Namun penggunaan antibakteri yang tidak terkontrol dapat mendorong
2
terjadinya perkembangan resistensi bakteri penyebab infeksi terhadap antibakteri yang diberikan (Ariyanti, Darmayasa, Sudirga, 2012). Resistensi dapat terjadi karena bakteri memiliki daya pertahanan untuk menghindar dari antibiotik yaitu dengan cara melakukan mutasi pada sisi aktif maupun sisi pengikatan, membentuk protein trans membran yang dikenal sebagai protein efluks dan plasmid yang mengkode gen resiten terhadap antibiotik (Fuda, dkk., 2005). Adanya resistensi ini dapat menimbulkan banyak masalah dalam pengobatan penyakit infeksi, sehingga diperlukan usaha untuk mengembangkan obat terutama obat berbahan herbal. Obat herbal mempunyai banyak kandungan senyawa baru yang berpotensi dapat digunakan sebagai antibakteri untuk mengatasi masalah terjadinya resistensi tersebut. Salah satu contoh tanaman yang dapat digunakan adalah sereh wangi Jawa (Cymbopogon winterianus). Sereh wangi Jawa merupakan salah satu tanaman yang sering dan mudah dijumpai didaerah tropis seperti di Indonesia selain itu harganya yang relatif murah. Sereh wangi Jawa memiliki kandungan senyawa yaitu sitronelal dan geraniol dalam minyak atsiri yang dapat berkhasiat sebagai antibakteri (Nakahara et al, 2003) dan diketahui memiliki nilai KBM sebesar 15% (Wijayanti, 2013). sehingga dapat berpotensi digunakan sebagai salah satu alternatif obat infeksi alami baru.
Sediaan salep merupakan salah satu alternatif yang dapat digunanakan sebagai pengobatan terutama untuk penyakit infeksi pada kulit karena merupakan sediaan topikal yang sesuai untuk terapi penyakit pada kulit yang disebabkan oleh bakteri, selain itu salep mempunyai stabilitas yang baik, berupa sediaan halus, mudah digunakan, mampu menjaga kelembapan kulit, tidak mengiritasi kulit dan
3
mempunyai tampilan yang menarik (Pongsipulung, Yamlean, Banne, 2012 ; Naibaho, Yamlean, Wiyono, 2013). Salep merupakan sediaan yang terdiri dari bahan obat yang terlarut ataupun terdispersi di dalam basis atau basis salep sebagai pembawa zat aktif. Basis salep yang digunakan dalam sebuah formulasi obat harus bersifat inert dengan kata lain tidak merusak ataupun mengurangi efek terapi dari obat yang dikandungnya (Naibaho, Yamlean, Wiyono,2013). Salah satu contoh basis salep adalah basis larut air dengan bahan utama PEG. Sediaan salep dengan basis PEG mempunyai kelebihan dapat melepaskan zat aktif bersifat non polar dengan lebih baik dibandingkan dengan basis yang larut minyak (Pasroni dkk, 2004). PEG 400 dan PEG 4000 merupakan salah satu contoh kombinasi pembuat sediaan salep basis larut air. PEG 400 merupakan polimer dalam bentuk cair sedangkan PEG 4000 dalam bentuk padat, dimana variasi kombinasi keduanya pada salep basis larut air akan membentuk viskositas dan daya sebar yang berbeda. Viskositas dan daya sebar yang dihasilkan mempunyai pengaruh terhadap pelepasan zat aktif yang dibawanya. Semakin tinggi viskositas dan semakin rendah daya sebar dari suatu sediaan salep akan menyebabkan penurunan pelepasan zat aktif (Paramita, 2005).
1. Perumusan Masalah
Berdasarkan latar belakang yang telah diuraikan diatas, permasalahan dalam penelitian ini adalah sebagai berikut :
4
a. Apakah sediaan salep basis larut air yang mengandung minyak atsiri sereh wangi Jawa dapat menghambat pertumbuhan bakteri Staphylococcus epidermidis?
b. Bagaimana pengaruh perbandingan PEG 400 dan PEG 4000 terhadap sifat fisik dan pelepasan zat aktif sediaan minyak atsiri sereh wangi Jawa basis larut air?
2. Keaslian Penelitian
Penelitian lain yang berkaitan dengan penelitian ini antara lain:
a. Penggunaan bahan alam minyak sereh wangi Jawa sebagai antibakteri adalah penelitian oleh Wijayanti, B.A, (2013) dengan judul : ”Uji Daya Antibakteri Emulgel Antiacne Minyak Sereh Wangi Jawa (Cymbopogon
winterianus) Terhadap Bakteri Staphylococcus epidermidis” dimana
dalam skripsi tersebut didapatkan nilai KBM minyak sereh wangi Jawa sebesar 15% yang kemudian akan digunakan dalam penelitian ini.
b. Penelitian oleh Miftakhurohmah, Rita Noveriza dan Agus Kardinan (2008) dengan judul : “Efektivitas Formula Minyak Sereh Wangi Terhadap Pertumbuhan Kapang Asal Buah Merah dan Sambiloto” dimana
penelitian tersebut menujukkan hasil Formula minyak serai wangi yang diuji mampu menghambat pertumbuhan kapang kontaminan Geotrichum sp, Fusarium culmorum, Ulocladium sp dan Fusarium sp dengan daya
hambat sebesar 16,07-66,67%.
5
Salep Ekstrak Etanolik Bawang Putih (Allium Sativum. L), Skripsi, Fakultas Farmasi Universitas Gadjah Mada, Yogyakarta”, dimana
penelitian tersebut menujukkan hasil bahwa semakin besar jumlah komposisi PEG 4000 akan berpengaruh terhadap naiknya nilai viskositas dan menyebabkan penurunan pelepasan zat aktif ekstrak etanolik bawang putih (Allium Sativum. L) terhadap aktivitasnya sebagai antibakteri.
d. Penelitian oleh Naibaho, O.H., Yamlean Paulina, V.Y., Wiyono Weny., (2013) program studi Farmasi, FMIPA UNSRAT Manado dengan judul “Pengaruh Basis Salep Terhadap Formulasi Sediaan Salep Ekstrak Daun
Kemangi (Ocimum sanctum L.) Pada kulit Punggung Kelinci Yang Dibuat Infeksi Staphylococcus aureus.” dimana hasil yang didapatkan menunjukkan perbedaan tipe basis salep yang digunakan pada formulasi salep ekstrak daun kemangi berpengaruh pada sifat fisik sediaan dan berpengaruh terhadap daya antibakteri, ditandai dengan penyembuhan infeksi pada kulit kelinci yang lebih cepat.
Namun, sejauh penelusuran penulis, skripsi dengan judul pengaruh variasi komposisi PEG 400 – PEG 4000 pada aktivitas antibakteri salep minyak sereh wangi Jawa terhadap bakteri Staphylococcus epidermidis belum pernah dilakukan.
3. Manfaat Penelitian a. Manfaat teoretis
6
kefarmasian mengenai pembuatan salep basis larut air dengan zat aktif minyak atsiri sereh wangi Jawa sebagai antibakteri untuk menghambat pertumbuhan Staphylococcus epidermidis.
b. Manfaat praktis
Dengan adanya penelitian ini diharapkan dapat menghasilkan formula sediaan salep antibakteri yang baik untuk mencegah atau mengatasi penyakit infeksi akibat bakteri Staphylococcus epidermidis.
B. Tujuan Penelitian
1. Untuk mengetahui aktivitas antibakteri salep minyak atsiri sereh wangi Jawa terhadap bakteri Staphylococcus epidermidis.
7 BAB II
PENELAAH PUSTAKA
A. Infeksi 1. Pengertian
Penyakit infeksi adalah penyakit yang disebabkan oleh pertumbuhan organisme patogenik dalam tubuh. Penyakit infeksi mungkin menular mungkin juga tidak (Tietjen Linda, 2004).
Infeksi adalah invasi tubuh patogen atau mikroorganisme yang mampu menyebabkan sakit (Perry & Potter, 2005).
2. Penyebab Infeksi
Tipe mikroorganisme penyebab infeksi dibagi menjadi empat kategori : a. Bakteri, merupakan penyebab terbanyak dari infeksi. Ratusan spesies
bakteri dapat menyebabkan penyakit pada manusia dan dapat hidup didalam tubuhnya. Bakteri bisa masuk antara lain melalui udara, tanah, air, makanan, cairan dan jaringan tubuh dan benda mati lainnya.
b. Virus, terutama berisi asam nukleat (nukleat acid) karenanya harus masuk dalam sel hidup untuk di produksi.
c. Parasit, hidup dalam organisme hidup lain. Protozoa, cacing dan arthropoda termasuk kelompok parasit.
d. Fungi, terdiri dari ragi dan jamur (Perry & Potter, 2005).
8
3. Tipe Infeksi
a. Kolonisasi, merupakan suatu proses dimana benih mikroorganisme menjadi flora yang menetap/residen. Mikroorganisme bisa tumbuh dan berkembang biak tetapi tidak bisa menimbulkan penyakit. Infeksi terjadi ketika mikroorganisme yang menetap tadi sukses menginvasi/menyerang bagian tubuh/host manusia yang system pertahanannya tidak efektif dan pathogen menyebabkan kerusakan jaringan.
b. Infeksi lokal, spesifik dan terbatas pada bagian tubuh dimana mikroorganisme tinggal.
c. Infeksi sistemik, terjadi bila mikroorganisme menyebar kebagian tubuh yang lain dan menimbulkan kerusakan.
d. Bakterimia, terjadi ketika didalam darah ditemukan adanya bakteri.
e. Septikimia, multiplikasi bakteri dalam darah sebagai hasil dari infeksi sistemik.
f. Infeksi akut, infeksi yang muncul dalam waktu singkat.
g. Infeksi kronik, infeksi yang terjadi secara lambat dalam periode yang lama (dalam hitungan bulan/tahun) (Perry & Potter, 2005).
B. Minyak Atsiri
Minyak atsiri yang dikenal sebagai minyak eteris merupakan mudah menguap pada suhu kamar. Minyak atsiri mempunyai rasa getir, berbau wangi sesuai dengan bau tanaman penghasilnya, umumnya larut dalam pelarut organik dan tidak larut dalam air (Guenther, 2006).
9
Minyak atsiri dapat bersumber dari bagian tanaman seperti daun, bunga, buah, biji, batang atau kulit dan akar. Pengambilan atau ekstraksi minyak atsiri dari bagian tanaman tersebut dapat dilakukan dengan cara penyulingan, pengempaan, ekstraksi menggunakan pelarut, atau absorbsi dengan lemak; tergantung dari jenis tanaman dan sifat fisiko-kimia minyak atsiri di dalamnya (Harris, 1994).
Nilai bobot jenis minyak atsiri berkisar antara 0,696-1,188 pada suhu 150C dan pada umumnya nilai tersebut lebih kecil dari 1.000 (Guenther, 2006).
C. Minyak Sereh Wangi
Minyak sereh wangi yang didapatkan dari daun dan batang sereh mengandung komponen utama, yaitu : sitronelal, sitronelol dan geraniol serta senyawa ester dari geraniol dan sitronelol. Senyawa-senyawa tersebut merupakan bahan dasar yang digunakan dalam parfum atau pewangi dan juga produk farmasi. Gabungan ketiga komponen utama tersebut (Sitronelal, sitronelol, dan geraniol) dikenal sebagai total senyawa yang dapat diasetilasi. Ketiga komponen ini menentukan intensitas bau harum, nilai dan harga minyak sereh. Menurut standar pasar internasional, kandungan sitronelal dan jumlah total alkohol (geraniol) masing-masing harus lebih tinggi dari 35% (Balchin, 2006).
Minyak sereh atau Citronella oil adalah minyak esensial yang didapatkan dari daun dan batang sereh (Cymbopogon nardus). Sereh yang biasa diperdagangkan dibagi dalam dua kategori yaitu Ceylon citronela oil yang diperoleh dari Cymbopogon nardus dan Java citronella oil dari Cymbopogon
10
winterianus. Java citronela oil adalah produk yang kualitasnya lebih tingggi
dibandingkan dengan Seilon (Balchin, 2006).
Kualitas minyak atsiri pada umumnya dan minyak sereh wangi pada khususnya ditentukan oleh faktor kemurnian. Kualitas minyak sereh wangi ditentukan oleh komponen utama di dalamnya yaitu kandungan sitronela dan geraniol yang biasa dinyatakan dengan jumlah kandungan geraniol. Minyak sereh wangi tidak boleh mengandung atau dikotori oleh bahan asing seperti minyak lemak, alkohol, ataupun minyak tanah (Harris, 1994).
Minyak sereh wangi biasanya berwarna kuning muda sampai kuning tua, bersifat mudah menguap. Pada suhu 15ºC mempunyai bobot jenis 0,886-0,894; indeks bias pada suhu 20ºC adalah 1,467-1,473. Dapat larut dalam 3 bagian volume alkohol 80% tetapi bila diencerkan kelarutannya berkurang dan larutan menjadi keruh (SNI, 1995).
Minyak sereh wangi asal Jawa mengandung komponen sebagai berikut : Sitronelal 32-45% ; Geraniol 12–18% ; Sitronelol 11 -15% ; Geranil asetat 3–8% ; Sitronelil asetat 2–4% ; Limonen 2-4 % ; Kadinen 2-4% dan selebihnya (2–36%) adalah Sitral, Kavikol, Eugenol, Elemol, Kadinol, Vanilin, Kamfen, α-Pinen, linalool, β-Kariofilen (Peter, 2007). Komponen utama minyak sereh wangi Jawa
adalah sitronela dan geraniol, yang memiliki sifat antibakteri dan antikapang, sehingga dapat dimanfaatkan sebagai pestisida nabati. (Miftakhurohmah et al, 2008).
Mekanisme minyak sereh wangi Jawa sebagai senyawa antibakteri menurut Lertsatitthanakorn et al, (2010) karena kandungan Sitronelal (monoterpen
11
aldehida) yang memiliki target membran protein fungsional akan meningkatkan permeabilitas membran bakteri. Aktifitas antibakteri gugus alkohol bertindak sebagai agen pendehidrasi pada dosis rendah dan agen pendenaturai pada dosis tinggi.
D. Sitronelal
Sitronelal merupakan senyawa monoterpena yang mempunyai gugus aldehid, ikatan rangkap dan rantai karbon yang memungkinkan mengalami reaksi siklisasi aromatisasi (Irna et al, 2007).
Aktivitas antibakteri sitronelal (monoterpen aldehida) yang ditemukan dalam minyak atsiri sereh wangi Jawa diperkirakan karena adanya senyawa elektronegatif yang dapat menggangu komponen nitrogen dari protein pada membran sitoplasmik, isi sitoplasmik dan asam nukleat (Lertsatitthanakorn, et al., 2010).
Gambar 1. Gambar struktus sitronelal
(Syamsuhidayat dan Hutapea, 1991).
E. Geraniol
Geraniol (sering disebut juga sebagai rhodinol), adalah salah satu senyawa monoterpenoid dan alkohol dengan formula C10H18O. Geraniol sering
12
dijumpai pada tanaman sereh wangi, geranium, palmarose, jeruk purut, laos merah dan jahe. Geraniol juga sering disebut dengan minyak rose. Geraniol berupa cairan berwarna kuning pucat. Senyawa ini tidak dapat larut dalam air, tetapi larut dalam bahan pelarut organik yang umum. Baunya menyengat dan sering digunakan sebagai parfum. Kandungan geraniol dalam minyak sereh wangi Jawa sebesar 11-15% (Singh et al, 2011).
Aktifitas antibakteri geraniol (gugus alkohol) bertindak sebagai agen pendehidrasi pada dosis rendah dan agen pendenaturai pada dosis tinggi. Alkohol dan fenol dapat menyebabkan pecahnya membran sitoplasma dan kerusakan dinding bakteri. Dinding sel bakteri Gram positif kehilangan struktur kaku dan komponen dinding yang pecah setelah diberi perlakuan dengan minyak sereh wangi Jawa. Akibatnya membran sitoplasma yang telah rusak menyebabkan kebocoran materi-materi intraseluler dan sel akhirnya lisis (Lertsatitthanakorn, et al., 2010).
Gambar 2. Gambar struktus geraniol
(Syamsuhidayat dan Hutapea, 1991).
F. Staphylococcus epidermidis
Staphylococcus epidermidis adalah salah satu spesies bakteri gram positif
13
(menyerang individu dengan sistem kekebalan tubuh yang lemah). Beberapa karakteristik bakteri ini adalah fakultatif anaerob, koagulase negatif, katalase positif, gram positif, berbentuk kokus, dan berdiameter 0,5–1,5 µm. Bakteri ini secara alami hidup pada kulit dan membran mukosa manusia. Secara klinis, bakteri ini menyerang orang-orang yang rentan atau imunitas rendah, seperti penderita AIDS, pasien kritis, pengguna obat terlarang (narkotika), bayi yang baru lahir, dan pasien rumah sakit yang dirawat dalam waktu lama. Organisme ini menghasilkan glycocalyx lendir yang menyebabkan resistensi terhadap fagositosis dan antibiotik. Resistensi dapat terjadi karena bakteri memiliki daya pertahanan untuk menghidar dari antibiotik yaitu dengan melakukan mutasi pada sisi aktif maupun sisi pengikatan, membentuk protein trans membran yang dikenal sebagai protein efluks dan plasmid yang mengkode gen resiten terhadap antibiotik (Fuda, dkk, 2005). Staphylococcus epidermidis hidup sebagai parasit pada manusia dan hewan berdarah panas lainnya. (Jawetz, 1996).
G. Antibakteri 1. Antibakteri
Antibakteri adalah obat pembasmi bakteri, khususnya bakteri yang merugikan manusia. Obat yang digunakan sebagai pembasmi bakteri penyebab infeksi pada manusia harus mempunyai toksisitas selektif setinggi mungkin, artinya obat tersebut haruslah bersifat toksik untuk bakteri tetapi relatif tidak toksik untuk hospes (Depkes RI, 1995).
14
Berdaskan sifat toksisitas selektif, antibakteri dibagi menjadi dua bagian, yaitu antibakteri yang bersifat menghambat pertumbuhan bakteri atau disebut bakteriostatik dan antibakteri yang bersifat membunuh bakteri atau yang disebut bakterisida. Aktivitas antibakteri dapat berubah dari menghambat pertumbuhan menjadi membunuh bakteri tergantung dari dosis (Edber, 1986).
H. Pengujian Daya Antibakteri
Pengujian daya antibakteri dapat dilakukan untuk mengetahui daya antibakteri suatu obat. Pengukuran aktivitas / uji khasiat obat dapat dikerjakan dengan berbagai cara, yaitu :
1.Metode dilusi atau pengenceran
Prinsipnya adalah pengenceran seri antibakteri sehingga diperoleh beberapa konsentrasi. Pada metode ini masing-masing konsentrasi cairan antibakteri dicampurkan dengan suspensi bakteri pada media agar dalam keadaan hangat, ditunggu memadat dan diinkubasikan. Pengamatan dilakukan dengan melihat kekeruhan media untuk mengetahui ada tidaknya pertumbuhan bakteri pada media agar (Edber, 1986).
2. Metode difusi
Antibakteri diukur berdasarkan pengamatan luas daerah hambatan pertumbuhan bakteri karena berdifusinya obat dari titik awal pemberian kedaerah difusi. Bakteri ditanam pada media yang sesuai dan diatasnya diletakkan paper disk yang mengandung bahan obat atau dibuat sumuran dengan diameter tertentu yang diisi larutan bahan obat (Edber, 1986).
15
a. Metode difusi dikenal beberapa cara, yaitu : Cara Kirby Bouwer
1) Cara tuang (Pour Plate)
Suspensi bakteri dengan komposisi 10-5 CFU/ml diambil menggunakan ose dan dimasukkan dalam media agar yang mempunyai suhu 50oC. Kemudian dibuat homogen dan dibiarkan membeku. Kemudian diatasnya diletakkan paper disk dan diinkubasikan pada suhu 37oC selama 18-24 jam (Edber, 1986).
2) Cara Sumuran
Pada agar yang telah ditanami bakteri dibuat sumuran dengan garis tengah tertentu dan ke dalam sumuran diberi larutan uji dan diinkubasikan pada suhu 37oC selama 18-24 jam (Edber, 1986).
Hasil dari metode difusi berupa :
1) Zona radikal yaitu daerah di sekitar disk yang sama sekali tidak ditemukan bakteri.
2) Zona irradikal yaitu daerah di sekitar disk yang menunjukkan pertumbuhan bakteri dihambat oleh larutan uji tetapi tidak dimatikan (Edber, 1986).
I. Salep 1. Pengertian salep
Salep adalah sediaan setengah padat ditujukan untuk pemakaian topikal pada kulit atau selaput lendir. Dasar salep yang digunakan sebagai pembawa dibagi dalam empat kelompok yaitu dasar salep senyawa hidrokarbon, dasar salep
16
serap, dasar salep yang dapat dicuci dengan air dan dasar salep larut dalam air. Salep obat menggunakan salah satu dari dasar salep tersebut (Depkes RI, 1995). 2. Dasar Salep
Menurut Farmakope Indonesia IV, dasar salep yang digunakan sebagai pembawa dibagi dalam 4 kelompok yaitu dasar salep senyawa hidrokarbon, dasar salep serap, dasar salep yang dapat dicuci dengan air, dasar salep larut dalam air. Setiap salep obat menggunakan salah satu dasar salep tersebut (Depkes RI, 1995). a. Dasar Salep Hidrokarbon, Dasar salep ini dikenal sebagai dasar salep
berlemak, antara lain vaselin putih dan salep putih. Hanya sejumlah kecil komponen berair yang dapat dicampurkan kedalamnya. Salep ini dimaksudkan untuk memperpanjang kontak bahan obat dengan kulit dan bertindak sebagai pembalut penutup. Dasar salep hidrokarbon dapat digunakan sebagai emolien yang mempunyai sifat sukar dicuci dengan air, tidak mudah mengering dan relative stabil (Ansel, 1989).
b. Dasar Salep Serap, Dasar salep serap ini dibagi dalam 2 kelompok. Kelompok pertama terdiri atas dasar salep yang dapat bercampur dengan air membentuk emulsi air dalam minyak (parafin hidrofilik dan lanolin anhidrat), dan kelompok kedua terdiri atas emulsi air dalam minyak yang dapat bercampur dengan sejumlah larutan air tambahan (lanolin). Dasar salep ini juga berfungsi sebagai emolien (Ansel, 1989).
17
untuk dasar kosmetika. Beberapa bahan obat dapat menjadi lebih efektif menggunakan dasar salep ini daripada dasar salep hidrokarbon. Keuntungan lain dari dasar salep ini adalah dapat diencerkan dengan air dan mudah menyerap cairan yang terjadi pada kelainan dermatologik (Ansel, 1989). d. Dasar Salep Larut Air, Kelompok ini disebut juga dasar salep tak berlemak
dan terdiri dari konstituen larut air. Dasar salep jenis ini memberikan banyak keuntungannya seperti dasar salep yang dapat dicuci dengan air dan tidak mengandung bahan tak larut dalam air, seperti paraffin, lanolin anhidrat atau malam. Dasar salep ini lebih tepat disebut PEG.
Pemilihan dasar salep tergantung pada beberapa faktor yaitu khasiat yang diinginkan, sifat bahan obat yang dicampurkan, ketersediaan hayati, stabilitas dan ketahanan sediaan jadi. Dalam beberapa hal perlu menggunakan dasar salep yang kurang ideal untuk mendapatkan stabilitas yang diinginkan. (Ansel, 1989).
J. PEG
Polyethylene glycol 200, 300, 400 dan 600 jernih, berbentuk cairan
viskos pada suhu ruangan. Glycol tidak terhidrolisis atau memburuk dibawah kondisi tertentu. Semakin meningkatnya berat molekul, maka kelarutan dalam air, tekanan uap, higroskopisitas dan kelarutan pada pelarut organik menurun; pada saat yang sama, rentan pembekuan atau pelelehan, titik nyala dan viskositas meningkat (Gennaro, 2000).
18
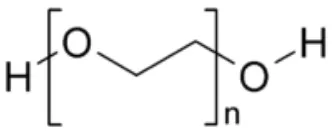
Gambar 3. Struktur Polyethylene glycol(Gennaro, 2000).
Bahan ini memiliki kelarutan dan kompatibilitas dalam rentang yang luas, yang membuatnya berguna dalam preparasi farmasetis dan kosmetik (Gennaro, 2000).
Polyethylene glycol digunakan dalam kosmetik dengan kandungan gugus
oxyethylene sebanyak 4 hingga 115.000 (disebut PEG 4 hingga 115M). Derivat cairnya digunakan sebagai pelarut dan humectants dalam minyak mandi, pewangi, shampo, kondisioner rambut, make-up wajah, krim, lotion, produk suntan dan produk pembersih (Smolinske, 1992)
1. Polietilenglikol – 400 (Polyethylenglycolum – 400)
Polietilenglikol–400 adalah polietilenglikol H(OCH2-CH2)nOH, harga n antara 8,2 dan 9,1. PEG 400 berupa cairan kental jernih, tidak berwarna atau praktik tidak berwarna, bau khas lemah, agak higroskopik. PEG 400 larut dalam air, dalam etanol (95%) P, dalam aseton P, dalam glikol lain dan dalam hidrokarbon aromatik, praktis tidak larut dalam eter P dan dalam hidrokarbon alifatik. PEG 400 disimpan dalam wadah tertutup rapat. Khasiat dan penggunaannya sebagai zat tambahan (Depkes RI, 1979).
2. Polietilenglikol – 4000 (Polyethylenglycolum–4000)
Polietilenglikol–4000 adalah polietilenglikol H(O-CH2-CH2)nOH harga n antara 68 dan 84. PEG 4000 berupa serbuk licin putih atau potongan putih kuning gading, praktis tidak berbau, tidak berasa. PEG 4000 mudah larut dalam air, dalam etanol (95%) P dan dalam kloroform P, praktis tidak larut dalam eter P.
19
Kesempurnaan melarut dan warna larutan 5 g dalam air hingga 50 ml praktis jernih dan tidak berwarna. PEG 4000 disimpan dalam wadah tertutup rapat. Khasiat dan penggunaan sebagai zat tambahan (Depkes RI, 1979).
Perbandingan campuran komposisi antara PEG 400 dan PEG 4000 akan berpengaruh terhadap sifat fisik sediaan yang terbentuk, dimana akan membentuk suatu konsistensi tertentu. Jumlah komposisi PEG 400 yang semakin banyak akan menurunkan nilai waktu leleh, titik leleh, viskositas dan kekerasan dari suatu sediaan. (Stiawan, 2006).
K. Uji Sifat Fisik Sediaan Salep
Uji sifat fisik sediaan salep meliputi beberapa hal, diantaranya adalah ; a. pH, merupakan salah satu karakteristik yang penting yang harus diukur
dan dikontrol, terutama jika produk akan digunakan pada makhluk hidup. Menurut SNI 16-4399-1997 pH sediaan topikal harus berada dalam rentang 4,5-8 karena pH yang terlalu asam atau basa dapat menyebabkan kulit menjadi kering dan mengalami iritasi akibat terjadinya kerusakan mantel asam pada lapisan sel kulit mati (Garg, dkk., 2002).
b. Viskositas, menyatakan tahanan dari suatu cairan untuk mengalir, makin tinggi akan semakin besar tegangan. Viskositas termasuk faktor yang penting dalam karakteristik sediaan semisolid. Viskositas suatu sediaan menentukan lamanya sediaan melekat pada kulit sehingga obat dapat terpenetrasi dengan baik (Garg, dkk., 2002). Standar viskositas menurut SNI 16-4399-1997 berkisar antara 2000-50.000 cP.
20
c. Daya sebar, untuk mengetahui kelunakan massa salep pada waktu dioleskan pada kulit yang diobati (Martin dkk, 1993). Daya sebar, pada prinsipnya, berkaitan dengan sudut kontak dari setetes cairan atau sediaan semi padat atau semi cair pada substrat terstandar dan berkaitan dengan koefisien gesekan (Garg dkk., 2002).
L. Landasan Teori
Infeksi disebabkan oleh mikroba pathogen seperti bakteri Staphylococcus epidermidis yang bersifat sangat dinamis. Organisme-organisme tersebut dapat
menyerang sebagian atau seluruh tubuh manusia terutama pada kulit yang mana merupakan bagian yang paling rentan terkena luka.
Salah satu usaha untuk mencegah atau mengobati infeksi kulit adalah dengan cara menghambat atau menekan pertumbuhan bakteri pathogen penyebab infeksi. Minyak atsiri sereh wangi Jawa diketahui mempunyai efek sebagai antibakteri untuk menekan / menghambat pertumbuhan bakteri Staphylococcus epidermidis. Minyak atsiri sereh wangi Jawa berdasarkan hasil penelitian
sebelumnya oleh Wijayanti, (2005) menunjukkan nilai KBM sebesar 15%. Oleh karena itu minyak atsiri sereh wangi Jawa berpotensi diformulasikan dalam sediaan topikal antibakteri. Formulasi sediaan salep minyak atsiri sereh wangi Jawa dengan basis, komposisi bahan serta dosis / konsentrasi minyak atsiri sereh wangi Jawa yang sesuai diharapkan dapat menjadi alternatif obat infeksi. Sediaan salep dengan basis PEG mempunyai kelebihan dapat melepaskan zat aktif bersifat non polar dengan lebih baik dibandingkan dengan basis yang larut minyak. PEG
21
4000 dan PEG 400 merupakan salah satu contoh kombinasi pembuat sediaan salep. PEG 400 merupakan polimer dalam bentuk cair sedangkan PEG 4000 dalam bentuk padat, dimana perbandingan kombinasi kedua bahan tersebut akan membentuk suatu konsistensi tertentu yaitu viskositas dan daya sebar yang berbeda. Menurut penelitian yang ada perbedaan nilai viskositas dan daya sebar akan berpengaruh terhadap pelepasan zat aktif yang dibawanya. Minyak atsiri sereh wangi Jawa yang digunakan sebagai zat aktif dalam sediaan salep basis PEG dengan jumlah perbandingan komposisi PEG 4000 yang lebih banyak dan PEG 400 yang lebih sedikit akan menghasilkan nilai viskositas yang tinggi dan daya sebar yang rendah. Semakin tingginya nilai viskositas dan semakin kecilnya nilai daya sebar akan memberikan pengaruh terhadap aktivitas antibakteri yaitu berupa penurunan pelepasan zat aktif yang dibawanya.
M.Hipotesis
1. Salep minyak atsiri sereh wangi Jawa memiliki aktivitas antibakteri terhadap bakteri Staphylococcus epidermidis.
2. Minyak atsiri sereh wangi Jawa memiliki perbedaan aktivitas antibakteri terhadap Staphylococcus epidermidis setelah diformulasikan dalam sediaan salep dengan perbandingan PEG 400 dan PEG 4000 yang berbeda.
22 BAB III
METODE PENELITIAN
A. Jenis Penelitian
Penelitian ini merupakan penelitian eksperimental murni dengan rancangan penelitian, acak lengkap pola dua arah.
B. Variabel Penelitian dan Definisi Operasional 1. Variabel Penelitian
a. Variabel bebas
Variasi komposisi PEG 400 dan PEG 4000 dalam formula sediaan salep. b. Variabel tergantung
Diameter zona hambat yang terbentuk terhadap bakteri Staphylococcus epidermidis, sifat fisik salep antibakteri minyak atsiri sereh wangi Jawa meliputi pH, viskositas dan daya sebar.
c. Variabel pengacu terkendali
23
wangi Jawa yang diinokulasikan dalam sumuran (50L), formula sediaan
salep basis larut air, kecepatan mixer dan lama pencampuran pembuatan salep.
d. Variabel pengacu tak terkendali
Karakteristik tanaman sereh wangi Jawa yang digunakan produsen sebagai sumber minyak atsiri sereh wangi Jawa serta metode destilasi yang digunakan karena tidak diketahui secara pasti oleh konsumen.
2. Definisi operasional
a. Minyak sereh wangi Jawa merupakan minyak atsiri dari tanaman sereh wangi sereh wangi Jawa yang diperoleh dari CV Indaroma dalam bentuk cair, berwarna kuning dan bau yang khas dan disertai dengan Certificate of Analysis.
b. Salep minyak sereh wangi Jawa merupakan sediaan topikal semipadat basis larut air yang dibuat dengan zat aktif berupa minyak atsiri sereh wangi Jawa sesuai formula yang ditentukan dan dibuat sesuai prosedur pembuatan salep pada penelitian ini.
c. Daya antibakteri sediaan salep minyak sereh wangi Jawa adalah kemampuan sediaan minyak sereh wangi Jawa untuk menghambat atau membunuh bakteri uji Staphylococcus epidermidis dimana ditunjukan oleh zona hambat yang dihasilkan yang mana dibandingkan dengan kontrol negatif.
24
C. Alat dan Bahan Penelitian 1. Alat penelitian
Cawan petri (Pyrex) tabung reaksi (Pyrex), gelas ukur (Pyrex), beaker glass (Pyrex), bunsen (Pyrex), neraca analitik (Natagata), autoklaf (Model KT-40,
ALP Co, Ltd, Hamurashi Tokyo, Jepang), Laminar Air Flow (ESCO Class II type A2), inkubator (merek Memmert, type BE 400, GmbH+CoKG-D91126,
Swahaban FRG, Germany), piknometer, pipet ukur, almari es (Sharp), kapas,
ose, yellow tip, mikropipet, korek, pipet, larutan Mc Farland 0.5, alat pembuat sumuran, rak tabung reaksi, magnetik stirrer, kertas label, gunting, aluminium foil, plastik web, tisu gulung, dan kertas pembungkus, mortir, stamper, labu ukur, alat-alat glass, alat uji sediaan salep, mixer (Philip).
2. Bahan dan media penelitian
Minyak atsiri sereh wangi Jawa (CV Indaroma), biakan murni Stapylococcus epidermidis ATCC 12228 (Balai Kesehatan Kota Yogyakarta), media Mueller
Hinton Agar (MERCK) dan Mueller Hinton Broth (HERCK), aqaudes, ethanol 70%, kapsul antibiotik Klindamisin, larutan standar Mc. Farlland 0.5, PEG 400 (BRATACHEM), PEG 4000 (BRATACHEM).
D. Skema Kerja
1. Identifikasi dan verifikasi minyak atsiri sereh wangi Jawa
Bahan yang diidentifikasi pada penelitian ini adalah minyak atsiri sereh wangi Jawa yang diperoleh dari CV Indaroma Yogyakarta dan telah diuji identitasnya. Verifikasi minyak sereh wangi Jawa meliputi:
25
a. Pengamatan organoleptis, pengamatan organoleptis berupa pengamatan bentuk, warna, dan bau minyak atsiri sereh wangi Jawa.
b. Penetapan bobot jenis (BJ), Bobot jenis minyak atsiri sereh wangi Jawa diukur dengan menggunakan piknometer yang telah dikalibrasi. Kalibrasi dilakukan dengan menetapkan bobot piknometer kosong dan bobot air pada suhu 25oC. Piknometer yang telah dikalibrasi diisi dengan minyak atsiri sereh wangi Jawa dan dikondisikan dalam suhu 25oC, kemudian piknometer ditimbang. Bobot piknometer yang telah diisi minyak atsiri sereh wangi Jawa, kemudian dikurangi dengan bobot piknometer kosong. Bobot jenis minyak atsiri sereh wangi Jawa merupakan perbandingan antara bobot minyak atsiri sereh wangi Jawa dengan bobot air dalam piknometer pada suhu 25oC (Tiran, 2014).
c. Penetapan indeks bias, Verifikasi indeks bias minyak atsiri sereh wangi Jawa diukur dengan menggunakan hand refractometer. Nilai indeks bias minyak atsiri sereh wangi Jawa ditunjukkan oleh garis batas yang memisahkan sisi gelap dan sisi terang. Minyak atsiri sereh wangi Jawa diteteskan di atas prisma utama, kemudian prisma ditutup dan ujung refraktometer diarahkan ke sumber cahaya yang terang (Tiran, 2014).
2. Uji aktivitas antibakteri minyak atsiri sereh wangi Jawa terhadap Staphylococcus epidermidis dengan metode difusi sumuran
26
15; 17,5; dan 20%(v/v). Kisaran konsentrasi tersebut dibuat berdasarkan penelitian Wijayanti, B, A., 2013 yang menunjukkan bahwa aktivitas antibakteri terhadap bakteri Staphylococcus epidermidis menujukkan nilai KBM sebesar 15%. Pembuatan seri konsentrasi menggunakan pelarut PEG 400.
b. Pembuatan suspensi bakteri uji. Sebanyak satu ose koloni bakteri uji Staphylococcus epidermidis diambil dari stok bakteri dan dimasukkan ke
dalam tabung reaksi yang telah berisi media MHB steril, kemudian diinkubasi selama 24 jam pada suhu 37oC di dalam inkubator, selanjutnya suspensi bakteri uji Staphylococcus epidermidis dilihat kekeruhannya dan disesuaikan dengan standar Mac Farland 0,5 (1,5 x 108 CFU/mL). Mac Farland 0,5 dipilih karena menurut hasil orientasi kekeruhannya sudah dapat menunjukkan pertumbuhan dan zona hambat yang jelas.
27
dan larutan antibiotik klindamisin 0,2 %. Cawan petri dibungkus dengan menggunakan plastik wrap, kemudian diinkubasi selama 24 jam pada suhu 37oC di dalam inkubator.
Selanjutnya diamati dan diukur diameter zona hambat yang dihasilkan. Konsentrasi dengan zona hambat terbesar kemudian diformulasikan dalam bentuk sediaan salep dan dilanjutkan dengan pengujian aktivitas antibakteri salep minyak atsiri sereh wangi Jawa tersebut.
3. Formulasi sediaan salep minyak atsiri sereh wangi Jawa (Cymbopogon winterianus)
Formula salep adalah sebagai berikut :
Tabel 1. Formula salep minyak atsiri sereh wangi Jawa (Cymbopogon winterianus) dengan basis larut air.
Formula salep yang digunakan mengacu pada jurnal penelitian yang ditulis oleh Faradiba, (2011) serta Naibaho, O.H., Yamlean Paulina V. Y., Wiyono Weny, (2013)
Cara pembuatan salep minyak sereh wangi Jawa basis larut air dilakukan secara aseptis dalam LAF :
28
a. Bahan-bahan ditimbang, lalu dimasukkan ke cawan porselen kemudian disterilisasi dengan oven pada suhu 180°C selama 1 jam.
b. Basis yang telah meleleh, diaduk homogen dengan mixer dengan kecepatan 500rpm dalam mortir hangat sampai dingin selama 10 menit.
c. Zat aktif minyak atsiri sereh wangi Jawa dimasukkan ke dalam campuran basis dan diaduk sampai homogen.
d. Salep dimasukkan dalam pot salep (Paramita, 2005).
4. Evaluasi sediaan
Uji sifat fisik yang dilakukan dalam penelitian ini adalah:
a. Uji pH. Pengukuran pH dilakukan dengan menggunakan pH indikator stick. Uji pH diukur dengan cara mencelupkan stik pH pada sampel dan perubahan warna yang terjadi dicocokan pada indikator warna pH yang ada diwadah.
b. Uji Viskositas. Pengukuran viskositas menggunakan alat viskotester. Viskositas diukur dengan cara salep dimasukkan ke wadah dan dipasangkan pada portable viskotester. Viskotester salep diketahui dengan mengamati gerakan jarum penunjuk viskositas dan dilakukan pembacaan pada skala dPas dari salep yang diuji (Martin, 1983).
c. Uji daya sebar. Salep ditimbang seberat 1 gram dan diletakkan ditengah kaca bulat berskala kemudian diletakkan kaca bulat yang lain sebagai penutup ditambahkan pemberat dengan berat total 125 gram kemudian didiamkan selama 1 menit dan dicatat diameter penyebarannya.
29
5. Uji aktivitas antibakteri salep minyak sereh wangi Jawa terhadap Staphylococcus epidermidis dengan metode difusi sumuran
a. Persiapan alat dan bahan uji. Alat-alat gelas yang digunakan dibungkus dengan menggunakan kertas payung kemudian disterilisasi dengan menggunakan autoklaf pada suhu 121oC selama 20 menit. Setelah selesai kemudian alat-alat yang telah disterilisasi disimpan dalam oven.
b. Pembuatan medium untuk peremajaan bakteri uji. Medium yang digunakan untuk peremajaan isolat Staphylococcus epidermidis adalah medium Mueller Hinton Agar (MHA) dan Mueller Hinton Broth (MHB).Tujuan peremajaan
adalah untuk memindahkan bakteri ke media baru dengan nutris lebih banyak agar bakteri tetap dapat bertahan hidup. Medium dilarutkan dalam aquades sesuai perbandingan yang ada, kemudian dipanaskan di atas hot plate dan diaduk dengan stearer hingga larut sempurna (bening). Larutan media kemudian di sterilisasi dalam autokaf pada suhu 121oC dan tekanan 1 atm selama 15 menit.
c. Pembuatan media untuk pengujian aktivitas antibakteri. medium yang digunakan untuk pelaksanaan uji antibakteri adalah medium MHA (Muller Hinton Agar). Sebanyak 3,4 gram MHA Oxoid dilarutkan dalam 100 mL
30
diawali dengan layer bawah dahulu dan ditunggu sampai memadat baru dituangkan layer atasnya dan kembali ditunggu sampai memadat dan selanjutnya baru dilakukan pembuatan sumuran.
d. Pembuatan suspensi bakteri uji. Jumlah bakteri yang akan diuji dihitung berdasarkan perhitungan kekeruhan yang disetarakan dengan Mc Farland 0,5 dengan jumlah bekteri 1,5 x 108 CFU/mL. Sebanyak 1 ose kultur bakteri uji dalam MHB divortex sampai kekeruhanya sama dengan larutan Mc Farland 0.5 sehingga diperoleh jumlah bakteri uji sebesar 150 juta/mL.
e. Pembuatan kontrol media. Media MHA steril dituang ke dalam cawan petri dan dibiarkan memadat, kemudian diinkubasi selama 24 jam pada suhu 37oC di dalam inkubator, selanjutnya diamati dan dibandingkan dengan perlakuan.
f. Pembuatan kontrol pertumbuhan bakteri uji. Media MHA steril diinokulasikan suspensi bakteri uji Staphylococcus epidermidis dengan kepadatan dan jumlah yang sama pada perlakuan, kemudian dituang ke dalam cawan petri steril dan digoyang agar pertumbuhan bakteri uji merata. Cawan petri yang telah berisi suspensi bakteri uji didiamkan hingga memadat, kemudian diinkubasi selama 24 jam pada suhu 37oC di dalam inkubator, selanjutnya pertumbuhan bakteri uji diamati dengan melihat kekeruhan media dan dibandingkan dengan perlakuan.
31
Klindamisin dilarutkan kedalam aquadest sesuai perhitungan agar didapatkan larutan dengan konsentrasi 0,2% kemudian diaduk hingga serbuk larut. h. Pembuatan kontrol positif salep klindamisin 1%. Bahan-bahan ditimbang,
lalu dimasukkan ke cawan porselen kemudian disterilisasi dengan oven pada suhu 180°C selama 1 jam (kecuali serbuk klindamisin). Basis yang telah meleleh, diaduk homogen dalam mortir hangat sampai dingin. Zat aktif klindamisin sebanyak 1% dilarutkan kedalam PEG 400 kemudian dicampurkan dengan PEG 4000 diaduk kembali sampai homogen.
32
pembanding kemampuan aktivitas minyak atsiri sereh wangai Jawa dalam menghambat bakteri uji dengan produk pasaran yang ada.
j. Uji aktivitas antibakteri salep minyak sereh wangi Jawa terhadap bakteri uji. Sebanyak 15 mL media MHA diisi ke dalam cawan petri steril dan dibiarkan memadat (lapis pertama), kemudian sebanyak 25 mL media MHA yang telah diinokulasikan suspensi bakteri uji Staphylococcus epidermidis dituangkan di atas lapisan pertama, sehingga menjadi lapisan kedua dan dibiarkan memadat, selanjutnya dibuat tujuh sumuran dengan diameter sumuran 0,8 cm. Sebanyak dua sumuran masing-masing diisi dengan 0,05 mL salep minyak sereh wangi Jawa (F I dan F II) dengan konsentrasi masing-masing 12%(b/b)), satu sumuran untuk minyak atsiri sereh wangi Jawa 15% v/v dengan pelarut PEG 400 dan sumuran yang tersisa masing-masing diisi dengan 0,05 mL basis salep (FI dan FII) sebagai kontrol basis dan salep klindamisin 1% sebagai kontrol positif. Cawan petri dibungkus dengan menggunakan plastik wrap, kemudian diinkubasi selama 24 jam pada suhu 37oC di dalam inkubator, selanjutnya diamati dan diukur diameter zona hambat yang dihasilkan.
6. Uji sterilitas sediaan salep
Media MHA steril sebanyak 25mL dituang ke dalam cawan petri dan dibiarkan memadat, kemudian sediaan salep minyak atsiri sereh wangi Jawa digoreskan diatas permukaan media secara aseptis dengan mengunakan ose. Kemudian diinkubasi selama 24 jam pada suhu 37oC di dalam inkubator, selanjutnya diamati apakah terlihat ada pertumbuhan bakteri atau tidak.
33
E. Analisis Hasil
Data yang diperoleh dalam penelitian ini adalah data aktivitas antibakteri minyak atsiri sereh wangi Jawa dan salep minyak atsiri sereh wangi Jawa dianalisis menggunakan software R 2.14.1.1. Analisis statistik digunakan untuk melihat signifikansi perbedaan dari data yang diperoleh. Uji normalitas data dilakukan dengan analisis statistik Saphiro-Wilk kemudian dilanjutkan menggunakan uji Levene test untuk melihat homogenitas data. Pada distribusi data normal dilakukan analisis statistik parametrik ANAVA satu arah dan dilanjutkan uji Tukey untuk melihat keberbedaannya, sedangkan pada distribusi data tidak normal digunakan analisis statistik non parametrik (Wilcoxon atau Kruskal-Wallis). Analisis data sifat fisik minyak dan sifat fisik salep dilakukan dengan
cara membandingkannya terhadap standar yang telah ditetapkan.
34 BAB IV
HASIL DAN PEMBAHASAN
A. Identifikasi dan Verifikasi Minyak Sereh Wangi Jawa
Identifikasi bahan dalam penelitian ini dilakukan dengan tujuan untuk menjamin kebenaran serta kesesuaian bahan yang digunakan dengan tujuan dari penelitian, sehingga dapat menghindari adanya resiko terjadinya bias pada hasil penelitian yang didapatkan. Pada penelitian ini digunakan minyak atsiri yang berasal dari tanaman sereh wangi Jawa yang diperoleh dari CV Indaroma Yogyakarta dan telah diuji identitasnya dengan disertakannya Certificate of Analysis (CoA) yang terlampir (Lampiran 1).
Dalam penelitian ini dipilih minyak sereh wangi Jawa sebagai bahan aktif karena berdasarkan penelitian yang telah dilakukan diketahui bahwa minyak sereh wangi Jawa diketahui memiliki aktifitas antibakteri dan mempunyai nilai KBM sebesar 15% (Wijayanti, 2013). Senyawa aktif pada minyak sereh yang berfungsi sebagai antibakteri pada penelitian tersebut adalah sitronelal dan geraniol (Nakahara et al, 2003).
Pada penelitian ini juga dilakukan verifikasi minyak sereh Jawa, tujuannya adalah memastikan keaslian minyak sereh wangi Jawa yang digunakan dalam penelitian ini. Verifikasi ini perlu dilakukan karena minyak atsiri yang berasal dari sumber dan jenis tanaman yang berbeda memiliki indeks bias dan bobot jenis yang berbeda sehingga perlu dilakukannya penegasan sebelum minyak
35
tersebut digunakan. Verifikasi yang dilakukan dalam penelitian ini meliputi pengamatan organoleptis, uji indeks bias dan uji bobot jenis sesuai dengan ketentuan yang ditetapkan oleh SNI. Hasil verifikasi minyak sereh wangi Jawa yang diperoleh adalah sebagai berikut (Lampiran 3).
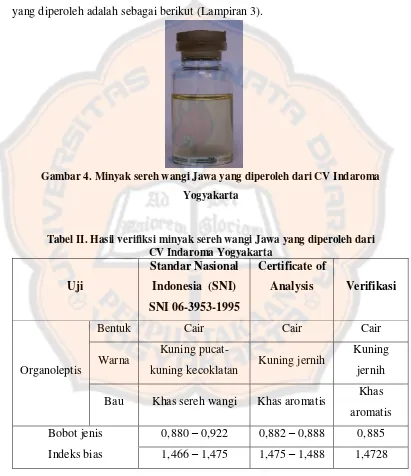
Gambar 4. Minyak sereh wangi Jawa yang diperoleh dari CV Indaroma Yogyakarta
Tabel II. Hasil verifiksi minyak sereh wangi Jawa yang diperoleh dari CV Indaroma Yogyakarta
kuning kecoklatan Kuning jernih
Kuning jernih
Bau Khas sereh wangi Khas aromatis Khas aromatis Bobot jenis
Indeks bias
0,880 – 0,922 0,882 – 0,888 0,885 1,466 – 1,475 1,475 – 1,488 1,4728
Berdasarkan hasil verifikasi diketahui bahwa minyak sereh wangi Jawa yang digunakan memenuhi persyaratan, yang mana berdasarkan hasil pengamatan minyak sereh wangi Jawa sesuai dengan karakteristik dan standar organoleptis,
36
bobot jenis dan indeks bias yang telah ditetapkan oleh Badan Standarisasi Nasional (1995). Dengan demikian dapat dikatakan minyak sereh wangi Jawa yang diperoleh dari CV Indaroma merupakan minyak sereh wangi dengan kualitas yang baik.
B. Uji Aktivitas Antibakteri Minyak Sereh Wangi Jawa terhadap Staphylococcus epidermidis dengan Metode Difusi Sumuran
Uji aktivitas antibakteri minyak sereh wangi Jawa pada penelitian ini merupakan uji pendahuluan yang dilakukan dengan tujuan untuk memastikan adanya daya antibakteri minyak sereh wangi Jawa dan melihat seberapa besar daya antibakteri yang ditimbulkan dari minyak sereh wangi Jawa terhadap bakteri uji yang selanjutnya dapat dipertimbangkan untuk digunakan dalam formulasi sediaan salep minyak sereh wangi Jawa.
Pada penelitian ini digunakan sebagai bakteri uji adalah Staphylococcus epidermidis ATCC 12228 yang diperoleh dari Balai Laboratorium Kesehatan
Yogyakarta dan telah diuji kemurniannya dengan surat keterangan kultur Staphylococcus epidermidis terlampir (Lampiran 2). Staphylococcus epidermidis
dipilih sebagai bakteri uji karena menurut Jawetz, Melnick, Adelberg (1996) bakteri ini merupakan salah satu flora normal yang banyak ditemukan dikulit dan merupakan penyebab infeksi pada kulit.
Uji aktivitas antibakteri dilakukan dalam Microbiological Safety Cabinet (MSC), tujuannya untuk meningkatkan kondisi lingkungan yang aseptis sehingga dapat meminimalisir terjadinya kontaminasi selama penelitian. Dalam penelitian
37
ini dipilih metode difusi sumuran untuk melihat aktivitas antibakteri minyak sereh wangi Jawa yang digunakan. Metode difusi sumuran dipilih karena dengan alasan kesesuaian dari bentuk dan sifat sampel yang digunakan. Minyak serai wangi Jawa bersifat lipofil, dimana jika digunakan metode paper disk tidak memungkinkan karena paper disk tesusun dari selulosa yang mempunyai sifat hidrofil sehingga jika digunakan sampel dengan sifat lipofil akan terjadi inkompatibilitas dan sampel minyak yang digunakan tidak dapat terdifusi dalam media secara maksimal.
Sifat bahan uji minyak sereh wangi Jawa memiliki tingkat kepolaran yang cenderung non polar, sedangkan media yang digunakan yaitu MHA mempunyai sifat lebih polar karena komposisi utamanya adalah air. Oleh sebab itu pengenceran variasi minyak sereh wangi Jawa dalam penelitian ini digunakan pelarut PEG 400 yang mana merupakan suatu pelarut dengan sifat cenderung lebih polar. Minyak sereh wangi Jawa akan terjerap dan terdispersi homogen dalam pelarut PEG 400, sehingga dengan tingkat kepolaran yang hampir sama (polar) antara pelarut dan media diharapkan dapat melarutkan minyak sereh wangi Jawa dan dapat meningkatkan kemampuan difusi minyak atsiri ke permukaan media MHA tanpa mempengaruhi aktivitas antibakteri minyak sereh wangi Jawa. Selain itu, pemilihan PEG 400 sebagai pelarut juga karena PEG 400 merupakan salah satu bahan cair yang digunakan dalam formulasi sediaan salep yang akan diuji dalam penelitian ini.
Suatu senyawa dikatakan memiliki aktivitas antibakteri apabila memiliki zona hambat berupa area jernih di sekeliling sumuran dan lebih besar dengan
38
perbedaan bermakna dari kontrol pelarut (kontrol negatif). Kontrol negatif atau kontrol pelarut berfungsi untuk mengetahui pelarut yang digunakan memiliki aktivitas antibakteri terhadap pertumbuhan Staphylococcus epidermidis. Pelarut yang memiliki aktivitas penghambatan bakteri uji dapat membiaskan hasil penelitian karena menyebabkan positif palsu zona hambat pada variasi konsentrasi. Variasi konsentrasi minyak sereh wangi Jawa yang digunakan dalam pengujian aktivitas anibakteri adalah 5; 7,5; 10; 12,5; 15; 17,5 dan 20% (v/v). Berikut merupakan hasil pengukuran rerata diameter zona hambat terhadap bakteri uji Staphylococcus epidermidis (lampiran 4).
Tabel III. Hasil pengukuran rerata diameter zona hambat minyak sereh wangi Jawa terhadap Staphylococcus epidermidis
Konsentrasi % (v/v) 𝒙 ± SD
Diameter Zona Hambat (mm)
5 4,33 ± 0,57
7,5 5,66 ± 1,15
10 6 ± 1
12,5 8,33 ± 1,15
15 10 ± 0
17,5 10,33 ± 1,15
20 11 ± 0
kontrol positif (Klindamisin 0.2%) 48 ± 0
kontrol negatif (PEG 400) 0 ± 0
39
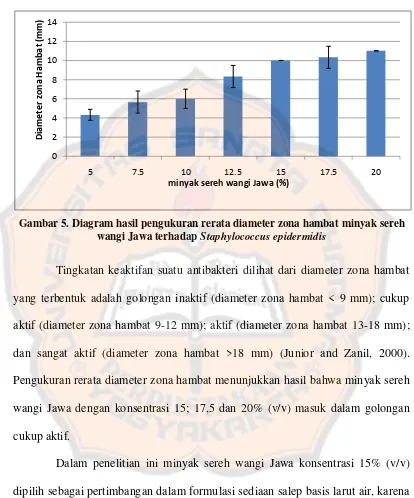
Gambar 5. Diagram hasil pengukuran rerata diameter zona hambat minyak sereh wangi Jawa terhadap Staphylococcus epidermidis
Tingkatan keaktifan suatu antibakteri dilihat dari diameter zona hambat yang terbentuk adalah golongan inaktif (diameter zona hambat < 9 mm); cukup aktif (diameter zona hambat 9-12 mm); aktif (diameter zona hambat 13-18 mm); dan sangat aktif (diameter zona hambat >18 mm) (Junior and Zanil, 2000). Pengukuran rerata diameter zona hambat menunjukkan hasil bahwa minyak sereh wangi Jawa dengan konsentrasi 15; 17,5 dan 20% (v/v) masuk dalam golongan cukup aktif.
40
Aktivitas antibakteri minyak sereh wangi Jawa sebagai senyawa antibakteri karena adanya kandungan Sitronelal (monoterpen aldehida). Menurut Lertsatitthanakorn, et al., (2010) Senyawa Sitronelal mempunyai aktivitas antibakteri yaitu dengan target membran protein fungsional. Senyawa tersebut akan menyebabkan peningkatan permeabilitas membran bakteri gram positif. Aktivitas antibakteri monoterpen aldehida yang ditemukan dalam minyak sereh wangi Jawa diperkirakan disebabkan karena senyawa elektronegatif yang dapat menggangu komponen nitrogen dari protein pada membran sitoplasmik, isi sitoplasmik dan asam nukleat.
Selain sitronelal, monoterpen alkohol berupa geraniol, sitronelal, monoterpen alkohol siskuiterpene juga ditemukan dalam minyak sereh wangi Jawa. Aktifitas antibakteri gugus alkohol bertindak sebagai agen pendehidrasi pada dosis rendah dan agen pendenaturai pada dosis tinggi. Alkohol dan fenol dapat menyebabkan pecahnya membran sitoplasma dan kerusakan dinding bakteri. Setelah diberi perlakuan dengan minyak sereh wangi Jawa dinding sel bakteri Gram positif akan kehilangan struktur kakunya dan komponen dinding yang rusak akan mengakibatkan kebocoran pada membran sitoplasma sehingga materi-materi intraseluler keluar dari sel dan sel akhirnya lisis (Lertsatitthanakorn, et al., 2010)
C. Formulasi Sediaan Salep Minyak Sereh Wangi Jawa
Pada penelitian ini minyak sereh wangi Jawa diformulasikan dalam bentuk sediaan salep dengan basis larut air. Sediaan salep dengan basis larut air
41
dipilih karena didasarkan pada sifat dari minyak sereh yaitu lipofil, sehingga diperlukan media pembawa yang mempunyai sifat yang lebih hidrofil supaya pelepasan zat aktif dapat optimal karena dengan afinitas yang rendah dapat mengobati penyakit infeksi yang disebabkan oleh bakteri. Kandungan air yang cukup besar dalam sediaan salep dengan basis larut air diharapkan dapat meningkatkan difusi minyak sereh wangi Jawa. Alasan lain dipilihnya basis larut air ini adalah agar bahan aktif yang mempunyai sifat berminyak dapat sedikit tertutupi sehingga diharapkan salep minyak sereh wangi Jawa basis larut air dapat digunakan dengan lebih nyaman. Selain itu dipilihnya basis salep larut air memiliki kelebihan tidak mudah tengik, tingkat penyebaran dan penetrasinya tinggi dan mudah dibersihkan dengan air. Adanya kelebihan yang ada diharapkan dapat meningkatkan penerimaan dan kenyamanan penggunanya. Bahan-bahan yang digunakan dalam formula salep minyak sereh wangi Jawa tidak mempunyai efek antibakteri (Raymond., Paul and Marian, 2009).
Pembuatan sedian salep minyak sereh wangi Jawa dilakukan secara aseptis dengan melakukan sterilisasi terhadap bahan – bahan yang akan digunakan yaitu PEG 400 dan PEG 4000 serta alat-alat yang digunakan dengan menggunakan oven pada suhu 180oC selama 1 jam. Metode sterilisasi menggunakan oven dipilih dengan alasan bahwa bahan-bahan yang digunakan yaitu PEG 400 maupun PEG 4000 menurut Raymond., Paul and Marian (2009) tahan terhadap panas dan dapat dilakukan sterilisasi dengan suhu tinggi seperti autoklaf dan oven. Pada formulasi sediaan salep minyak sereh wangi Jawa dibuat juga kontrol negatif. Tujuan dibuatnya kontrol negatif ini adalah sebagai
42
pembanding terhadap aktivitas antibakteri salep minyak sereh wangi Jawa terhadap bakteri uji Staphylococcus epidermidis dan sebagai faktor koreksi dalam pengamatan aktivitas antibakteri salep minyak sereh wangi Jawa, sehingga dapat diketahui diameter zona hambat yang berasal dari minyak sereh wangi Jawa dan bukan berasal dari basis. Kontrol positif dalam penelitian ini dibuat dengan tujuan untuk membandingkan aktivitas antibakteri salep sereh wangi Jawa yang dibuat dengan salah satu produk atau agen antibakteri yang telah beredar dipasaran selain itu juga merupakan hasil dari orientasi. Hasil orientasi menunjukkan hasil bahwa diameter zona hambat sesuai dengan yang diinginkan peneliti, yaitu tidak terlalu kecil dan tidak terlalu besar. Diameter zona hambat yang terlalu besar akan menyebabkan kemmungkinan terjadinya hasil yang overlap dan dapat membiaskan dalam pengamatan. Klindamisin dibuat dengan konsentrasi 1% yang diformulasikan kedalam dalam bentuk sediaan dan basis yang sama yang digunakan dalam penelitiaan ini. Klindamisin adalah antibiotika linkosamid semisintetik yang diturunkan dari linkomisin. Mekanisme kerja antibiotika ini serupa dengan eritromisin, dengan mengikat ribosom 50S dan menekan sintesis protein bakteri (Bonner M, Benson P, James W. 2008). Klindamisin dengan konsentrasi 1% dipilih karena merupakan konsentrasi umum yang digunakan dalam produk pasaran. Salep klindamisin diformulasikan secara mandiri dalam bentuk salep dengan formula yang sama dengan salep minyak sereh wangi Jawa karena cukup sulit ditemukan klindamisin dalam bentuk salep dipasaran. Selain itu, keuntungan dibentuknya salep klindamisin dengan formula yang sama dengan salep minyak sereh wangi Jawa adalah untuk meminimalisir terjadi bias pada
43
pengukuran diameter zona hambat akibat pengaruh formula, sehingga dapat diketahui diameter zona yang dihasilkan hanya berasal dari bahan aktif yang terkandung dalam salep klindamisin saja ataupun minya sereh wangi saja. Berikut ini adalah hasil formulasi sediaan salep sereh wangi Jawa ( Lampiran 6).
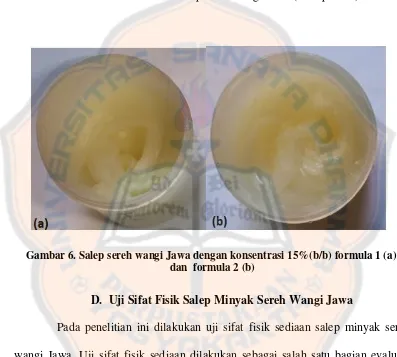
Gambar 6. Salep sereh wangi Jawa dengan konsentrasi 15%(b/b) formula 1 (a); dan formula 2 (b)
D. Uji Sifat Fisik Salep Minyak Sereh Wangi Jawa
Pada penelitian ini dilakukan uji sifat fisik sediaan salep minyak sereh wangi Jawa. Uji sifat fisik sediaan dilakukan sebagai salah satu bagian evaluasi dari formulasi yang dilakukan pada penelitian ini. Tujuannya adalah untuk mengetahui apakah sediaan salep yang dihasilkan telah memiliki sifat fisik dan stabilitas yang baik. Sifat fisik dan stabilitas dapat menentukan kualitas dari suatu sediaan farmasi serta kemudahannya untuk digunakan bagi konsumen. Parameter sifat fisik yang diamati diantaranya meliputi pH, daya sebar dan viskositas yang diuji 48 jam setelah proses pembuatan. Tujuan dilakukannya uji 48 jam setelah