i
Pemeriksaan I
Nama / Paraf Asisten Pemeriksaan II
& Stempel Lab. OTK
Terlambat: hari (Paraf dan stempel pada saat laporan di kumpulkan) FAKULTAS TEKNIK UNTIRTA
JURUSAN TEKNIK KIMIA
LABORATORIUM OPERASI TEKNIK KIMIA
LABORATORIUM OPERASI TEKNIK KIMIA HALAMAN JUDUL
LEMBAR PENUGASAN
Program *) : - TK.404 Lab. Operasi Teknik Kimia I - TK.405 Lab. Operasi Teknik Kimia II Percobaan No. : 3
Nama Percobaan : Distilasi
DITUGASKAN KEPADA KELOMPOK NO :
NIM : 3335210007 Nama : Ahmad Daerobi NIM : 3335210100 Nama : Puan Maharani NIM : 3335210102 Nama : Selviroh Praktikum Tanggal : 02 Oktober 2023
Sifat Tugas : Biasa / Ulangan / Perbaikan
Keterangan Tugas:
Cilegon, 2023
Dr. H. Rudi Hartono, S.T., M.T. IPM
NIP. 196702062001121001
Form. 01/Lab OTK/2023
ii Catatan :
Cilegon, 2023 Cilegon, 2023
Asisten Dosen Pembimbing
Ghiyats Febriyanto Dr. H. Rudi Hartono, S.T., M.T. IPM
NIM. 3335190076 NIP. 196702062001121001
iii
LEMBAR PENGESAHAN PEMBICARAAN AKHIR MODUL : DISTILASI
Catatan :
Cilegon, 2023
Dosen Pembimbing
Dr. H. Rudi Hartono, S.T., M.T. IPM NIP. 196702062001121001
iv
package dan menentukan pengaruh konsentrasi, temperature, serta proses refluks pada proses distilasi. Aplikasi industri distilasi salah satunya yakni pada proses pegolahan minyk mentah yang mengandung banyak senyawa hidrokarbon, lalu dipisahkan dengan kolom distilasi untuk mengahsilkan produk yang diinginkan.
Percobaan ini dilakukan dengan tahapan persiapan alat dan bahan, kalibrasi refaktometer, proses distilasi refluks total dan parsial. Prosedur diawali dengan periapan alat dan bahan lalu kalibrasi refaktometer, kemudia percobaan proses distilasi dengan refluks total dilanjut refluks parsial. Hasil percobaan menunjukkan efisiensi kolom distilasi package terbaik berada pada konsentrasi umpan 50%
dengan proses refluks total yaitu sebesar 81% serta semakin besar konsentrasi, maka fraksi mol etanol pada distilat akan semakin besar. Refluks parsial menghasilkan fraksi mol distilat yang lebih tinggi, namun kemurniannya lebih rendah dibandingkan refluks total.
Kata kunci: Distilasi, Efisiens,i Etanol-ail, Fraksi, Refluks, Volatilitas
v DAFTAR ISI
Halaman
HALAMAN JUDUL ... i
LEMBAR PENGESAHAN PEMBICARAAN AWAL ... ii
LEMBAR PENGESAHAN PEMBICARAAN AKHIR ... iii
RINGKASAN ... Error! Bookmark not defined. DAFTAR ISI ... v
DAFTAR GAMBAR ... viii
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Rumusan Masalah ... 2
1.3 Tujuan Percobaan ... 2
1.4 Ruang Lingkup ... 2
BAB II TINJAUAN PUSTAKA ... 3
2.1 Distilasi ... 3
2.2 Menara Distilasi ... 7
2.3 Faktor-faktor yang Memengaruhi Distilasi ... 7
2.4 Kesetimbangan Uap Cair (VLE) ... 8
2.4.1 Harga-K dan Volatilitas Relatif... 9
2.5 Dew Point dan Bubble Point ... 11
2.6 Refraktometer ... 12
2.6.1 Hand Refraktometer ... 12
2.6.2 Refraktometer Imersi (Refraktometer Celup) ... 13
2.6.3 Refraktometer ABBE ... 13
2.7 Pengenceran Larutan ... 15
vi
3.1.1 Diagram Alir Kalibrasi Alat Refraktometer ... 17
3.1.2 Diagram Alir Percobaan Refluks Total ... 17
3.1.3 Diagram Alir Percobaan Refluks Parsial ... 19
3.2 Alat dan bahan... 20
3.2.1 Alat ... 20
3.2.2 Bahan ... 20
3.3 Prosedur percobaan ... 20
3.3.1 Kalibrasi Alat Refraktometer ... 21
3.3.2 Percobaan Refluks Total ... 21
3.3.3 Percobaan Refluks Parsial ... 21
3.4 Gambar Alat ... 22
3.5 Variabel Percobaan ... 22
BAB IV HASIL DAN PEMBAHASAN ... 23
4.1 Kalibrasi Refraktometer ... 23
4.2 Pengaruh Konsentrasi Umpan dan Refluks terhadap Distilasi ... 25
4.3 Pengaruh Refluks dan Konsentrasi Umpan Terhadap Efisiensi dan Yield .. 27
4.3.1 Pengaruh Refluks dan Konsentrasi Umpan Terhadap Nilai Efisiensi 27 4.3.2 Pengaruh Refluks dan Konsentrasi Umpan Terhadap Nilai Yield ... 28
4.4 Hubungan Yield dan Efisiensi yang Diperoleh ... 30
BAB V KESIMPULAN DAN SARAN ... 31
5.1 Kesimpulan ... 31
5.2 Saran ... 31
vii
DAFTAR PUSTAKA ... 32 LAMPIRAN
A. Contoh Perhitungan B. MSDS
C. Jurnal Penelitian D. Fotocopy Logbook E. Blanko Percobaan
viii
Gambar 2.2 Distilasi Fraksional ... 5
Gambar 2.3 Distilasi Vakum ... 5
Gambar 2.4 Distilasi Ekstraktif ... 6
Gambar 2.5 Diagram pada Dew Point dan Bubble Point ... 11
Gambar 2.6 Hand Refraktometer... 12
Gambar 2.7 Refraktometer Imersi ... 13
Gambar 2.8 Refraktometer ABBE... 14
Gambar 3.1 Diagram Alir Kalibrasi Alat Refraktometer ... 17
Gambar 3.2 Diagram Alir Percobaan Refluks Total ... 19
Gambar 3.3 Diagram Alir Percobaan Refluks Parsial ... 20
Gambar 3.4 Perangkat Distilasi Batch ... 22
Gambar 4.1 Grafik Pengaruh Fraksi Mol terhadap Indkes Bias... 23
Gambar 4.2 Grafik Pengaruh Fraksi Volume Mol Etanol terhadap ... 24
Gambar 4.3 Grafik Pengaruh Konsentrasi dan Refluks Terhadap Distilasi ... 25
Gambar 4.4 Grafik Konsentrasi vs Efisiensi ... 27
Gambar 4.5 Grafik Konsentrasi vs Yield ... 29
1 BAB I PENDAHULUAN 1.1 Latar Belakang
Industri kimia merupakan salah satu sektor terpenting dalam ekonomi global yang perannya untuk pembuatan berbagai produk kimia, bahan kimia, dan material penting dalam kebutuhan manusia sehari-hari. Dalam industi kimia, pemisahan bahan-bahan kimia menjadi komponan yang lebih murni menjadi tahapan kritis dalam banyak proses manufaktur. Salah satu metode pemisahan yang diterapkan adalah distilasi (Ariono, 2019).
Distilasi merupakan proses pemisahan campuran cairan berdasarkan perbedaan titik didih dan tekanan uap komponen-komonennya. Umumnya digunakan untuk pemisahan komponen-komponen dalam campuran kimia dengan tujuan menghasilkan produk yang lebih murni. Salah satu perangkat yang digunakan dalam distilasi adalah distilasi package (Budiman, 2019).
Distilasi Package yakni perangkat yang digunakan untuk melakukan distilasi fraksional dalm jumlah besar. Kolom ini mengandung sejumlah baki atau tray yang digunakan untuk memisahkan komponen campuran cairan.
Efisiensi dari kolom distilasi package menjadi parameter penting dalam industri kimia karena dapat memengaruhi kualitas produk yang dihasilkan (Budiman, 2019).
Selain itu peningkatan efisiensi dari kolom distilasi package akan dipengaruhi oleh faktor-faktor selama proses distilasi. Terdapat tiga faktor utama yakni konsentrasi, suhu dan proses refluks. Maka dengan dilakukannya percoabaan ini agar dapat memahami peningkatan efisienasi dan pengaruh faktor-faktor pada proses distilasi (Ariono, 2019). Sehingga nantinya dapat mendukung industri dalam meningkatkan kualitas produk kimia sesuai yang diinginkan dan meninimalisir limbah.
1.2 Rumusan Masalah
Rumusan masalah pada percobaan ini dalam setiap proses industri kimia tentu mengingkan produk kahir yang murni dan menimimalisi hasil limbah sisa produksi. Sehingga dilakukan distilasi, salah satunya distilasi package yang dimana dalam prosesnya menentukan efisiensi dan memahami faktor-faktor berupa konsentrasi, suhu, dan proses refkuks menjadi sangat penting.
1.3 Tujuan Percobaan
Tujuan pada percobaan distilasi yakni untuk menentukan efisiensi dari kolom distilasi package dan menentukan pengaruh konsentrasi, temperature, serta proses refluks pada proses distilasi.
1.4 Ruang Lingkup
Ruang lingkup dalam percobaan distilasi yaitu dengan menggunakan metode kuantitatif pada metode distilasi package dengan bukaan valve penuh dan parsial. Lalu untuk bahan yang digunakan berupa ethanol dan aquades.
Percobaan ini di lalukan pada Laboratorium Operasi Teknik Kimia Fakultas Teknik Universitas Sultan Ageng Tirtayasa.
3 BAB II
TINJAUAN PUSTAKA 2.1 Distilasi
Penyulingan atau distilasi adalah proses pemisahan komponen cairan atau padatan dari berbagai macam campuran berdasarkan titik didih uap atau kecepatan menguap bahan yang dikenal dengan volatilitas. Proses pemisahan campuran dengan cara penyulingan dilakukan dengan dua proses, yaitu penguapan dan pengembunan (Rusli, 2010). Prinsip dislitasi yaitu mendapatkan minyak melalui proses penyulingan dari suatu bahan akibat perpindahan panas, penguapan, dan pengembunan. Perpindahan panas terjadi dari sumber panas menuju bahan yang akan disuling.
Jika suatu bahan dipanaskan secara terus-menerus, maka akan terjadi proses penguapan dan menjadi uap jenuh. Uap jenuh akan bersentuhan dengan permukaan yang dingin sehingga terjadi proses kondensasi, yaitu perubahan uap jenuh menjadi air (kondensat) dan akan mengalir ke bawah mengikuti kemiringan kaca karena pengaruh gravitasi dan akan tertampung dalam penampungan. Kondensat yang tertampung dalam penampungan yang akan menjadi minyak (Miftakhur, R, F., 2018).
Distilasi adalah metode yang paling umum digunakan untuk pemisahan campuran homogen dengan metode pemisahan menggunakan perbedaan titik didih dan juga volatilitas antar komponen dalam suatu campuran, tetapi distilasi pada prosesnya memerlukan energi yang tinggi meskipun demikian terdapat banyak keuntungan jika proses pemisahan menggunakan distilasi.
Berikut ini adalah keuntungan dari distilasi:
a. Distilasi memiliki kemampuan untuk memisahkan jenis campuran dengan berbagai macam konsentrasi dan juga produk hasil dari pemisahan relatif murni.
b. Distilasi memiliki kemampuan untuk mengatasi berbagai aliran umpan masuk. Tidak hanya cocok untuk aliran yang rendah, tetapi distilasi juga
cocok untuk aliran yang sangat tinggi sehingga dapat menyesuaukan dengan rancangan pengguna.
c. Memiliki kemampuan untuk memisahkan produk dengan kemurnian yang tinggi. Jika menggunakan alternatif pemisahan selain distilasi, biasanya hanya melakukan pemisahan saja dan tidak dapat menghasilkan produk dengan kemurnian tinggi seperti yang dihasilkan dari proses distilasi (Smith dan Jobson, 2000).
Distilasi dapat dibedakan menjadi beberapa macam menurut Fattimura et al, (2014), yaitu:
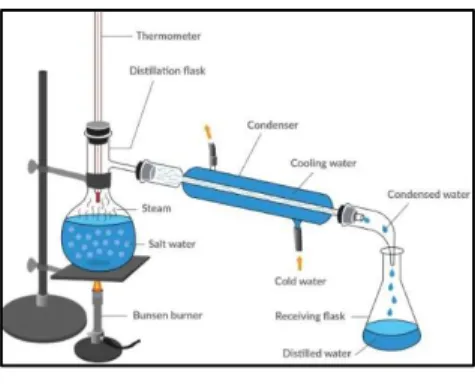
a. Distilasi konvensional (sederhana). Distilasi konvensional adalah proses distilasi yang berlangsung jika campuran dipanaskan sehingga sebagian komponen volatil menguap naik dan didinginkan sampai mengembun di dinding kondensor. Pada distilasi sederhana tidak terjadi fraksionasi pada saat kondensasi karena komponen campuran tidak banyak. Distilasi sederhana sering digunakan untuk tujuan pemurnian sampel dan bukan pemisahan kimia dalam arti sebenarnya.
Gambar 2.1 Distilasi Konvensional
b. Distilasi fraksional atau distilasi bertingkat. Distilasi fraksional merupakan proses yang komponen-komponennya secara bertingkat diuapkan dan diembunkan. Penyulingan terfraksi berbeda dari distilasi biasa karena ada kolom fraksinasi yang memiliki proses refluks. Refluks pada proses penyulingan dilakukan untuk memisahkan campuran bioetanol dan air dapat terjadi dengan baik. Fungsi kolom fraksinasi agar kontak antara cairan
5
dengan uap terjadi sedikit lebih lama sehingga komponen yang lebih ringan dengan titik didih yang lebih rendah akan terus menguap ke kondensor.
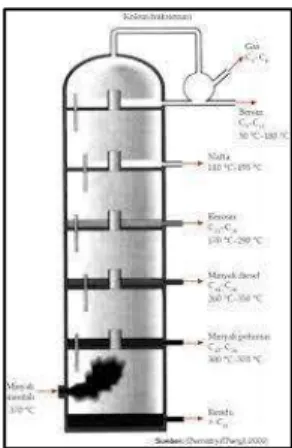
Distilasi jenis ini dapat digunakan untuk memisahkan zat yang mempunyai rentang perbedaan titik didih hingga di bawah 300°C. Distilasi ini biasa digunakan dalam pengolahan minyak bumi karena sangat berguna untuk memisahkan kandungan minyak bumi.
Gambar 2.2 Distilasi Fraksional
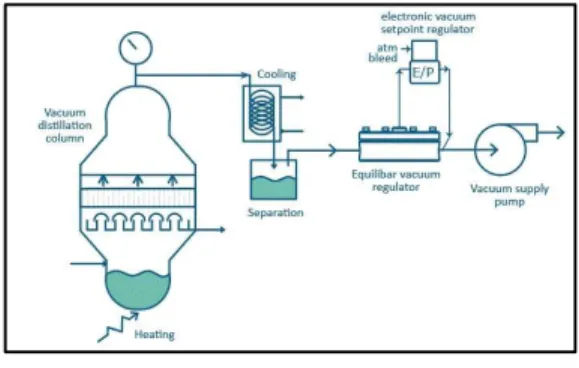
c. Distilasi vakum. Distilasi ini merupakan distilasi yang dilakukan dengan cara cauran diuapkan pada tekanan rendah. Tujuan utamanya adalah untuk menurunkan titik didih cairan yang bersangkutan, dan volatilitas relative meningkat jika tekanan diturunkan. Alat distilasi ini merupakan alat yang tidak sederhana karena memerlukan sistem tertutup.
Gambar 2.3 Distilasi Vakum
d. Distilasi uap. Distilasi ini dilakukan untuk memisahkan komponen campuran pada temperatur lebih rendah dari titik ddih normalnya. Dengan
car aini, pemisahan dapat berlangsung tanpa merusak komponen-komponen yang akan dipisahkan. Ada du acara melakukan distilasi uap. Yang pertama dengan menghembuskan uap secara kontinyu di atas campuran yang sedang diuapkan. Cara kedua adalah dengan cara mendidihkan senyawa yang dipisahkan bersamaan dengan pelarutnya. Dalam model distilasi uap, temperatur dari komponen yang dipisahkan dapat diturunkan dengan cara menguapkannya. Temperature penguapan dalam hal ini lebih rendah dari temperature didih senyawa-senyawa yang dipisahkan. Hal ini juga untuk menjaga senyawa-senyawa yang dipisahkan tidak rusak karena panas.
e. Distilasi azeotrope. Distilasi ini dilakukan dengan cara menguapkan zat cair tanpa perubahan komposisi. Jadi, terdapat perbedaan komposisi antara fase cair dan fase uap, dan hal ini merupakan syarat utama supaya pemisahan dengan distilasi dapat dilakukan. kalau komposisi fase uap sama dengan komposisi fase cair, maka pemisahan dengan jalan distilasi tidak dapat dilakukan. Distilasi ini sering digunakan dalam proses isolasi komponen, pemekatan larutan, dan juga pemurnian komponen cair.
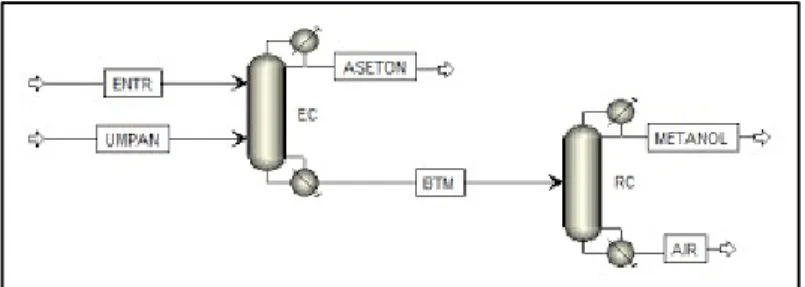
f. Distilasi ekstraktif. Distilasi ini memiliki kemiripan dengan distilasi azeotropik dalam hal penambahan senyawa lain untuk mempermudah proses pemisahan. Dalam hal ini, pelarut yang melakukan ekstraksi karena senyawa yang ditargetkan dapat larut dengan baik dalam pelarut yang dipilih.
Gambar 2.4Distilasi Ekstraktif
7
2.2 Menara Distilasi
Menara distilasi adalah tempat terjadinya proses distilasi, yaitu pemisahan campuran bahan menjadi fraksi-fraksi yang lebih murni berdasarkan perbedaan volatilitas fraksi-fraksi penyusunnya. Campuran yang masuk ke dalam kolom distilasi akan dipanaskan oleh uap panas (steam) pada bagian reboiler sehingga fraksi yang mudah menguap akan naik ke bagian atas kolom distilasi untuk selanjutnya dikondensasikan (diembunkan). Bagian yang tidak menguap akan dikeluarkan sebagai bottom product kolom distilasi. Berikut ini adalah bagian- bagian dari kolom distilasi:
a. Kolom vertical adalah tempat terjadinya pemisahan fraksi dari larutan.
b. Tray sebagai tempat terjadinya pertukaran panas antara cairan dari bagian atas menara menuju ke bawah dengan fraksi uap dari bawah yang menuju ke atas. Pertukaran panas ini berguna untuk meningkatkan kemurnian fraksi yang diambil sebagai distilat.
c. Reboiler atau ketel pemanas berfungsi untuk memanaskan kembali umpan (feed) yang berada di bagian dasar menara distilasi. Tipe lain reboiler adalah steam yang langsung masuk ke dalam bagian dasar menara untuk memanaskan umpan.
d. Kondensor berfungsi untuk mengondensasikan overhead product (distilat) yang akan ditampung pada akumulator (refluks drum).
e. Distilat dan bottom product adalah hasil pemisahan dari menara distilasi.
f. Refluks adalah distilat yang dikembalikan ke dalam menara distilasi.
Refluks berfungsi untuk meningkatkan kemurnian distilat tersebut (Perdana, dkk, 2010).
2.3 Faktor-faktor yang Memengaruhi Distilasi
Berikut ini adalah faktor-faktor yang memengaruhi distilasi menurut (Sinnott,2005), yaitu:
a. Kondisi feed. Keadaan campuran dan kondisi feed memengaruhi garis operasi dan jumlah stage yang digunakan dalam pemisahan distilasi. Hal ini juga memengaruhi letak lokasi feed tray.
b. Kondisi refluks. Pemisahan semakin baik jika menggunakan sedikit tray untuk mendapatkan tingkat pemisahan. Tray minimum di bawah kondisi total refluks, yakni tidak ada penarikan distilat. Sebaliknya, refluks berkurang, maka garis operasi untuk bagian reaktifikasi bergerak terhadap garis kesetimbangan.
c. Kondisi aliran uap. Kondisi aliran uap yang merugikan proses distilasi dapat menyebabkan hal-hal yang tidak diinginkan, seperti foaming, entrainment, dan weeping atau dumping. (1) Foaming mengacu pada ekspansi liquid melewati uap atau gas. Walaupun menghasilkan kontak antar fase liquid- uap yang tinggi, foaming yang berlebihan sering mengarah pada terbentuknya liquid pada tray. (2) Entrainment mengacu pada liquid yang terbawa uap atau gas menuju tray di atasnya yang disebabkan laju alir uap yang tinggi sehingga mengurangi efisiensi tray. Bahan yang sukar menguap akan terbawa menuju plate yang menahan liquid dengan bawah yang mudah menguap. Hal ii dapat mengurangi kemurnian distilat serta entrainment yang berlebihan dapat menyebabkan flooding. (3) weeping/dumping merupakan fenomena yang disebabkan aliran uap yang rendah. Tekanan yang dihasilkan uap tidak cukup untuk menahan liquid pada tray. Karena itu, liquid mulai merembes melalui perforasi.
d. Flooding. Flooding terjadi karena aliran uap berlebih yang menyebabkan liquid terjebak pada uap di atas kolom. Peningkatan tekanan dari uap berlebih menyebabkan kenaikan liquid yang tertahan pada plate di atasnya.
Flooding ditandai dengan adanya penurunan tekanan diferensial dalam kolom dan penurunan yang signifikan pada efisiensi pemisahan.
2.4 Kesetimbangan Uap Cair (VLE)
Apabila suatu campuran zat cair berada dalam kesetimbangan dengan campuran uap pada temperatur dan tekanan yang sama, maka dapat dikatakan bahwa sistem campuran zat cair tersebut berada pada kesetimbangan uap cair.
Suatu sistem dikatakan setimbang secara termodinamika jika sistem tersebut
9
tidak mengalami kecenderungan ke arah perubahan pada skala makroskopis (Andika, D., Naomi, H, A., 2017).
2.4.1 Harga-K dan Volatilitas Relatif
Harga-K (K-Value) adalah ukuran tendensi suatu komponen untuk menguap. Jika harga-K suatu komponen tinggi, maka komponen tersebut cenderung untuk terkonsentrasi di fase uap. Sebaliknya, jika harga-K rendah, maka komponen cenderung untuk terkonsentrasi di fase cair.
Berikut ini adalah persamaan untuk menyataakn harga-K, yaitu:
𝐾 =𝑦
𝑥 (2.1)
Keterangan:
𝑦 : Fraksi mol komponen i di fase uap 𝑥 : Fraksi mol komponen i di fase cair
Harga-K adalah fungsi dari temperatur, tekanan, dan komposisi.
Dalam kesetimbangan, jika dua di antara variabel-variabel tersebut telah ditetapkan, maka variabel ketika akan ditentukan harganya. Dengan demikian, harga-K dapat ditampilkan sebagai fungsi dari tekanan dan komposisi, temperatur dan komposisi, atau tekanan dengan temperatur.
Volatilitas relatif (relative volatility) merupakan ukuran kemudahan terpisahkan lewat eksploitasi perbedaan volatilitas. Volatilitas relatif antara komponen i dan j dijelaskan pada persamaan berikut:
𝑎 , =𝐾
𝐾 (2.2)
Keterangan:
𝐾 : harga-K untuk komponen i 𝐾 : harga-K untuk komponen j
Menurut Geankoplis (1983), volatilitas relatif merupakan perbandingan harga-K dari komponen yang lebih mudah menguap terhadap harga-K komponen yang lebih sulit menguap.
𝑎 , = 𝑦 𝑥⁄
𝑦 ⁄𝑥 = 𝑦 𝑥⁄
(1 − 𝑦 )(1 − 𝑥 ) (2.3)
Pada persamaan (3) merupakan volatilitas relatif secara numerik yang menyatakan pemisahan antara komposisi vapor pada yA dengan komposisi liquid pada xA. Persamaan tersebut menjelaskan rasio konsentrasi A pada fase vapor daripada konsentrasi A pada fase liquid yang dibagi dengan rasio konsentrasi B pada fase vapor dan konsentrasi B pada fase liquid dengan 𝑎 = volatilitas relatif A dan B dalam sistem binari.
Jika pada sistem mengikuti Hukum Raoult, seperti sistem pada benzene-toluena, persamaannya sebagai berikut:
𝑦 =𝑃 𝑥
𝑃 𝑦 =𝑃 𝑥
𝑃 (2.4)
Dengan mensubstitusikan Persamaan (4) ke Persamaan (3) pada sistem ideal menghasilkan persamaan baru berikut:
𝑦 = 𝛼𝑥
1 + (𝛼 − 1)𝑥 (2.5)
Dengan 𝛼 = 𝛼 apabila nilainya di atas 1, maka pemisahan mungkin dilakukan. Adanya kemungkinan nilai dari 𝛼 berubah seiring konsentrasi berubah juga. Ketika sistem binari mengikuti Hukum Raoult, maka variasi volatilitas relatif hanya sedikit pada rentang konsentrasi yang besar secara konstan terhadap tekanan total.
11
2.5 Dew Point dan Bubble Point
Ketika cairan dipanaskan perlahan-lahan pada tekanan konstan, temperatur pada saat pertama kali uap gelembung terbentuk disebut temperatur bubble point pada cairan yang diberi tekanan. Ketika uap didinginkan secara perlahan pada temperatur konstan, temperatur pada saat pertama kali tetes terbentuk disebut temperatur dew point pada saat diberi tekanan (Anonim, 2008).
Temperature dew point terjadi ketika tetesan pertama cairan muncul sebagai campuran uap yang didinginkan (pada tekanan konstan). Temperatur bubble point terjadi ketika gelembung pertama uap muncul sebagai campuran cairan yang dipanaskan (tekanan konstan).
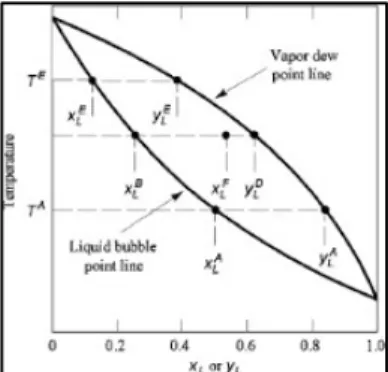
Gambar 2.5 Diagram pada Dew Point dan Bubble Point
Gambar 2.4 adalah diagram titik didih yang menunjukkan komposisi saat kesetimbangan sebagai fungsi dari temperature pada tekanan konstan. Garid yang berada di bawah adalah garis bubble point cairan, tempat terdapatnya titik-titik dimana cairan yang dipanaskan membentuk gelembung uap yang pertama. Garis yang berada di atas adalah garis dew point uap, menunjukkan titik-titik dimana uap saat mengalami penurunan suhu membentuk tetesan cairan yang pertama.
2.6 Refraktometer
Refraktometer adalah alat yang digunakan untuk menentukan konsentrasi atau kadar dari bahan terlarut dengan memanfaatkanw indeks bias suatu cahaya seperti gula atau garam. Indeks bias adalah kecepatan atau perbandingan dengan sinus sudut datang dengan sinus sudut biasa. Nilai pada indeks bias suatu zat terlarut selalu berubah, tergantung nilai suhu dan panjang gelombang yang dibiaskan (Rita, M, H., dkk, 2018). Pengukuran indeks bias dapat dilakukan menggunakan refractometer. Refraktometer menggunakan prinsip pembiasan cahaya ketika mengenai suatu larutan (Hidayanto, E., dkk, 2010).
Prinsip kerja alat refraktometer menggunakan prinsip pembiasan. Jika sampel merupakan larutan dengan konsentrasi rendah, maka yang terjadi sudut refraksi akan lebar dikarenakan perbedaan refraksi dan prisma dan sampel besar. maka skala yang terbaca akan jatuh pada skala rendah. Sedangkan, jika sampel dengan konsentrasi tinggi, maka sudut refraksi akan kecil karena perbedaan refraksi prisma dan sampel kecil. Berikut ini adalah jenis-jenis refraktometer:
2.6.1 Hand Refraktometer
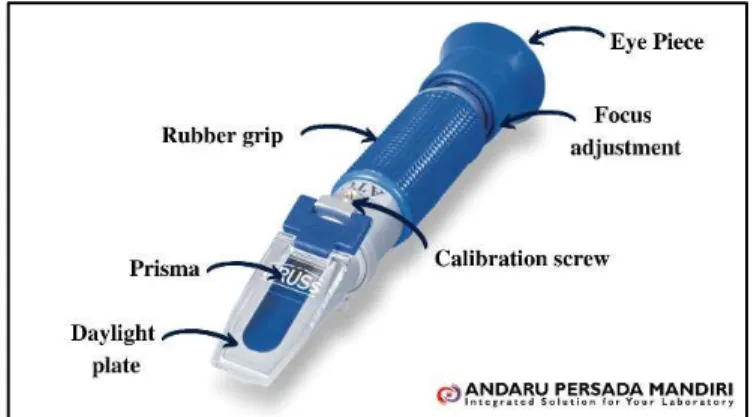
Pada hand refractometer, indeks biasnya sudah dikonversikan sehingga dapat dibaca langsung kadasrnya. Alat ini biasanya hanya untuk mengukur kadar zat tertentu saja. Perbedaan dengan refraktometer lain adalah hand refractometer mempunyai 1 lubang pengamatan.
Gambar 2.6 Hand Refraktometer
13
2.6.2 Refraktometer Imersi (Refraktometer Celup)
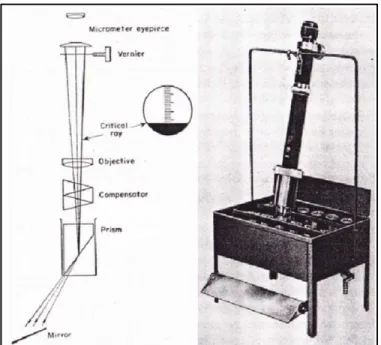
Jenis refractometer ini paling sederhana digunakan, tetapi memerlukan sebanyak 1015 ml sampel. Refraktometer ini menggunakan cahaya buatan dan cahaya putih, terdiri dari kompensator amici. Prisma tunggal dibingkai kuat di dalam teleskop yang berisi kompensator dan bukaan mata (eyepiece). Skala ditempatkan di bawah bukaan mata di dalam tabung. Permukaan lebih bawah prism aitu dicelupkan ke dalam gelas beker yang berisi sampel dengan kaca di bawah untuk merefleksikan cahaya melewati cairan. Instrumen lengkap pada posisinya, dengan penangas air untuk menjaga temepratur refraktometer tetap konstan.
Gambar 2.7 Refraktometer Imersi 2.6.3 Refraktometer ABBE
Refraktometer ABBE memiliki rentang indeks refraksi dari n = 1,30 – 1,71 dan 1,45 – 1,84; kecuali pada beberapa model terbaru.
Reprodusibilitas pembacaan indeks refraksinya adalah ± 0,0002.
Instrumen ini membaca indeks refraksi secara langsung, butuh waktu
lama hingga mendapatkan hasilnya. Hanya memerlukan setetes sampel, dan hasil pengukuran disperse parsialnya baik.
Refraktometer ABBE tidak cocok untuk mengukur indeks refraksi dari larutan yang memiliki komponen volatile atau berbentuk padatan karena ketelitiannya akan berkurang. Sampel padat dapat disisipkan ke permukaan prisma ABBE yang bawah. Specimen yang permukaan bidangnya bening dibuat sedemikian rupa agar kontak optik dengan muka prisma, yaitu dengan cara meletakkan tetes cairan ke permukaan prisma atau dengan cara menekan dengan hati-hati padatan ke tempatnya.
Cahaya putih (white light) digunakan untuk menghindari warna akibat batas tak jelas antara cahaya dan bidang gelap. Peristiwa ini disebabkan oleh perbedaan indeks refraksi cahaya dengan panjang gelombang berbeda-beda yang berasal dari cahaya putih. Dua prisma visi-langsung, disebut prisma Amici ditempatkan di atas lainnya di muka lensa objektif teleskop. Prisma Amici dibuat dari kaca dan didesain agar tidak mendeviasi cahaya garis natrium D. Cahaya dengan panjang gelombang lain akan terdeviasi. Dengan cara merotasi prisma Amici ini, maka dapat meniadakan disperse cahaya pada antarmuka cairan.
Gambar 2.8Refraktometer ABBE
15
2.7 Pengenceran Larutan
Pengenceran larutan adalah proses penurunan konsentrasi larutan dengan penambahan zat pelarut seperti air ke dalam larutan yang pekat. Tujuan pengenceran larutan ini adalah untuk menurunkan konsentrasi larutan dari yang semula pekat menjadi lebih encer. Pada prinspnya, pengenceran hanya menambahkan pelarut sehingga jumlah mol zat terlarut sebelum pengenceran sama dengan jumlah mol zat terlarut sesudah pengenceran.
Berikut in adalah rumus dari pengenceran:
𝑉 𝑀 = 𝑉 𝑀 (2.6)
Keterangan:
V1 = Volume larutan sebelum diencerkan M1 = Molaritas larutan sebelum diencerkan V2 = Volume larutan setelah diencerkan M2 = Molaritas larutan setelah diencerkan
2.8 Height of Packing Equivalent to a Theoritical Plate (HETP)
Performa packed coloumns untuk distilasi atau absorbs sering dinyatakan dengan height of packing equivalent to a theoretical plate (HETP).
Berdasarkan Fenske Equation, Nmin bisa dihitung menggunakan persamaan di bawah ini:
𝑁 =
log 𝑥 , 𝑥 ,
𝑥 , 𝑥 ,
𝑙𝑜𝑔𝛼 , (2.7)
Dimana:
𝛼 , = 𝑦 𝑥
𝑦 𝑥 (2.8)
Nilai q didapatkan dari persamaan:
𝑞 =(𝐻 − 𝐻 ) + 𝑐 (𝑇 − 𝑇 )
𝐻 − 𝐻 (2.9)
Nilai q disubstitusikan ke persamaan di bawah untuk mendapatkan:
1 − 𝑞 = 𝛼, 𝑥
𝛼, − 𝜑 (2.10)
Dengan memasukkan nilai 𝛼 sehingga persamaannya menjadi:
𝛼, = 𝑦 𝑥
𝑦 𝑥 (2.11)
Lalu, untuk mendapatkan nilai Rmin menggunakan Persamaan Underwood
𝑅 + 1 = 𝛼, 𝑥
𝛼, − 𝜑 (2.12)
Selanjutnya mensubstitusi nila Rmin untuk mencari nilai X menggunakan Persamaan Gilliland:
𝑋 = 𝑅 − 𝑅
𝑅 + 1 (2.13)
Untuk mencari N dapat menggunakan persamaan di bawah ini:
𝑁 − 𝑁
𝑁 + 1 = 1 − 𝑒𝑥𝑝 1 + 54,4𝑋 11 + 117,2𝑋
𝑋 − 1 𝑋 ,
17 BAB III
METODOLOGI PERCOBAAN 3.1 Diagram alir
Berikut merupakan diagram alir dari praktikum proses distilasi diantaranya:
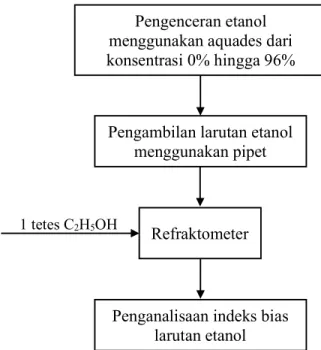
3.1.1 Diagram Alir Kalibrasi Alat Refraktometer
Gambar 3.1 Diagram Alir Kalibrasi Alat Refraktometer 3.1.2 Diagram Alir Percobaan Refluks Total
Pengenceran etanol menggunakan aquades dari konsentrasi 0% hingga 96%
Pengambilan larutan etanol menggunakan pipet
Refraktometer
Penganalisaan indeks bias larutan etanol
Pengukuran indeks bias dan densitas tiap larutan
X 1 tetes C2H5OH
X
Labu didih
Pemasangan labu didih ke pemanas dan kolom distilasi
Penyalaan pompa air pendingin
Pembukaan valve secara penuh pada kondensor
Penyalaan pemanas 85℃ dan memulai penghitungan waktu
Pencatatan perubahan temperatur bawah dan distilat setiap 5 menit
selama 1 jam operasi
Penganalisaan indeks bias pada distilat setiap 5 menit selama 1 jam
operasi
X Larutan C2H5OH
19
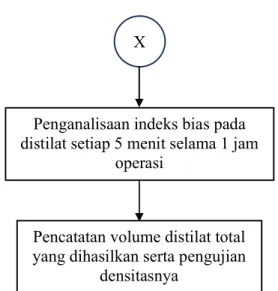
Gambar 3.2 Diagram Alir Percobaan Refluks Total 3.1.3 Diagram Alir Percobaan Refluks Parsial
X
Penganalisaan indeks bias pada distilat setiap 5 menit selama 1 jam
operasi
Pencatatan volume distilat total yang dihasilkan serta pengujian
densitasnya
Pengubahan bukaan valve pada refluks menjadi parsial ½ bukaan
Penyalaan pemanas 85℃ dan memulai penghitungan waktu
Pencatatan perubahan temperatur bawah dan distilat setiap 5 menit selama 1 jam operasi
Penganalisaan indeks bias pada distilat setiap 5 menit selama 1 jam operasi
Pencatatan volume distilat total yang dihasilkan serta pengujian densitasnya
X
Gambar 3.3 Diagram Alir Percobaan Refluks Parsial 3.2 Alat dan bahan
3.2.1 Alat
Berikut ini adalah peralatan yang digunakan dalam praktikum distilasi.
a. Gelas beker b. Gelas ukur c. Kolom distilasi d. Kondensor e. Labu didih f. Pemanas listrik g. Termometer
h. Valve pengatur refluks 3.2.2 Bahan
Berikut ini adalah bahan-bahan yang digunakan dalam praktikum distilasi.
a. Aquades b. Etanol 96%
3.3 Prosedur percobaan
Dalam praktikum distilasi terdapat tiga buah prosedur percobaan sebagai berikut:
X
Pencatatan volume bottom (umpan) yang tersisa serta pengujian densitasnya
21
3.3.1 Kalibrasi Alat Refraktometer
Pertama-tama, mengencerkan etanol menggunakan aquades sebanyak 11 variasi konsentrasi yaitu 0%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, dan 96% menggunakan labu ukur. Kemudian, mengambil larutan etanol yang sudah diecncerkan tersebut menggunakan pipet sebanyak 1 tetes lalu memasukkannya ke kaca pada refraktometer.
Setelah itu, menganalisis indeks bias larutan etanol yang ditunjukkan oleh refraktometer melalui eyepiece.
3.3.2 Percobaan Refluks Total
Pertama-tama, mengencerkan etanol menggunakan aquades sebanyak 3 variasi konsentrasi yaitu 50%, 65%, dan 80%. Lalu, mengukur indeks bias dan densitas tiap larutan yang sudah dibuat.
Setelah itu, memasukkan larutan ke labu pendidih serta memasangkan labu pendidih ke pemanas dan kolom distilasi. Berikutnya, menyalakan pompa air pendingin dilanjut dengan membuka valve secara penuh untuk melangsungkan refluks total. Menyalakan pemanas pada temperature bottom 85℃ dan memulai menghitung waktu menggunakan stopwatch.
Mencatat perubahan temperatur bawah dan distilat setiap 5 menit selama 1 jam operasi. Lalu, menganalisa indeks bias pada distilat setiap 5 menit.
Mengulangi Langkah yang sama selama 1 jam operasi. Kemudian, setelah 1 jam operasi, mencatat volume distilat total yang dihasilkan serta menguji densitasnya. Proses distilasi dapat langsung diteruskan ke proses parsial tanpa harus mematikan ataupun mengganti umpan yang akan diuji.
3.3.3 Percobaan Refluks Parsial
Jangan menghentikan percobaan refluks total sebelumnya setelah 1 jam operasi. Lalu, mengubah bukaan valve pada refluks menjadi parsial
½ bukaan. Kemudian, menyalakan pemanas pada temperature bottom 85℃ dan memulai menghitung waktu menggunakan stopwatch.
Mencatat perubahan temperatur bawah dan distilat setiap 5 menit selama
1 jam operasi. Lalu, menganalisa indeks bias pada distilat setiap 5 menit.
Mengulangi Langkah yang sama selama 1 jam operasi. Kemudian, setelah 1 jam operasi, mencatat volume distilat total yang dihasilkan dan volume bottom (umpan) yang tersisa lalu menguji densitas keduanya.
3.4 Gambar Alat
Berikut ini adalah gambar perangkat distilasi batch yang digunakan selama praktikum distilasi.
Gambar 3.4 Perangkat Distilasi Batch
3.5 Variabel Percobaan
Terdapat tiga buah variabel percobaan dalam praktikum distilasi, yaitu variabel bebas, variabel terikat, dan variabel kontrol. Variabel bebasnya berupa konsentrasi umpan (etanol) serta perbandingan refluks (total dan parsial).
Variabel terikatnya berupa volume distilat total yang dihasilkan dan volume bottom (umpan) yang tersisa, densitas distilat dan densitas bottom, serta indeks bias distilat. Adapun variabel kontrolnya adalah temperatur bottom, waktu pengamatan perubahan temperatur dan waktu pengamatan indeks bias, tinggi packing, dan jenis packing yang digunakan.
23
BAB IV
HASIL DAN PEMBAHASAN 4.1 Kalibrasi Refraktometer
Percobaan diawali dengan melaukan kalibrasi refaktometer, kalibrasi refaktometer dilakukan dengan menggunakan analisa indeks bias pada campuran etanol-air. Perbandingan sampel analisa etanol-air pada kalibrasi yakni 10:0 mL hingga 0:10 mL dengan range volume 1 mL. Nilai indeks bias yang dihasilkan refaktometer mengidentifikasi kemurnian suatu zat, konsentrasi larutan, dan dapat digunakan sebagai pembanding terhadap analisa yang dilakukan. Berikut ini dapat diamati grafik pengaruh fraksi mol etanol terhadap indeks biar yang telah didapatkan dalam proses kalibrasi.
Gambar 4.1 Grafik Pengaruh Fraksi Mol terhadap Indkes Bias Pada Gambar 4.1 menunjukkan pengaruh fraksi mol etanol terhadap indeks bias. Indeks bias didefinisikan sebagai rasio cepat rambat cahaya di udara terhadap cepat rambat cahaya di larutan etanol. Nilai fraksi mol dihasilkan dengan persamaan berikut.
𝐹𝑟𝑎𝑘𝑠𝑖 𝑀𝑜𝑙 𝐸𝑡𝑎𝑛𝑜𝑙 =
%
% % …………(4.1)
Berdasarkan hasil yang didapat pada grafik pengaruh fraksi mol terhadap indeks bias, grafik mengalami kenaikan. Maka menandakan bahwa
semakin besar konsentrasi maka semakin besar indeks bias larutan sehingga semakin besar pula fraksi mol etanol yang diperoleh. Hal ini sesuai dengan teori bahwa peningkatan konsentrasi larutan berbanding lurus terhadap indeks bias larutan tersebut (Parmitasari, 2013). Fraksi mol etanol berpengaruh terhadap banyaknya kandungan etanol yang terdapat dalam suatu campuran, masih berhubungan dengan konsnetrasi campuran dimana fraksi mol etanol semakin besar pada campuran dengan kandungan etanol atau volume etanol yang semakin bsar pula.
Selain itu, dapat diamati grafik pengaruh volume etanol terhadap indeks biar yang telah didapatkan dalam proses kalibrasi.
Gambar 4.2 Grafik Pengaruh Fraksi Volume Mol Etanol terhadap Indeks Bias
Pada Gambar 4.2 menunjukkan pengaruh fraksi mol etanol terhadap indeks bias. Indeks bias didefinisikan sebagai rasio cepat rambat cahaya di udara terhadap cepat rambat cahaya di larutan etanol. Nilai fraksi volume dihasilkan dengan persamaan berikut.
𝐹𝑟𝑎𝑘𝑠𝑖 𝑉𝑜𝑙𝑢𝑚𝑒 𝐸𝑡𝑎𝑛𝑜𝑙 = ( % )
( % ) ( ) ( ( % )) …………(4.2)
Berdasarkan hasil yang didapat pada grafik pengaruh fraksi mol terhadap indeks bias, grafik mengalami kenaikan. Data pada grafik menjelaskan bahwa nilai indeks bias meningkat dengan meningkatnya rasio
25
volume etanol yang digunakan. Hal tersebut sesuai dengan literratur yang menegmukakan bahwa hubungan indeks bias dengan konsentrasi larutan berbanding lurus, yaitu semakin besar indeks bias maka konsentrasi larutan yang diperoleh akan semakin besar (Parmitasari, 2013). Volume etanol yang lebih besar dibandingkan air pada sampel menyebabkan konsentrasi air- etanol dalam sampel lebih besar, sehingga kerapatan antar partikelnya semakin tinggi. Maka hal tersebut yang menyebabkan peningkatan kemampuan cahaya untuk menembus larutan.
4.2 Pengaruh Konsentrasi Umpan dan Refluks terhadap Distilasi
Berikut ini grafik hasil yang diperoleh mengani pengaruh konsnetrasi umpan dan refluks pada proses distilasi.
(a)
(b)
Gambar 4.3 Grafik Pengaruh Konsentrasi dan Refluks Terhadap Distilasi
Kondisi operasi berlangsung pada 3 variasi konsentrasi dan 2 variasi refluks, yaitu konsentrasi umpan etanol sebesar 50%, 65%, dan 80% serta refluks total dan parsial. Proses distilasi dilakukan dengan memperhatikan beberapa faktor dintaranya adalah konsentrasi larutan umpan dan proses refluks. Konsentrasi larutan umpan dapat mempengaruhi fraksi mol distilat yang dihasilkan, semakin besar kadar etanol dalam umpan dapat menurunkan titik didih campuran sehingga mendekati titik didih etanol.
Semakin rendah suhu keluar pre-heater akan menaikkan kadar distilat karena penurunan suhu akan mengubah nilai “q line” pada garis umpan sehingga ketika ditarik pada garis dew point akan menaikkan fraksi mol etanol (Suharto dkk, 2020). Pada percobaan yang telah dilakukan, hasil yang diperoleh pada konsentrasi umpan 80% memiliki fraksi mol terbesar diantara 2 konsentrasi yang lain baik pada refluks total ataupun parsial yakni sebesar 0.5 yang dapat dilihat pada Gambar 4.3 (a). Sementara fraksi mol etanol naik, fraksi mol air akan turun yakni keduanya saling berbanding terbalik. Dapat dikatakan bahwa percobaan yang dilakukan telah sesuai dengan teori tersebut bahwa semakin besar konsentrasi etanol dalam umpan maka makin banyak etanol yang diuapkan sehingga fraksi mol yang dihasilkan akan semakin besar.
Proses refluks yang digunakan dalam operasi distilasi dapat mempengaruhi terhadap produk etanol pada distilat yang dihasilkan.
Refluks total sendiri memiliki definisi yaitu seluruh produk distilat dikembalikan pada kolom distilasi, sedangkan pada refluks parsial jumlah distilat yang dihasilkan ada yang dikembalikan ke dalam kolom distilasi ada yang ditampung sebagai produk, yang keduanya memiliki persentase sama besar 50%. Dengan melihat definisi tersebut, dapat diketahui bahwa pada proses distilasi secara refluks parsial akan memiliki fraksi mol yang lebih besar dibandingkan secara refluks total, namun memiliki kadar kemurnian yang lebih rendah daripada refluks total. Pada refluks total, kondensat yang dikembalikan dalam kolom akan mengalami pemanasan berulang pada
27
kondisi operasi dan waktu tinggal yang sama. Kondensat mengalami kontak ulang, sehingga menghasilkan konsentrasi distilat yang lebih murni, namun akan memakan waktu yang lebih lama (Erlinawati dkk, 2023). Pada percobaan yang telah dilakukan, hasil yang diperoleh pada distilasi refluks parsial memiliki fraksi mol yang didapat lebih besar dibandingkan pada refluks total, dapat dilihat pada Gambar 4.3 menggunakan refluks parsial konsentrasi 80% memiliki nilai fraksi mol yang lebih besar yakni 0.5325 dengan refluks total sebesar 0.5102. Dapat dikatakan bahwa percobaan yang dilakukan telah membuktikan teori bahwa volume distilat yang dihasilkan pada refluks parsial akan lebih besar dibandingkan pada refluks total karena jumlah produk kondensat yang dikembalikan ke kolom hanya separuh sedangkan pada refluks total seluruh produknya dikembalikan untuk dikontakkan kembali.
4.3 Pengaruh Refluks dan Konsentrasi Umpan Terhadap Efisiensi dan Yield
4.3.1 Pengaruh Refluks dan Konsentrasi Umpan Terhadap Nilai Efisiensi
Berikut ini grafik hasil yang diperoleh mengenai pengaruh refluks konsnetrasi umpan terhadap nilai efisiensi.
Gambar 4.4 Grafik Konsentrasi vs Efisiensi
Efisiensi merupakan hasil kali antara jumlah pelat teoritis (Hteoritis) dengan jumlah pelat aktual (Haktual). Hteoritis diperoleh dari hasil kali antara jumlah tahap minimum (Nmin) dengan tinggi isian packing kolom distilasi (HETP). Dari penurunan rumus tersebut dapat dinilai bahwa ketika konsentrasi makin besar, jumlah tahap minimum akan semakin banyak dan tentunya hal ini akan menjadi tidak efisien karena akan memerlukan fixed cost dan operational cost yang lebih tinggi.
Berbanding terbalik dengan proses refluks, jenis parsial akan lebih efisien karena pada refluks total jarak antara garis operasi dengan kurva kesetimbangan xy paling jauh sehingga menyebabkan jumlah pelat teoritis menjadi minimum. Keadaan ini akan meningkatkan kebutuhan energi pada reboler (labu didih) dan pada kondensor. Operasi secara refluks total juga membutuhkan waktu yang relatif lebih lama untuk menghasilkan produk distilat sehingga menjadi tidak efektif. Pada percobaan yang telah dilakukan, pada konsentrasi yang lebih rendah (50%) lebih efisien dengan persentase sebesar 81%, sedangkan pada proses refluks total lebih besar efisiensi yang diperoleh dari ketiga variasi konsentrasi yang dapat dilihat pada Gambar 4.4. Dapat dikatakan bahwa pada pengaruh konsentrasi telah sesuai dengan pernyataan di atas sedangkan proses refluks belum sesuai. Kondisi ini dapat terjadi karena pada refluks parsial, bila ditinjau dari ketiga variasi konsentrasi memerlukan jumlah tahap minimum yang lebih banyak dibandingkan dengan refluks total yang tentunya hal ini menjadi tidak efisien.
4.3.2 Pengaruh Refluks dan Konsentrasi Umpan Terhadap Nilai Yield
Berikut ini grafik hasil yang diperoleh mengenai pengaruh refluks konsnetrasi umpan terhadap nilai yield.
29
Gambar 4.5 Grafik Konsentrasi vs Yield
Yield merupakan rasio antara besar output produk yang dihasilkan (distilat) dengan besar input umpan. Semakin besar nilai yield menunjukkan bahwa produk etanol murni yang dihasilkan semakin banyak. Untuk memperoleh harga yield yang besar diperlukan jumlah output yang sangat besar dan jumlah input yang minimal. Pada proses distilasi secara refluks total akan menghasilkan jumlah produk distilat yang lebih sedikit dibandingkan refluks parsial, karena seluruh produknya dikembalikan ke dalam kolom distilasi. Konsentrasi dapat mempengaruhi terhadap %yield yang dihasilkan bila semakin tinggi konsentrasinya maka yield yang diperoleh akan semakin besar karena larutan etanol yang diuapkan akan semakin banyak. Pada percobaan yang telah diperoleh, yield terbesar terjadi pada konsentrasi 50%, dan pada proses refluks parsial memiliki yield paling besar yang dapat dilihat pada Gambar 4.5. Pada pengaruh konsentrasi, belum sesuai dengan teori yang telah disebutkan bahwa semakin besar konsentrasi maka angka yield yang dihasilkan akan semakin besar. Kondisi ini dapat terjadi karena pada konsentrasi 80%, uap etanol terjadi flooding yang menyebabkan larutan umpan terjebak pada uap di atas kolom karena adanya aliran uap berlebih dari etanol sehingga produk distilat yang dihasilkan tidak maksimal.
4.4 Hubungan Yield dan Efisiensi yang Diperoleh
Pada percobaan distilasi, diperoleh yield sebagai hasil akhir.
Berdasarkan Gambar 4.4, diperoleh bahwa yield terbesar ada pada konsentrasi etanol 50% untuk variasi refluks parsial total sebesar 36%, sedangkan nilai yield terkecil ada pada konsentrasi etanol 80% untuk variasi refluks parsial sebesar 1%. Perolahan hasil ini menunjukkan bahwa refluks memengaruhi yield yang dihasilkan.
Selain memengaruhi yield, refluks juga memengaruhi efisiensi yang diperoleh pada distilasi. Hal ini dijelaskan oleh Muhrinsyah, F (2014) bahwa peningkatan efisiensi pemisahan dapat dilakukan dengan cara mengalirkan kembali sebagian produk hasil puncak dan/atau hasil dasar masuk kembali ke dalam kolom. Cara ini dikenal sebagai operasi distilasi dengan sistem refluks Untuk efisiensi pada percobaan, nilai efisiensi terbesar ada pada konsentrasi 50% untuk variasi refluks total sebesar 81%, sedangkan nilai efisiensi terkecil ada pada konsentrasi 80% untuk variasi refluks parsial sebesar 76%
Ketika konsentrasi etanol pada umpan 50% dengan refluks total yang merupakan rasio refluks terbesar, efisiensi yang diperoleh 81% dengan yield sebesar 20%. Hal ini berbeda dengan yang sudah dijelaskan bahwa yield terbesar diperoleh pada konsentrasi etanol pada umpan 50% dengan refluks parsial sebesar 36% meskipun nilai efisiensinya 80%. Fenomena ini sesuai dengan teori yang dijelaskan Gilbert, J., C., & Martin, S., F. (2010) bahwa rasio refluks yang terlalu kecil dapat menyebabkan terjadinya pemisahan komponen yang tidak tepat sehingga akan menghasilkan fraksi yang belum murni karena memiliki kandungan komponen lain yang tidak diinginkan. Sedangkan rasio refluks yang terlalu besar akan menghasilkan pemisahan komponen yang berlangsung lambat dan tidak efisien walaupun mampu menghasilkan kemurnian komponen yang tinggi.
31
BAB V
KESIMPULAN DAN SARAN 5.1 Kesimpulan
Berdasarkan percobaan yang telah dilakukan, maka dapat diambil beberapa kesimpulan sebagai berikut.
a. Efisiensi kolom distilasi package terbaik berada pada konsentrasi umpan 50% dengan proses refluks total yaitu sebesar 81%.
b. emakin besar konsentrasi, maka fraksi mol etanol pada distilat akan semakin besar. Refluks parsial menghasilkan fraksi mol distilat yang lebih tinggi, namun kemurnian lebih rendah dibandingkan refluks total.
5.2 Saran
Berikut saran yang dapat diberikan untuk percobaan distilasi.
a. Memakai distilasi batch pada variasi refluks parsial dan total sebagai perbandingan
b. Menggunakan variasi temperatur bottom untuk melihat pengaruhnya terhadap distilat yang dihasilkan
c. Menggunakan air es pada konsendor untuk melihat pengaruhnya terhadap distilat yang dihasilkan
DAFTAR PUSTAKA
Andika, D dan Naomi, H. (2017). Pengukuran Kesetimbangan Uap-Cair Sistem Biner Isothermal 2-Butanol+Dietil Karbonat dan Tert-Butanol+Dietil Karbonat pada Temperatur 303.15-323.15 K. Departemen Teknik Kimia.
Fakultas Teknologi Industri. Institur Teknologi Sepuluh Nopember.
Anonim. (2008).
Ariono, D. (2019). Perkembangan Teknologi Pemisahan Difusional. Institut Teknologi Bandung. Bandung.
Budiman, A. (2019). In A. Budiman, DISTILASI : Teori dan Pengendalian Operasi.
Yogyakarta: Gajah Mada Univercity Press.
Fattimura, M. (2014). Tinjauan Teoritis Faktor-Faktor Yang Mempengaruhi Operasi Pada Kolom Destilasi. Jurnal Media Teknik. Vol. 11. No. 1. Hal.
23-31.
Geankoplis. (1983). Transport Process and Unit Operations Third Edition.
Prentice-Hall International, Inc.
Hidayanto, E, dkk. (2010). Aplikasi Portable Brix Meter untuk Pengukuran Indeks Bias. Berkala Fisika. Volume 13. Hal. 113-118.
Miftakhur, R, F. (2018). Kajian Mutu Minyak Atsiri Kulit Jeruk Siam (Citrus nobilis Lour var. macrocarpa Hassk) Berdasarkan Perbedaan Jumlah Bahan dengan Metode Distilasi. Jurusan Teknik Pertanian. Fakultas Teknologi Pertanian. Universitas Jember.
Perdana, Y., dkk. (2010). Studi Perancangan Kontrol Prediktif pada Kolom Distilasi Di Crude Distillation Unit PT Pertamina UP VI Balongan. Vol.
2 . No. 2. Divisi Riset Instrumentasi dan Kontrol Fakultas Teknologi Industri, Institut Teknologi Bandung.
Erlinawati, Rahman, M., Zikri, A., & Aditya, M. (2023). Pengaruh Jumlah Tray dan Refluks Kolom Distilasi Pada Proses Purifikasi Metanol. CHEMTAG, 19- 27.
Rusli, M. (2010). Sukses Memproduksi Minyak Atsiri. Jakarta: PT Agromedia Pustaka.
33
Sinnot, R.K. (2005). Coulson and Richardson’s: Chemical Engineering Design, Vol 64th ed. Elsevier Ltd. Oxford.
Suharto, M., Wibowo, A., & Suharti, P. (2020). Optimasi Pemurnian Etanol Dengan Distilasi Ekstraktif Menggunakan ChemCad. Distilat, 1-7.
Smith dan Jobson. (2000). Distillation. Department of Process Integration.
Manchester, UK.
Parmitasari, P. (2013). Analisis Kolerasi Indeks Bias dengan Konsentrasi Sukrosa Beberapa Jenis Madu Menggunaan Portable Brix Meter. Youngster Physics Journal, 191-198.