ISOLASI DAN KARAKTERISASI cDNA HORMON PERTUMBUHAN IKAN KERAPU BEBEK (Cromileptes altivelis)
MOCHAMAD SYAlFUDlN
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
ABSTRAK
MOCHAMAD SYAIFUDIN. Isolasi- dan Karakterisasi cDNA Hormon Pertumbuhan Ikan Kerapu Bebek (Cromileptes altivelis). Dibimbing oleh KOMAR SUMANTADINATA, AGUS OMAN SUDRAJAT dan UTUT WIDYASTUTI.
Hormon pertumbuhan (GH) merupakan protein 22 kDa dari pituitari yang terkonse~asi akibat evolusi vertebrata. Hormon pertumbuhan ikan berperan dalam pertumbuhan, adaptasi air laut, reproduksi
dan
fungsi imun. Kerapu bebek(C.
altivelis) adalah salah satu ikan air laut yang mempunyai nilai ekonomispenting. Pertumbuhan ikan ini tergolong lambat, sehingga perlu diketahui mekanisme kontrol dari ekspresi GH. Salah satu tahap awal yaitu dengan mengisolasi dan mengkarakterisasi cDNA GH. cDNA diisolasi dari kelenjar pituitari menggllnakan rnetode RT PCR (Reverse Transcriptase Polymerase
Chain reaction). Hasil penelitian ini menunjukkan bahwa fragmen cDNA GH
kerapu bebek mempunyai 618 bp yang mengkodekan 205 asam amino. Komposisi asam amino terbesar yang menyusun GH kerapu bebek adalah Leusina (14.63%), sedangkan komposisi terkecil adalah triptophan (0.49%). Fragmen cDNA GH kerapu bebek ini mengandung domain protein yang terkonse~atif yaitu : Somatotropin-1, Somatotropin-2, Kasein kinase 11, Protein kinase C, N-
miristoilasi dan N-glikosilasi. Homologi protein deduksi cDNA GH kerapu bebek dengan kelompok ikan grouper yaitu 0.882
-
0.895, sedangkan dengan kelompok ikaii-ikan lainnya adalah 0.660-
0.895. Kesamaan paling dekat protein deduksi cDNA GH kerapu bebek adalah dengan Epinephelus coioides (nomor akses padaGenbank : Q90VV6)
Kala kunci : isolasi, karakrerisasi, cDNA GH, kerapu bebek (Cromileptes
I. PENDAHULUAN
1.1. Latar Belakang
Teknologi rekombinan DNA mulai dikembangkan dalam bidang buddidaya perairan, khususnya program pembenihan guna meningkatkan kualitas dan kuantitas strain ikan. Salah satu penelitian DNA rekombinan yang potensial untuk dikembangkan adalah penggunaan hormon pertumbuhan (Growth HormonelGH).
Hormon pertumbuhan adalah polipeptida esensial yang disekresikan oleh somatotroph kelenjar piiuitari. f:ormon ini berperan dalam pengaturan pertumbuhan somatik dan pemeliharaan metabolisme protein, lemak, karbohidrat maupun mineral. GH mempakan protein pituitari dengan berat molekul 22 kDa dan konsewatif akibat evolusi vertebrata (Calduch-giner et al. 2000). Sekresi hormon ini diatur oleh GHRH (Growth Hormone Releasing Hormone) dari hipothalamus dan oleh somatostatin (hormon penghambat) (Price & Wilson 1995).
Isolasi
dan
karakterisasi cDNA (complementary deoxyribonucleic acid) GH sangat berguna dalam bidang perikanan, temtama dalam program pembenihandan
penyusunan formulasi pakan. Penelitian tentang cDNA yang menyandi hormon ini telah banyak dilakukan seperti pada beberapa mamalia
dan
piscine (Lemaire et al. 1994, Ayson et al. 2000). Analisis DNA rekombinan dari GHs (KiHs) menunjukkan bahwa GH mampu meningkatkan pertumbuhan ikan (Tsai et al. 1994), memacu selera makan, dan efisiensi pakan (Donaldson 1986). Ban (2002) menambahkan bahwa kombinasi GH dan kortisol mempunyai peranan penting dalam meningkatkan toleransi terhadap air laut dari salmon dengan menstimulasi aktivitas ~ a ' , K+-~Tpase pada insang.ABSTRAK
MOCHAMAD SYAIFUDIN. Isolasi- dan Karakterisasi cDNA Hormon Pertumbuhan Ikan Kerapu Bebek (Cromileptes altivelis). Dibimbing oleh KOMAR SUMANTADINATA, AGUS OMAN SUDRAJAT dan UTUT WIDYASTUTI.
Hormon pertumbuhan (GH) merupakan protein 22 kDa dari pituitari yang terkonse~asi akibat evolusi vertebrata. Hormon pertumbuhan ikan berperan dalam pertumbuhan, adaptasi air laut, reproduksi
dan
fungsi imun. Kerapu bebek(C.
altivelis) adalah salah satu ikan air laut yang mempunyai nilai ekonomispenting. Pertumbuhan ikan ini tergolong lambat, sehingga perlu diketahui mekanisme kontrol dari ekspresi GH. Salah satu tahap awal yaitu dengan mengisolasi dan mengkarakterisasi cDNA GH. cDNA diisolasi dari kelenjar pituitari menggllnakan rnetode RT PCR (Reverse Transcriptase Polymerase
Chain reaction). Hasil penelitian ini menunjukkan bahwa fragmen cDNA GH
kerapu bebek mempunyai 618 bp yang mengkodekan 205 asam amino. Komposisi asam amino terbesar yang menyusun GH kerapu bebek adalah Leusina (14.63%), sedangkan komposisi terkecil adalah triptophan (0.49%). Fragmen cDNA GH kerapu bebek ini mengandung domain protein yang terkonse~atif yaitu : Somatotropin-1, Somatotropin-2, Kasein kinase 11, Protein kinase C, N-
miristoilasi dan N-glikosilasi. Homologi protein deduksi cDNA GH kerapu bebek dengan kelompok ikan grouper yaitu 0.882
-
0.895, sedangkan dengan kelompok ikaii-ikan lainnya adalah 0.660-
0.895. Kesamaan paling dekat protein deduksi cDNA GH kerapu bebek adalah dengan Epinephelus coioides (nomor akses padaGenbank : Q90VV6)
Kala kunci : isolasi, karakrerisasi, cDNA GH, kerapu bebek (Cromileptes
ISOlASI DAN KARAKTERISASI eDNA HORMON PERTUMBUHAN IKAN KERAPU BEBEK (Cromileptes a/tive/is)
MOCHAMAD SYAIFUDIN
SEKOlAH PASCASARJANA INSTITUT PERTANIAN BOG OR
I. PENDAHVLVAN
1.1. Latar Belakang
Teknologi rekombinan DNA mulai dikembangkan dalam bidang buddidaya
perairan, khususnya program pembenihan guna meningkatkan kualitas dan
kuantitas strain ikan. Salah satu penelitian DNA rekombinan yang potensial untuk
dikembangkan adalah penggunaan hormon pertumbuhan (Growth Hormone!GH).
Hormon pertumbuhan adalah polipeptida esensial yang disekresikan oleh
somatotroph kelenjar pituitari. Hormon ini berperan dalam pengaturan
pertumbuhan somatik dan pemeliharaan metabolisme protein, lemak, karbohidrat
maupun mineral. GH merupakan protein pituitari dengan berat molekul 22 kDa
dan konservatif akibat evolusi vertebrata Hc。ャ、オ」ィセァゥョ・イ@ et at. 2000). Sekresi
hormon ini diatur oleh GHRH (Growth Hormone Releasing Hormone) dari
hipothalamus dan oleh somatostatin (hormon penghambat) (Price & Wilson 1995).
Isolasi dan karakterisasi cDNA (complementary deoxyribonucleic acid) GH
sangat berguna dalam bidang perikanan, terutama dalam program pembenihan dan
penyusunan formulasi pakan. Penelitian tentang cDNA yang menyandi hormon
ini telah banyak dilakukan seperti pada beberapa mamalia dan piscine (Lemaire et at. 1994, Ayson et al. 2000). Analisis DNA rekombinan dari GHs (rGHs)
menunjukkan bahwa GH mampu meningkatkan pertumbuhan ikan (Tsai et al.
1994), memacu selera makan, dan efisiensi pakan (Donaldson 1986). Ban (2002)
menambahkan bahwa kombinasi GH dan kortisol mempunyai peranan penting
dalam meningkatkan toleransi terhadap air laut dari salmon dengan menstimulasi
aktivitas Na +, K+ -ATPase pada insang.
Isolasi cDNA GH dan karakterisasinya merupakan langkah awal pada proses
transfer gen guna mendapatkan spesies ikan yang mempunyai karakter
pertumbuhan cepat. Isolasi eDNA GH pada ikan telah di lakukan di Eropa, seperti
rainbow trout (Oncorhynchus mykiss) (Yao et al. 1991), red sea bream, ikan
salmon (Voigt & Botta 1990), Ictalurus punctatus (Tang et al. 1993),
Pangasionodon gigas (Lemaire et al. 1994) dan Pangasius pangasius (Lemaire &
2
Ikan kerapu bebek (Cromileptes altivelis) merupakan ikan karang yang
penyebarannya meliputi wilayah Pasifik Barat, mulai Jepang bagian selatan
sampai Palau, Guam, Kaledonia Bam, Kepulauan Australia bagian selatan serta
Laut India bagian timur dari Nieobar sampai Broome, sedangkan di Indonesia
ikan kerapu bebek ini banyak ditemukan di wilayah perairan Teluk Banten, Ujung
Kulon, Kepualuan Riau, Kepulauan Seribu, Kepulauan Karimunjawa, Madura,
Kalimantan dan Nusa Tenggara (Heemstra & Randall 1986). Spesies ini banyak digemari sebagai ikan hias pada saat ukurannya keeil, dan ikan konsumsi saat
ukuran individu sekitar I kg. Usaha budidaya kerapu bebek telah banyak
dilakukan, namun ada kendala dalam mendapatkan produksi yang optimum. Hal
ini disebabkan oleh faktor internal, yaitu karakter genetik dan faktor ekstemal,
baik pakan maupun lingkungan.
1.2. Perumusan Masalah
Ikan kerapu bebek adalah ikan kamivora laut yang banyak dibudidayakan,
namun ikan ini mempunyai karakter perturnbuhan yang lambat. Lambatnya
pertumbuhan ini disebabkan oleh faktor genetik ataupun faktor pakan dan
lingkungan. Seeara genetik, karakter perturnbuhan bisa diperbaiki kualitasnya
melalui teknik rekombinan DNA atau yang dikenal dengan teknik transfer gen.
Ikan kerapu yang perturnbuhannya eepat dapat dihasilkan dengan
menambahkan kopi eDNA GH dengan teknologi transgenesis. Dalam hal ini,
isolasi dan karakterisasi eDNA GH dari ikan target adalah langkah pertama untuk
konstruksi ikan transgenik.
1.3. Tujuan
Tujuan penelitian ini adalah untuk mendapatkan eDNA GH dan
II. TINJAUAN PUSTAKA
2.1. Ikan Kerapu
2.1.1. Biologi Kerapu Bebek
Ikan kerapu bebek (Cromileptes altivelis) termasuk dalam famili Serranidae
yang mempunyai bentuk tubuh memanjang gepeng (compressed) dan panjang
bisa mencapai 1 meter dengan tubuh tertutup oleh sisik -sisik kecil (Gambar 1).
!h.tJ. kerapu di dunia intemasional dikenal sebagai groupers, rocleod, hinds dan
sea basses yang tergolong dalam sub famili Epinephelinae dengan 15 genus dan
159 spesies. Adapun klasifikasi kempl! bebek menurut Heemstm and Randa!!
(1993) yaitu :
Sub filum : Vertebrata
Kelas : Teleostei
Sub kelas : Osteicanthopterygii (Actinopterygii)
Ordo : Perciforma
Sub ordo : Perciodea
Famili : Serranidae
Genus : Cromileptes
Spesies : Cromileptes altivelis
Gambar L Morfologi ikan kerapu bebek (Cromileptes altivelis)
Ikan kerapu bebek ini mempunYai banyak nama lokal. Ikan ini di Australia
dikenal dengan nama Baramundi cod, Sarasa-hata (Jepang), Lapu-Lapung
4
Malaysia, ikan ini dikenal dengan nama kerapu bebek, kerapu tikus, kerapu belida
dan kerapu sonoh (Heemstra and Randall 1993).
Heemstra & Randall (1993) menyatakan bahwa seluruh permukaan tubuh kerapu bebek berwama putih keabuan, berbintik bulat hitam serta moncong
kepala lancip menyerupai tikus atau bebek. Kelompok groupers, termasuk kerapu
bebek ュ・ューセュケ。ゥ@ masa hidup yuang panjang hingga 50 tahun dengan perturnbuhan dan pematangan yang lambat (Huntsman et al. 1999). Kerapu bebek
mempunyai strategi seksual protogini di mana ikB.r1 ini pertB.mB. hE mata!'.g sebagai betina kemudian berubah kelamin menjadi jantan (Sadovy 1996). Kerapu
bebek ternB.suk ke rh1am predator yang d0minan pada habitat karang denga!'.
makanan utamanya adalah ikan, krustasea dan cephalopoda (Heemstra and
Randall 1999)
2.1.2. Habitat
Ikan kerapu bebek terse bar luas di Pasifik Bara!, mulai Jepang bagian
selatan sampai Palau, Guam, Kaledonia Barn, kepulauan Australia bagian selatan
serta Laut India bagian timur dari Nicobar sampai Broome. Di Indonesia, ikan
kerapu bebek banyak ditemukan di wilayah perairan Teluk Banten, Ujung Kulon,
Kepl.1R.lUall Rial.l, Kepulauan Seribl.l, Kepulauan Karimunjawa, Madura,
Kalimantan dan Nusa Tenggara (Heemstra & Randall 1993).
Menurut Kuiter (1992), ikan kerapu bebek tergolong ibn kamivora, hidup
soliter dan banyak terdapat di daerah terumbu karang serta muara sungai. Utoyo
et al. (1999) menyatakan bahwa ikan ini hidup secara soliter pada daerah terurnbu
karang yang berasosiasi dengan jenis Porites sp., Acropora sp., Foliosa, Sponge,
Pinctada dan Tridacna. Kerapu bebek banyak dijumpai pada perairan berbatu
karang, atau karang berlurnpur dengan kedalaman 40 sampai 60 meter. Ikan ini
menghin<lari pengaruh matahari langsung dengan membuat naungan sebagai
tempat bersembunyi. Dalam siklus hidupnya, ikan kerapu bebek muda hidup di
perairan karang dengan kedalaman 0,5-3 meter, kemudian saar dewasa menuju ke
perairan lebih dalam, dimana perpindahan ini biasanya terjadi pada siang dan
senja hari. Tell.lf dan larva kerapu bebek bersifat pelagis, sedangkan kerapu muda
5
termasuk dalam kelompok stcnohaline sehingga mampu beradaptasi pada
lingkungan perairan yang berkadar garam rendah (Breet & Groves 1979).
2.2. Hormon Pertumbuhan
2.2.1. Hormon dan Sistem Regulasi
Horman adalah bahan kimia pembawa sinyal yang dibentuk dalam sel-sel
khusus pada kelenjar endokrin. Hormon disekresikan ke dalam darah kemudian
disalurkan ke organ-organ yang menjalankan fungsi-fungsi regulasi tertentu
secara fisiologik dan biokimia. Sel kelenjar yang khusus mensintesis harmon dari
prekursomya dapat menyimpan dan mensekresikannya ke dalam aliran darah
sesuai kebutuhan. Horman dan metaboliknya dikeluarkan melalui sistem ekskresi,
kebanyakan melalui ginjal. Sel-sel sasaran pada organ sasaran memiliki reseptor
yang dapat mengikat hormon, sehingga informasi yang diperoleh dapat diteruskan
ke sel-sel dan akhimya menghasilkan suatu respon (Kooiman & Rohm 2001). Pesan hormon disampaikan pada sel-sel sasaran menurut dua prinsip yang
berbeda. Hormon lipofilik masuk ke dalam sel dan bekeIja pada inti sel,
sedangkan hormon hidrofilik bekeIja pada membran sel. Horman steroid dan
tiroksin termasuk dalam kelompok hormon lipofilik. Horman ini menembus
membran sel dan berikatan pada suatu reseptor spesifik di dalam sel sasaran.
Kelompok hormon hidrofilik merupakan harmon yang tersusun dari asam amino,
semua peptida dan proteohormon. Hormon-hormon hidrofilik berikatan pada
bagian luar sel sasaran pada reseptor spesifik yang difiksasi di dalam membran sel
(Kooiman & Rohm 2001).
Hormon pertumbuhan merupakan salah satu kelompok harmon hidrofilik
karena harmon ini merupakan suatu polipeptida. Horman peptide tersusun atas
asam-asam amino. Horman ini mengikat permukaan sel reseptor, sehingga tidak
masuk ke dalam sel (Gambar 2). Komplek yang dihasilkan akan mengaktifkan enzim yang mengkatalis sintesis AMP siklik dari ATP. AMP siklik mengaktifkan
enzim lain yang tidak aktif. AMP siklik merupakan pembawa pesan kedua
(second messenger), sedangkan hormon adalah pembawa pesan pertama
Luar sel
honnon peptida
dalam sel
pA TP セ@ enzim non aktif
_ reseptor
MGイMMNセ@
cAMP _ enzim aktif _ reaksi kimiaGambar 2. Mekanisme keIja hormon peptida
U:,
.!"elL2.2.2. Sekresi Hormon Pertumbuhan (GH)
6
Hormon pertumbuhan (GH) atau disebut juga somatotropin merupakan
hormon polipeptida yang diJepaskan dari adenohipofisa yang menginduksi hati
agar mensintesis somatomedin yang berperan langsung dalam pertumbuhan, baik
pertumbuhan tulang, otot maupun sel-sel yang lain. Hormon ini menunda
katabolisme asam-asam amino dan memacu inkorporasinya ke dalam
protein-protein tubuh. Kerja somatototropin dipermudah oleh hormon pankreas, korteks
adrenal dan tiroid yang bekelja bersama-sama dalam memacu metabolisme lemak dan karbohidrat (Calduch-Giner et a1. 2000; Walsh 2002). Walsh (2002)
menyatakan bahwa hormon ini memacu retensi tubuh berbagai mineral dan
elemen esensial lain untuk pertumbuhan normal. Selain itu GH mempunyai
peranan penting dalam adaptasi terhadap air laut, reproduksi dan fungsi imun
(Calduch-Giner et a1. 2000). Hormon somatotropin mempunyai peranan yang
penting pada proses transfer asam amino ekstraseluller melintasi membran sel,
khususnya ke dalam sel-sel otot dan menahan asam amino tersebut tetap di dalam
sel. Menurut Matty (1985), GH mampu meningkatkan nafsu makan, konversi
pakan, sintesis protein, menurunkan kehilangan nitrogen, merangsang
metabolisme lemak, oksidasi dan memacu sintesis dan pelepasan insulin.
GH merupakan protein pituitari dengan berat molekul 22 kDa dan
konservatif akibat aksi pleitropik selarna evolusi vertebrata (Calduch-Giner et a1.
7
polipeptida yang disekresikan oleh somatotroph pada bagian anterior kelenjar
pituitari. Price & Wilson (1995) dan Walsh (2002) mengemukakan bahwa sekresi GH dari pituitari diatur oleh regulator hipotalarnik yaitu GHRF (Growth
Hormone Releasing Factor). Pelepasan GH dapat dirangsang oleh kondisi
hiplogikemia dan asarn amino seperti arginina (Price & Wilson 1995). Pelepasan horrnon ini diharnbat oleh faktor hipotalamik kedua yaitu horrnon penghambat
pelepasall GH atau yang dikenal dengan somatostatin.
5-HT
a。セ@
'---J:'
セ@
' \
セ@
>;
a
セ@
Somatotrophセ@
SRIF
セ@
-I -U
1
Penghambat Stimulasi
CCK : kolesistokinin; DA : dopamin; GRF : GH-releasing factor; GnRH : Gonadotropin-releasing homlOne; NPY : neuropeptide Y: NE : norepinephrine; 5-HT : serotonin; SRIF : somatostatin; TRH : thyrotropin releasing hormone).
Garnbar 3. Model pengaturan neuroendokrin multifaktor sekresi horrnon pertumbuhan (GH) pada ikan mas dan koki. (Peter & Marchant 1995).
Peter & Marchant (1995) mengemukakan bahwa sekresi GH terjadi oleh pengaruh multifaktor, baik yang bersifat memacu ataupun mengharnbat. Hal ini
digarnbarkan secara ringkas pada Gambar 3. Pemacu utama sekresi hormon
pertumbuhan yaitu GHRF, cGnRH-Il dan dopamin. Hasil pengujian secara in
vitro menunjukkan potensi stimulasi GH oleh kolesistokinin (CCK), neuropeptide
Y (NPY) dan horrnon pelepas tirotropin (Tyrolropin Releasing Hormone ITRH).
Sedangkan somatostatin, norepineprin dan serotonin menghambat sekresi GH
secara langsung. Norepineprin dan serotonin dapat mendorong sekresi GH secara
tidak langsung melalui aksi stimulasi pada GnRH yang kemudian menstimulasi
8
Faktor-faktor ekstrinsik seperti photoperiod dan temperatur dapat
mempengaruhi kandungan GH pada pituitari yellow perch (Robert et al. 2004).
Pada Eurasians perch (Perca fluviatilis) kandungan GH pituitari mencapai level
maksimum di bulan Mei/Juni saat photoperiod terpanjang (Swift & Pickford 1965). Jourdan et al. (2000) menambahkan bahwa photoperiod (18:6 atau 24:0
L:D) mampu meningkatkan pertumbuhanjuvenil Eurasian perch.
2.2.3. Aksi Hormon Pertumbuhan
Walsh (2002) menyatakan bahwa GH mengenali efek anaboliknya dengan
pengikatan ke reseptor permukaan sel spesifik. Reseptor tersebut terdiri dari 3
bagian, yaitu : pengikatan ligand ekstraseluler, transmembran dan efektor
intraseluler. Bentuk potongan bagian ujung reseptor GH, tepatnya bagian
pengikatan ligand ekstraseluler ditemukan pada serum. Serum protein ini mampu
mengikat GH dan berperan penting dalam tubuh. Reseptor GH telah terdeteksi
pada banyak jaringan. Setelah tahap larva, lokasi pengikatan GH spesifik telah
terdeteksi pada beberapa jaringan ekstra hepatik rainbow trout (seperti : testis,
otot, otak, insang, jaringan adipose, limpa dan tulang rawan) (Perez-Sanchez et 01.
1991, Yao et 01. 1991). Pengukuran reseptor GH (GHRs) pada hepatik, tingkat sirkulasi GH dan IGFs merupakan parameter yang berguna untuk memonitor
status nutrisi dan performan pertumbuhan (Peter & Marchant 1995). Calduch-Giner et of. (2000) menambahkan bahwa hati merupakan target jaringan
terpenting untuk aksi langsung GH. Meskipun demikian, pada ikan maupun
vertebrata yang lebih tinggi, pengikatan GH banyak teljadi di jaringan seperti
testis, otot, insang, jaringan adipose, limpa, sistem saraf pusat dan sel
haemopoetik.
Aksi somatogenik GH dimediasi oleh IGF-I, meskipun demikian efek
langsung GH adalah terhadap pertumblli1.an jaringan. GH dan IGF-I bertindak
bersama-sama untuk memacu pertumbuhan setelah penetasan (post-natal) di mana
GH memulai diferensiasi stem cell, dan IGF-I sebagai media clonal expansion
(Issakson et 01. 1985). Selain itu fungsi GH dimediasi oleh protein kinase (Ralph
9
sintesis proteoglikan tulang rawan (cartilage), dimana GH bergantung pada IGF-I
dalam aksi ini.
[image:90.563.67.471.60.789.2]Produksi GH Pituitari (Sistemiklaksi endokrin)
...
...
Efek I angsung ···Bfek tdk langsung ..•...
'.
-'-...
....
-' . ....
" .
IGFs .... '. -. Liver
.' . ..
セ@
Produksi GH Ekstrapituitari
Aksi 10k al
nlparakrin) (autokri
Pertumbuhan Jaringan
Gambar 4. Aksi autokrinlparakrin dari honnon pertumbuhan (GH) (Perez-Sanchez & Le Bail 1999).
Honnon pertumbuhan mempunyai pengaruh terhadap pertumbuhan jaringan,
baik secara langsung maupun tidak (Gambar 4). Honnon ini berpengaruh utama
pada hati, yang selanjutnya menstimulasi sintesis somatomedin atau insulin-like
growth factor-l (IGF-I). Pada tahap awal perkembangan vertebrata, aksi
somatogenik GH mempunyai efek langsung yang lebih besar dari IGFs hepatik.
Efek sistem yang dimediasi oleh IGFs hepatik secara luas dipengaruhi oleh
manipulasi lingkungan dan makanan (Perez-Sanchez & Le Bail 1999). Laju perturnbuhan pada ikan budidaya mungkin distimulasi oleh faktor neuroendokrin
yang ditambahkan ke pakan, preparasi rekombinan GH, atau dengan
memproduksi transgenik GH ikan (Peter & Marchant 1995).
2.3. Teknologi DNA Rekombinan
Teknologi DNA rekombinan (kloning gen) merupakan penyisipan ke vektor
DNA (umumnya plasmid) untuk membentuk molekul DNA baru yang
diperbanyak pada sel inang (Glick & Pasternak 2003). Kloning gen dapat dilakukan melalui beberapa tahap, yaitu : (a) isolasi asam nukleat (gen), (b)
10
introduksi vektor rekombinan yang membawa slslpan ke dalam sel inang
(Suharsono,2000b).
2.3.1. Isolasi asam nokleat (gen)
Oen dapat diisolasi dengan berbagai eara yaitu (Suharsono, 2000b) :
a. Pemotongan dengan enzim restriksi
Oen yang sudah diketahui ukuran dan situs restriksinya dapat diisolasi seeara
langsung dari gel setelah dilakukan pemotongan DNA dan migrasi di dalam gel.
Untuk gen yang berada pada organisme dengan genom besar d:::pat dilakukan
dengan pembuatan pustaka genom. Genom suatu individu dipotong dengan enzim
restriksi, disisipkan ke vektor kemudian vektor rekombinan diintroduksikan ke sel
mango
b. Pembuatan eDNA
eDNA atau DNA komplementer adalah DNA yang dibuat berdasarkan mRNA
(messenger RNA). mRNA dapat di ubah menjadi eDNA dengan menggunakan
enzim reverse trancriptase.
C. Transposon.
Transposon merupakan molekul DNA yang bisa 「・イーゥョ、。Nセ@ temp at di sepanjang
kromosom. Apabila transposon menyisip pada suatu gen, maka gen tersebut tidak
dapat diekspresikan karena adanya mutasi. Oen yang bertanggung jawab terhadap
sifat yang mengalarni mutasi ini bisa diisolasi menggunakan pelaeak berupa
molekul transposon.
2.3.2. Kloning Vektor
Vektor merupakan pembawa molekul DNA sisipan dalarn pengkJonan gen
ke dalam sel inang. Beberapa jenis vektor yang dapat digunakan dalarn kloning
gen yaitu plasmid, fage, kromosom buatan dari kharnir (Y AC = yeast artificial
chromosome) dan kosmid (cosmid). Penggunaan vektor sangat tergantung dari
tujuan pengklonan. Pembuatan pustaka eDNA dapat menggunakan plasmid
scbagai vcktomya, scdangkan pustaka genom yang mengandung fragmen besar
11
2.3.3. Introduksi Vektor
Vektor rekombinan diintroduksikan ke dalam sel inang agar dapat
mengalami replikasi (penggandaan). Bertambalmya jumlah vektor rekombinan
menyebabkan DNA yang tersisip juga mengalami replikasi. Introduksi vektor
rekombinan dapat dibedakan menjadi 2 macam yaitu transformasi dan transfeksi.
Istilah transformasi digunakan apabila vektor yang digunakan adalah plasmid,
sedangkan transfeksi menggunakan vektor virus dan turunarmya.
Keberhasilan transformasi sangat dipengaruhi oleh sifat kompeten bakteri
dalam pengambilan molekul DNA asing (Glick & Pasternak 2003). Sifat kompeten dapat terjadi secara alami pada beberapa bakteri, seperti pada genus
Bacillus atau Streptococcus yang mempunyai mekanisme pengikatan dan
pengambilan molekul DNA secara efisien (Suharsono 2000a). Sifat kompeten
tidak dimiliki pada Eschericia coli, sehingga perlu dilakukan induksi dengan
beberapa bahan kimia dan kejutan suhu. Sel pada fase mid-log disuspensikan pada
kalsium klorida (CaCh), kemudian dipertahankan pada suhu -70°C hingga
diperJukan. Pada saat dilakukan transformasi, sel yang membeku dicairkan
(thawing) di atas es dan dilakukan kejutan suhu 42°C selama 1-2 menit. DNA
dapat masuk ke dalam bakteri melalui pori-pori dinding dan membran yang
terbuka. Bahan kimia lain yang digunakan adalah Mg atau detergen (triton-X)
(Suharsono 2000b). Metode lain dalam transformasi adalah menggunakan kejutan
listrik yang dikenal dengan elektroporasi (Sambrook et al. 1989). Kejutan listrik
pada tegangan tertentu dalam waktu singkat dapat membuka pori-pori membran
sel inang.
2.3.4. Seleksi
Sel inang (bakteri) yang membawa DNA sisipan dapat diketahui dengan
penanda seleksi, yaitu berupa sifat ketahanan terhadap antibiotika. Bakteri yang
membawa vektor rekombinan (mengandung DNA sisipan) akan resisten terhadap
antibiotik tf!rtentu dan yang bukan vektor rekombinan akan mati. Sel inang yang
membawa vektor rekombinan yang membawa DNA sisipan atau tidak, dapat
diseleksi dengan penambahan X-gal dan IPTG pada media tumbuh, sehingga
memberikan koloni berwarna biru dan putih (Suharsono 2000b). Gen lacZ pada
12
tidak berwarna menjadi molekul berwama biru. Gen laeZ diinduksi oleh IPTG
(isopropil thiogalaktosida). Apabila gen lacZ tersisipi oleh molekul DNA lain,
maka lacZ tidak dapat diekspresikan, sehingga sel yang mengandung sisipan tidak
mampu merubah X-gal menjadi berwama biru. Dengan penambahan IPTG pada
media yang mengandung antibiotik, maka dapat diseleksi : (1) sel yang
mengandung plasmid, (2) sel yang mengandung plasmid dan sisipan pada daerah
III. BAHAN DAN METODE
3.1. Waktu dan Tempat Penelitian
Penelitian ini dilakukan selama 10 bulan mulai Januari sampai Oktober 2005
bertempat di Laboratorium Biorin (Biotechnology Research Indonesian The
Netherlands), Biologi Seluler dan Molekuler Tanaman, Pusat Penelitian Sumber
Daya Hayati dan Bioteknologi Institut Pertanian Bogor (PPSHB-IPB) dan
Laboratorium Genetika Ikan, Program Studi Budidaya Perairan, Fakultas
Perikanan dan Ilmu kelautan (FPIK), IPB .
3.2. Bahan dan Alat
a. Bahan yang digunakan dalam penelitian ini adalah organ hipofisa dari 6 ekor
ikan kerapu bebek (c. altivelis).
b. Bahan-bahan kimia dan peraiatan untuk isolasi RNA total, sintesis eDNA dan
sekuensing (Lampiran 1).
3.3. Metode Penelitian
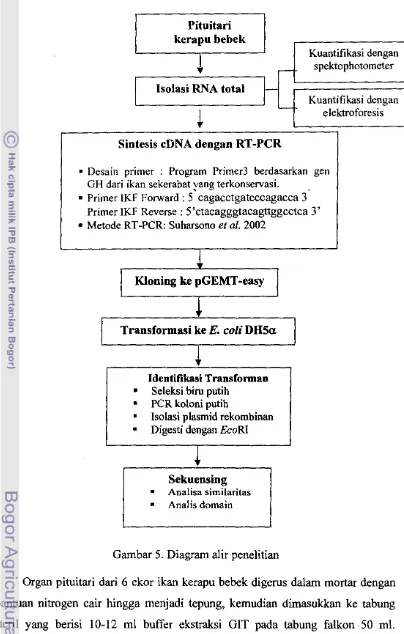
Penelitian mcngenai isolasi dan karakterisasi eDNA hormon pertumbuhan
ikan kerapu bebek dilakukan melalui beberapat tahap (Gambar 5) yaitu : isolasi
RNA total, sintesis eDNA, kloning ke pGEMT-easy, transformasi ke E. coli
DHsu, identiftkasi transforman dan sekuensing.
3.3.1. Isolasi RNA total
Ikan kerapu bebek yang masih hidup berukuran 440-480 g (6 ekor) dipotong
bagian kepalanya. Hipofisa dikeluarkan seeara aseptis dan seeepatnya disimpan
dalam botol sampel dengan bantuan nitrogen eair, selanjutnya dilakukan ekstraksi
RNA. Apabila pelaksanaan ekstraksi masih lama, sampel disimpan pada suhu -20
Dc.
Isolasi RNA menggunakan GIT (Guanidine Isothiocyanate) mengikuti metode Suharsono (2002). Untuk meminimalkan pengaruh RNAse dari bahan kimia, alatdan tubuh manusia, bahan isolasi RNA diperlakukan dengan air bebas nuklease
(air-DEPC). Alat-alat yang digunakan 、ゥウエ・イゥャゥウ。セゥ@ pada suhu 121°C selama 15
menit. SelaIlla proses isolasi selalu menggunakan sarung tangan dan kondisi
14
Pituitari kerapu bebek
セ@
-
Kuantifikasi dengan spektophotometerIsolasi RNA total
I--Kuantifikasi dengan
セ@
-
elektroforesisSintesis eDNA dengan RT-PCR
• Desain primer : Program Primer3 berdasarkan gen GH dari ikan sekerabat vang terkonservasi.
,
• Primer lKF Forward: 5 cagacctgatcccagacca 3 Primer IKF Reverse: 5'ctacagggtacagttggcctca 3' • Metode RT -PCR: Suharsono et al. 2002
1
KIoning ke pGEMT -easy
Transformasi ke E. coli DH5a.
Identifikasi Transforman
•
Seleksi bim putih•
PCR koloni putih•
Isolasi plasmid rekombinan• Digesti dengan Eco RI
J
Sekuensing
• Analisa similaritas
• Analis domain
Gambar 5. Diagram alir penelitian
Organ pituitari dari 6 ekor ikan kerapu bebek digcrus dalam mortar dengan
bantuan nitrogen cair hingga menjadi tepung, kemudian dirnasukkan ke tabung
steril yang berisi 10-12 ml buffer ekstraksi GIT pada tabung falkon 50 ml.
[image:95.561.71.475.63.697.2]15
supernatannya diarnbiJ dan disentrifugasi lagi pada 10.000 rpm selarna 10 menit 4
°c.
Tabap selanjutnya adalah membuat gradien 1.5 ml CsCl: 1 ml CsCIIGIT
(1:1) (200 III x 5) dan bertabap 200 III supematan, kemudiandisentrifugasi 32.000
rpm selarna 20 jam pada suhu 20°C. Pelet yang terbentuk ditarnbab dengan 600
III 0,5% SDS (b/v) - 10mM Tris-HCl pH 7.5 dan disuspensikan. Carnpuran diekstraksi dengan fenol klorofom (1:1) dan disentrifugasi 15.000 rpm, selarna 5
menit (bisa dilakukan hingga 2 kali). Fase eair yang terbentuk ditambab 2.5 x
volume EtOH absolut dan 0.25 M NaOAC pH 4, kemudian diaduk perlahan.
Inkubasi pada suhu -45 GC selama 15 menit. Presipitasikan dengan sentrifugasi
15.000 rpm selarna 20 menit. Endapan yang terbentuk dibilas dengan EtOH 70%
(v/v), dikeringkan dan diresuspensikan dengan DEPC 0.1 %.
Kualitas dan kuantitas RNA total hasil isolasi dapat diketabui dengan
analisis kemumian dan kandungan RNA dengan menggunakan spektrofotometer
UV-VIS. Absorbansi diukur pada panjang gelombang 260 (1..260) dan 280 (1..280).
Kemumian RNA yang baik ditunjukkan oleh nilai rasio 1..26011..280 lebih besar atau
sarna dengan 1.80 (kemumian RNA terhadap penyangga reaksi) dan rasio
1..26011..230 lebih besar atau sarna dengan 2.00 (kemurnian RNA terhadap protein).
Kandungan RNA ditentukan dari pengukuran pada 1..260 (pada panjang gelombang
260, ssDNA = 40 Ilglml). Selanjutnya dilakukan elektroforesis pada gel agarose
1 % (b/v) dengan lOx buffer MOPS, voltase 100 volt selarna 45 menit. Visualisasi
RNA dilakukan di atas transluminator GelDoe (Labquip) dan difoto menggunakan
kamera digital fl.8 Full bright (olympus). Adanya pita unit-unit RNA ribosom
menunjukkan keberhasilan isolasi RNA.
3.3.2. Sintesis eDNA dengan RT -peR
Sintesis eDNA GH menggunakan paket sintesis eDNA SuperScrip?M
Double-Stranded eDNA Synthesis Kit dari Invitrogen. Kit ini memiliki
kemampuan SuperSeriplMII Rnase H rewrse transcriptase pada reaksi strand
pertama. RT-PCR (Reverse Transcriptase peR) dari RNA total pituitari ikan
kerapu bebek menggunakan primer spesifik yang terkonservasi dari 6 aksesi dari
16
(AF23271 I), E. coioides (AY038606, A Y513647, AF376771) dan Sebastes schlegeli
(A Y542484). Primer yang didapatkan dari program analisa Primer3 adalah IKF
Forward 5' cagacctgatcccagacca 3' (\ 9 pb) dan IKR Reverse 5'
ctacagggtacagttggcctca 3' (22 pb) dengan panjang sekuen yang diharapkan adalah
615 pb (Lampiran 2).
Satu mikrogram RNA total digunakan sebagai sampel untuk RT, kemudian
dicampur dengan 2x campuran reaksi (reaction mixture) 25 Ill, 0.5 III primer
forward maupun reverse (20 pmolllll), Taq enzym I Ill, 1.2 III MgS04 (2.5 mM)
kemudian diIambahkan air DEPC sehingga mencapai volume akhir 50 Ill. Proses
RT-PCR (PTC_IOO™ dari MJ Research Inc.) dijalankan pada suhu 45°C (30
menit); 92 °c (2 menit) sebanyak I siklus; (92 °C,15 detik; 45°C, 30 detik; 68°C,
I menit 30 detik) sebanyak 35 siklus dan 72 °c (5 menit).
3.3.3. Kloning eDNA ke dalam pGEMT-easy
cDNA yang berhasil disintesis, disisipkan ke dalam pGEM®-T Easy
(Lampiran 3) mengikuti prosedur Promega (2003). Vektor pGEM®-T Easy dan
Control insert DNA disentrifuse agar kandungannya terkumpul pada dasar tabung,
selanjutnya reaksi ligasi dicampur pada tabung dengan komposisi yaitu : 2 x
rapid ligase buffer 5 Ill, I III Vektor pGEM®-T Easy (SOng), I III T4 DNA ligase
(3 weiss units/ill) dan produk RT-PCR sebanyak 3 Ill. Tahap berikutnya adalah
campuran reaksi diinkubasi semalam pada suhu 4°C.
3.3.4. Transformasi ke bakteri E. coli DHSa
Pembuatan Bakteri Kompeten. Metode yang dilakukan mengikuti
Suharsono (2002). Sebuah koloni bakteri E.coli DHsu diambil dari biakan di
media SOB dan dikultur dalam 2 ml medium cair LB (digunakan tabung 50
ml), selanjutnya diinkubasi semalam pada suhu 37°C pada shaker (275 rpm).
Hasil kultur sebanyak 200 III dicampur dengan 2 ml LB, diinkubasi 2-3 jam
hingga mencapai OD60o
=
0.4-0.5. Setelah itu, masukkan ke dalam tabungependorf 1.5 ml dan diinkubasi pada es selama 10 menit.
Bakteri diendapkan dengan sentrifugasi pada 3.000 rpm selama 10 menit,
17
III (0.3 volume asal) bufer transformasi (TFB) dengan vortex pelan-pelan. Di
inkubasikan dalam es 10 menit. Disentrifugasi pada 3000 rpm selama 10 menit
pada suhu 4°C untuk pengendapannya. Cairan dibuang, endapan disuspensikan
dalam TFB 41.25 III (0.08 volume asal). Kemudian ditambahkan DMSO
sebanyak 3.3 III (7-8 % volume dari 1112 volume TFB), go yang dan biarkan di
dalam es selama 10 menit. Bakteri siap untuk ditransformasi.
Transformasi. Sel kompeten (E. coli DHsu) yang siap ditransformasi
dimasukkan dalam es, biarkan sebentar agar mencair. Selanjutnya, diambil 100
III bakteri ォッュー・エセョ@ dan ditambahkan 10-50 ng cDNA (volume 10 セエAI@ dan
inkubasi dalam es selama 20-25 menit. Campuran tersebut diberi kejutan panas
pada suhu 42°C selama 45 detik (jangan digoyang), kemudian diletakkan
dalam es selama 5 menit. Pindahkan ke suhu ruang, ditambahkan 100 III
medium 2 x YT/SOB dan diinkubasikan pada suhu 37°C dengan shaker pada
kecepatan 250 rpm selama 20 menit. 100-150 III bakteri tersebut disebar pada
medium selektif yang mengandung ampicillin (100 Ilg/ml).
Untuk menyeleksi adanya sisipan di dalam plasmid yang mengandung
gen lacZ, tambahkan 0.1 M IPTG (10 Ililcawan) dan 2% X-gal (50 Ililcawan)
pada permukaan medium. Bakteri yang mengandung plasmid, berisi fragmen
yang disisipkan pada situs pengklonan (MCS) di daerah lacZ, akan membentuk
koloni berwarna putih, sedangkan bakteri yang mengandung plasmid yang di
dalam MCS di daerah lacZ tidak tersisipi fragmen DNA akan menghasilkan
koloni berwama biru. Bakteri yang tidak mengandung plasmid akan mati
(tidak membentuk koloni). Kultur di inkubasikan semalam pada suhu 37°C.
Bakteri yang telah tertransformasi diperbanyak dalam medium LB yang
mengandung antibiotik (100 Ilg/ml ampicilin). lnkubasikan pada 37°C.
Bakteri siap digunakan dalam perbanyakan plasmid.
3.3.5. Identifikasi Transforman
Plating dan peR. Koloni yang berwarna putih (GH rekombinan) dilakukan pengujian kembali dengan pembuatan plating koloni dan PCR.
Koloni putih diambil dengan tusuk gigi steril kemudian digoreskan pada media
18
pada media. Adapun Prosedur PCR yang dilakukan adalah sebagai berikut :
Koloni berwarna putih yang sudah diplating dieampurkan ke dalam 7.15 III
ddH20, kemudian dilakukan hot start PCR pada suhu 95 °C,IO menit dan 15°C
selama 5 menit. Selanjutnya ditambahkan buffer 1 Ill; 0.5 III primer maju
(forward) maupun mundur (reverse) (20 pmoVlll), 0.05 III taq enzym (5 U/lll)
dan 0.8 III dNTP (25 mM). Proses PCR dijalankan pada suhu 94°C (2 menit) sebanyak 1 siklus; (94 °C,30 detik; 45°C, 30 detik; 68°C, 1 menit 30 detik)
sebanyak 30 siklus dan 72 °c (5 menit).
Isolasi plasmid. Plasmid pGEM®-T Easy yang mengandung eDNA diisolasi
dari bakteri E coli mengikuti prosedur Suharsono (2002). Satu koloni bakteri yang mengandung plasmid rekombinan ditumbuhkan di dalam 2 ml media luria bertani
(LB) (10 gil tripton, 5 gil ekstrak khamir, 10 gil NaCl, pH 7.5) yang mengandung ampisilin 100 mgll pada inkubator bergoyang (250 rpm) pada suhu 37°C selama
semalam. Bakteri diendapkan dengan sentrifugasi pada 10000 rpm (Jouan BR-4i)
pada suhu 4 °c selama 10 menit. Peletlendapan yang terbentuk ditambahkan
dengan 250 III buffer resuspensi, divortek, kemudian ditambahkan 250 III bUt"Ier
!isis dan 250 III buffer netralisasi dan dibolak-balik. Selanjutnya disentrifugasi pada kecepatan 10.000 rpm pada suhu 4 °c selama 20 menit. Supernatan/cairan
yang terbentuk ditarnbahkan dengan 0.1 V NaOAe 3 MpH 5.2! 0.25 V NaOAe 2
M dan 2 kali volume EtOH absolut, kemudian diinkubasi pada suhu -20°C
selama 2 jam. Setelah itu sentrifuse dengan kecepatan 14.000 rpm pada suhn 4 °c
selama 30 menit, kemudian endapan dieuei dengan 600 III Et OH 70% dan sentrifuse kembali dengan kecepatan 14.000 rpm pada suhu 4 °c selama 20
memt. Pelet yang terbentuk dikeringkan, dan ditambahkan TE sebanyak 15 Ill.
Guna menghilangkan sisa-sisa RNA, tambahkan RNase (l00 Ilglml) dan
inkubasi pada suhu 37°C sclama semalam. Selanjutnya tambahkan TE hingga
volume akhlr 500 Ill, kemudian diekstraksi dengan fenol : kloroform :
isoamilalkohol (25:24: 1) sebanyak 1 kali volume. Larutan disentifugasi pada
kecepatan 14.000 rpm pada suhu 20°C selama 10 menit. Cairan yang terbentuk
pada bagian atas dipindahkan dan selanjutnya dipresipitasi dengan penambahan
19
diinkubasi pada suhu -20°C selama 2 jam. DNA plasmid diendapkan dengan
sentrifugasi pada keeepatan 14.000 rpm, suhu 4 °c selama 20 menit. DNA
plasmid dibilas dengan ethanol 70% (v/v) dan dikeringkan dengan vakum. DNA
disuspensikan di dalam H20.
Pemotongan plasmid dengan enzim restriksi EcoRI. Plasmid
pGEM"'-T Easy rekombinan dipotong menggunakan enzim restriksi EcoRi
(Promega) untuk mengeluarkan sisipan eDNA GH dari vektornya. Sebanyak 1 J.!g
DNA plasmid dimasukkan ke dalam tabung eppendorf 1500 J.!I, kemudian
ditambah 0.5 J.!I enzim EcoRI (20 U/J.!I), 2 J.!I (IX buffer reaksi), dan ditambah
ddH20 steril hingga volume akhirnya menjadi 20 J.!l. Campuran reaksi ini
diinkubasi pada suhu 37°C selama semalam.
3.3.6. Pengurutan eDNA
Pengurutan DNA dilakukan terhadap klon-klon eDNA GH terpilih
menggunakan prosedur Sanger et al. (1977) yang didasarkan pada
"dideoxy-nucleotide chain-termination" menggunakan mesin otomatis ABI PRISM 310.
3.4. Analisis Data
Urutan nukleotida yang diperoleh dari hasil sekuensing dilakukan analisis
dengan program Bioedit guna mendapatkan sekuen eDNA GH. Selanjutnya
dilakukan analisis kesamaan (Similarity) dengan menggunakan software BlastN
(Basic Local Alignment Search Tool) untuk nukleotida dan BlastP untuk protein.
Matrik kesamaan antara spesies hasil BlastN maupun BlastP dianalisis
menggunakan software sequence identitiy matrix pada program Bioedit dengan
urutan program sebagai berikut : BlastNIP, Format Fasta, Kesejajaran (alignment),
Bioedit. Kesejajaran nukleotida dan protein deduksi eDNA GH dianalisis dengan
program ClustalW di web \','WW.ebi.ae.uk/c\ustalw/index.html. Untuk melakukan
kesejajaran, urutan DNA atau asam arnino dituliskan kembali dalam format Fasta
(Pearson 1990) dan disimpan sebagai suatu file teks menggunakan NOTEPAD.
Pohon filogenetik disusun berdasarkan urutan asam amino yang dideduksi dari
eDNA GH menggunakan program TreeCon. Komposisi asam amino dari sekuen
eDNA GH dianalisis menggunakan program Bioedit dengan urutan keIja yaitu :
20
eDNA GH menggunakan program Prosite Database di web
http://\\\\\\'''''l1ClS\cilicl!i-bin. Peta restriksi eDNA GH dianalisis menggunakan
21
IV. HASIL DAN PEMBAHASAN
4.1. Isolasi RNA
Isolasi RNA total dari kelenjar pituitari kerapu bebek (Cromileptes altivelis)
dengan menggunakan metode GIT (Guanidine Isothiocyanate) telah berhasil
dilakukan dengan kuantifikasi berdasarkan spektrofotometer (Tabel 1) dan
pengeeekan kualitas berdasarkan elektroforesis pada gel agaros 1 % (b/v) (Gambar
6).
Tabel 1. Kuantifikasi RNA total ikan kerapu bebek (Cromileptes altivelis)
Pituitari 0.l40 0.161 0.869
, _ 28S
_ 18S
{RNA} (p.g/p.I)
3.920
Gambar 6. Hasil isolasi RNA pituitari ikan kerapu bebek (Cromileptes altivelis) yang dielektroforesis dengan lOx buffer MOPS pada gel agarose 1% (b/v) .
Berdasarkan hasil elektroforesis ini dapat dilihat bahwa isolasi RNA berhasil
dilakukan dengan terbentuknya 2 pita RNA. Pita ini menunjukkan pita ribosom
RNA yang mempunyai usuran 28 S dan 18 S. Konsentrasi RNA yang diperoleh
adalah sebesar 3.920 llg/lll, sedangkan volume sampel yang dielektroforesis
sebesar 2 Ill.
4.2. RT·PCR
Fragmen eDNA GH diperoleh dengan RT-PCR (Reverse
Trancriptase-Polymerase Chain Reaction) menggunakan primer spesifik yang terkonservasi
dari 6 aksesi data Genbank. Berdasarkan hasil elektroforesis pada gel agarose 1 %
(b/v) dapat diketahui bahwa eDNA yang diperoleh mempunyai ukuran sekitar 650
pb (Gambar 7). Ukuran eDNA GH ini mendekati sekuen yang diharapkan
650pb
Keterangan :
1 : A 100 ng
2 :cDNAGH
M : Marker 1 Kb plus.
Gambar 7. Hasil RT-PCR pada suhu penempelan (annealing) 45°C.
4.3. Transfonnasi ke E. coli DHsu
Putih
Biru
Gambar 8. Hasil transformasi E. coli DHsu. oleh eDNA GH ikan kerapu bebek (Cromileptes altivelis)
eDNA GH ikan kerapu bebek diligasikan ke vektor pGEM®-T Easy,
kemudian diintroduksikan ke dalam E. coli DHS<l dengan media LA + Amp +
IPTG (Isopropil Thiogalaktosida). Transformasi
E.
coli DHsu dengan eDNA GHberhasil dilakukan yang ditunjukkan dengan adanya koloni yang berwarna putih
pada media seleksi (Gambar 8). Koloni berwarna biru adalah nontransforman,
sedangkan yang berwarna putih adalah transforman yang mengandung sisipan
eDNA GH. Bakteri
E.
coli DHsu yang mengandung pGEM@-T Easy rekombinanhidup pada media ampicillin. Bakteri ini tidak mampu menghasilkan
fJ-galaktosidase karena adanya sisipan eDNA GH (insertional inactivation) pada
[image:103.561.63.442.35.786.2]23
Koloni yang mengandung pGEM@ -T Easy non rekombinan tidak mengalami
penyisipan eDNA GH pada gen lacZ. Gen ini mampu menghasilkan
p-galaktosidase yang mengubah molekul X-gal dari tidak berwama menjadi
molekul yang berwama biru pada koloni.
4.4. Identifikasi Transforman
4.4.1. Koloni peR
Koloni yang berwama putih diuji dengan PCR dan plating koloni ke media
LA + Amp yang barn guna mengetahui adanya sisipan eDNA GH. Koloni yang
mempunyai ukuran sekitar 650 pb merupakan plasmid yang membawa eDNA GH
seperti ditunjukkan pada sumur (well) nomor 2,3 dan 4 (Gambar 9).
1 2 3 4
Keterangan :
[image:104.561.38.463.0.789.2]1 : eDNA OH hasil RT-PCR 2,3,4 : sisipan eDNA OH. 650pb , .
Gambar 9. Identifikasi sisipan eDNA GH dengan PCR.
4.4.2. Isolasi Plasmid eDNA GH
Koloni berwama putih yang mengandung sisipan eDNA GH disub kultur
dalam media LB selama 16 jam, kemudian dilakukan isolasi eDNA (Gambar 10).
Pita yang terbentuk pada hasil isolasi ini mempunyai 2-3 ukuran. Hal ini
menggambarkan topologi dari DNA plasmid. Topologi DNA plasmid yang
lengkap ditunjukkan oleh 3 pita. Topologi DNA plasmid tersebut yaitu sirkuler
terbuka (OC), linier, dan superkoil (CCC). Demikian pula ukuran masing-masing
pita DNA dapat kita tentukan berat molekulnya dengan menggunakan topologi
linier dan memperkirakannya berdasarkan ukuran pita DNA pada marker yang
tersedia. Ada tiga topologi DNA plasmid utuh yang dapat dilihat jelas pada
sumur I, yaitu sirkular terbuka (OC) yang terletak di atas dan linier yang terletak
24
ketiga topologi DNA tersebut ditentukan oleh keeepatan migrasinya
masing-masing. Keeepatan migrasi ini ditentukan oleh gaya geseknya dengan gel
agarose. Gaya gesek paling keeil menyebabkan DNA bermigrasi sangat eepat.
Migrasi topologi superkoil paling eepat karena bentuknya kompak sehingga gaya
geseknya paling keeil.
12000 6000
4000
3000
1000
800
100
Keterangan :
1-3
=
plasmid rekombinan M=
Marker I KbGambar 10. Hasil isolasi plasmid yang mengandung sisipan eDNA GH pada gel elektroforesis 1 % (b/v)
4.4.3. Pemotongan DNA Plasmid
Pemotongan DNA plasmid dengan enzim restriksi EcoRl bertujuan untuk
melepaskan eDNA GH dari vektomya. Enzim restriksi EcoRl memotong plasmid
menjadi 2 situs pemotongan. Berdasarkan hasil pemotongan dengan EcoRl yang
dimigrasikan pada gel elektroforesis, terbentuk 2 pita dimana pita paling atas
merupakan vektor pGEMT-easy yang berukuran sekitar 3000 pb dan dibawalmya
adalah eDNA GH yang berukuran 650 pb (Gambar 11). Hal ini menunjukkan
bahwa pengklonan eDNA GH ke dalarn plasmid pGEM®-T Easy telah berhasil
dilakukan.
4.5. Analisis Urutan Nuldeotida
Urutan nukleotida yang diperoleh dari hasil sekuensing (Lampiran 4)
dilakukan pengolahan dengan program Bioedit (Lampiran 5 dan 6) guna
mendapatkan sekuen eDNA GH. Nukleotida GH ikan kerapu bebek mempunyai
25
kodon akhir TGA = 615-618) (Gambar 12). Asam-asam amino yang diperoleh ini
merupakan deduksi (turunan) dari eDNA GH kerapu bebek.
pb
5000 4000
M 1
,.. 3000pb
,.. 650pb
Keterangan : M : Marker I Kb
I : hasil pemotongan
Gambar 11. Pemotongan DNA plasmid dengan enzim EcoRI.
4.5.1. Kesamaan (Similarity)
Analisis kesamaan nukleotida eDNA GH dengan menggunakan BlastN dari
50 kesejajaran (Lampiran 7) yang selanjutnya ditampilkan dalam bentuk matrik
kesamaan menunjukkan bahwa sekuen eDNA GH ikan kerapu bebek (c. altivelis) mempunyai kesamaan yang tinggi yaitu berkisar antara 0.805 - 0.969 (Tabel 2)
dengan kelompok ikan-ikan laut maupun tawar. Kesamaan tertinggi adalah
dengan Epinephelus coioides (0.969), selanjutuya E. awoara (0.953), E. akaara
(0.948), Lepomis cyanellus (0.889) dan Acanthopagrus latus (0.889). Ketiga
spesies pertarna merupakan satu kelompok grouper dengan kerapu bebek (c.
altive/is). Kelompok tersebut mewakili ikan-ikan yang hidup di air laut.
Sedangkan kesamaan pada 5 kesejajaran di urutan bawah berturut-turut adalah
Monopterus albus (0.846), Oreochromis niloticus (0.823), Mugil planatus
(0.817), Lateolabrax japonicus (0.815) dan Siniperca kneri (0.805). Ketiga
spesies yang pertama mewakili ikan-ikan yang hidup di air tawar dan pay au. Matriks kesamaan nukleotida ini juga bisa digunakan untuk melihat kesamaan
antara ikan-ikan lainnya selain ikan kerapu bebek, eontohnya kesamaan antara
ikan nila (0. niloticus) dengan ikan kakap (Lates calcarifer) yang menunjukkan
F (19 pb)
セ@
-26
'1 ATG MC TGT GTC GTC CTT CCT GCT GTT CM GTA GTG TCT CTG GGT 45 1 Met Asn cys Val val Leu Pro Ala val Gln val val ser Leu Gly 15
'46 GTT TCC TCT CAG CCA ATC ACA GAC GGC CAG CGT CTG TTC TCC ATC 90 :16 val ser ser Gln pro Ile Thr ASp Gly Gln Arg Leu phe Ser Ile 30
91 GCC GTC AGC AGA GTT CAA CAT CTC CAC CTG CTT GCT CAG AGA CTC 135 31 Ala val Ser Arg val Gln His Leu His Leu Leu Ala Gln Arg Leu 45
136 TTC TCT GAC TTT GAG AGC ACT CTG CAG ACG GAG GAG CAG CGA CAG 180 46 phe ser ASp Phe Glu ser Thr Leu Gln Thr Glu Glu Gln Arg Gln 60
,181 CTC MC MG ATC TTC CTG CAG GAC TTC TGT AAC TCT GAT TAC ATC 225 61 Leu Asn Lys Ile phe Leu Gln ASp phe cys Asn ser ASp Tyr Ile 75
,226 ATC AGC CCC ATC GAC MG CAT GM ACG CAG CGC AGC TCC GTG TTG 270 '76 Ile ser Pro Ile ASp Lys His Glu Thr Gln Arg ser ser val Leu 90
,271 AAG CTG TTG TeA ATe TeC TAT CGG CTG GTG GAG TeC TGG GAG TTC 315 91 Lys Leu Leu ser Ile ser Tyr Arg Leu val Glu ser Trp Glu phe 105
316 CCC AGT CGG TeC CTG TCC GGA GGT TCT GCT CCC AGA AAC CAG ATT 360 106 pro ser Arg ser Leu Ser Gly Gly ser Ala Pro Arg Asn Gln Ile 120
361 TCT CCC AM CTG TCT GAA TTG AAG ACC GGG ATC CTG CTG CTG ATC 405
121 ser pro Lys Leu ser Glu Leu Lys Thr Gly Ile Leu Leu Leu Ile 135
406 AGG GCA AAT CAG GAT GGA GCA GAG CTC TTC CCT GAC AGC TCC GCC 450 136 Arg Ala Asn Gln ASp Gly Ala Glu Leu phe pro ASp ser ser Ala 150
451 CTC CAG CTG GCT CCT TAT GGG GAC TAT TAT CAG AGT CTG GGC GCC 495 ,151 Leu Gln Leu Ala pro Tyr Gly ASp Tyr Tyr Gln ser Leu Gly Ala 165
·496 GAC GAG TCG CTG CGA CGA ACG TAC GAA CTG CTG GCG TGT TTC AM 540 ,166 ASp Glu Ser Leu Arg Arg Thr Tyr Glu Leu Leu Ala cys phe Lys 180
.541 AM GAC ATG CAC AAG GTG GAG ACC TAC CTG ACG GTG GCT AM TGT 585 181 Lys ASp Met His Lys val Glu Thr Tyr Leu Thr val Ala Lys cys 195
586 CGA CTC TCT CCT GAG GCC AAC TGT ACC CTG TAG 618 196 Arg Leu Ser pro Glu Ala ASn cys Thr Leu End
R(22 pb)
Tanda ( _ ) kodon awal; Tanda ( ••• ) kodon akhir; F (primer majulforward primer); R
[image:107.563.50.470.38.772.2](primer mundurlreverse primer).
Gambar 12. Urutan nukleotida dan asam amino deduksi eDNA GH kerapu bebek
(Cromileptes altivelis).
4.5.2. Situs Pemotongan eDNA GH
Situs pemotongan eDNA GH sangat berguna sekali dalam rekayasa gen,
terutama dalam pemotongan urutan sekuen tertentu dan menyambungkannya
kembali. Analisis situs pemotongan dari nukleotida GH kerapu bebek
Tabe12. Matrik kesamaan sekuen eDNA GH ikan kerapu bebek (Cromileptes altivelis) dengan ikan-ikan air laul dan lawar
C.oItivt/1s F..""""*, F . . _ F . . - ' Lcyunttlhu A._ S._1'Qki A.JClt/egd/ S.kneri A.htdJtrl
R._'"
lW_b S.o«llatus M.-n/b lセヲエャイ@0 . _
O·tzTlMrin
D.""""
L_=
H.bnmlhn P.jIaI'e,"1/S
...
..,..,."pNセ@
, - ,
c.ka:ilta M.aJlNs O.nllotInuM_
C. ail Epico Euwo Eakal ャセ」ケオ@ A.1o S.OJIT A .. 'idr S.kM A.btl/C /barb /Uta sNocセ@ M._ iセcqi@ O.1xxr Ocrg D.Jab Ljap H.bras P jlav SqNi. P.c:ro 5.1ItClI" c.ia: Mmra/ O.mlo M.pIan
ID 0.969 0.953 0.948 0.889 0,389 0.885 0.838 0.805 0.886 0.883 0.883 0.180 0.862 0.860 0.857 0.857 0.859 0.815 0.851 0.851 0.349 0,349 0.809 0.852 0.846 0.823 0.8\7 0,969 ID 0.973 0.969 0.902 0,895 0.897 0.894 0.824 0.892 0.895 0.895 0,895 0.871 0.881 0.866 0.871 0.868 0.816 0.865 0.869 0.866 0.868 0.809 0.865 0,860 0,g32 0,821 0.953 0.973 ID 0.995 0.892 0.834 0.834 0.882 0.810 0.878 0.881 0.882 0.887 0.853 0,869 0.852 0.855 0.850 O.8{)4 0.848 0.855 0.860 0.858 0.798 0.853 0.856 0.822 0.816 0.948 0.969 0.995 ID 0.887 0.879 0.882 0.878 0.806 0.873 0.876 0.878 0.882 0.848 0.865 0.850 0.8s) 0.845 0.800 0.147 0.850 0.856 0.855 0.793 0.853 0.856 0.820 0.811 0.889 0.902 0.892 0.887 ID 0.894 0.895 0.892 0.850 0.891 0.889 0.894 0.904 0.889 0.881 0.852 0.853 0.891 0.8\9 0.8S) 0.871 0.881 0.878 0.814 0.878 0866 0.836 0.824 0.889 0.895 0.884 0.879 0.894 ID 0.969 0.998 0.824 0.99\ 0.956 0.959 0.902 0.882 0.876 0.839 0.8-40 0.879 0.897 0.&40 0.869 0.865 0.882 0.891 0.876 0.865 0.827 0.813 0.885 0.897 0.884 C.882 0.895 0.969 10 0.967 0.828 0.960 0.970 0.965 0.905 0.884 0.879 0.840 0.1142 0.881 0.879 0.1148 0.861 0.865 0.892 0.869 0.873 0.856 0.828 0.817 0.888 0.894 0.882 0.878 0.892 0.998 0.967 ID 0.822 0.990 0.954 0.957 0.900 0.881 0.874 0.839 0.140 0.878 0.895 0.839 0.868 0.863 0.881 0.889 0.876 0863 0.825 0.811 0.805 0.824 0.8\0 0.806 0.850 0.824 0.828 0.822 ID 0.816 0.821 0.828 0.840 0.816 0.822 0.787 0.188 0.813 0.151 0.790 0.810 0.810 0.818 0.141 0.813 0.813 0.772 0.765 0.886 0.892 0.878 0.873 0.89\ 0.991 0.960 0.990 0.816 10 0.947 0.954 0.891 0.881 0.873 0.834 0.835 0.878 0.892 0.835 086) 0.858 0.879 0.886 0.871 0.856 0.819 0.806 0.883 0.895 0.88\ 0.816 0.889 0.956 0.970 0.954 0.821 0.947 lD 0.95\ 0.902 0.876 0.871 0.834 0.8)5 0.873 0.871 0.142 0.856 0.861 0.879 0.861 0.861 0.85) 0.824 0.813 0.883 0.895 0.882 0.878 0.894 0.959 0.965 0.957 0.828 0.954 0.951 lD 0.907 0.886 0.876 0.840 0.842 0.819 0.865 0.840 0.863 0865 0.895 0.855 0.869 0.858 0.828 0.817 0880 0.895 0.8n 0.882 0904 0.902 O.90S 0.900 0840 0.897 0.902 0.907 ID 0.895 0.887 0.855 O.U) 0.892 0.826 0.856 0871 0.878 0.943 0817 0.874 0.lt81 (l.M8 0.8)5 0.862 0.871 0.85) 0.848 0.889 0.U2 0.834 0.881 0.816 0.88\ 0.876 0.886 0.895 lD 0.869 0.831 0.839 0.973 0.804 0.348 0.855 0855 0.871 0.801 0.850 0.852 0.819 0.809 0.860 0.88\ 0.869 0.865 0.88\ 0.876 0.879 0.874 0.822 0.87) 0.871 0.876 0.887 0.869 lD 0.858 0.860 0.168 0.798 0.869 0873 0.892 0.861 0.793 0.348 0.876 0.835 0.822 0.857 0.866 0.852 0.850 0.852 0.839 0.840 0.839 0.787 0834 0.834 0.840 0.855 0.131 0.858 ID 0.991 0.839 0.770 0865 0.837 0.1B4 0.8)S 0.764 0.822 0.855 0827 0.827 0.857 0.87\ 0.855 PNXセI@ 0.853 0.840 0.842 0.840 0.188 0.835 0.835 0.342 0.8S) 0.8)9 0.860 0.991 ID 0.840 0.770 0.865 0.837 0.835 0.837 0.764 0.826 0.860 0.828 0.829 0.859 0.851 0.850 0.845 0.89\ 0.879 0.881 0.&78 0.813 0.878 0.873 0.879 0.892 0.973 0.861 0.839 0.840 lD 0.108 0.842 0.855 0.850 0.861 0.804 0.845 0.850 0.8\9 0.808 0.815 0.816 0.&04 0.800 0.8\9 0.897 0.879 0.895 0.751 0.892 0.87\ 0.865 0.826 0.804 0.798 0.170 0.770 0.808 m 0.775 0.79) 0.788 0.813 0.985 0.798 0.796 0.758 0.798 0.851 0.865 0.841 0.847 0.853 0.840 0.848 0.839 0.790 0.835 0.842 0.840 0.856 0.848 0.869 0.865 0.865 0.842 0.175 lD 0.842 0.853 0.837 O.77S 0.832 0.142 0.819 0.817 0.851 0.869 0.855 0.850 0.871 0.869 0.86\ 0.868 0.810 0.163 0.856 0.863 0.871 0.855 0.873 0.837 0.837 0.855 0.793 0.842 lD 0.1145 0.147 0.788 0.843 0.860 0.808 0.809 0.849 0.866 0.860 0.856 0.881 0.865 0.865 0.863 0.810 0.858 0.86\ 0.865 0.878 0.855 0.892 0.834 0.835 0.850 11.788 0.853 0.845 ID Q853 0.783 0.839 0.868 0.824 0.82\ 0.849 0.868 0.858 0.855 0.878 0.882 0.892 0.88\ 0.818 0.879 0.879 0.895 0.943 0.871 0.861 0.835 0.837 0.861 0.811 0.837 0.847 0853 ID 0.804 0.842 0.856 0.827 0.813 0.809 0.809 0.798 0.793 0.814 0.891 0.869 0.889 0.747 0.886 0.861 0.855 0.817 0.801 0.793 0.764 0.764 0.804 0.985 0.775 0.188 0.783 0.804 ID 0.793 0.791 0.753 0.795 0.852 0.865 0.853 0.8S) 0.878 0.876 0.873 0.876 0.813 0.111 0.861 0.869 0.874 0.850 0.&48 0.822 0 .• 26 0.&45 0.798 0.832 0.843 0.839 0.842 0.793 lD PNXSセ@ 0.808 0.795 0.846 0.860 0.856 0.856 0.866 0.865 0.856 0.863 0.813 0.856 0.853 0.85' 0.88t 0.852 0.876 0.855 0.860 0.'50 0.796 0.842 0.860 0.868 0.856 0.791 0.835 ID 0.836 0.824 0.823 0.832 0.822 0.820 0.836 0.827 0.828 0.825 0.772 0.819 0.824 0.828 0.848 0.819 0.835 0.827 0.828 0.819 0.758 0.819 0.808 0.824 0.827 0.753 0.808 0.836 ID "00
0.BI7 0.821 0.SJ6 0.811 0.824 0.813 0.817 0.811 0.765 0.806 0.813 0.817 0.835 0.809 0.822 0.821 0.829 0.&08 0.798 0.817 0.809 0.821 0.813 0.795 0.795 0.124 0808 ID
Keterangan :
Epinephelu, coioide, (AY038606). E. awaara (AF2327 11). E.akaara (AY326406). Lep"mj, cyanellu, (AYS30822). Acanlhopagrus latus (SS8867). Sparus aurala (A Y038038). A. ,chlegeli
(AY714371). Sin/perca Imeri (AYI55227). A.bulcheri (X59377). Rhob<iosargu' :tarOO (AYSS3207). Red sea bream (X06962). Sc/aenop' oce/latus (AF06S165). Morone saxali/i, (S78253). Late,
calcarifer (X59378), Odonthestes bonariensis (AYI87284), O.argenlinensts (AF236091), DicenIrtD"Chus Iabrax (X65716). Lateolabraxjaponicus (U3629), Hemiramphus brasiliensis (AY775149),
Perea f1avescens (AY007303), Seriola quinqueradiata (M35627), Pseudosciaena crocea (AF231941). Sebasticus marmoratu.s(U3627), CoitUS kazika(AB079538), Monopterus albus(AY265351),
28
tersebut antara lain, Bamffl, BanII, san, HaeII, Sac!, BsaI, NspI dan BanI
(Gambar 13), sedangkan situs pemotongan seeara lengkap tereantum pada
Lampiran 8.
セ@ . NEB qe cutter restriction enzymes . Main non·omlapping, milL 618 aa ORr, ::=54%, atセVE@
: ,i 5' extension
LNZセ@ I 3' i'XteI'lsion
fnzII" .... cole
fr.'ailtlle frcJ tEB
k。セ@ other sャiーセャゥ・イ@
rid HセゥAtiNZMイZ[セャ[セゥ@ GZh[ャLゥlG[セ@
• I oM 1 ,",MIl (enz ... ): aoiJigooJS sitt
11 , ! I 618
'i' I. I III '
.Btg1! 8sp'1! Sbi! Ssai!
*E&el SliI1! BgIll 'BspE!
1l\I,! 6s<II! :l:AYall
'Sau96! Bsr! 1Ior! SstH! BsaJ! .PspG!
I j' III il
PwlI *fl:iI Sap! Bpo! EciI So:! BollI fok! BtsC! Bstf5! 'Bell BaoIi! £los!
III II
BSlfl5! tHincii tPl::cI 'SolI il".lll Bs4! Mst>! *SsiWI 'IWlII!V 'lIaelI *Sfoi 'Na-! 'BsaH!
*Hcil *Banl
Tsp5(I9! 'lias!
[image:109.561.23.473.29.460.2]セA@
Gambar 13. Situs Pemotongan eDNA GH kerapu bebek (Cromileptes altivelis).
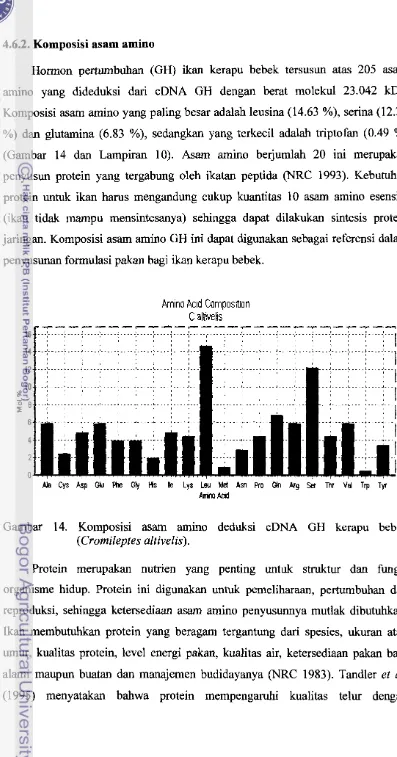
4.6. Analisis Protein Deduksi eDNA GH Kerapu Bebek
4.6.1. Kesamaan (Similarity)
Analisis protein deduksi (turunan) dari eDNA GH berdasarkan BlastP dari
50 kesejajaran (Lampiran 9) yang selanjutnya ditampilkan dalam bentuk matrik
kesamaan menunjukkan bahwa protein GH kerapu bebek mempunyai kesamaan
antara 0.651 - 0.895 (Tabel 3). Protein deduksi eDNA GH kerapu bebek
mempunyai kesamaan tertinggi (0.895) dengan Epinephelus coioides, kemudian
berturut-turut dengan E. awoara (0.886), E. Akaara (0.882), Siniperca kneri
(0.877) dan Lepomis cyanellus (0.868). Sedangkan kesamaan pada 5 kesejajaran
paling rendah adalah Limanda yokohamae (0.651), Platichthis bicoloratus
(0.656), Hippoglossus hippoglossus (0.660), Fugu rubripes (0.701) dan Sciaenops
rrabel3. Matrik kesamaan protein deduksi eDNA GH ikan kerapu bebek (Cromilepte3 altiveli3) denpn ikan-ikan air laut dan taW8l!
C.dtwlll £-..,
E . _ g _
H .. rl
lセBGN@
,.-,
..
-aNセᄋ@
s ... ", ...
tNiセ@
'-""""""
'''"''"'"
'-'
H.bn>tIIl c ....
....,."ID 0.1195 O.lII!6 0.1112 om