ISOLASI DAN IDENTIFIKASI STEROID/TRITERPENOID
PADA SPONGE (Xestospongia sp de Laubenfels) DARI
PANTAI LHOKNGA ACEH BESAR
SKRIPSI
OLEH:
RIZKY MAYA SARI
NIM 121524081
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
ISOLASI DAN IDENTIFIKASI STEROID/TRITERPENOID
PADA SPONGE (Xestospongia sp de Laubenfels)DARI
PANTAI LHOKNGA ACEH BESAR
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada
Fakultas FarmasiUniversitas Sumatera Utara
OLEH:
RIZKY MAYA SARI
NIM 121524081
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
ISOLASI DAN IDENTIFIKASI STEROID/TRITERPENOID
PADA SPONGE (Xestospongia sp de Laubenfels)DARI
PANTAI LHOKNGA ACEH BESAR
OLEH:RIZKY MAYA SARI NIM 121524081
Dipertahankan di hadapan Panitia Penguji Skripsi Fakultas FarmasiUniversitas Sumatera Utara Pada Tanggal: 11 Mei 2015
Disetujui Oleh:
Pembimbing I, Panitia Penguji,
Dra. Aswita Hafni Lubis, M.Si., Apt Dra. Herawaty Ginting, M.Si., Apt. NIP 195304031983032001 NIP 195112231980032002
Dra. Aswita Hafni Lubis, M.Si., Apt. Pembimbing II, NIP 195304031983032001
Dr NIP 195107231982032001 NIP 195109081985031002
Drs. Awaluddin Saragih, M.Si., Apt NIP 195008221974121002
Medan, Juli 2015 Fakultas Farmasi
Universitas Sumatera Utara Wakil Dekan I,
Prof. Dr. Julia Reveny, M.Si., Apt. NIP 195311281983031002
Dra. Herawaty Ginting, M.Si., Apt. NIP 195112231980032002
Dra. Aswita Hafni Lubis, M.Si., Apt. NIP 195304031983032001
Drs.Suryadi Achmad, M.Sc., Apt. NIP 195109081985031002
KATA PENGANTAR
Skripsi ini disusun sebagai salah satu syarat mencapai gelar Sarjana
Farmasi pada Fakultas Farmasi Universitas Sumatera Utara, dengan judul “Isolasi
dan Identifikasi Steroid/triterpenoid pada Sponge (Xestospongia sp de Laubenfels)
dari Pantai Lhoknga Aceh Besar”.
Pada kesempatan ini dengan segala kerendahan hati penulis mengucapkan
terima kasih yang sebesar-besarnya kepada Bapak Prof. Dr. Sumadio
Hadisahputra, Apt., selaku Dekan Fakultas Farmasi USU Medan, yang telah
memberikan fasilitas sehingga penulis dapat menyelesaikan pendidikan. Ibu Dr.
Poppy Anjelisa Zaitun Hasibuan M.si., Apt selaku pembimbing akedemik. Ibu
Dra. Aswita Hafni Lubis, M.Si., Apt dan Ibu Dra. Suwarti Aris, M.Si., Apt., yang
telah membimbing dan memberikan petunjuk serta saran-saran selama penelitian
hingga selesainya skripsi ini.
Bapak dan Ibu staf pengajar Fakultas Farmasi USU Medan yang telah
mendidik selama perkuliahan. Bapak dan Ibu Kepala Laboratorium Penelitian dan
Fitokimia yang telah memberikan fasilitas, petunjuk dan membantu selama
penelitian. Ibu Dra. Herawaty Ginting, M.Si., Apt., Bapak Suryadi Achmad,
M.Sc., Apt., Bapak Awaluddin Saragih, M.Si., Apt., selaku dosen penguji yang
telah memberikan kritik, saran dan arahan kepada penulis dalam menyelesaikan
skripsi ini.
Penulis juga mengucapkan terima kasih dan penghargaan yang tiada
terhingga kepada Ayahanda Bustami, dan Ibunda Darwani, yang telah
jabarkan baik moril maupun materi, juga kepada Abang-abang,kakak tercinta adek
tercinta, Uzir Farizal, Rahmad Zulmi, Sri Wahyuni, Asriani, Rizka Khaira.
Penulis menyadari sepenuhnya bahwa dalam penulisan skripsi ini masih
jauh dari kesempurnaan, oleh karena itu penulis menerima kritik dan saran demi
kesempurnaan skripsi ini. Penulis berharap semoga skripsi ini dapat memberikan
manfaat bagi kita semua.
Medan, Februari 2015
Penulis
ISOLASI DAN IDENTIFIKASI STEROID/TRITERPENOID PADA SPONGE Xestospongia sp de Laubenfels DARI
PANTAI LHOK NGA ACEH BESAR yarat untuk memperolehgelar Sarjana
bABSTRAK
Sponge merupakan salah satu hewan invertebrata laut yang hidup pada terumbu karang yang mempunyai potensi bioaktif yang belum banyak dimanfaatkan dalam berbagai keperluan, terutama untuk obat-obatan. Senyawa metabolit sekunder yang terdapat dalam sponge adalah alkaloid, steroid/triterpenoid dan sesquiterpenoid. Senyawa steroid/triterpenoid digunakan dalam bidang pengobatan sebagai kardiotonik, prekursor vitamin D, kontrasepsi oral dan antiinflamasi. Steroid/triterpenoid merupakan kelompok penting dari produk alami yang memiliki profil farmakologi yang luas, diantaranya sebagai pengatur hormon, antioksidan, anti-asma, bronkodilator dan menormalkan darah Tujuan penelitian ini adalah untuk mengetahui karakterisasi simplisia, skrining fitokimia dan isolasi senyawa steroid/triterpenoid dari sponge Xestospongia sp de Laubenfels.
Ekstraksi dilakukan secara maserasi menggunakan pelarut adalah n-heksana, ekstrak diuapkan dan di analisis dengan kromatografi lapis tipis (KLT) dengan berbagai perbandingan pengembang, dilanjutkan isolasi menggunakan kromatografi lapis tipis (KLT) preparatif. Terhadap isolat yang diperoleh dilakukan uji kemurnian secara kromatografi lapis tipis 2 arah, selanjutnya di karakterisasi secara spektrofotometri ultraviolet (UV) dan spektrofotometri inframerah (IR).
Hasil karakterisasi simplisia Xestospongia adalah kadar air 6,00%, kadar sari yang larut dalam air 4,47%, kadar sari yang larut dalam etanol 5,43%, kadar abu total 10,13%, dan kadar abu tidak larut asam 7,07%. Hasil skrining fitokimia kimia diperoleh senyawa alkaloid, steroid/triterpenoid, glikosida dan saponin. Hasil isolasi diperoleh isolat harga Rf = 0,85 untuk fase (gerak 1) dan Rf 0,8 (fase gerak 2). Hasil analisis isolat secara spektrofotometri UV memberikan absorbansi maksimum pada panjang gelombang 203 nm dan hasil secara spektrofotometri IR menunjukkan adanya gugus fungsi –OH, CH-alifatis, C=C, CH3, C=O. Isolat yang diperoleh termasuk golongan senyawa steroid/triterpenoid.
ISOLATION OF STEROIDAL/TERPENOIDAL COMPOUNDS FROM OF SPONGE (Xeastospongia sp de Laubenfels) FROM LHOKNGA BEACH ACEH BESAR
bABSTRACT
Sponge is one of ocean invertebrate which lives on coral reef and it has Bioactive potential that has not been widely used in various occasion, especially in drugs. Secondary metabolite compound that can be isolated from sponge is Alkaloida from Xestospongia sp., Diterpenoida from Oceanapia sp., sesquiterpenoida from Dysidea herbaceae, isonitril and terpenoid from
Halicandria sp., and sesterterpenoid from Hyrtios erecta. Triterpenoid compound
can be used in various needs such as to treat diabetes, menstruation problem, snakebite, skin problems, livers, malaria, infection, Analgesic and cancer. The purpose of this research was to determine the simplex characterization, phytochemical screening and isolating the steroidal/triterpenoidal compound of
Xestospongia sp leaves
Extraction accomplished by maceration of dried powdered plant material with n-hexane, then the extract was fractionated preparative Thin Layer
Chromatography. The purity of isolates were confirmed by two-dimensional Thin Layer Cromatography and the pure isolate was characterized with ultraviolet and infrared spectrophotometric methods.
The result of simplex characterization gave water content 6.00%, water-soluble extract 4.47%, ethanol-water-soluble extract 5.43%, total ash 10.13%, and acid-insoluble ash 7.077%. The result of phytochemical screening of Xestospongia sp leaves gave positive results for the presence of flavonoid, steroid/triterpenoid, glycoside and saponin. Three pure isolates were obtained, with Rf = 0,8, the measurement of uv spectrum gave maximum absorption at 203 nm. The result of infrared spectrophotometric measurement indicated the presence of –OH, CH, C=C, C-H3, C-O functional groups. The isolates were inferred as steroid/triterpenoid compounds.
DAFTAR ISI
JUDUL ... i
HALAMAN PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 2
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 3
1.5 Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Uraian Sponge ... 5
2.1.1Habitat ... 5
2.1.2Morfologi dan anatomi ... 5
2.1.3Klasifikasi ... 12
2.1.4Klasifikasi sponge... 13
2.2.1Alkaloid ... 13
2.2.2Glikosida ... 14
2.2.3Saponin ... 14
2.3.3 Steroid/triterpenoid ... 15
2.3 Ekstraksi ... 16
2.4 Kromatografi ... 17
2.4.1Kromatografi lapis tipis ... 18
2.4.2Kromatografi preparatif ... 19
2.5 Spektrofotometri ... 20
2.5.1Spektrofotometri sinar ultraviolet (UV) ... 20
2.5.3 Spektrofotometri sinar inframerah (IR) ... 20
BAB III METODE PENELITIAN... 21
3.1 Alat-alat yang digunakan... 21
3.2 Bahan-bahan yang digunakan ... 22
3.3 Pengumpulan dan Pengolahan Sponge ... 22
3.3.1 Pengumpulan sponge ... 22
3.3.2 Identifikasi sponge ... 22
3.3.3 Pengolahan sponge ... 22
3.4 Lokasi Penelitian ... 23
3.5 Pembuatan Larutan Pereaksi ... 23
3.5.1 Larutan pereaksi asam klorida 2 N ... 23
3.5.2Larutan pereaksi natrium klorida 2 N ... 23
3.5.4Larutan pereaksi Mayer ... 23
3.5.5Larutan pereaksi Dragendorff ... 23
3.5.6 Larutan pereaksi besi (III) klorida 1 % ... 24
3.5.7 Larutan pereaksi Libermann-Burchard ... 24
3.5.8 Larutan pereaksi Molish ... 24
3.5.9 Laruran air kloroform ... 24
3.5.10 Larutan kloralhidrat ... 24
3.5.11 Larutan pereaksi timbal (II) asetat 0,4 N ... 24
3.5.12 Larutan pereaksi asam sulfat 50% dalam metanol ... 24
3.5.13 Larutan asam nitrat 0,5 N ... 25
3.6 Pemeriksaan Karakteristik Simplisia ... 25
3.6.1 Pemeriksaan makroskopik... 25
3.6.2 Pemeriksaan mikroskopik ... 25
3.6.3 Penetapan kadar air ... 25
3.6.4 Penetapan kadar sari yang larut dalam air ... 26
3.6.5 Penetapan kadar sari yang larut dalam etanol ... 26
3.6.6 Penetapan kadar abu total ... 27
3.6.7 Penetapan kadar abu yang tidak larut dalam asam ... 27
3.7 Skrining Senyawa Kimia ... 27
3.7.1 Pemeriksaan alkaloida ... 28
3.7.2 Pemeriksaan flavonoid ... 28
3.7.3 Pemeriksaan saponin ... 28
3.7.4 Pemeriksaan tanin ... 29
3.7.6 Pemeriksaan antrakinon ... 29
3.7.7 Pemeriksaan steroid/triterpenoid ... 30
3.8Pembuatan Ekstrak ... 30
3.9 AnalisisEkstrak n-heksana Secara Kromatoografi KLT ... 30
3.10 IsolasiSenyawa Streroid/triterpenoid SecaraKromatografi Lapis Tipis Preparatif ... 31
3.11 Uji Kemurnian Terhadap Isolat ... 32
3.11.1 Uji KLT satu arah ... 32
3.11.2 Uji KLT dua arah ... 32
3.12 Karakterisasi Isolat ... 32
3.12.1 Karakterisasi isolat dengan spektrofotometri UV ... 33
3.12.2 Karakterisasi isolat dengan spektrofotometrI IR ... 33
BAB IV HASIL DAN PEMBAHASAN ... 34
4.1 Hasi dan Identifikasi Sponge ... 34
4.2 Hasil Pemeriksaan Kareteristik ... 34
4.3 Hasil Skrining Senyawa Kimia ... 35
4.4 Hasi Ekstraksi ... 36
4.5 Hasil Isoasi Senyawa Steroid/triterpenoidSecara KLT ... 37
4.6 Hasil Isolasi Senyawa Steroid/triterpenoid Secara KLT Preparatif ... 37
4.7 Hasil Uji Kemurnian Kromatografi Lapis Tipis Satu Arah . 37 4.8 Hasil Uji Kemurnia Kromatografi Lapis Tipis Dua Arah ... 38
4.9 Hasil KarakterisasiIsolat Dengan SpektrofotometriUltraviolet (UV) ... 39
BAB V KESIMPULAN DAN SARAN ... 40
5.1 Kesimpulan ... 40
5.2 Saran ... 40
DAFTAR PUSTAKA ... 41
DAFTAR TABEL
Tabel Halaman
4.1 Hasil karakterisasi simplisia dari sponge ... 35
4.2 Hasil skrining fitokimia dari simplisia Xeastospongia sp
de Laubenfels ... 36
DAFTAR GAMBAR
Gambar Halaman
2.1 Bagian organ sponge ... 7
2.2 Tipe morfologi sponge ... 8
2.3 Tipe spikula ... 9
2.4 Megasklera ... 10
2.5 Mikrosklera ... 10
2.6 Megaskleras monoaxone ... 11
2.7 Megasklera tetraxon ... 11
2.8 Struktur dasar steroid ... 15
DAFTAR LAMPIRAN
Lampiran Halaman
1 Identifikasi sampel ... 44
2 Gambar sponge Xestospongia sp de Laubenfels segar ... 45
3 Gambar sponge Xeatospongia sp de Laubenfels ... 46
4 Gambar makroskopik sponge ... 47
5 Gambar mikroskopik serbuk Simplisia ... 48
6 Bagan pembuatan ekstrak n-heksana sponge ... 49
7 Bagan perolehan isolat ... 50
8 Hasil analisis senyawa steroid/terpenoid secara KLT ... 51
9 Hasil isolasi senyawa steroi/triterpenoid secara KLT preparatif. 52 10 Hasil uji kemurnian KLT satu arah ... 53
11 Hasil uji kemurnia KLT dua arah ... 54
12 Perhitungan penetapan kadar ... 55
ISOLASI DAN IDENTIFIKASI STEROID/TRITERPENOID PADA SPONGE Xestospongia sp de Laubenfels DARI
PANTAI LHOK NGA ACEH BESAR yarat untuk memperolehgelar Sarjana
bABSTRAK
Sponge merupakan salah satu hewan invertebrata laut yang hidup pada terumbu karang yang mempunyai potensi bioaktif yang belum banyak dimanfaatkan dalam berbagai keperluan, terutama untuk obat-obatan. Senyawa metabolit sekunder yang terdapat dalam sponge adalah alkaloid, steroid/triterpenoid dan sesquiterpenoid. Senyawa steroid/triterpenoid digunakan dalam bidang pengobatan sebagai kardiotonik, prekursor vitamin D, kontrasepsi oral dan antiinflamasi. Steroid/triterpenoid merupakan kelompok penting dari produk alami yang memiliki profil farmakologi yang luas, diantaranya sebagai pengatur hormon, antioksidan, anti-asma, bronkodilator dan menormalkan darah Tujuan penelitian ini adalah untuk mengetahui karakterisasi simplisia, skrining fitokimia dan isolasi senyawa steroid/triterpenoid dari sponge Xestospongia sp de Laubenfels.
Ekstraksi dilakukan secara maserasi menggunakan pelarut adalah n-heksana, ekstrak diuapkan dan di analisis dengan kromatografi lapis tipis (KLT) dengan berbagai perbandingan pengembang, dilanjutkan isolasi menggunakan kromatografi lapis tipis (KLT) preparatif. Terhadap isolat yang diperoleh dilakukan uji kemurnian secara kromatografi lapis tipis 2 arah, selanjutnya di karakterisasi secara spektrofotometri ultraviolet (UV) dan spektrofotometri inframerah (IR).
Hasil karakterisasi simplisia Xestospongia adalah kadar air 6,00%, kadar sari yang larut dalam air 4,47%, kadar sari yang larut dalam etanol 5,43%, kadar abu total 10,13%, dan kadar abu tidak larut asam 7,07%. Hasil skrining fitokimia kimia diperoleh senyawa alkaloid, steroid/triterpenoid, glikosida dan saponin. Hasil isolasi diperoleh isolat harga Rf = 0,85 untuk fase (gerak 1) dan Rf 0,8 (fase gerak 2). Hasil analisis isolat secara spektrofotometri UV memberikan absorbansi maksimum pada panjang gelombang 203 nm dan hasil secara spektrofotometri IR menunjukkan adanya gugus fungsi –OH, CH-alifatis, C=C, CH3, C=O. Isolat yang diperoleh termasuk golongan senyawa steroid/triterpenoid.
ISOLATION OF STEROIDAL/TERPENOIDAL COMPOUNDS FROM OF SPONGE (Xeastospongia sp de Laubenfels) FROM LHOKNGA BEACH ACEH BESAR
bABSTRACT
Sponge is one of ocean invertebrate which lives on coral reef and it has Bioactive potential that has not been widely used in various occasion, especially in drugs. Secondary metabolite compound that can be isolated from sponge is Alkaloida from Xestospongia sp., Diterpenoida from Oceanapia sp., sesquiterpenoida from Dysidea herbaceae, isonitril and terpenoid from
Halicandria sp., and sesterterpenoid from Hyrtios erecta. Triterpenoid compound
can be used in various needs such as to treat diabetes, menstruation problem, snakebite, skin problems, livers, malaria, infection, Analgesic and cancer. The purpose of this research was to determine the simplex characterization, phytochemical screening and isolating the steroidal/triterpenoidal compound of
Xestospongia sp leaves
Extraction accomplished by maceration of dried powdered plant material with n-hexane, then the extract was fractionated preparative Thin Layer
Chromatography. The purity of isolates were confirmed by two-dimensional Thin Layer Cromatography and the pure isolate was characterized with ultraviolet and infrared spectrophotometric methods.
The result of simplex characterization gave water content 6.00%, water-soluble extract 4.47%, ethanol-water-soluble extract 5.43%, total ash 10.13%, and acid-insoluble ash 7.077%. The result of phytochemical screening of Xestospongia sp leaves gave positive results for the presence of flavonoid, steroid/triterpenoid, glycoside and saponin. Three pure isolates were obtained, with Rf = 0,8, the measurement of uv spectrum gave maximum absorption at 203 nm. The result of infrared spectrophotometric measurement indicated the presence of –OH, CH, C=C, C-H3, C-O functional groups. The isolates were inferred as steroid/triterpenoid compounds.
BAB I
PENDAHULUAN
1.1Latar Belakang
Indonesia merupakan negara kepulauan yang memiliki sumber daya alam
hayati laut yang besar. Salah satu sumber daya alam tersebut adalah terumbu
karang yang merupakan bagian dari ekosistem laut, dan merupakan sumber
kehidupan bagi beranekaragam biota laut. Ekosistem terumbu karang hidup
beribu-ribu jenis karang, beratus-ratus jenis ikan dan berpuluh-puluh jenis
Molusca, Crustaceae, Sponge, Alga dan biota lainnya (Amir dan Budiyanto,
1996).
Sponge merupakan salah satu hewan invertebrata laut yang hidup pada
terumbu karang yang mempunyai potensi bioaktif yang belum banyak
dimanfaatkan dalam berbagai keperluan, terutama obat-obatan. Sponge laut
tergolong kedalam Filum Porifera yang merupakan hewan multiseluler paling
sederhana dengan bentuk tubuh dan warna yang beraneka ragam (Handayani,
dkk., 2009). Penelusuran pustaka diketahui bahwa hewan laut ini mengandung
senyawa kimia dengan bioaktivitas yang beraneka ragam antara lain:
Discodermolide yang memiliki aktivitas antikanker, Manoalide yang memiliki
aktivitas antiinflamasi, Manzamine-A yang memiliki aktivitas sitotoksik (Hillisch,
2002), Spongouridin yang memiliki aktivitas antivirus dan Taraxeron yang
memiliki aktivitas antibakteri (Handayani, dkk., 2009). Senyawa metabolit
sekunder yang berhasil diisolasi dari sponge yaitu alkaloida dari Xestospongia sp.,
dan terpenoid dari Halicandria sp. dan seskuiterpenoid dari Hyrtios erecta (Crews
dan Hunter, 1993).
Steroid/triterpenoid memiliki aktivitas biologi antara lain untuk
peningkatan ataupun pengendalian reproduksi pada manusia contohnya estradiol,
progesteron dan testosteron. Senyawa steroid/triterpenoid digunakan dalam
bidang pengobatan sebagai kardiotonik, prekursor vitamin D, kontrasepsi oral dan
antiinflamasi (Tyler, 1984). Steroid/triterpenoid merupakan kelompok penting
dari produk alami yang memiliki profil farmakologi yang luas, diantaranya
sebagai pengatur hormon, antioksidan, anti-asma, bronkodilator dan menormalkan
tekanan darah (Okwu, 2010).
Berdasarkan uraian diatas penulis telah melakukan penelitian meliputi
karakterisasi simplisia, skrining fitokimia, analisis kromatografi lapis tipis (KLT)
serta isolat senyawa yang diperoleh di karakterisasi secara spektrofotometri
ultraviolet (UV) dan spektrofotometri infrared (IR).
1.2 Perumusan Masalah
Berdasarkan uraian dari latar belakang penelitian di atas, perumusan
masalahnya sebagai berikut:
a. Apakah karakterisasi simplisia sponge Xestospongia sp de Laubenfels
memenuhi persyaratan mutu simplisia?
b. Apakah golongan senyawa kimia yang terkandung sponge Xestospongia sp de
Laubenfels?
c. Apakah senyawa steroid/triterpenoid dari sponge Xestospongia sp de
Laubenfels dapat diisolasi dan isolat yang diperoleh dapat diidentifikasi secara
1.3 Hipotesis
Berdasarkan perumusan masalah diatas, maka hipotesis dari penelitian ini
sebagai berikut:
a. Karakterisasi simplisia sponge Xestospongia sp de Laubenfels memenuhi
persyaratan mutu simplisia
b. Golongan senyawa kimia dari sponge Xestospongia sp de Laubenfels adalah
alkaloid, steroid/triterpenoid, glikosida dan saponin.
c. Senyawa steroid/triterpenoid dari sponge Xestospongia sp de Laubenfels
dapat diisolasi dan isolat yang diperoleh dapat diidentifikasi dengan
spektrofotometri ultraviolet (UV) dan spektrofotometri infrared (IR).
1.4 Tujuan Penelitian
Tujuan penelitian ini adalah:
a. Untuk mengetahui karakterisasi simplisia sponge (Xestospongia sp de
Laubenfels) .
b. Untuk mengetahui golongan senyawa kimia yang terdapat didalam sponge
(Xestospongia sp de Laubenfels) .
c. Untuk mengetahui isolat yang terdapat didalam sponge (Xestospongia sp de
Laubenfels) dan mengidentifikasi isolatnya dengan spektrofotometri
1.5 Manfaat Penelitian
Manfaat penelitian ini adalah untuk menambah informasi tentang
steroid/triterpenoid pada biota laut yang diperoleh dari sponge Xestospongia sp
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Sponge
2.1.1 Habitat
Habitat sponge terdapat pada daerah jernih dan menempel pada permukaan
substrat. Sponge Xestospongia sp merupakan salah satu jenis sponge yang banyak
terdapat di perairan Indonesia (Krisyunida, 2011). Habitat sponge yang melekat
pada pasir atau bebatuan menyebabkan hewan ini sulit untuk bergerak, untuk
mempertahankan diri dari serangan predator dan infeksi bakteri patogen, sponge
mengembangkan sistem “biodefense” yaitu dengan menghasilkan zat racun dari
tubuhnya, zat ini umumnya yang dimanfaatkan sebagai bahan farmasi (Murniasih,
2003). Porifera yang sudah teridentifikasi ada 10.000 spesies, sebagian besar
hidup dilaut dan hanya 159 spesies hidup di air tawar, semuanya termasuk famili
Spongilidae. Umumnya sponge terdapat di perairan jernih dangkal dan menempel
di substrat, beberapa menetap didasar perairan berpasir atau berlumpur
(Suwignyo, dkk., 2005).
2.1.2 Morfologi dan anatomi
Morfologi luar sponge laut sangat dipengaruhi oleh faktor fisik, kimiawi
dan biologis lingkungannya. Spesimen yang berada dilingkungan yang terbuka
dan berombak besar cenderung pendek pertumbuhannya atau juga merambat.
Sebaliknya spesimen dari jenis yang sama pada lingkungan yang terlindung atau
pada perairan yang lebih dalam dan beruas terang, pertumbuhannya cenderung
tegak dan tinggi. Perairan yang lebih dalam sponge cenderung memiliki tubuh
yang lebih stabil apabila dibandingkan dengan jenis yang sama yang hidup pada
perairan yang dangkal (Suparno, 2005). Sponge adalah biota multiseluler primitif
yang bersifat filter feeder menghisap air dan bahan-bahan lain di sekelilingnya
melalui pori-pori kemudian dialirkan ke seluruh bagian tubuhnya melalui kanal
dan dikeluarkan melalui pori-pori yang terbuka (ostula/osculum) (Vacelet, 2008).
Hewan ini dapat hidup dengan baik pada arus air yang kuat, karena aliran
air “filter feeder” menyediakan kumpulan makanannya dan oksigen. Makanan
sponge terdiri dari detritus organik seperti bakteri, zooplankton dan phytoplankton
yang kecil-kecil yang mana secara efektif ditangkap oleh sel-sel berbulu
cambuknya. Sponge dapat menyaring partikel yang sangat kecil (diameter <
50μm) yang tidak tersaring oleh hewan-hewan laut lainnya (Amir dan Budiyanto,
1996).
Sponge memiliki warna yang berbeda walaupun dalam satu jenis,
beberapa sponge juga memiliki warna dalam tubuh yang berbeda dengan
pigmentasi luar tubuhnya. Sponge yang hidup di lingkungan yang gelap akan
berbeda warnanya dengan sponge sejenis yang hidup pada lingkungan yang cerah.
Warna sponge tersebut sebagian dipengaruhi oleh fotosintesa mikrosimbionnya
(misalnya berwarna ungu dan merah jambu). Mikrosimbion sponge umumnya
adalah cyanophita (cyanobacteria dan eukariot alga seperti dinoflagella atau
zooxanthella) (Amir dan Budiyanto, 1996). Ukuran tubuh porifera sangat
bervariasi dari sebesar kacang polong sampai 90 cm, bentuk tubuh sponge juga
bermacam-macam, beberapa simetri radikal, tetapi kebanyakan berbentuk tidak
Pada dasarnya dinding tubuh porifera terdiri atas tiga lapisan, (Suwignyo, dkk.,
2005) yaitu:
a) Pinococyte atau Pinacoderm, seperti epidermis berfungsi untuk melindungi
tubuh bagian dalam. Bagian sel pinacocyte dapat berkontraksi atau berkerut,
sehingga seluruh tubuh hewan dapat sedikit membesar atau mengecil.
b) Mesohyl atau Mesoglea, terdiri dari zat semacam agar, mengandung bahan
tulang dan sel amebocyte yang mempunyai banyak fungsi, antara lain untuk
pengangkut dan cadangan makanan, membuang partikel sisa metabolisme,
membuat spikula, serat sponge dan membuat sel reproduktif.
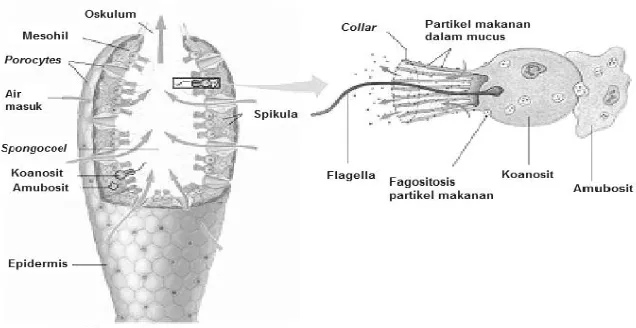
c) Choanocyte, yang melapisi rongga atrium atau spongocoel. Bentuk choanocyte
agak lonjong, ujung yang satu melekat pada mesohyl dan ujung yang lain
berada di spongocoel serta dilengkapi sebuah flagelum yang dikelilingi
kelopak dari fibril. Getaran flagel pada lapisan choanocyte menghasilkan arus
air di dalam spongocoel ke arah osculum, sedangkan fibril berfungsi sebagai
alat penangkap makanan. Gambar organ sponge dapat dilihat pada Gambar 2.1
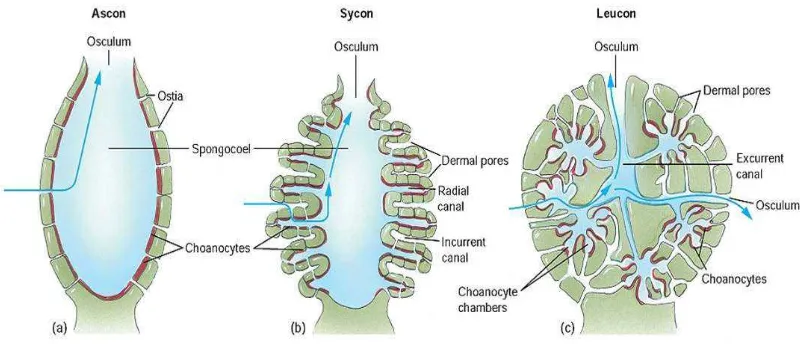
Berdasarkan sistem aliran air (bukan secara taksonomi), bentuk tubuh
porifera dibagi menjadi tiga tipe, (Suwignyo, dkk., 2005) yaitu:
1. Asconoid
Asconoid merupakan bentuk yang paling primitif, menyerupai vas bunga
atau jambangan kecil. Pori-pori atau lubang merupakan saluran pada sel porocyte
yang berbentuk tabung, memanjang dari permukaan tubuh sampai spongocoel
2. Syconoid
Sponge memperlihatkan lipatan-lipatan dinding tubuh secara horizontal,
sehingga potongan melintangnya seperti jari-jari
3. Leuconoid
Tingkat pelipatan dinding spongocoel paling tinggi terdapat pada
leuconoid. Gambar tipe morfologi sponge dapat dilihat pada Gambar 2.2.
Gambar 2.2. Tipe morfologi sponge
Sumber : (Haris, dkk., 2012)
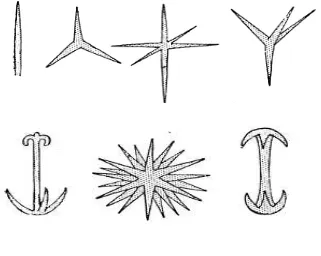
Spikula ibarat ‘rangka’ bagi tubuh sponge. Tulang yang berukuran kecil
dan tajam, dapat dilihat dengan mata telanjang dan mikroskop. Tubuh sponge
yang lunak dapat berdiri karena ditunjang oleh sejumlah besar spikula serta serat
organik yang berfungsi sebagai kerangka. Spikula kapur dari CaCO3 dan spikula
silikat H2SiO7. Bentuk spikula bermacam–macam, sehingga dipakai sebagai
indikator untuk identifikasi. Gambar tipe spikula dapat dilihat pada gambar 2.3
Gambar 2.3. Tipe spikula Sumber : Vacelet, 2008
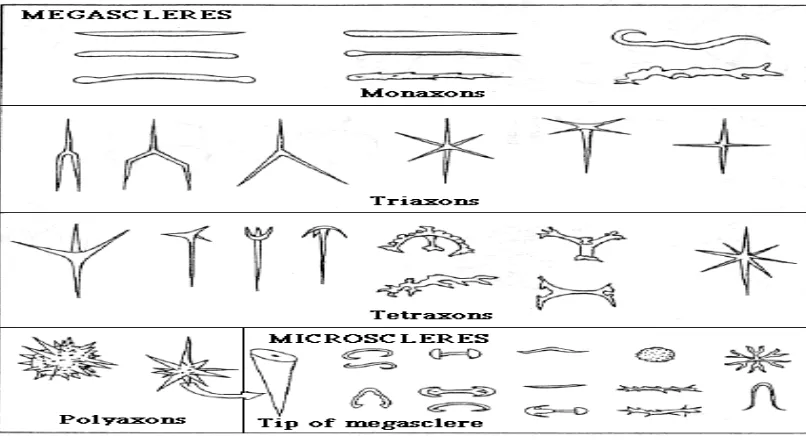
Megasklera adalah komponen dari kerangka primer yang berperan untuk
membentuk sponge dan perkembangan sub struktur internal. Mikrosklera tidak
berfungsi seperti peranan megasklera, tetapi membentuk kelompok antara
kumpulan megasklera atau tersebar pada permukaan atau membran internal.
Ukuran, bentuk dan susunan dari masing-masing spikula yang dikandung oleh
Budiyanto, 1996). Gambar megasklera dapat dilihat pada gambar 2.4 dan gambar
mikrosklera dapat dilihat pada Gambar 2.5
Gambar 2.4. Megasklera Sumber : Haris, dkk., 2012.
Gambar 2.5 Mikrosklera (Haris, et al., 2012). Sumber : Haris, dkk., 2012
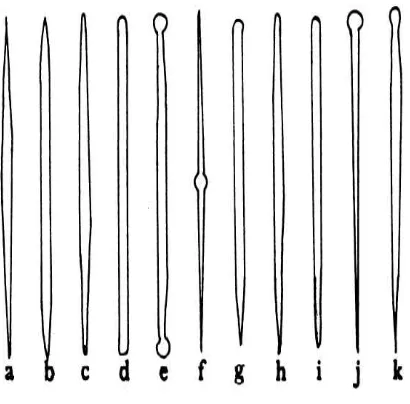
Tipe megasklera dapat dibagi menjadi monoaxons, triaxons, tetraxons dan
mempuyai tiga percabangan. Tetraxon berbentuk empat percabangan. Polyaxon
berbentuk banyak percabangan memijar dari satu pusat.
Gambar megasklera monoaxon dapat dilihat pada Gambar 2.6 dan Gambar
2.7.
Gambar 2.6 Megasklera monoaxon Sumber : (Walker, 1932)
Keterangan: a. fusiform oxea, b. Hastate oxea, c. Strongyloxea, d. Strongyle, e. Tylote, f. Centrotylote oxea, g. Hastate style, h. Fusiform style, i. Styloid, j. Tylostyle, k. Subtylostyle.
.
Gambar 2.7 Megasklera Tetraxon (triaene) Sumber : Walker, 1932
Hewan avertebrata laut lainnya seperti pada karang, sponge juga tidak
memiliki ciri seksual sekunder yang dapat digunakan untuk menentukan jenis
seksualitasnya oleh karena itu, satu-satunya cara yang dapat dilakukan untuk
pengamatan tersebut adalah pengamatan histologik pada jaringannya. Seksualitas
pada sponge dapat dikelompokkan atas dua yaitu:
1) Hermaprodit, yaitu jenis sponge yang menghasilkan baik gamet jantan atau
betina selama hidupnya, tetapi menghasilkan telur dan sperma dalam waktu
yang berbeda.
2) Gonokhorik, yaitu jenis sponge yang memproduksi hanya gamet jantan atau
betina saja selama hidupnya (Haris, dkk., 2012).
2.1.3 Klasifikasi
Filum Porifera yang dibagi dalam 3 kelas (Amir dan Budiyanto, 1996):
1. Kelas Hexactinellida
Hexactinellida merupakan sponge gelas dengan spikula yang terdiri dari
silikat dan tidak mengandung spongin. Spikulanya berbentuk bidang "triaxon",
dimana masing-masing bidang terdapat dua jari-jari. Sponge dari kelas ini belum
banyak dikenal, karena sulit mendapatkan dan hanya terdapat di laut dalam (< 500
meter).
2. Kelas Calcarea
Spikula sponge ini tersusun dari kalsium karbonat dan tidak mengandung
spongin. Sebagian besar sponge dari kelas ini bentuknya kecil-kecil dan berwarna
putih keabu-abuan dan ada beberapa jenis berwana kuning, pink, atau hijau.
Elemen kerangka dari kelas Calcarea berbentuk spikula "triaxon" dan tidak ada
umum adalah Sycon gelatinosum (berbentuk silinder berwarna coklat muda),
Clathrina sp. dan Leucetta sp.
3. Kelas Demospongiae
Hampir 75% jenis sponge yang dijumpai di laut adalah dari kelas
Demospongiae. Sponge dari kelas ini tidak memiliki spikula "triaxon" (spikula
kelas Hexactinellidae). Beberapa jenis sponge kelas ini ada yang tidak
mengandung spikula tetapi hanya mengandung serat-serat kolagen atau spongin
saja.
2.1.4 Klasifikasi sponge
Klasifikasi hewan sponge menurut ITS (2014) dan Walker (1932) adalah
sebagai berikut:
Kingdom : Animalia
Filum : Porifera
Kelas : Demospongiae
Ordo : Haploscleridae
Sub ordo : Petrosina
Famili : Petrosidae
Genus : Xestospongia
Spesies : Xestospongia sp de Laubenfels
2.2 Kandungan Kimia
2.2.1 Alkaloid
Alkaloida merupakan golongan zat sekunder yang terbesar. Alkaloida
biasanya sebagai bagian dari sistem siklik. Alkaloida mempunyai aktivitas
fisiologi yang menonjol, sehingga banyak diantaranya digunakan dalam bidang
pengobatan (Harborne, 1987).
2.2.2 Glikosida
Glikosida adalah suatu golongan senyawa bila dihidrolisis akan terurai
menjadi gula (glikon) dan senyawa lain (aglikon atau genin). Umumnya glikosida
mudah terhidrolisis oleh asam mineral atau enzim. Hidrolisis oleh asam
memerlukan panas, sedangkan hidrolisis oleh enzim tidak memerlukan panas
(Sirait, 2007).
Berdasarkan ikatan antara glikon dan aglikon, glikosida dapat dibedakan
menjadi:
a. Tipe O-glikosida, ikatan antara bagian glikon dengan aglikon melalui jembatan
O. Mayoritas glikosida termasuk ke dalam kelompok ini.
b. Tipe C-glikosida, ikatan antara bagian glikon dengan aglikon melalui jembatan
C, yakni gula melekat pada aglikon melalui ikatan karbon-karbon.
c. Tipe S-glikosida, ikatan antara bagian glikon dengan aglikon melalui jembatan
S. Contoh: sinigrin yang termasuk ke dalam glikosida glukosinolat dari
tumbuhan dari tumbuhan Brassicaceae.
d. Tipe N-glikosida, ikatan antara bagian dari glikon dengan aglikon melalui
jembatan N. Contoh: nikleosidin, kronotosidin.
2.2.3 Saponin
Saponin tersebar luas diantara tanaman tingkat tinggi. Saponin merupakan
senyawa berasa pahit, menusuk, menyebabkan bersin dan mengakibatkan iritasi
yang menyerupai sabun (bahasa Latin sapo berarti sabun). Saponin adalah
senyawa aktif permukaan yang kuat dan menimbulkan busa jika dikocok dalam
air dan pada konsentrasi yang rendah sering menyebabkan hemolisis sel darah
merah. Saponin sangat beracun dalam larutan yang sangat encer, untuk ikan dan
tumbuhan yang mengandung saponin telah digunakan oleh penduduk sebagai
racun ikan selama beratus-ratus tahun. Beberapa saponin bekerja sebagai
antimikroba (Robinson, 1995).
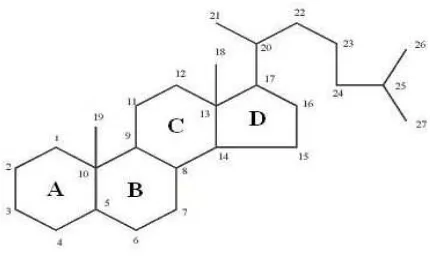
2.2.4 Steroid/triterpenoid
Steroid adalah triterpena yang kerangka dasarnya sistem cincin
siklopentana perhidropenantren (Harbone, 1987). Triterpenoid adalah senyawa
yang kerangka karbonnya berasal dari enam satuan isoprena dan secara biosintesis
masuk jalur asam mevalonat yang diturunkan dari hidrokarbon C30 asiklik, yaitu
skualena. Uji yang banyak digunakan ialah reaksi Liebermann-Burchard yang
dengan kebanyakan triterpen dan sterol memberikan warna hijau-biru (Harborne,
1987). Steroid pada umumnya berupa alkohol dengan gugus hidroksil pada C3
sehingga steroid sering juga disebut sterol (Robinson, 1995). Gambar struktur
[image:32.595.203.418.565.693.2]dasar dapat dilihat pada Gambar 2.8.
2.3 Ekstraksi
Ekstraksi adalah penyarian komponen aktif dari suatu jaringan tumbuhan
atau hewan dengan menggunakan pelarut yang cocok (Handa, 2008). Beberapa
metode ekstraksi dengan menggunakan pelarut (Depkes, 2000) yaitu:
A. Cara dingin
1. Maserasi
Maserasi adalah proses pengekstrakan simplisia dengan menggunakan
pelarut dengan beberapa kali pengocokan atau pengadukan pada temperatur
kamar. Maserasi kinetik berarti dilakukan pengadukan yang kontinu (terus
menerus). Remaserasi berarti dilakukan penyaringan berulang dan seterusnya
2. Perkolasi
Perkolasi adalah proses penyarian simplisia dengan pelarut yang selalu
baru sampai sempurna yang umumnya dilakukan pada temperatur ruangan. Proses
perkolasi terdiri dari tahap pengembangan bahan, tahap maserasi antara, tahap
perkolasi sebenarnya (penetesan/penampungan ekstrak), terus menerus sampai
diperoleh ekstrak (perkolat) yang jumlahnya 1–5 kali bahan Cara panas
3. Refluks
Refluks adalah ekstraksi dengan menggunakan pelarut pada temperatur
titik didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang relatif
konstan dengan adanya pendingin balik.
4. Digesti
Digesti adalah maserasi kinetik (dengan pengadukan kontinu) pada
temperatur lebih tinggi dari temperatur ruangan (kamar), yaitu secara umum
5. Sokletasi
Sokletasi adalah proses penyarian dengan menggunakan alat soklet dengan
pelarut yang selalu baru sehingga terjadi ekstraksi kontinu dengan jumlah pelarut
yang relatif konstan dengan adanya pendingin balik.
6. Infus
Infus adalah ekstraksi dengan pelarut air pada temperatur penangas air
(bejana infus tercelup dalam penangas mendidih, temperatur terukur 96–98oC)
selama waktu tertentu (15–20 menit).
7. Dekok
Dekoktasi adalah infus pada waktu yang lebih lama (≥ 30 menit) dan
temperatur sampai titik didih air
2.4 Kromatografi
Kromatografi adalah suatu metode pemisahan berdasarkan perbedaan
perpindahan dari komponen-komponen senyawa di antara dua fase yaitu fase
diam (dapat berupa zat cair atau zat padat) dan fase gerak (dapat berupa gas atau
zat cair). Kromatografi serapan dikenal jika fase diam berupa zat, jika zat cair
dikenal sebagai kromatografi partisi (Sastrohamidjojo, 1985).
1. Fase gerak zat cair–fase diam padat:
- Kromatografi lapis tipis
- Kromatografi penukar ion
2. Fase gerak gas–fase diam padat:
- Kromatografi gas padat
- Kromatografi cair kinerja tinggi
4. Fase gerak gas–fase diam zat cair:
- Kromatografi gas cair
- Kromatografi kolom kapiler
Pemisahan dan pemurnian kandungan tumbuhan dilakukan dengan
menggunakan salah satu atau gabungan dari beberapa teknik tersebut dan dapat
digunakan pada skala mikro maupun makro (Harborne, 1987).
2.4.1 Kromatografi lapis tipis
Kromatografi lapis tipis ialah metode pemisahan fisikokimia. Lapisan
pemisah terdiri atas bahan berbutir-butir (fase diam), ditempatkan pada penyangga
berupa plat gelas, logam atau lapisan yang cocok. Campuran yang akan dipisah
berupa larutan yang di totolkan baik berupa bercak ataupun pita. Plat atau lapisan
dimasukkan ke dalam bejana tertutup rapat yang berisi larutan pengembang yang
cocok (fase gerak), pemisahan terjadi selama perambatan kapiler (pengembangan)
(Stahl, 1985). Fase gerak akan bergerak sepanjang fase diam karena pengaruh
kapiler pada pengembangan secara menaik (ascending) atau karena pengaruh
gravitasi pada pengembangan secara menurun (descending) (Rohman, 2007).
Pendeteksian bercak hasil pemisahan dapat dilakukan dengan beberapa
cara. Pengamatan dengan sinar ultraviolet adalah cara sederhana yang dilakukan
untuk senyawa tak berwarna. Beberapa senyawa organik bersinar atau
berfluorosensi jika disinari dengan sinar ultraviolet gelombang pendek (254 nm)
atau gelombang panjang (366 nm). Jika dengan cara itu senyawa tidak dapat
bercak tersebut tampak yaitu pertama tanpa pemanasan, kemudian bila perlu
dengan pemanasan (Rohman, 2007).
2.4.2 Kromatografi preparatif
Kromatografi lapis tipis (KLT) preparatif merupakan salah satu metode
pemisahan dengan menggunakan peralatan sederhana. Ketebalan penjerap yang
sering dipakai adalah 0,5-2 mm. Plat kromatografi biasanya berukuran 20 x 20
cm. Pembatasan ketebalan lapisan dan ukuran plat sudah tentu mengurangi jumlah
bahan yang dapat dipisahkan dengan KLT preparatif. Penjerap yang paling umum
digunakan adalah silika gel. Penotolan cuplikan dilakukan dengan melarutkan
cuplikan dalam sedikit pelarut. Cuplikan ditotolkan berupa pita dengan jarak
sesempit mungkin karena pemisahan tergantung pada lebar pita. Penotolan dapat
dilakukan dengan pipet tetapi lebih baik dengan penotol otomatis. Pengembangan
plat KLT preparatif dilakukan dalam bejana kaca yang dapat menampung
beberapa plat. Bejana dijaga tetap jenuh dengan pelarut pengembang dengan
bantuan kertas saring yang diletakkan berdiri disekeliling permukaan bagian
dalam bejana (Hostettmann, et al., 1995).
2.5 Spektrofotometri
2.5.1 Spektrofotometri sinar ultraviolet (UV)
Spektrum ultraviolet adalah suatu gambaran yang menyatakan hubungan
antara panjang gelombang atau frekuensi sinar UV terhadap intensitas serapan
(absorbansi). Sinar ultraviolet mempunyai panjang gelombang antara 200-400 nm.
Serapan cahaya oleh molekul dalam daerah spektrum ultraviolet tergantung pada
Suatu atom atau molekul menyerap sinar UV maka energi tersebut akan
menyebabkan tereksitasinya elektron pada kulit terluar ke tingkat energi yang
lebih tinggi. Tipe eksitasi tergantung panjang gelombang cahaya yang diserap.
Gugus kromofor disebut juga gugus yang dapat mengabsorpsi cahaya
(Dachriyanus, 2004).
2.5.2 Spektrofotometri sinar inframerah (IR)
Spektrofotometri inframerah pada umumnya digunakan untuk:
1. Menentukan gugus fungsi suatu senyawa organik
2. Mengetahui informasi struktur suatu senyawa organik dengan membandingkan
daerah sidik jarinya.
Pengukuran pada spektrum infrared dilakukan pada daerah cahaya infrared
tengah (mid-infrared) yaitu pada panjang gelombang 2.5–50 �m atau bilangan
gelombang 4000–200 cm-1. Energi yang dihasilkan oleh radiasi ini akan
menyebabkan vibrasi atau getaran pada molekul. Pita absorpsi sinar infrared
sangat khas dan spesifik untuk setiap tipe ikatan kimia atau gugus fungsi
(Dachriyanus, 2004).
Jenis absorpsi energi yang lain, molekul-molekul dieksitasikan ke tingkat
energi yang lebih tinggi ketika molekul-molekul ini menyerap radiasi infrared.
Hanya frekuensi (energi) tertentu dari radiasi infrared yang dapat diserap oleh
suatu molekul, agar molekul dapat menyerap radiasi infrared, maka molekul
tersebut harus mempunyai gambaran spesifik, yakni momen dipol molekul harus
BAB III
METODE PENELITIAN
Metode yang digunakan adalah metode deskriptif meliputi pengumpulan
dan pengolahan sponge, pemeriksaan karakteristik, pembuatan ekstrak, analisis
senyawa metabolit sekunder secara kromatografi lapis tipis (KLT) dan
kromatrografi lapis tipis preparatif. Terhadap isolat yang diperoleh dilakukan uji
kemurnian LKT satu arah dan KLT dua arah, dilanjutkan dengan karekterisasi
secara UV dan IR
3.1 Alat-alat yang digunakan
Alat-alat yang digunakan dalam penelitian ini adalah tanur (Nabertherm),
seperangkat alat destilasi, seperangkat alat penetapan kadar air, oven listrik
(Stork), mikroskop (Olympus), eksikator, neraca analitik (Vibra AJ), penangas
air, lemari pengering dan alat-alat gelas Laboratorium.
3.2 Bahan-bahan yang digunakan
Bahan-bahan yang digunakan pada penelitian ini adalah sponge dan air
suling dan bahan-bahan kimia yang digunakan kecuali dinyatakan lain berkualitas
pro analisis yaitu etil asetat, asam asetat anhidrida, asam sulfat pekat, kloroform,
toluen, timbal (II) asetat, amil alkohol, metanol, natrium hidroksida, asam klorida
pekat, serbuk magnesium, serbuk seng, kloralhidrat, isopropanol, natrium sulfat
anhidrida, α-naftol, amonia pekat, besi (III) klorida, iodium, raksa (II) klorida,
kalium iodida, bismut (III) nitrat dan asam nitrat pekat, n-heksana (destilasi),
3.3 Pengumpulan dan Pengolahan Sponge
3.3.1 Pengumpulan sponge
Pengumpulan sponge dilakukan dengan cara purposif yaitu tanpa
membandingkan dengan hewan serupa dari daerah lain. Sponge yang digunakan
adalah Sponge jenis Xestospongia sp de Laubenfels yang diambil dari Pantai
Lhoknga Aceh Besar. Gambar sponge Xestospongia sp de Laubenfels segar dapat
dilihat pada Lampiran 2 halaman 46.
3.3.2 Identifikasi sponge
Identifikasi sponge di Laboratorium Ekologi Prodi Biologi FMIPA-Institut
Teknologi Sepuluh November (ITS) Surabaya. Hasil dilihat pada Lampiran 1
halaman 45.
3.3.3 Pengolahan sponge
Sponge yang telah dikumpulkan, didisortasi basah yaitu memisahkan
sponge dari kotoran-kotoran atau bahan asing lainnya, kemudian sponge yang
telah terkumpul dicuci untuk menghilangkan pengotor yang melekat. Pencucian
dilakukan dengan air mengalir, ditiriskan, dikeringkan dengan cara
diangin-anginkan (terlindung dari sinar matahari langsung) lalu ditimbang (berat basah).
Dikecilkan ukuranya, kemudian dimasukkan ke dalam lemari pengering dengan
suhu 40-50oC. Simplisia yang telah kering disortasi kering yaitu memisahkan
benda-benda asing seperti pengotoran-pengotoran lain yang terjadi selama
pengeringan. Simplisia ditimbang (berat kering), kemudian diserbuk dengan
menggunakan blender. Serbuk simplisia disimpan dalam kantung plastik untuk
mencegah pengaruh lembab dan pengotoran lainnya. Gambar serbuk sponge
3.4 Lokasi Penelitian
Penelitian dilakukan di Laboratorium Fitokimia Fakultas Farmasi
Unversitas Sumatera Utara Medan.
3.5 Pembuatan Larutan Pereaksi
3.5.1 Larutan pereaksi asam klorida 2 N
Sebanyak 17 ml asam klorida pekat diencerkan dengan air suling hingga
100 ml (Ditjen POM, 1979).
3.5.2 Larutan pereaksi natrium hidroksida 2 N
Sebanyak 8,002 g natrium hidroksida dilarutkan dalam air suling bebas
karbondioksida hingga 100 ml (Ditjen POM, 1979).
3.5.3 Larutan pereaksi Bouchardat
Sebanyak 4 g kalium iodida ditimbang, kemudian dilarutkan dalam air
suling, ditambahkan iodium sebanyak 2 g dan dicukupkan dengan air suling
hingga 100 ml (Ditjen POM, 1979).
3.5.4 Larutan pereaksi Mayer
Larutan raksa (II) klorida P 2,27% b/v sebanyak 60 ml dicampur dengan
10 ml larutan kalium iodida P 50% b/v, kemudian ditambahkan air secukupnya
hingga 100 ml (Ditjen POM, 1979).
3.5.5 Larutan pereaksi Dragendorff
Larutan bismut nitrat P 40% b/v dalam asam nitrat P sebanyak 20 ml
dicampur dengan 50 ml kalium iodida P 54,4% b/v, didiamkan sampai memisah
sempurna. Lalu diambil lapisan jernih dan diencerkan dengan air secukupnya
3.5.6 Larutan pereaksi besi (III) klorida 1%
Sebanyak 1 g besi (III) klorida dilarutkan dalam air suling hingga 100 ml
(Ditjen POM, 1979).
3.5.7 Larutan pereaksi Liebermann-Burchard
Sebanyak 20 bagian asam asetat anhidrat dicampurkan dengan 1 bagian
asam sulfat pekat. Larutan penyemprotnya dibuat dengan 20 bagian asam asetat
anhidrida dengan 1 bagian asam sulfat pekat dan 50 bagian kloroform. Larutan
penyemprot ini harus dibuat baru (Harborne, 1987).
3.5.8 Larutan pereaksi Molisch
Sebanyak 3 g α-naftol dilarutkan dalam asam nitrat 0,5 N hingga diperoleh
volume 100 ml (Ditjen POM, 1979).
3.5.9 Larutan air kloroform
Sebanyak 2,5 ml kloroform dikocok dengan 900 ml air suling, encerkan
dengan air suling hingga 1000 ml (Ditjen POM, 1995).
3.5.10 Larutan kloralhidrat
Sebanyak 50 gram kloralhidrat ditimbang dan dilarutkan dalam 20 ml air
suling (Ditjen POM, 1979).
3.5.11 Larutan pereaksi timbal (II) asetat 0,4 N
Sebanyak 15,17 gram timbal (II) asetat dilarutkan dalam air suling bebas
karbondioksida secukupnya hingga 100 ml (Ditjen POM, 1979).
3.5.12 Pereaksi asam sulfat 50% dalam metanol
Sebanyak 5 ml asam sulfat pekat ditambahkan hati-hati kepada 5 ml
3.5.13 Pereaksi asam nitrat 0,5 N
Sebanyak 3,4 ml asam nitrat pekat diencerkan dengan air suling hingga
volume 100 ml (Ditjen POM, 1979).
3.6 Pemeriksaan Karakteristik Simplisia
Pemeriksaan karakteristik simplisia meliputi pemeriksaan makroskopik
dan mikroskopik, penetapan kadar air, penetapan kadar sari yang larut dalam air,
penetapan kadar sari yang larut dalam etanol, penetapan kadar abu total, dan
penetapan kadar abu yang tidak larut dalam asam.
3.6.1 Pemeriksaan makroskopik
Pemeriksaan makroskopik dilakukan dengan mengamati bentuk, warna,
dan bau. Hasil dilihat pada Lampiran 4 halaman 48.
3.6.2 Pemeriksaan mikroskopik
Pemeriksaan mikroskopik dilakukan terhadap serbuk simplisia dengan
cara menaburkan serbuk simplisia di atas kaca objek yang telah ditetesi dengan
kloralhidrat dan ditutupi dengan cover glass (kaca penutup) kemudian dilihat di
bawah mikroskop. Hasil dilihat pada Lampiran 5 halaman 49.
3.6.3 Penetapan kadar air
Penetapan kadar air dilakukan dengan metode Azeotropi (destilasi toluen)
(Depkes, 1995).
Cara kerja :
Sebanyak 200 ml toluen dan 2 ml air suling dimasukkan ke dalam labu
alas bulat, didestilasi selama 2 jam. Kemudian toluen didinginkan selama 30
menit dan volume air pada tabung penerima dibaca dengan 0,05 ml.
2. Penetapan kadar air simplisia
Sebanyak 5 g serbuk simplisia yang telah ditimbang seksama dimasukkan
ke dalam labu yang berisi toluen tersebut, lalu dipanaskan hati-hati selama 15
menit. Setelah toluen mendidih, kecepatan tetesan diatur lebih kurang 2 tetesan
perdetik, sampai sebagian air terdestilasi, kemudian kecepatan destilasi dinaikkan
hingga 4 tetes perdetik. Setelah semua air terdestilasi, bagian dalam pendingin
dibilas dengan toluen. Destilasi dilanjutkan selama 5 menit, kemudian tabung
penerima dibiarkan dingin sampai suhu kamar. Setelah air dan toluen memisah
sempurna, volume air dibaca dengan ketelitian 0,05 ml. Selisih kedua volume air
dibaca sesuai dengan kandungan air yang terdapat dalam bahan yang diperiksa.
3.6.4 Penetapan kadar sari yang larut dalam air
Sebanyak 5 g serbuk yang telah dikeringkan di udara dimaserasi selama 24
jam dengan 100 ml air-kloroform dalam labu bersumbat sambil berkali-kali
dikocok selama 6 jam pertama kemudian dibiarkan selama 18 jam lalu disaring.
Sejumlah 20 ml filtrat diuapkan hingga kering dalam cawan penguap berdasar rata
yang telah ditara. Sisa dipanaskan pada suhu 105oC sampai bobot tetap. Kadar sari
larut dalam air dihitung dengan persen terhadap bahan yang telah kering (Depkes,
1995).
3.6.5 Penetapan kadar sari yang larut dalam etanol
Sebanyak 5 g serbuk yang telah dikeringkan di udara dimaserasi selama 24
jam. Kemudian disaring cepat untuk menghindari penguapan etanol 96%,
sejumlah 20 ml filtrat diuapkan sampai kering dalam cawan penguap berdasar
rata yang telah ditara dan sisanya dipanaskan pada suhu 105oC sampai bobot
tetap. Kadar sari larut dalam etanol dihitung dalam persen terhadap bahan yang
telah kering (Depkes, 1995).
3.6.6 Penetapan kadar abu total
Sebanyak 2 g serbuk yang telah digerus dan ditimbang seksama
dimasukkan ke dalam cawan porselin yang telah dipijar dan ditara, kemudian
diratakan. Krus dipijar perlahan- lahan sampai arang habis, pemijaran dilakukan
pada suhu 500-600 oC selama 3 jam kemudian didinginkan dan ditimbang sampai
diperoleh bobot tetap. Kadar abu dihitung terhadap bahan yang telah kering
(Depkes, 1995).
3.6.7 Penetapan kadar abu yang tidak larut dalam asam
Abu yang telah diperoleh dalam penetapan kadar abu dididihkan dalam 25
ml asam klorida encer selama 5 menit, bagian yang tidak larut dalam asam
dikumpulkan, disaring melalui kertas saring dipijarkan sampai bobot tetap,
kemudian didinginkan dan ditimbang. Kadar abu yang tidak larut dalam asam
dihitung terhadap bahan yang kering (Depkes, 1995).
3.7 Skrining Senyawa Kimia
Skrining senyawa kimia serbuk simplisia meliputi pemeriksaan senyawa
gologan alkaloid, flavonoida, glikosida, glikosida antrakinon, saponin, tanin dan
n-heksana dilakukan dengan cara yang sama dengan skrining fsenyawa kimia
serbuk simplisia.
3.7.1 Pemeriksaan alkaloida
Serbuk simplisia ditimbang sebanyak 0,5 g, kemudian ditambah 1 ml asam
klorida 2 N dan 9 ml air suling, dipanaskan di atas penangas air selama 2 menit,
didinginkan dan disaring. Filtrat dipakai untuk percobaan berikut :
a. Filtrat sebanyak 3 tetes ditambah dengan 2 tetes larutan pereaksi Mayer, akan
terbentuk endapan menggumpal berwarna putih atau kuning bila terdapat
alkaloida.
b. Filtrat sebanyak 3 tetes ditambah dengan 2 tetes larutan pereaksi Bouchardat,
akan terbentuk endapan berwarna coklat sampai hitam bila terdapat alkaloida.
c. Filtrat sebanyak 3 tetes ditambah dengan 2 tetes pereaksi Dragendorf akan
terbentuk warna merah atau jingga bila terdapat alkaloida.
3.7.2 Pemeriksaan flavonoida
Sebanyak 10 g serbuk simplisia ditambah 100 ml air panas, dididihkan
selama 5 menit dan saring dalam keadaan panas. Kedalam 5 ml filtrat
ditambahkan serbuk magnesium, 1 ml asam klorida pekat dan 2 ml amil alkohol,
dikocok kuat dan dibiarkan memisah. Flavonoida ditunjukkan dengan timbulnya
warna merah, kuning atau jingga pada lapisan amil alkohol.
3.7.3 Pemeriksaan saponin
Sebanyak 0,5 g serbuk simplisia, dimasukkan ke dalam tabung reaksi,
ditambahkan 10 ml air panas, didinginkan kemudian dikocok selama 10 detik.
Jika terbentuk busa setinggi 1 sampai 10 cm yang stabil tidak kurang dari 10
3.7.4 Pemeriksaan tanin
Sebanyak 0,5 g serbuk simplisia, disari dengan 10 ml air suling lalu
disaring, filtratnya diencerkan dengan air sampai tidak berwarna. Larutan diambil
sebanyak 2 ml dan ditambahkan 1-2 tetes pereaksi besi (III) klorida 1%. Jika
terjadi warna biru atau hijau kehitaman bila adanya tanin.
3.7.5 Pemeriksaan glikosida
Sebanyak 3 g serbuk simplisia disari dengan 30 ml campuran etanol 95%
dengan air (7:3) dan 10 ml asam sulfat 2 N, direfluks selama 1 jam, didinginkan
dan disaring. Pada 20 ml filtrat ditambahkan 25 ml air dan 25 ml timbal asetat 0,4
M, dikocok, diamkan 5 menit lalu disaring. Filtrat disari dengan 20 ml campuran
isopropanol dan kloroform (2:3), dilakukan sebanyak 3 kali. Kumpulan sari air
diuapkan pada temperatur tidak lebih dari 50oC. Sisanya dilarutkan dalam 2 ml
metanol. Larutan sisa dimasukkan dalam tabung reaksi selanjutnya, diuapkan di
atas penangas air, pada sisa ditambahkan 2 ml air dan 5 tetes pereaksi Molisch.
Tambahkan hati- hati 2 ml asam sulfat pekat melalui dinding tabung, terbentuknya
cincin ungu pada batas kedua cairan bila adanya gula.
3.7.6 Pemeriksaan antrakinon
Sebanyak 0,2 g serbuk simplisia dicampur dengan 5 ml asam sulfat 2 N,
dipanaskan sebentar, lalu didinginkan, ditambahkan 10 ml benzena, dikocok,
didiamkan. Lapisan benzena dipisahkan dan disaring. Kocok lapisan benzena
dengan 2 ml NaOH 2 N, diamkan. Lapisan air berwarna merah dan lapisan
benzena tidak berwarna bila adanya glikosida antrakinon.
3.7.7 Pemeriksaan steroida/triterpenoida
2 jam, disaring, filtrat diuapkan dalam cawan penguap dan pada sisanya
ditambahkan 2 tetes Liebermann-Burchard. Apabila terbentuk warna ungu atau
merah berubah menjadi ungu atau biru hijau bila adanya steroida/triterpenoida.
3.8 Pembuatan Ekstrak
Cara kerja :
Sejumlah 500 gram serbuk simplisia dimasukkan ke dalam wadah
bertutup, dituangkan 75 bagian n-heksan, ditutup, dibiarkan selama 5 hari
terlindung dari cahaya sambil sering-sering diaduk, diserkai, diperas, ampas
dicuci dengan n-heksan hingga diperoleh 100 bagian penyari, dipindahkan ke
dalam bejana tertutup, dibiarkan di tempat sejuk, terlindungi cahaya selama 2 hari.
Dienaptuangkan atau disaring, kemudian dipekatkan dengan rotary evaporator
pada suhu 40-50oC sampai diperoleh ekstrak kental. Bagan pembuatan ekstrak
n-heksan sponge dapat dilihat pada Lampiran 6 halaman 50.
3.9 Analisis Ekstrak n-heksana secara Kromatografi Lapis Tipis
Ekstrak dianalisis secara KLT menggunakan fase diam silika gel GF 254
dengan fase gerak campuran (n-heksana-etil asetat) dengan perbandingan (90:10),
(80:20), (70:30), (60:40) dan (50:50). Sebagai penampak bercak digunakan
pereaksi Liebermann–Burchard.
Cara kerja :
Ekstrak ditotolkan pada plat lapis tipis, kemudian dimasukkan ke dalam
chamber yang telah jenuh dengan uap fase gerak. Setelah pengembangan selesai
dipanaskan dalam oven pada suhu 110 0C selama 5 menit lalu diamati perubahan
warna yang terjadi. Bagan perolehan isolat dari ekstrak sponge dapat dilihat pada
Lampiran 7 halaman 51 dan hasil analisis ekstrak n-heksana secara KLT dapat
dillihat pada Lampiran 8 halaman 52.
3.10 Isolasi Senyawa Steroid/triterpenoid secara Kromatografi Lapis Tipis Preparatif
Hasil yang menunjukan fase terbaik digunakan untuk pengembang pada
KLT Preparatif sebagai penampak bercak digunakan pereaksi Liebermann-
Burchard dan sebagai fase gerak digunakan n-heksana-etilasetat (70:30) dan fase
diam silika gel GF 254.
Cara kerja:
Ekstrak n-heksana ditotolkan seperti pita pada jarak 2 cm dari tepi bawah
plat KLT berukuran 20 x 10 cm yang telah diaktifkan, setelah kering plat KLT
dimasukkan ke dalam bejana yang telah jenuh dengan uap, fase gerak,
pengembang dibiarkan naik membawa komponen yang ada, setelah mencapai
batas pengembangan plat dikeluarkan dari bejana lalu dikeringkan. Bagian tengah
plat ditutup dengan kaca yang bersih sedangkan pada sisi kanan dan kiri plat
disemprot dengan penampak bercak Liebermann-Burchard. Bagian tengah plat
yang sejajar dengan bercak berwarna ungu dikerok dan dikumpulkan, direndam
dengan metanol satu malam lalu disaring kemudian pelarutnya diuapkan,
kemudian dilakukan uji kemurnian dengan KLT terhadap isolat yang diperoleh
(Hostettmann, 1995). Hasil isolasi senyawa steroid/triterpenoid secara KLT
3.11 Uji Kemurnian Terhadap Isolat
3.11.1 Uji kromatografi lapis tipis satu arah
Uji kemurnian isolat dilakukan dengan KLT menggunakan fase gerak
n-heksana-etilasetat (70:30).
Cara kerja:
Isolat ditotolkan pada plat lapis tipis, lalu dimasukan ke dalam chamber
yang telah jenuh dengan uap fase gerak. Setelah pengembangan selesai plat
dikeluarkan dan dikeringkan, plat disemprot dengan penampak bercak
Liebermann-Burchard dan dipanaskan di oven pada suhu 110 oC (Gritter, 1991).
Hasil uji KLT satu arah dapat dilihat pada Lampiran 10 halaman 54.
3.11.2 Uji kromatografi lapis tipisdua arah
Terhadap isolat hasil isolasi dilakukan KLT 2 arah menggunakan fase
gerak n-heksana-etilasetat (70:30) dan toluen-etilasetat (80:20).
Cara kerja:
Isolat ditotolkan pada plat pra lapis silika gel GF254 ukuran 20x20 lalu
dikembangkan memakai fase gerak I yaitu n-heksana-etilasetat (70:30), hingga
mencapai batas pengembangan, kemudian plat dikeluarkan dari dalam bejana dan
dikeringkan, setelah plat kering dikembangkan kembali dengan arah yang berbeda
90 oC memakai fase gerak II yaitu toluen-etilasetat (80:20) disemprot dengan
memakai penampak bercak Liebermann-Burchard, setelah itu plat dipanaskan
pada suhu 110 oC selama 10 menit lalu ditandai bercak yang terbentuk (Gandjar
dan Rohman, 2012). Hasil uji KLT dua arah dapat dilihat pada lampiran 11
3.12 Karakterisasi Isolat
Karakterisasi isolat dengan spektrofotometri ultraviolet dan
spektrofotometri inframerah dilakukan di Laboratorium Penelitian Fakultas
Farmasi USU Medan.
3.12.1 Karakterisasi isolat dengan spektrofotometri ultraviolet (UV)
Cara kerja:
Isolat hasil isolasi dilarutkan dalam pelarut metanol, kemudian
dimasukkan kedalam kuvet yang telah dibilas dengan metanol, selanjutnya
absorbansi larutan sampel diukur pada panjang gelombang 200-400 nm.
3.12.2 Karakterisasi isolat dengan spektrofotometri infrared (IR)
Cara kerja:
Karakterisasi isolat dengan spektrofotometri infrared dilakukan dengan
cara mencampurkan 1 mg isolat dengan 100 mg kalium bromida menggunakan
alat mixture vibrator kemudian dicetak menjadi pelet pada tekanan 11,5 ton dan
dimasukkan ke dalam spektrofotometer inframerah serta diukur pada bilangan
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil dan Identifikasi Sponge
Hasil identifikasi sponge yang dilakukan oleh Laboratorium Ekologi Prodi
Biologi FMIPA-Institut Teknologi Sepuluh November (ITS) Surabaya adalah
Xeastospongia sp de Laubenfels.
4.2 Hasil Pemeriksaan Karakteristik
Hasil karakterisasi simplisia sponge Xeastospongia sp de Laubenfels
meliputi dari pemeriksaan karakteristik sponge secara makroskopik, Pemeriksaan
karakteristik serbuk simplisia secara mikroskopik, pemeriksaan kadar air, kadar
sari larut air, kadar sari larut etanol, kadar abu total, kadar abu yang tidak larut
asam,dapat dilihat pada Tabel 4.1
Pemeriksaan karakteristik sponge secara makroskopik dilakukan untuk
memperoleh identitas (kebenaran simplisia). Hasil pemeriksaan Xeastospongia sp
de Laubenfels diperoleh tempat spesimen itu hidup melekat pada batu-batuan
atau karang-karang mati, tubuh besar dan tumbuh tegak berbentuk seperti bunga,
warna ketika diambil berwarna coklat terang, berbau tak sedap.
Pemeriksaan karakteristik serbuk simplisia secara mikroskopik dilakukan
untuk memperoleh identitas simplisia (kebenaran simplisia). Hasil pemeriksaan
karakteristik serbuk simplisia Xeastospongia sp de Laubenfels secara mikroskopik
terlihat adanya spikula megasklera monoaxon jenis Hastate oxea. Hasil dapat
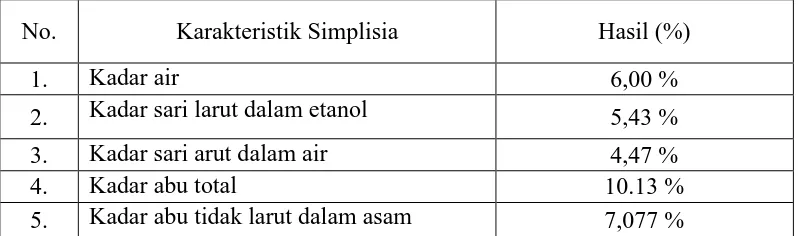
Tabel 4.1 Hasil karakterisasi simplisia sponge
No. Karakteristik Simplisia Hasil (%)
1. Kadar air 6,00 %
2. Kadar sari larut dalam etanol 5,43 %
3. Kadar sari arut dalam air 4,47 %
4. Kadar abu total 10.13 %
5. Kadar abu tidak larut dalam asam 7,077 %
Hasil penepatapan kadar air pada sponge Xeastospongia sp de Laubenfels
yaitu 6,00 % dengan tujuan untuk memberikan batasan minimal kandungan air
yang masih dapat ditolerir di dalam ekstrak karena tingginya kandungan air
menyebabkan ketidakstabilan sediaan obat, bakteri dan jamur cepat tumbuh dan
bahan aktif yang terkandung didalamnya dapat terurai. Kadar sari yang larut
dalam etanol dengan bobot persen 5,43 % penetapan kadar sari yang larut dalam
air dan etanol dilakukan untuk mengetahui banyaknya senyawa polar yang larut
dalam air dan etanol.
4.3 Hasil Skrining Senyawa Kimia
Hasil skrining Senyawa kimia terhadap simplisia dan ekstrak sponge
dilakukan untuk mendapatkan informasi golongan senyawa metabolit sekunder
yang terdapat di dalamnya. Skrining fitokimia sponge Xeastospongia sp de
Laubenfels hanya dilakukan pada simplisia saja karena keterbatasan ekstrak. Hasil
Tabel 4.2 Hasil skrining senyawa kimia simplisia Xeastospongia sp de Laubenfels
No Nama Senyawa Hasil
1. Alkaloid +
2. Flavonoid -
3. Steroid/Triterpenoid +
4. Tanin -
5. Glikosida +
6. Saponin +
7. Glikosida antrakuinon -
Keterangan : (+) = mengandung golongan senyawa (-) = tidak mengandung golongan senyawa
Hasil skrining senyawa kimia pada serbuk simplisia sponge Xeastospongia
sp de Laubenfels mengandung senyawa alkaloid, saponin, glikosida dan
steroid/triterpenoid. Serbuk simplisia sponge yang ditambah dengan periaksi
Dragendorff memberikan endapan jingga kecoklatan, dengan pereaksi Bouchardat
memberikan endapan warna kuning kecoklatan dan dengan pereaksi Mayer
terbentuk edapan putih dan kekeruhan, hal ini menunjukkan simplisia
mengandung alkaloid. Alkaloid dianggap positif jika terjadi endapan pada paling
sedikit dua atau tiga dari pereaksi yang ditambahkan (Depkes RI, 1995).
Penambahan Liebermann-Burchard memberikan warna merah ungu menunjukkan
adanya senyawa steroid (Harborne, 1987). Skrining saponin menghasilkan busa
yang stabil dengan tinggi busa 3 cm dan tidak hilang dengan penambahan HCl 2
N,). Skrining glikosida menghasilkan adanya cincin ungu pada kedua batas cairan
karena adanya gula.
4.4 Hasil Ekstraksi
Sejumlah 500 gram serbuk simplisia dimasukkan kedalam wadah bertutup,
[image:53.595.113.499.125.246.2]cahaya sambil sering-sering diaduk, diserkai, diperas, ampas dicuci dengan
n-heksan hingga diperoleh 100 bagian penyari, dipindahkan kedalam bejana
tertutup, dibiarkan ditempat sejuk, terlindungi cahaya selama 2 hari.
Dienaptuangkan atau disaring, kemudian dipekatkan dengan rotary evaporator
pada suhu 40-50oC sampai diperoleh ekstrak kental. Ekstrak yang diperoleh
sebanyak 8 gram. Penggunaan pelarut n-heksana untuk menarik senyawa kimia
non polar, seperti triterpenoid dan steroid bebas.
4.5 Hasil Analisis Ekstrak Steroid/triterpen secara Kromatografi Lapis Tipis
Hasil analisis KLT menggunakan fase diam silika gel GF 254 dengan
penampak bercak Liebermann-Burchard diperoleh fase gerak terbaik n-heksan-etil
asetat dengan perbandingan (70:30) karena menghasilkan pemisahan noda yang
paling baik.
4.6 Hasil Isolasi Senyawa Steroid/Triterpenoid Secara Kromatografi Lapis Tipis Preparatif
Hasil kromatografi lapis tipis preparatif dari ekstrak sponge terdapat 3 pita
berwarna merah keunguan, masing-masing dikerok dan direndam selama satu
malam dalam metanol kemudian disaring lalu diuap dan diperoleh 3 isolat
selanjutnya masing-masing isolat direndam dengan metanol dingin sehingga
diperoleh kristal amorf yang berwarna putih yang berupa isolat murni.
4.7 Hasil Uji Kemurnian Kromatografi Lapis Tipis Satu Arah
Terhadap isolat hasil isolasi KLT satu arah menggunakan fase diam silika
Rf 0,43 dengan penampak bercak Liebermann-Burchard. Hasil elusi menunjukkan
satu noda pada fase gerak yang digunakan diduga bahwa isolat yang diperoleh
telah murni.
4.8 Hasil Uji Kemurnian Kromatografi Lapis Tipis Dua Arah
KLT dua arah dilakukan untuk memastikan kemurnian steroid/triterpenoid
menggunakan fase gerak 1 n-heksana-etil asetat (70:30) dengan nilai Rf 0,85 dan
fase gerak ke 2 toluen-etil asetat (80:20) dengan nilai Rf 0,80.
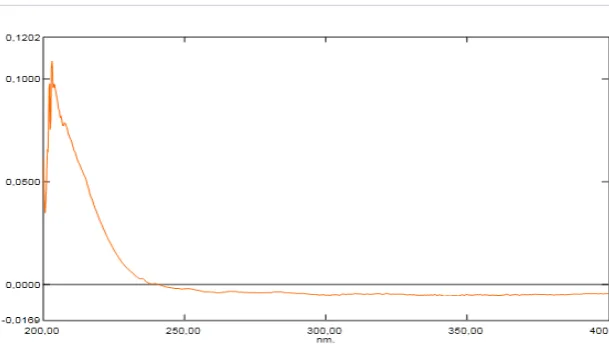
4.9 Hasil Karakterisasi Isolat dengan Spektofometri Ultraviolet (UV)
Hasil isolasi menunjukkan absorbsi pada panjang gelombang 203 nm yang
menunjukan adanya gugus kromofor. Berikut ini adalah gambar spektrum
ultraviolet dari senyawa isolat. Gambar spektrofotometri UV dari isolat dapat
dilihat pada Gambar 4.1.
4.10 Hasil Karakterisasi Isolat dengan Spektrofotometri Infrared (IR)
Hasil menunjukkan pada bilangan gelombang 3433,29 cm-1 terdapat
[image:55.595.162.467.459.638.2]apakah gugus -OH ini berasal dari isolat atau berasal dari pelarut, karena pelarut
yang digunakan adalah metanol, Gugus -OH tersebut dikuatkan oleh serapan C=O
pada bilangan gelombang 1099,43 cm-1 dan puncak pada bilangan gelombang
1377,17 cm-1 menunjukkan adanya gugus metil (CH3). Bilangan gelombang 1635,
64 cm-1 adanya gugus C=C, dicocokkan dengan melihat CH-alifatis pada bilangan
gelombang 2949,30 cm-1 yang berada disebelah kanan dari bilangan gelombang
3000 cm-1. Hasil identifikasi dengan spektrofotometer inframerah dapat dilihat
[image:56.595.116.512.333.420.2]pada Tabel 4.3 di bawah ini.
Tabel 4.3 Hasil Spektrofotometer Infraramerah dari isolat
No. Bilangan Gelombang (cm-1) Gugus Fungsi
1 1099,43 C=O
2 1377,17 -CH3
3 1635,64 C=C
4 2949,30 C-H alifatis
[image:56.595.116.509.466.674.2]5 3433,29 -OH
Gambar spektrum inframerah dari senyawa isolat dapat dilihat pada Gambar
4.2 dibawah ini
BAB V
KESIMPULAN DAN SARAN
5.1Kesimpulan
1. Penelitian yang dilakukan menggunakan prosedur karakterisasi simplisia
pada Materia Medika, dengan hasil pemeriksaan karakterisasi simplisia
sponge Xestospongia sp diperoleh kadar air 6,00%, kadar sari yang larut
dalam air 4,47%, kadar sari yang larut dalam etanol 5,43%, kadar abu total
10,13% dan kadar abu yang tidak larut dalam asam 7,07%.
2. Hasil penelitian menunjukkan bahwa golongan senyawa kimia yang
terkandung dalam simplisia sponge Xestospongia sp adalah alkaloid,
steroid/triterpenoid, glikosida dan saponin.
3. Hasil isolat menunjukkan golongan senyawa steroid/triterpenoid dan hasil
identifikasi dengan spektrofotometri ultraviolet, isolat memberikan panjang
gelombang absorbsi maksimum 203 nm dan hasil pengukuran
spektrofotometri inframerah menunjukkan adanya gugus –OH, CH alifatis,
C=C, –CH3 dan C=O. Isolat yang diperoleh merupakan isolat tunggal dan
termasuk golongan senyawa steroid/triterpenoid.
5.2 Saran
Disarankan kepada peneliti selanjutnya untuk melakukan elusidasi struktur
DAFTAR PUSTAKA
Amir, I.,dan., Budiyanto, A. (1996). Mengenal Spons Laut (Demospongiae) Secara Umum. Oceana. XXI (2). Halaman 15-31.
Crews, P.,dan. Hunter, L. C. (1993). The Search for Antiparasitic Agents from Marine Animals. Dalam: Marine Biotechnology. Volume I Pharmaceutical and Bioactive Natural Products. Disunting Oleh: David H. Attaway dan Oskar R. Zaborsky. New York: Plenum Press. Halaman 352-376.
Dachriyanus. (2004). Analisis Struktur Senyawa Organik Secara Spektroskopi. Padang: Andalas University Press. Halaman 3-5, 21.
Depkes RI. (1995). Materia Medika Indonesia. Jilid VI. Departemen Kesehatan RI. Jakarta. Halaman 321-326.
Depkes RI. (2000). Parameter Standar Umum Ekstrak Tumbuhan Obat. Jakarta: Departemen Kesehatan RI. Halaman. 1, 10-11.
Ditjen RI. (1979). Farmakope Indonesia. Edisi III. Jakarta: Departemen Keseha