PENETAPAN KADAR TIMBAL (Pb) DAN TEMBAGA
(Cu) PADA GARAM YANG BEREDAR DIPASARAN
SECARA SPEKTROFOTOMETRI SERAPAN ATOM
SKRIPSI
OLEH:
MARISA
NIM 060804033
PROGRAM STUDI SARJANA FARMASI
UNIVERSITAS SUMATERA UTARA
PENETAPAN KADAR TIMBAL (Pb) DAN TEMBAGA
(Cu) PADA GARAM YANG BEREDAR DIPASARAN
SECARA SPEKTROFOTOMETRI SERAPAN ATOM
SKRIPSI
Diajukan untuk Melengkapi Salah Satu Syarat untuk
Memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
MARISA
NIM 060804033
PROGRAM STUDI SARJANA FARMASI
UNIVERSITAS SUMATERA UTARA
PENGESAHAN SKRIPSI
PENETAPAN KADAR TIMBAL (Pb) DAN TEMBAGA
(Cu) PADA GARAM YANG BEREDAR DIPASARAN
SECARA SPEKTROFOTOMETRI SERAPAN ATOM
OLEH:
MARISA
NIM 060804033
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: Juni 2012
Disetujui Oleh:
Pembimbing I, Panitia Penguji,
Drs. Maralaut Batubara, M.Phill., Apt. Drs.Chairul A.Dalimunthe,M.Sc., Apt NIP 195101311976031003 NIP 194907061980021001
Pembimbing II, Drs. Maralaut Batubara, M.Phill, Apt NIP 195101311976031003
Drs. Muchlisyam, M.Si., Apt.
NIP 195006221980021001 Drs. Immanuel S. Meliala M.Si., Apt NIP 195001261983031002
Dra. Sudarmi M.Si., Apt NIP 195409101983032001
Medan, Juni 2012 Fakultas Farmasi
Universitas Sumatera Utara Dekan,
KATA PENGANTAR
Bismillahirrahmanirrahiim,
Puji syukur penulis ucapkan kepada Allah SWT atas segala limpahan
rahmat dan karuniaNya, sehingga penulis dapat menyelesaikan penelitian dan
penyusunan skripsi ini, serta Shalawat dan Salam kepada Nabi Allah: Rasulullah
Muhammad SAW sebagai suri tauladan dalam kehidupan.
Skripsi ini disusun untuk melengkapi salah satu syarat mencapai gelar
Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara, dengan
judul:“Penetapan Kadar Pb dan Cu pada garam yang beredar dipasaran
Secara Spektrofotometri Serapan Atom”.
Pada kesempatan ini dengan segala kerendahan hati penulis mengucapkan
terima kasih yang sebesar-besarnya kepada Ayahanda Mustafrin dan Ibunda
Masniar, Mertua Ayahanda Alm. Mawardi Wahab dan Ibunda Nurmala yang telah
memberikan cinta dan kasih sayang yang tidak ternilai dengan apapun, doa yang
tulus serta pengorbanan baik materi maupun non-materi. Suami tercinta Tahta
Amrullah, S.Stp, yang telah setia mendampingi penulis, yang telah memberikan
cinta dan kasih sayang dan doa yang tulus serta selalu memberikan dukungan dan
semangat kepada penulis.
Bapak Drs. Muchlisyam, M.Si., Apt., dan bapak Drs. Maralaut Batubara
M.Phil., Apt., yang telah membimbing dan memberikan petunjuk serta
saran-saran selama penelitian hingga selesainya skripsi ini. Bapak Prof. Dr. Sumadio
Hadisahputra., Apt., selaku Dekan, staf pengajar dan staf administrasi Fakultas
Farmasi yang telah mendidik penulis selama masa perkuliahan dan membantu
akademik yang telah memberikan bimbingan kepada penulis selama masa
perkuliahan dan selaku Kepala Laboratorium Kimia Farmasi Kualitatif Farmasi
USU yang telah memberikan izin dan fasilitas untuk penulis sehingga dapat
mengerjakan dan menyelesaikan penelitian.
Kakanda (Geri, Rikki, ilma, rina, dan ita) dan anak-anakku tercinta
(Nurmawaddah Permaisuri dan Haura Nahda Athifah), serta seluruh keluarga
yang selalu mendoakan dan memberikan semangat.
Spesial untuk sahabat-sahabat ku (Fika, Mimil, Siti, Jack, Siti, Cici, Rico),
k.ira, winda, Tika, Uti, Vytra, Ika, Noni dan seluruh teman-teman angkatan 2006,
terima kasih untuk perhatian, semangat, doa, dan kebersamaannya selama ini.
Serta seluruh pihak yang telah ikut membantu penulis namun tidak tercantum
namanya.
Penulis menyadari sepenuhnya bahwa dalam penulisan skripsi ini masih
jauh dari kesempurnaan, oleh karena itu dengan segala kerendahan hati, penulis
menerima kritik dan saran demi kesempurnaan skripsi ini.
Akhirnya, penulis berharap semoga skripsi ini dapat memberi manfaat
bagi kita semua.
Medan, Juni 2012 Penulis,
PENETAPAN KADAR TIMBAL (Pb) DAN TEMBAGA (Cu) PADA GARAM DAPUR YANG BEREDAR DIPASARAN SECARA
SPEKTROFOTOMETRI SERAPAN ATOM
ABSTRAK
Garam yang beredar dipasaran merupakan garam yang dipakai sehari-hari oleh masyarakat, baik yang dikonsumsi maupun yang digunakan untuk keperluan industri. Pada proses pembuatan garam dari air laut kemungkinan telah mengandung timbal (Pb) dan tembaga (Cu). Tujuan penelitian ini adalah untuk mengetahui kadar timbal (Pb) dan tembaga (Cu) dalam berbagai macam garam yang beredar dipasaran.
Penetapan kadar dilakukan dengan menggunakan spektrofotometer serapan atom tanpa nyala. Analisis kuantitatif dilakukan pada logam timbal (Pb) pada panjang gelombang 283 nm dan logam tembaga (Cu) pada panjang gelombang 324 nm.
Hasil penelitian menunjukkan bahwa kadar Cu pada garam dolina108,5135 ± 8,4845 ppb, garam tradisional adalah 355,7413 ± 33,9138 ppb, garam ikan adalah 192,9603 ± 10,8610 ppb, dan garam A1 adalah 229,5659 ± 33,9138 ppb. Kadar Pb pada garam dolina adalah 603,6946 ± 71,8142 ppb, garam tradisional seadalah 765,6632 ± 90,0570 ppb, garam ikan adalah 678,4345 ± 232,4502 ppb, dan garam A1 adalah 634,0952 ± 195,3195 ppb.
Hasil uji beda berdasarkan uji statistik menunjukkan kandungan Cu dan Pb pada garam tradisional ternyata berbeda signifikan dengan garam dolina, garam ikan dan garam A1.
Kadar logam Timbal dan tembaga didalam keempat garam yg di periksa tidak melebihi batas maksimum SNI No.01- 3556- 1994. Dari keempat jenis garam didapat bahwa garam tradisional memiliki kandungan Cu dan Pb yang lebih besar dibandingkan garam dolina, garam ikan dan garam A1.
THE STANDART DETERMINATION OF TIMBAL (Pb) AND THE COPPER (Cu) FOR THE CIRCULATION SALT IN THE MARKET
IN ATOM ABSORPTION SPEKTROFOTOMETRI
ABSTRACT
Circulating salt in the market, was used everyday by the community, both that was consumed by their self or used for the need of the industry. In the process of the production of salt from water sea possibility contained the plumbum (Pb) and copper (Cu). The aim of this research was to know the level of plumbum (Pb) and copper (Cu) in various circulating salt sorts in the market.
The determination the level of was carried out with used spektrofotometer the absorption of the atom without the flame. The quantitative analysis was used to plumbum metal (Pb) in long the wave 283 nm and copper metal (Cu) in long the wave 324 nm.
Results of the research showed that the level of Cu to dolina’s salt was 108.5135 ± 8.4845 ppb, traditional salt was 355.7413 ± 33.9138 ppb, fish salt was 192.9603 ± 10.8610 ppb , and salt A1 was 229.5659 ± 33.9138 ppb. The level of Pb to dolina’s salt was 603.6946 ± 71.8142 ppb, traditional salt was 765.6632 ± 90.0570 ppb, fish salt was 678.4345 ± 232.4502 ppb, and salt A1 was 634.0952 ± 195.3195 ppb.
Result of the difference test of being based on the statistical test showed the Cu content and the Pb to traditional salt evidently different significant with dolina’s salt, fish salt and salt A1.
The level of plumbum metal and copper in the four salts which checked, did not exceed the maximum limit of SNI No.01-3556-1994. From the four salt, was gotten that traditional salt had the Cu content and the Pb that were bigger compared with dolina salt, fish salt and salt A1.
DAFTAR ISI
Halaman
JUDUL ...
i
LEMBAR JUDUL ...
ii
LEMBAR PENGESAHAN ...
iii
KATA PENGANTAR ...
iv
ABSTRAK ... vi
ABSTRACT ...
vii
DAFTAR ISI ...
viii
DAFTAR TABEL ...
xi
DAFTAR GAMBAR ...
xii
DAFTAR LAMPIRAN ...
xiii
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 3
1.5 Manfaat Penelitian ... 3
BAB II TINJAUAN PUSTAKA ... 4
2.1 Garam ... 4
2.3 Kegunaan dan Jenis Garam ... 6
2.4 Kegunaan Timbal ... 7
2.4.1 Toksisitas timbal ... 8
2.5 Kegunaan Tembaga ... 9
2.5.1 Toksisitas tembaga ... 9
2.6 Pencemaran Logam Berat ... 9
2.7 Logam dalam Tubuh Makhluk Hidup ... 11
2.8 Spektrofotometri Serapan Atom ... 12
2.8.1 Prinsip dasar spektrofotometri serapan atom ... 12
2.8.2 Bahan bakar dan bahan pengoksidasi ... 16
2.9 Validasi Metode Analisis ... 17
BAB III METODE PENELITIAN ... 20
2.1 Tempat dan Waktu Penelitian ... 20
2.2 Bahan – bahan ... 20
2.2.1 Sampel ... 20
2.3 Alat-alat ... 20
2.4 Pembuatan pereaksi ... 21
2.4.1 Larutan HNO3 5N ... 21
2.5 Prosedur Penelitian ... 21
2.5.1. Pengambilan sampel ... 21
2.5.2 Proses destruksi ... 21
2.5.3 Pembuatan larutan sampel ... 21
2.6 Pemeriksaan Kuantitatif ... 22
2.6.2 Pembuatan kurva kalibrasi tembaga ... 22
2.7 Penetapan Kadar Dalam Sampel ... 22
2.7.1 Penetapan kadar timbal ... 22
2.7.2 Penetapan kadar tembaga ... 23
2.7.3 Penentuan batas deteksi dan batas kuantitasi ... 23
2.7.4 Uji akurasi dengan persen perolehan kembali ... 24
2 .8 Analisis Data Secara Statistik ... 24
2.8.1 Penolakan hasil pengamatan ... 24
2.8.2 Pengujian beda nilai rata-rata ... 25
2.8.3 Simpangan baku relatif ... 26
BAB III HASIL DAN PEMBAHASAN ... 27
3.1 Kurva Kalibrasi Pb dan Cu ... 27
3.1.1 Kurva kalibrasi tembaga (Cu) dengan panjang gelombang 324 nm ... 27
3.1.2 Kurva kalibrasi timbal (Pb) dengan panjang gelombang 283 nm ... 28
3.2 Kadar Tembaga (Cu) dan Timbal (Pb) pada Garam ... 28
3.3 Uji Validasi ... 32
3.3.1 Batas deteksi dan batas kuantitasi ... 32
3.3.2 Uji perolehan kembali ... 32
BAB IV KESIMPULAN DAN SARAN ... 34
4.1 Kesimpulan ... 34
4.2 Saran ... 34
DAFTAR PUSTAKA ... 34
DAFTAR TABEL
Halaman
Tabel 1. Persen Uji Perolehan Kembali (recovery) ... 25
Tabel 2. Data Kadar Cu ... 29
Tabel 3. Data Kadar Pb ... 29
Tabel 4. Uji Beda Nilai Rata – rata Kadar Tembaga (Cu) dalam
Garam ... 30
DAFTAR GAMBAR
Halaman
Gambar 1. Kurva Kalibrasi Larutan Standar Tembaga ... 27
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Bagan alir proses destruksi ... 36
Lampiran 2. Bagan alir pembuatan sampel ... 37
Lampiran 3. Hasil Pengukuran Absorbansi Larutan Timbal (Pb), Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r) dari Data Kalibrasi Pb ... 38
Lampiran 4. Hasil Pengukuran Absorbansi Larutan Standar Tembaga (Cu), Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r) dari Data Kalibrasi Cu ... 40
Lampiran 5. Perhitungan Batas Deteksi dan Batas Kuantitasi Pb ... 42
Lampiran 6. Perhitungan Batas Deteksi dan Batas Kuantitasi Cu ... 43
Lampiran 7. Contoh Perhitungan Hasil Penetapan Kadar Pb Dalam Garam Dolina ... 44
Lampiran 8. Data Hasil Berat Sampel, Absorbansi, Konsentrasi dan Kadar Logam Pb Dengan 6 Kali Replikasi ... 46
Lampiran 9. Contoh Perhitungan Hasil Penetapan Kadar Cu Dalam Garam Dolina ... 48
Lampiran 10. Data Hasil Berat Sampel, Absorbansi, Konsentrasi dan Kadar Logam Cu Dengan 6 kali replikasi ... 49
Lampiran 11. Perhitungan Kadar Timbal (Pb) Dan Tembaga (Cu) ... 51
Lampiran 12. Perhitungan Statistik Kadar Pb pada Sampel ... 65
Lampiran 13. Perhitungan Statistik Kadar Cu pada Sampel ... 71
Lampiran 14. Pengujian Beda Nilai Rata-Rata Timbal Dalam Keempat Sampel ... 77
Lampiran 15. Pengujian Beda Nilai Rata-Rata Kadar Tembaga Dalam Keempat Sampel ... 88
garam Dolina untuk Recovery ...
... 99
Lampiran 17. Perhitungan Uji Perolehan Kembali Untuk Pb ... . 101
Lampiran 18. Data % Recovery Cu ... . 102
Lampiran 19. Perhitungan Kadar Logam Pb dalam Sampel untuk Recovery ... ... 103
Lampiran 20. Perhitungan Uji Perolehan Kembali untuk Pb ... 105
Lampiran 21. Data % Recovery Pb ... 106
Lampiran 22. Tabel Nilai Kritik Distribusi t ... 107
Lampiran 23. Gambar Alat Spektrofotometer Serapan Atom ... 108
Lampiran 24. Gambar sampel ... 109
PENETAPAN KADAR TIMBAL (Pb) DAN TEMBAGA (Cu) PADA GARAM DAPUR YANG BEREDAR DIPASARAN SECARA
SPEKTROFOTOMETRI SERAPAN ATOM
ABSTRAK
Garam yang beredar dipasaran merupakan garam yang dipakai sehari-hari oleh masyarakat, baik yang dikonsumsi maupun yang digunakan untuk keperluan industri. Pada proses pembuatan garam dari air laut kemungkinan telah mengandung timbal (Pb) dan tembaga (Cu). Tujuan penelitian ini adalah untuk mengetahui kadar timbal (Pb) dan tembaga (Cu) dalam berbagai macam garam yang beredar dipasaran.
Penetapan kadar dilakukan dengan menggunakan spektrofotometer serapan atom tanpa nyala. Analisis kuantitatif dilakukan pada logam timbal (Pb) pada panjang gelombang 283 nm dan logam tembaga (Cu) pada panjang gelombang 324 nm.
Hasil penelitian menunjukkan bahwa kadar Cu pada garam dolina108,5135 ± 8,4845 ppb, garam tradisional adalah 355,7413 ± 33,9138 ppb, garam ikan adalah 192,9603 ± 10,8610 ppb, dan garam A1 adalah 229,5659 ± 33,9138 ppb. Kadar Pb pada garam dolina adalah 603,6946 ± 71,8142 ppb, garam tradisional seadalah 765,6632 ± 90,0570 ppb, garam ikan adalah 678,4345 ± 232,4502 ppb, dan garam A1 adalah 634,0952 ± 195,3195 ppb.
Hasil uji beda berdasarkan uji statistik menunjukkan kandungan Cu dan Pb pada garam tradisional ternyata berbeda signifikan dengan garam dolina, garam ikan dan garam A1.
Kadar logam Timbal dan tembaga didalam keempat garam yg di periksa tidak melebihi batas maksimum SNI No.01- 3556- 1994. Dari keempat jenis garam didapat bahwa garam tradisional memiliki kandungan Cu dan Pb yang lebih besar dibandingkan garam dolina, garam ikan dan garam A1.
THE STANDART DETERMINATION OF TIMBAL (Pb) AND THE COPPER (Cu) FOR THE CIRCULATION SALT IN THE MARKET
IN ATOM ABSORPTION SPEKTROFOTOMETRI
ABSTRACT
Circulating salt in the market, was used everyday by the community, both that was consumed by their self or used for the need of the industry. In the process of the production of salt from water sea possibility contained the plumbum (Pb) and copper (Cu). The aim of this research was to know the level of plumbum (Pb) and copper (Cu) in various circulating salt sorts in the market.
The determination the level of was carried out with used spektrofotometer the absorption of the atom without the flame. The quantitative analysis was used to plumbum metal (Pb) in long the wave 283 nm and copper metal (Cu) in long the wave 324 nm.
Results of the research showed that the level of Cu to dolina’s salt was 108.5135 ± 8.4845 ppb, traditional salt was 355.7413 ± 33.9138 ppb, fish salt was 192.9603 ± 10.8610 ppb , and salt A1 was 229.5659 ± 33.9138 ppb. The level of Pb to dolina’s salt was 603.6946 ± 71.8142 ppb, traditional salt was 765.6632 ± 90.0570 ppb, fish salt was 678.4345 ± 232.4502 ppb, and salt A1 was 634.0952 ± 195.3195 ppb.
Result of the difference test of being based on the statistical test showed the Cu content and the Pb to traditional salt evidently different significant with dolina’s salt, fish salt and salt A1.
The level of plumbum metal and copper in the four salts which checked, did not exceed the maximum limit of SNI No.01-3556-1994. From the four salt, was gotten that traditional salt had the Cu content and the Pb that were bigger compared with dolina salt, fish salt and salt A1.
BAB I PENDAHULUAN
1.1 Latar Belakang
Garam merupakan salah satu komoditi strategis karena selain merupakan
kebutuhan manusia, juga digunakan sebagai bahan baku industri. Untuk
kebutuhan garam konsumsi manusia, garam telah dijadikan sarana fortifikasi zat
yodium menjadi garam konsumsi beryodium dalam rangka penanggulangan
Gangguan Akibat Kekurangan Yodium (GAKY). Garam merupakan salah satu
sumber sodium dan klorida dimana kedua unsur tersebut diperlukan untuk
metabolisme manusia (Burhanuddin, 2001).
Garam beryodium mengacu kepada Standar Nasional Indonesia (SNI) No.
01 – 3556 – 1994, dimana pada cemaran logam untuk logam Timbal (Pb)
persyaratan kualitas maks 10.000 ppb dan untuk logam Tembaga (Cu) persyaratan
kualitas maks 10.000 ppb (Burhanuddin, 2001).
Kehidupan manusia dibumi sangat bergantung pada lautan, manusia harus
menjaga kebersihan dan kelangsungan kehidupan organisme yang hidup di
dalamnya. Dengan demikian laut seakan-akan merupakan sabuk pengaman
kehidupan manusia di muka bumi ini. Di lain pihak, lautan merupakan tempat
pembuangan benda-benda asing dan pengendapan barang sisa yang diproduksi
oleh manusia (Darmono, 2001).
Di laut banyak terdapat pencemaran dimana salah satu nya minyak
pembuangan dari kapal – kapal nelayan. Minyak merupakan bahan bakar (energi)
yang terbentuk dari fosil biologi. Bahan bakar tersebut banyak digunakan dalam
pembangkit tenaga listrik, minyak untuk kendaraan, bahan bakar untuk mesin
mudah didapatkan karena diproduksi secara besar-besaran. Tetapi dilain pihak,
limbahnya cukup berbahaya untuk makhluk hidup dan sekitar nya, karena
biasanya limbah tersebut mengandung logam arsen (As), Kadmium (Cd), timah
hitam (Pb), dan Merkuri (Hg) (Darmono, 1995).
Walaupun logam berbahaya tersebut kandungannya sangat kecil dalam
bahan bakar minyak, tetapi kekuatan untuk menyebabkan keracunan sangat besar.
Logam tersebut biasanya terikat dalam bentuk bahan organik dan fraksi mineral
(Darmono, 1995).
Berbagai literatur telah mencantumkan beberapa metode untuk penetapan
kadar tembaga dan timbal, antara lain Kompleksometri, Spektrofotometri visible,
dan Spektrofotometri Serapan Atom. Pada penelitian ini digunakan metode
spektrofotometri serapan atom karena memiliki keuntungan antara lain kecepatan
analisisnya, ketelitiannya dan dapat menentukan konsentrasi dalam jumlah yang
sangat kecil dan spesifik untuk setiap unsur tanpa diperlukan pemisahan
(Khopkar, 1990).
Berdasarkan uraian diatas, maka peneliti tertarik untuk meneliti
kandungan Pb dan Cu yang terdapat dalam garam dapur. Pemilihan ini didasarkan
karena garam dapur umumnya dikonsumsi oleh masyarakat.
1.1Perumusan Masalah
1. Apakah garam dapur mengandung Pb dan Cu?
2. Berapa kadar Pb dan Cu yang diperoleh di dalam garam dapur tersebut?
1. Garam dapur mengandung Pb dan Cu.
2. Pada garam dapur mengandung Pb dan Cu dalam jumlah tertentu.
1.3Tujuan Penelitian
1. Menetapkan adanya kandungan Pb dan Cu dalam garam dapur.
2. Menentukan kadar Pb dan Cu dalam garam dapur tersebut dengan
Spektrofotometri serapan atom.
1.4 Manfaat Penelitian
Hasil penelitian ini dapat dipublikasikan kepada masyarakat sebagai
informasi dan memberikan informasi kepada masyarakat mengenai besarnya
kandungan Pb dan Cu dalam garam dapur.
TINJAUAN PUSTAKA
2.1Garam
Secara fisik, garam adalah benda padatan berwarna putih berbentuk kristal
yang merupakan kumpulan senyawa dengan bagian terbesar Natrium Chlorida
(>80 %) serta senyawa lainnya seperti Magnesium Chlorida, Magnesium Sulfat,
Calsium Chlorida dan lain-lain. Garam mempunyai sifat/karakteristik higroskopis
yang berarti mudah menyerap air, bulk density (tingkat kepadatan) sebesar
0,8 – 0,9 dan titik lebur pada tingkat suhu 801oC (Burhanuddin, 2001).
Pembuatan garam di Indonesia adalah dengan sistem penguapan air laut
menggunakan sinar matahari (solar energy) diatas lahan tanah, namun ada
beberapa daerah memproduksi garam dengan cara memasak karena kondisi tanah
yang berpori yaitu propinsi Aceh dan Bali (Burhanuddin, 2001).
Penggunaan garam secara garis besar dapat dibagi ke dalam 3 (tiga)
kelompok yaitu (Burhanuddin, 2001) :
1. Garam untuk konsumsi manusia.
2. Garam untuk pengasinan aneka pangan
3. Garam untuk industri
2.2Teknologi Pembuatan Garam dan Persyaratan Faktor Sumber Daya Alam Dominan yang Berpengaruh Dalam Proses Pembuatan Garam di Indonesia
Hampir keseluruhan garam di Indonesia diperoleh dengan Teknologi
jumlah yang sangat kecil diperoleh dari sumber air dalam tanah (bleng) seperti
yang terdapat di Purwodadi – Grobongan, Jawa Tengah (Burhanuddin, 2001).
Dalam proses pembuatan garam yang berasal dari air laut, maka faktor
sumber daya alam dominan, yang berpengaruh baik kualitas maupun kuantitas
garam yang dihasilkan adalah sebagai berikut :
1. Air Laut
- Kandungan garam relatif tinggi dan tidak tercampur aliran muara sungai tawar.
- Jernih, tidak tercampur dengan lumpur, sampah (limbah buangan lainnya). - Mudah masuk kedalam areal/lading garam (pasang surut mencapai
areal/daratan pembikinan garam).
Faktor lokasi berpengaruh secara langsung terhadap kualitas maupun
kuantitas penyediaan air laut. Lokasi yang sangat bagus untuk dipilih adalah yang
jauh dari air tawar atau muara sungai besar. Tempat yang berdekatan dengan
muara-muara sungai akan memberikan air laut dengan mutu rendah (konsentrasi
rendah). Adapun lokasi di teluk yang tertutup akan memberikan air laut dengan
mutu yang relatif baik (konsentrasi tinggi) (Burhanuddin, 2001).
Guna menjamin kontinuitas ketersediaan bahan baku sebaiknya dipilih
lokasi yang aliran lautnya tidak terganggu oleh selat sempit, sehingga pasang
surut air laut berjalan dengan normal. Pasang surut air laut bagi lahan- lahan
penggaraman, untuk antisipasi dapat dibuat waduk-waduk penampungan air laut
tersebut (Burhanuddin, 2001).
a. Topografi Tanah
Kondisi topografi tanah sangat berpengaruh terhadap pengaturan
pengeluaran maupun sirkulasi air di penggaraman. Topografi tanah yang ideal
adalah yang permukaannya landai dengan tingkat kemiringan yang kecil.
Ketinggian tanah maksimal 3 meter diatas permukaan air laut dengan luas
minimal 1 Ha.
b. Sifat fisis Tanah
Tanah harus kedap air sehingga air yang ditampung tidak bocor kedalam
tanah. Tanah liat memiliki tingkat permeabilitas yang kecil tetapi pada kondisi
tingkat kelembapan yang rendah akan mudah retak/pecah sehingga tingkat
kebocorannya tinggi.
c. Kehidupan
Lahan/areal yang digunakan sebagai penggaraman sebaiknya tak terdapat
kehidupan. Terdapatnya binatang yang hidup ditanah akan merusak penggaraman,
sedangkan tumbuh-tumbuhan akan menghalangi sinar matahari. Dengan demikian
kedua hal tersebut sangat mempengaruhi produktifitas areal (Burhanuddin, 2001).
2.3Kegunaan dan Jenis Garam
Pengelompokkan tersebut khususnya di Indonesia dengan spesifikasi
sebagai berikut :
A. Garam konsumsi
Garam dengan kadar NaCl = 97% atas dasar persen berat kering (dry
basis), kandungan impuritis (Sulfat, Magnesium dan Kalsium) = 2%, dan kotoran
kebutuhan Garam konsumsi antara lain untuk konsumsi rumah tangga, industri
makanan, industri minyak goreng, industri pengasinan dan pengawetan ikan.
B. Garam Industri
Garam dengan kadar NaCl = 97,5 % dengan kandungan impuritis (Sulfat,
Magnesium dan Kalsium serta kotoran lainnya) yang sangat kecil.
Kelompok kebutuhan Garam industri antara lain untuk :
a) Industri perminyakan, tekstil dan penyamakan kulit.
NaCl 97,5%
Sulfat maksimal 0,5%
kalsium maksimal 0,2%
Magnesium maksimal 0,3%
Kadar air maksimal 3 – 5%
b) CAP (Chlor Alkali Plant) Industri garam yang digunakan untuk proses
kimia dasar pembuatan soda dan chlor.
NaCL 98,5% (dry basis)
Sulfat maksimal 0,2%
kalsium maksimal 0,1%
Magnesium maksimal 0,06%
c) Garam dibidang farmasi
NaCL 99,5% (dry basis)
Impur itis mendekati 0 (Burhanuddin, 2001).
Timbal merupakan salah satu logam yang populer dan banyak dikenal oleh
orang awam. Hal ini dikarenakan timbal banyak digunakan dipabrik-pabrik baik
dalam bentuk murni maupun dalam bentuk campurannya dengan logam lain
(Darmono, 1995).
2.4.1 Toksisitas Timbal
Keracunan yang ditimbulkan oleh persenyawaan Pb dapat terjadi karena
masuknya persenyawaan tersebut ke dalam tubuh. Proses masuknya Pb ke dalam
tubuh dapat melalui beberapa jalur, yaitu melalui makanan dan minuman, udara
dan perembesan atau penetrasi melalui selaput atau lapisan kulit (Palar, 2004).
Meskipun jumlah Pb yang diserap oleh tubuh hanya sedikit, logam ini
ternyata menjadi sangat berbahaya. Hal ini disebabkan karena Timbal (Pb) adalah
logam toksik yang bersifat kumulatif dan bentuk senyawanya dapat memberikan
efek racun terhadap fungsi organ yang terdapat dalam tubuh (Suharto, 2005).
Gejala yang khas dari keracunan Pb antara lain (Darmono, 1995) :
1. Anemia: Pb dapat menghambat pembentukan hemoglobin (Hb) sehingga menyebabkan anemia. Selain itu, lebih dari 95% Pb yang terbawa dalam
aliran darah dapat berikatan dengan eritrosit yang menyebabkan mudah
pecahnya eritrosit tersebut.
2. Aminociduria: terjadinya kelebihan asam amino dalam urin disebabkan ikut sertanya senyawa Pb yang terlarut dalam darah lalu menuju ke sistem
urinaria (ginjal) yang mengakibatkan terjadinya kerusakan pada saluran
ginjal.
kontraksi saluran lumen dan usus terhenti, peristaltik menurun sehingga
terjadi konstipasi.
2.5Kegunaan Tembaga
Beberapa jenis enzim yang sangat bergantung pada Cu seperti
seruplasmin, superoksid-dismutase dan sitokrom-C-oksidase. Dari saluran
pencernaan, Cu diabsorpsi dan diangkut melalui darah (berikatan dengan protein
albumin dan transkuperin) kedalam hati lewat sistem darah porta hepatis
(Darmono, 1995).
Dalam hati, hampir semua Cu berikatan dengan enzim, terutama enzim
seruloplasmin yang mengandung 90-94% Cu dari total Cu dalam tubuh. Nama
kimia dari seruplasmin adalah alfa2-glikoprotein yang mengandung 6 atom Cu
dan terikat dengan erat. Pada janin biasanya Cu disimpan didalam hati, kemudian
digunakan lagi pada waktu akan dilahirkan (Darmono, 1995).
2.5.1 Toksisitas Tembaga
Pemberian Cu dalam waktu yang lama walaupun dalam dosis rendah,
dapat merusak kemampuan sel kebal untuk berpoliferasi (memperbanyak diri)
baik sel T ataupun sel B poliklonal mitogen. (Darmono, 2001).
2.6 Pencemaran Logam Berat
Pencemaran logam berat dapat terjadi pada daerah lingkungan yang
bermacam-macam dan ini dapat dibagi menjadi tiga golongan, yaitu udara,
tanah/daratan, dan air/lautan. Pencemaran udara oleh logam berat sangat erat
terjadi pada proses-proses industri yang menggunakan suhu tinggi, sedangkan
logam seperti As, Cd, Hg dan Pb, adalah logam yang biasanya relatif mudah
menguap (Darmono, 1995).
Pencemaran daratan dan air (air sungai/laut) biasanya terjadi karena
pembuangan limbah dari industri penggunaan logam yang bersangkutan secara
tidak terkontrol(pabrik aki/baterai) atau penggunaan bahan yang mengandung
logam itu sendiri (pestisida dan insektisida) (Darmono, 1995).
Kandungan logam dalam tanah sangat berpengaruh terhadap kandungan
logam dalam tanaman yang tumbuh di atasnya, sehingga kandungan logam yang
kurang atau berlebihan dalam jaringan tanaman akan mencerminkan kandungan
logam dalam tanah. Tetapi ada kekecualian, yaitu dengan adanya suatu interaksi
di antara logam itu sendiri, sehingga terjadi suatu hambatan penyerapan
kandungan logam tersebut dalam tanaman (Darmono, 1995)
Dalam menyimpulkan dan menginterpretasikan suatu hasil analisis
kandungan logam tersebut dalam sampel, perlu diketahui kandungan normal dari
logam tersebut. Konsentrasi logam dalam alam lingkungan (tanah, air dan udara)
adalah sangat rendah, sehingga kenaikan kadar logam dalam alam lingkungan
tersebut perlu dicurigai adanya suatu pencemaran. Dalam sistem jaringan biologi,
kandungan logam juga mempunyai konsentrasi tertentu, baik logam esensial
maupun nonesensial (Darmono,1995).
Jika diketahui kandungan yang sangat rendah pada logam esensial, maka
perlu dicurigai adanya suatu gejala defisiensi. Pada logam nonesensial,
kandungannya yang melebihi normal perlu dicurigai adanya gejala toksisitas.
nilai ambang batas konsentrasi menjadi relatif sangat berbeda untuk keperluannya
(Darmono, 1995).
2.7 Logam dalam Tubuh Makhluk Hidup
Pada tubuh makhluk hidup termasuk manusia logam dan mineral
mengalami proses biokimiawi dalam membantu proses fisiologis atau sebaliknya
menyebabkan toksisitas. Dalam sistem fisiologis manusia, unsur tersebut juga
dibagi menjadi dua bagian yaitu makroelemen, yang ditemukan dalam jumlah
relatif besar (lebih dari 0,005% dari berat badan) dan mikroelemen yang
ditemukan dalam jumlah relatif kecil (kurang dari 0,005% dari berat badan)
(Darmono, 2001).
Pada manusia jumlah makroelemen dari yang terbesar ke terkecil
berturut-turut adalah: kalsium (Ca), fosfor (P), potassium/ kalium (K), sulfur/ belerang (S),
sodium/natrium (Na), klor (Cl) dan magnesium (Mg). Sedangkan yang
mikroelemen berturut-turut: besi (Fe), iodium (I), tembaga (Cu), seng (Zn),
mangan (Mn), dan kobal (Co) (Darmono, 2001).
Logam atau mineral tersebut ada yang berikatan dengan protein dan ada
yang bersifat katalisator dalam cairan jaringan seperti menjaga pH darah maupun
membantu transfer sistem saraf motorik. Beberapa mineral yang sangat sedikit
terlibat dalam ikatan protein ialah: ion Na+, K+, Mg dan Co. Di lain pihak, logam
berbahaya (Cd, Pb, Hg, As) yang dapat menyebabkan toksik biasanya terikat
dengan protein sebagai metalotionein (Darmono, 2001).
Proses biokimiawi dalam tubuh makhluk hidup hampir selalu melibatkan
logam esensial sangat berperan aktivitasnya, baik dalam ikatannya dengan
protein, enzim maupun dalam bentuk lainnya (Darmono, 2001).
Manusia yang sehat dalam jaringan tubuhnya selalu ditemukan ion logam
yang normal. Sedangkan ion logam yang ditemukan terlalu rendah pada jaringan
tertentu, misalnya darah (Fe), hati (Cu), dapat digunakan untuk mendiagnosis
adanya kelainan pada orang yang bersangkutan, yang kemungkinan menderita
defisiensi atau penyakit lainnya (Darmono, 2001).
2.8 Spektrofotometri Serapan Atom
2.8.1 Prinsip Dasar Spektrofotometri Serapan Atom
Spektrofotometri serapan atom adalah suatu metode yang digunakan untuk
mendeteksi atom-atom logam dalam fase gas. Metode ini seringkali
mengandalkan nyala untuk mengubah logam dalam larutan sampel menjadi
atom-atom logam berbentuk gas yang digunakan untuk analisis kuantitatif dari logam
dalam sampel (Bender, 1987).
Spektroskopi serapan atom digunakan untuk analisis kuantitatif
unsur-unsur logam dalam jumlah sekelumit (trace) dan sangat kelumit (ultratrace). Cara analisis memberikan kadar total unsur logam dalam suatu sampel dan tidak
tergantung bentuk molekul dari logam dalam sampel tersebut (Rohman, 2007).
Cara ini cocok untuk analisis sekelumit logam karena mempunyai
kepekaan tinggi (batas deteksi kurang dari 1 ppm), pelaksanaan relatif sederhana,
dan interferensi sedikit. Spektrofotometri serapan atom didasarkan pada
penyerapan energi sinar oleh atom-atom netral dalam bentuk gas. Proses yang
serapan atom dengan cara absorbsi yaitu penyerapan energi radiasi oleh
atom-atom yang berada pada tingkat dasar. Atom-atom-atom tersebut menyerap radiasi pada
panjang gelombang tertentu, tergantung pada sifat atom tersebut (Rohman, 2007).
Sebagai contoh Timbal menyerap radiasi pada panjang gelombang 283
nm, dan Tembaga menyerap radiasi pada panjang gelombang 324 nm. Dengan
menyerap energi, maka atom akan memperoleh energi sehingga suatu atom pada
keadaan dasar dapat ditingkatkan menjadi ke tingkat eksitasi. Secara
eksperimental akan diperoleh puncak-puncak serapan sinar oleh atom-atom yang
dianalisis (Rohman, 2007).
Garis-garis spektrum serapan atom yang timbul karena serapan sinar yang
menyebabkan eksitasi atom dari keadaaan azas ke salah satu tingkat energi yang
lebih tinggi disebut garis-garis resonansi (Resonance line). Garis-garis ini akan dibaca dalam bentuk angka oleh Readout. Metode spektrofotometri serapan atom berdasarkan pada prinsip absorbsi cahaya oleh atom. Atom-atom akan menyerap
cahaya pada panjang gelombang tertentu, tergantung pada sifat unsurnya
(Rohman, 2007).
Kelemahan spektrofotometri serapan atom adalah sampel harus dalam
bentuk larutan dan tidak mudah menguap dan satu lampu katoda hanya digunakan
untuk satu unsur saja (Fifield, 1983).
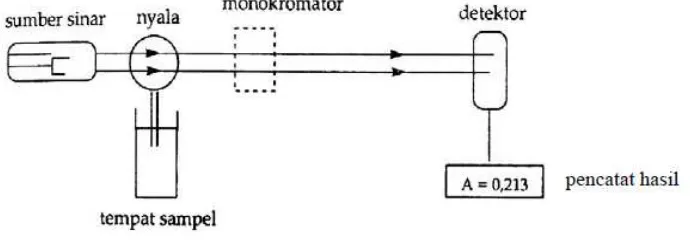
Adapun instrumentasi spektrofotometer serapan atom adalah sebagai
berikut:
Sumber radiasi yang digunakan adalah lampu katoda berongga (hallow cathode lamp). Lampu ini terdiri atas tabung kaca tertutup yang mengandung suatu katoda dan anoda. Katoda berbentuk silinder berongga yang dilapisi dengan
logam tertentu (Rohman, 2007).
b. Tempat Sampel
Dalam analisis dengan spektrofotometer serapan atom, sampel yang akan
dianalisis harus diuraikan menjadi atom-atom netral yang masih dalam keadaan
azas. Ada berbagai macam alat yang digunakan untuk mengubah sampel menjadi
uap atom-atomnya, yaitu:
1. Dengan nyala (Flame)
Nyala digunakan untuk mengubah sampel yang berupa cairan menjadi
bentuk uap atomnya dan untuk proses atomisasi. Suhu yang dapat dicapai oleh
nyala tergantung pada gas yang digunakan, misalnya untuk gas asetilen-udara
suhunya sebesar 22000C. Sumber nyala asetilen-udara ini merupakan sumber
nyala yang paling banyak digunakan. Pada sumber nyala ini asetilen sebagai
bahan pembakar, sedangkan udara sebagai bahan pengoksidasi (Rohman, 2007).
2. Tanpa nyala (Flameless)
Pengatoman dilakukan dalam tungku dari grafit. Sejumlah sampel diambil
sedikit (hanya beberapa µL), lalu diletakkan dalam tabung grafit, kemudian
tabung tersebut dipanaskan dengan sistem elektris dengan cara melewatkan arus
listrik pada grafit. Akibat pemanasan ini, maka zat yang akan dianalisis berubah
menjadi atom-atom netral dan pada fraksi atom ini dilewatkan suatu sinar yang
berasal dari lampu katoda berongga sehingga terjadilah proses penyerapan energi
Mesin AAS model ini sangat sensitif untuk mendeteksi logam-logam
dalam konsentrasi yang sangat kecil dalam sampel (ppb). Biasanya larutan yang
diperlukan hanya 1-100 uL dan dengan temperatur pembakaran dapat mencapai
3000oC (pembakaran secara elektrik) (Darmono, 1995).
Proses atomisasi dengan temperatur tinggi tersebut dapat
menyempurnakan proses pengatoman dari suatu larutan sampel. Logam yang
dapat dideteksi dengan mesin ini ialah Cd, Cu, Co, Zn, Pb, Mn, yang jumlahnya
relatif sedikit dalam jaringan biologi (Darmono, 1995).
Sistem kerja dari mesin ini melalui tiga tahap, yaitu pengeringan,
pengabuan, dan pembakaran cairan sampel, yaitu masing-masing dengan
temperature 500, 700, dan 3000oC. Tetapi temperatur dari tiga proses tahapan
tersebut dapat diatur dan disesuaikan dengan logam yang diukur secara
komputerisasi. Semua proses tahapan tersebut berjalan secara elektrik dan
otomatik yang dikontrol dengan komputer (Darmono,1995)
3. Monokromator
Monokromator merupakan alat untuk memisahkan dan memilih spektrum
sesuai dengan panjang gelombang yang digunakan dalam analisis dari sekian
banyak spektrum yang dihasilkan lampu katoda berongga (Rohman, 2007).
4. Detektor
Detektor digunakan untuk mengukur intensitas cahaya yang melalui
tempat pengatoman (Rohman, 2007).
Amplifier merupakan suatu alat untuk memperkuat signal yang diterima dari detektor sehingga dapat dibaca alat pencatat hasil (Readout) (Rohman, 2007).
6. Readout
Readout merupakan suatu alat penunjuk atau dapat juga diartikan sebagai pencatat hasil. Hasil pembacaan biasa dapat berupa angka atau berupa kurva yang
[image:33.595.124.469.285.407.2]menggambarkan absorbansi atau intensitas emisi (Rohman, 2007).
Gambar 1. Komponen Spektrofotometer Serapan Atom
2.8.2 Bahan Bakar dan Bahan Pengoksidasi
Umumnya bahan bakar yang digunakan adalah hidrogen, asetilen, dan
propan, sedangkan oksidatornya adalah udara, oksigen, dan NO2.
Gangguan-gangguan dapat terjadi pada saat dilakukan analisis dengan alat
spektrofotometer serapan atom, gangguan itu antara lain adalah:
a. Gangguan oleh penyerapan non-atomik
Gangguan ini terjadi akibat penyerapan cahaya dari sumber sinar yang
bukan berasal dari atom-atom yang akan dianalisis. Penyerapan non-atomic dapat
disebabkan adanya penyerapan cahaya oleh partikel-partikel pengganggu yang
berada di dalam nyala. Cara mengatasi penyerapan non-atomik ini adalah bekerja
b. Gangguan spektrum
Gangguan spektrum dalam spektrofotometer serapan atom timbul akibat
terjadinya tumpang tindih antara frekuensi-frekuensi garis resonansi unsur yang
dianalisis dengan garis-garis yang dipancarkan oleh unsur lain. Hal ini disebabkan
karena rendahnya resolusi monokromator (Mulja, 1995).
c. Gangguan kimia yang dapat mempengaruhi jumlah atau banyaknya atom di
dalam nyala.
Pembentukan atom-atom netral dalam keadaan azas di dalam nyala sering
terganggu oleh dua peristiwa kimia, yaitu:
● Disosiasi senyawa-senyawa yang tidak sempurna disebabkan terbentuknya
senyawa refraktorik (sukar diuraikan dalam api), sehingga akan mengurangi
jumlah atom netral yang ada di dalam nyala.
● Ionisasi atom-atom di dalam nyala akibat suhu yang digunakan terlalu tinggi.
Prinsip analisis dengan spektrofotometer serapan atom adalah mengukur
absorbansi atom-atom netral yang berada dalam keadaan azas. Jika terbentuk ion
maka akan mengganggu pengukuran absorbansi atom-atom yang mengalami
ionisasi tidak sama dengan spektrum atom dalam keadaan netral (Rohman, 2007).
2.9 Validasi Metode Analisis
Validasi metode analisis adalah suatu tindakan penilaian terhadap
parameter tertentu berdasarkan percobaan laboratorium untuk membuktikan
bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya. Beberapa
parameter analisis yang harus dipertimbangkan dalam validasi metode analisis
a. Kecermatan
Kecermatan adalah ukuran yang menunjukkan derajat kedekatan hasil
analisis dengan kadar analit yang sebenarnya. Kecermatan dinyatakan sebagai
persen perolehan kembali (recovery) analit yang ditambahkan. Kecermatan ditentukan dengan dua cara, yaitu:
• Metode Simulasi
Metode simulasi (Spiked-placebo recovery) merupakan metode yang dilakukan dengan cara menambahkan sejumlah analit bahan murni ke dalam suatu
bahan pembawa sediaan farmasi (plasebo), lalu campuran tersebut dianalisis dan
hasilnya dibandingkan dengan kadar analit yang ditambahkan (kadar yang
sebenarnya) (Harmita, 2004).
• Metode penambahan baku
Metode penambahan baku (standard addition method) merupakan metode yang dilakukan dengan cara menambahkan sejumlah analit dengan konsentrasi
tertentu pada sampel yang diperiksa, lalu dianalisis dengan metode yang akan
divalidasi. Hasilnya dibandingkan dengan sampel yang dianalisis tanpa
penambahan sejumlah analit. Persen perolehan kembali ditentukan dengan
menentukan berapa persen analit yang ditambahkan ke dalam sampel dapat
ditemukan kembali (Harmita, 2004).
Menurut Miller (2005), suatu metode dikatakan teliti jika nilai
recoverynya antara 80-120%. Recovery dapat ditentukan dengan menggunakan metode standar adisi.
Keseksamaan atau presisi diukur sebagai simpangan baku relatif atau
koefisien variasi. Keseksamaan atau presisi merupakan ukuran yang dapat
menunjukkan derajat kesesuaian antara hasil uji individual ketika suatu metode
dilakukan secara berulang untuk sampel yang homogen. Nilai simpangan baku
relatif yang memenuhi persyaratan adanya keseksamaan metode yang dilakukan
(Harmita, 2004).
c. Selektivitas (Spesifisitas)
Selektivitas atau spesifisitas suatu metode adalah kemampuannya yang
hanya mengukur zat tertentu secara cermat dan seksama dengan adanya
komponen lain yang ada di dalam sampel (Harmita, 2004).
d. Linearitas dan rentang
Linearitas adalah kemampuan metode analisis yang memberikan respon
baik secara langsung maupun dengan bantuan transformasi matematika,
menghasilkan suatu hubungan yang proporsional terhadap konsentrasi analit
dalam sampel. Rentang merupakan batas terendah dan batas tertinggi analit yang
dapat ditetapkan secara cermat, seksama dan dalam linearitas yang dapat diterima
(Harmita, 2004).
e. Batas deteksi dan batas kuantitasi
Batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat
dideteksi yang masih memberikan respon signifikan, sedangkan batas kuantitasi
merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi
kriteria cermat dan seksama (Harmita, 2004).
BAB III
2.1 Tempat dan Waktu Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Farmasi Kualitatif
Fakultas Farmasi Universitas Sumatera Utara dan di Laboratorium Penelitian
Fakultas Farmasi Universitas Sumatera Utara Medan pada bulan Juli
2011-Februari 2012.
2.2Bahan–bahan
Bahan yang digunakan semua pro analisis keluaran E.Merck, kecuali
disebutkan lain yaitu asam nitrat 65%, aquabidest, larutan baku Pb dan Cu
masing-masing dengan konsentrasi 10.000 ng/ml untuk Pb dan konsentrasi
10,000ng/ml untuk Cu.
2.2.1 Sampel
Sampel yang digunakan dalam penelitian ini adalah garam yang beredar
dipasaran sebanyak 4 macam yaitu garam dolina (A), garam tradisional (B),
garam ikan (C), garam A1 (D).
2.3 Alat – alat
Spektrofotometer Serapan Atom Hitachi Z-2000 lengkap dengan lampu
katoda tembaga dan timbal alat–alat gelas (Pyrex), hot plate, kertas saring Whatman no. 42, neraca analitik, pisau stainless stell, dan spatula.
2.4 Pembuatan Pereaksi
Larutan HNO3 5N dibuat dengan mengencerkan 340 ml HNO3 65%
dengan air suling hingga 1000 ml (Ditjen POM, 1995).
2.5 Prosedur Penelitian
2.5.1 Pengambilan sampel
Metode pengambilan sampel untuk garam tradisional dan garam ikan
dilakukan dengan cara acak, dan untuk garam dolina dan garam A-1 dilakukan
dengan cara sampling purposif yang dikenal juga sebagai sampling pertimbangan dimana sampel ditentukan atas dasar pertimbangan bahwa sampel yang diambil
dapat mewakili populasi (Sudjana, 2002).
2.5.2 Proses Destruksi
Sampel ditimbang sebanyak 20 gram dalam erlenmeyer, ditambahkan 15
ml HNO3 (e), didiamkan selama 24 jam, lalu dipanaskan hingga larutan berubah
menjadi jernih pada suhu 80oC selama kurang lebih 4 jam, didinginkan (Friel,
dengan modifikasi, 1986).
2.5.3 Pembuatan Larutan Sampel
Sampel hasil destruksi dimasukkan ke dalam labu tentukur 250 ml dan
diencerkan dengan akuabides hingga garis tanda. Kemudian disaring dengan
kertas saring Whatman No. 42, 10 ml filtrat pertama dibuang untuk menjenuhkan kertas saring kemudian filtrat selanjutnya ditampung ke dalam botol. Larutan ini
digunakan untuk analisa kualitatif dan kuantitatif.
2.6 Pemeriksaan Kuantitatif
Larutan baku Timbal (10.000 ppb) dipipet sebanyak 1 ml, dimasukkan ke
dalam labu tentukur 10 ml dan dicukupkan hingga garis tanda dengan akuabides
(konsentrasi 1000 ppb). Larutan untuk kurva kalibrasi logam Timbal dibuat
dengan memipet larutan sebanyak 0,5 ml, 1 ml, 1,5 ml, 2 ml, 2,5 ml, dilarutkan
dalam labu 25 ml sehingga didapatkan kosentrasi berturut-turut 20 ppb; 40 ppb;
60 ppb; 80 ppb; 100 ppb dan diukur pada panjang gelombang 283 nm dengan
menggunakan tipe nyala argon (Haswell, 1991).
2.6.2 Pembuatan Kurva Kalibrasi Tembaga
Larutan baku Tembaga (10000 ppb) dipipet sebanyak 1 ml, dimasukkan ke
dalam labu tentukur 10 ml dan dicukupkan hingga garis tanda dengan akuabides
(konsentrasi 1000 ppb). Lalu diambil larutan untuk kurva kalibrasi logam tembaga
dibuat dengan memipet larutan sebanyak 0,6 ml, 1,2 ml, 1,8 ml, 2,4 ml, 3 ml,
dilarutkan dalam labu 10 ml sehingga didapatkan kosentrasi berturut-turut 60
ppb; 120 ppb; 180 ppb; 240 ppb; 300 ppb dan diukur pada panjang gelombang
324 nm dengan menggunakan tipe nyala argon (Haswell, 1991).
2.7 Penetapan Kadar dalam Sampel
2.7.1 Penetapan Kadar Timbal
Larutan sampel diukur absorbansinya dengan menggunakan
spektrofotometer serapan atom pada panjang gelombang 283 nm. Nilai absorbansi
yang diperoleh harus berada dalam rentang kurva kalibrasi larutan baku Timbal.
Konsentrasi Timbal dalam sampel ditentukan berdasarkan persamaan garis regresi
dari kurva kalibrasi.
Larutan sampel diukur absorbansinya dengan menggunakan
spektrofotometer serapan atom pada panjang gelombang 324 nm. Nilai absorbansi
yang diperoleh harus berada dalam rentang kurva kalibrasi larutan baku tembaga.
Konsentrasi tembaga dalam sampel ditentukan berdasarkan persamaan garis
regresi dari kurva kalibrasi.
Kadar logam Timbal dan logam Tembaga dalam sampel dapat dihitung
dengan cara sebagai berikut:
(g) Sampel Berat
(ml) Volume x
(ng/ml) i
Konsentras (ng/g)
Logam
Kadar =
2.7.3 Penentuan Batas Deteksi (Limit of Detection) dan Batas Kuantitasi (Limit of Quantitation)
Batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat
dideteksi yang masih memberikan respon signifikan. Sedangkan batas kuantitasi
merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi
kriteria cermat dan seksama.
Batas deteksi dan batas kuantitasi ini dapat dihitung dengan rumus sebagai
berikut (Harmita, 2004):
Simpangan Baku =
(
)
2
2
− −
∑
n Yi Y
Batas deteksi (LOD) =
slope SB x
3
Batas kuantitasi (LOQ) =
slope SB x
10
2.7.4 Uji Akurasi dengan Persen Perolehan Kembali (Recovery)
logam dalam sampel ditentukan terlebih dahulu, selanjutnya dilakukan penentuan
kadar logam dalam sampel setelah penambahan larutan standar dengan
konsentrasi tertentu. Garam yang telah diketahui kadarnya ditimbang sebanyak 20
gram, lalu ditambahkan larutan baku tembaga 5000 ppb dan baku Timbal 4000
ppb, kemudian dilanjutkan dengan prosedur destruksi basah seperti yang telah
dilakukan sebelumnya.
Persen perolehan kembali dapat dihitung dengan rumus di bawah ini
(Harmita, 2004):
= 100%
an ditambahak yang
baku jumlah
awal sampel dalam
logam jumlah sampel
dalam logam al
jumlah tot − ×
2.8 Analisis Data Secara Statistik
2.8.1 Penolakan Hasil Pengamatan
Kadar Tembaga dan Timbal yang diperoleh dari hasil pengukuran masing-
masing ke enam larutan sampel, diuji secara statistik dengan uji Q (Rohman,
2009):
Q =
terendah Nilai
tertinggi Nilai
terdekat yang
Nilai dicurigai
yang Nilai
− −
Hasil pengujian atau nilai Q yang diperoleh ditinjau terhadap daftar harga Q
apabila Q>Qkritis maka data tersebut ditolak.
Tabel 1 Nilai Qkritis pada Taraf Kepercayaan 95% (Rohman, 2007) Banyak data Nilai Qkritis
4 0,831
5 0,717
6 0,621
7 0,570
Untuk menentukan kadar timbal dan tembaga di dalam sampel dengan interval kepercayaan 95%, α = 0,05, dk = n-1, dapat digunakan rumus (Wibisono,
2005) :
µ = X ± (t(α/2, dk) x SD / )
Keterangan :
−
X = Kadar rata-rata sampel SD = Standar Deviasi
dk = Derajat kebebasan (dk = n-1) α = interval kepercayaan
n = jumlah pengulangan 2.8.2 Pengujian Beda Nilai Rata-Rata
Sampel yang dibandingkan adalah independen dan jumlah pengamatan
masing-masing lebih kecil dari 30 dan variansi (σ) tidak diketahui sehingga
dilakukan uji F untuk mengetahui apakah variansi kedua populasi sama (σ1 = σ2)
atau berbeda (σ1≠ σ2) dengan menggunakan rumus:
Fo = 2
2 2 1
S S
Apabila dari hasilnya diperoleh Fo tidak melewati nilai kritis F maka dilanjutkan
dengan uji t dengan rumus:
(X1 – X2) to =
Sp √1/n1 + 1/n2
dan jika Fo melewati nilai kritis F maka dilanjutkan dengan uji t dengan rumus :
(X1 – X2) to =
√S12/n1 + S22/n2
Kedua sampel dinyatakan berbeda apabila to yang diperoleh melewati nilai kritis t,
dan sebaliknya (Sabri dan Hastono, 2006).
Keseksamaan atau presisi diukur sebagai simpangan baku relatif atau
koefisien variasi. Keseksamaan atau presisi merupakan ukuran yang menunjukkan
derajat kesesuaian antara hasil uji individual ketika suatu metode dilakukan secara
berulang untuk sampel yang homogen. Nilai simpangan baku relatif yang
memenuhi persyaratan menunjukkan adanya keseksamaan metode yang
dilakukan.
Adapun rumus untuk menghitung simpangan baku relatif adalah (Harmita, 2004):
Keterangan :
RSD = Relatif Standar Deviasi SD = Standar Deviasi
BAB IV
HASIL DAN PEMBAHASAN
3.1 Kurva Kalibrasi Tembaga (Cu) dan Pb (Timbal)
Kurva kalibrasi logam Pb dan Cu diperoleh dengan cara mengukur
absorbansi dari larutan standar Pb dan Cu pada panjang gelombang
masing-masing 283nm dan 324nm. Dari pengukuran kurva kalibrasi untuk Pb dan Cu
diperoleh persamaan garis regresi yaitu y = 0,00288x – 0,0155 untuk logam Cu, y
= 0,00177x + 0,00499 untuk logam Pb.
Kurva kalibrasi larutan standar Pb dan Cu dapat dilihat pada Gambar 1
dan Gambar 2.
Gambar 1. Kurva Kalibrasi Larutan Standar Tembaga
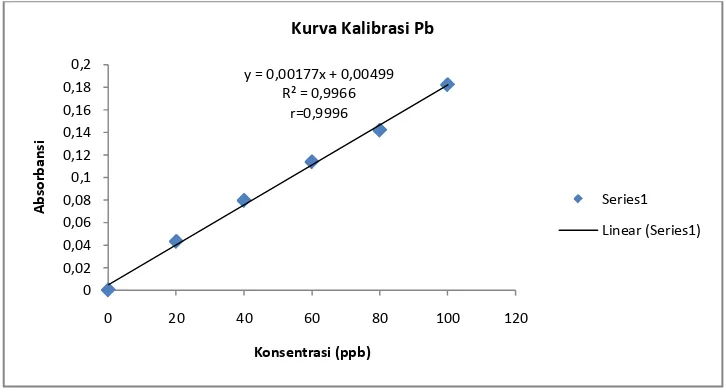
3.1.2 Kurva kalibrasi Timbal (Pb) dengan panjang gelombang 283 nm
Gambar 2. Kurva Kalibrasi Larutan Standar Timbal
Berdasarkan kurva di atas diperoleh hubungan yang linear antara
konsentrasi dengan absorbansi, dengan koefisien korelasi (r) untuk Cu sebesar
0,9983 dan untuk Pb sebesar 0,9983. Nilai r ≥ 0,95 menunjukkan bukti adanya
korelasi linear yang menyatakan adanya hubungan antara X dan Y (Shargel dan
y = 0,00288x - 0,0155 R² = 0,9965
r=0,9983
-0,1 0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 0,8 0,9
0 50 100 150 200 250 300 350
A
bs
o
rba
ns
i
Konsentrasi (ppb) Kurva Kalibrasi Cu
Series1 Linear (Series1)
y = 0,00177x + 0,00499 R² = 0,9966
r=0,9996
0 0,02 0,04 0,06 0,08 0,1 0,12 0,14 0,16 0,18 0,2
0 20 40 60 80 100 120
A
b
so
rb
a
n
si
Konsentrasi (ppb)
Kurva Kalibrasi Pb
[image:44.595.113.476.402.598.2]Andrew, 1999). Data hasil pengukuran absorbansi dan perhitungan persamaan
garis regresi larutan standar Cu dan Pb dapat dilihat pada Lampiran 3, halaman 38
sampai denganLampiran 4, halaman 40.
3.2 Kadar Tembaga (Cu) timbal (Pb) pada Garam
Penetapan kadar Cu dan Pb dilakukan secara spektrofotometri serapan
atom terhadap sampel garam dengan kode A, kode B, kode C, dan kode D yang
didestruksi basah dengan HNO3 sampai di peroleh larutan jernih, kemudian
didiamkan selama 24 jam, dilarutkan dengan aquabidest hingga 250 ml, dan
diukur pada spektrofotometer serapan atom pada panjang gelombang 324 nm
untuk Cu dan 283 nm untuk Pb.
Kadar Cu dan Pb dalam garam dengan kode A, kode B, kode C, dan kode
D diperoleh dari persamaan garis regresi larutan standarnya. Hasil analisis
kuantitatif Cu dan Pb dalam dalam garam dengan kode A, kode B, kode C dan
[image:45.595.108.504.522.668.2]kode D dapat dilihat pada Tabel 2 dan Tabel 3
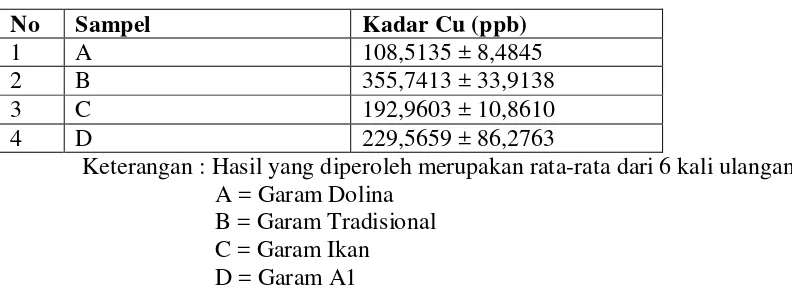
Tabel 2. Data kadar Cu (ppb) dalam garam berbagai merek
No Sampel Kadar Cu (ppb)
1 A 108,5135 ± 8,4845
2 B 355,7413 ± 33,9138
3 C 192,9603 ± 10,8610
4 D 229,5659 ± 86,2763
Keterangan : Hasil yang diperoleh merupakan rata-rata dari 6 kali ulangan A = Garam Dolina
B = Garam Tradisional C = Garam Ikan D = Garam A1
Tabel 3. Data kadar Pb (ppb) dalam berbagai merek
No Sampel Kadar Pb (ppb)
1 A 603,6946 ± 71,8142
3 C 678,4345 ± 232,4502
4 D 634,0952 ± 195,3195
Keterangan : Hasil yang diperoleh merupakan rata-rata dari 6 kali ulangan A = Garam Dolina
B = Garam Tradisional C = Garam Ikan D = Garam A1
Setelah itu dilakukan Uji beda nilai rata-rata kadar Cu dan Pb dalam garam
dolina, garam tradisional, garam ikan dan garam A1. Berdasarkan hasil uji beda
nilai rata–rata, terdapat perbedaan yang signifikan kadar rata–rata Tembaga (Cu)
[image:46.595.108.508.84.189.2]dan Timbal (Pb) dalam garam kode A, kode B, kode C dan kode D.
Tabel 4. Uji beda nilai rata - rata kadar Tembaga (Cu) dalam Garam
Jenis garam A B C D
A - b b b
B b - a a
C b a - a
D b a b -
Keterangan : a = Terdapat perbedaan yang signifikan b = Tidak terdapat perbedaan yang signifikan A = Garam Dolina
B = Garam Tradisional C = Garam Ikan D = Garam A1
Dari Tabel 4 dapat dilihat bahwa kandungan Cu pada garam dengan kode
A tetapi terdapat perbedaan yang signifikan dengan garam kode A, kode B dan
kode C. Kandungan Cu pada garam dengan kode B tidak terdapat perbedaan yang
signifikan dengan garam kode A, tetapi terdapat perbedaan yang signifikan
terhadap garam kode C, dan kode D. Kandungan Cu pada garam dengan kode C
terdapat perbedaan yang signifikan dengan garam kode B tetapi tidak terdapat
pada garam dengan kode D terdapat perbedaan yang signifikan dengan garam
kode B tetapi tidak terdapat perbedaan yang signifikan dengan garam kode A dan
kode C. Hasil uji beda nilai rata-rata Tembaga (Cu) dapat dilihat pada Lampiran
[image:47.595.106.518.223.447.2]13.
Tabel 5. Uji beda nilai rata kadar Timbal (Pb) dalam Garam
Jenis garam A B C D
A - a b b
B a - b b
C b b - b
D b b b -
Keterangan : a = Terdapat perbedaan yang signifikan b = Tidak terdapat perbedaan yang signifikan A = Garam Dolina
B = Garam Tradisional C = Garam Ikan
D = Garam A1
Dari Tabel 5 dapat dilihat bahwa kandungan Pb pada garam dengan kode
A terdapat perbedaan yang signifikan dengan garam kode B tetapi tidak terdapat
perbedaan yang signifikan terhadap garam kode C dan garam kode D. Kandungan
Pb pada garam kode B terdapat perbedaan yang signifikan terhadap garam kode A
tetapi tidak terdapat perbedaan yang signifikan terhadap garam kode C dan garam
kode D. Kandungan Pb pada garam kode C tidak terdapat perbedaan yang
signifikan terhadap kode A, kode B dan kode D. Kandungan Pb pada garam kode
D tidak terdapat perbedaan yang signifikan terhadap garam kode A, garam kode B
dan garam kode C. Hasil uji beda nilai rata-rata kadar timbal dapat dilihat pada
3.2 Uji Validasi
3.2.1 Batas Deteksi dan Batas Kuantitasi
Hasil pengujian sampel untuk pemeriksaan Cu diperoleh LOD 22,1600
ppb dengan LOQ 81,6991 ppb dan Pb diperoleh LOD 7,35 ppb dengan LOQ
24,46 ppb. Hasil yang diperoleh pada pengukuran sampel berada diatas batas
deteksi dan batas kuantitasi. Sehingga penetapan kadar Cu dan Pb memenuhi
persyaratan. Hasil pengujian batas deteksi dan batas kuantitasi dapat dilihat pada
Lampiran 3, halaman 22 sampai dengan Lampiran 4, halaman 23.
3.2.2 Uji Perolehan Kembali.
Hasil yang didapat dari uji perolehan kembali menunjukkan bahwa metode
ini memberikan ketepatan yang memuaskan, di mana didapat % uji perolehan
kembali untuk Cu adalah 81,39% dan Pb adalah 95,07%. Suatu metode dikatakan
teliti jika nilai recovery-nya antara 80-120% (Ermer dan Miller, 2005).
Berdasarkan hasil analisis di atas maka proses penetapan kadar Cu dan Pb
didalam keempat jenis garam tersebut telah memenuhi syarat uji validasi. Data
hasil dari uji perolehan kembali dari Tembaga dan Timbal dapat dilihat pada
BAB IV
KESIMPULAN DAN SARAN
4.1 Kesimpulan
1. Kadar Cu pada garam dolina adalah 108,5135 ± 8,4845 ppb, garam
tradisional adalah 355,7413 ± 33,9138 ppb, garam ikan adalah 192,9603 ±
10,8610 ppb, dan garam A1 adalah 229,5659 ± 33,9138 ppb.
2. Kadar Pb pada garam dolina adalah 603,6946 ± 71,8142 ppb, garam
tradisional seadalah 765,6632 ± 90,0570 ppb, garam ikan adalah 678,4345
± 232,4502 ppb, dan garam A1 adalah 634,0952 ± 195,3195 ppb.
3. Dari keempat jenis garam didapat bahwa garam tradisional memiliki
kandungan Cu dan Pb yang lebih besar dibandingkan garam dolina, garam
ikan dan garam A1.
4.2 Saran
Disarankan kepada peneliti selanjutnya agar memeriksa adanya
kemungkinan logam berbahaya lain yang terdapat dalam garam.
DAFTAR PUSTAKA
Bender, G.T. (1987). Principal of Chemical Instrumentation. Philadelphia: W.B.Sounders Company. Halaman 98.
Burhanuddin, S. (2001). Forum Pasar Garam Indonesia. Jakarta: Departemen Kelautan dan Periklanan. Halaman 15-29.
Darmono. (1995). Logam dalam Sistem Biologi Makhluk Hidup. Jakarta: Universitas Indonesia. Halaman 124.
Darmono. (2001). Lingkungan hidupdan Pencemaran. Jakarta: Universitas Indonesia. Halaman 47, 109.
Ditjen POM. (1995). Farmakope Indonesia. Edisi ke-empat. Jakarta: Departemen Kesehatan RI. Halaman 1067.
Ermer, J., dan Miller, J.H.M. (2005). Method Validation in Pharmaceutical Analysis. A Giude to Best Practice. Weinheim: Wiley-VCH. Halaman 89. Fifield, F.W. (1983). Principles and Practice of Analytical Chemistry. Edisi
Kedua. London: International Textbook Company Limited. Halaman. 10, 277.
Harmita. (2004). Majalah Ilmu Kefarmasian . Review Artikel. Petunjuk Pelaksanaan Validasi Metoda dan Cara Perhitungannya. Halaman 119, 130, 131.
Haswell, S.J. (1991). Atomic Absorption Spectrometry. Amsterdam: Elsevier. Halaman 202, 207, 208.
Khopkar, S.M. (1990). Konsep Dasar Kimia Analitik. Penerjemah: A. Saptorahardjo. Jakarta: UI Press. Halaman 283.
Mulja, M. (1995). Metode Spektrofotometri Serapan Atom. Bandung: Penerbit Universitas Gajah Mada. Halaman. 87.
Palar, H. (2004). Pencemaran dan Toksikologi Logam Berat. Jakarta: Penerbit Rineka Cipta. Hal. 24, 76-84.
Rohman, A. (2007). Kimia Farmasi Analisis. Yogyakarta: Pustaka Pelajar. Halaman 22.
Shargel, L., dan Andrew, B. C. (1999). Applied Biopharmaceutics and Pharmacokinetics. USA: Prentice-Hall International, INC. Halaman 15. Sabri, L., dan Hastono, S.P. (2006). Statistik Kesehatan. Jakarta: PT Raja
Grafindo Persada. Halaman 112-118.
Hal.93, 168- 169.
Suharto. (2005). Dampak Pencemaran Logam Timbal (Pb) terhadap Kesehatan Masyarakat.
http://pusdiknakes.or.id/pusatdata/?show=detailnews&kode=880&tbl= kesling
Wibisono, Y. (2005). Metode Statistik. Cetakan Pertama.Yogyakarta: Gadjah Mada University Press. Hal. 451-452.
Lampiran 2. Bagan alir pembuatan larutan sampel Garam
Didinginkan
Hasil
Ditimbang 20 gram
Ditambahkan 15ml HNO3 5N
Lampiran 3. Hasil Pengukuran Absorbansi Larutan Standar Timbal(Pb), Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r)
dari Data Kalibrasi Pb.
1. Hasil pengukuran absorbansi larutan standar Pb
Dimasukkan dalam labu tentukur 250ml
Dicukupkan volumenya dengan aquabidest sampai garis tanda
Disaring dengan kertas whatmann no.42 dengan membuang 10 ml larutan pertama
Larutan digunakan untuk uji kuantitatif Sampel hasil
destruksi
No Konsentrasi (ppb) Absorbansi
1 0 0,0003
2 20 0,0433
3 40 0,0796
4 60 0,1138
5 80 0,1418
6 100 0,1822
2. Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r)
No X Y X2 Y2 XY
1 0 0,0003 0 9.10-8 0
2 20 0,0433 400 1,874.10-3 0,866
3 40 0,0796 1600 6,336.10-3 3,184
4 60 0,1138 3600 0,0129 6,828
5 80 0,1418 6400 0,0201 11,344
6 100 0,1822 10000 0,0331 18,22
∑X = 300
∑Y = 0,561 ∑X2 = 22000 ∑Y2=0,0743 XY = 40,442
X = 50 Y= 0,0935
a =
( )( )
( )
n x x
n y x -xy
2
2
∑
∑
∑
∑
∑
−
a =
6 300 220000
6 ) 561 , 0 )( 300 ( 40,422
2
− −
a = 1,7702.10-3
b = y- ax
= 0,0935 – (1,7702.10-3)(50)
= 4,99.10-3
r =
( )( )
(
) ( )
(
) ( )
− −∑
∑
∑
∑
∑
∑
∑
n y y n x x n y x -xy 2 2 2 2(
) ( )
(
) (
−)
− − = 6 561 , 0 0743 , 0 6 300 22000 6 ) 561 , 0 )( 300 ( 442 , 40 r 2 2r = 0,9983
Lampiran 4. Hasil Pengukuran Absorbansi Larutan Standar Tembaga (Cu), Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r) dari Data Kalibrasi Cu
1. Hasil Pengukuran Absorbansi Larutan Standar Cu
No Konsentrasi (ppb) Absorbansi
1 0 0,0014
2 60 0,1285
3 120 0,3256
4 180 0,5164
5 240 0,6940
6 300 0,8340
2. Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r)
No X Y X2 Y2 XY
1 0 0,0014 0 0,00001 0
2 60 0,1285 3600 0,0165 7,7100
3 120 0,3256 14400 0,1060 39,0720
4 180 0,5164 32400 0,2666 92,9520
5 240 0,6940 57600 0,4816 166,5600
6 300 0,8340 90000 0,6956 250,2000
∑X = 900 ∑Y = 2,4999 ∑X2 = 198000 ∑Y2
=1,5663 XY = 566,4940
X = 150
a =
( )( )
( )
n x x n y x -xy 2 2∑
∑
∑
∑
∑
− a = 6 (900) 198000 6 ) 4999 , 2 )( 900 ( 566,4940 2 − −a = 2,881.10-3
b = y- ax
= 0,4166 – (2,881.10-3)(150)
= -0,0155
Persamaan Regresinya adalah y = 2,881.10-3x – 0,0155
r =
( )( )
(
) ( )
(
) ( )
− −∑
∑
∑
∑
∑
∑
∑
n y y n x x n y x -xy 2 2 2 2(
) ( )
(
) (
−)
− − = 6 4999 , 2 5663 , 1 6 900 198000 6 ) 4999 , 2 )( 900 ( 494 , 556 r 2 2r = 0,9996
Lampiran 5. Perhitungan Batas Deteksi dan Batas Kuantitasi Pb Persamaan garis regresi : Y = 1,7702.10-3 x + 4,99.10-3
No
Konsentrasi (X)
Absorbansi
(Y) Yi Y – Yi
(. 10 -3)
(Y – Yi)2 .
10 -5
1 0 0.0003 0,0049 -4,69 2,199
2 20 0.0433 0,0404 3 0,9
4 60 0.1138 0,1112 2,6 0,676
5 80 0.1418 0,1466 -4,8 2,304
6 100 0.1822 0,1820 0,2 0,004
n = 6 ∑ (Y – Yi)2
= 7,523 x 10-5
SD =
(
)
2 -n
Yi 2
∑
Y−=
4
0,00007523
= 4,336 x 10-3
LOD = Slope SD x 3 LOD = 0,0018 0,004336 x 3
= 7,35 ppb
LOQ = Slope SD x 10 LOQ = 0,0018 0,004336 x 10
= 24,46 ppb
Lampiran 6. Perhitungan Batas Deteksi dan Batas Kuantitasi Cu Persamaan garis regresi : Y = 2,881.10-3 x - 0,0155
No
Konsentrasi (X)
Absorbansi
(Y) Yi Y – Yi (Y – Yi)2 .
10 -4
1 0 0.0014 -0,0155 0,0169 2,8561
2 60 0.1285 0,1574 -0,0280 7,84
3 120 0.3256 0,3302 0,0046 0,2116
4 180 0.5164 0,5031 0,0132 1,7424
5 240 0.694 0,6759 0,0181 3,2761
6 300 0.834 0,8488 0,0148 2,19
n = 6 ∑(Y – Yi)2
= 18,11 x 10-4
SD =
(
)
2 -n
Yi 2
∑
Y−LOD =
0,002881 0,021 x 3
= 22,16 ppb
LOQ =
Slope SD x 10
LOQ =
0,002881 0,021 x 10
= 81,6991 ppb
Lampiran 7. Contoh Perhitungan Hasil Penetapan kadar Pb dalam Garam Dolina
Dengan Menggunakan Persamaan Garis Regresi
Contoh perhitungan konsentrasi Pb dalam sampel yang beratnya 20,012 g dan
absorbansi 0,0858.
X = Konsentrasi sampel
Y = Absorbansi sampel
Persamaan garis regresi yang diperoleh dari kurva kalibrasi adalah
Y = 1,7702.10-3 X + 4,99.10-3
X =
00177 , 0
00499 , 0 0858 ,
0 −
X = 45,6554 ppb
Maka konsentrasi sampel tersebut adalah 45,6554 ppb
Kadar =
W CxV
Keterangan : C = Konsentrasi larutan sampel (ppb)
V = Volume larutan sampel (ml)
Fp = Faktor Pengenceran
Kadar =
g ml ppbx
012 . 20
250 6554
, 45
= 0,5703 ppb
Maka kadar Pb yang terkandung dalam sampel adalah 0,5703 ppb.
Lampiran 8. Data Hasil Berat Sampel, Absorbansi, Konsentrasi, dan Kadar Logam Pb dalam dengan 6 kali Replikasi
Garam Dolina
No Perlakuan Berat Sampel (g)
Absorbansi Konsentrasi (ppb)
Kadar (ppb)
1 Garam Dolina
20,012 0,0858 45,6554 570,3503 20,023 0,0909 48,5367 606,0118 20,014 0,0861 45,8249 572,4106 20,034 0,0968 51,8700 647,4867 20,046 0,1059 57,0114 711,0072 20,000 0,0779 41,1921 514,9013
Garam Tradisional
No Perlakuan Berat Sampel (g)
Absorbansi Konsentrasi (ppb)
2 Garam Tradisional
20,032 0,1293 70,2316 876,4926 20,012 0,1208 65,4294 817,3771 20,022 0,1223 66,2768 827,5496 20,000 0,0992 53,2259 665,3237 20,002 0,1030 55,3729 692,0920 20,009 0,1063 57,2373 715,1444
Garam Ikan
No Perlakuan Berat Sampel (g)
Absorbansi Konsentrasi (ppb)
Kadar (ppb)
3 Garam Ikan 20,040 0,1118 60,3446 752,8019 20,008 0,0895 47,7457