LAMPIRAN A
FLOWCHART
A.1 FLOWCHART PROSEDUR PENELITIAN
A.1.1 Flowchart Prosedur Analisis pH
A.1.2 Flowchart Prosedur Analisis M-Alkalinity
Mulai
Dimasukkan 5 ml sampel ke dalam beaker glass
Selesai
Dicatat volume HCl yang terpakai
Ditambahkan aquadest hingga volume larutan menjadi 80 ml
Diaduk campuran hingga homogen dengan magnetic stirrer
Dimasukkan pH elektroda ke dalam beaker glass
Apakah bacaan pH mencapai 4,8±0,02?
Dititrasi campuran dengan HCl 0,1 N
Tidak
Ya
Dihitung nilai alkalinitas menggunakan persamaan 3.1
A.1.3 Flowchart Prosedur Analisis Total Solids (TS)
Mulai
Dipanaskan cawan penguap selama 2 jam pada suhu 105 oC
Diambil sampel dan masukkan ke dalam cawan
Selesai
Didinginkan cawan penguap selama 15 menit di dalam desikator
Ditimbang berat cawan
Didinginkan cawan penguap selama 15 menit di dalam desikator
Dimasukkan cawan berisi sampel ke oven pada suhu 103-105oC selama 1 jam
Didinginkan cawan penguap selama 15 menit di dalam desikator
Ditimbang berat cawan
Apakah berat cawan sudah konstan?
Tidak
Ya
Dihitung nilai total solids(TS) menggunakan persamaan 3.2
A.1.4 Flowchart Prosedur Analisis Volatile Solids (VS)
Gambar A.4 Flowchart Prosedur Analisis Volatile Solids (VS)
Gambar A.5 Flowchart Prosedur Analisis Total Suspended Solids (TSS)
A.1.6 Flowchart Prosedur Analisis Volatile Suspended Solids (VSS)
A.1.7 Flowchart Prosedur Analisis Chemical Oxygen Demand (COD)
A.1.8 Flowchart Prosedur Loading Up dan Operasi Target
LAMPIRAN B
DATA HASIL ANALISA
B.1 KARAKTERISTIK LIMBAH CAIR PABRIK KELAPA SAWIT
(LCPKS)
Tabel B.1 Hasil Analisis Karakteristik LCPKS dari PTPN IV PKS Adolina
No Parameter Satuan Hasil Uji Metode Uji
1. pH - 3,5–4,8 APHA 4500-H
2. Chemical Oxygen Demand (COD)
mg/L 41.818 SNI 06–6989.15–2004
3. Total Solid (TS) mg/L 16.040–61.000 APHA 2540B
4. Volatile Solid (VS) mg/L 16.060–52.360 APHA 2540E 5. Total Suspended
Solid (TSS)
mg/L 2.920–24.700 APHA 2540D 6. Volatile Suspended
Solid (VSS)
mg/L 9.100–22.680 APHA 2540E
7. Lemak % 31,8 Ekstraksi Sokletasi
8. Protein % 0,14 Kjeldahl
9. Karbohidrat % 1,99 Lane Eynon
10. Volatile fatty acids - Asam asetat - Asam propionat - Asam butirat
mg/L
1.508,987 560,030 1.088,613
APHA 2540E
* Laporan hasil uji laboratorium terlampir
B.2 DATA HASIL PENELITIAN
B.2.1 Data Hasil Penelitian pada Variasi Hydraulic Retention Time (HRT)
Tabel B.2 Data Hasil Analisis pH, Alkalinitas, TS, VS, TSS dan VSS pada Variasi
Hydraulic Retention Time (HRT)
HRT Hari
Ke- pH
Alkalinitas (mg/L) TS (mg/L) VS (mg/L) TSS (mg/L) VSS (mg/L) 20
1 5,9 2.600 32.980 17.300
2 5,9 3.000 31.900 24.220
3 5,8 2.700 30.040 21.220
4 5,8 2.200 38.300 22.000
5 6,0 4.200 37.960 23.320
6 5,9 2.850 36.580 25.060
7 5,8 4.100 40.180 22.500
8 6,0 3.600 46.320 24.980
9 6,1 2.500 38.980 19.400
10 6,4 3.350 40.540 23.860 14.300 1.060
12 6,2 3.400 37.940 25.680
13 6,1 3.100 3.8160 20.100 20.240 16.680
14 6,0 3.000 31.320 20.460
15 5,7 2.800 27.500 11.040 13.820 7.380
15
1 5,9 2.300 24.180 12.620
2 5,8 2.250 38.420 24.980
3 5,9 2.600 39.140 23.840
4 5,9 2.450 37.720 27.040
5 6,0 2.550 35.680 26.240
6 6,1 3.400 36.760 25.840
7 6,2 3.500 22.140 27.460
8 6,1 3.300 38.560 23.540
9 6,0 3.500 35.000 24.600
10 6,1 3.000 43.240 24.600 17.880 14.940
11 6,1 3.800 33.280 29.920
12 6,1 3.200 33.460 23.960
13 6,5 2.900 33.460 22.160 22.160 19.260
14 6,1 3.200 34.980 26.080
15 6,1 3.200 28.700 20.100 18.380 16.080
10
1 6,2 1.850 26.520 20.760
2 6,1 1.500 30.020 22.660
3 6,2 1.500 30.360 23.540
4 5,9 1.500 31.960 24.000
5 5,9 1.600 29.800 23.840
6 6,0 1.500 40.400 32.000
7 5,9 1.900 35.780 27.960
8 6,0 2.100 28.220 21.760
9 6,0 3.000 30.800 23.220
10 6,1 2.000 26.360 20.000 11.740 10.840
11 6,2 2.600 45.980 13.180
12 6,2 2.700 32.460 16.080
13 6,2 1.850 32.220 25.220 15.060 13.220
14 6,1 1.500 32.700 24.560
15 6,0 1.500 33.180 24.340 14.880 12.400
4
1 6,2 2.800 32.580 22.900
2 6,2 2.600 29.620 22.560
3 6,2 1.300 30.000 21.740
4 6,0 1.700 22.480 16.180
5 6,2 2.100 32.640 24.200
6 6,0 1.600 31.780 23.220
7 5,8 1.700 26.620 19.940
8 5,8 1.400 37.340 30.080
9 5,9 1.400 38.980 31.820
10 6,0 2.000 35.140 24.540 22.680 21.060
11 5,9 3.000 34.620 23.280
12 6,1 2.700 35.420 25.360
14 6,1 2.400 36.220 25.020
15 5,9 1.800 33.900 24.540 23.040 21.460
Tabel B.3 Data Hasil Analisis Chemical Oxygen Demand (COD) pada Variasi
Hydraulic Retention Time (HRT)
HRT Hari ke-
COD
Influent
(mg/L)
Effluent
(mg/L) Reduksi (%) Rata-Rata (%)
20 10 13 15 41.818,20 25.454,55 18.181,82 12.727,27 39,13 56,52 69,57 55,07 15 10 13 15 41.818,20 27.272,73 27.272,73 18.181,82 34,78 34,78 56,52 42,03 10 10 13 15 41.818,20 21.818,18 25.454,55 23.636,36 47,83 39,13 43,48 43,48 4 10 13 15 41.818,20 27.272,73 23.636,36 21.818,18 34,78 43,48 47,83 42,03
Tabel B.4 Data Hasil Analisis Pembentukan Volatile Fatty Acid (VFA) pada Variasi
Hydraulic Retention Time (HRT)
HRT Hari ke- VFA (mg/L)
Asetat Propionat Butirat Total
20 10 13 15 2.910,000 2.735,549 2.629,137 1.068,946 1.201,619 1.186,063 813,024 1.248,874 2.182,688 4.791,969 5.186,042 5.997,888 15 10 13 15 2.307,918 1.684,699 2.087,888 1.029,314 973,829 1.079,020 945,973 729,765 1.279,975 4.283,205 3.388,294 4.446,883 10 10 13 15 555,301 2.550,048 1.657,315 885,528 1.050,648 1.073,538 297,263 1.358,740 1.376,889 1.738,092 4.959,436 4.107,743 4 10 13 15 2.860,277 2.787,013 1.631,733 728,631 789,227 604,556 1.703,050 2.541,272 1.338,564 5.291,958 6.117,512 3.574,848
Tabel B.5 Data Perhitungan Rasio VFA/Alkalinitas pada Variasi Hydraulic
Retention Time (HRT)
HRT Rata-Rata Total VFA (mg/L)
Rata-Rata
Alkalinitas (mg/L) VFA/Alkalinitas
20 5.325,300 3093,333 1,72
15 4.039,461 3010,000 1,34
10 3.601,757 2050,000 1,76
B.2.2 Data Hasil Penelitian pada Variasi Laju Pengadukan
Tabel B.6 Data Hasil Analisis pH, Alkalinitas, TS, VS, TSS dan VSS pada Variasi Laju Pengadukan
Laju Pengadukan
(rpm)
Hari ke- pH Alkalinitas (mg/L) TS (mg/L) VS (mg/L) TSS (mg/L) VSS (mg/L) 50 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 6,29 6,18 6,15 6,07 5,97 6,10 6,20 6,18 6,15 6,01 6,12 6,20 6,11 5,98 5,90 2.380 2.330 2.210 2.280 2.100 2.190 2.370 2.410 2.250 1.860 2.270 2.430 2.230 2.280 2.290 31.180 31.480 29.760 27.560 26.560 29.420 28.800 31.140 30.000 31.390 28.600 34.100 23.920 16.600 21.100 21.660 22.140 21.800 19.440 18.700 20.500 21.300 23.120 21.780 26.450 20.620 21.520 21.320 13.020 15.140 11.360 11.020 9.820 8.600 7.933 6.900 100 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 6.20 6.07 6,12 6,00 6,20 6,00 5,95 5,85 5,90 6,00 5,95 6,05 6,10 6,18 5,92 2.650 2.490 2.550 2.450 2.700 2.470 2.190 2.210 1.940 2.290 2.210 2.320 2.220 2.310 2.290 35.960 34.220 32.120 33.260 28.740 27.280 29.600 25.740 27.340 27.040 30.360 26.960 23.680 21.780 23.160 24.700 23.980 21.360 24.460 15.340 15.380 16.680 16.760 18.800 18.740 22.200 20.580 16.240 16.120 15.900 9.860 9.180 10.520 6.313 7.713 5.907 150 1 2 3 4 5 6 7 8 9 10 11 6,20 6,20 6,20 6,00 6,20 6,00 5,80 5,80 5,90 6,00 5,90 2.800 2.600 1.300 1.700 2.100 1.600 1.700 1.400 1.400 2.000 3.000 32.580 29.620 30.000 22.480 32.640 31.780 26.620 37.340 38.980 35.140 34.620 22.900 22.560 21.740 16.180 24.200 23.220 19.940 30.080 31.820 24.540 23.280
12 13 14 15 6,10 6,10 6,10 5,90 2.700 2.600 2.400 1.800 35.420 35.500 36.220 33.900 25.360 26.380 25.020 24.540 20.240 13.820 17.867 8.567 200 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 6,22 6,15 5,97 6,22 6,20 6,15 6,21 6,20 6,12 5,98 5,80 6,01 6,18 6,20 6,05 2.690 2.450 2.300 2.500 2.390 2.550 2.470 2.580 2.410 2.250 2.310 2.390 2.370 2.400 2.280 24.620 33.520 39.660 31.340 28.840 27.400 29.340 30.660 31.120 31.680 29.120 26.440 32.480 32.600 20.020 17.400 23.960 29.640 21.200 20.440 19.780 19.940 22.440 22.140 24.360 21.360 15.620 23.940 19.680 17.300 14.300 22.220 9.820 11.720 15.060 8.180
Tabel B.7 Data Hasil Analisis Chemical Oxygen Demand (COD) pada Variasi Laju Pengadukan Laju Pengadukan (rpm) Hari ke- COD Influent (mg/L) Effluent
(mg/L) Reduksi (%) Rata-Rata (%)
50 10 13 15 41.304,35 20.652,17 25.000,00 25.000,00 50,00 39,47
39,47 42,98
100 10 13 15 41.304,35 28.260,87 23.913,04 22.826,09 31,58 42,11 44,74 39,47 150 10 13 15 41.818,20 27.272,73 23.636,36 21.818,18 34,78 43,48 47,83 42,03 200 10 13 15 41.304,35 19.565,22 28.260,87 20.652,17 52,63 31,58 50,00 44,74
Tabel B.8 Data Hasil Analisis Pembentukan Volatile Fatty Acid (VFA) pada Variasi Laju Pengadukan Laju Pengadukan (rpm) Hari ke- VFA (mg/L)
Asetat Propionat Butirat Total
13 15 2.508,672 2.218,381 1.064,353 1.230,436 1.317,243 2.165,420 4.890,268 5.614,237 150 10 13 15 2.860,277 2.787,013 1.631,733 728,631 789,227 604,551 1.703,050 2.541,272 1.338,564 5.291,958 6.117,512 3.574,848 200 10 13 15 906,065 428,591 671,321 1.090,132 885,677 948,569 1.630,893 1.705,870 910,731 3.627,090 3.020,137 2.530,621
Tabel B.9 Data Perhitungan Rasio VFA/Alkalinitas pada Variasi Laju Pengadukan
Laju Pengadukan (rpm) Rata-Rata Total VFA (mg/L) Rata-Rata Alkalinitas (mg/L) VFA/Alkalinitas
50 3.382,265 2.258,667 1,50
100 4.626,646 2.352,667 1,97
150 4.994,773 2.073,333 2,41
LAMPIRAN C
CONTOH PERHITUNGAN
C.1 PERHITUNGAN REDUKSI COD
Adapun contoh perhitungan Reduksi COD untuk data HRT 4 data diambil dari Tabel B.3 menunjukan data COD influent dan COD efflent yaitu sebagai berikut:
COD influent = 41.818,20 mg/L COD effluent = 24.242,42 mg/L
Degradasi COD (%) = 100%
COD COD COD × − influent effluent influent
= 100%
20 , 818 . 41 42 , 242 . 24 20 , 818 . 41 × − = 42,03 %
C.2 PERHITUNGAN STANDAR DEVIASI
Adapun contoh perhitungan standar deviasi pada VS untuk rasio laju pengadukan 100 rpm adalah sebagai berikut dan dari Tabel A.5 menunjukkan data VS pada variasi rasio laju pengadukan 100 rpm
Tabel B.1 Data VS untuk variasi laju pengadukan 100 rpm Hari ke VS (mg/L) Hari ke VS (mg/L)
1 2 3 4 5 6 7 8 24,700 23,980 21,360 24,460 15,340 15,380 16,680 16,760 9 10 11 12 13 14 15 18,800 18,740 22,200 20,580 16,240 16,120 15,900
Standar deviasi =
(
)
(
1)
2 2 − −∑
∑
n n X Xn i i
∑
2 iX = 7.011.012.400
Standar deviasi =
(
)
(
15 1)
15
287.700
-.400) (7.011.012
15 2
LAMPIRAN D
DOKUMENTASI
Gambar D.1 Tangki Umpan
Gambra C.3 Botol Keluaran Fermentor (Discharge)
Gambar D.4 Botol Penampung Biogas (Gas Collector)
Gambar D.6 Rangkaian Peralatan
Gambar D.7 Peralatan Analisis M-Alkalinity
Gambar D.9 Peralatan Analisis Padatan Tersuspensi
Gambar D.10 Peralatan Analisis Chemical Oxygen Demand (COD)
Gambar D.12 Desikator
Gambar D.13 Oven
LAMPIRAN E
HASIL UJI LABORATORIUM
E.1 HASIL UJI LABORATORIUM UNTUK ANALISIS LEMAK
E.2 HASIL UJI LABORATORIUM UNTUK ANALISIS PROTEIN
DALAM LIMBAH CAIR PABRIK KELAPA SAWIT (LCPKS)
E.3 HASIL UJI LABORATORIUM UNTUK ANALISIS
KARBOHIDRAT DALAM LIMBAH CAIR PABRIK KELAPA
E.4 HASIL UJI LABORATORIUM UNTUK ANALISIS VOLATILE
E.5 HASIL UJI LABORATORIUM UNTUK ANALISIS VOLATILE
DAFTAR PUSTAKA
[1] Harsono Soni Sisbudi, Philipp Grundmann and S. Soebronto. Anaerobic Treatment of Palm Oil Mill Effluent : Potential Cantribution to Net Energy Yield and Reduction of Greenhouse Gas Emission from Biodisel Production. Journal of
Cleaner Production 64 (2014) page : 619-627
[2] Yunus Ahmed, Zahira Yaakob, Parul Akhtar and Kamaruzzaman Sopian. Production of Biogas and Performance Evaluation of Existing Treatment Processes in Palim Oil Mill Effluent (POME). Renewable and Sustainable Energy Review 42 (2015) page : 1260-1278
[3] Ratih Rosita, Haryadi dan Amril. Determinan Ekspor CPO Indonesia. Jurnal
Perspektif Pembiayaan dan Pembangunan Daerah Vol.1 No.4 April-Juni 2014 ISSN
2338-4603
[4] Edwi Mahajoeno, Bibiana Widiyati Lay. Surjono Hadi Sutjahjo dan Siswanto.
Potensi Limbah Cair Pabrik Minyak Kelapa Sawit untuk Produksi Biogas.
Biodiversitas Vol.9 No.1 ISSN:1412-033X Januari 2008 Hal : 48-52
[5] Okwute Ojonoma L and Ijah Udeme J.J. Bioremediation Of Palm Oil Mill Effluent (Pome) Polluted Soil Using Microorganisms Found In Organic Wastes. The
International Journal of Biothecnology Vol.3(3) (2014) page : 32-46
[6] Joo-Young Jeong, Sung-Min Son, Jun-Hyeon Pyon and Joo-Yang Park. Performance Comparison Between Mesophilic and Thermophilic Anaerobic Reactors fro Treatment of Palm Oil Mill Effluent. Bioresource Technology 165 (2014) page 74-82
[7] Elijah Ige Ohimain and Sylvester Chibueze Izah. Potential Of Biogas Production From Palm Oil Mills Effluent In Nigeri. Sky Journal of Soil Science and
Environmental Management Vol. 3(5) ISSN 2315-8794 (June 2014) page : 50–58
[8] Ojikutu Abimbola O and Osokoya Olumide O. Evaluation of Biogas Production from Food Waste. The International Journal of Engineering and Science
(IJES) Vol.3 Issue 03 pp:01-07 ISSN(e): 2319-1813 ISSN(p): 2319-1805. 01 July
2014
[9] Alexander Kowalczyk, Eva Harnisch, Sebastian Schwede, Mandy Gerber and Ronald Span. Different Mixing Modes for Biogas Plants Using Energy Crop. Applied
Energy 112 (2013) page 465-472
Two-State CSTR System : Effect of Hydraulic Time. Journal International Bioresource
Technology 175 (2015) page : 553-562
[11] Johan Lindmark, Per Eriksson and Eva Thorin. The Effect of Different Mixng Intensities During Anaerobic Digestion of The Organic Fraction of Municipal Solid Waste. Waste Management 34 (2014) page 1391-1397
[12] Sophia Ghanimeh, Mutasem El Fadel and Pascal Saikaly. Mixing Effect on Thermophilic Anaerobic Digestion of Source-Sorted Organic Fraction of Municipal Solid Waste. Bioresource Technology 117 (2012) page : 63-71
[13] K. Kamemoto, Y.G. Lim, N. Nagao. Y. Onoue, C. Niwa and T. Toda. Effect ot Temperature on VFA’s and Biogas Production in Anaerobic Solubilization on Food Waste. Waste Management 29 (2009) page : 2950-2955
[14] Maneerat Khemkhao, Somkiet Techkarnjanaruk and Chantaraporn Phalakornkule. Simultaneous Tratment of Raw Palm Oil Mill and Biodegradation of Palm Fiber in a High-Rate CSTR. Bioresource Technology 177 (2015) page 17-27 [15] Man Kee Lam and Keat Teong Lee. Renewable and Sustainable Bioenergies Production from Palm Oil Mill Effluent (POME): Win–Win Strategies Toward Better Environmental Protection. Journal Biotechnology Advances Vol.29 (2011) page : 124-141
[16] Anwar Ahmad, Rumana Ghufran, Zularisam and Wahid. Bioenergy from Anaerobic Degradation of Lipid in Palm Oilm Mill Effluent. Rev. Environ Sci.
Biotechnol (2011) page : 353-376
[17] Ta Yeong Wu, Abdul Wahab Mohammad, Jamaliah Md. Jahim and Nurina Anuar. Pollution control technologies for the treatment of palm oil mill effluent (POME) through end-of-pipe processes. Journal of Enviromental Management Vol.91 (2010) page : 1467-1490
[18] Peraturan Menteri Negara Lingkungan Hidup. Petunjuk Teknis Standar
Pelayanan Bidang Lingkungan Hidup daerah Kabupaten/Kota. 2008
[19] Peraturan Menteri Negara Lingkungan Hidup. Baku Mutu Limbah Cair Bagi
Kegiatan Industri. 1995
[20] Jorge del Real Olvera and Alberto Lopez-Lopez. Biogas Production from
Anaerobic Treatment of Agro-Industrial Wastewater. Enviromental Technology Unit.
Centre of Research and Assistance in Technology and Design of The State of Jalisco (CIATEJ). Mexico. March, 2012
Production from Lignocellulosic Biomass by Organosolv Pretreatment. Hindawi Publishing Corporation. BioMed Research International Article ID 350414. 6 pages. 2014
[22] David Bahrin, Destilia Anggraini dan Mutiara Bunga Pertiwi. Pengaruh Jenis
Sampah, Komposisi Masukan dan Waktu Tinggal Terhadap Komposisi Biogas dari Sampah Organik Pasar di Kota Palembang. Prosiding Seminar Nasional AvoER
ke-3 ISBN:979-587-ke-395-4 Palembang 26-27 Oktober 2011
[23] Gerhard Angrinz GmbH. Biogas Purification and Assesment of The Natural
Gas Grid in Southern and Eastern Europe. Leitbnitz, Austria. 2008
[24] B. Velmurugan and R. Alwar. Anaerobic Digestion of Vegetable Wastes for Biogas Production in a Fed-Batch Reactor. Int. J. Emerg. Sci. 1(3) september 2011 ISSN:2222-4254 page : 478-486
[25] Jingxin Zhang, Yaobin Zhang, Xie Quan and Shuo Chen. Enhancement of Anaerobic Acidogenesis By Integrating an Electrochemical System Into an Acidogenic Reactor : Effect of Hydraulic Retention Time (HRT) and Role of Bacteria and Acidophilic Methanogenic Archaea. Bioresource Technology 179 (2015) page 43-49
[26] Rina. S. Soetopo, Sri Purwati, Yusup Setiawan dan Krisna Adhytia W. Efektivitas Proses Kontinyu Digesti Anaerobik Dua Tahap Pada Pengolahan Lumpur IPAL Biologi Industri Kertas. Balai Besar Pulp dan Kertas : Jurnal Riset Industri Vol.5 No.2 (2011) Hal. 131-142
[27] Irvan, Bambang Trisakti, Vivian Wongistani and Yoshimasa Tomiuchi. Methane Emission From Digestion Of Palm Oil Mill Effluent (Pome) In A Thermophilic Anaerobic Reactor. Internat. J. of Sci. and Eng Vol.3 No.1 ISSN: 2086-5023 April 2012 page : 32-35
[28] Djoko Padmono. Kemampuan Alkalinitas Kapasitas Penyangga (Buffer Capacity) dalam Sistem Anaerobic Fixed Bed. Jurnal Teknik Lingkungan Vol.8 No.2 ISSN 1441-318 (Mei 2007) Hal : 119-127
[29] Teodorita Al Seadi, Dominik Rutz, Heinz Prassl, Michael Köttner, Tobias Finsterwalder, Silke Volk and Rainer Janssen. Biogas Handbook. University of Southern Denmark Esbjerg. Niels Bohrs Vej 9-10 DK-6700 Esbjerg. pp 21-28. Denmark. 2008
[31] Gita Khaerunnisa dan Ika Rahmawati. Pengaruh pH Dan Rasio COD : N Terhadap Produksi Biogas Dengan Bahan Baku Limbah Industri Alkohol (Vinasse).
Jurnal Teknologi Kimia dan Industri Vol. 2 No. 3 2013. Hal : 1-7
[32] Ervid Mifthah P. Dan Hastih Dwi S. Peningkatan Kualitas Biogas Dengan Pengaturan Rasio Nutrisi Dan pH. Jurnal Teknologi Kimia dan Industri Vol. 2 No. 3 2012. Hal : 143-147
[33] Kristina W. Golub, Stacey R. Golub, Daniel M. Meysing and Mark T. Holtzapple. Propagated Fixed-Bed Mixed-Acid Fermentation : Effect of Volatile Solid Loading Rate and Agitation at Near-Neutral pH. Bioresource Technology 124 (2012) page 146-156
[34] Remm A. Alrawi, Anees Ahmad, Norli Ismail and Mohd Omar A. Kadir. Anaerobic Digestion of Palm Oil Mill Effluent With Tumen Fluid as a co-Substrate. Desalination 269 (2011) page : 50-57
[35] APHA, AWWA and WCF. Standard methods for the examinion of water and
wastewer. Edisi 20 (Washington DC, USA, : American Public Health Associion,
1999) page 236- 244
[36] Yee-Shian Wong, Tjoon Tow Teng, Soon-An Ong, M.Norhashimah, M.Rafatullah and Hong-Chen Lee. Anaerobic Acidogenesis Biodegradation of Palm Oil Mill Effluent Using Suspended Close Anaerobic Bioreactor (SCABR) at Mesophilic Temperature. Procedia Environmental Sciences 18 ( 2013 ) page : 433 – 441
[37] Bambang Trisakti, Veronoca Manalu, Irvan, Taslim, and Muhammad Turmuzi. Acidogenesis of Palm Oil Mill Effluent to Produce Biogas : Effect of Hydraulic Retention Time and pH. Procedia-Sosial And Behavioral Sciences 195 (2015) page : 2466-2474
[38] Zhuoli Tian, Diane Chauliac and Pratap Pullammanappallil. Comparison of non-agitated and agitated batch, thermophilic anaerobic digestion of sugarbeet tailings. Bioresource Technology 129 (2013) 411-420
[39] Berlian Sitorus, Sukandar and Seno D. Penjaitan. Biogas Recovery from Anaerobic Digestasi Process of Mixed Fruit-Vegetable Waste. Energy Procedia 32 (2013) page : 176-182
[41] S.M. Ratusznei, J.A.D. Rodrigues, E.F.M. Camargo, M. Zaiat and W. Borzani. Feasibility og a Stirred Anaerobic Sequencing Batch Reactor Containing Immobilized Biomass of Wastewater Treatment. Bioresource Technology 75 (2000) page : 127-132
[42] Savoporn Supaphol, Sasha N. Jenkins, Pichamon Intomo, Ian S.Waite and Anthony G. O’Donnell. Microbial Community Dynamics in Mesophilic Anaerobic Co-Digestion of Mixed Waste. Bioresource Technology 102 (2011) page : 4021-4027
[43] X. Gomez, M.J. Cuetos, J. Cara, A. Moran and A.I. Garcia. Anaerobic Co-Digestion of Primary Sludge and The Fruit and Vegetable Fraction of The Municipal Solid Wastes Conditions For Mixing and Evaluation of The Organic Loading Rate. Renewable Energy 31 (2006) page : 2017-2024
[44] Khursheed Karim, Rebecca Hoffmann, K. Thomas Klasson and M.H. Al-Dahhan. Anaerobic Digestion of Animal Waste : Effect of Mode of Mixing. Water Research 39 (2005) page : 3597-3606
[45] M. Hamdi. Effect of Agitation and Pretreatment on The Batch Anaerobic Digestion of Olive Mill Wastewaater. Bioresource Technology 36 (1991) page : 173-178
[46] Standar Nasional Indonesia. Air dan Air Limbah – Bagian 15: Cara uji
Kebutuhan Oksigen Kimiawi (KOK) Refluks Terbuka dengan Refluks Terbuka secara Titrimetri. SNI 06-6989.15-2004.
BAB III
METODOLOGI PENELITIAN
3.1 LOKASI PENELITIAN
Penelitian ini dilakukan di Laboratorium Ekologi, Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatera Utara (USU), Medan.
3.2 BAHAN DAN PERALATAN
3.2.1 Bahan-Bahan
3.2.1.1 Bahan Utama
1) Starter dari hasil olahan penelitian asidogenesis sebelumnya 2) Sampel LCPKS dari fat pit PKS Adolina
3.2.1.2 Bahan Tambahan
1) Natrium Bikarbonat (NaHCO3)
3.2.1.3 Bahan Analisa 1) Asam klorida (HCl) 0,1 N 2) Aquadest (H2O)
3.2.2 Peralatan
3.2.2.1 Peralatan Utama
1. Fermentor tangki berpengaduk/jar fermentor (EYELA model No: MBF 300ME)
2. Pompa sludge/slurry pump (HEISHIN, model No.:3NY06F) 3. Gas meter (SHINAGAWA, model No.:W-NK-0.5B)
4. Tangki umpan (service tank) 5. Pengaduk
6. Sensor temperatur 7. pH elektroda
10. Gas collector
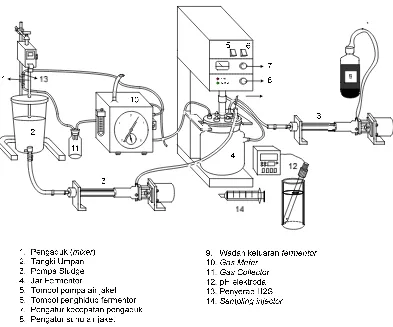
[image:35.595.123.516.170.497.2]Adapun rangkaian peralatan yang digunakan dalam penelitian ini dapat dilihat pada gambar 3.1.
Gambar 3.1 Rangkaian Peralatan 3.2.2.2 Peralatan Analisa
1. Buret 25 ml
2. Timbangan analitik 3. Oven
4. Desikator
3.3 TAHAPAN PENELITIAN
3.3.1 Analisis Bahan Baku Limbah Cair Pabrik Kelapa Sawit (LCPKS) 3.3.1.1 Pengukuran pH
Adapun prosedur pengukuran pH adalah [35]:
1) Kalibrasi pH meter dilakukan ke dalam pH 4, pH 7, dan pH 10. 2) Bagian elektroda dari pH meter dicuci dengan aquadest.
3) Elektoda dimasukkan ke dalam sampel yang akan diukur pH-nya.
4) Nilai bacaan pH meter ditunggu sampai konstan lalu dicatat nilai bacaannya.
3.3.1.2 Analisis M-Alkalinity
Adapun prosedur analisis M-alkalinity adalah [35]:
1) Sampel dimasukkan sebanyak 5 ml ke dalam beaker glass lalu ditambahkan dengan aquadest hingga volume larutan 80 ml.
2) Beaker glass diletakkan di atas magnetic stirrer, dan diletakkan pH elektroda di
dalam beaker gelas, kemudian stirrer dihidupkan dan kecepatan diatur sedemikian rupa hingga sampel tercampur sempurna dengan aquadest.
3) Campuran dititrasi dengan larutan HCl 0,1 N hingga pH mencapai 4,8 ± 0,02. 4) Analisis M-Alkalinity dilakukan untuk Limbah Cair Pabrik Kelapa Sawit
(LCPKS) dan limbah fermentasi pada Jar fermentor.
5) M-Alkalinity dapat dihitung berdasarkan rumus sebagai berikut: M-Alkalinity mg NaHCO3 /L =
Sampel Vol
50000 x M x terpakai yang
Vol.HCl HCl
3.3.1.3 Analisis Total Solids (TS)
Adapun prosedur analisis Total Solids (TS) adalah [35]:
1) Cawan penguap kosong yang telah dibersihkan, dipanaskan pada 105oC di dalam oven selama 1 jam. Apabila akan dilanjutkan untuk analisis zat tersuspensi organik, cawan dipanaskan pada 550oC, selama 1 jam.
2) Cawan didinginkan selama 15 menit di dalam desikator, lalu ditimbang.
3) Sampel dikocok merata, lalu dituangkan ke dalam cawan. Volume sampel diatur sehingga berat residu antara 2,5-200 mg.
4) Cawan berisi sampel dimasukkan ke dalam oven, suhu 98oC untuk mencegah percikan akibat didihan air di dalam cawan. Namun bila volum sampel kecil dan dinding cawan cukup tinggi maka langkah ini tidak perlu.
5) Pengeringan diteruskan di dalam oven dengan suhu 103-105oC selama 1 jam. 6) Cawan yang berisi residu zat padat tersebut didinginkan di dalam desikator
sebelum ditimbang.
7) Langkah 5 dan 6 diulang sampai didapat berat yang konstan atau berkurang berat lebih kecil 4% berat semula atau 0,5 mg, biasanya pemanasan 1-2 jam sudah cukup. Penimbangan harus dikerjakan dengan cepat untuk mengurangi galat.
8) Kandungan TS dapat dihitung berdasarkan rumus sebagai berikut:
mL sampel, volume
1000 B) -(A tal/L
padatan to
mg = ×
Keterangan: A = berat residu kering + cawan porselen, mg B = berat cawan porselen, mg
3.3.1.4 Analisis Volatile Solids (VS)
Adapun prosedur analisis Volatile solids (VS) adalah [35]:
1) Cawan penguap setelah dari TS dipanaskan dengan menggunakan muffle furnace pada suhu 550oC selama 1 jam.
2) Setelah itu cawan penguap didinginkan di dalam desikator hingga mencapai suhu kamar.
3) Berat cawan penguap ditimbang.
4) Kandungan VS dapat dihitung berdasarkan rumus sebagai berikut:
mL sampel, volume
1000 B) -(A latil/L
padatan vo
mg = ×
Keterangan: A = berat residu+cawan porselen sebelum pembakaran, mg B = berat residu + cawan porselen setelah pembakaran, mg
3.3.1.5 Analisis Total Suspended Solids (TSS)
Adapun prosedur analisis Total Suspended Solids (TSS) adalah [35]: 1) Berat kertas saring kering yang digunakan ditimbang.
(3.2)
2) Kertas saring dibasahi dengan sedikit air suling.
3) Sampel diaduk dengan magnetic stirrer untuk memperoleh sampel yang lebih homogen.
4) Sampel dipipetkan ke penyaringan dengan volume tertentu pada waktu contoh diaduk dengan magnetic stirer.
5) Kertas saring dicuci atau disaring dengan 3 x 10 ml aquadest.
6) Kertas saring dipindahkan secara hati-hati dari peralatan penyaring ke wadah timbang dengan aluminium sebagai penyangga.
7) Dikeringkan di dalam oven setidaknya selama 1 jam pada suhu 103ºC sampai dengan 105ºC, didinginkan dalam desikator untuk menyeimbangkan suhu dan massanya.
8) Tahapan pengeringan, pendinginan dalam desikator, dan penimbangan diulangi sampai diperoleh berat konstan atau sampai perubahan berat lebih kecil dari 4% terhadap penimbangan sebelumnya atau 0,5 mg.
9) Kandungan TSS dapat dihitung berdasarkan rumus sebagai berikut:
mL sampel, volume 1000 B) -(A total/L rsuspensi padatan te
mg = ×
Keterangan: A = berat kertas saring + berat residu, mg B = berat kertas saring, mg
3.3.1.6 Analisis Volatile Suspended Solids (VSS)
Adapun prosedur analisis Volatile Solids (VSS) adalah [35]:
1) Sampel residu hasil analisa TSS dibakar mengunakan api bunsen di dalam cawan porselen yang telah dikering dan diketahui beratnya.
2) Setelah terbakar sempurna atau bebas asap, selanjutnya sampel diabukan di dalam furnace pada suhu 550oC selama 1 jam.
3) Setelah 1 jam, furnace dimatikan dan sampel diambil setelah suhu furnace sekitar 100oC dan disimpan di dalam desikator selama 15 menit lalu ditimbang. 4) Kandungan VSS dapat dihitung berdasarkan rumus sebagai berikut:
mL sampel, volume 1000 B) -(A volatil/L rsuspensi padatan te
mg = ×
(3.4)
Keterangan: A = berat residu + cawan porselen sebelum pembakaran, mg B = berat residu + cawan porselen setelah pembakaran, mg
3.3.1.7 Analisis Chemical Oxygen Demand (COD)
Analisis ini dilakukan di luar Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatera Utara yaitu di Balai Teknik Kesehatan Lingkungan dan Pengendalian Penyakit (BTKLPP) Kelas 1 Medan dengan Metode Open Reflux. Adapun prosedur analisis Chemical Oxygen Demand (COD) adalah [46]:
1) Dimasukkan 10 ml contoh uji ke dalam erlenmeyer 250 ml.
2) Ditambahkan 0,2 g serbuk raksa (II) sulfat (HgSO4) dan beberapa batu didih.
3) Ditambahkan 5 ml larutan kalium dikromat, (K2Cr2O7) 0,25 N.
4) Ditambahkan 15 ml pereaksi asam sulfat (H2SO4) – perak sulfat (Ag2SO4)
perlahan-lahan sambil didinginkan dalam air pendingin.
5) Dihubungkan dengan pendingin Liebig dan dididihkan di atas hot plate selama 2 jam.
6) Didinginkan dan dicuci bagian dalam dari pendingin dengan air suling hingga volume contoh uji menjadi lebih kurang 70 ml.
7) Didinginkan sampai temperatur kamar, ditambahkan indikator ferroin 2 sampai dengan 3 tetes, dititrasi dengan larutan ferro ammonium sulfat atau FAS 0,1 N sampai warna merah kecoklatan, dicatat kebutuhan larutan FAS.
8) Langkah 1 sampai dengan 7 dilakukan terhadap air suling sebagai blanko. Kebutuhan larutan FAS dicatat. Analisis blanko ini sekaligus melakukan pembakuan larutan FAS dan dilakukan setiap penentuan COD.
9) Kandungan COD dapat dihitung berdasarkan rumus sebagai berikut:
sampel ml
N)8000 )(
B A ( O mg/l 2
− =
Keterangan: A = ml FAS untuk titrasi blanko B = ml FAS untuk titrasi sampel N = Normalitas FAS
8000 = berat miliekivalen oksigen ×1000 ml/l
3.3.2 Loading Up dan Operasi Target
Adapun prosedur loading up dan operasi target adalah:
1) Starter asidogenesis sebanyak 2 L dimasukkan ke dalam fermentor.
2) Bahan baku LCPKS dimasukkan ke dalam tangki umpan.
3) Kecepatan di dalam tangki umpan LCPKS segar diatur hingga kecepatan 150 rpm agar larutan LCPKS akan tercampur dengan baik.
4) Bahan baku LCPKS dialirkan dari tangki umpan ke dalam fermentor.
5) Suhu di dalam fermentor selama proses loading up dan operasi target dijaga pada suhu 45 oC dengan kecepatan pengadukan pada 150 rpm pada proses
loading up dan laju pengadukan 50, 100 dan 200 rpm pada operasi target.
6) HRT awal dimulai dengan HRT 20 hari karena untuk adaptasi hidrolitik bakteri dengan umpan dimasukkan secara bertahap yaitu 2 kali sehari.
7) Setelah 15 hari, percobaan dilanjutkan untuk HRT 15, 10, 5 dan 4. Dilakukan analisis untuk tiap HRT.
8) pH di dalam fermentor di atur 6 untuk loading up dan operasi target dengan penambahan NaHCO3 hingga pH yang dinginkan tercapai. Dilakukan analisis
untuk setiap run.
3.3.3 Pengujian Sampel (Sampling)
Prosedur yang dilakukan untuk pengujian sampel sama seperti prosedur yang dilakukan untuk analisis bahan baku, ditambah dengan analisis VFA, sedangkan analisis gas dilakukan jika pada penelitian ada terbentuk gas yaitu gas CO2 dan H2S.
[image:40.595.109.547.560.739.2]tabel 3.1 berikut merupakan jadwal analisis influent dan effluent. Tabel 3.1 Jadwal Analisis Influent dan Effluent Hari ke
Analisis 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 pH M-Alkalinity TS VS TSS VSS COD VFA Gas Keterangan: = Analisis influent
3.3 JADWAL PENELITIAN
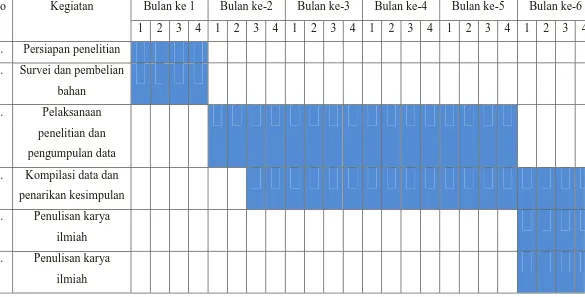
[image:41.595.10.595.174.471.2]Pelaksanaan penelitian direncanakan selama 7 (tujuh) bulan. Jenis kegiatan dan jadwal pelaksanaannya dapat dilihat dilihat pada Tabel 3.2.
Tabel 3.2 Jenis Kegiatan dan Jadwal Pelaksanaan Penelitian
No .
Kegiatan Bulan ke 1 Bulan ke-2 Bulan ke-3 Bulan ke-4 Bulan ke-5 Bulan ke-6 1 2 3 4 1 2 3 4 1 2 3 4 1 2 3 4 1 2 3 4 1 2 3 4 1. Persiapan penelitian
2. Survei dan pembelian bahan
3. Pelaksanaan penelitian dan pengumpulan data 4. Kompilasi data dan
penarikan kesimpulan 5. Penulisan karya
ilmiah 6. Penulisan karya
ilmiah
BAB IV
HASIL DAN PEMBAHASAN
4.1 KARAKTERISASI LIMBAH CAIR PABRIK KELAPA SAWIT
(LCPKS)
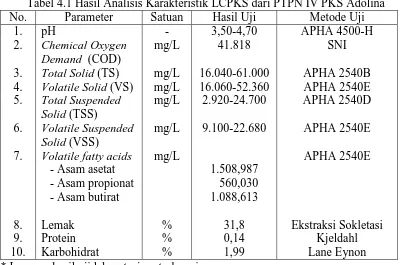
[image:42.595.113.514.289.554.2] [image:42.595.114.513.291.553.2]Bahan baku LCPKS yang digunakan dalam penelitian yaitu LCPKS yang berasal dari PTPN IV PKS Adolina. Adapun hasil analisis karakteristik dari bahan baku LCPKS yang digunakan dalam penelitian ini dapat dilihat pada Tabel 4.1 dibawah ini.
Tabel 4.1 Hasil Analisis Karakteristik LCPKS dari PTPN IV PKS Adolina
No. Parameter Satuan Hasil Uji Metode Uji
1. pH - 3,50-4,70 APHA 4500-H
2. Chemical Oxygen Demand (COD)
mg/L 41.818 SNI
3. Total Solid (TS) mg/L 16.040-61.000 APHA 2540B
4. Volatile Solid (VS) mg/L 16.060-52.360 APHA 2540E 5. Total Suspended
Solid (TSS)
mg/L 2.920-24.700 APHA 2540D 6. Volatile Suspended
Solid (VSS)
mg/L 9.100-22.680 APHA 2540E 7.
8. 9. 10.
Volatile fatty acids
- Asam asetat - Asam propionat - Asam butirat Lemak Protein Karbohidrat mg/L % % % 1.508,987 560,030 1.088,613 31,8 0,14 1,99 APHA 2540E Ekstraksi Sokletasi Kjeldahl Lane Eynon * Laporan hasil uji laboratorium terlampir
Dari Tabel 4.1 diatas menunjukkan hasil analisis karakteristik LCPKS dari PTPN IV PKS Adolina dimana dari beberapa parameter yang di analisis berada di atas ambang baku mutu limbah buangan.
Keputusan Menteri Negara Lingkungan Hidup Nomor: KEP 51-/MENLH/10/1995 yaitu 6,0-9,0 [19].
Selain itu dari Table 4.1 menunjukkan LCPKS PKS Adolina memiliki kandungan COD yang tinggi yaitu 41.818 mg/L. Nilai COD yang diperoleh telah melewati batas yang diizinkan oleh Kementerian Lingkungan Hidup dalam Keputusan Menteri Negara Lingkungan Hidup Nomor: KEP 51-/MENLH/10/1995 yaitu sebesar 500 mg/L [19].
Pada Tabel 4.1 juga menunjukkan konsentrasi lemak, protein dan karbohidrat yang tinggi yaitu sebesar 31,8%, 0,14% dan 1,99%. Kementerian Lingkungan Hidup dalam Keputusan Menteri Negara Lingkungan Hidup Nomor: KEP 51-/MENLH/10/1995 juga memiliki baku mutu minyak dan lemak yaitu sebesar 30 mg/L [19]. Lemak, protein dan karbohidrat inilah senyawa yang nantinya akan di konversi menjadi senyawa VFA kemudian menjadi biogas [29, 20, 16]. Sehingga LCPKS ini merupakan substrat yang bisa digunakan untuk penelitian ini.
4.2 HASIL PENELITIAN VARIASI HRT (PROSES LOADING UP)
Pada penelitian ini dilakukan variasi HRT yang dimulai dari HRT 20, 15, 10, dan 4 hari. Proses loading up (variasi HRT) dilakukan untuk membantu proses adaptasi dan pertumbuhan mikroba pada starter yang diambil dari kolam pengasaman PTPN III PKS Torgamba sehingga proses asidogenesis dapat berlangsung pada HRT operasi target (variasi laju pengadukan). Selama proses
loading up, fermentor dioperasikan dengan penurunan HRT dari 20, 15, 10 dan 4
hari pada kondisi temperatur 45oC, laju pengadukan sebesar 150 rpm dan pH dijaga konstan pada 6 (±0,2) dengan penambahan natrium bikarbonat (NaHCO3). Adapun
4.2.1 Pengaruh HRT Terhadap Profil pH dan Alkalinitas
[image:44.595.133.508.215.408.2]Alkalinitas dapat digunakan sebagai indiaktor kestabilan proses. Kondisi operasi dipengaruhi oleh jenis proses yang digunakan, temperatur, pencampuran dan HRT yang mempengaruhi pertumbuhan mikroba [12]. Adapun hubungan pengaruh pH dan Alkalinitas pada variasi HRT dapat dilihat pada Gambar 4.1 yang menunjukkan pengaruh HRT terhadap pH dan Alkalinitas.
Gambar 4.1 Pengaruh HRT terhadap Profil pH dan Alkalinitas
Pada Gambar 4.1 menunjukkan grafik pH yang relatif stabil pada setiap HRT 20, 15, 10 dan 4 yaitu 6 (± 0,2). Proses asidognesis pada umumnya berlangsung pada pH yang rendah. pH optimal pada proses hidrolisis dan asidogenesis yang dapat meningkatkan aktivitas bakteri yaitu berkisar 5 - 6 [25]. pH keluaran fermentor
berfluktuasi disebabkan karena seiring dengan penambahan umpan baru yang
memiliki pH yang rendah sekitar 3,40 - 4,70. Penambahan umpan baru yang
mengakibatkan pH berfluktuasi juga mengakibatkan nilai alkalinitas berfluktuasi
juga.
Nilai alkalinitas yang diperoleh pada HRT 20 berfluktuasi antara 2.200 - 4.200 mg/L, pada HRT 15 alkalinitas berfluktuasi antara 2.250 - 3.800 mg/L, pada HRT 10 alkalinitas berfluktuasi antara 1.500 - 3.000 mg/L, pada HRT 4 alkalinitas berfluktuasi antara 1.300 - 3.000 mg/L. Nilai alkalinitas yang diperoleh antara 1.300 - 4.200. Alkalinitas yang menurun dapat menunjukan hilangnya kestabilitas yang mengakibatkan proses terganggu [12].
0 1 2 3 4 5 6 7 0 500 1.000 1.500 2.000 2.500 3.000 3.500 4.000 4.500
0 5 10 15 20 25 30 35 40 45 50 55 60
p H A lk a li n it a s (m g /L ) Hari ke-Alkalinitas pH HRT 4
HRT 15 HRT 10
Pada proses variasi HRT, penambahan NaHCO3 diberikan untuk
mempertahankan pH. Adanya alkalinitas dalam reaktor dengan konsentrasi tertentu dapat menjadi penyangga (Buffer) agar pH tetap pada kondisi netral apabila terjadi penambahan asam, sehingga kesetimbangan proses secara keseluruhan dapat tetap berjalan dengan normal dengan menambahkan senyawa bikarbonat atau hidroksida [28, 33].
Pada proses variasi HRT penurunan HRT tidak memberikan dampak yang signifikan pada alkalinitas dan pH. Grafik pH dan alkalinitas berfluktuasi pada kisaran pH dan alkalinitas asidognesis. Oleh karena itu, pada proses loading up penurunan HRT tidak berpengaruh secara signifikan terhadap alkalinitas dan pH yang diperoleh. pada setiap perubahan HRT terjadi hal yang sama seperti HRT sebelumnya yaitu mengalami fluktuasi.
4.2.2 Pengaruh HRT Terhadap Profil Pertumbuhan Mikroba
Volatile Suspensed Solid (VSS) merupakan konsentrasi yang dapat digunakan
[image:45.595.131.509.485.670.2]sebagai indikator berlimpahnya mikroba [12]. Adapun pengaruh pH dan alkalinitas terhadap pertumbuhan mikroba dapat dilihat pada Gambar 4.2 yang menunjukan grafik hubungan pH dan alkalinitas terhadap pertumbuhan mikroba.
Gambar 4.2 Pengaruh HRT terhadap Profil Pertumbuhan Mikroba
0 1 2 3 4 5 6 7 0 5.000 10.000 15.000 20.000 25.000
0 5 10 15 20 25 30 35 40 45 50 55 60
p H V S S ( m g /L ) Hari ke-VSS Alkalinity pH HRT 4
HRT 15 HRT 10
Pada Gambar 4.2 menunjukkan konsentrasi VSS yang berfluktuasi pada HRT 20, 15, 10 dan mengalami peningkatan pada HRT 4. Perubahan nilai pH memberikan pengaruh terhadap perubahan konsentrasi mikroorganisme dalam fermentor. Perubahan ini dapat dilihat pada HRT 15 dari hari ke-28 ke hari 30 dimana pH menurun dari 6 menjadi 5,8 dan terjadi penurunan VSS dari 19.260 mg/L ke 16.080 mg/L. Selain suhu, pH merupakan faktor penting yang mempengaruhi pertumbuhan mikroorganisme pada proses digestasi anaerobik. Bakteri aktif bekerja di kisaran pH tertentu dan menunjukkan maksimum aktivitas di pH optimum. pH optimum yang dibutuhkan oleh bakteri asidogenesis berkisar 5 - 6,5 sedangkan pH optimum untuk bakteri metanogenesis lebih tinggi dari 6,5 [39].
HRT juga merupakan faktor yang mempengaruhi pertumbuhan mikroorganisme karena HRT mempengaruhi ketersediaan nutrisi bagi mikroorganisme untuk melakukan metabolisme. Pada HRT 4 mikroorganisme mengalami pertumbuhan dengan bertambahnya waktu asidognesis. Setelah mengalami fluktuasi pada HRT 20, 15 dan 10, mikroba mengalami pertumbuhan yang stabil pada HRT 4. Optimalisasi HRT sangat penting untuk meningkatkan kinerja asidogenesis. HRT yang pendek biasa digunakan untuk tahap asidogenesis
untuk mempertahankan pH rendah. Namun HRT yang terlalu rendah juga dapat
mengurangi efisiensi proses esidogenesis [25]. Perubahan HRT dapat menyebabkan
perubahan jumlah mikroba [12]
4.2.3 Pengaruh HRT Terhadap Reduksi Chemical Oxygen Demand (COD)
Efesiensi pengasaman merupakan salah satu parameter yang paling penting
pada proses asidogenesis yang dapat menunjukan jumlah produksi VFA dan COD
[image:47.595.168.473.199.352.2]limbah yang diolah [25]. Adapun hubungan reduksi COD pada variasi HRT dapat dilihat pada Gambar 4.3 yang menunjukkan pengaruh HRT terhadap Reduksi COD.
Gambar 4.3 Pengaruh HRT Terhadap Reduksi COD
Pada Gambar 4.3 menunjukkan penurunan HRT dari HRT 20, 15, 10 dan 4 reduksi COD cenderung menurun namun pada HRT 4 terjadi peningkatan. Reduksi COD pada HRT 20, 15, 10 dan 4 masing masing adalah 55 %, 42%, 43% dan 42%. Nilai reduksi COD dipengaruhi oleh HRT. Reduksi COD semakin rendah dengan seiring semakin rendahnya HRT [36]. Penurunan aktifitas diamati ketika konsentrasi COD meningkat [45]. Reduksi COD tertinggi diperoleh pada HRT 20. Hasil yang sama diperoleh oleh Yee sian wong et al [36] dimana reduksi COD tertinggi diperoleh pada HRT yang lebih lama. Pada proses asidognesis reduksi COD yang tinggi harus dihindari karena reduksi COD yang tinggi akan menyebabkan terbentuknya gas metana.
Pada operasi target ini reduksi COD terendah dihasilkan pada HRT 15 dan HRT 4 yaitu 42 %. Sehingga HRT 4 merupakan HRT yang lebih baik untuk digunakan pada opersi target.
55%
42% 43% 42%
0% 10% 20% 30% 40% 50% 60%
0 15 30 45 60
R
ed
u
k
si
C
O
D
Hari
4.2.4 Pengaruh HRT Terhadap Pembentukan Volatile Fatty Acid (VFA)
VFA merupakan hasil biokonversi senyawa organik polimer menjadi monomer pada proses asidogenesis. Stabilitas proses digestasi terlihat dari konsentrasi produk intermediate seperti asam lemak bebas (VFA). Asam lemak bebas merupakan senyawa intermediate (asetat, propionat, butirat, laktat) yang dihasilkan selama proses asidogenesis dengan rantai karbon hingga enam atom [26].
Efesiensi pengasaman merupakan salah satu parameter yang paling penting pada
proses asidogenesis yang dapat menunjukan jumlah produksi VFA dan COD limbah
yang diolah [25]. Adapun bungan pembentukan VFA pada proses variasi HRT dapat
dilihat pada Gambar 4.4 yang menunjukan pengaruh HRT terhadap pembentukan
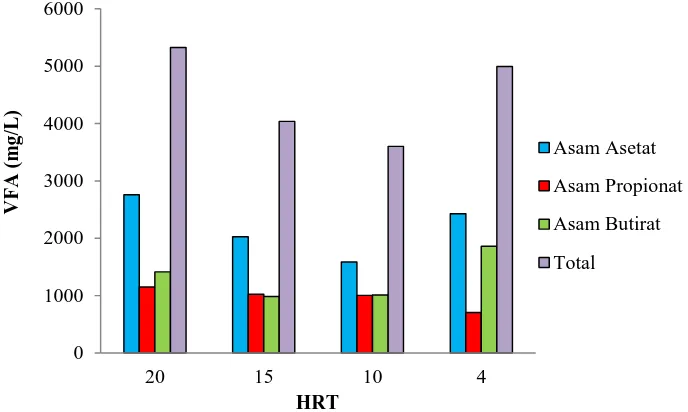
[image:48.595.143.487.319.525.2]VFA.
Gambar 4.4 Pengaruh HRT terhadap pembentukan VFA
Pada proses asidognesis, VFA merupakan produk utama yang ingin dihasilkan. Komposisi dari VFA mempengaruhi keberlangsungan proses digestasi anaerobik. Semakin pendek HRT maka produktivitas mikroba semakin tinggi sehingga produk inhibitor semakin kecil. Produktivitas yang rendah di HRT tertinggi
disebabkan oleh keterbatasan substrat untuk mikroba yang semakin rendah sehingga
mempengaruhi pertumbuhan mikroba [10].
Gambar 4.4 menunjukkan bahwa profil pembentukan total VFA yang menurun dari HRT 20 sampai HRT 10, namun meningkat pada HRT 4 dimana total VFA pada HRT 20, 15, 10 dan 4 masing-masing sebesar 5.325,300; 4.039,461;
0 1000 2000 3000 4000 5000 6000
20 15 10 4
V
F
A
(
m
g
/L
)
HRT
Asam Asetat
Asam Propionat
Asam Butirat
3.601,757 dan 4.994,773 mg/L. Total VFA dari masing-masing HRT bernilai lebih besar dari total VFA LCPKS segar yang bernilai 3.158,630 mg/L yang menandakan bahwa selama proses loading up terjadi pembentukan VFA. Dimana Seiring dengan konsentrasi VSS tertinggi terdapat pada HRT 4, namun konsentrasi VSS terjadi fluktuasi dari HRT 20 sampai HRT 4 sehingga tidak sejalan dengan total pembentukan VFA. Hal ini mengindikasikan bahwa pertumbuhan mikroba yang tinggi tidak menjamin hasil VFA yang tinggi pula. VFA yang diproduksi dapat bernilai tinggi apabila efektivitas kinerja mikroba juga tinggi. Sesuai dengan penelitian yang dilakukan oleh Yee-Shiang Wong et, al. [36] dimana produksi VFA tertingi sesuai dengan semakin kecilnya HRT yaitu HRT 12 sebesar VFA 11.569,71 mg asam asetat/L dengan HRT 2 sebesar 16.956,00 mg asam asetat/L.
Pada penelitian yang dilakukan oleh Sohpia Ghanimeh et, al. [12], Konsentrasi tinggi dari asam propionat di digester B meningkat namum masih ditoleransi, dimana nilai toleransi 3000 mg/L. Asam propionat sulit untuk dikonversi pada tahap berikutnya dan biasanya berlangsung lebih lama dari senyawa VFA lainnya. Propinonat yang tinggi menunjukan sedikitnya jumlah mikroba.
4.2.5 Pengaruh HRT Terhadap Rasio VFA/Alkalinitas
[image:50.595.170.475.166.348.2]Adapun hubungan Rasio VFA/Alkalinitas terhadap proses variasi HRT dapat dilihat pada Gambar 4.5 yang menunjukkan rasio VFA/alkalinitas pada proses variasi HRT.
Gambar 4.5 Pengaruh HRT Terhadap Rasio VFA/Alkalinitas
Pada Gambar 4.5 menunjukkan rasio VFA/Alkalinitas mengalami penurunan pada HRT 15 namun meningkat sampai HRT 4 dengan nilai rasio VFA/Alkalinitas pada HRT 20,15,10 dan 4 masing masing adalah 1,72; 1,34; 1,76 dan 2,41. Proses digestasi anaerobik tahap asidognesis dan metanognesis memiliki rasio VFA/Alkalinitas yang berbeda. Pada proses asidognesis rasio VFA/Alkalinitas harus lebih besar dari 1 sedangkan rasio VFA/Alkalinitas pada proses metanognesis lebih kecil dari 0,8. rasio VFA/alkalinitas dapat digunakan sebagai ukuran stabilitas proses [10]. Nilai pH lebih rendah dari 5 dapat menurunkan efisiensi asidogenesis
dan hasil VFA [25]. Sesuai dengan menurut Bambang Trisakti et. al [37] dimana
rasio VFA/Alkalinitas > 1 diasumsikan menunjukan kestabilan untuk proses
asidogenesis.
4.3 HASIL PENELITIAN VARIASI LAJU PENGADUKAN (OPERASI
TARGET)
Pada operasi target (variasi laju pengadukan) fermentor dijalankan pada HRT 4, pH 6, dan suhu 45oC dimana dilakukan variasi laju pengadukan yaitu 50 rpm, 100 rpm, 150 rpm dan 200 rpm. Dengan adanya pengadukan kondisi substrat menjadi homogen dan kontak mikroba dengan substrat menjadi lebih intensif, sehingga perkembangbiakan mikroba bekerja lebih optimum [4]. Pengadukan juga berfungsi agar tidak terbentuk kerak pada permukaan, agar tidak terjadi pengendapan dibawah permukaan, memastikan suhu yang homogen dalam digester dan distribusi homogen pada penyebaran nutrisi [9]. Percobaan untuk masing-masing variasi laju pengadukan dijalankan selama 15 hari yang mana merupakan hasil perkiraan waktu yang dibutuhkan agar proses stabil. Adapun data-data analisis yang diambil selama tahapan operasi target berupa pengukuran pH, alkalinitas, TS, VS, TSS, VSS, COD, dan VFA.
4.3.1 Pengaruh Laju Pengadukan terhadap Profil Alkalinitas
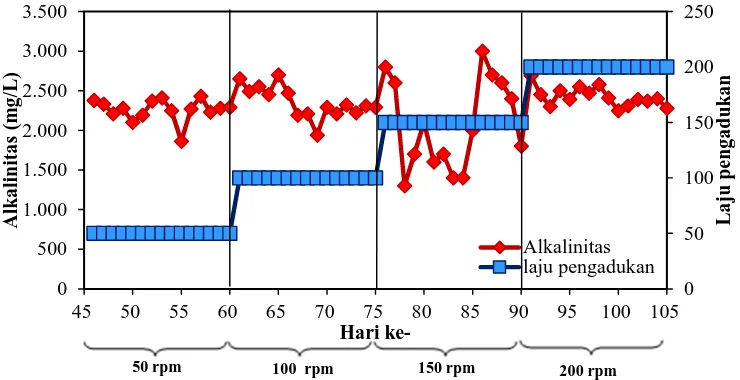
Gambar 4.6 Pengaruh Laju Pengadukan terhadap Profil Alkalinitas
Gambar 4.7 Pengaruh Laju Pengadukan terhadap Rata-rata Alkalinitas (Error Bar Menyatakan Standar Deviasi)
Pada Gambar 4.6 menunjukan grafik laju pengadukan dan alkalinitas yang berfluktuasi. Nilai alkalinitas yang diperoleh pada laju pengadukan 50 rpm berfluktuasi antara 1.860 - 2.430 mg/L, pada 100 rpm alkalinitas berfluktuasi antara 1.940 – 2.700 mg/L, pada 150 rpm alkalinitas berfluktuasi antara 1.300 – 3.000 mg/L, dan pada 200 rpm alkalinitas berfluktuasi antara 2.250 – 2.690 mg/L.
Alkalinitas menunjukkan kemampuan dari fermentor untuk menjaga kestabilan pH. Fermentor dioperasikan pada pH 6, untuk menjaga pH sesuai yang diinginkan ditambahkan NaHCO3 [37]. Alkalinitas yang menurun dapat menunjukan
hilangnya kestabilitas yang mengakibatkan proses terganggu [12]. Keadaan yang homogen diperlukan untuk menyatakan kestabilan proses dalam digestasi anaerobik, oleh karena itu diperlukan pencampuran [40]. Rendahnya alkalinitas ditunjukan
0 50 100 150 200 250 0 500 1.000 1.500 2.000 2.500 3.000 3.500
45 50 55 60 65 70 75 80 85 90 95 100 105
L a ju p en g a d u k a n A lk a li n it a s (m g /L ) Hari ke-Alkalinitas laju pengadukan 200 rpm 100 rpm 150 rpm
50 rpm 500 1.000 1.500 2.000 2.500 3.000 3.500
50 100 150 200
Laju Pengadukan (rpm)
dengan rendahnya konsentrasi VFA dan pH [41]. Sehingga alkalinitas yang dihasilkan lebih tinggi pada laju pengadukan 150 rpm. Penurunan alkalinitas terjadi pada saat pH fermentor turun. Penurunan alkalinitas ini disebabkan karna penambahan LCPKS segar dengan pH yang lebih rendah menyebabkan terjadinya penurunan pH dan alkalinitas dari fermentor, dimana pH LCPKS segar sekitar 3,50 - 4,70.
Pada Gambar 4.7 menunjukkan nilai rata-rata alkalinitas dari variasi laju pengadukan 50 rpm, 100 rpm, 150 rpm dan 200 rpm masing masing adalah 2.259 (±141) mg/L, 2.353 (±199) mg/L, 2.073 (±569) mg/L dan 2.423 (±121) mg/L. Semakin tinggi laju pengadukan, alkalinitas yang diperoleh cenderung meningkat. Grafik pH dan alkalinitas berfluktuasi pada kisaran pH dan alkalinitas asidognesis. Alkalinitas tertinggi diperoleh pada laju pengadukan 200 rpm. Adapun Standard deviasi alkalinitas pada laju pengadukan 50 rpm, 100 rpm, 150 rpm dan 200 rpm yang tinggi terjadi pada laju pengadukan 150 rpm. Standar deviasi terendah diperoleh pada laju pengadukan 200 rpm. Hasil ini menunjukkan laju pengadukan 200 rpm memiliki nilai alkalinitas yang lebih stabil selama proses asidognesis. Kestabilan proses ini dapat memberikan dampak pada produksi VFA.
4.3.2 Pengaruh Laju Pengadukan terhadap Profil Pertumbuhan Mikroba
Faktor yang mempengaruhi pengadukan yaitu dipengaruhi oleh strategi pengadukan (dilakukan terus menerus atau intermiten), durasi pengadukan (lamanya pengaduakan) dan intensitas pengadukan (kecepatan yang digunakan) [38]. Volatile
Suspensed Solid (VSS) merupakan konsentrasi yang dapat digunakan sebagai
[image:54.595.182.458.511.674.2]indikator berlimpahnya mikroba [12]. Adapun pengaruh laju pengadukan terhadap pertumbuhan mikroba daat dilihat pada Gambar 4.8 yang menunjukan grafik hubungan laju pengadukan terhadap pertumbuhan mikroba dan pada Gambar 4.9 Pengaruh Laju Pengadukan terhadap Rata-rata Konsentrasi VSS.
Gambar 4.8 Pengaruh Laju Pengadukan terhadap Profil Konsentrasi VSS
Gambar 4.9 Pengaruh Laju Pengadukan terhadap Rata-rata Konsentrasi VSS (Error
Bar Menyatakan Standar Deviasi)
0 50 100 150 200 250 0 5.000 10.000 15.000 20.000 25.000
45 50 55 60 65 70 75 80 85 90 95 100 105
L a ju p en g a d u k a n V S S ( m g /L ) Hari ke-VSS Laju pengadukan 200 rpm 100 rpm 150 rpm
50 rpm 0 5.000 10.000 15.000 20.000 25.000
0 50 100 150 200 250
V S S (m g /L )
Pada Gambar 4.8 menunjukan grafik laju pengadukan dan VSS yang berfluktuasi. Nilai VSS yang diperoleh pada laju pengadukan 50 rpm berfluktuasi antara 6.900 - 8.600 mg/L, pada 100 rpm berfluktuasi antara 5.907 - 7.713 mg/L, pada 150 rpm alkalinitas berfluktuasi antara 8.567 - 17.867 mg/L, dan pada 200 rpm alkalinitas berfluktuasi antara 8.180 - 15.060 mg/L. Kondisi yang lebih asam mengakibatkan peningkatan VSS [42].
Pada Gambar 4.9 menunjukkan nilai rata-rata VSS dari variasi laju pengadukan 50 rpm, 100 rpm, 150 rpm dan 200 rpm masing masing adalah 7.811 (±857) mg/L, 6.664 (±948) mg/L, 12.893 (±4.684) mg/L dan 11.653 (±3.440) mg/L.
Pengurangan konsentrasi VSS selama proses juga mengakibatkan peningkatan pH [42]. Adapun Penelitian yang dilakukan oleh Bambang et al , 2015 [37] HRT yang terbaik yaitu pada HRT 4 dimana juga menunjukan konsentrasi mikroorganisme sebasar 20,62 mg VSS/L dengan pH operasi sebesar 6,0. Hasil yang diperoleh pada penelitian ini memberikan nilai VSS yang lebih tinggi pada laju pengadukan 100 rpm. Mikroorganisme yang hidup dalam proses anaerobik lebih seimbang pertumbuhannya pada pencampuran yang minimal [43]. Konsentrasi VSS cenderung meningkat namun terjadi penurunan pada laju pengadukan 200 rpm. Hal ini disebabkan karena besarnya laju pengadukan yang digunakan sehingga pertumbuhan mikroba di dalam fermentor terganggu.
4.3.3 Pengaruh Laju Pengadukan terhadap Volatile Solid (VS)
Faktor-faktor yang mempengaruhi kestabilan proses anaerobik yaitu suhu, jumlah substrat dan pencampuran [40]. Adapun pengaruh laju pengadukan terhadap pertumbuhan mikroba dapat dilihat pada Gambar 4.10 yang menunjukan grafik hubungan laju pengadukan terhadap VS dan pada Gambar 4.11 Pengaruh Laju Pengadukan terhadap Rata-rata Konsentrasi VS.
Gambar 4.10 Pengaruh Laju Pengadukan terhadap Reduksi VS
Gambar 4.11 Pengaruh Laju Pengadukan terhadap Rata-rata Reduksi VS (Error Bar Menyatakan Standar Deviasi)
0 50 100 150 200 250 0 5.000 10.000 15.000 20.000 25.000 30.000 35.000
45 50 55 60 65 70 75 80 85 90 95 100 105
L a ju p en g a d u k a n V S ( m g /L ) Hari ke-VS effluent Laju pengadukan 200 rpm 100 rpm 150 rpm
50 rpm 5.000 10.000 15.000 20.000 25.000 30.000
50 100 150 200
V S (m g/ L )
Laju Pengadukan (rpm)
Pada Gambar 4.10 menunjukkan grafik laju pengadukan dan nilai VS yang berfluktuasi. Nilai VS ini berfluktuasi dengan perubahan laju pengadukan dari fermentor yang diperoleh. Pada laju pengadukan 50 rpm nilai VS berfluktuasi diantara 13.020 mg/L – 26.450 mg/L, pada laju pengadukan 100 rpm nilai VS berfluktuasi diantara 15.340 mg/L – 24.700 mg/L, pada laju pengadukan 150 rpm nilai VS berfluktuasi diantara 16.180 mg/L – 31.820 mg/L, pada laju pengadukan 200 rpmnilai VS berfluktuasi diantara 15.620 mg/L – 29.640 mg/L. Mikroorganisme yang hidup dalam proses anaerobik lebih seimbang pertumbuhannya pada pencampuran yang minimal [43].
Pada Grafik 4.11 menunujukan nilai VS fermentor pada laju pengadukan 50 rpm adalah 20.567 (±3.173) mg/L dengan persen reduksi VS sebesar 31 %, VS fermentor pada laju pengadukan 100 rpm adalah 19.149 (±3.460) mg/L dengan persen reduksi VS sebesar 11 %, VS fermentor pada laju pengadukan 150 rpm adalah 24.117 (±3.725) mg/L dengan persen reduksi VS sebesar 28 %, dan VS fermentor pada laju pengadukan 200 rpm adalah 21.279 (±3.443) mg/L dengan persen reduksi VS sebesar 19 %. Pencampuran dapat meningkatkan efisiensi konversi substrat, namum pencampuran yang intermediet lebih optimal dibandingkan tanpa pencampuran dan pencampuran yang terlalu cepat [44].
4.3.4 Pengaruh Laju Pengadukan terhadap Reduksi Chemical Oxygen
Demand (COD)
Pencampuran berfungsi untuk membantu mendistribusikan substrat ke organisme menjadi seragam dan mentransfer panas. pencampuran juga berfungsi untuk memperkecil ukuran partikel sehingga proses lebih cepat dan menghilangkan gas yang menghambat proses [44]. Seperti yang dinyatakan sebelumnya nilai COD menunjukkan banyaknya bahan organik yang terdapat dalam bahan. Adapun hubungan laju pengadukan terhadap reduksi COD dapat dilihat pada Gambar 4.12 yang menunjukkan pengaruh laju pengadukan terhadap reduksi COD.
Grafik 4.12 Pengaruh Laju Pengadukan terhadap Reduksi COD
Pada Gambar 4.12 menunjukan Reduksi COD pada laju pengadukan 50 rpm, 100 rpm, 150 rpm dan 200 rpm masing masing adalah 43%, 39%, 42% dan 45%. Dengan nilai 23.551 mg/L, 25.000 mg/L, 24.242 mg/L dan 22.826 mg/L. Reduksi COD tertinggi diperoleh pada laju pengadukan 200 rpm. Pada proses digestasi anaerobik tahap asidognesis reduksi COD yang tinggi harus dihindari. Reduksi COD yang tinggi memungkinkan terbentuknya biogas atau terjadinya proses metanognesis. Oleh karena itu Reduksi COD yang rendah merupakan terbaik yaitu pada laju pengadukan 100 rpm dengan nilai Reduksi COD sebesar 39%. Penurunan aktivitas diamati ketika konsentrasi COD meningkat [45].
Oleh karena itu, variasi laju pengadukan pada proses asidogenesis ini yang menghasilkan nilai reduksi COD terendah yaitu pada laju pengadukan 100 rpm dengan nilai reduksi COD sebesar 39 %. Sehingga laju pengadukan 100 rpm merupakan laju pengadukan yang lebih baik dibandingkan dengan laju pengadukan yang lain.
43%
39% 42%
45%
0% 10% 20% 30% 40% 50%
45 60 75 90 105
R
ed
u
k
si
C
O
D
hari
ke-100 rpm
4.3.5 Pengaruh Laju Pengadukan Terhadap Pembentukan Volatile Fatty Acid
(VFA)
VFA merupakan hasil biokonversi senyawa organik polimer menjadi monomer pada proses asidogenesis. Stabilitas proses digestasi tercermin dari konsentrasi produk intermediate seperti asam lemak bebas (VFA). Asam lemak bebas merupakan senyawa intermediate (asetat, propionat, butirat, laktat), dihasilkan selama asidogenesis, dengan rantai karbon hingga enam atom [26]. Efesiensi pengasaman merupakan salah satu parameter yang paling penting pada proses
asidogenesis yang dapat menunjukan jumlah produksi VFA dan COD limbah yang
diolah [25]. Adapun hubungan pembentukan VFA pada proses variasi laju
pengadukan dapat dilihat pada Gambar 4.13 yang menunjukan pengaruh laju
pengadukan terhadap pembentukan VFA.
Gambar 4.13 Pengaruh Laju Pengadukan terhadap pembentukan VFA
Pada proses asidognesis, VFA merupakan produk utama yang ingin dihasilkan. Komposisi dari VFA mempengaruhi keberlangsungan proses digestasi anaerobik. Semakin pendek HRT maka produktivitas mikroba semakin tinggi sehingga produk inhibitor semakin kecil. Produktivitas yang rendah di HRT tertinggi disebabkan oleh keterbatasan substrat untuk mikroba yang semakin rendah sehingga mempengaruhi pertumbuhan mikroba [10].
Gambar 4.13 menunjukkan bahwa profil pembentukan total VFA yang meningkat dari laju pengadukan 50 rpm sampai 150 rpm dan menurun pada laju pengadukan 200 rpm dimana total VFA yang dihasilkan pada laju pengadukan 50,
0 1000 2000 3000 4000 5000 6000
50 100 150 200
V
F
A
(
m
g
/L
)
Laju Pengadukan
Asam Asetat
Asam Propionat
Asam Butirat
100, 150 dan 200 rpm masing-masing sebesar 3.382,265; 4.626,646; 4.994,773 dan 3.059,283 mg/L. Total VFA dari masing-masing laju pengadukan bernilai lebih besar dari total VFA LCPKS segar yang bernilai 3.158,630 mg/L yang menandakan bahwa selama proses operasi target terjadi pembentukan VFA. Dimana Seiring dengan konsentrasi VSS tertinggi terdapat pada laju pengadukan 150 rpm, namun konsentrasi VSS terjadi fluktuasi dari laju pengadukan 50 rpm sampai 200 rpm sehingga tidak sejalan dengan total pembentukan VFA. Hal ini mengindikasikan bahwa pertumbuhan mikroba yang tinggi tidak menjamin hasil VFA yang tinggi pula. VFA yang diproduksi dapat bernilai tinggi apabila efektivitas kinerja mikroba juga tinggi.
Pada penelitian yang dilakukan oleh Sohpia Ghanimeh et, al. [12], Konsentrasi tinggi dari asam propionat di digester B meningkat namum masih ditoleransi, dimana nilai toleransi 3000 mg/L. Asam propionat sulit untuk dikonversi pada tahap berikutnya dan biasanya berlangsung lebih lama dari senyawa VFA lainnya. Propinonat yang tinggi menunjukan sedikitnya jumlah mikroba. Pencampuran yang terlalu tinggi dapat menghasilkan produksi propionat yang tinggi yang merupakan inhibitor pada tahap metanogenesis. pencampuran yang terlalu tinggi juga dapat mengganggu kestabilan proses dan meningkatkan penggunaan energi [11].
Pada penelitian yang dilakukan oleh M.hamdi [45] kecepatan pengadukan hingga 50 rpm dapat meningkatkan VFA selama produksi tetapi pada kecepatan pengadukan 200 rpm produksi VFA terganggu dan pada penelitian yang dilakukan oleh Johan Lindmark et. al [11] VFA tertinggi dihasilkan dengan seiring dengan peningkatan laju pengadukan yaitu minimally mixed sebesar 1,42 gr asam asetat/L, laju pengadukan 50 rpm sebesar 1,34 gr asam asetat/L dan laju pengadukan 150 rpm sebesar 1,43 gr asam asetat/L.
4.3.6 Pengaruh Laju Pengadukan Terhadap Rasio VFA/Alkalinitas
Adapun hubungan Rasio VFA/Alkalinitas terhadap proses variasi laju pengadukan dapat dilihat pada Gambar 4.14 yang menunjukkan rasio VFA/alkalinitas pada proses variasi laju pengadukan.
Gambar 4.14 Pengaruh Laju Pengadukan Terhadap Rasio VFA/Alkalinitas
Pada Gambar 4.14 menunjukkan rasio VFA/Alkalinitas pada laju pengadukan 50, 100, 150 dan 200 rpm masing masing adalah 1,50; 1,97; 2,41 dan 1,26. Proses digestasi anaerobik tahap asidognesis dan metanognesis memiliki rasio VFA/Alkalinitas yang berbeda. Pada proses asidognesis rasio VFA/Alkalinitas harus lebih besar dari 1 sedangkan rasio VFA/Alkalinitas pada proses metanognesis lebih kecil dari 0,8. rasio VFA/alkalinitas dapat digunakan sebagai ukuran stabilitas proses [10].
Pada penelitian ini, proses asidognesis telah berlangsung pada semua laju pengadukan dimana rasio VFA/Alkalinitas yang diperoleh lebih besar dari 1. Rasio VFA/Alklinitas tertinggi diperoleh pada laju pengadukan 150 rpm yaitu 2,41. Perubahan laju pengadukan mengakibatkan perubahan VFA/Alkalinitas yang signifikan. Hasil ini menunjukkan laju pengadukan 150 rpm merupakan laju pengadukan yang paling stabil dan terbaik.
1,50
1,97
2,41
1,26
0 1 2 3 4 5
0 50 100 150 200
V
F
A
/A
lk
a
li
n
it
a
s
[image:61.595.164.489.164.352.2]BAB V
KESIMPULAN DAN SARAN
5.1 KESIMPULAN
Adapun kesimpulan yang diperoleh dari penelitian pengaruh HRT dan laju pengadukan pada proses asidogenesis LCPKS pada temperatur 45oC adalah:
1. Pada proses variasi HRT dan laju pengadukan tidak berpengaruh secara signifikan terhadap profil pH dan Alkalinitas karena pH dijaga konstan 6 (± 0,2).
2. HRT terbaik di tunjukan pada HRT 4 dengan nilai VSS sebesar 21.460 mg/L, reduksi COD sebesar 42 %, total VFA sebesar 4.994,773 mg/L dan rasio VFA/Alkalinitas sebesar 2,41.
3. laju pengadukan terbaik di tunjukan pada laju pengadukan 150 rpm dengan nilai VSS sebesar 21.460 mg/L, reduksi COD sebesar 42 %, total VFA sebesar 4.994,773 mg/L dan rasio VFA/Alkalinitas sebesar 2,41.
4. Kondisi terbaik juga ditunjukan pada variasi laju pengadukan yaitu 100 rpm dengan nilai reduksi COD sebesar 39% sedangkan laju pengadukan 150 rpm sebesar 42%, dimana semakin rendahnya reduksi COD maka proses berjalan baik pada tahap asidogenesis.
5.2 SARAN
Adapun saran yang dapat diberikan untuk peneliti berikutnya adalah:
1. Melakukan proses loading up (variasi HRT) dengan laju pengadukan 100 rpm pada temperatur 45oC berdasarkan hasil terbaik pada penelitian ini.
BAB II
TINJAUAN PUSTAKA
2.1 LIMBAH CAIR PABRIK KELAPA SAWIT (LCPKS)
Kelapa sawit merupakan salah satu minyak nabati yang populer di dunia dan konsumsinya yang terus meningkat [6]. Tingginya peningkatan permintaan biofuel maka terjadi peningkatan produksi minyak kelapa sawit sehingga peningkatan limbah dari pengolahan tersebut juga meningkat [14]. Pabrik minyak kelapa sawit dalam mengolah setiap ton tandan buah segar akan menghasilkan rata-rata 120-200 kg minyak kelapa sawit mentah, 230-250 kg tandan kosong kelapa sawit, 130-150 kg serat/fiber, 60-65 kg cangkang, 55-60 kg kernel, dan 0,7 m3 LCPKS [4]. Limbah
pabrik kelapa sawit mentah yang terdiri dari materi senyawa organik kompleks yang tebal, berwarna kecoklatan, berbentuk bubur koloid dari air, minyak dan padatan termasuk sekitar 2% padatan tersuspensi yang berasal terutama dari sisa-sisa komponen selulosa [5]. Limbah cair pabrik minyak kelapa sawit merupakan suspensi koloid yang mengandung 95-96% air, 0,6-0,7% minyak dan 4-5% total padatan termasuk 2-4% padatan tersuspensi [15]. COD yang tinggi pada LCPKS karena memiliki jumlah karbon rendah (8-20) dari asam amino dan asam lemak yang