UJI TOKSISITAS AKUT EKSTRAK ETANOL
BUNGA PEPAYA JANTAN (
Carica papaya
L
.)
PADA MENCIT JANTAN
SKRIPSI
OLEH:
FADLY AR RAZI
NIM 091501077
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
UJI TOKSISITAS AKUT EKSTRAK ETANOL
BUNGA PEPAYA JANTAN (
Carica papaya
L
.)
PADA MENCIT JANTAN
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh
Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
FADLY AR RAZI
NIM 091501077
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
2014
PENGESAHAN SKRIPSI
UJI TOKSISITAS AKUT EKSTRAK ETANOL
BUNGA PEPAYA JANTAN (
Carica papaya
L
.)
PADA MENCIT JANTAN
OLEH:FADLY AR RAZI NIM 091501077
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal : 14 Juli 2014
Pembimbing I, Panitia Penguji,
Dr. Edy Suwarso, S.U., Apt. Dr. Kasmirul Ramlan Sinaga, M.S., Apt.
NIP 130953857 NIP 195504241983031003
Pembimbing II, Dr. Edy Suwarso, S.U., Apt. NIP 130953857
Dr. Marline Nainggolan, M.S., Apt. Marianne, S.Si., M.Si., Apt. NIP 195709091985112001 NIP 198005202005012006
Dra. Erly Sitompul, M.Si., Apt. NIP 195006121980032001
Medan, Juli 2014 Fakultas Farmasi
Universitas Sumatera Utara Dekan,
KATA PENGANTAR
Puji dan syukur kehadirat Allah SWT yang telah melimpahkan rahmat dan karunia kepada penulis sehingga dapat menyelesaikan penyusunan skripsi yang berjudul Uji Toksisitas Akut Ekstrak Etanol Bunga Pepaya Jantan (Carica papaya L.) Pada Mencit Jantan. Skripsi ini diajukan untuk melengkapi salah satu syarat untuk memperoleh gelar Sarjana Farmasi di Fakultas Farmasi Universitas Sumatera Utara.
Pada kesempatan ini, dengan segala kerendahan hati penulis mengucapkan terima kasih kepada Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas Farmasi yang telah menyediakan fasilitas kepada penulis selama perkuliahan di Fakultas Farmasi. Penulis juga mengucapkan terima kasih kepada Bapak Dr. Edy Suwarso, S.U., Apt., dan Ibu Dr. Marline Nainggolan, M.S., Apt., yang telah membimbing penulis dengan penuh kesabaran, memberikan petunjuk dan saran-saran selama penelitian hingga selesainya skripsi ini. Ucapan terima kasih juga penulis sampaikan kepada Bapak Dr. Kasmirul Ramlan Sinaga, M.S., Apt., selaku ketua penguji juga kepada Ibu Marianne, S.Si., M.Si., Apt., dan Ibu Dra. Erly Sitompul, M.Si., Apt., selaku anggota penguji yang telah memberikan evaluasi dan masukan kepada penulis dalam penyusunan skripsi ini .
Panggabean, serta abangda tercinta Rizky Al Akbar, yang senantiasa memberikan doa, dukungan, semangat dan kasih sayang yang tak ternilai dengan apapun. Penulis juga mengucapkan terima kasih kepada teman-teman Farmasi Klinis dan Komunitas 2009 atas doa dan dukungan dalam penyelesaian skripsi ini.
Penulis menyadari bahwa skripsi ini masih jauh dari kesempurnaan, sehingga penulis mengharapkan kritik dan saran yang bersifat membangun. Akhir kata, semoga tulisan ini dapat bermanfaat bagi pembaca dan menjadi sumbangan yang berarti bagi ilmu pengetahuan khususnya dalam bidang ilmu farmasi.
Medan, 14 Juli 2014 Penulis,
Fadly Ar Razi NIM 091501077
Uji Toksisitas Akut Ekstrak Etanol Bunga Pepaya Jantan (Carica Papaya L.) Pada Mencit Jantan
Abstrak
Uji toksisitas akut merupakan suatu pengujian untuk mendeteksi efek toksik yang muncul setelah pemberian sediaan uji dengan dosis tunggal yang diberikan secara oral pada hewan uji. Bunga pepaya jantan (Carica papaya L.)
termasuk famili Caricaceae, ekstrak etanolnya berkhasiat sebagai antimutagenik, antioksidan, antibakteri dan antikanker. Tujuan dari penelitian ini adalah mengetahui efek toksik dan mengetahui dosis toksik ekstrak etanol bunga pepaya jantan (EEBPJ).
Serbuk simplisia dimaserasi dengan pelarut etanol kemudian diuapkan dengan rotary evaporator ± 40oC selanjutnya di freeze dryer ± -40oC selanjutnya ekstrak yang diperoleh diuji toksisitas akutnya menggunakan mencit sebanyak 30 ekor dibagi dalam 6 kelompok yaitu kontrol diberi akuades, perlakuan diberi EEBPJ dosis 1000, 2000, 4000, 8000 dan dosis 16000 mg/kg bb yang diberikan secara oral hanya satu kali pemberian pada awal masa penelitian. Pengamatan dilakukan setiap hari meliputi gejala toksik, kematian mencit, LD50, berat badan, berat organ dan makropatologi.
Perhitungan LD50 EEBPJ menggunakan metode Thomson dan Weil, kemudian
dilakukan analisis statistic dengan uji ANOVA menggunakan Statistical Program Service Solution (SPSS) versi 19.
Hasil pengamatan tidak ditemukan gejala toksik pada kelompok kontrol, EEBPJ dosis 1000, 2000 dan 4000 mg/kg bb, sedang pada dosis 8000 dan 16000 mg/kg bb ditemukan gejala toksik. Pemberian EEBPJ kelompok kontrol, dosis 1000, 2000 dan 4000 mg/kg bb tidak ada dijumpai mencit yang mati sedang dosis 8000 dan 16000 mg/kg bb dijumpai. Nilai LD50 EEBPJ yaitu
7413,10 mg/kg dikategorikan sebagai toksisitas ringan. Hasil uji statistik tidak ada perbedaan yang signifikan antara kenaikan berat badan dengan pemberian EEBPJ (p > 0,05) tetapi terdapat perbedaan yang signifikan antara perbandingan berat organ relatif dengan pemberian EEBPJ (p < 0,05). Hasil makropatologi tidak dijumpai perubahan warna organ pada kelompok kontrol, EEBPJ dosis 1000, 2000 dan 4000 mg/kg bb sedang pada dosis 8000 dan 16000 mg/kg bb ditemukan perubahan.
Acute Toxicity Test Ethanol Extract Of Male Pepaya (Carica Papaya L.) Flowers On Male Mice
Abstract
Acute toxicity test is a test to detect the toxic effects that appear after administration of the test preparation with single doses which are given orally to test animals. Male papaya flowers (Carica papaya L.) is included in Caricaceae family which its ethanol extract can be used as antimutagenic, antioxidant, antibacterial and anticancer. The purpose of this study is to determine the toxic effects and toxic dose of ethanol extract of male papaya flowers (EEBPJ).
Simplex powder was macerated by ethanol 80% and evaporated by using rotary evaporator ± 40oC and freeze dried ± -40oC then obtained extract was tested for its acute toxicity using 30 mice which were divided into 6 groups: control group was given distilled water and the treatment groups which were given with EEBPJ dose 1000, 2000, 4000, 8000 and 16000 mg/kg bw EEBPJ which were administered orally with only a one-time provision at the beginning of the study period. Observations were conducted everyday including toxic symptoms, death of mice, LD50, weight gain, weight organ and
macropathology. The data is processed using formulas LD50 by Thomson and
Weil way, then data were analyzed by ANOVA using the Statistical Program Service Solution ( SPSS ) version 19.
The results showed that there were no toxic symptoms in the control group and treatment groups given with EEBPJ dose 1000, 2000 and 4000 mg/kg bw, while treatment groups given with EEBPJ dose 8000 and 16000 mg/kg bw showed toxic symptoms. EEBPJ control group, dose 1000, 2000 and 4000 mg/kg bw didnt show animals death, while EEBPJ dose 8000 and 16000 mg/kg bw showed. The value LD50 of EEBPJ 7413,10 mg / kg bw, be
categorized as slightly toxicity. Result of statistic showed no significant difference in weight gain within treatment groups given with EEBPJ (p > 0.05) but significant difference in relative organ weight within treatment groups given with EEBPJ (p < 0.05). Macrophatology results showed that there were no changed damaged in the control group and treatment groups given with EEBPJ dose 1000, 2000 and 4000 mg/kg bw, while treatment groups given with EEBPJ dose 8000 and 16000 mg/kg bw showed changed damaged.
DAFTAR ISI Halaman
JUDUL ... i
HALAMAN PENGESAHAN ... ii
KATA PENGANTAR ... iii
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 3
1.5 Manfaat Penelitian ... 4
1.6 Kerangka Pikir Penelitian ... 5
BAB II TINJAUAN PUSTAKA ... 6
2.1 Uraian Tumbuhan ... 6
2.1.1 Habitat tumbuhan ... 6
2.1.2 Nama lain ... 6
2.1.4 Morfologi tumbuhan ... 7
2.1.5 Kandungan kimia ... 8
2.1.6 Khasiat tumbuhan ... 8
2.2 Metode Ekstraksi ... 9
2.3 Toksisitas ... 11
2.3.1 Uji toksisitas akut ... 12
2.3.1.1 Metode penentuan LD50 ... 14
2.3.2 Uji toksisitas subkronik ... 16
2.3.3 Uji toksisitas kronik ... 17
2.4 Hati ... 18
2.5 Ginjal ... 19
2.6 Hewan Percobaan ... 19
BAB III METODE PENELITIAN ... 21
3.1 Alat dan Bahan ... 21
3.1.1 Alat ... 21
3.1.2 Bahan ... 21
3.2 Hewan Percobaan ... 21
3.3 Penyiapan Sampel ... 22
3.3.1 Pengumpulan tumbuhan ... 22
3.3.2 Identifikasi tumbuhan ... 22
3.3.3 Pembuatan simplisia ... 22
3.4 Pembuatan Ekstrak Etanol Bunga Pepaya Jantan ... 22
3.5.1 Pembuatan suspensi ekstrak etanol bunga pepaya jantan 23
3.5.2 Uji pendahuluan ... 23
3.5.3 Uji toksisitas akut ... 24
3.5.4 Pengamatan ... 24
3.5.4.1 Gejala toksik ... 24
3.5.4.2 Kematian hewan ... 24
3.5.4.3 Nilai LD50 ... 25
3.5.4.4 Berat badan ... 25
3.5.4.5 Berat organ ... 25
3.5.4.6 Makropatologi ... 25
3.6 Analisis Statistik ... 25
BAB IV HASIL DAN PEMBAHASAN ... 26
4.1 Hasil Identifikasi Tumbuhan ... 26
4.2 Hasil Ekstraksi Serbuk Bunga Pepaya Jantan ... 26
4.3 Hasil Uji Pendahuluan ... 26
4.4 Hasil Pengujian Toksisitas Akut ... 26
4.4.1 Hasil pengamatan gejala toksik ... 27
4.4.2 Hasil pengamatan kematian ... 28
4.4.3 Hasil nilai LD50 ... 29
4.4.4 Hasil pengamatan berat badan ... 30
4.4.5 Hasil pengamtan berat organ ... 31
BAB V
KESIMPULAN DAN SARAN ... 35
5.1 Kesimpulan ... 35
5.2 Saran ... 35
DAFTAR PUSTAKA ... 36
DAFTAR TABEL
Tabel Halaman
4.1 Hasil pengamatan gejala toksik ... 27 4.2 Hasil pengamatan kematian ... 28 4.3 Perhitungan nilai LD50 berdasarkan cara Thomson dan Weil .... 29
DAFTAR GAMBAR Gambar Halaman
DAFTAR LAMPIRAN
Lampiran Halaman
1 Hasil identifikasi tumbuhan ... 41
2 Gambar tumbuhan, simplisia dan serbuk simplisia bunga pepaya jantan ... 42
3 Bagan pembuatan ekstrak ….. ... 43
4 Bagan alur penelitian uji toksisitas akut ... 44
5 Contoh perhitungan dosis ... 45
6 Konversi perhitungan dosis dari mencit ke manusia ... 46
7 Hasil uji pendahuluan (orientasi) ... 48
8 Gambar alat, bahan dan objek yang digunakan ... 47
9 Gambar hewan percobaan yang digunakan ... 48
10 Gambar perbandingan organ antar kelompok ... 51
11 Tabel perhitungan LD50 dengan jumlah hewan 5 menurut Thomson dan Weil ... 53
12 Perhitungan LD50 dengan metode Thomson dan Weil ... 55
13 Hasil analisis spss berat badan ... 56
14 Hasil analisi spss berat organ hati ... 61
15 Hasil analisis spss berat organ ginjal kanan ... 66
Uji Toksisitas Akut Ekstrak Etanol Bunga Pepaya Jantan (Carica Papaya L.) Pada Mencit Jantan
Abstrak
Uji toksisitas akut merupakan suatu pengujian untuk mendeteksi efek toksik yang muncul setelah pemberian sediaan uji dengan dosis tunggal yang diberikan secara oral pada hewan uji. Bunga pepaya jantan (Carica papaya L.)
termasuk famili Caricaceae, ekstrak etanolnya berkhasiat sebagai antimutagenik, antioksidan, antibakteri dan antikanker. Tujuan dari penelitian ini adalah mengetahui efek toksik dan mengetahui dosis toksik ekstrak etanol bunga pepaya jantan (EEBPJ).
Serbuk simplisia dimaserasi dengan pelarut etanol kemudian diuapkan dengan rotary evaporator ± 40oC selanjutnya di freeze dryer ± -40oC selanjutnya ekstrak yang diperoleh diuji toksisitas akutnya menggunakan mencit sebanyak 30 ekor dibagi dalam 6 kelompok yaitu kontrol diberi akuades, perlakuan diberi EEBPJ dosis 1000, 2000, 4000, 8000 dan dosis 16000 mg/kg bb yang diberikan secara oral hanya satu kali pemberian pada awal masa penelitian. Pengamatan dilakukan setiap hari meliputi gejala toksik, kematian mencit, LD50, berat badan, berat organ dan makropatologi.
Perhitungan LD50 EEBPJ menggunakan metode Thomson dan Weil, kemudian
dilakukan analisis statistic dengan uji ANOVA menggunakan Statistical Program Service Solution (SPSS) versi 19.
Hasil pengamatan tidak ditemukan gejala toksik pada kelompok kontrol, EEBPJ dosis 1000, 2000 dan 4000 mg/kg bb, sedang pada dosis 8000 dan 16000 mg/kg bb ditemukan gejala toksik. Pemberian EEBPJ kelompok kontrol, dosis 1000, 2000 dan 4000 mg/kg bb tidak ada dijumpai mencit yang mati sedang dosis 8000 dan 16000 mg/kg bb dijumpai. Nilai LD50 EEBPJ yaitu
7413,10 mg/kg dikategorikan sebagai toksisitas ringan. Hasil uji statistik tidak ada perbedaan yang signifikan antara kenaikan berat badan dengan pemberian EEBPJ (p > 0,05) tetapi terdapat perbedaan yang signifikan antara perbandingan berat organ relatif dengan pemberian EEBPJ (p < 0,05). Hasil makropatologi tidak dijumpai perubahan warna organ pada kelompok kontrol, EEBPJ dosis 1000, 2000 dan 4000 mg/kg bb sedang pada dosis 8000 dan 16000 mg/kg bb ditemukan perubahan.
Acute Toxicity Test Ethanol Extract Of Male Pepaya (Carica Papaya L.) Flowers On Male Mice
Abstract
Acute toxicity test is a test to detect the toxic effects that appear after administration of the test preparation with single doses which are given orally to test animals. Male papaya flowers (Carica papaya L.) is included in Caricaceae family which its ethanol extract can be used as antimutagenic, antioxidant, antibacterial and anticancer. The purpose of this study is to determine the toxic effects and toxic dose of ethanol extract of male papaya flowers (EEBPJ).
Simplex powder was macerated by ethanol 80% and evaporated by using rotary evaporator ± 40oC and freeze dried ± -40oC then obtained extract was tested for its acute toxicity using 30 mice which were divided into 6 groups: control group was given distilled water and the treatment groups which were given with EEBPJ dose 1000, 2000, 4000, 8000 and 16000 mg/kg bw EEBPJ which were administered orally with only a one-time provision at the beginning of the study period. Observations were conducted everyday including toxic symptoms, death of mice, LD50, weight gain, weight organ and
macropathology. The data is processed using formulas LD50 by Thomson and
Weil way, then data were analyzed by ANOVA using the Statistical Program Service Solution ( SPSS ) version 19.
The results showed that there were no toxic symptoms in the control group and treatment groups given with EEBPJ dose 1000, 2000 and 4000 mg/kg bw, while treatment groups given with EEBPJ dose 8000 and 16000 mg/kg bw showed toxic symptoms. EEBPJ control group, dose 1000, 2000 and 4000 mg/kg bw didnt show animals death, while EEBPJ dose 8000 and 16000 mg/kg bw showed. The value LD50 of EEBPJ 7413,10 mg / kg bw, be
categorized as slightly toxicity. Result of statistic showed no significant difference in weight gain within treatment groups given with EEBPJ (p > 0.05) but significant difference in relative organ weight within treatment groups given with EEBPJ (p < 0.05). Macrophatology results showed that there were no changed damaged in the control group and treatment groups given with EEBPJ dose 1000, 2000 and 4000 mg/kg bw, while treatment groups given with EEBPJ dose 8000 and 16000 mg/kg bw showed changed damaged.
BAB I
PENDAHULUAN
1.1 Latar Belakang
Obat-obat modern walaupun telah mendominasi dalam pelayanan kesehatan, namun penggunaan obat tradisional tetap mendapat tempat yang penting bahkan terus berkembang (Depkes, 2000). Menurut perkiraan badan kesehatan dunia (WHO), 80% penduduk dunia masih tergantung pada pengobatan tradisional untuk mempertahankan kesehatan masyarakat (Iwuanyanwu, et al., 2012). Obat tradisional yang berasal dari tanaman telah banyak diteliti kandungan kimia dan khasiatnya, namun masih banyak tanaman yang belum diketahui efek toksisitasnya sehingga perlu diteliti lebih lanjut (Hyeronimus, 2006).
Obat tradisional agar dapat diterima di masyarakat maupun pelayanan kesehatan, maka harus didukung secara ilmiah adanya khasiat dan keamanan penggunaannya pada manusia. Tahapan pengembangan obat tradisional menjadi fitofarmaka adalah sebagai berikut: seleksi, uji preklinik (uji toksisitas dan farmakodinamika), pembuatan sediaan terstandar dan uji klinik (Dewoto, 2007).
senyawa alkaloid, flavonoid, tanin, triterpenoid/steroid, dan karbohidrat (Indrawati, dkk., 2002).
Beberapa penelitian yang telah dilakukan terhadap tumbuhan tersebut adalah bunganya, yaitu ekstrak etanolnya sebagai antibakteri terhadap bakteri
Escherichia coli dan Staphylococcus aureus (Iman, 2009), sebagai antimutagenik dan hasil karakterisasi simplisia bunga pepaya jantan diperoleh untuk kadar air 7,32%, kadar sari larut dalam air 19,25%, kadar sari larut dalam etanol 10,61%, kadar abu total 2,52% dan kadar abu tidak larut asam 0,22% (Sitorus, 2012), fraksi etilasetat bunga pepaya jantan sebagai antimutagenik (Francisca, 2012), sediaan gel ekstrak etanol bunga pepaya jantan sebagai antioksidan (Henova, 2012), ekstrak etanol fraksi n-heksan dan fraksi etilasetat bunga pepaya jantan sebagai antioksidan (Sianipar, 2013) dan ekstrak etanol sebagai antikanker payudara (Suwarso, dkk., 2013).
Tolak ukur kuantitatif yang paling sering digunakan untuk menyatakan kisaran dosis toksik adalah lethal dose (LD50). LD50 didefinisikan sebagai dosis
tunggal suatu zat yang diperkirakan akan membunuh 50% hewan percobaan. Penentuan nilai LD50 merupakan tahap awal untuk mengetahui tingkat
toksisitas (Loomis, 1978). Pengamatan dilakukan selama 24 jam pertama sejak diberikan perlakuan sampai hari ke-14. Hal ini bertujuan untuk mengetahui perubahan gejala yang terjadi setelah diberi perlakuan. Kriteria pengamatan dilakukan terhadap gejala–gejala toksik, perubahan berat badan, jumlah hewan yang mati pada masing–masing kelompok uji (Donatus, 1996). Oleh karena itu, harus dilakukan serangkaian uji yaitu selain uji khasiat, juga pengujian toksisitas dan uji klinik agar dapat dijadikan sebagai obat fitofarmaka (Depkes, 2000).
Penelitian ini menggunakan dosis 1000, 2000, 4000, 8000 dan 16000 mg/kg bb berdasarkan metode Thomson dan Weil dengan menggunakan kelipatan dosis. Dari uraian di atas, maka dilakukan uji toksisitas akut terhadap ekstrak etanol bunga pepaya jantan (EEBPJ) yang mempunyai potensi cukup tinggi untuk dijadikan sebagai bahan obat.
1.2 Perumusan Masalah
Perumusan masalah dalam penelitian ini adalah:
d. apakah EEBPJ berpengaruh terhadap berat organ hati dan ginjal mencit jantan?
e. apakah EEBPJ memberikan efek toksik pada organ hati dan ginjal mencit jantan?
1.3 Hipotesis
Berdasarkan perumusan masalah di atas, maka hipotesis:
a. EEBPJ memberikan efek terhadap gejala toksik mencit jantan. b. EEBPJ termasuk kategori toksik ringan terhadap mencit jantan. c. EEBPJ tidak berpengaruh terhadap berat badan mencit jantan.
d. EEBPJ berpengaruh terhadap berat organ hati dan ginjal mencit jantan. e. EEBPJ memberikan efek toksik pada organ hati dan ginjal mencit jantan.
1.4 Tujuan Penelitian
Adapun tujuan penelitian ini adalah untuk mengetahui: a. pengaruh EEBPJ terhadap gejala toksik mencit jantan. b. kategori toksisitas EEBPJ terhadap mencit jantan. c. pengaruh EEBPJ terhadap berat badan mencit jantan.
d. pengaruh EEBPJ terhadap berat organ hati dan ginjal mencit jantan. e. pengaruh EEBPJ terhadap organ hati dan ginjal mencit jantan.
1.5 Manfaat Penelitian
1.6 Kerangka Pikir Penelitian
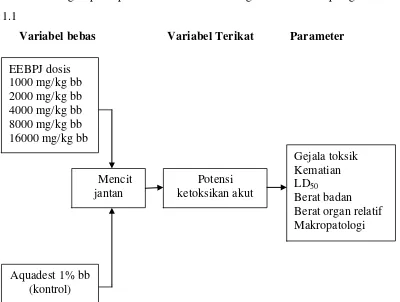
Kerangka pikir penelitian ini adalah sebagai berikut terdapat gambar 1.1
Variabel bebas Variabel Terikat Parameter
Gambar 1.1 Diagram kerangka pikir penelitian Aquadest 1% bb
(kontrol)
Potensi ketoksikan akut EEBPJ dosis
1000 mg/kg bb 2000 mg/kg bb 4000 mg/kg bb 8000 mg/kg bb 16000 mg/kg bb
Mencit jantan
Gejala toksik Kematian LD50
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
2.1.1 Habitat tumbuhan
Pepaya (Carica papaya L.) merupakan tanaman yang berasal dari Amerika, berada pada daerah tropis dan pusat penyebarannya diduga di daerah sekitar Meksiko bagian selatan dan Nikaragua (Kalie, 2008). Pada pertengahan abad ke-16 pepaya mulai banyak ditanam serta dibudidayakan di Cina dan Malaysia, diperkirakan mulai masuk ke Indonesia pada abad ke-17 yang dibawa oleh bangsa Portugis (Suprapti, 2005). Di Indonesia tanaman pepaya tersebar dimana-mana bahkan telah menjadi tanaman perkarangan. Sentra penanaman pepaya di Indonesia adalah daerah Jawa Barat (kabupaten Sukabumi), Jawa Timur (kabupaten Malang), Yogyakarta (Sleman), Lampung Tengah, Sulawesi Selatan (Toraja), Sulawesi Utara (Manado). Tanaman pepaya banyak ditanam orang, baik di daerah tropis maupun subtropis, di daerah-daerah basah dan kering atau di dataran tinggi dan pegunungan sampai 1000 m di atas permukaan laut
2.1.2 Nama lain
mentela, gadang , bandas (Kalimantan). Gedang, kates, kampaja, kalu jawa, padu, kaut panja, kalailu, paja, kapala, hango, muu jawa, muku jawa, kasi (Nusa Tenggara). Kapalay, papaya, pepaya, keliki, sumoyori, unti jawa, tangan-tangan nikare, kaliki, rianre (Sulawesi). Tele, palaki, papae, papaino, papau, papaen, papai, papaya, sempain, tapaya, kapaya (Maluku). Sampain, asawa, menam, siberiani, tapaya (Papua) (Depkes, 1985).
2.1.3 Sistematika tumbuhan
Sistematika tumbuhan pepaya adalah sebagai berikut (Suprapti, 2005). Kingdom : Plantae (tumbuh-tumbuhan)
Divisi : Spermatophyta (tumbuhan berbunga) Kelas : Dicotyledonae (biji berkeping dua) Ordo : Cistales
Famili : Caricaceae Genus : Carica
Spesies : Carica papaya L.
2.1.4 Morfologi Tumbuhan
bagian tengah yang berisi banyak biji. Di dalam buah terdapat biji dalam jumlah banyak, berwarna hitam keabu-abuan dan berbentuk bulat kecil (Mangan, 2008).
Bunga pepaya jantan termasuk bunga majemuk yang tersusun pada sebuah tangkai. Bunganya hanya memiliki benang sari yang berjumlah 10 buah. Bunga berbentuk tabung ramping dengan panjang kira kira 2,5 cm. Mahkota bunga terdiri dari lima helai dan berukuran kecil-kecil (Kalie, 2008).
2.1.5 Kandungan kimia
Berdasarkan penelitian yang telah dilakukan, hasil skrining bunga pepaya jantan menunjukkan adanya golongan senyawa alkaloid, flavonoid, tanin, steroid-triterpenoid (Indrawati, dkk., 2002; Sitorus, 2012; Henova, 2012).
2.1.6 Khasiat tumbuhan
Hampir seluruh bagian tumbuhan pepaya memiliki khasiat. Daunnya berkhasiat mengobati penyakit malaria (Rehena, 2010), melancarkan air susu ibu (Rengga dan Handayani, 2008) dan mengobati penyakit demam berdarah (Ahmad, 2011). Bijinya berkhasiat mengobati penyakit asam urat (Arsyiyanti, 2012), penyakit jantung koroner (Lusiana, dkk., 2011), sebagai antibakteri (Martiasih, dkk., 2012) dan antioksidan (Osato, et al., 1993). Getahnya berkhasiat untuk penyembuhan luka bakar (Fitria, dkk., 2014) dan obat jerawat (Anggraini, dkk., 2005). Akarnya berkhasiat antidiuretik (BPOM, 2010).
etil asetat sebagai antimutagenik (Fransisca, 2012), ekstrak etanol sebagai antioksidan (Henova, 2012), fraksi n-heksan dan fraksi etilasetat sebagai antioksidan (Sianipar, 2013), ekstrak metanol sebagai antibakteri (Iman, 2009) dan ekstrak etanol sebagai antikanker payudara (Suwarso, dkk., 2013).
2.2 Metode Ekstraksi
Ekstrak adalah sediaan pekat yang diperoleh dengan mengekstraksi zat aktif dari simplisia nabati atau hewani menggunakan pelarut yang sesuai, kemudian semua atau hampir semua pelarut diuapkan (Depkes, 2000). Ekstrak adalah sediaan kering, kental atau cair dibuat dengan menyari simplisia nabati atau hewani menurut cara yang cocok, diluar pengaruh cahaya matahari langsung (BPOM, 2012).
Ekstraksi (dalam istilah farmasi) yaitu proses pemisahan bagian senyawa aktif yang berkhasiat sebagai obat dari jaringan tanaman atau hewan dengan menggunakan pelarut tertentu, sesuai prosedur standart yang akan menghasilkan ekstrak (Depkes, 1979). Zat aktif yang terdapat dalam simplisia dapat digolongkan ke dalam golongan minyak atsiri, alkaloid, flavonoid dan lain-lain (Ditjen POM, 2000). Tujuan utama ekstraksi adalah untuk mendapatkan atau memisahkan sebanyak mungkin zat-zat yang memiliki khasiat pengobatan (Syamsuni, 2006).
Metode ekstraksi yang umum digunakan antara lain yaitu: • Maserasi
sedangkan remaserasi merupakan pengulangan penambahan pelarut setelah dilakukan penyaringan maserat pertama, dan seterusnya (Ditjen POM, 2000). Maserasi digunakan untuk simplisia yang zat aktifnya tidak tahan terhadap pemanasan. Pelarut yang dipakai adalah air atau pelarut organik (BPOM, 2012).
• Perkolasi
Perkolasi adalah proses penyarian simplisia dengan pelarut yang selalu baru sampai terjadi penyarian sempurna yang umumnya dilakukan pada temperatur kamar. Proses perkolasi terdiri dari tahap pelembapan bahan, tahap perendaman, tahap perkolasi (penetesan/penampungan ekstrak) terus-menerus sampai diperoleh perkolat (Depkes, 2000). Perkolasi umumnya digunakan untuk mengekstraksi serbuk kering simplisia terutama untuk bahan yang keras seperti kulit batang, kulit buah, biji kayu dan akar. Pelarut yang digunakan umumnya adalah etanol atau campuran etanol-air (BPOM, 2012).
• Refluks
Refluks adalah proses penyarian simplisia dengan menggunakan alat pada temperatur titik didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan adanya pendingin balik (Depkes, 2000).
• Digesti
Digesti adalah cara maserasi dengan menggunakan pemanasan pada suhu 40 – 500C. Cara maserasi ini hanya dapat dilakukan untuk simplisia yang zat aktifnya tahan terhadap pemanasan (BPOM, 2012).
Sokletasi adalah ekstraksi kontinu menggunakan alat soklet, dimana pelarut akan terdestilasi dari labu menuju pendingin, kemudian jatuh membasahi dan merendam sampel yang mengisi bagian tengah alat soklet, setelah pelarut mencapai tinggi tertentu maka akan turun ke labu destilasi, demikian berulang-ulang (Ditjen POM, 2000).
• Infundasi
Infundasi adalah proses penyarian dengan menggunakan pelarut air pada temperatur 90°C selama 15 menit (Depkes, 2000).
• Dekoktasi
Dekoktasi adalah proses penyarian dengan menggunakan pelarut air pada temperatur 90°C selama 30 menit (Depkes, 2000).
2.3 Toksisitas
Toksisitas adalah potensi bahan kimia untuk meracuni tubuh orang yang terpapar (Wisaksono, 2002). Toksisitas adalah kemampuan suatu zat asing dalam menimbulkan kerusakan pada organisme baik saat digunakan atau saat berada dalam lingkungan (Priyanto, 2009).
dapat digunakan untuk mengevaluasi resiko akibat pajanan bahan kimia yang terjadi (Klassen, 2012).
Penelitian toksisitas konvensional pada hewan coba sering mengungkapkan serangkaian efek akibat pajanan toksikan dalam berbagai dosis untuk berbagai masa pajanan. Penelitian toksikologi biasanya dibagi menjadi tiga kategori (Lu, 1995):
1. Uji toksisitas akut dilakukan dengan memberikan bahan kimia yang sedang diuji sebanyak satu kali atau beberapa kali dalam jangka waktu 24 jam.
2. Uji toksisitas jangka pendek (dikenal dengan subkronik) dilakukan dengan memberikan bahan kimia berulang-ulang, biasanya setiap hari, selama jangka waktu kurang lebih tiga bulan untuk tikus dan satu atau dua tahun untuk anjing.
3. Uji toksisitas jangka panjang dilakukan dengan memberikan bahan kimia berulang-ulang selama masa hidup hewan coba atau sekurang-kurangnya sebagian besar dari masa hidupnya, misalnya 18 bulan untuk mencit, 24 bulan untuk tikus, dan 7-10 tahun untuk anjing dan monyet.
2.3.1 Uji toksisitas akut
atau dosis berulang yang diberikan dalam waktu tidak lebih dari 24 jam; apabila pemberian dilakukan secara berulang, maka interval tidak kurang dari 3 jam (OECD, 2001).
Prinsip toksisitas akut yaitu pemberian secara oral suatu zat dalam beberapa tingkatan dosis kepada beberapa kelompok hewan uji (OECD, 2001). Takaran dosis yang dianjurkan pada toksisitas akut paling tidak terdapat empat peringkat dosis. Dari dosis terendah yang tidak atau hampir tidak mematikan seluruh hewan uji sampai dengan dosis tertinggi yang dapat mematikan seluruh atau hampir seluruh hewan uji (Donatus, 1996). Penilaian toksisitas akut ditentukan dari kematian hewan uji sebagai parameter akhir. Hewan yang mati selama percobaan dan yang hidup sampai akhir percobaan diotopsi untuk dievaluasi adanya gejala-gejala toksisitas dan selanjutnya dilakukan pengamatan secara makropatologi (OECD, 2001).
Tujuan uji toksisitas akut adalah untuk mengidentifikasi bahan kimia yang toksik dan memperoleh informasi tentang bahaya terhadap manusia bila terpajan. Uji toksisitas akut digunakan untuk menetapkan nilai LD50 suatu zat
Penelitian uji toksisitas akut sebagian besar dirancang untuk menentukan dosis lethal (LD50). LD50 didefinisikan sebagai dosis dari bahan
kimia yang dapat menyebabkan kematian sampai 50% dari jumlah hewan yang diuji (Darmono, 2011). LD50 yaitu dosis tunggal suatu bahan yang secara
statistik diharapkan akan membunuh 50% hewan coba. Pengujian ini dapat menunjukkan organ sasaran yang mungkin dirusak serta memberikan petunjuk tentang dosis yang sebaiknya digunakan dalam pengujian yang lebih lama (Lu, 1995).
Nilai LD50 sangat berguna untuk mengklasifikasikan zat kimia sesuai
dengan toksisitas relatifnya yaitu sebagai berikut:
Kategori LD50
Supertoksik 5 mg/kg atau kurang
Amat sangat toksik 5-50 mg/kg
Sangat toksik 50-500 mg/kg
Toksik sedang 0,5-5 g/kg
Toksik ringan 5-15 g/kg
Praktis tidak toksik >15 g/kg
2.3.1.1 Metode penentuan LD50
Penentuan LD50 merupakan tahap awal untuk mengetahui keamanan
bahan yang akan digunakan manusia dengan menentukan besarnya dosis yang menyebabkan kematian 50% pada hewan uji setelah pemberian dosis tunggal (Lu, 1995).
Untuk menghitung nilai LD50 dengan cara ini digunakan tabel
yang dibuat oleh Thompson dan Weil. Pada penggunaan tabel, percobaan harus memenuhi beberapa syarat berikut (Priyanto, 2009):
• Jumlah hewan uji tiap kelompok peringkat dosis sama • Interval merupakan kelipatan (d) tetap.
• Jumlah kelompok paling tidak terdapat 4 peringkat dosis. Rumus :
Log m = log D + d (f + 1) Dimana :
m = nilai LD50
D = Dosis terkecil yang digunakan d = log dari kelipatan dosis
f = suatu nilai dalam tabel Thompson dan Weil dari variasi angka kematian
b. Perhitungan nilai LD50 berdasarkan cara Farmakope Indonesia III (FI III)
Untuk menghitung LD50 berdasarkan FI III, uji harus
memenuhi syarat-syarat sebagai berikut (Priyanto, 2009):
• Menggunakan seri dosis atau konsentrasi yang berkelipatan tetap • Jumlah hewan percobaan tiap kelompok harus sama
• Dosis harus diatur sedemikian rupa supaya memberikan respon dari 0-100% dan hitungan dibatasi direntang tersebut.
m = log LD50
a = logaritma dosis terendah yang masih menyebabkan jumlah kematian 100% tiap kelompok
b = beda log dosis yang berurutan pi = jumlah hewan yang mati
2.3.2 Uji toksisitas subkronik
Uji toksisitas subkronik adalah uji ketoksikan sesuatu senyawa yang diberikan dengan dosis berulang pada hewan uji tertentu, selama kurang dari tiga bulan. Uji toksisitas subkronik sesuatu zat uji, utamanya ditujukan untuk mengungkapkan efek toksik dan jenis organ yang terkena, maupun hubungan antara dosis dan efek toksik. Selain itu, dengan uji toksisitas subkronik, memungkinkan terlihatnya wujud dan sifat efek toksik yang munculnya lambat dan tidak dapat terdeteksi pada uji toksisitas akut (Donatus, 1996).
Tujuan uji toksisitas subkronik oral adalah untuk memperoleh informasi adanya efek toksik zat yang tidak terdeteksi pada uji toksisitas akut, memperoleh informasi kemungkinan adanya efek toksik setelah pemaparan sediaan uji secara berulang dalam jangka waktu tertentu, memperoleh informasi dosis yang tidak menimbulkan efek toksik dan mempelajari adanya efek kumulatif dan reversibilitas atau irreversibiltas zat uji (OECD, 2008). Efek reversibilitas adalah efek toksik yang hilang bila pemaparan sediaan uji berhenti atau mereda. Efek irreversibilitas adalah efek toksik yang tidak akan hilang atau permanen meskipun sediaan uji telah berhenti atau hilang (Wisaksono, 2002). Uji toksisitas subkronik bertujuan untuk menentukan organ sasaran (organ yang rentan) (Priyanto, 2009).
2.3.3 Uji toksisitas kronik
Uji toksisitas kronik oral adalah suatu pengujian untuk mendeteksi efek toksik yang muncul setelah pemberian sediaan uji secara berulang sampai seluruh umur hewan. Perlu dilakukan uji toksisitas kronik mengingat pemakaian obat seringkali memerlukan waktu yang relatif panjang, bahkan mungkin sepanjang masa hidup si pemakai. Uji toksisitas kronik pada prinsipnya sama dengan uji toksisitas subkronik, tetapi sediaan uji diberikan selama tidak kurang dari 12 bulan (OECD, 2008). Keracunan yang bersifat kronis efek toksisitasnya baru dapat terlihat atau teridentifikasi dalam waktu lama, yang umumnya tidak disadari (Wirasuta dan Niruri, 2006).
yang panjang, memperoleh informasi efek toksik zat uji yang tidak terdeteksi pada uji toksisitas subkronik dan untuk menetapkan tingkat dosis yang tidak menimbulkan efek toksik (OECD, 2008). Pada uji toksisitas kronis ini dilakukan evaluasi patologi lengkap (Loomis, 1978).
2.4 Hati
Hati merupakan kelenjar yang paling besar dalam tubuh dan banyak sekali fungsinya. Fungsi hati adalah sebagai berikut (Setiadi, 2007):
1. Mengubah zat makanan yang diabsorpsi dan yang di simpan di suatu tempat dalam tubuh, dikeluarkan sesuai dengan pemakaiannya dalam jaringan.
2. Mengubah zat buangan dan bahan racun untuk diekskresi dalam empedu dan urin.
3. Menghasilkan enzim glikogenik glukosa menjadi glikogen.
4. Sekresi empedu, garam empedu di buat di hati, dibentuk dalam sistem retikuloendotelium, dialirkan ke empedu.
5. Pembentukan ureum, hati menerima asam amino diubah menjadi ureum, dikeluarkan dari darah oleh ginjal dalam bentuk urin.
6. Menyiapkan lemak untuk pemecahan terakhir asam karbonat dan air.
2.5 Ginjal
Ginjal mempunyai bagian fungsional yang disebut nefron yang terdiri dari glomerulus, tubulus proksimal, lengkung henle dan tubulus distal serta kandung kemih (Priyanto, 2009).
Fungsi ginjal adalah (Syaifuddin, 2006): 1. Mengatur volume air (cairan) dalam tubuh.
2. Mengatur keseimbangan osmotik dan mempertahankan keseimbangan ion yang optimal dalam plasma (keseimbangan elektrolit).
3. Ekskresi sisa hasil metabolisme (ureum, asam urat, kreatinin), zat-zat toksik, obat-obatan, hasil metabolisme hemoglobin dan bahan kimia asing. 4. Mempertahankan keseimbangan kadar asam dan basa dari cairan tubuh.
2.6 Hewan Percobaan
BAB III
METODE PENELITIAN
Penelitian ini menggunakan metode eksperimental dengan tahapan penelitian yaitu pengumpulan tumbuhan, identifikasi tumbuhan, pembuatan simplisia, pembuatan ekstrak, pengamatan gejala toksik, kematian, LD50, berat
badan, berat organ relatif dan makropatologi, kemudian dilakukan analisis statistik.
3.1 Alat dan Bahan
3.1.1 Alat
Alat-alat yang digunakan dalam penelitian ini adalah alat-alat gelas laboratorium, alat bedah (Wells spencer), alumunium foil, blender (Miyako), cawan porselin, Freeze dryer (Edwards), kamera digital, kandang mencit, lemari pengering, mortir dan stamfer, neraca hewan (Presica Geinweigher GW-1500), neraca listrik (Vibra), oral sonde, rotary evaporator
(Heidolph VV-300) , spuit ukuran 1 ml (Terumo).
3.1.2 Bahan
Bahan-bahan yang digunakan dalam penelitian ini meliputi bahan tumbuhan yaitu bunga pepaya jantan (Carica pepaya L.) dan bahan kimia yaitu akuades, etanol 80% dan natrium klorida 0,9%.
3.2 Hewan Percobaan
diaklimasi terlebih dahulu selama 7-14 hari. Sebanyak 30 ekor mencit dibagi dalam 6 kelompok.
3.3 Penyiapan Sampel
3.3.1 Pengumpulan tumbuhan
Pengumpulan tumbuhan dilakukan secara purposif yaitu tanpa membandingkan dengan tumbuhan yang sama dari daerah lain. Tumbuhan yang digunakan adalah bunga pepaya jantan (Carica pepaya L.) yang diperoleh dari desa Gunung Berkat, Kecamatan Bandar Pulau, Kabupaten Asahan, Provinsi Sumatera Utara.
3.3.2 Identifikasi tumbuhan
Identifikasi bunga pepaya jantan (Carica pepaya L.) dilakukan di
Herbarium Medanense (MEDA), Universitas Sumatera Utara.
3.3.3 Pembuatan simplisia
Bunga pepaya jantan (Carica pepaya L.) yang masih segar dipisahkan dari tangkainya, dicuci kemudian ditiriskan lalu ditimbang beratnya sebagai berat basah. Selanjutnya dikeringkan pada lemari pengering hingga kering yang ditandai dengan sampel mudah dipatahkan, kemudian diblender dan ditimbang sebagai berat serbuk simplisia.
3.4 Pembuatan Ekstrak Etanol Bunga Pepaya Jantan
Pembuatan EEBPJ dilakukan secara maserasi menggunakan etanol 80%.
Sebanyak 400 g serbuk simplisia bunga pepaya jantan dimasukkan ke dalam bejana, kemudian dituangi dengan 3 liter etanol 80%. Ditutup dan dibiarkan selama 5 hari terlindung dari cahaya sambil sering diaduk, diserkai dan diperas. Ampas dicuci kembali dengan 1 liter etanol 80%, dipindahkan ke dalam bejana tertutup, dibiarkan di tempat sejuk, terlindung dari cahaya selama 2 hari, selanjutnya disaring (Depkes RI, 1979). Maserat etanol yang diperoleh diuapkan dengan menggunakan rotary evaporator ± 40oC sampai diperoleh ekstrak kental kemudian dipekatkan dengan freeze dryer ± -40oC.
3.5 Pengujian Efek Toksisitas
Pengujian efek toksisitas meliputi pembuatan sediaan uji EEBPJ, uji pendahuluan, pengujian toksisitas akut meliputi gejala-gejala klinis, kematian hewan, LD50, perubahan berat badan dan makropatologi.
3.5.1 Pembuatan suspensi ekstrak etanol bunga pepaya jantan
Sediaan uji dibuat dengan konsentrasi 25% dan 50%, ditimbang ekstrak kemudian dimasukkan ke dalam lumpang, ditambahkan akuades digerus hingga merata. Sediaan uji EEBPJ dimasukkan ke dalam labu ukur, cukupkan dengan akuades hingga dicapai batas volume.
3.5.2 Uji pendahuluan
3.5.3 Uji toksisitas akut
Penelitian ini dilakukan berdasarkan metode Thomson dan Weil dengan menggunakan kelipatan dosis. Dari hasil uji pendahuluan maka didapatkan dosis untuk pengujian toksisitas akut. Mencit dikelompokkan menjadi 6 kelompok, masing-masing terdiri dari 5 ekor mencit yaitu: kelompok kontrol (1) dan kelompok perlakuan (2-6).
- Kelompok 1 : Kontrol normal,diberikan akuades 1% bb. - Kelompok 2 : diberi EEBPJ dosis 1000 mg/kg bb. - Kelompok 3 : diberi EEBPJ dosis 2000 mg/kg bb. - Kelompok 4 : diberi EEBPJ dosis 4000 mg/kg bb. - Kelompok 5 : diberi EEBPJ dosis 8000 mg/kg bb. - Kelompok 6 : diberi EEBPJ dosis 16000 mg/kg bb.
3.5.4 Pengamatan
Penimbangan mencit dilakukan pada hari ke-0, kemudian pada hari ke-1 diberi sediaan uji secara oral dan dilakukan pengamatan selama 14 hari (Angelina, dkk., 2008).
3.5.4.1 Gejala toksik
Pengamatan dilakukan setiap hari selama 14 hari, setelah pemberian diamati adanya kejang, salivasi, diare, lemas, tidur dan koma (OECD 2001).
3.5.4.2 Kematian hewan
3.5.4.3 Nilai LD50
Perhitungan nilai LD50 berdasarkan metode Thomson dan
Weil (Priyanto, 2009) dengan rumus: Log m = log D + d (f + 1)
Dimana : m = nilai LD50
D = dosis terkecil yang digunakan d = log dari kelipatan dosis
f = suatu nilai dalam tabel Weil, karena angka kematian tertentu (r)
3.5.4.4 Berat badan
Perubahan berat badan dianalisis seminggu sekali. Pada akhir penelitian, hewan yang masih hidup ditimbang dan diotopsi (OECD, 2001).
3.5.4.5 Berat Organ relatif
Organ yang akan ditimbang harus dikeringkan terlebih dahulu dengan kertas penyerap, kemudian segera ditimbang. Kemudian yang dianalisis adalah berat relatif, yaitu berat organ dibagi berat badan (OECD, 2001).
3.5.4.6 Makropatologi
Mencit yang mati segera diotopsi dan dilakukan pengamatan warna, permukaan dan konsistensi organ hati secara visual (Anggraini, 2008).
3.6 Analisis Statistik
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Identifikasi Tumbuhan
Identifikasi tumbuhan dilakukan di Herbarium Medanense (MEDA), Universitas Sumatera Utara Medan, disebutkan tumbuhan yang digunakan adalah tumbuhan bunga pepaya jantan (Carica papaya L.) suku Caricaceae. Hasil identifikasi dapat dilihat pada Lampiran 1 dan gambar tumbuhan pada Lampiran 2.
4.2 Hasil Ekstraksi Serbuk Bunga Pepaya Jantan
Pembuatan ekstrak dilakukan dengan metode maserasi menggunakan pelarut etanol 80% yang bertujuan untuk menarik senyawa metabolit sekunder yang terdapat dalam serbuk bunga pepaya jantan. Hasil maserasi dari 400 gram serbuk simplisia diperoleh ekstrak kental 31,5 gram (randemen 7,875%).
4.3 Hasil Uji Pendahuluan
Hasil uji pendahuluan selama 14 hari tidak ditemukan adanya gejala toksik dan kematian pada kelompok kontrol maupun kelompok perlakuan dosis 100, 200, 400 dan 800 mg/kg bb. Hasil uji pendahuluan dapat dilihat pada Lampiran 6.
4.4 Hasil Pengujian Toksisitas Akut
8000 dan 16000 mg/kg bb. Pengamatan dilakukan selama 14 hari meliputi gejala klinis, kematian hewan, berat badan dan makropatologi.
4.4.1 Hasil pengamatan gejala toksik
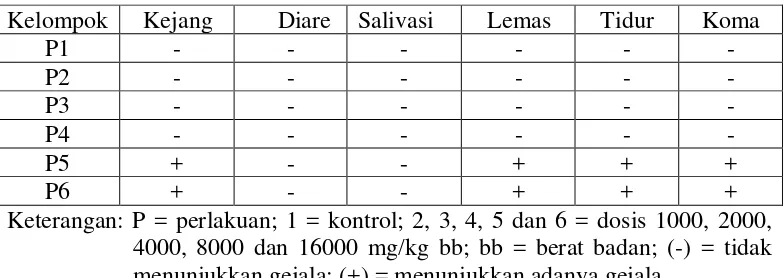
Hasil pengamatan yang dilakukan setiap hari selama 14 hari terhadap adanya kejang, diare, salivasi, lemas, tidur dan koma (OECD, 2001) dapat dilihat pada Tabel 4.1.
Tabel 4.1 Hasil pengamatan gejala toksik
Kelompok Kejang Diare Salivasi Lemas Tidur Koma
P1 - - - -
P2 - - - -
P3 - - - -
P4 - - - -
P5 + - - + + +
P6 + - - + + +
Keterangan: P = perlakuan; 1 = kontrol; 2, 3, 4, 5 dan 6 = dosis 1000, 2000, 4000, 8000 dan 16000 mg/kg bb; bb = berat badan; (-) = tidak menunjukkan gejala; (+) = menunjukkan adanya gejala
Berdasarkan tabel di atas terlihat bahwa pemberian EEBPJ tidak ditemukan adanya gejala toksik pada kelompok kontrol dan perlakuan pada dosis 1000, 2000 dan 4000 mg/kg bb. Pada dosis 8000 dan 16000 mg/kg bb ditemukan gejala klinis yaitu terjadi kejang, lemas, tidur dan koma pada mencit. Hal tersebut menunjukkan adanya hubungan antara dosis dan efek toksik, dimana makin besar dosis yang diberikan maka makin besar pula efek toksik yang timbul (Lu, 1995). Zat dapat menimbulkan efek yang tidak diinginkan berkaitan dengan dosis yang diberikan yaitu efek samping, efek merugikan dan efek toksik (Priyanto, 2009).
Evaluasi toksisitas akut tidak hanya mengenai LD50, tetapi juga
mendapatkan gambaran tentang sebab kematian (Darmansjah dan Wiria, 2007). Setiap zat bila diberikan dengan dosis yang cukup besar akan menimbulkan gejala-gejala toksik (Wirasuta dan Niruri, 2006). Dalam uji toksisitas akut, data yang dikumpulkan berupa tolak ukur ketoksikan kuantitatif yaitu kisaran dosis letal/toksik dan tolak ukur ketoksikan kualitatif yaitu gejala klinis (Donatus, 1996).
4.4.2 Hasil pengamatan kematian
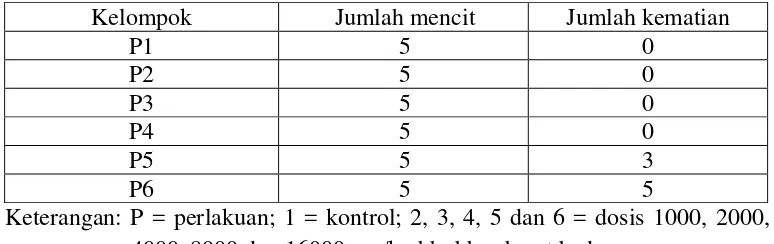
Hasil pengamatan kematian hewan selama waktu pemberian sediaan uji dapat dilihat pada Tabel 4.2
Tabel 4.2 Hasil pengamatan kematian
Kelompok Jumlah mencit Jumlah kematian
P1 5 0 4000, 8000 dan 16000 mg/kg bb; bb = berat badan
Berdasarkan tabel di atas menunjukkan bahwa pemberian EEBPJ pada kelompok kontrol, dosis 1000, 2000 dan 4000 mg/kg bb tidak terdapat mencit yang mati, dosis 8000 mg/kg bb terdapat 3 ekor mencit yang mati dan pada dosis 16000 mg/kg bb terdapat kematian mencit terbesar dari semua kelompok perlakuan yaitu 5 ekor mencit yang mati. Hal tersebut dikarenakan besarnya dosis EEBPJ yang menyebabkan kematian pada mencit. Efek toksik bertambah dengan naiknya dosis (Koeman, 1987).
4.4.3 Hasil nilai LD50
Pengaruh LD50 secara umum diukur menggunakan dosis bertingkat dan
berkelipatan tetap (Priyanto, 2009). Dosis bertingkat terdiri dari kelompok kontrol dan beberapa tingkat dosis yang berbeda (Donatus, 1996). Setelah toksikan diberikan, jumlah hewan yang mati harus diamati untuk memperkirakan LD50 (Lu, 1995).
Penghitungan LD50 berdasarkan cara Thomson dan Weil didasarkan
pada jumlah kematian hewan percobaan (Priyanto, 2009), dapat dilihat pada Tabel 4.3.
Tabel 4.3 Perhitungan nilai LD50 berdasarkan cara Thomson dan Weil
Kelompok Log dosis Kematian % kematian Keterangan
P3 3,3 0 0 Variasi
Data tabel di atas dapat dihitung nilai LD50 EEBPJ menggunakan rumus
dan tabel Thomson dan Weil karena terdapat kombinasi angka kematian dari 5 dosis tersebut. Jumlah kematian hewan percobaan dari lima tingkat dosis menghasilkan empat nilai r, yaitu 0, 0, 3, dan 5 dengan asumsi bahwa semua hewan coba mengalami kematian pada dosis lebih besar dari 16000 mg/kg bb. Nilai r tersebut memiliki nilai f sebesar 0,90000 dan δf sebesar 0,24493 yang kemudian digunakan untuk menghitung nilai LD50. Tabel Thomson dan Weil
dapat dilihat pada Lampiran 10.
Hasil perhitungan nilai LD50 yang didapat adalah 7413,10 mg/kg bb.
nilai LD50 diantara 5-15 g/kg bb. Perhitungan LD50 dapat dilihat pada
Lampiran 11.
4.4.4 Hasil pengamatan berat badan
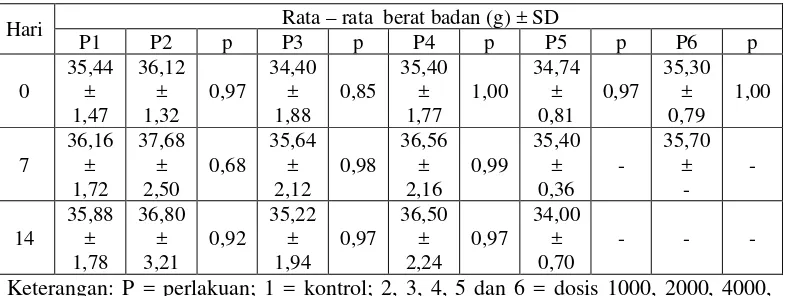
Hasil rata-rata berat badan tiap kelompok mencit sebelum dan sesudah diberi EEBPJ ditunjukkan pada Tabel 4.4
Tabel 4.4 Hasil rata-rata berat badan
Hari Rata – rata berat badan (g) ± SD
Berdasarkan tabel di atas terlihat bahwa hasil uji statistik menunjukkan tidak ada perbedaan yang signifikan antara kenaikan berat badan dengan pemberian EEBPJ (p > 0,05). Hal ini dapat dinyatakan bahwa pemberian EEBPJ tidak berpengaruh terhadap perkembangan berat badan mencit.
4.4.5 Hasil pengamatan berat organ relatif
Hasil berat organ relatif hati, ginjal kanan dan ginjal kiri dapat dilihat pada Tabel 4.5
Tabel 4.5 Hasil rata-rata berat organ relatif
Kelompok 4000, 8000 dan 16000 mg/kg bb; bb = berat badan; SD = standar deviasi; p = angka kebermaknaan
Perubahan pada berat organ merupakan indikator yang berguna bagi pengujian toksisitas (Lu, 1995). Hati dan ginjal umumnya merupakan target organ dari efek toksik senyawa kimia (Priyanto, 2009). Kenaikan dosis akan menyebabkan banyak organ yang dikenai sehingga akan timbul kerja yang lebih berat. Pada efek toksik yang menimbulkan kematian, berbagai organ akan mengalami kegagalan satu persatu (Ariens, dkk., 1986).
4.4.6 Hasil pengamatan makropatologi
Hasil pengamatan makropatologi meliputi pengamatan warna, permukaan dan konsistensi organ dapat dilihat pada Tabel 4.6
Tabel 4.6 Hasil pengamatan warna organ mencit
Organ Warna Organ
P1 P2 P3 P4 P5 P6
Hati mk mk mk mk mh mh
Ginjal mk mk mk mk mh mh
Keterangan: P = perlakuan; 1 = kontrol; 2, 3, 4, 5 dan 6 = dosis 1000, 2000, 4000, 8000 dan 16000 mg/kg bb; bb = berat badan; g = gram; mk=merah kecoklatan; mh=merah kehitaman
semua kelompok. Hasil gambar makropatologi organ hati dan ginjal dapat dilihat pada Lampiran 9.
Adanya perubahan warna organ menjadi salah satu parameter terjadinya suatu efek toksik. Pengamatan terhadap organ bertujuan mendapatkan informasi mengenai toksisitas zat uji dalam kaitannya dengan organ sasaran dan efek terhadap organ tersebut (Lu, 1995). Jika zat yang digunakan dalam jumlah besar maka dapat menimbulkan kerusakan. Efek toksik segera terjadi setelah senyawa toksik mencapai organ hati dan ginjal pada konsentrasi yang tinggi (Wirasuta dan Niruri, 2006).
Hati terlibat dalam metabolisme zat makanan serta sebagian besar obat dan toksikan (Ariens, dkk., 1986). Zat makanan, sebagian besar obat-obatan serta toksikan yang masuk melalui saluran cerna setelah diserap oleh epitel usus akan dibawa oleh vena porta ke hati. Oleh sebab itu, hati menjadi organ yang sangat potensial menderita keracunan lebih dahulu sebelum organ lain (Santoso dan Nurlaili, 2006). Terjadinya kerusakan pada hati dapat menjadi petunjuk apakah suatu zat yang diberikan bersifat toksik atau tidak (Elya, dkk., 2010).
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan penelitian yang telah dilakukan, maka kesimpulan dari penelitian ini adalah:
a. EEBPJ pada dosis di atas 8000 mg/kg bb memberikan gejala toksik terhadap mencit jantan.
b. EEBPJ termasuk kategori toksisitas ringan dengan nilai LD50 7413,10
mg/kg bb.
c. EEBPJ sampai dengan dosis 16000 mg/kg bb tidak berpengaruh terhadap berat badan mencit jantan.
d. EEBPJ pada dosis di atas 2000 mg/kg bb berpengaruh terhadap berat organ hati sedang sampai dengan dosis 16000 mg/kg bb tidak berpengaruh terhadap berat organ ginjal mencit jantan.
e. EEBPJ pada dosis di atas 8000 mg/kg bb memberikan efek toksik terhadap organ hati dan ginjal mencit jantan.
5.2 Saran
Berdasarkan penelitian yang telah dilakukan, maka disarankan kepada peneliti selanjutnya untuk:
a. menguji toksisitas kronik pada organ hati, ginjal, jantung dan lain sebagainya.
DAFTAR PUSTAKA
Ahmad, N. (2011). Dengue Fever Treatment With Carica papaya Leaves Extracts. Asian Pacific Journal of Tropical Biomedicine. Pages 417-420.
Angelina, M., Hartati, S., Dewijanti, I.D., Banjarnahor, S.D.S., dan Meilwati, L. (2008). Penentuan LD50 Daun Cinco (Cyclea barbata Miers.) Pada
Mencit. Makara Sains 12(1): 23-26. Halaman 2.
Anggraini, D., Malik, M., dan Susiladewi, M. (2005). Formulasi Krim Serbuk Getah Buah Pepaya (Carica papaya L.) Sebagai Anti Jerawat. Padang:
Skripsi. Fakultas Farmasi Universitas Andalas.
Anggraini, D.R. (2008). Gambaran Makroskopik dan Mikroskopik Hati dan Ginjal Mencit Akibat Pemberian Plumbum Asetat. Tesis. Medan: Sekolah Pascasarjana Universitas Sumatera Utara. Halaman 52.
Ariens E.J., Mutschler, E., dan Simonis, A.M. (1986). Pengantar Toksikologi Umum. Terjemahan oleh Yoke R Watimena, Mathilda B Widianto. Elin Yulinah Sukandar. Yogyakarta: Gajah Mada University Press. Halaman 134.
Arsyiyanti, C. (2012). Pengaruh Pemberian Jus Biji Pepaya (Carica papaya L.) Terhadap Kadar Asam Urat Tikus Sprague dawley Dislipidemia.
Artikel Penelitian. Semarang: Program Studi Ilmu Gizi Fakultas Kedokteran Universitas Dipenogoro.
BPOM RI. (2010). Direktorat Obat Asli Indonesia. Volume 5. Jakarta: Badan Pengawasan Obat dan Makanan RI. Halaman 74.
BPOM RI. (2012). Pedoman Teknologi Formulasi Sediaan Berbasis Ekstrak . Volume 1. Jakarta: Badan Pengawasan Obat dan Makanan RI. Halaman 6, 12-14.
Darmansjah, I., dan Wiria, M.S.W. (2009). Dasar Toksikologi. Dalam: Ganiswara, S.G. Farmakologi dan Terapi. Edisi 5. Jakarta: Departemen Farmakologi dan Terapeutik Fakultas Kedokteran Universitas Indonesia. Halaman 824.
Depkes RI. (1985). Tanaman Obat Indonesia. Jilid II. Jakarta: Departemen Kesehatan RI. Halaman 27.
Depkes. (2000). Parameter Standar Umum Ekstrak Tumbuhan Obat. Jakarta: Direktorat Jenderal Pengawasan Obat dan Makanan. Halaman 3.
Depkes RI. (1979). Farmakope Indonesia. Edisi Ketiga. Jakarta: Departemen Kesehatan RI. Halaman 7.
Ditjen POM. (2000). Parameter Standar Umum Ekstrak Tumbuhan Obat. Cetakan Pertama. Jakarta: Departemen Kesehatan RI. Halaman 3-5, 10-11.
Dewoto, H.R. (2007). Pengembangan Obat Tradisional Indonesia Menjadi Fitofarmaka. Jakarta: Fakultas Kedokteran Universitas Indonesia 57(7). Halaman 208.
Donatus, I.A. (1996). Petunjuk Praktikum Toksikologi. Edisi 6. Yogyakarta: Laboratorium Farmakologi dan Toksikologi Fakultas Farmasi Universitas Gajah Mada. Halaman 21, 27, 29.
Elya, B., Amin, J., dan Emiyanah. (2010). Toksisitas Akut Daun Justicia gendarussa Burm. Makara Sains 14(2): 129-134. Halaman 132.
Fitria, M., Saputra, D., dan Revilla, G. (2014). Pengaruh Papain Getah Pepaya Terhadap Pembentukan Jaringan Granulasi Pada Penyembuhan Luka Bakar Tikus Percobaan. Jurnal Kesehatan Andalas 3(1). Halaman 74. Francisca, N. (2012). Uji Antimutagenik Fraksi Etilasetat Bunga Pepaya Jantan
(Carica papaya L.) Pada Mencit Yang Diinduksi Dengan Siklofosfamid. Skripsi. Medan: Fakultas Farmasi Universitas Sumatera Utara.
Gupta, D., dan Bhardwaj, S. (2012). Study of Acute, Subacute and Chronic Toxicity Test. International Journal of Advanced Research in Pharmaceutical and Bio Sciences (IJARPB). 1(2): 103. Page 14.
Henova, F. (2012). Uji Aktivitas Antioksidan Ekstrak Etanol Bunga Jantan Tumbuhan Pepaya (Carica papaya L.) Serta Formulasi Sediaan Gel Berbasis Hpmc. Skripsi. Medan: Fakultas Farmasi Universitas Sumatera Utara.
Iman, M.N. (2009). Aktivitas Antibakteri Ekstrak Metanol Bunga Pepaya Jantan (Carica papaya L.) Terhadap Escherichia coli dan Staphylococcus aureus Multiresisten Antibiotik. Skripsi. Surakatra: Fakultas Farmasi UMS. Halaman 4.
Indrawati, Y., Kosasih., Soetarno, S., Gana, S.A. (2002). Telaah Fitokimia Bunga Pepaya Gantung (Carica papaya L.) dan Uji Aktivitas Antioksidannya. Tesis. Sekolah Farmasi ITB. Bandung.
Iwuanyanwu K.C.P., Amadi, U., Charles, I.A., dan Ayalogu, E.O. (2012). Evaluation of Acute and Subchronic Oral Toxicity Studi of Baker Cleanser Bitters A Polyherbal Drug On Experimental Rat. EXCLI Journal. 11(1): 632-640.
Kalie, M.B. (2008). Bertanam Pepaya. Jakarta: Penebar Swadaya. Halaman 1, 10-11, 17-18.
Klassen, C.D. (2012). Prinsip Toksikologi dan Penanganan Keracunan. Dalam: Goodman., dan Gilman. Dasar Farmakologi dan Terapi. Edisi 10. Volume 1. Jakarta: Penerbit Buku Kedokteran. Halaman 65.
Koeman, J.H. (1987). Pengantar Umum Toksikologi. Terjemahan oleh Yudono R.H. Yogyakarta: Gadjah Mada University Press. Halaman 55.
Loomis, T.A. (1978). Toksikologi Dasar. Edisi III. Edisi Terjemahan Alih Bahasa Imuno Argo Donatus. Semarang: IKIP press. Halaman 16. Lu, F.C. (1995). Toksikologi Dasar: Asas, Organ Sasaran, dan Penilaian
Resiko. Edisi Ke-2. Cetakan Pertama. Terjemahan: Edi Nugroho. Jakarta: UIP. Halaman 85-86, 210.
Lusiana, K., Magatra, P., dan Martono, Y. (2011). Ekstrak Limbah Biji Pepaya (Carica papaya Seeds) Anti Penyakit jantung Koroner. Skripsi. Salatiga: Fakultas Sains dan Matematika Universitas Kristen Satya Wacana.
Mangan, Y. (2008). Cara Bijak Menaklukkan Kanker. Jakarta: Agromedia Pustaka. Halaman 82.
Martiasih, M., Sidharta, B.B.R., dan Atmodjo, P.K. (2012). Aktivitas Antibakteri Ekstrak Biji Pepaya (Carica Papaya L.) Terhadap
Escherichia Coli Dan Streptococcus Pyogenes. Skripsi. Yogyakarta. Fakultas TeknobiologiUniversitas Atma Jaya.
OECD. (2001). Acute Oral Toxicity – Acute Toxic Class Method. OECD
OECD. (2008). Organization for Economic Cooperation and Development Guidelines for the Testing of Chemicals TG 407. Pages 1-13.
Osato, J.A., Santiago, L.A., Remo, G.M., Cuadra, M.S., dan Mori, A. (1993). Antimicrobial and Antioxidant Activities of Unripe Papaya. Life Science 53. Pages 1383-1389.
Priyanto. (2009). Toksikologi Mekanisme, Terapi Antidotum dan Penilaian Resiko. Depok: Lembaga Studi dan Konsultasi Farmakologi. Halaman 8, 54, 55.
Rehena, J.F. (2010). Uji Aktivitas Daun Pepaya (Carica papaya. L) sebagai Antimalaria in vitro. Jurnal Ilmu Dasar 11(1). Halaman 98.
Rengga, W.D.P., dan Handayani, P.A. (2008). Serbuk Instan Manis Daun Pepaya Sebagai Upaya Memperlancar Air Susu Ibu. Skripsi. Semarang: Fakultas Teknik Universitas Negeri Semarang.
Ridwan, E. (2013). Etika Pemanfaatan Hewan Percobaan dalam Penelitian Kesehatan. Artikel Pengembangan Pendidikan Keprofesian Berkelanjutan 63(3). Halaman 116.
Santoso, H.B., dan Nurliani, A. (2006). Efek Doksisiklin Selama Masa Organogenesis pada Struktur Histologi Organ Hati dan Ginjal Fetus Mencit. Bioscientiae 3(1). Halaman 3.
Sianipar, M.P. (2013). Uji Aktivitas Antioksidan Ekstrak Etanol Fraksi N -Heksan Dan Fraksi Etilasetat Bunga Pepaya Jantan (Carica papaya L.) Dengan Metode Dpph. Skripsi. Medan. Fakultas Matematika Dan Ilmu Pengetahuan Alam Universitas Muslim Nusantara Al – Washliyah. Sihombing, M., dan Raflizar. (2010). Status Gizi dan Fungsi Hati Mencit
(Galur Cbs-Swiss) dan Tikus Putih (Galur Wistar) Di Laboratorium Hewan Percobaan Puslitbang Biomedis dan Farmasi. Media Litbang Kesehatan 20(1). Halaman 33, 37.
Sitorus, W. (2012). Uji Antimutagenik Ekstrak Etanol Bunga Jantan Tumbuhan Pepaya (Carica papaya L.) Pada Mencit Jantan Yang Diinduksi Siklofosfamid. Skripsi. Medan : Fakultas Farmasi Universitas Sumatera Utara. Halaman 33.
Suprapti, M.L. (2005). Aneka Olahan Pepaya Mentah dan Mengkal. Yogyakarta: Kanisius. Halaman 13, 17.
Suwarso, E., Sinaga, K.R., dan Nainggolan, M. (2013). Kajian Ekstrak Etanol Bunga Papaya Jantan (Carica papaya. L) Sebagai Komopreventif Karsinogenesis Kanker Payudara Pada Tikus Betina Yang Mendapat Paparan 7, 12-Dimetilbenz (Α) Antrasena (DMBA). Medan: Laporan Hasil Penelitian Hibah Bersaing Tahun I.
Syaifuddin. (2006). Anatomi Fisiologi untuk Mahasiswa Keperawatan. Edisi Ketiga. Jakarta: Penerbit Buku Kedokteran EGC. Halaman 122, 178. Setiadi. (2007). Anatomi dan Fisiologi Manusia. Edisi Pertama. Yogyakarta:
Graha Ilmu. Halaman 77.
Syamsuni, H.A. (2006). Ilmu Resep. Jakarta: Penerbit Buku Kedokteran EGC. Halaman 23, 32.
Warisno. (2003). Budi Daya Pepaya. Yogyakarta: Penerbit Kanisius. Halaman 9.
Wirasuta, M.A.G., dan Niruri, R. (2006). Toksikologi Umum. Bali: Jurusan Farmasi Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Udayana. Halaman 22, 60.
Lampiran 2. Gambar tumbuhan, simplisia dan serbuk simplisia bunga pepaya jantan (Carica papaya L.)
Simplisia bunga pepaya jantan
Serbuk simplisia bunga pepaya jantan
Lampiran 3. Bagan pembuatan ekstrak
Dimasukkan ke dalam bejana
Ditambah pelarut etanol 80 %
Dibiarkan selama 5 hari terlindung dari cahaya sambil sesekali di aduk
Diserkai, diperas
Dicuci dengan pelarut etanol 80 % Dipindahkan ke dalam bejana tertutup
Dibiarkan di tempat sejuk, terlindung dari cahaya selama 2 hari
Dienap tuangkan dan di saring Serbuk
simplisia
Ampas Maserat I
Digabung
Dipekatkan dengan alat rotary evaporator
40oC
Dikeringkan dengan alat freeze dryer -40oC
Lampiran 5. Contoh perhitungan dosis
Berat badan mencit 35 g dengan dosis EEBPJ 1000 mg/kg bb Dosis = 1000 mg/kg bb
= 1000 mg
1000 g x 35 g = 35 mg
Konsentrasi ekstrak yang dibuat 25% = 25 g/100 ml = 25000 mg/100 ml = 250 mg/ml Jumlah obat yang disuntikkan = 35 mg
Lampiran 6. Konversi perhitungan dosis dari mencit terhadap manusia
Dosis pemberian EEBJP pada mencit yaitu 1000 mg/kg BB.
Maka, berat ekstrak yang diberikan untuk mencit dengan berat 35 gram yaitu :
Faktor konversi dari dosis pada mencit berat 35 gram terhadap manusia dengan berat 70 kg adalah 387,9, maka dosis yang harus diberikan kepada manusia untuk memberikan efek yang sama yaitu:
Berat EEBJP pada mencit = 35 g
1000 g× 1000 mg = 35 mg
Berat EEBJP pada manusia = 35 mg × 387,9 = 13576,5 mg
Pada pengerjaan sampel (bunga jantan pepaya), dari berat basah 3000 gram diperoleh berat ekstrak kental sebanyak 31,5 gram
Maka, untuk memperoleh ekstrak kental 13,5765 g dibutuhkan bunga pepaya segar sebanyak :
Jadi, untuk memberikan efek yang sama dengan EEBJP dosis 1000 mg/kg BB, kita harus mengkonsumsi bunga pepaya segar kira-kira 1,293 kg .
13,5765 g
� g =
31,5 g 3000 g
Lampiran 7. Hasil uji pendahuluan (orientasi) 1. Hasil pengamatan kematian
Keterangan: P = perlakuan; 1 = kontrol; 2, 3, 4 dan 5 = dosis 100, 200, 400 dan 800 mg/kg bb; bb = berat badan
2. Hasil pengamatan gejala klinis
Kelompok Kejang Diare Salivasi Lemas Tidur Koma
P1 - - - -
P2 - - - -
P3 - - - -
P4 - - - -
P5 - - - -
Keterangan: P = perlakuan; 1 = kontrol; 2, 3, 4 dan 5 = dosis 100, 200, 400 dan 800 mg/kg bb; bb = berat badan
Kelompok Jumlah mencit Jumlah kematian
P1 2 0
P2 2 0
P3 2 0
P4 2 0
Lampiran 8. Gambar alat yang digunakan
Oral sonde dan spuit
Lampiran 9. Gambar hewan percobaan yang digunakan
Mencit
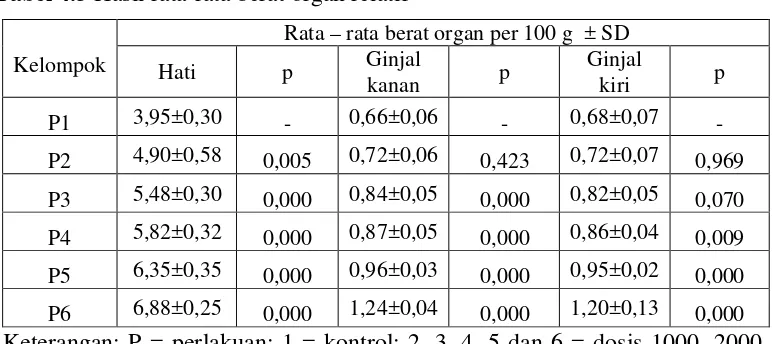
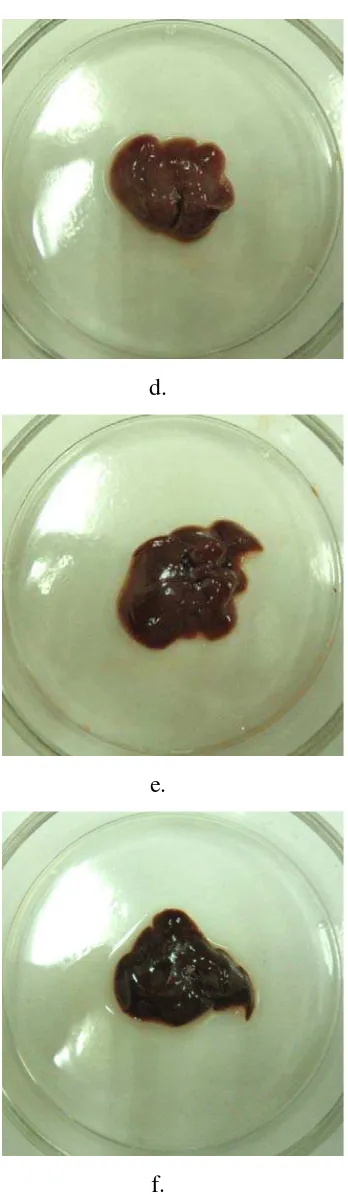
Lampiran 10. Gambar perbandingan organ antar kelompok Gambar organ hati
a.
b.
c.
d.
e.
Keterangan: a, kontrol diberi akuades, b, c, d, e dan f berturut-turut diberi dengan EEBPJ dosis 1000, 2000, 4000, 8000 dan 16000 mg/kg bb
Gambar organ ginjal
a.
b.
d.
Lampiran 12. Perhitungan LD50 dengan metode Thomson dan Weil
Rumus: Log m = log D + d (f + 1) Dimana :
D = 2000 mg/kg d = 2
r = 0,0,3 dan 5
f = dari tabel untuk r (kematian dalam kelompok uji) = 0,900 Log m = log D + log d (f + 1)
= log 2000 + log 2 (0.900 +1) = 3,30 + 0,3 (0,900 + 1) = 3,87
LD50 = anti log m
Lampiran 13. Hasil analisis spss berat badan
a. Test distribution is Normal.
Lampiran 13. (Lanjutan) BBharike0 kontrol 5 35.44
0
Lampiran 13. (Lanjutan)
ANOVA
Sum of
Squares df
Mean
Square F Sig.
BBharike0 Between
Groups
8.995 5 1.799 .910 .491
Within Groups 47.452 24 1.977
Total 56.447 29
BBharike7 Between
Groups
14.892 5 2.978 .728 .612
Within Groups 73.664 18 4.092
Total 88.556 23
BBharike1
4
Between
Groups
15.382 4 3.846 .730 .584
Within Groups 89.536 17 5.267
Lampiran 13. (Lanjutan) Tukey HSD
Dependent
Variable (I) perlakuan (J) perlakuan
Lampiran 14. Hasil analisis spss berat organ hati Descriptive Statistics
N Mean Std. Deviation Minimum Maximum
dosis 30 3.50 1.737 1 6
berathati 30 5.58170 1.051051 3.667 7.221
One-Sample Kolmogorov-Smirnov Test
dosis berathati
N 30 30
Normal Parametersa,b Mean 3.50 5.58170
Std. Deviation 1.737 1.051051
Most Extreme Differences Absolute .139 .107
Positive .139 .079
Negative -.139 -.107
Kolmogorov-Smirnov Z .764 .588
Asymp. Sig. (2-tailed) .604 .879
a. Test distribution is Normal.
Lampiran 14. (Lanjutan)
Descriptives
berat organ hati
N Mean
Std.
Deviation Std.
Error
95% Confidence
Interval for Mean
Minimum Maximum Lower
Bound
Upper
Bound
kontrol 5 3.94960 .297001 .132823 3.58083 4.31837 3.667 4.382
1000mg/kg 5 4.89640 .581322 .259975 4.17459 5.61821 4.189 5.563
2000mg/kg 5 5.48560 .305341 .136553 5.10647 5.86473 5.142 5.814
4000mg/kg 5 5.82400 .316616 .141595 5.43087 6.21713 5.619 6.385
8000mg/kg 5 6.34840 .354190 .158399 5.90861 6.78819 5.790 6.686
16000mg/kg 5 6.98620 .248656 .111202 6.67745 7.29495 6.628 7.221
Total 30 5.58170 1.051051 .191895 5.18923 5.97417 3.667 7.221
ANOVA
berathati
Sum of Squares df Mean Square F Sig.
Between Groups 28.809 5 5.762 42.844 .000
Within Groups 3.228 24 .134
Lampiran 14. (Lanjutan)
kontrol 1000mg/kgbb -.946800* .231935 .005 -1.66393 -.22967
2000mg/kgbb -1.536000* .231935 .000 -2.25313 -.81887
4000mg/kgbb -1.874400* .231935 .000 -2.59153
-1.15727
8000mg/kgbb -2.398800* .231935 .000 -3.11593
-1.68167
16000mg/kgbb -3.036600* .231935 .000 -3.75373
-2.31947
1000mg/kgbb kontrol .946800* .231935 .005 .22967 1.66393
2000mg/kgbb -.589200 .231935 .152 -1.30633 .12793
4000mg/kgbb -.927600* .231935 .006 -1.64473 -.21047
8000mg/kgbb -1.452000* .231935 .000 -2.16913 -.73487
16000mg/kgbb -2.089800* .231935 .000 -2.80693
-1.37267
2000mg/kgbb kontrol 1.536000* .231935 .000 .81887 2.25313
1000mg/kgbb .589200 .231935 .152 -.12793 1.30633
4000mg/kgbb -.338400 .231935 .692 -1.05553 .37873
8000mg/kgbb -.862800* .231935 .012 -1.57993 -.14567
16000mg/kgbb -1.500600* .231935 .000 -2.21773 -.78347
4000mg/kgbb kontrol 1.874400* .231935 .000 1.15727 2.59153
1000mg/kgbb .927600* .231935 .006 .21047 1.64473
2000mg/kgbb .338400 .231935 .692 -.37873 1.05553
16000mg/kgbb -1.162200* .231935 .001 -1.87933 -.44507
8000mg/kgbb kontrol 2.398800* .231935 .000 1.68167 3.11593
1000mg/kgbb 1.452000* .231935 .000 .73487 2.16913
2000mg/kgbb .862800* .231935 .012 .14567 1.57993
4000mg/kgbb .524400 .231935 .248 -.19273 1.24153
16000mg/kgbb -.637800 .231935 .102 -1.35493 .07933
16000mg/kgbb kontrol 3.036600* .231935 .000 2.31947 3.75373
1000mg/kgbb 2.089800* .231935 .000 1.37267 2.80693
2000mg/kgbb 1.500600* .231935 .000 .78347 2.21773
Lampiran 14. (Lanjutan)
berat organ hati
Tukey HSDa
dosis N
Subset for alpha = 0.05
1 2 3 4 5
kontrol 5 3.94960
1000mg/kgbb 5 4.89640
2000mg/kgbb 5 5.48560 5.48560
4000mg/kgbb 5 5.82400 5.82400
8000mg/kgbb 5 6.34840 6.34840
16000mg/kgbb 5 6.98620
Sig. 1.000 .152 .692 .248 .102
Means for groups in homogeneous subsets are displayed.