PENGGUNAAN NATRIUM TRIPOLIFOSFAT UNTUK
PEMBUATAN NANOPARTIKEL KITOSAN
DARI CANGKANG BELANGKAS
SKRIPSI
WIWI WIJAYANTI PUTRI 110802022
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PENGGUNAAN NATRIUM TRIPOLIFOSFAT UNTUK
PEMBUATAN NANOPARTIKEL KITOSAN
DARI CANGKANG BELANGKAS
SKRIPSI
Diajukanuntukmelengkapi tugasdanmemenuhisyaratmencapaigelarsarjanasains
WIWI WIJAYANTI PUTRI 110802022
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : Penggunaan Natrium Tripolifosfat untuk Pembuatan Nanopartikel Kitosan dari Cangkang Belangkas
Kategori : Skripsi
Nama : Wiwi Wijayanti Putri
NIM : 110802022
Program Studi : Sarjana (S1) Kimia Departemen : Kimia
Fakultas : Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara
Disetujui di, Medan, Mei 2015
Komisi Pembimbing :
Dosen Pembimbing 2, Dosen Pembimbing 1,
Prof. Dr. Zul Alfian,M.Sc. Prof. Dr. Harry Agusnar,M.Sc.,M.Phill. NIP.195504051983031002 NIP.195308171983031002
Disetujui Oleh
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
PENGGUNAAN NATRIUM TRIPOLIFOSFAT UNTUK PEMBUATAN NANOPARTIKEL KITOSAN
DARI CANGKANG BELANGKAS
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing – masing disebutkan sumbernya.
Medan, Mei 2015
PENGHARGAAN
Puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Pemurah dan Maha Penyayang, dengan limpah karunia-Nya, skripsi ini berhasil diselesaikan dalam waktu yang telah ditetapkan.
Ucapan terima kasih penulis sampaikan kepada Ibu, Bapak, dan sanak keluarga yang selama ini memberikan bantuan dan dorongan yang diperlukan. Ucapan terima kasih juga penulis sampaikan kepada Prof. Dr. Harry Agusnar, M.Sc. selaku pembimbing I dan Prof. Dr. Zul Alfian, M.Sc. selaku pembimbing II pada penyelesaian skripsi ini yang telah memberikan panduan dan penuh kepercayaan kepada penulis untuk menyempurnakannya. Ucapan terima kasih juga ditujukan kepada ketua dan sekretaris Departemen Kimia, Dr. Rumondang Bulan, MS. dan Drs. Albert Pasaribu, M.Sc., kepala dan laboran Laboratorium Kimia Analitik FMIPA USU, Prof. Dr. Harlem Marpaung dan Sri Pratiwi Aritonang, M.Si., dosen penasehat akademik, Dr. Juliati br. Tarigan, M.Si., kakak-abang-adik, serta rekan-rekan kuliah. Akhirnya, tidak terlupakan kepada kakak-abang-adik asisten LA, rekan asisten seperjuangan: Fayek, Andy, Emi, Berbun, dan Beyek yang selama ini memberikan bantuan dan dorongan yang diperlukan, seluruh asisten LAKO khususnya Berny, Hotplate, Batu yang telah menemani penelitian hingga malam, serta adik yang paling nakal si Nina, Kak Dee, kak Annisa, dan ko Joshua, yang telah mencarikan solusi ketika penulis berada dalam kesulitan. Semoga Tuhan Yang Maha Esa akan membalasnya.
PENGGUNAAN NATRIUM TRIPOLIFOSFAT UNTUK PEMBUATAN NANOPARTIKEL KITOSAN
DARI CANGKANG BELANGKAS
ABSTRAK
Telah dilakukan penggunaan natrium tripolifosfat untuk pembuatan nanopartikel kitosan dari cangkang belangkas. Kitosan cangkang belangkas dilarutkan dengan larutan asam asetat 2%, ditambahkan larutan natrium tripolifosfat 0,75 mg/mL kemudian diaduk hingga terbentuk suspensi nanopartikel kitosan. Suspensi nanopartikel kitosan yang terbentuk disentrifugasi dengan kecepatan 11000 rpm selama 30 menit, direndam dengan akua steril, serta didekantasi supernatan yang terbentuk. Kemudian nanopartikel kitosan dikeringkan dengan menggunakan freeze dryer dan dikarakterisasi menggunakan PSA dan FTIR. Hasilnya nanopartikel kitosan yang terbentuk berukuran 58 nm.
THE USE OF SODIUM TRIPOLYPHOSPHATE FOR PREPARATION OF NANOPARTICLE CHITOSAN FROM
HORSESHOE-CRAB’S SHELL
ABSTRACT
The use of sodium tripolyphosphate for preparation of nanoparticle chitosan from horseshoe-crab’s shell have been done. Horseshoe-crab’s shell chitosan dissolved in acetid acid 2%, and added into it, sodium tripolyphosphate 0.75 mg/mL then have it stirred until suspension of chitosan nanoparticles are formed. Suspension of chitosan nanoparticles centrifugated in 11000 rpm for 30 minutes, soaked with sterile aqua, also performed a decantation to supernatan formed. Further action was to dry the chitosan nanoparticles with freeze dryer and characterized them by using Particle Size Analyzer and Fourier Transform Infra Red. The result is chitosan nanoparticles with the sizes of 58 nm.
DAFTAR ISI
Bab 1 Pendahuluan 1.1. Latar Belakang 1
Bab 3 Metode Penelitian
3.1. Alat 24
3.2. Bahan 24
3.3. Prosedur Penelitian 25
3.3.1. Pembuatan Pereaksi 25
3.3.2. Pembuatan Nanopartikel Kitosan 25
3.4. Bagan Penelitian 26
3.4.1. Pembuatan Pereaksi 26
3.4.2. Pembuatan Nanopartikel Kitosan 27
Bab 4 Hasil dan Pembahasan 4.1. Hasil 28
4.2. Pembahasan 29
Bab 5 Kesimpulan dan Saran 5.1. Kesimpulan 33
5.2. Saran 33
Daftar Pustaka 34
DAFTAR TABEL
Nomor Judul Halaman
Tabel
2.1 Spesifikasi Kitin 7 2.2 Kelarutan Kitosan pada berbagai Pelarut Asam Organik 9 2.3 Spesifikasi Kitosan 10 4.1 Perbandingan Larutan Asam Asetat dan Larutan Natrium
DAFTAR GAMBAR
Nomor Judul Halaman Gambar
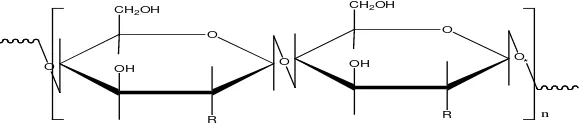
2.1 Struktur Polimer Selulosa dan Kitin 6
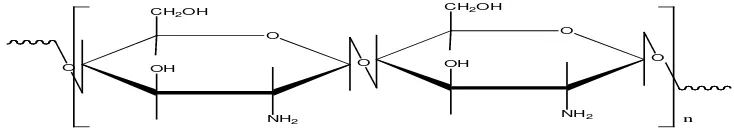
2.2 Struktur Polimer Kitosan 8
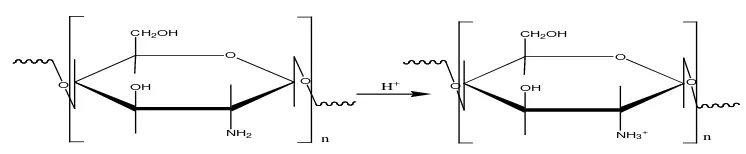
2.3 Kitosan sebagai Polielektrolit Kationik 10
2.4 Disosiasi Natrium Tripolifosfat dalam Air 13
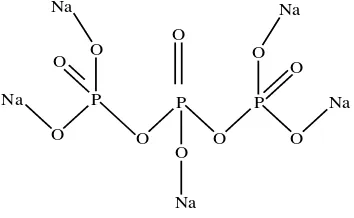
2.5 Struktur Natrium Tripolifosfat 14
2.6 Ikat Silang Ionik Kitosan dengan Natrium Tripolifosfat 19
4.1 Grafik Distribusi Persen Jumlah dan Ukuran Partikel 28
DAFTAR LAMPIRAN
Nomor Judul Halaman
Lampiran
1 Pengadukan Campuran Larutan Kitosan dengan Natrium
Tripolifosfat 38
2 Hasil Sentrifugasi Suspensi Nanopartikel Kitosan 38
3 Hasil Pengeringan Nanopartikel Kitosan 38
4 Freeze Dryer 39
5 Particle Size Analyzer 39
PENGGUNAAN NATRIUM TRIPOLIFOSFAT UNTUK PEMBUATAN NANOPARTIKEL KITOSAN
DARI CANGKANG BELANGKAS
ABSTRAK
Telah dilakukan penggunaan natrium tripolifosfat untuk pembuatan nanopartikel kitosan dari cangkang belangkas. Kitosan cangkang belangkas dilarutkan dengan larutan asam asetat 2%, ditambahkan larutan natrium tripolifosfat 0,75 mg/mL kemudian diaduk hingga terbentuk suspensi nanopartikel kitosan. Suspensi nanopartikel kitosan yang terbentuk disentrifugasi dengan kecepatan 11000 rpm selama 30 menit, direndam dengan akua steril, serta didekantasi supernatan yang terbentuk. Kemudian nanopartikel kitosan dikeringkan dengan menggunakan freeze dryer dan dikarakterisasi menggunakan PSA dan FTIR. Hasilnya nanopartikel kitosan yang terbentuk berukuran 58 nm.
THE USE OF SODIUM TRIPOLYPHOSPHATE FOR PREPARATION OF NANOPARTICLE CHITOSAN FROM
HORSESHOE-CRAB’S SHELL
ABSTRACT
The use of sodium tripolyphosphate for preparation of nanoparticle chitosan from horseshoe-crab’s shell have been done. Horseshoe-crab’s shell chitosan dissolved in acetid acid 2%, and added into it, sodium tripolyphosphate 0.75 mg/mL then have it stirred until suspension of chitosan nanoparticles are formed. Suspension of chitosan nanoparticles centrifugated in 11000 rpm for 30 minutes, soaked with sterile aqua, also performed a decantation to supernatan formed. Further action was to dry the chitosan nanoparticles with freeze dryer and characterized them by using Particle Size Analyzer and Fourier Transform Infra Red. The result is chitosan nanoparticles with the sizes of 58 nm.
BAB 1
PENDAHULUAN
1.1. Latar Belakang
Di alam, kitin dikenal sebagai polisakarida yang paling melimpah setelah selulosa.
Kitin umumnya banyak dijumpai pada hewan avertebrata laut, darat, dan jamur
dari genus Mucor, Phycomyces, dan Saccharomyces (Hirano, 1986).
Dewasa ini, secara komersial, kitin dan kitosan dihasilkan dari buangan
organisme akuatik (Crestini et al., 1996, Nwe dan Stevens, 2008). Selama ini,
sebagaimana yang kita ketahui limbah organisme akuatik seperti kulit udang,
cangkang belangkas dan lain-lain di Indonesia hanya dimanfaatkan untuk pakan
ternak, hidrolisat protein, silase, bahan baku terasi, petis, dan kerupuk udang.
Kitin dapat diisolasi melalui proses deproteinasi yang diikuti dengan
demineralisasi. Kitin juga dapat diubah menjadi kitosan setelah lebih dari 70%
gugus asetil (CH3CO-)nya dihilangkan.
Belangkas merupakan komoditas andalan dan bernilai ekonomis sebagai
salah satu hasil perikanan utama (selain udang dan kepiting) di kota Medan,
Sumatera Utara. Secara umum, belangkas dimanfaatkan telurnya sebagai bahan
pangan, sedangkan cangkangnya dibuang. Cangkang belangkas ini dapat
memberikan nilai ekonomis bila dimanfaatkan sebagai bahan untuk menghasilkan
Belangkas termasuk golongan hewan Arthropoda yaitu Crustaceae yang
pada cangkangnya mengandung senyawa kitin. Ternyata penghilangan gugus
asetil kitin meningkatkan kelarutannya, sehingga kitosan lebih banyak digunakan
daripada kitin, antara lain di industri kertas, pangan, farmasi, fotografi, kosmetika,
fungisida, dan tekstil. Kitosan juga telah terbukti efektif untuk mengurangi
padatan tersuspensi dalam limbah pengolahan dari sayuran, unggas dan telur, serta
pada lumpur aktif (Muzzarelli, 1977). Selain itu, kitosan juga bersifat nontoksik,
biokompatibel, dan biodegradabel sehingga aman digunakan.
Perkembangan teknologi dan sains pada saat ini khususnya di bidang
material sangat berkembang pesat. Nanosains dan nanoteknologi merupakan
kajian ilmu dan rekayasa material dalam skala nanometer yang sedang
dikembangkan oleh para ilmuwan di dunia. Nanomaterial dibuat untuk membawa
inovasi yang signifikan dan kemajuan bagi masyarakat serta manfaat untuk
kesehatan manusia dan lingkungan.
Sejumlah sifat nanomaterial ini dapat diubah melalui pengontrolan ukuran
material, pengaturan komposisi kimiawi, modifikasi permukaan, dan pengontrolan
interaksi antar partikel. Perilaku material yang berukuran nanometer sangat
berbeda dibanding dengan perilaku pada material ukuran yg lebih besar (bulk).
Perbedaan yg sangat signifikan terjadi pada sifat fisika, kimia, dan sifat
biologisnya. Material berukuran nanometer memiliki sejumlah sifat kimia dan
fisika yang lebih unggul dari material berukuran besar (bulk) karena semakin kecil
ukuran suatu material, maka luas permukaannya akan semakin besar sehingga
material dalam orde nanometer mempunyai jarak antar atom yang sangat kecil
yang akan memudahkan terjadinya reaksi antar atom.
Ukuran pori dari partikel kitosan dapat diperkecil untuk meningkatkan luas
kontak partikel dengan suatu materi. Salah satu usaha untuk memperkecil ukuran
pori kitosan adalah dengan memodifikasinya menjadi nanopartikel kitosan.
Sekarang ini banyak ahli menggunakan kitosan dengan nanoteknologi,
kitosan dilarutkan dalam larutan asam lemah kemudian ditambahkan larutan yang
bersifat basa seperti larutan amoniak, natrium hidroksida atau kalium hidroksida,
distirer dengan kecepatan 300 rpm sehingga diperoleh gel kitosan putih dan
dibilas dengan akuades sampai netral. Kemudian, ditempatkan dalam ultrasonic
batch untuk memecah partikel-partikel gel kitosan menjadi lebih kecil. Sebagian
ahli juga mencoba metode lain untuk menyiapkan nanopartikel kitosan dengan
menambahkan larutan tripolifosfat ke dalam larutan kitosan sehingga diperoleh
emulsi kitosan sambil distirer dengan kecepatan 1200 rpm kemudian emulsi
dibuat pH 3,5 dengan menambahkan asam asetat hasilnya akan berupa suspensi
kitosan.
Pembuatan nanopartikel menggunakan kitosan dapat dilakukan dengan
metode gelasi ionik. Metode ini cukup sederhana. Salah satu contoh metode gelasi
ionik ini yaitu dengan mereaksikan kitosan dengan natrium tripolifosfat. Metode
ini menghasilkan interaksi antara muatan positif pada gugus amino kitosan dengan
muatan negatif pada tripolifosfat (Mohanraj dan Chen, 2006). Noviary (2012)
telah berhasil mensintesis kitosan dari cangkang belangkas dan memodifikasi
nanopartikelnya melalui ikat silang dengan genepin, sedangkan Kurniawan (2012)
membuat nanopartikel kitosan dengan metode gelasi ionik dan dihasilkan
nanopartikel kitosan dengan ukuran 62,2 nm.
Berdasarkan hal di atas, peneliti tertarik untuk membuat nanopartikel
kitosan cangkang belangkas.
1.2. Permasalahan
Bagaimana pengaruh dari polianion tripolifosfat dalam pembuatan
1.3. Pembatasan Masalah
1. Sampel yang digunakan adalah kitosan cangkang belangkas.
2. Pelarut yang digunakan adalah larutan asam asetat 2%.
3. Polianion yang digunakan berasal dari natrium tripolifosfat.
4. Karakteristik yang dilakukan menggunakan PSA dan spektrofotometer
FTIR.
1.4. Tujuan Penelitian
Untuk mengetahui apakah kitosan cangkang belangkas dapat dimodifikasi
menjadi nanopartikel kitosan.
1.5. Manfaat Penelitian
Hasil yang diperoleh dari penelitian ini diharapkan dapat menjadi salah
satu informasi ilmiah bahwa modifikasi pada kitosan cangkang belangkas dapat
memperkecil pori hingga berukuran nano.
1.6. Lokasi Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Analitik, Fakultas
Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara.
Pengeringan suspensi nanopartikel kitosan menggunakan freeze dryer dan
pengukuran ukuran partikel menggunakan Particle Size Analyzer di Laboratorium
Kimia Fisika, Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas
Sumatera Utara. Analisis gugus fungsi menggunakan spektrofotometer Fourier
Transform Infra Red (FTIR) di Laboratorium Kimia Organik, Fakultas
1.7. Metodologi Penelitian
1. Penelitian ini dilakukan secara eksperimen laboratorium.
2. Pembuatan nanopartikel kitosan dengan melarutkan kitosan cangkang
belangkas dengan asam asetat 2%, kemudian ditambahkan natrium
tripolifosfat. Suspensi nanopartikel kitosan yang terbentuk
disentrifugasi dan didekantasi supernatan yang terbentuk, kemudian
dikeringkan menggunakan freeze dryer. Produk dianalisis dengan PSA
BAB 2
TINJAUAN PUSTAKA
2.1. Kitin
Kitin adalah kopolimer dari unit N-asetil-D-glukosamin dan D-glukosamin yang bertautan dengan ikatan β-(1-4) glikosida, di mana unit N-asetil-D-glukosamin adalah yang mendominasi dalam rantai polimerik. Bentuk deasetilasi dari kitin
adalah kitosan. Kitin dan kitosan dapat ditemukan sebagai material penyusun
dalam banyak organisme akuatik, organisme yang hidup di daratan, dan beberapa
mikroorganisme (Tokura dan Tamura, 2007).
Kitin dan kitosan adalah polisakarida yang menarik karena kehadiran
gugus fungsi amino yang cocok untuk memodifikasi struktur yang diinginkan.
Selain dari gugus amino, mereka memiliki 2 gugus hidroksil untuk membantu
modifikasi kimia. Sama seperti selulosa, kitin dan kitosan dapat mengalami
banyak reaksi seperti eterifikasi, esterifikasi, dan ikat silang.
Struktur kitin menyerupai struktur selulosa dan berbeda pada gugus yang
terikat di posisi atom C-2. Gugus pada C-2 selulosa adalah gugus hidroksil,
sedangkan pada C-2 kitin adalah gugus N-asetil (-NHCOCH3, asetamida) seperti yang dapat dilihat pada gambar di bawah ini (Gambar 2.1.) :
O
Kitin merupakan bahan yang tidak beracun dan bahkan mudah terurai
secara hayati (biodegradabel). Bentuk fisiknya merupakan padatan amorf yang
berwarna putih dengan kalor spesifik 0,373±0,03 kal/g ̊ C (Knorr, 1984) dan derajat rotasi spesifik [α]D18+ 22 ̊ pada konsentrasi asam metanasulfonat 1,0%. Sebagai biopolimer kristalin, kitin terdapat dalam 3 bentuk kristal di alam, yaitu α, β, dan γ (Sugita, 2009).
Kitin hampir tidak larut dalam air, asam encer, dan basa, tetapi larut dalam
asam format, asam metanasulfonat, N,N-dimetilasetamida yang mengandung 5%
litium klorida, heksafluoroisopropil alkohol, heksafluoroaseton, dan campuran
1,2-dikloroetana-asam trikloroasetat dengan nisbah 35:65(%[v/v]) (Hirano,
1986). Asam mineral pekat seperti H2SO4, HNO3, dan H3PO4 dapat melarutkan kitin sekaligus menyebabkan rantai panjang kitin terdegradasi menjadi
satuan-satuan yang lebih kecil (Bastaman, 1989). Sifat fisika dan kimia kitin di atas telah
dijadikan bagian dalam spesifikasi kitin (Tabel 2.1.).
Tabel 2.1. Spesifikasi kitin
Parameter Ciri – ciri
Ukuran partikel Serpihan dalam bentuk serbuk
Kadar air (%) ≤ 10,0
Kadar abu (%) ≤ 2,0
N-deasetilasi (%) ≥ 15,0
Kelarutan dalam :
- Air Tidak larut
- Asam encer Tidak larut
- Pelarut organik Tidak larut
- LiCl2/ dimetilasetamida Sebagian larut
Enzim pemecah Lisozim dan kitinase
2.2. Kitosan
Kitosan adalah poli-(2-amino-2-deoksi-β-(1 4)-D-glukopiranosa) dengan rumus molekul (C6H11NO4)n yang dapat diperoleh dari deasetilasi kitin. Kitosan juga dijumpai secara alamiah di beberapa organisme. Struktur polimer kitosan
dapat dilihat pada gambar (Gambar 2.2.) di bawah ini :
O
Gambar 2.2. Struktur polimer kitosan (Sugita, 2009)
Proses deasetilasi kitosan dapat dilakukan dengan cara kimiawi maupun
enzimatik. Proses kimiawi menggunakan basa, misalnya NaOH, dan dapat
menghasilkan kitosan dengan derajat deasetilasi yang tinggi, yaitu mencapai
85-93 % (Tsigos et al., 2000). Namun proses kimiawi menghasilkan kitosan dengan
bobot molekul yang beragam dan deasetilasinya juga sangat acak (Martinou et al.,
1995; Tsigos et al., 2000), sehingga sifat fisik dan kimia kitosan tidak seragam.
Selain itu, proses kimiawi juga dapat menimbulkan pencemaran lingkungan, sulit
dikendalikan, dan melibatkan banyak reaksi samping yang dapat menurunkan
rendemen (Chang et al., 1997; Tokuyasu et al., 1997).
Proses enzimatik dapat menutupi kekurangan proses kimiawi. Pada
dasarnya deasetilasi secara enzimatik bersifat selektif dan tidak merusak struktur
rantai kitosan, sehingga menghasilkan kitosan dengan karakteristik yang lebih
Kitosan merupakan padatan amorf yang berwarna putih kekuningan
dengan rotasi spesifik [∝]D11 -3 hingga -10 ̊ (pada konsentrasi asam asetat 2%). Kitosan larut pada kebanyakan larutan asam organik (Tabel 2.2.) pada pH sekitar
4,0, tetapi tidak larut pada pH lebih besar dari 6,5, juga tidak larut dalam pelarut
air, alkohol, dan aseton. Dalam asam mineral pekat seperti HCl dan HNO3, kitosan larut pada konsentrasi 0,15-1,1 %, tetapi tidak larut pada konsentrasi 10%.
Tabel 2.2. Kelarutan kitosan pada berbagai pelarut asam organik
Konsentrasi asam organik Konsentrasi asam organik (%)
10 50 >50
Kitosan tidak larut dalam H2SO4 pada berbagai konsentrasi, sedangkan di dalam H3PO4 tidak larut pada konsentrasi 1% sementara pada konsentrasi 0,1% sedikit larut. Perlu untuk kita ketahui, bahwa kelarutan kitosan dipengaruhi oleh
bobot molekul, derajat deasetilasi, dan rotasi spesifiknya yang beragam
bergantung pada sumber dan metode isolasi serta transformasinya. Sifat fisika dan
kimia kitosan di atas telah dijadikan bagian dalam penentuan spesifikasi kitosan,
Tabel 2.3. Spesifikasi kitosan
Parameter Ciri – ciri
Ukuran partikel Serpihan sampai bubuk
Kadar air (%) ≤ 10,0
Kadar abu (%) ≤ 2,0
Warna larutan Tidak berwarna
N-deasetilasi (%) ≥ 70,0
Kelas viskositas (cps) :
- Rendah < 200
- Medium 200799
- Tinggi pelarut organik 8002000
(Sugita, 2009)
Kitosan dalam bentuk terprotonasi menunjukkan kerapatan muatan yang
tinggi dan bersifat sebagai polielektrolit kationik, seperti yang dapat dilihat pada
Gambar 2.3 dan sangat efektif berinteraksi dengan biomolekul bermuatan negatif
dan biomolekul permukaan. Sedangkan dalam bentuk netralnya, kitosan mampu
mengompleks ion logam berat berbahaya seperti Cu, Cr, Cd, Mn, Co, Ph, Hg, Zn,
dan Pd.
2.3. Kegunaan Kitin dan Kitosan
Dewasa ini aplikasi kitin dan kitosan sangat banyak dan meluas. Di bidang
industri, kitin dan kitosan berperan antara lain sebagai koagulan polielektrolit
pengolahan limbah cair, pengikat dan penjerap ion logam, mikroorganisme,
mikroalga, pewarna, residu pestisida, lemak, tanin, PCB (poliklorinasi bifenil),
mineral dan asam organik, media kromatografi afinitas, gel dan pertukaran ion,
penyalut berbagai serat alami dan sintetik, pembentuk film dan membran mudah
terurai, meningkatkan kualitas kertas, pulp, dan produk tekstil. Sementara di
bidang pertanian dan pangan, kitin dan kitosan digunakan antara lain untuk
pencampur ransum pakan ternak, anti mikrob, anti jamur, serat bahan pangan,
penstabil, pembentuk gel, pembentuk tekstur, pengental dan pengemulsi produk
olahan pangan, pembawa zat aditif makanan, flavor, zat gizi, pestisida, herbisida,
virusida tanaman, dan deasidifikasi buah-buahan, sayuran, dan penjernih sari
buah. Fungsinya sebagai antimikrob dan antijamur juga diterapkan di bidang
kedokteran.
Kitin dan kitosan dapat mencegah pertumbuhan Candida albicans dan
Staphvlacoccus aureus. Selain itu, biopolimer tersebut juga berguna sebagai antikoagulan, antitumor, antivirus, pembuluh darah-kulit dan ginjal sintetik, bahan
pembuat lensa kontak, aditif kosmetik, membran dialisis, bahan sampo dan
kondisioner rambut, zat hemostatik, penstabil liposom, bahan ortopedik, pembalut
luka dan benang bedah yang mudah diserap, serta mempertinggi daya kekebalan,
2.4. Aplikasi Kitosan dalam Bidang Lingkungan
Lingkungan sangat berpotensi tercemar zat organik, anorganik, maupun
logam berat. Keberadaan zat-zat pencemar tersebut akan mengganggu ekosistem
yang ada, termasuk juga manusia. Oleh sebab itu, kelestarian lingkungan dari zat
pencemar harus dijaga dan terus mendapatkan perhatian dari masyarakat sekitar,
yang merupakan elemen dari lingkungan hidup itu sendiri. Salah satu cara yang
dapat digunakan untuk mengurangi zat pencemar pada lingkungan adalah dengan
menggunakan kitosan sebagai adsorben.
Kitosan lazimnya disintesis dari deasetilasi kitin yang berasal dari limbah
kulit udang atau kepiting. Oleh karena itu, penggunaan kitosan sejak awal telah
berperan dalam mengurangi pencemaran lingkungan. Manfaat kitosan dalam
bidang lingkungan adalah untuk menjerap logam berat maupun zat warna yang
banyak dihasilkan dari industri tekstil atau kertas. Logam berat merupakan limbah
yang sangat berbahaya. Hal tersebut dikarenakan logam berat dapat menimbulkan
toksisitas akut pada manusia maupun habitat yang ada di lingkungan perairan.
Logam berat didefinisikan sebagai logam yang memiliki densitas atau
kerapatan tinggi dan merupakan pencemar yang banyak dijumpai baik di
lingkungan darat maupun di perairan. Keberadaan logam berat akan membawa
pengaruh pada kehidupan organisme di lingkungan (termasuk manusia), karena
sifatnya yang meracun dan dapat menyebabkan kematian apabila jumlahnya
melewati ambang batas yang ditetapkan. Kandungan logam berat di lingkungan
dapat dikurangi dengan cara menjerapnya, salah satunya dengan menggunakan
2.5. Modifikasi Kitosan
Kitosan dapat dimodifikasi, kitosan sebagai adsorben dapat berada dalam
berbagai bentuk, antara lain bentuk butir, serpih, hidrogel, dan membran (film).
Kitosan sebagai adsorben sering dimanfaatkan untuk proses adsorpsi ion logam
berat. Besranya afinitas kitosan dalam mengikat ion logam sangat bergantung
pada karakteristik makrostruktur kitosan yang dipengaruhi oleh sumber dan
kondisi pada proses isolasi.
Perbedaan bentuk kitosan akan berpengaruh pada luas permukaannya.
Semakin kecil ukuran kitosan, maka luas permukaan kitosan akan semakin besar,
dan proses adsorpsi pun dapat berlangsung lebih baik. Modifikasi kimia kitosan
menjadi gel kitosan dapat meningkatkan kapasitas jerapnya. Keunggulan ini
disebabkan oleh bentuk butiran gel mempunyai volume pori yang lebih besar
dibandingkan dengan bentuk serpihan, tetapi daya absorpsi butiran gel kitosan
dipengaruhi oleh kestabilan sifat gel yang dibentuk (Rao, 1993).
2.6. Natrium Tripolifosfat
Tripolifosfat atau biasa disebut juga natrium tripolifosfat merupakan suatu
serbuk berwarna putih dan sedikit higroskopis. Tripolifosfat bersifat mudah larut
dalam air dan tidak larut dalam etanol. Disosiasi natrium tripolifosfat dalam air
dapat dilihat pada gambar (Gambar 2.4.) di bawah ini :
��5�3�10 + 5�2� →5��++�5�3�10+ 5��− �5�3�10 +��−→ �4�3�10−+�2� �4�3�10−+��−→ �3�3�102−+�2�
Tripolifosfat ada dalam bentuk garam natrium yang terdapat dalam bentuk
anhidrat maupun heksahidratnya (FAO, 2006). Salah satu contoh senyawa
polifosfat adalah natrium tripolifosfat dengan rumus molekul Na5P3O10 dan memiliki bobot molekul 368 g/mol. Natrium tripolifosfat dibuat dengan memanaskan campuran dinatrium fosfat (Na2HPO4) dan natrium fosfat (NaH2PO4) sesuai dengan persamaan reaksi berikut :
2��2���4+���2��4 → ��5�3�10+ 2�2� (2.1)
Alasan digunakan tripolifosfat karena sifatnya sebagai anion multivalen
yang dapat membentuk ikatan ikat silang dengan kitosan yang bersifat kationik
(Yu-Shin et.al., 2008). Natrium tripolifosfat merupakan senyawa anorganik
berbentuk padatan yang digunakan dalam berbagai bidang aplikasi, misalnya
bahan pengawet makanan dan daging serta industri keramik. Dalam bidang kimia,
natrium tripolifosfat digunakan untuk surfaktan, larutan bufer, bahan pengemulsi
(emulsifier), dan hidrolisis lemak. Selain itu, natrium tripolifosfat juga sering
digunakan untuk pengikat silang pada pembuatan membran kitosan. Membran
yang terikat silang natrium tripolifosfat lebih fleksibel dan stabilitas kimianya
menjadi lebih baik (Sugita, 2009). Struktur natrium tripolifosfat dapat dilihat pada
gambar (Gambar 2.5.) di bawah ini :
2.7. Nanopartikel Kitosan
Secara umum nanopartikel didefinisikan sebagai partikel dengan ukuran
10 – 1000 nm (Mohanraj dan Chen, 2006). Pembuatan nanopartikel yang
menggunakan polimer dapat diklasifikasikan menjadi dua tipe; pertama
nanopartikel dibentuk bersamaan dengan polimernya menggunakan reaksi
polimerisasi, kedua polimer dibuat terpisah umtuk selanjutnya digunakan untuk
membuat nanopartikel (Swarbick, 2007).
Ada empat metode pembuatan nanopartikel yang menggunakan kitosan
sebagai polimer yaitu mikroemulsi, emulsifikasi difusi pelarut, kompleks
polielektrolit, dan gelasi ionik.
2.7.1. Metode Mikroemulsi
Pada pembuatan nanopartikel menggunakan metode ini kitosan dilarutkan
dalam larutan asam. Kemudian surfaktan dilarutkan dalam n-heksan. Larutan
kitosan dan glutaraldehid kemudian ditambahkan ke dalam larutan surfaktan
dalam n-heksan dengan pengadukan menggunakan pengaduk magnetik pada
temperatur kamar. Nanopartikel akan terbentuk dengan adanya surfaktan.
Pengadukan dibiarkan selama semalam untuk memaksimalkan proses
cross-linking, di mana gugus amin dari kitosan akan berikatan dengan
glutaraldehid. Pelarut organik kemudian diuapkan dengan penguapan tekanan
rendah. Surfaktan yang masih terkandung dalam nanopartikel dihilangkan melalui
proses presipitasi dengan menggunakan CaCl2 kemudian presipitan dihilangkan dengan sentrifugasi. Kemudian suspensi nanopartikel didialisis sebelum dilakukan
Nanopartikel yang dihasilkan dengan menggunakan metode ini memiliki
ukuran kurang dari 100 nm dan ukuran partikel tersebut dapat diatur dengan
melakukan variasi glutaraldehid yang dapat mengubah derajat cross-linking.
Namun, metode ini memiliki kerugian yaitu penggunaan pelarut organik, lamanya
waktu proses pembuatan, dan tahapan pencucian yang kompleks (Kurniawan,
2012).
2.7.2. Metode emulsifikasi difusi pelarut
Pada metode ini, dibuat emulsi minyak dalam air dengan cara
mencampurkan fase organik sedikit demi sedikit ke dalam larutan kitosan yang
mengandung penstabil seperti poloxamer dengan pengadukan menggunakan
pengaduk magnetik, dilanjutkan dengan homogenisasi tekanan tinggi. Emulsi
kemudian dilarutkan ke dalam sejumlah besar fase air. Presipitasi polimer terjadi
akibat difusi dari pelarut organik ke dalam fase air, yang mana akan membentuk
nanopartikel. Metode ini sesuai untuk zat aktif yang hidrofobik. Kelemahan
metode ini adalah penggunaan pelarut organik dan tekanan tinggi selama
pembuatan nanopartikel (Kurniawan, 2012).
2.7.3. Metode Kompleks Polielektrolit
Mekanisme polielektrolit kompleks melibatkan reaksi netralisasi muatan
antara polimer kationik dan polimer anionik yang akan membentuk kompenen
polielektrolit. Beberapa polimer kationik seperti gelatin dan polietilamin juga
dapat digunakan pada proses ini. Metode ini menawarkan cara pembuatan yang
sederhana. Nanopartikel akan terbentuk secara spontan setelah penambahan
larutan polimer anionik ke dalam larutan kitosan dalam asam asetat dengan
pengadukan menggunakan pengaduk magnetik pada temperatur kamar
2.7.4. Metode Gelasi Ionik
Metode ini melibatkan proses ikat silang antara polielektrolit dengan
adanya pasangan ion multivalennya. Pembentukan ikatan ini akan memperkuat
kekuatan mekanis dari partikel yang terbentuk. Contoh pasangan polimer yang
dapat digunakan untuk metode gelasi ionik ini adalah kitosan dengan tripolifosfat
dan kitosan dengan karboksimetilselulosa (Swabrick, 2007).
Mekanisme pembentukan nanopartikel berdasarkan interaksi elektrostatik
antara gugus amin dari kitosan dan gugus negatif dari polianion seperti
tripolifosfat. Prosesnya diawali dengan melarutkan kitosan dalam asam asetat,
kemudian tripolifosfat ditambahkan ke dalam larutan kitosan dengan pengadukan
menggunakan magnetik stirer (Kurniawan, 2012).
2.8. Reaksi Ikat Silang
Ikatan silang merupakan ikatan yang menghubungkan rantai polimer yang
satu dengan rantai polimer yang lain di mana ikatan tersebut berupa ikatan
kovalen atau ionik. Reaksi ikat silang memberikan pengaruh yang besar baik
dalam sifat kimia maupun sifat mekanik dari polimer (Nicholson, 2006).
Pembentukan ikat silang dilakukan dengan penambahan suatu agen pengikat
silang ke dalam larutan bahan yang akan dimodifikasi (Berger et.al., 2004).
Ikatan silang dapat terjadi dengan dua cara, yaitu dengan membentuk
ikatan kovalen dan dengan membentuk ikatan ionik. Dalam reaksi pembentukan
ikatan silang kovalen, agen pengikat silang yang umum digunakan adalah
dialdehid, contohnya glioksal (Qing et.al., 2004) dan glutaraldehid (Monteiro dan
Akan tetapi, kedua agen pengikat silang tersebut bersifat toksik.
Glutaraldehid bersifat neurotoksik, sedangkan glioksal bersifat mutagenik.
Meskipun hasil modifikasi tersebut dimurnikan sebelum pemberian, keberadaan
dialdehid bebas yang tidak ikut bereaksi tidak seluruhnya dapat dihilangkan dan
dapat memberikan efek toksik.
Agen pengikat silang kovalen lainnya yang dapat digunakan untuk
membentuk reaksi ikat silang dengan kitosan telah banyak diteliti sebagai
alternatif pilihan. Di samping dialdehid, asam oksalat dan genipin terbukti dapat
digunakan sebagai agen pengikat silang. Akan tetapi, sampai saat ini belum ada
data yang lengkap mengenai biokompatibilitas dari senyawa-senyawa tersebut.
Kebanyakan agen pengikat silang yang membentuk ikatan kovalen dapat
menginduksi toksisitas jika sebelum pemberian masih terdapat sisa dari pereaksi.
Untuk mengatasi masalah toksisitas yang terjadi tersebut, dapat dilakukan reaksi
ikat silang ionik. Kitosan bersifat polikationik dalam lingkungan asam. Sifat ini
menyebabkan terjadinya interaksi dengan komponen bermuatan negatif (anionik),
baik berupa ion-ion maupun molekul, yang membentuk hubungan ionik antara
rantai polimer. Interaksi ionik terjadi antara muatan negatif dari agen pengikat
silang dengan muatan positif dari rantai polimer kitosan.
Di antara molekul-molekul anionik, gugus pelepas fosfat, seperti β -gliserofosfat dan sebagian tripolifosfat, umum digunakan sebagai agen pengikat
silang ionik (Berger et al., 2004). Selain itu, sebagai alternatif dapat juga
digunakan natrium sitrat atau natrium sulfat sebagai agen pengikat silang (Shu dan
2.9. Kitosan Tripolifosfat
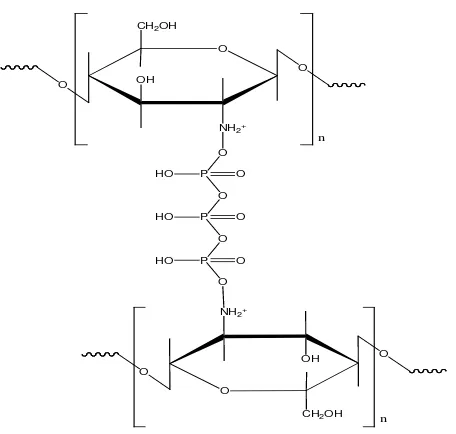
Gambar 2.6. Ikat silang ionik kitosan dengan natrium tripolifosfat (Bhumkar,
2006)
Kitosan mikropartikel dan nanopartikel telah dibuat dengan cara ikat
silang menggunakan glutaraldehid, glioksal, dan etilen glikol diglicidil eter.
Walaupun senyawa berikut merupakan agen pengikat silang yang baik namun
jarang digunakan karena toksisitasnya.
Ikatan silang antara kitosan dengan natrium tripolifosfat bergantung pada
ketersediaan gugus kationik dan gugus anionik. Pada proses terjadinya ikatan
silang tersebut ada 3 faktor yang berperan penting yaitu konsentrasi kitosan, pH,
dan konsentrasi natrium tripolifosfat. Pada larutan natrium tripolifosfat dengan pH
asam (pH 3) hanya akan dihasilkan ion tripolifosfat yang akan berinteraksi dengan
gugus –NH3+ dari kitosan. Sedangkan pada pH basa (pH 9) dihasilkan ion OH -dan tripolifosfat -dan keduanya dapat berkompetisi untuk dapat berinteraksi
2.10. Karakteristik Nanopartikel
2.10.1. Particle Size Analyzer (PSA)
Ada beberapa cara yang dapat digunakan untuk mengetahui ukuran suatu
partikel yaitu :
1. Metode ayakan (sieve analyses)
2. Laser diffraction (LAS)
3. Metode sedimentasi
4. Electronical zone sensing (EZS)
5. Analisis gambar (mikrografi)
6. Metode kromatografi
7. Ukuran aerosol submikron dan perhitungan
Sieve analyses (analisis ayakan) dalam dunia farmasi sering kali
digunakan dalam bidang mikromeritik, yaitu ilmu yang mempelajari tentang ilmu
dan teknologi partikel kecil. Metode yang paling umum digunakan adalah analisis
gambar (mikrografi). Metode ini meliputi metode mikroskopi dan metode
holografi. Alat yang sering digunakan biasanya SEM, TEM, dan AFM. Namun
seiring dengan berkembangnya ilmu pengetahuan yang lebih mengarah ke era
nanoteknologi, para peneliti mulai menggunakan laser diffraction (LAS). Metode
ini dinilai lebih akurat bila dibandingkan dengan metode analisis gambar maupun
metode ayakan, terutama untuk sampel-sampel dalam orde nano maupun
Contoh alat yang menggunakan metode LAS adalah particle size analyzer
(PSA). Metode LAS dibagi dalam dua metode :
1. Metode basah, metode ini menggunakan media pendispersi untuk
mendispersikan material uji.
2. Metode kering, metode ini memanfaatkan udara atau aliran udara untuk
melarutkan partikel dan membawanya ke sensing zone. Metode ini baik
digunakan untuk ukuran yang kasar, di mana hubungan antar partikel
lemah dan kemungkinan untuk beraglomerasi kecil.
Keunggulan penggunaan particle size analyzer (PSA) untuk mengetahui
ukuran partikel :
1. Lebih akurat. Pengukuran partikel dengan menggunakan PSA lebih akurat
jika dibandingkan dengan pengukuran partikel dengan alat lain seperti
XRD ataupun SEM. Hal ini dikarenakan partikel didispersikan ke dalam
media sehingga ukuran partikel yang terukur adalah ukuran dari single
particle.
2. Hasil pengukuran dalam bentuk distribusi, sehingga dapat
menggambarkan keseluruhan kondisi sampel.
3. Rentang pengukurandari0,6nanometer hingga7mikrometer.(Rusli, 2011)
Pengukuran partikel dengan menggunakan PSA biasanya menggunakan
metode basah. Metode ini dinilai lebih akurat jika dibandingkan dengan metode
kering ataupun pengukuran partikel dengan metode ayakan dan analisis gambar.
Terutama untuk sampel-sampel dalam orde nanometer dan submikron yang
biasanya memiliki kecenderungan aglomerasi yang tinggi. Hal ini dikarenakan
partikel didispersikan ke dalam media sehingga partikel tidak saling
Dengan demikian ukuran partikel yang terukur adalah ukuran dari single
particle. Selain itu hasil pengukuran dalam bentuk distribusi, sehingga hasil
pengukuran dapat diasumsikan sudah menggambarkan keseluruhan kondisi
sampel. Beberapa analisis yang dilakukan, antara lain :
1. Menganalisis ukuran partikel.
2. Menganalisis nilai zeta potensial dari suatu larutan sampel.
3. Mengukur tegangan permukaan dari partikel clay bagi industri keramik
dan sejenisnya.
4. Mengetahui zeta potensial koagulan untuk proses koagulasi partikel
pengotor bagi industri water treatment plant (Nanortim, 2010).
2.10.2. FTIR (Fourier Transform Infra Red)
Jumlah energi yang diperlukan untuk meregangkan suatu ikatan
tergantung pada tegangan ikatan dan massa atom yang terikat. Bilangan
gelombang suatu serapan dapat dihitung menggunakan persamaan yang
diturunkan dari hukum Hooke :
�= 1
Persamaan di atas menghubungkan bilangan gelombang dari vibrasi
regangan (�) terhadap konstanta gaya ikatan (�) dan massa atom (dalam gram)
yang digabungkan oleh ikatan (m1 dan m2). Konstanta gaya merupakan ukuran tegangan dari suatu ikatan. Persamaan tersebut menunjukkan bahwa ikatan yang
lebih kuat dan atom yang lebih ringan menghasilkan frekuensi yang lebih tinggi.
Semakin kuat suatu ikatan, makin besar energi yang dibutuhkan untuk
meregangkan ikatan tersebut. Frekuensi vibrasi berbanding terbalik dengan massa
atom sehingga vibrasi atom yang lebih berat terjadi pada frekuensi yang lebih
Pancaran infra merah pada umumnya mengacu pada bagian spektrum
elektromagnetik yang terletak di antara daerah tampak dan daerah gelombang
mikro. Sebagian besar kegunaannya terbatas di daerah antara 4000 cm-1 dan 666 cm-1 (2,5-15,0 µm). Akhir-akhir ini muncul perhatian pada daerah infra merah dekat, 14290-4000 cm-1 (0,7-2,5 µm) dan daerah infra merah jauh, 700-200 cm-1 (14,3-50 µm) (Silverstain, 1967).
Salah satu hasil kemajuan instrumentasi IR adalah pemrosesan data
seperti Fourier Transform Infra Red (FTIR). Teknik ini memberikan informasi
dalam hal kimia, seperti struktur dan konformasional pada polimer dan
polipaduan, perubahan induksi tekanan dan reaksi kimia. Dalam teknik ini
padatan diuji dengan cara merefleksikan sinar infra merah yang melalui tempat
kristal sehingga terjadi kontak dengan permukaan cuplikan. Degradasi atau
induksi oleh oksidasi, panas, maupun cahaya, dapat diikuti dengan cepat melalui
infra merah. Sensitivitas FTIR adalah 80-200 kali lebih tinggi dari instrumentasi
dispersi standar karena resolusinya lebih tinggi (Kroschwitz, 1990).
Teknik pengoperasian FTIR berbeda dengan spektrofotometer infra
merah. Pada FTIR digunakan suatu interferometer Michelson sebagai pengganti
monokromator yang terletak di depan monokromator. Interferometer ini akan
memberikan sinyal ke detektor sesuai dengan intensitas frekuensi vibrasi molekul
yang berupa interferogram (Bassler, 1986).
Interferogram juga memberikan informasi yang berdasarkan pada
intensitas spektrum dari setiap frekuensi. Informasi yang keluar dari detektor
diubah secara digital dalam komputer dan ditransformasikan sebagai domain,
tiap-tiap satuan frekuensi dipilih dari interferogram yang lengkap (fourier transform).
Kemudian sinyal itu diubah menjadi spektrum IR sederhana. Spektrofotometer
FTIR digunakan untuk :
1. Mendeteksi sinyal lemah.
2. Menganalisis sampel dengan konsentrasi rendah.
BAB 3
METODE PENELITIAN
3.1. Alat
- Batang pengaduk
- Bola karet
- Gelas beaker Pyrex
- Labu ukur Pyrex
- Pipet ukur Pyrex
- Neraca analitik Mettler PM 400
- Magnet pengaduk
- Seperangkat alat stirer Fisher
- Seperangkat alat sentrifuge Hitachi CF 16RX II
- Seperangkat alat freeze dryer Alpha 1-2 LD plus
- Seperangkat alat particle size analyzer Horiba LA-950V2
- Seperangkat alat spektrofotometer FTIR Shimadzu
-3.2. Bahan
- Kitosan cangkang belangkas
- Asam asetat glasial p.a (E.Merck)
3.3. Prosedur Penelitian
3.3.1. Pembuatan Pereaksi
a. Larutan asam asetat 2%
Sebanyak 2 mL asam asetat glasial dimasukkan ke dalam labu
ukur 100 mL, kemudian diencerkan dengan akua steril sampai garis
tanda, dan dihomogenkan.
b. Larutan natrium tripolifosfat 0,75 mg/mL
Sebanyak 0,0375 g natrium tripolifosfat dilarutkan dengan akua steril,
kemudian diencerkan dengan akua steril dalam labu ukur 50 mL sampai
garis tanda, dan dihomogenkan.
3.3.2. Pembuatan Nanopartikel Kitosan (Sivakami, 2013)
Sebanyak 0,02 g kitosan cangkang belangkas dilarutkan dengan 40 mL
larutan asam asetat 2%, ditambahkan 20 mL larutan natrium tripolifosfat
0,75mg/mL secara perlahan-lahan dengan pengadukan hingga terbentuk suspensi nanopartikel kitosan, kemudian disentrifugasi dan direndam dalam akua steril dan
didekantasi supernatan yang terbentuk. Nanopartikel kitosan dikeringkan
3.4. Bagan Penelitian
3.4.1. Pembuatan Pereaksi
a. Larutan asam asetat 2%
2 mL asam asetat glasial
diencerkan dengan akua steril sampai garis tanda dihomogenkan
Hasil
dimasukkan ke dalam labu ukur 100 mL
b. Larutan natrium tripolifosfat 0,75 mg/mL
0,0375 g natrium tripolifosfat
Hasil
dilarutkan dengan akua steril
dimasukkan ke dalam labu ukur 50 mL
diencerkan dengan akua steril sampai garis tanda
3.4.2. Pembuatan Nanopartikel Kitosan
0,02 g kitosan cangkang belangkas
dilarutkan dengan 40 mL larutan asam asetat 2%
ditambahkan 20 mL larutan natrium tripolifosfat 0,75 mg/mL secara perlahan-lahan dengan pengadukan
suspensi nanopartikel kitosan
disentrifugasi
direndam dengan akua steril
didekantasi supernatan yang terbentuk
dikeringkan dengan menggunakan freeze dryer
dikarakterisasi menggunakan PSA dan FTIR
BAB 4
HASIL DAN PEMBAHASAN
4.1. Hasil
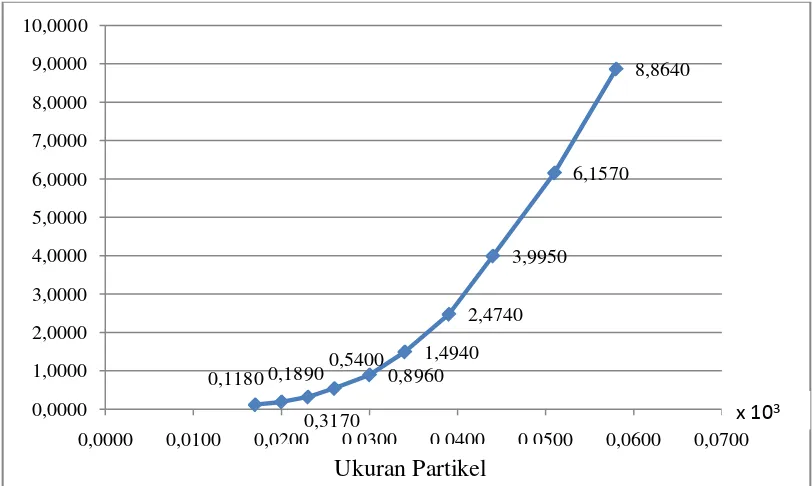
Grafik distribusi persen jumlah dan ukuran partikel dari nanopartikel
kitosan dapat dilihat di bawah ini.
Gambar 4.1. Grafik Distribusi Persen Jumlah dan Ukuran Partikel
Dari hasil karakterisasi menggunakan particle size analyzer terhadap
nanopartikel kitosan didapatkan diameter nanopartikel kitosan sebesar 58 nm.
Secara umum nanopartikel didefinisikan sebagai partikel dengan ukuran 10 –
1000 nm (Mohanraj dan Chen, 2006). Artinya, nanopartikel kitosan yang dibuat
telah berukuran nano.
0,0000 0,0100 0,0200 0,0300 0,0400 0,0500 0,0600 0,0700
x 103
4.2. Pembahasan
Pada penelitian ini; pembuatan nanopartikel kitosan dengan metode gelasi
ionik menggunakan kitosan cangkang belangkas dan natrium tripolifosfat, yang
melibatkan campuran dua fase larutan yaitu larutan polimer kitosan dan larutan
polianion natrium tripolifosfat. Metode ini berdasarkan interaksi elektrostatik
antara gugus positif amin dari kitosan dan gugus negatif dari polianion
tripolifosfat untuk membentuk partikel dengan ukuran nano.
Pada pembuatan nanopartikel kitosan ini, konsentrasi larutan asam asetat
yang digunakan adalah sebesar 2% dan konsentrasi larutan natrium tripolifosfat
yang digunakan adalah sebesar 0,75 mg/mL. Pelarut yang digunakan dalam pembuatan larutan-larutan tersebut adalah akua steril.
Perbandingan larutan asam asetat dan larutan natrium tripolifosfat yang
digunakan adalah 2 : 1 (2 bagian larutan asam asetat dengan 1 bagian larutan
natrium tripolifosfat) seperti yang tertera pada tabel (Tabel 4.1) di bawah ini :
Tabel 4.1. Perbandingan larutan asam asetat dan larutan natrium tripolifosfat
No. Massa Kitosan Volume Larutan Asam
Asetat 2%
Volume Larutan Natrium
Tripolifosfat 0,75 mg/mL
1. 0,02 g 40 mL 20 mL
Mula-mula 0,02 g kitosan cangkang belangkas dilarutkan dengan 40 mL larutan
asam asetat 2% sehingga menghasilkan larutan bening. Kitosan cangkang
Kemudian, 20 mL larutan natrium tripolifosfat ditambahkan ke dalam
larutan kitosan sehingga terjadi perubahan di mana larutan kitosan yang
sebelumnya bening menjadi larutan koloid yang dapat dilihat pada lampiran 1.
Campuran larutan tersebut distirer hingga terbentuk suspensi nanopartikel kitosan
yang dapat dilihat pada lampiran 2, kemudian disentrifugasi selama 30 menit
dengan kecepatan 11000 rpm menggunakan alat sentrifugasi, sehingga interaksi
antara gugus amin dari kitosan dengan ion tripolifosfat dari natrium tripolifosfat
membentuk nanopartikel dengan ukuran yang lebih kecil.
Hasil sentrifugasi direndam dalam akua steril untuk menetralkannya dan
supernatan yang terbentuk didekantasi dengan menggunakan pipet tetes.
Kemudian nanopartikel kitosan tersebut dikeringkan menggunakan freeze dryer
untuk memperoleh serbuk nanopartikel kitosan seperti pada lampiran 3. Serbuk
nanopartikel kitosan tersebut dikarakterisasi dengan alat PSA, untuk mengetahui
apakah serbuk nanopartikel kitosan tersebut telah berukuran nanometer, dan alat
FTIR, untuk mengetahui apakah telah terjadi interaksi antara gugus amin dari
kitosan dengan gugus tripolifosfat dari natrium tripolifosfat dengan
membandingkan spektrum FTIR dari kitosan cangkang belangkas (dapat dilihat
pada lampiran 6) dan nanopartikel kitosan.
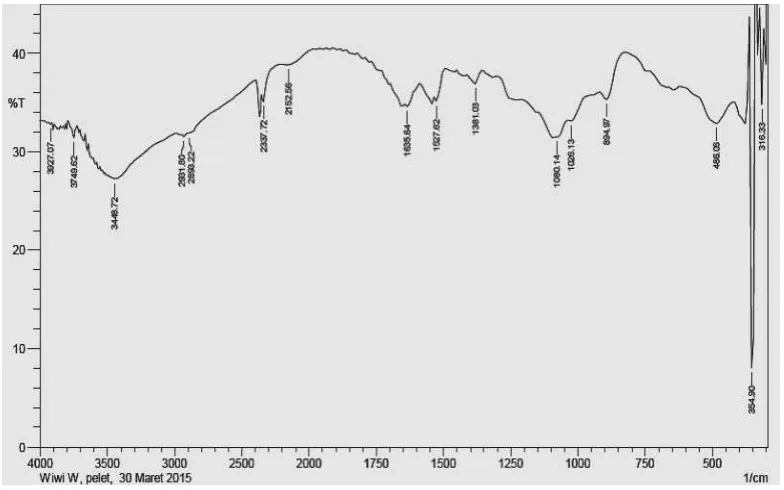
Hasil spektrum FTIR nanopartikel kitosan dapat dilihat pada gambar 4.2 di
atas. Pada spektrum nanopartikel kitosan muncul 2 puncak baru yaitu pada
bilangan gelombang 1635,64 dan 1527,62 cm-1. Hal ini disebabkan karena adanya interaksi antara NH3+ dari kitosan dengan ion tripolifosfat. Hal tersebut sesuai dengan penelitian yang dilakukan oleh Bhumkar dan Pokharkar (2006), yang
menyatakan bahwa pada spektrum nanopartikel kitosan muncul dua puncak baru
pada 1645 dan 1554 cm-1. Adanya puncak pada serapan bilangan gelombang 2931,80 cm-1 dan 2893,22 cm-1 menunjukkan adanya regangan C-H pada CH3 dan CH2. Adanya puncak pada serapan bilangan gelombang 1635,64 cm-1 menunjukkan adanya regangan C=O. Adanya puncak pada serapan bilangan
gelombang 1527,62 cm-1 menunjukkan adanya tekukan N-H.
Analisis kuantitatif dari spektrofotometri FTIR dapat dilakukan
berdasarkan spektra infra merah yang dihasilkan, di mana penentuan derajat
deasetilasi dari kitosan menggunakan persamaan Domzy dan Robers (Khan,
2002). Berikut adalah persamaan Domzy dan Robers :
%��= 1− ��1655
�3450�
1
1,33� � 100%
Di mana :
A1655 = absorbansi pada bilangan gelombang 1655 cm-1 A3450 = absorbansi pada bilangan gelombang 3450 cm-1
Berikut perhitungan derajat deasetilasi dari kitosan cangkang belangkas :
Berikut perhitungan derajat deasetilasi dari nanopartikel kitosan :
%��= 1− ��1655
Berdasarkan Proton Laboratories, Inc (Julianti, 2012) menyatakan bahwa kitosan
memiliki derajat deasetilasi ≥70% maka dapat dinyatakan telah diperoleh polimer kitosan. Dari pernyataan di atas dapat disimpulkan bahwa nanopartikel kitosan
BAB 5
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Dari hasil penelitian yang dilakukan, dapat diambil kesimpulan bahwa
kitosan cangkang belangkas dapat dimodifikasi menjadi nanopartikel kitosan
dengan metode gelasi ionik menggunakan natrium tripolifosfat. Hal ini dapat
dilihat dari ukuran diameter nanopartikel kitosan yang terbentuk adalah sebesar 58
nm serta pada spektra FTIR nanopartikel kitosan muncul 2 puncak baru yaitu pada
bilangan gelombang 1635,64 dan 1527,62 cm-1 yang menunjukkan adanya interaksi antara gugus amin dari kitosan dengan ion tripolifosfat dari natrium
tripolifosfat.
5.2. Saran
1. Disarankan bagi peneliti selanjutnya agar menggunakan kitosan yang
memiliki derajat deasetilasi yang tinggi dalam membuat nanopartikel
kitosan agar hasil yang didapat lebih maksimal.
2. Disarankan bagi peneliti selanjutnya agar membuat variasi perbandingan
campuran antara larutan kitosan dengan larutan natrium tripolifosfat untuk
mengetahui perbandingan mana yang bisa mendapatkan hasil yang lebih
DAFTAR PUSTAKA
Bassler. 1986. Penyidikan Spektrometrik Senyawa Organik. Jakarta : Erlangga.
Bastaman, S. 1989. Studies on Degradation and Extraction of Citin and Chitosan from Prawn Shell (Nephrops norvegicus) [tesis]. Belfast : Faculty of Engineering, The Queen’s University of Belfast.
Berger, J., M. Reist, J. M. Mayer, O. Felt, N. A. Peppas, and Gurny, R. 2004. Structure and Interactions in Covalently and Ionically Crosslinked Chitosan Hydrogels for Biomedical Applications. European Journal of Pharmaceutics and Biopharmaceutics, 57, 19-34.
Bhumkar, D. R., dan Pokharkar, V. B. 2006. Studies on Effect of pH on Crosslinking of Chitosan with Sodium Tripolyphosphte : A Technical Note. AAPS Pharmasitech, 7 (2), 1-6.
Bruice, P. Y. 2001. Organic Chemistry. New Jersey : Prentice-Hall.
Chang, K. L., Tsai, G., Lee, J., Fu, W. R. 1997. Heterogeneous N-deacetylation of Chitin in Alkaline Solution. Carbohydrate Research 303 : 327-332.
Codex Alimentarius Team. 2006. Food Chemical Codex. FAO. http:// www.fao.org/ag/agn/jecfaadditives/specs/Monograph1/Additive-307.pdf.
Crestini, C., Kovac, B., and G. Giovannozzi-Sermanni. 1996. Production and Isolation of Chitosan by Submerged and Solid State Fermentation from Lentinus edodes. Biotechnology and Bioengineering 50 : 207-210.
Hirano, S. 1986. Chitin and Chitosan. Weinheim. New York.
Julianti, S. 2012. Pembuatan Kitosan Oligomer Melalui Proses Degradasi Oksidatif dengan Penambahan H2O2 dan Ultrasonic Bath dan Pengaruhnya Terhadap Viskositas dan Berat Molekul. Medan : USU.
Knorr, D. 1984. Use Chitinious in Food. Food Tech. 38(1) : 85.
Kroschwitz, J. 1990. Polymer Characterization and Analysis. Canada : John Wiley & Sons.
Lee, S. T. , Mi, F. L., Shen, Y. J., dan Shyu, S. S. 2000. Equilibrium and Kinetic Studies of Copper (II) Ion Uptake by Chitosan Tripolyphosphate Chelating Resin. Polymer, 42, 1879-1892.
Li, Q. 1997. Application and Properties of Chitosan. Lancaster. Technomic Publishing, pp 3-29.
Lusi. 2011. Cara Mengetahui Ukuran Suatu Partikel. 20&catid=46&Itemid=67&lang=in.
Martinou, A., Kafetzopoulos, D., Bouriotis, V. 1995. Chitin Deacetylation by Enzymatic Means : Monitoring of Deacetylation Processes. Carbohydrate Research 273 : 235-242.
Mohanraj, V. J. and Y. Chen. 2006. Nanoparticles. Nigeria : Tropical J. Pharm Res: 561-573.
Monteiro, O. A. C., Airoldi, C. 1999. Some Studies of Crosslinking Chitosan-Glutaraldehyde Interaction in a Homogeneous System. International Journal of Biological Macromolecules, 26, 119-128.
Muzzarelli, R. A. A. 1977. Chitin. First Edition. Oxford : Pergamon Press.
Nanortim. 2010. Jasa Analisa dan Pengujian Sampel. 32&Itemid=58.
Nicholson, J. W. 2006. The Chemistry of Polymers 3rd Edition. UK : RSC Publishing, 56.
Noviary, H. 2011. Studi Karakterisasi Pembuatan Kitin dan Kitosan dari Cangkang Belangkas untuk Penentuan Berat Molekul. Skripsi. Medan : USU.
Nwe, N. and W. F. Stevens. 2008. Production of Chitin and Chitosan and their Applications in The Medical and Biological Sector. In Recent Research in Biomedical Aspects of Chitin and Chitosan, ed. H. Tamura, pp. 161-176. Research Signpost, Trivandrum, Kerala, India.
Qing, Y., Fengdong, D., Borun, L., dan Qing, S. 2004. Studies of Cross-linking Reaction on Chitosan Fiber with Glyoxal. Carbohydrate Polymers, 59, 205-210.
Rusli, P. R. 2011. Pembuatan dan Karakterisasi Nanopartikel Titanium Dioksida Fase Anatase dengan Metode Sol-Gel. Skripsi. Medan : Unimed.
Shu, X. Z. and Zhu, K. J. 2002. Controlled Drug Release Properties of Ionically Cross-linked Chitosan Beads : The Influence of Anion Stucture. International Journal of Pharmaceutics 233 : 217-225.
Silverstein, R. M. 1967. Spectrometric Identification of Organic Compounds. New York : John Wiley and Sons.
Sivakami, M. S. 2013. Preparation and Characterization of Nano Chitosan for Treatment Wastewater. India : Tamil Nadu.
Sugita, P. 2009. Kitosan : Sumber Biomaterial Masa Depan. Bogor : IPB Press.
Swabrick, J. 2007. Encyclopedia of Pharmaceutical Technology. Third Edition. Volume IV. New York : Informa Healthcare USA Inc.
Szeto, Y. S. and Zhigang H. 2007. Chitosan Nanoparticles for Functional Textile Finishes.
Tokura, S. and H. Tamura. 2007. Chitin and Chitosan. In Comprehensive Glycoscience, eds. H. Kamerling, G. Boons, Y. C. Lee, A. Suzuki, N. Taniguchi, and A. G. J. Voragen, pp. 449-475. Elsevier Ltd., Amsterdam, The Netherlands.
Tokuyasu, K., Ono, H., Kameyama, M. O., Hayashi, K., Moil, Y. 1997. Deacetylation of Chitin Oligosaccharides of dp 2-4 by Chitin Deacetylase from Colletotrichum lindemuthianum. Carbohydrate Research 303 : 353-358.
Tsigos, I., Martinou, A., Kafetzopoulos, D., Bouriotis, V. 2000. Chitin Deacetylases : New, Versatile Tools in Biotechnology. TIBTECH 18 : 305-312.
Lampiran1.Pengadukan Campuran Larutan Kitosan dengan Natrium Tripolifosfat
Lampiran 2. Hasil Sentrifugasi Suspensi Nanopartikel Kitosan
Lampiran 4. Freeze Dryer
Lampiran 5. Particle Size Analyzer